Elemente des Periodensystems
Werbung
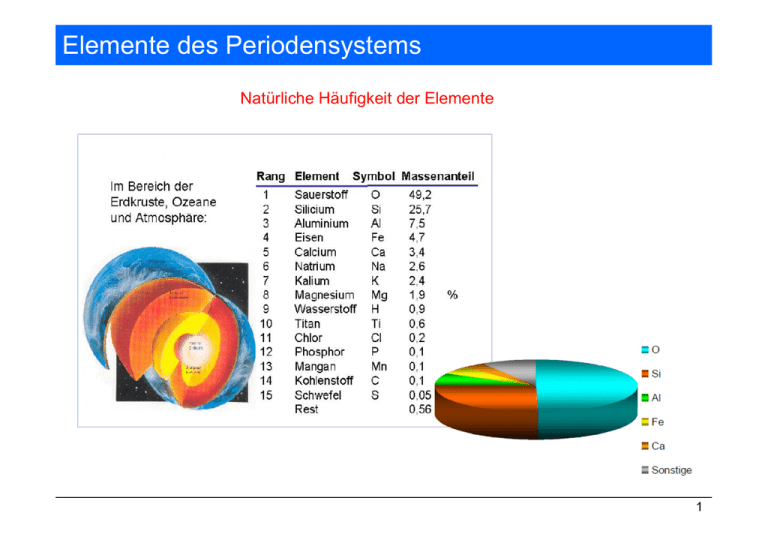
Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff • • • • • Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel …und auf der Erde 3 Eigenschaften 4 Ein Element – verschiedene Bindungstypen im Inneren des Jupiter (90 % H2, 10 % He) T = 20 000 K p > 4 Mio bar 5 Darstellung im Labor Herstellung im Labor im Kipp´schen Apparat 6 Technische Verfahren zur H2-Gewinnung Ca. 90 % des Wasserstoffs werden aus fossilen Energieträgern gewonnen Kohlevergasung (Wassergas, Synthesegas) Basis für die Synthese organischer Chemikalien (z. B. Methanol, Alkane, Alkene) Kohlenoxid-Konvertierung oder Wassergas-Shift-Reaktion (an Co3O4-Kat. bei 450°C) liefert Energie 7 Elektrolyse von Wasser Das lohnt sich nur bei günstig verfügbarer Elektroenergie. 8 Wasserstofftechnologie der Zukunft 9 Reaktionen Knallgas-Reaktion ΔH = - 572 kJ/mol H2 ist bei Raumtemperatur reaktionsträge. Reaktion durch Zündung initiiert. eine Kettenreaktion die zur Explosion führt 1986: Challenger-Katastrophe 10 Verwendung als Brenngas 11 Wasserstoffverbindungen Ionische Hydride (1. und 2. Hauptgruppe) Kovalente Wasserstoffverbindungen (3. – 7. Hauptgruppe) mehr oder weniger polar HF Metallische Hydride (Einlagerungsverbindungen) meist nicht stöchiometrisch 12 Industrielle Verwendung von Wasserstoff 13 Wasserstoff – Energieträger der Zukunft Funktionsprinzip einer PEM-Brennstoffzelle Anode H2 2 H+ + 2 eKatode O2 + 2 e- O2- Elektrolyt Protonenaustauscher-Membran Proton Exchange Membrane (PEM) 2 H+ + O2- H2O 14 Zusammenfassung - Wasserstoff Leichtestes Gas mit niedrigem Siede- und Schmelzpunkt Technische Gewinnung durch Steam-Reforming aus CH4 oder Koks und Wasserdampf Darstellung im Labor durch Reaktion unedler Metalle mit Säuren oder Wasser Hohe Bindungsenergie der H-H-Bindung erfordert meist höhere Reaktionstemperaturen Mit Elementen der 1. und 2. HG bilden sich salzartige Hydride mit dem H- Anion H2 reagiert mit vielen Nichtmetallen zu Molekülen mit (polar) kovalenten Bindungen, in denen H partiell positiv geladen ist H2 kann viele Metalloxide zum Metall reduzieren H2 wird als Brennstoff und in vielen chemischen Synthesen gebraucht 15 Weitere Elemente der 1. Hauptgruppe (Alkalimetalle) „al-qary“ (arabisch) Look! He´s positive... Somebody stole his electron Help!!! He is stealing my electron Help!!! There is water in here! = salzhaltige Asche • • • • • Eigenschaften Vorkommen Gewinnung Verwendung Wichtige Verbindungen 16 Eigenschaften der Elemente weiche Metalle geringer Dichte (Li, Na und K schwimmen auf dem Wasser) mit dem Messer schneidbar Natrium Kalium 17 Eigenschaften der Elemente Heftige Reaktion mit Wasser M + H2O x MOH + ½ H2 M x M+ + e- H+ + e- x ½ H2 Reaktion mit den meisten Nichtmetallen z. B. Halogene, Sauerstoff, Wasserstoff Ionischer Charakter, großer Radius, geringe Ladungsdichte ximmer als M+-Kationen auf, Bildung leicht löslicher, farbloser Salze xStabilisierung großer, niedrig geladener Anionen (z. B. HCO3-, O2-) 18 Natürliche Vorkommen LiAl[Si2O6] Spodumen NaCl (Steinsalz, Halit) Na2CO3 . 10 H2O (Soda) NaNO3 (Chlilesalpeter) KCl (Sylvin) NaAl[Si3O8] (Natronfeldspat, Albit) Na3AlF6 (Kryolith) KAl[Si3O8] (Kalifeldspat) 19 Gewinnung der Alkalimetalle - Alkalichloridelektrolyse Smp. 580 °C Kathode: Na+ + e- x Na (flüssig) Anode: 2Cl- x Cl2 (gasf.) + 2 e20 Verwendung der Alkalimetalle Natrium ¾ Synthese einer Vielzahl von Natriumverbindungen z. B. Na2O2, NaNH2,NaH, NaCN ¾ Als Reduktionsmittel zur Gewinnung von Metallen, z. B. von Titan ¾ Trockenmittel für organische Lösungsmittel ¾ Na-Dampflampen Kalium, Lithium ¾ Synthese von Li- und K-organischen Verbindungen ¾ K- und Na-Legierungen als Kühlmittel in Kernreaktoren 21 Hydoxide MOH sind von allen Hydroxiden die stärksten Basen sehr hygroskopische weiße Feststoffe, zerfließen beim Stehen an Luft extrem ätzend („Ätznatron, Ätzkali“, OH- reagiert mit Proteinen der Haut, NaOH als Abflußreiniger) NaOH für anorganische, KOH für organische Synthesen (löst sich besser in organischen Lösungsmitteln reagieren mit CO2 zu Hydrogencarbonaten NaOH 22