Identifikation und Analyse unbekannter und seltener Mutationen des
Werbung

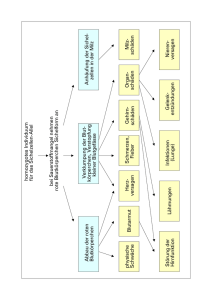
Identifikation und Analyse unbekannter und seltener Mutationen des ‐1‐Antitrypsin Gens Herr C1, Kotke V2, Greulich T2, Koczulla R2, Beißwenger C1, Vogelmeier C2, Bals R1 1Klinik für Innere Medizin V, Pneumologie, Allergologie und Beatmungsmedizin, Universität des Saarlandes, 66424 Homburg / Saar 2Klinik für Innere Medizin, Abteilung Pneumologie, Philipps Universität Marburg, 35043 Marburg Einleitung: Alpha‐1‐Antitrypsin‐Mangel (AAT‐Mangel) ist eine genetische Mutation und stellt einen Risikofaktor für die Entstehung einer chronisch obstruktiven Lungenerkrankung (COPD) dar. Die Häufigkeit in Nordamerika und Nordeuropa ist mit der Mukoviszidose vergleichbar. Neben den häufigsten pathologischen Allelen, dem Z‐ und S‐Allel, existieren eine Vielzahl seltener Mutationen. Das Ziel dieser Arbeit ist es, in einem laufenden AAT‐Screening‐Programm Personen mit seltenen oder unbekannten Mutationen zu identifizieren. Methoden: Personen mit AAT‐Mangel (n=16180) wurden durch PCR‐Analyse eines „dried‐blood‐spot“ (DBS) und isoelektrischer Fokussierung (IEF) genotypisiert. Konnte der Genotyp nicht eindeutig dem S‐ oder Z‐Allel zugeordnet werden, erfolgte eine Exonsequenzierung aller 7 Exons des AAT‐ Gens. Die Analyse und Auswertung erfolgte durch einen Vergleich der Sequenzdaten mit einer Referenzsequenz und bis dahin publizierten bekannten Mutationen. Abb.3 Abb.1 kein S‐, kein Z‐Allel; n=10322; 65.19% (A) (B) SS; n=51; 0.32% Erstes Allel: Z, zweites Allel: kein S / Z; n=3095; 19.55% SZ; n=257; 1.62% ZZ; n=1058; 6.68% Sequenziert; n=261; 1.65% Erstes Allel: S, zweites Allel: kein S / Z; n=789; 4.98% N=16180 Abb.1: (A) Das SERPIN‐A1 Gen beinhaltet 4 Proteinkodierende Exons (II‐V) und 3 nicht‐kodierende Exons (IA‐C). (B) Die Nomenklatur der Mutationen erfolgt nach dem Laufverhalten des Proteins bei der Isoelektrischen Fokussierung und einer Ortsangabe (Geburtsort des Trägers). Abb.2 (A) Basis‐Allele Abb.3: Zusammensetzung der Genotpyen, die durch Isoelektrische Fokussierung und PCR Analyse identifiziert werden konnten. Nur etwa 1,65 % der Proben mussten durch Exon‐Sequenzierung identifiziert werden. Abb.4 (A) “At‐Risk Allele” Stop‐Mutationen (B) P‐StLouis; n=1 M‐Malton;n= 2 P‐Brescia; n=2 M‐Nichinan; n=7 M‐Würzburg; n=9 P‐Lowell; n=14 Q0‐Saarbrücken; n=1 Q0‐Lisbon; n=1 Q0‐Bolton; n=1 Q0‐Kowloon; n=1 Q0‐Granite‐Falls; n=4 M‐Procida; n=24 Q0‐Bellingham; n=5 M‐Heerlen; n=46 Q0‐Clayton;n= 8 Q0; n=21 (B) (C) M2/Q0; n=1 M1/Q0; n=4 M3/Rare at risk; n=10 Z/Q0; n=14 Abb.2: (A) Die Mutationen werden in Basis‐Allel, „At‐Risk Allele“ und Stop‐ Mutationen unterteilt. Basis‐Allele verursachen keine Veränderung des Serum‐AAT‐Spiegels, während „At‐Risk Allele“ zu unterschiedlich starker Verringerung des Serum‐AAT‐Spiegels führen und damit das Risiko für eine Leber‐ oder Lungenerkrankung erhöhen. Stop‐Mutationen führen dazu, dass auf Grund eines Stop‐Codons zu einem vorzeitigen Abbruch der Proteinsynthese kommt. (B) AAT‐Mangel ist in Europa etwa so häufig wie Mukoviszidose. M2/Rare at risk; n=22 M1/Rare at risk; n=44 Z/Rare at risk; n=91 Abb.3: Die Ergebnisse der Sequenzierung zeigen, dass (A) M‐Heerlen und M‐ Procida die beiden häufigsten seltenen „At‐Risk“ Mutationen sind. (B) Unter den Stop‐Mutationen kommen Q0‐Clayton und Q0‐Belingham am häufigsten vor. (C) Die Kombination von einem Z‐Allel und einem seltenen „At‐Risk“ Allel ist am häufigsten zu finden, gefolgt von der Kombination aus einem normalen (M1) Allel mit einem seltenen „At‐Risk“ Allel. Zusamenfassung: Die Diagnose von AAT‐Mangel Patienten durch DBS PCR‐ Analyse und isoelektrischer Fokussierung stellt eine zuverlässige Methode zur Diagnose dar. Die genomische Sequenzierung und genetische Analyse ist eine wertvolle Ergänzung und liefert wichtige Daten zur Identifikation unbekannter Mutationen. Des Weiteren ermöglicht die umfassende Identifikation der Mutationen eines laufenden Screening‐Programmes eine genauere Analyse der Verteilung und Häufung bekannter und bislang nicht erkannter Mutationen.