Pneumonie Lungenentzündungen
Werbung

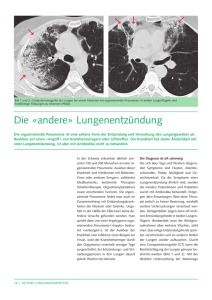
Lungenentzündungen Internistische Klinik I. Station für Infektiologie Beáta Kovács 2016 Definition Pneumonien sind akute Entzündungen des alveolären und/oder interstitiellen Lungengewebes. Sie werden am häufigsten durch Bakterien verursacht, Viren und Pilze spielen aber von der Immunität des Patienten abhängig ebenfalls eine wichtige Rolle. Eine Entzündung kann sich auch durch physikalische oder chemische Noxen (z.B. Strahlen, Aspiration) herausbilden, in diesem Fall spricht man über eine Pneumonitis. Einteilung Während früher die Einteilung nach der morphologischen Ausbreitung der Pneumonie im Lungenparenchym (Bronchopneumonie, Lobärpneumonie, interstitielle Pneumonie) bestimmt wurde, wird die Pneumonie heute nur nach klinischen Gesichtspunkten unterschieden. Nach den klinischen Symptomen und dem physikalischen Lungenbefund kann die Pneumonie in zwei Gruppen („klassisch” vs. „atypisch”) unterteilt werden. Die klassischen oder atypischen Symptome können auf die Erreger hinweisen. Am wichtigsten ist, das mögliche Erregerspektrum zu bestimmen. Aufgrund dieser Bestimmung kann die Therapie angefangen werden. Zuerst stellt sich die Frage, ob eine Immunsuppression vorliegt oder nicht. Die Art der Immunstörung (Neutropenie, HIVInfektion, medikamentöse Immunsuppression, Knochenmarktranspantation) muss definiert werden, damit die Differentialdiagnose der Erreger gestellt werden kann. Bei immunkompetenten Patienten werden die ambulant erworbene Pneumonie und die nosokomiale Pneumonie unterschieden. Zwischen diesen zwei Gruppen gibt es einen Unterschied im zu erwartenden Erregerspekrum und es determiniert die auszuwählende Therapie. Ambulant erworbene Pneumonie (AEP) community-acquired pneumonia (CAP) Außerhalb des Krankenhauses oder während der ersten 48 Stunden nach Aufnahme ins Krankenhaus erworbene Pneumonie wird als AEP bezeichnet. Nosokomiale Pneumonie hospital-acquired pneumonia (HAP) ventilator- associated pneumonia (VAP) Nosokomiale Pneumonie ist im Krankenhaus entstanden und kann somit erst 48-72 Stunden nach der Krankenhausaufnahme oder bei Wiederaufnahme innerhalb von 30 Tagen nach Entlassung diagnostiziert werden. Die Beatmungspneumonie ist die häufigste Form der nosokomialen Pneumonie, die 48-72 Stunden nach der Intubation auftritt. Epidemiologie • Sowohl in der Praxis als auch im Klinikbereich ist weltweit die Pneumonie die häufigste registrierte Infektionserkrankung. • Etwa 90% der Fälle werden durch Bakterien ausgelöst. • In Deutschland liegt die Inzidenz in der Gesamtbevölkerung zwieschen 3,7 und 10 Fällen pro 1000 Einwohner in einem Jahr. Diese Zahl entspricht etwa 400000 - 680000 Fälle pro Jahr in Deutschland. Über 30% der Erkrankten müssen im Krankhenhaus, davon 10% auf der Intensivstation behandelt werden (d. h. ca. 3% aller Patienten mit einer ambulant erworbenen Pneumonie). Etwa 20000 Menschen sterben jährlich in Deutschland an einer Pneumonie. Sterblichkeit ist bei Patienten in Alters- und Pflegeheime höher. Ätiologie der ambulant erworbenen Pneumonie • Die Ätiologie kann in maximal 60% aller Fälle festgestellt werden. • Das Erregerspektrum der ambulant erworbenen Pneumonie hängt von der Komorbidität und dem Lebensalter der Patienten ab. • Die folgenden Bakterien als die häufigste Erreger können bei Patienten im Alter unter 65 Jahren und mit keiner Komorbidität vorkommen: -Streptococcus pneumoniae (30-50%) -Haemophilus influenzae (10%) -Mycoplasma pneumoniae (10%) -Chlamydophila pneumoniae (20%) -Legionella pneumophila (3-5%) -Staphylococcus aureus (2%) -Chlamydophila psittaci (<1%) -Coxiella burnetii (<1%) -Viren (Influenzaviren, das Respiratiry-syncytial-Virus, das humane Metapneumovirus, Adenoviren, Varizella-Zoster-Virus, Humanes Cytomegalievirus) • Das Respiratory-syncytial-Virus und das humane Metapneumovirus bekannt als Erreger von Pneumonien im Säuglings- und Kleinkindesalter. • Legionella pneumophila, Mycoplasma pneumoniae, Chlamydophila pneumoniae, Chlamydophila psittaci und Coxiella burnetii verursachen die atypischen Pneumonien. Ätiologie der ambulant erworbenen Pneumonie • Bei Patienten im Alter über 65 Jahren und/oder mit einer Grundkrankheit (z.B. COPD, Diabetes mellitus, chronisches Nierenversagen, Herzinsuffizienz, fortgeschrittene Leberkrankheit, dauernde Steroideinnahme, fortgeschrittene maligne Krankheit) kann eine AEP neben der früher angeführten Krankheitserregern durch aerobe gramnegative Stäbchen, wie Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, Haemophilus influenzae und auch Moraxella catarrhalis oder Mycobacterium tuberculosis verursacht werden. • Etwa 40% der Influenza-Infektionen bei Patienten über 65 Jahren gehen mit pulmonalen Infiltraten einher. Die Influenza-Infektion begünstigt die Entstehung einer bakteriellen Superinfektion durch die Schädigung des Atemwegsepithels. Ätiologie der nosokomialen Pneumonie • Eine nosokomiale Infektion kann sich durch eine endogene oder exogene Infektion herausbilden, dadurch entsteht das Erregerspektrum der nosokomialen Pneumonien einerseits aus dem oropharyngealen und intestinalen Keimespektrum des Patienten, andererseits aus der Flora des jeweiligen Krankenhauses. • Bei Patienten mit einer nosokomialen Pneumonie kommen die folgenden Erreger am häufigsten vor: gramnegative Bakterien (50-70%) - Enterobacter spp. (8-12%) - Klebsiella spp. (5-8%) - Escherichia coli (4-8%) - Pseudomonas aeruginosa (15-25%) - Haemophilus influenzae (5-10%) - Legionella spp. grampositive Kokken (10-20%) - Staphylococcus aureus (10-30%) - Streptococcus pneumoniae (5-10%) - Anaerobier (0-35%) Pilze (0-14%) Viren und Protozoen (selten) Nosokomiale Pneumonie • Eine Aspirationspneumonie wird durch die Aspiration von Mageninhalt hervorgerufen. Die häufigsten Keime der Aspirationspneumonie sind die gramnegativen und anaeroben Bakterien. • Exogene Infektionen, z.B. durch infizierte Bronchoskope, inadäquate Desinfektion, können auftreten. Diese Infektionen können durch multiresistente Bakterien (z.B. Pseudomonas aeruginosa, Methicillin-resistenter Staphylococcus aureus) verursacht werden. • Bei immunkonpromittierten Patienten kann Humanes Cytomegalievirus, Varizella-Zoster-Virus, Pneumocystis jiroveci (früher: P. carinii), Mycobacterium tuberculosis als Erreger vorliegen. Infektionsweg wird meistens durch Tröpfcheninfektion aber auch durch Deszension über den Oropharynx oder hämatogenen Weg ausgelöst. • Pneumonie • Tierische Erregerreservoire spielen bei Ornithose (Chlamydophila psittaci), Q-Fieber (Coxiella burnetii) und der aviären Influenza eine Rolle. C. psittaci wird durch Inhalation der infektiösen Staubpartikeln (wie der eingetroknete aufgewirbelte Vogelkot) übertragen. C. burnetii wird von Schafen, Kühen oder Ziegen erworben, wobei die Infektion durch Einatmen erregerhaltigen Staubpartikeln oder auf oralem Weg durch Trinken roher Milch erfolgt. • Legionella-Infektion wird durch kontaminiertes Wasser übertragen. Legionellen haben hohe Temperaturtoleranz (bis zu 60 °C). Legionellen können im Warmwasser, im Leitungswasser und in den Klimaanlagen leben. Frei im Wasser lebende Amöben ermöglichen den Erregern eine intrazelluläre Persistenz und schützen sie vor physikalischen und chemischen Einflüssen, z.B. Chlorierung. Eine Infektion kann auch durch Inhalation beim Duschen verursacht werden. Symptome • Die auf eine Pneumonie hinweisenden respiratorischen Symptome sind: Fieber, Schüttelfrost Husten mit oder ohne Auswurf Atemnot atemabhängige einseitige Thoraxschmerzen (bei Pleurabeteiligung). Verwirrtheit kann durch Sauerstoffmangel auftreten. • Extrapulmonale Symptome können auftreten: Müdigkeit Kopschmerzen Glieder- und Muskelschmerzen abdominelle Beschwerden (Übelkeit, Erbrechen, Bauchschmerzen, Durchfall) • Bei Kindern stehen folgende Symptome im Vordergrund: - Atemnot mit erschwerter Atmung (erhöhte Atemfrequenz, Nasenflügelatmung, Einsatz der Atemhilfsmuskulatur) - quälender Husten, der sich bei symptomatischer Therapie nicht bessert - Blässe, in schweren Fällen auch Zyanose. Symptome • Bei der klassischen/typischen Pneumonie treten respiratopische Symptome auf. • Für eine atypische Pneumonie sind die extrapulmonalen Symptome typisch, aber die respiratorischen Symptome sind nicht immer ausgeprägt. (Es gibt kein Fieber, sondern nur erhöhte Temperatur und Husten ohne Auswurf). Bei atypischer Pneumonie treten Hautsymptome, wie maculopapulöse Exantheme, Erythema nodosum oder Erythema multiforme häufig auf. Die atypische Pneumonie wird durch Mycoplasma pneumoniae, Chlamydophila pneumoniae, Chlamydophila psittaci, Coxiella burnetii und Legionella spp. ausgelöst. Risikostratifizierung Der CURB-65-Index ist gut geeignet für Beurteilung des Schweregrades der Pneumonie. Maximal werden 5 Punkte vergeben, die mit unterschiedlicher Mortalität assoziiert sind und dadurch einen Hinweis geben, ob Patienten ambulant versorgt werden können oder stationär oder gar intensivmedizinisch behandelt werden müssen. 0 C = confusion (Verwirrtheit): AMT-score (abbreviated mental test) unter 8 1 Mortalität niedriges Risiko; Behandlung meist zu Hause 0.7 % 3.2 % niedriges Risiko; Behandlung meist zu Hause 13 % höheres Risiko; Kurze Hospitalisierung oder eine überwachte Heimtherapie 17 % hohes Risiko; Hospitalisierung und eventuell intensivmedizinische Betreuung 41.5 % hohes Risiko; Hospitalisierung und eventuell intensivmedizinische Betreuung 57% hohes Risiko; Hospitalisierung und eventuell intensivmedizinische Betreuung U = urea (Serumharnstoff): >7 mmol/l R = respiratory (Atemfrequenz): >30/min B = blood pressure (Blutdruck): systolisch unter 90 mmHg oder diastolisch unter 60 mmHg 2 3 4 65 = Patient ist über 65 Jahre alt 5 Weitere Risikofaktoren Immuninkompetenz (Abwehrschwäche) Infektion. begünstigt die Entstehung einer • primäre (angeborene) Immunmangelzustände (Agammaglobulinämie oder IgG-Subklassenmangel, Komplementmangel) • sekundäre (erworbene) Immundefizienzen (hämatologische oder onkologische Grundkrankheit, Organtransplantpation, HIV-Infektion, Neutropenie, Verbrennung) Bei HIV-Patienten, Organtransplantierten und Knochenmarkempfängern kann es mit der Herausbildung einer Pneumonie von Pneumocystis jiroveci, Mycobacterium tuberculosis oder CMV gerechnet werden. • vorbestehende Steroidtherapie (von mindestens 10 mg/Tag PrednisolonÄquivalent über eine Dauer von mindestens vier Wochen oder einer kumulativen Dosis von 700 mg) • Eine Infektion durch gramnegative Keime kann bei älteren Patienten über 65 Jahren häufiger vorkommen. Weitere Risikofaktoren • Grundkrankheiten (Diabetes mellitus, COPD, Leberzirrhose, Nierenversagen) begünstigen einen schwereren Verlauf der Infektion. S. aureus und P. aeruginosa sind häufige Erreger bei Patienten mit Bronchiektasie und Mukoviszidose. Haemophilus influenzae und Moraxella catarrhalis kommen oft bei Patienten mit chronischer Bronchitis vor. • Eine verstärkte Exposition liegt in Pflegeheimen/Altersheimen vor. In diesem Fall soll der Möglichkeit einer Aspirationspneumonie Rechnung getragen werden. • Chroniser Alkoholabusus ist mit S.-peumoniae-Pneumonien Aspirationspneumonien assoziiert. und Weitere Risikofaktoren • Bei Reiseanamnese in Ländern mit hoher Legionnellose-Prävalenz oder Exposition gegenüber Wasser aus speziellen Anlagen (Klimaanlagen in Flugzeugen, in Konferenzräumen, in Hotelzimmern) kann auf eine LegionellaInfektion hinweisen. Eine Legionella-Infektion kann auch beim Duschen durch kontaminierte Duschköpfe auftreten. • Es ist wichtig die Tierkontakte zu ermitteln. Papageien und Hausgeflügel können Ornithose und aviäre Influenza übertragen. Schafe, Ziegen und Kühe können Q-Fieber übertagen. Diagnostik • Der typische physikalische Befund ist die Krepitation (feinblasige, klingende Rasselgeräusche). • Zur Labordiagnostik gehören ein Differenzialblutbild, CRP, Leberenzyme, Kreatinin und Harnstoff-N. (Leberenzyme – GOT/AST, GPT/ALT - sind typischerweise bei atypischer Pneumonie erhöht.) Zur Abschätzung der Gasaustauschstörung sollte eine arterielle Blutgasanalyse vorgenommen werden. • Infiltrate der Lunge können durch eine Röntgen-Thoraxaufnahme in zwei Ebenen festgestellt werden. • Nach der stazionären Aufname soll eine Blutkultur entnommen werden. Der Erreger kann in 20% der Fällen nachgewiesen werden. • Der Erreger kann aus dem Sputum im Labor gezüchtet werden, aber die Patienten können nur schwerlich eine für mikrobiologische Züchtung entspechende, kontaminationsfreie Sputum-Probe produzieren. Diagnostik • Zur Erregerdiagnostik beim beatmeten Patienten steht die bronchoalveoläre Lavage (BAL) zur Verfügung. • Es ist möglich das Pneumokokken-Antigen im Urin nachzuweisen. Mit einem immunchromatographischen Membrantest kann das PneumokokkenZellwand-Polysaccharid nachgewiesen werden. Alle Serotypen von S. pneumoniae, S. oralis und S. mitis können mit dieser Methode analisiert werden. Diese Methode hat eine gute Spezifizität (90%) aber eine niedrige Sensitivität (50-80%). (Ein negativer Test kann die Pneumokokken-Infektion nicht ausschließen, aber ein positives Ergebnis kann den Verdacht verstärken.) • Ein positiver Legionella-Antigentest im Urin weist bei allen Patienten mit erhöhter Wahrscheinlichkeit auf eine Legionellen-Infektion hin. Der Test erfasst ausschließlich das Antigen der L.-pneumophyla-Serogruppe 1. Er weist eine Sensitivität von über 90% auf und führt zu einer raschen Diagnosestellung. Eine schnelle Diagnosestellung ist wichtig in schweren Fällen von Legionellen-Infektionen aber der Test kann eine LegionellenInfektion nicht ausschließen. Diagnostik • Für Influenza-Viren stehen Schnelltests zur Vefügung, die innerhalb von 15-20 Minuten eine ätiologische Diagnose mit einer Sensitivität von 70-90% geben. • Infektionen durch M. pneumoniae, C. pneumoniae, C. psittaci, C. burnetii, Legionella spp. und reschpiratorische Viren werden häufig nur serologisch nachgewiesen. Bei diesen Erregern beginnt die Produktion der Antikörper nur spät, und zu Beginn der Erkrankung ist der Antikörperspiegel niedrig und nicht nachweisbar. Deswegen kann man die Serologie für retrospektive Diagnosestellung verwenden. • Nukleinsäure-Amplifikationsverfahren (PCR) haben nur eine geringe Bedeutung außer der Tuberkulose. Therapie • Die symptomatische Therapie bestecht aus ausreichender Flüssigkeitszufuhr, der Gabe von Analgetika bei Pleuraschmerzen und Sauerstoffgabe bei schwerer Gasaustauschstörung. Zusätzlich kann die Expektoration durch die Gabe von Mukolytika begünstigt werden. • Die entsprechende Antibiotikum-Therapie hängt von den Risikofaktoren, der Art der Pneumonie, der epidemiologischen Aspekte und der lokalen Resistenzsituation ab. Therapie bei ambulanten Patienten ohne Risokofaktoren im Alter unter 65 Jahren • Die häufigsten Erreger sind M. pneumoniae, S. pneumoniae, C. pneumoniae, H. influenzae, Legionella spp., S. aureus und Viren. Unter jungen Erwachsenen liegt die Proportion von atypischen Erregern von 20-40%. Die atypischen Erreger haben natürliche Resistenz gegen ß-LaktamAntibiotika. Gegen atypische Erreger sind Makrolid-Antibiotika, Doxycyclin und Fluorochinolone der 3. und 4. Generation wirksam. Q-Fieber und Ornithose sollen immer mit Doxycyclin behandelt werden. Die Makrolid-Resistenz der Pneumokokken kann hoch (~ 30%) sein. Die therapeutischen Möglichkeiten sind: - Makrolid-Monotherapie Azithromycin 1x500 mg/Tag oder Clarithromycin 2x500 mg/Tag - Aminopenicillin ± ß-Laktamase-Inhibitor Amoxicillin+Clavulansäure 2x1g/Tag per os oder 3x1,2 g i.v. - Doxycyclin 2x100 mg/Tag - Cephalosporine der 2. Generation Cefuroxim-Axetil 2x500 mg/Tag per os Bei Therapieversagen kann man Fluorchinolone (Levofloxacin, Moxifloxacin) verabreichen. Therapie bei ambulanten Patienten mit Risokofaktoren und/oder im Alter über 65 Jahren • Die häufigsten Erreger sind S. pneumoniae, C. pneumoniae, M. pneumoniae, Legionella spp., aerobe gramnegative Stäbchen (Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, Haemophilus influenzae) und auch Moraxella catarrhalis oder Mycobacterium tuberculosis. Die Therapie der Wahl ist in dieser Gruppe: • Eine Aminopenicillin/ß-Lactamase-Inhibitor-Kombination (Amoxicillin+Clavulansäure 2x1g/Tag per os oder 3x1,2 g i.v.) Diese Kombination ist auch gegen S. aureus, die ß-Lactamase-bildenden Enterobakterien sowie Anaerobier wirksam. • Alternativ einsetzbare Antibiotika sind Cephalosporine der 2. oder 3. Generation (Cefuroxim-Axetil 2x500 mg/Tag per os) • Wenn atypische Erreger erfasst werden sollen, kann zusätzlich ein MakrolidAntibiotikum gegeben werden. (Azithromycin 1x500 mg/Tag, Clarithromycin 2x500 mg/Tag) • Eine weitere Alternative ist die Monotherapie mit einem neueren Fluorchinolon (Levofloxacin 1-2x500 mg/Tag, Moxifloxacin 1x400 mg/Tag). Diese Antibiotika sind auch gegen Pneumokokken und atypiche Erreger wirksam. Moxifloxacin hat auch ein anaerobes Spektrum. Therapie bei hospitalisierten Patienten • Die gleichen Erreger lösen die Pneumonie aus, aber der Verlauf der Krankheit ist schwerer, deshalb soll mit einer parenteralen Behandlung begonnen werden und die initiale Therapie kann auf eine orale Sequenztherapie umgesetzt werden. • In erster Linie sollen ß-Laktam-Antibiotika (Aminopenicillin+ß-LactamaseInhibitor, Cephalosporine der 2. oder 3. Generation, wie Cefuroxim-Axetil, Ceftriaxon, Cefotaxim, Cefepim) mit Makroliden kombiniert werden. • Als Alternative können die Pneumokokken-wirksamen Fluorchinolone (Levofloxacin, Moxifloxacin) eingesetzt werden. • Bei Patienten mit Risiko für eine Infektion mit P. aeruginosa (pulmonale Komorbidität – COPD, Mukoviszidose; stationärer Aufenthalt in den Letzten 30 Tagen, Glukokortikoid-Therapie, Aspiration, Breitspektrum-Antibiotikatherapie über mehr als sieben Tage innerhalb des letzten Monats, Malnutrition) ist ein Pseudomonas-aktives ß-Laktam-Antibiotikum (Cefepim, Piperacillin+Tazobactam, Carbapeneme) in Kombination mit einem Makrolid oder eine Therapie mit einem Pseudomonasaktiven Fluorchinolon (Ciprofloxacin) zu empfehlen. Bei Gabe von Ciprofloxacin muss zusätzlich ein Antibiotikum mit Wirksamkeit gegen grampositive Kokken (ßLaktam-Antibiotikum) verabreicht werden. Therapie • Im Allgemeinen dauert eine Antibiotikum-Therapie 7-10 Tagen bei ambulant erworbener Pneumonie. Die Therapie einer atypischen Pneumonie soll 14-21 Tage dauern. Legionella-Pneumonie soll 21 Tage behandelt werden. • Bei einer Influenza-Pneumonie kann ein Neuraminidase-Hemmer (Oseltamivir, Zanamivir) verabreicht werden. Die Therapie muss innerhalb von 36 Stunden nach Beginn der Symptomatik anfangen. Zanamivir 2x10 mg/Tag für 5 Tage Oseltamivir 2x75 mg/Tag für 5 Tage • Eine Varizellen-Pneumonie sollte sofort mit Aciclovir (3x10 mg/kg/Tag i.v. über 5-10 Tage) behandelt werden. Therapie der nosokomialen Pneumonie • Es ist wichtig, das lokale Erregerspektrum der Intensivstation und das Resistenzverhalten der Erreger zu kennen. Häufigste Bakterien sind S. aureus (auch Methicillin-resistente Stämme), grammnegative Enterobakterien (Klebsiella spp. > E. coli > Enterobacter spp.) und P. aeruginosa. • Bei spontan atmenden Patienten werden multiresistente Erreger seltener gefunden. Typisches frühes Erregerspektrum ist S. aureus, S. pneumoniae, Enterobacterien. Eine Monotherapie steht zur Verfügung: - Cephalosporine der 2. oder 3. Generation oder - Aminopenicilline in Kombination mit einem BLI oder - Fluorchinolone der Gruppe 3 oder 4. Therapie der nosokomialen Pneumonie • Bei künstlich beatmeten Patienten, wenn die Pneumonie innerhalb der ersten fünf Tage nach der Krankenhausaufnahme aufgetreten ist, sind die möglichen Erreger: S. aureus, H. influenzae, S. pneumoniae und Enterobacteriaceae. Bei einer Monotherapie können: - Acylpenicilline+BLI (z.B. Piperacillin+Tasobactam) oder - Cephalosporine der 3. Generation oder - Fluorchinolone der Gruppe 2 oder 3 oder - Carbapeneme (Imipenem, Meropenem) verwendet werden. • Bei künstlich beatmeten Patienten, wenn die Pneumonie nach dem fünften Tag auftritt, sind die möglichen Erreger: MRSA, P. aeruginosa, Acinetobacter baumanii, Enterobacter spp. Eine Kombinationstherapie ist erforderlich: - Acylpenicilline+BLI (z.B. Piperacillin+Tasobactam) oder - Cephalosporine der 3. Generation oder - Carbapeneme (Imipenem, Meropenem) in Kombination mit einem Fluorchinolon der Gruppe 2 (Ciprofloxacin) oder 3 (Levofloxacin). • Die Therapiedauer sollte sich nach dem Verlauf der klinischen Symptome richten. Therapie von Q-Fieber und Ornithose • Akutes Q-Fieber und akute Ornithose sind durch hohes Fieber, starke Kopfschmerzen, atypische Pneumonie und eine Hepatitis gekennzeichnet. Selten können Perimyokarditis, Meningoenzephalitis, und ein makulopapulöses Exanthem vorkommen. • Q-Fieber und Ornithose sollen immer (unabhängig vom Lebensalter und von der Komorbidität) über 2-3 Wochen mit Doxycyclin behandelt werden. • Q-Fieber kann chronischen Verlauf haben, wenn der Patient nicht gut behandelt ist. Als Spätkomlikationen können Endokarditis, Osteomyelitis und granulomatöse Hepatitis vorkommen. • Alle Patienten, die akutes Q-Fieber hatten, sollen in 2 und 6 Monaten serologisch kontrolliert werden. Wenn der Titer von Phase I IgG hoch erhöht (>1:1024) bleibt, soll eine transösophageale Echokardiographie durchgeführt werden, um eine Endokarditis auszuschließen. • Eine Q-Fieber-Endokarditis soll 18-24 Monate mit der Kombination von Doxycyclin und Hydroxichloroquin behandelt werden. Prävention • Die aktive Immunisierung steht gegen Pneumokokken (Polysaccharid- und Konjugat-Impfstoffe), gegen H. influenzae Typ b und gegen Influenza zur Verfügung. Alle Impfungen werden für die bestimmte Risikogruppen (wie Patienten mit chronischen Lungen- und Herzkrankheiten, Diabtes mellitus) empfohlen. Die Impfungen gegen Pneumokokken und H. influenzae Typ b sind schon der Teil der Grundimmunisierung im Kindesalter. • Humorale Immundefekte (Hypogammaglobulinämie, Aspleniesyndrom) stellen eine weitere Indikation für die Pneumokokken-, Haemophilus- und Meningococcus-Impfung dar. Die Impfung kann nur der Sepsis und der Meningitis, aber der Pneumonie nicht vorbeugen.