Hypophysenadenome
Werbung

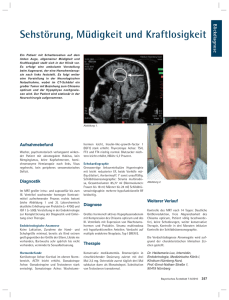
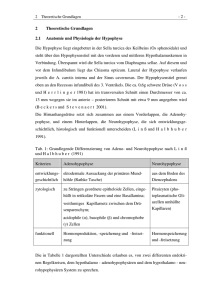
Augenärztliche Fortbildung Hypophysenadenome (Pituitary adenomas) Annette Schmidt-Bacher Augenklinik der St. Vincentius-Kliniken Karlsruhe Zusammenfassung: Die Betreuung von Patienten mit Hypophysenadenomen erfordert eine interdisziplinäre Zusammenarbeit von Augenärzten, Endokrinologen, Neuroradiologen, Neu­ rochirurgen und Strahlentherapeuten. Bei Sehstörungen mit Gesichtsfelddefekten oder Be­ einträchtigung der Okulomotorik ist der Augenarzt oft derjenige, der zur Diagnosefindung beiträgt. Aber auch im Rahmen von Verlaufsuntersuchungen unter medikamentöser, neu­ rochirurgischer oder strahlentherapeutischer Behandlung ist eine augenärztliche Untersu­ chung wichtig. Das klinische Bild von Patienten mit Hypophysenadenomen wird dadurch beeinflusst, ob und welche Hypophysen­hormonstörung vorliegt und ob durch die Größe des Hypo­physenadenoms zusätzliche Lokalsymptome vorhanden sind. Ziel dieses Artikels ist es, die verschiedenen Aspekte der interdisziplinären Betreuung von Patienten mit Hypophysen­ adenomen herauszuarbeiten. Z. prakt. Augenheilkd. 33: 347 – 358 (2012) Stichworte: Hypophysen­ adenome, Interdisziplinäre Behandlung, Gesichtsfeld­ defekte, Optische Kohärenz­ tomographie, Hypophysen­ apoplex Summary: The care of patients with pituitary adenomas needs the interdisciplinary work of different disciplines: ophthalmology, endocrinology, neuroradiology, neurosurgery and radio­therapy. For patients with ophthalmological symptoms such as visual field defects the ophthalmologist is often the first to make the diagnosis. Ophthalmological follow up examinations are necessary during medical, neurosurgical and radiotherapeutical treat­ ment. The clinical manifestations of patients with pituitary adenomas are affected by existing hormonal abnormalities and the nature of hormonal changes. Size and location of the pituitary adenoma is responsible for neurological symptoms, such as visual impairment or head­ache. The clinical presentation, evaluations and management of individual pituitary adenomas will be discussed. Z. prakt. Augenheilkd. 33: 347 – 358 (2012) Keywords: Pituitary adenomas, interdisciplinary work, visual field defect, optical coherence tomo­ graphy, pituitary apoplex Professor Dr. Gerold Kolling zum 65. Geburtstag gewidmet Hirntumore im Bereich des Chiasma opticum Im Bereich des Chiasma opticum liegen 15 bis 20 % aller Hirntumore [8]. Unter den chiasmal gelegenen Tumoren sind Hypo­ physenadenome mit 50 % die häufigsten [7]. Am zweithäufigsten sind Kraniopharyngeome mit 25 %, danach folgen Meningeome mit 10 % und Gliome mit 5 %. Bei Hypophysen­ adenomen handelt es sich um eine gutartige Neubildung hormonproduzierender Zellen der Z. prakt. Augenheilkd. 33: 347 – 358 (2012) Hypophyse. In Deutschland beträgt die Inzi­ denz von Hypophysenadenomen zirka 30 bis 40 pro einer Million Einwohner/Jahr [9]. Am häufigsten treten Hypophysenadenome im Alter zwischen 35 und 45 Jahren auf. Interdisziplinäre Zusammenarbeit Die Therapie von Hypophysentumoren er­ fordert eine interdisziplinäre Zusammen­ arbeit von Augenärzten, Neuroradiologen, Endokrinologen, Neurochirurgen und Strah­ lentherapeuten. Da ein Teil der Patienten sich aufgrund von Beeinträchtigungen des Sehens – wie z. B. Sehverschlechterung, Unabhängigkeitserklärung der Autoren: Die Autoren versichern, dass sie keine Verbindungen zu einer der Firmen, deren Namen oder Produkte in dem Artikel aufgeführt werden, oder zu einer Firma, die ein Konkurrenz­produkt vertreibt, unterhalten. Die Autoren unterlagen bei der Erstellung des Beitrages keinerlei Beeinflussung. Es lagen keine kommerziellen Aspekte bei der inhaltlichen Gestaltung zugrunde. 347 A. Schmidt-Bacher: Hypophysenadenome Auch während der Behandlung der Patienten durch Endokrinologen, Neurochirurgen und Strahlentherapeuten ist der Augenarzt ein wichtiger Partner. Abbildung 1: Mit freundlicher Genehmigung der Neuroradiologischen Klinik, Heidelberg Hypophysenadenome sind benigne Tumoren der Adenohypophyse, die nahezu alle monoklonal aufgebaut sind. Gesichtsfelddefekte oder Doppelbilder – zunächst beim Augenarzt vorstellen, ist es wichtig, dass er diese Patienten erkennt und zur geeigneten Bildgebung überweist. Auch während der Behandlung der Patien­ ten durch Endokrinologen, Neurochirurgen und Strahlentherapeuten ist der Augenarzt ein wichtiger Partner, der eine Verschlechte­ rung im Gesichtsfeld oder neu aufgetretene Störungen der Okulomotorik verifiziert und eine Verlaufs­untersuchung unter Therapie durchführt. < 10 mm, Makroadenome mit einem Durchmesser von > 10 mm (Abbildung 1) und < 40 mm und Giant-Adenome mit einem Durchmesser von > 40 mm un­ terschieden werden [2]. Die Anatomie der Sellaregion wird in Abbildung 2 ge­ zeigt. Hierbei wird deutlich, dass Mikro­ adenome, die per definitionem kleiner als 10 mm sind, aufgrund des anatomischen Ab­ standes des Chiasmas von 10 mm oberhalb der Sella keine Sehstörungen hervorrufen können. Pathogenese und klinische Einteilung von Hypopyhsenadenomen Typische Symptome von Hypophysenadenomen Die Hypophyse besteht aus Adeno- und Neurohypophyse. Hypophysenadenome sind benigne Tumoren der Adenohypophyse, die nahezu alle monoklonal aufgebaut sind. Sie entstehen durch somatische Mutation von Zellen des Hypophysenvorderlappens [1]. Exogene Faktoren spielen bei der Patho­ genese keine nennenswerte Rolle [3]. Nach der Tumorgröße können Mikro­ adenome mit einem Durchmesser von Abbildung 1: Hypophysenmakroadenom in­ tra- und suprasellär gelegen, asymmetrisch konfiguriert, den linken Uncus erreichend (MRT T1 gewichtet). 348 Typische Zeichen von Hypophysen­adenomen sind: n Lokalsymptome wie Ausfälle einzelner Hirnnerven, Gesichtsfelddefekte und zentral­ nervöse Symptome; n Hypophysen-Insuffizienz mit Mangel bzw. komplettem Ausfall eines oder mehrerer Hor­ mone der Hirnanhangdrüse; n Überproduktion einzelner Hypophysenhor­ mone. Abbildung 2: Neuroophthalmologisch relevante Strukturen und Lagebezeichnung im Be­ reich des Chiasma opticum (modifiziert nach Lang et al., 1979) Z. prakt. Augenheilkd. 33: 347 – 358 (2012) A. Schmidt-Bacher: Hypophysenadenome Gesichtsfelduntersuchung Welches Gesichtsfeldprogramm ist bei Ver­ dacht auf Gesichtsfelddefekte bei chiasma­ nah gelegenen Raumforderungen geeignet? Da zirka 70 % des Querschnitts des Chiasma opticum Informationen der zentralen 30° des Gesichtsfeldes weiterleiten, sollte ein Ge­ sichtsfeldprogramm gewählt werden, das mit lichtschwachen Stimuli die zentralen 30° des Gesichtsfeldes prüft (Abbildung 4). Die mit reiz­ starken Marken getesteten Gesichtsfeldau­ ßengrenzen können selbst bei deutlichen De­ fekten innerhalb des zentralen 30°-Bereichs noch intakt sein. Die Computerperimetrie wird routinemäßig genutzt, um Gesichtsfelddefek­ te zu erkennen und über den zeitlichen Ver­ lauf der Erkrankung quantitativ zu erfassen. Wichtige statistische Parameter sind der Mit­ telwert und die Pattern Standardabweichung. Patienten mit hormon­ inaktiven Hypophysentumoren haben signifikant häufiger Gesichtsfelddefekte als Patienten mit hormonaktiven Hypophysentumoren. Abbildung 3: Schematischer Sehbahnfaser­ verlauf im Bereich des Chiasma opticum nebst zugehörigen schematisierten Ge­ sichtsfelddefekten und deren prozentualer Häufigkeitsverteilung. Die Auswirkungen von Läsionen in verschiedenen Sehbahn­ abschnitten in Chiasmanähe auf das 30°-Ge­ sichtsfeld sind exemplarisch dargestellt: 1. z. B. kompressive Optikusläsion 2. partielle prächiasmale Läsion 3.„Anterior-junction-Syndrom“ unter (par­ tieller) Schädigung des vorderen Wilbrand‘­ schen Knies, das den kontralateralen nasal unteren Netzhaut- und somit temporal obe­ ren Gesichtsfeldquadranten repräsentiert und zusätzlich mit fortgeschrittenem oder sogar vollständigem Funktionsverlust des ipsilateralen Sehnervs einhergeht. 4. Läsion des unmittelbar zentralen Chias­ mabereichs 5. „Posterior-junction-Syndrom“ unter Schä­ digung des hinteren Wilbrand’schen Knies, das den ipsilateralen nasal oberen Netz­ haut- und somit temporal unteren Gesichts­ feldquadranten repräsentiert und zusätzlich mit einer homonymen Hemianopsie zur Ge­ genseite einhergeht. 6. Läsion des Tractus opticus Z. prakt. Augenheilkd. 33: 347 – 358 (2012) 349 (aus Schiefer U. et al.: Praktische Neuroophthalmologie, Kaden Verlag 2003) Gesichtsfelddefekte sind nur bei einem Teil der Patienten vorhanden. Nach einer Stu­ die von Wittkowski 2004 hatten 43 % von 96 Patienten, die wegen eines Hypophy­ senadenoms operiert wurden, keine Ge­ sichtsfelddefekte [10]. Patienten mit hor­ moninaktiven Hypophysentumoren haben signifikant häufiger Gesichtsfelddefekte als Patienten mit hormonaktiven Hypophysen­ tumoren. Typische Gesichtsfelddefekte sind bi­ temporale Gesichtsfelddefekte, die im obe­ ren Quadranten beginnen oder Gesichtsfeld­ defekte, die zumindest an einem Auge die Mittellinie respektieren (Abbildung 3). Lokale Irritationen durch ein Hypophysenadenom führen neben Gesichtsfelddefekten auch zu Ausfällen einzelner Hirnnerven, Kopfschmer­ zen und zentralnervösen Symptomen. A. Schmidt-Bacher: Hypophysenadenome Im Folgenden wird exemplarisch der Verlauf des Gesichtsfeldes nach operativer Entfernung eines hormoninaktiven Hypo­physenadenoms gezeigt (Abbildung 5). Optische Kohärenztomographie gibt Hinweise auf die Prognose Die optische Kohärenztomographie (OCT) mit der Messung der retinalen Nervenfaserdicke Messung (RNFL) und der Messung der Gan­ Abbildung 4a: Papillenfotos einer 70-jährigen Patientin mit Makro­adenom der Hypophyse, das in den rechten Sinus cavernosus wächst und eine leichte Kompression der A. carotis interna von kaudal hin sowie eine kraniale Verlagerung und Kompression des Chiasma und der Nervi optici verursacht. Visus rechts 0,5, links 0,4. Oben Foto der linken Papille mit horizontalerr Abblassung, unten Foto der rechten Papille mit horizontaler Blässe 350 glienzellschicht im Bereich der Makula vor einer Hypophysenoperation gibt Hinweise auf die Prognose der postoperativen Gesichts­ felddefektrückbildung (Abbildung 5b, c). Die beste Korrelation zeigte die Dicke der tem­ poralen RNFL mit der Gesichtsfeldeinschrän­ kung nach der Operation. Die Messung des Ganglienzellkomplexes, die sowohl die re­ tinalen Ganglienzellen als auch die Nerven­ faserschicht misst, ist ein weiterer wichtiger prognostischer Faktor, der mit der postopera­ Abbildung 4b: (oben) 30°- und (unten) 90°-Octopus-Gesichtsfeld der Patientin aus Ab­ bildung 4a vor Therapie mit Bromocriptin. Inkompletter bitemporaler Gesichtsfelddefekt. Z. prakt. Augenheilkd. 33: 347 – 358 (2012) A. Schmidt-Bacher: Hypophysenadenome tiven Sehschärfe eine sogar bessere Korrela­ tion zeigt als die Nervenfaserdicke [4]. Hypophysenapoplex Eine gefürchtete Komplikation eines Hypo­ physenadenoms ist die Hypophysennekrose mit Hypophysenapoplex, die zu plötzlicher beidseitiger Erblindung und Augenmuskelpa­ resen führen kann. Ein Hypophysenapoplex ist ein neurochirurgischer Notfall! Die Patien­ Abbildung 5a: Horizontale Papillenabblas­ sung R>L bei einer 37 jährigen Patientin mit hormoninaktivem Hypophysenadenom. Visusverlauf: Bei Erstuntersuchung 10/2010 rechts 0,2, links 1,0; Ende Oktober 2010 transsphenoidale Exzision des Hypophysen­ adenoms, 11/2010: rechts 0,3, links 1,0; 1/2011 rechts 0,4p, links 1,0; 8/2011 rechts 0,4, links 1,0; 2/2012 rechts 0,4, links 1,0 Z. prakt. Augenheilkd. 33: 347 – 358 (2012) ten klagen über akut aufgetretene stärkste Kopfschmerzen, akute Visusminderung bis zur Erblindung und Doppelbilder. Teilweise zusätzlich über Übelkeit und Erbrechen oder Zeichen der meningealen Reizung, teilweise über Bewußtseinseintrübung. Durch eine Ein­ blutung oder Ischämie eines Makroadenoms der Hypophyse kommt es zu akuter Vergröße­ rung der Hypophyse mit Optikuskompression und ggf. Störung der Okulomotorik. Einige Fälle von Hypophysenapoplex sind beschrie­ Ein Hypophysenapoplex ist ein neurochirurgischer Notfall! Abbildung 5 b: Spectraldomänen- OCT der Papille, Kreisscan R/L der Patientin aus 5 a. Vergleich der retinalen Nervenfaserschicht R zu L 8/2011. Man erkennt deutlich R/L die pathologische, horizontale Verdünnung der nasalen und temporalen Nervenfaserschicht sowie die Nervenfaserschicht im Gesamten. 351 A. Schmidt-Bacher: Hypophysenadenome Bei akuter Kompression des Chiasmas sollte eine sofortige neurochirurgische Dekompression erfolgen. ben, die bis hin zum Tod geführt haben [5]. Bei akuter Kompression des Chiasmas soll­ te eine sofortige neurochirurgische Dekom­ pression erfolgen, damit eine Chance auf eine Erholung des Sehvermögens besteht. Verlaufskontrollen Für die Verlaufskontrollen von Patienten mit Hypophysenadenomen sind Gesichtsfeld­ untersuchungen von entscheidender Bedeu­ tung. Zunächst muss der Ausgangsbefund dokumentiert werden. Dann sollte unter medikamentöser Behandlung oder nach neuro­chirurgischem Eingriff bei unkom­ pliziertem Verlauf nach 6 Wochen und im Verlauf des ersten Jahres in dreimonatigen Abständen eine Kontrolle erfolgen. Später sind Kontroll­intervalle in Jahresabständen notwendig. Bei komplikationslosem Verlauf können nach einem Zeitraum von 5 Jahren Untersuchungen in 2-jährlichem Abstand ausreichen. Bei hormonellen Veränderungen wie Schwangerschaft und Hormonbehand­ lung sind deutlich kürzere Untersuchungs­ intervalle erforderlich – sie sind ggf. sogar monatlich anzusetzen. Endokrinologische Aspekte von Hypophysenadenomen Der Hypophysenvorderlappen produziert Hormone, die ihrerseits peripher endokrine Drüsen steuern. Hierzu gehören das n Wachstumshormon (GH), n Prolaktin, n adrenokortikotropes Hormon (ACTH), n thyroideastimulierendes Hormon (TSH), n luteinisierendes Hormon (LH) sowie n follikelstimulierendes Hormon (FSH). Das Wachstumshormon kontrolliert den Insulin-like-growth-factor-1 (IGF-1), ACTH das Kortisol, TSH Thyroxin (T4) und LH und FSH Östrogen und Testosteron. Abbildung 5c: OCT Verlaufsuntersuchung bei Patientin aus 5a. Linkes Auge 352 Abbildung 5c: Spectral-Domänen-optische Kohärenztomographie (SD-OCT) der linken Papille respektive rechten Papille, Kreisscan Verlaufsuntersuchungen. Es zeigt sich eine horizontal verminderte Nervenfaserschicht­ dicke, die im Verlauf stabil bleibt. Bild oben: Erstuntersuchung vor transsphenoi­ daler Exzision eines Hypophysenadenoms Bild Mitte: Folgeuntersuchung 3 Monate nach Operation Bild unten: 9 Monate nach Operation Z. prakt. Augenheilkd. 33: 347 – 358 (2012) A. Schmidt-Bacher: Hypophysenadenome Hypophysenadenome können in hormon­ produzierende und nicht hormonprodu­ zierende Tumoren unterschieden werden. Endokrinaktive Tumore werden nach ihrem hypersezernierten Hormon eingeteilt. Man unterscheidet Prolaktin-, Wachstumshor­ mon-, adrenokortikotropes Hormon- produ­ zierende Tumore sowie Gonadotropin (FSH/ LH)-, TSH-sezernierende und gemischte Hypo­physenadenome. Der Hypophysenvorderlappen wird sei­ nerseits durch hypothalamische Peptide reguliert. Hierzu gehören Growth-Hormonreleasing-Hormon (GHRH), Ghrelin (Growth Hormone Release Inducing: Wachstumshor­ monfreisetzung einleitend), Somatostatin, Dopamin, Corticotropin-releasing-Hormon (CRH),Thyreotropin-releasing-Hormon (TRH) und Gonadotropin-releasing-Hormon (GnRH). Dies ist das endokrinologische Basiswissen für Hypophysentests und zur medikamentösen Therapie von hormonaktiven Hypophysentu­ moren. Die Testung der Hypophysenachsen durch Endokrinologen ist zum Beispiel bei Pa­ tienten mit Hypophysentumoren, nach Ope­ ration oder Bestrahlung der Sellaregion oder nach Schädel-Hirn-Trauma sinnvoll und nötig. Die klinischen Symptome eines erhöhten Prolaktinspiegels sind bei Frauen Menstrua­ tionsstörungen, Galaktorrhoe, bei Frauen und Männern Libidoabnahme und Infertilität. Die typischen Symptome einer Akromegalie sind im Kindesalter Gigantismus und im höheren Erwachsenenalter bei neu auftretender Akro­ megalie Vergröberung der Gesichtszüge und Verknöcherungen der vorspringenden Teile des Gesichts (Nase, Überaugenwülste und Unterkiefer). Weichteile wie Lippen, Zunge, Kehlkopf und Finger können fleischig an­ schwellen. Bei Kindern beschleunigt ein erhöh­ ter Wachstumshormon-Spiegel den Schluss der Wachstumsfugen der Knochen und das Längenwachstum des Körpers. 10 – 20 % der Patienten mit Akromegalie entwickeln einen Diabetes mellitus, da durch das Wachstums­ hormon die Regulierung des Blutzuckerspie­ gels gestört wird. Z. prakt. Augenheilkd. 33: 347 – 358 (2012) Therapie von Hypophysentumoren Die Behandlung erfolgt je nach Hypopysen­ tumor medikamentös, chirurgisch oder ra­ diotherapeutisch. Die Therapie ist abhängig von der Größe des Tumors. Eine Operation ist bei suprasellären Makroadenomen mit Chiasma­syndrom, bei suprasellären Makro­ adenomen ohne Chiasmasyndrom und ge­ planter Schwangerschaft und bei suprasellä­ rem Makroadenom ohne Chiasmasyndrom Die Behandlung erfolgt je nach Hypopysentumor medikamentös, chirurgisch oder radiotherapeutisch. Abbildung 5c: OCT Verlaufsuntersuchung bei Patientin aus 5a. Rechtes Auge 353 A. Schmidt-Bacher: Hypophysenadenome Prolaktinome werden primär medikamentös mit Dopamin­ agonisten behandelt, hierunter kommt es bei den meisten Prolaktinomen zu einer deutlichen Senkung des Prolaktinspiegels und zur Schrumpfung des Tumors. mit Dopamin-Agonisten-Unverträglichkeit angezeigt [8]. Die medikamentöse Behand­ lung von Hypophysenadenomen lässt sich in die eigentliche pharmakologische Thera­ pie und die Hormonsubstitution gliedern. Die Pharmakotherapie wird derzeit vorwiegend bei den Prolaktinomen oder den HGH-sezernie­ renden Adenomen eingesetzt. Dabei stehen hauptsächlich die Dopaminagonisten und die Somatostatin­analoga zur Verfügung. Dopaminagonisten Prolaktinome werden primär medikamentös mit Dopaminagonisten behandelt, hierunter kommt es bei den meisten Prolaktinomen zu einer deutlichen Senkung des Prolaktin­ spiegels und zur Schrumpfung des Tumors. Das Präparat zeigt seinen Wirkungsbeginn binnen 72 Stunden [5]. Ist bereits eine parti­ elle Optikusatrophie eingetreten, so wird es zu keiner Verbesserung des Gesichtsfeldes Abbildung 5 d: 30° Compu­ ter-Perimetrie linkes Auge (OS) und rechtes Auge (OD) bei Erstuntersuchung mit in­ kompletter, rechts betonter, inkongruenter, bitemporaler Hemianopsie. Mittlere Sen­ sitivität (MS): rechts 13,8 dB, links 22,4 dB; Mittlerer Defekt (MD): rechts 14,2 dB, links 5,5 dB 354 Z. prakt. Augenheilkd. 33: 347 – 358 (2012) A. Schmidt-Bacher: Hypophysenadenome Abbildung 5e: 30° Compu­ ter-Perimetrie linkes Auge (OS) und rechtes Auge (OD) mit inkompletter, inkongru­ enter, bitemporaler Hemian­ opsie. 3 Monate nach neurochirur­ gischem, transsphenoidalem Eingriff sieht man eine deut­ liche Befundbesserung der Gesichtsfelddefekte. Mittlere Sensitivität: (MS) rechts 26,3 dB, links 23,3 dB; Mittlerer Defekt: (MD) rechts 1,6 dB, links 4,6 dB Abbildung 5f: 9 Monate postoperativ zeigt sich ein weitgehend stabiler Befund der bitemporalen Hemian­ opsie. Mittlerer Defekt (MD) rechts 2,3 dB, links 4,6 dB Abbildung 5g: 15 Monate nach Hypophysentumor­ exzison ist es zu einer Rückbildung der Tiefe der Gesichtsfelddefekte mit in­ kompletter, inkongruenter, bitemporaler Hemianopsie gekommen. Mittlerer Defekt (MD) rechts 0,8 dB, links 3,8 dB Z. prakt. Augenheilkd. 33: 347 – 358 (2012) 355 A. Schmidt-Bacher: Hypophysenadenome Die Somatostatinanaloga (z. B. Octreotid) stellen die wirksamsten Medikamente zur Behandlung der Akromegalie dar. Der Augenarzt sollte an den Neurochir­urgen Anamnese, aktuelle ophthalmologische Befunde, bereits vorliegende Zusatzbefunde und eine zusammenfassende Beurteilung weitergeben. kommen. Wird ein Prolaktinom jedoch früh erkannt, können sich Gesichtsfelddefekte innerhalb eines Jahres zurückbilden. Dopaminagonisten wirken über den Dopa­ min-D2-Rezeptor-Subtyp hemmend auf die Ausschüttung von Prolaktin aus der Adeno­ hypophyse. Zu den Dopamin­agonisten der ersten Generation zählt Bromocriptin (Pravi­ del®); zu den Präparaten der zweiten Gene­ ration Cabergolin (Dostinex®) und Quinagolid (Norprolac®). Vorteile der Präparate der zwei­ ten Generation sind die längere Wirksamkeit und bessere Verträglichkeit. Typische Nebenwirkungen unter der Thera­ pie mit Dopaminagonisten sind: Übelkeit, Er­ brechen, orthostatische Dysregulation, sel­ tener Obstipation, Schwindel und Schwel­ lung der Nasenschleimhaut. Somatostatinanaloga Die Somatostatinanaloga (z. B. Octreotid) stellen die wirksamsten Medikamente zur Behandlung der Akromegalie dar. Jedoch Exemplarische Krankengeschichte Ein Beispiel aus dem klinischen Alltag ist die Erkrankung einer 28-jährigen Frau, die sich notfallmäßig in der Sprechstunde vor­ stellte, da sie erstmalig 3 Tage zuvor neu aufgetretene Doppel­ bilder beim Blick in die Ferne bemerkt hatte. Bei regelrechtem Visus und Gesichtsfeld bestand in der Ferne ein manifestes In­ nenschielen rechts mit einem Schielwinkel sowohl bei Rechtsals auch bei Linksfixation von simultan C6°, alternierend C8°. In der Nähe bestand ein manifestes Innenschielen mit C3° simultan und C6° alternierend. Beim Blick nach rechts war der Schielwinkel bei C5°, beim Blick nach links C8,5°. Die Motilität war beidseits 30° über der Mittellinie. Auf Nachfrage berichtete die Patientin über Schwindel und Kopfschmerzen in den letzten Tagen. Ein kraniales MRT (Abbildung 1) zeigte ein intra- und supraselläres Hypophysenadenom mit Verlagerung des linken Uncus. Die Bestimmung des Prolaktinspiegels ergab eine mehr als 100-fache Erhöhung (103 705, Normwert 60 – 620). Hiermit konnte die Diagnose eines Prolaktinoms gesichert und die Therapie mit Dopamin­agonisten begonnen werden. 356 sollte bei Wachstumshormon produzie­ renden Tumoren primär die Operation an­ gestrebt werden [8]. Somatostatinanaloga normalisieren den IGF-1-Spiegel bei 66 % der Patienten. Bei Unverträglichkeit der me­ dikamentösen Therapieformen oder bei Ver­ sagen dieser Therapie ist der Wachstums­ hormonantagonist Pegvisomant zugelassen und erreicht eine Normalisierung des IGF-1Spiegels bei 90 % der Patienten mit Akro­ megalie. Nur noch selten kommen zusätzlich Dopamin­agonisten zur Sekretionshemmung des Wachstumshormons zum Einsatz. Eine Hypophyseninsuffizienz kann sowohl partiell als auch vollständig (Panhypo­pituitarismus) auftreten und prä- und/oder postopera­ tiv vorkommen. Die Substitutionstherapie richtet sich nach der Stärke und der Art der Achsenausfälle. Die kortikotrope und thyre­ otrope Achse sind lebenswichtig und sollten in jedem Fall mit Hydrokortison bzw. Schild­ drüsenhormonen ersetzt werden. Die Dosis­ anpassung ist dabei individuell vorzuneh­ men und muss beim Hydrokortison körper­ lichen Belastungen bzw. Stress­situationen angepasst werden. Ein Ausfall der gonadotropen Achse wird beim Mann durch die Gabe von Testosteron und bei der Frau durch Östrogen/Gestagen­ präparate substituiert. Neurochirurgische Aspekte der Behandlung von Hypophysen­ tumoren Ziel der operativen Behandlung ist die se­ lektive Adenomektomie unter Erhaltung der Hypophysenfunktion. Der Augenarzt sollte an den Neurochir­urgen Anamnese, aktuelle ophthalmologische Be­ funde, bereits vorliegende Zusatzbefunde und eine zusammenfassende Beurteilung weiter­ geben. Ist es noch zu keiner Optikus­atrophie gekommen, bestehen gute Chancen, dass sich Visusminderung, Farbentsättigung und Gesichtsfelddefekte nach einem neurochirur­ gischen Eingriff wieder verbessern können [8]. Z. prakt. Augenheilkd. 33: 347 – 358 (2012) A. Schmidt-Bacher: Hypophysenadenome Operation transnasal transsphenoidal oder transkranial Es stehen zwei Zugangswege zur Verfügung, die transnasale transsphenoidale Operation und die transkraniale Operation. Die Mehr­ zahl der Patienten (90 %) kann transnasal operiert werden. Eine transkraniale Operati­ on ist nötig bei großen, asymmetrisch nach suprasellär, retrosellär und subfrontal entwi­ ckelten Hypophysenadenomen (10 %). Der Zugang erfolgt über einen Bügelschnitt hinter der Stirn-Haar-Grenze, transkranial über eine Trepanation mit einem kleinen fronto-lateralen Knochendeckel, ggf. mit Erweiterung nach temporal (pterionaler Zugang). Bei subfrontal entwickelten Hypo­physenadenomen sowie bei größeren supra- und retrosellär entwi­ ckelten Tumoren ist der Zugang eine kleine subfrontale Trepanation. Die Häufigkeit und Schwere von Komplikati­ onen korrelieren mit der Größe des Tumors. Komplikationen sind Liquorfisteln, Meningi­ tiden, Nachblutung und Hormonstörungen. Sehverschlechterungen treten nach trans­ sphenoidalen Operationen sehr selten auf (<0,5 %), nach transkranialen Operationen bei 10 – 20 % der Patienten [6]. Als wesentliche Kriterien für den Behand­ lungserfolg dienen die erhobenen Resttumorund Rezidivraten. Für beide Merkmale finden sich im Schrifttum extrem große Variabilitäten von zirka 10 % bis über 80 % [10]. Strahlentherapeutische Optionen der Therapie Falls operative und medikamentöse Be­ handlungsmaßnahmen nicht ausreichen, kann die fraktionierte Strahlentherapie ein­ gesetzt werden. Die Radiochirurgie wirkt rascher und stärker als die fraktionierte Z. prakt. Augenheilkd. 33: 347 – 358 (2012) Strahlentherapie und kann bei inoperablen Adenomresten oder Rezidiven eingesetzt werden. Als weitere strahlentherapeutische Option kommt die Hochpräzisionsstrahlen­ therapie infrage, die heutzutage in der Regel die stereotaktische Methode benutzt, d. h. ein Koordinatensystem zur Lokalisation der Zielstruktur. Die fraktionierte, stereotakti­ sche Strahlentherapie steht für größere Adenome und solche, die das optische System erreichen, zur Verfügung. Fazit Bitemporale Gesichtsfelddefekte oder Ge­ sichtsfelddefekte, die zumindest an einem Auge die Mittellinie respektieren, lassen ei­ nen chiasmanah gelegenen Tumor vermuten. Falls der Tumor das Chiasma opticum noch nicht erreicht hat, aber in den Sinus caverno­ sus gewachsen ist, können Doppelbilder und Kopfschmerzen die wegweisenden Sympto­ me zur Diagnose sein. Hypophysenadenome sind die häufigsten chiasmanah gelegenen Tumoren. Unter den Hypophysenadenomen finden sich am häu­ figsten Prolaktinome. Bei Hypophysentumo­ ren ist die Therapie von der Größe und dem Typ des Hypophysenadenoms abhängig. Bei suprasellären Hypophysenmakroadeno­ men mit Chiasmasyndrom ist in der Regel eine Operation angezeigt [5]. Diese wird bei 90% der Patienten transnasal, transspheno­ idal durchgeführt. Bei großen asymmetrisch nach suprasellär, retrosellär und subfrontal entwickelten Hypophysenadenomen (10%) ist ein transkranialer Zugang erforderlich. Falls operative und medikamentöse Behand­ lungsmaßnahmen nicht ausreichen, kann die Strahlentherapie eingesetzt werden. Bitemporale Gesichtsfeld­ defekte oder Gesichtsfeld­ defekte, die zumindest an einem Auge die Mittellinie respektieren, lassen einen chiasmanah gelegenen Tumor vermuten. ➝ 357 A. Schmidt-Bacher: Hypophysenadenome Literatur Korrespondenzadresse: Dr. med. Annette Schmidt-Bacher Augenklinik der St. Vincentius-Kliniken Steinhäuserstraße 18 76135 Karlsruhe E-Mail: [email protected] 358 1. Buchfelder M (1999) Hypophysenadenome. Der On­ kologe 5: 94 – 102 2. Hardy J (1979) Transsphenoidal microsurgical treat­ ment of pituitary tumors In: Recent advances in the diagnosis and treatment of pituitary tumors (Hrsg: Linfoot JA) S. 375 – 388. Raven Press, New York 3. Jipp P (2001) Erkrankungen endokriner Organe. Thieme, Stuttgart 4. Moon CH, Hwang SC, Kim B-T, Ohn Y-H, Park TK (2011) Visual prognostic value of optical coherence tomography and photopic negative response in chi­ asmal compression. IOVS 52: 8527 – 8533 5. Noble JD (2006) Pituitary apoplexy goes tot he bar: litigation for delayed diagnosis, deficient vision, and death. J Neuro-Ophthalmol 26: 128 – 133 6. Petersenn S et al (2006) Therapie von Hypophysen­ tumoren. Dtsch Ärztebl 103: A 474 – 481 7. Sanno N et al (2003) Pathology of pituitary tumors. Neurosurg Clin N Am 14: 25 – 39 8. Schiefer U, Wilhelm H, Zrenner E, Burk A (2003) Praktische Neuroophthalmologie, Kaden, Heidelberg 9. Stalla GK (2001) Der aufmerksame Hausarzt erkennt die Frühsymptome. MMW. Fortschr Med 143: 908 10.Wittkowski B (2004) Ergebnisse nach chirurgischer Behandlung von Hypophysenadenomen. Eine retrospektive Analyse des Krankengutes der Uni­ versitätsklinik und Poliklinik für Neuro­chirurgie an der Martin-Luther-Universität Halle-Wittenberg der Jahre 1996 – 2001, Halle/Saale, Dissertation. Med Fak der MLU Halle-Wittenberg Z. prakt. Augenheilkd. 33: 347 – 358 (2012)