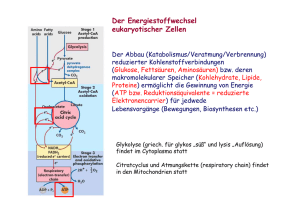
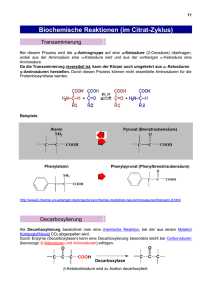
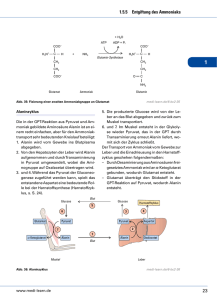
Leseprobe - Beck-Shop
Werbung

103 7.1 Einführung A 7 7.1 Oxidativer Abbau von Pyruvat: Die Reaktionen der Pyruvat-Dehydrogenase und des Citratzyklus 7 Oxidativer Abbau von Pyruvat: Die Reaktionen der Pyruvat-Dehydrogenase und des Citratzyklus Einführung 7.1 Einführung Die Abbauwege aller Kohlenhydrate vereinigen sich letztlich in der Glykolyse und führen zu deren Endprodukt, dem Pyruvat. Im Rahmen des Energiestoffwechsels kann Pyruvat anschlieûend entweder reduziert oder oxidiert werden: n Reduktion zu Lactat im Zytosol unter Regeneration von NAD+: bei Mangel an Sauerstoff oder Fehlen von Mitochondrien. n Oxidation zu CO 2 in den Mitochondrien, wenn in einer Zelle hinreichende Mengen an Sauerstoff vorhanden sind. Dabei wird Pyruvat zunächst von der Pyruvat-Dehydrogenase (PDH) zu Acetyl-CoA umgesetzt. Dieses wird anschlieûend im Citratzyklus unter Energiegewinn zu CO2 abgebaut. Die Details dieses Abbauweges werden hier beschrieben. E Merke. Die Reaktionen der PDH und des Citratzyklus nehmen eine zentrale Pyruvat entsteht im Zytosol aller Zellen des Körpers als Endprodukt der Glykolyse. Dieses Kapitel beschreibt, wie es in Gegenwart von Sauerstoff in den Mitochondrien von der Pyruvat-Dehydrogenase zu Acetyl-CoA und dann im Citratzyklus unter Energiegewinn zu CO2 oxidiert wird. F Merke Stellung im Stoffwechsel ein, denn n Pyruvat ist nicht nur das Endprodukt der Glykolyse, sondern auch des Abbaus aller kleinen Aminosäuren (Glycin [R = H], Alanin [R = CH3], Serin [R = OH] und Cystein [R = SH]). n Acetyl-CoA entsteht nicht nur in den Reaktionen der PDH, sondern auch beim Abbau der Aminosäuren Lysin, Leucin und Isoleucin sowie der aromatischen Aminosäuren. Acetyl-CoA ist darüber hinaus der zentrale Metabolit des gesamten Lipidstoffwechsels: Es ist das Endprodukt des Abbaus aller Fettsäuren und die Ausgangssubstanz für die Synthese aller Fettsäuren und aller Steroide (Cholesterin, Gallensäuren und Steroidhormone). n Beim Abbau der anderen, oben nicht aufgeführten Aminosäuren entstehen Zwischenprodukte des Citratzyklus. Der Weg von der Glykolyse über die PDH bis zum Citratzyklus (Abb. A-7.1) stellt somit den zentralen Abbauweg des gesamten Stoffwechsels dar. A-7.1 Die Stellung der PDH zwischen Glykolyse und Citratzyklus Glykolyse O Pyruvat H3C C COO– Zytosol Mitochondrien NAD+ HS Coenzym A PyruvatDehydrogenase NADH CO2 O Acetyl-CoA H3C C S Coenzym A Acetylgruppe Citratzyklus Rassow, Hauser, Netzker, Deutzmann, Duale Reihe, Biochemie (ISBN 3131253517), ã 2006 Georg Thieme Verlag KG A-7.1 104 E Exkurs A-7.2 A 7 Die Reaktionen der Pyruvat-Dehydrogenase und des Citratzyklus E Exkurs. Der Energieträger Acetyl-CoA Für die vielfältigen Funktionen des Acetyl-CoA ist es von entscheidender Bedeutung, dass die Thioesterbindung, über die die Acetylgruppe an das Coenzym A gebunden ist (Abb. A-7.1), zu den energiereichen Bindungen gehört. Unter Standardbedingungen wird bei der Hydrolyse von Acetyl-CoA genauso viel Energie frei wie bei der Hydrolyse von ATP (!), nämlich ca. 35 kJ/Mol. Dieser Energiegehalt des Acetyl-CoA kommt auch in dem inzwischen nur noch selten verwendeten Synonym ¹aktivierte Essigsäureª zum Ausdruck. Viele grundlegende Untersuchungen zur Biochemie des Acetyl-CoA wurden in den beiden Jahrzehnten nach dem 2. Weltkrieg im Labor von Feodor Lynen durchgeführt, dem bedeutendsten deutschen Biochemiker seiner Zeit. Geboren 1911 in München, leitete er ab 1954 in seiner Heimatstadt das neu gegründete Max-Planck-Institut für Zellchemie, aus dem später das Max-Planck-Institut für Biochemie hervorging. 1964 erhielt er für seine Arbeiten zum Acetyl-CoA und zur Biochemie der Lipide den Nobelpreis für Physiologie/Medizin. Feodor Lynen starb im Jahr seiner Emeritierung, am 6. August 1979 in München. A-7.2 Feodor Lynen (1911 ± 1979) Für seine Arbeiten zum Acetyl-CoA und zur Biochemie der Lipide erhielt Feodor Lynen 1964 den Nobelpreis für Physiologie/Medizin. 7.2 Die Pyruvat-Dehydrogenase (PDH) 7.2 Die Pyruvat-Dehydrogenase (PDH) 7.2.1 Grundlagen 7.2.1 Grundlagen Funktion: n Pyruvat ? Acetyl-CoA + CO 2 n 1 NAD+ ? NADH Funktion: Die PDH n setzt Pyruvat unter Freisetzung von CO 2 zu Acetyl-CoA um. n Dabei wird ein NAD+ zu NADH reduziert. E Merke 7.2.2 Der Aufbau der Pyruvat-Dehydrogenase E Merke E Merke. Die Reaktion der PDH ist irreversibel. Acetyl-CoA kann also nicht in Pyruvat bzw. Glucose umgesetzt werden. Kohlenhydrate können zwar zu Acetyl-CoA abgebaut und aus diesem können Fettsäuren und Triacylglycerine (Fettspeicher!) synthetisiert werden, aber aus Fettsäuren bzw. Triacylglycerinen können keine Kohlenhydrate gebildet werden. 7.2.2 Der Aufbau der Pyruvat-Dehydrogenase E Merke. Die PDH ist ein Multienzymkomplex aus drei unterschiedlichen Enzymen und im Mitochondrium lokalisiert. Zur Katalyse ihrer Reaktionen benötigt die PDH insgesamt fünf Coenzyme (Tab. A-7.1). Rassow, Hauser, Netzker, Deutzmann, Duale Reihe, Biochemie (ISBN 3131253517), ã 2006 Georg Thieme Verlag KG A 105 7.2 Die Pyruvat-Dehydrogenase (PDH) Die drei Enzymkomponenten (E1, E2, E3) sind: n E1 = Pyruvat-Dehydrogenase im engeren Sinne des Wortes: Sie bindet Pyruvat und katalysiert mithilfe des Coenzyms Thiaminpyrophosphat (TPP) die Decarboxylierung von Pyruvat. Dabei entsteht CO2. n E2 = Dihydroliponamid-Acetyltransferase: Sie katalysiert den Transfer des vom Pyruvat übrig gebliebenen Acetylrests auf Coenzym A (CoA). Hierbei werden zwei Schwefelatome ihres Coenzyms Liponsäure (Liponamid) zu SH-Gruppen reduziert. n E3 = Dihydroliponamid-Dehydrogenase: Sie übernimmt mithilfe ihres Coenzyms FAD die Elektronen der beiden SH-Gruppen des Liponamids und überträgt sie auf NAD+. Auf diese Weise wird das Liponamid regeneriert. A-7.1 Die Enzymkomponenten der Pyruvat-Dehydrogenase und ihre Coenzyme Enzymkomponente Coenzym Beschaffenheit des Coenzyms (enzymgebunden/löslich) PyruvatDehydrogenase (E1) Thiaminpyrophosphat (TPP) = aktiviertes Thiamin (Thiamin = Vitamin B1) Liponsäure (Liponamid) enzymgebunden (feste, aber nichtkovalente Bindung) DihydroliponamidAcetyltransferase (E2) DihydroliponamidDehydrogenase (E3): Coenzym A FAD NAD+ A-7.1 enzymgebunden (kovalent: Amidbindung an einen Lysinrest von E2, daher ¹Liponamidª) löslich enzymgebunden (feste, aber nichtkovalente Bindung) löslich Neben diesen drei Enzym-Untereinheiten enthält die PDH zwei regulatorische Untereinheiten, die die PDH je nach Bedarf an- bzw. abschalten (S. 109). Die meisten Untereinheiten der PDH sind in einem PDH-Multienzymkomplex in mehreren (bis zu 60) Kopien enthalten. Die Komplexe sind dadurch gröûer als ein Ribosom (Abb. A-7.3). A-7.3 Die PDH ist ein Multienzymkomplex aus 3 Enzymen (E1 ± 3) und 5 Coenzymen; Tab. A-7.1): n E1 = Pyruvat-Dehydrogenase im engeren Sinne: enthält TPP, decarboxyliert Pyruvat. n E2 = Acetyltransferase: enthält Liponsäure (Liponamid), überträgt den Acetylrest auf CoA. n E3 = Dihydroliponamid-Dehydrogenase: enthält FAD, übernimmt Elektronen vom reduzierten Liponamid des E2 und überträgt sie auf NAD+. Bakterielle PDH-Komplexe im elektronenmikroskopischen Bild Rassow, Hauser, Netzker, Deutzmann, Duale Reihe, Biochemie (ISBN 3131253517), ã 2006 Georg Thieme Verlag KG Auûerdem enthält die PDH zwei regulatorische Untereinheiten. Der PDH-Multienzymkomplex ist gröûer als ein Ribosom (Abb. A-7.3). A-7.3 106 A 7.2.3 Die einzelnen Reaktionsschritte 7.2.3 Die einzelnen Reaktionsschritte E Überblick 7 Die Reaktionen der Pyruvat-Dehydrogenase und des Citratzyklus E Überblick. Die PDH-Reaktion läuft in folgenden Schritten ab: 1. Pyruvat wird unter Abspaltung von CO2 auf Thiaminpyrophosphat (Coenzym von E1) übertragen. Dabei entsteht ein Hydroxyethylrest = aktivierter Acetaldeyd. 2. Dieser wird von Thiaminpyrophosphat (E1) auf Liponamid (Coenzym von E2) übertragen und zu einer Acetylgruppe oxidiert. 3. Liponamid überträgt die Acetylgruppe auf Coenzym A, wodurch Acetyl-CoA entsteht. Dabei wird die Disulfidgruppe des Liponamids in zwei SH-Gruppen umgewandelt. 4. Die Disulfidgruppe des Liponamids wird regeneriert, indem das Elektron jeder SH-Gruppe unter Vermittlung von E3-gebundenem FAD an NAD+ abgegeben wird. Dabei wird NADH gebildet. Da die PDH sowohl die Decarboxylierung des Pyruvats als auch die Oxidation des aktivierten Acetaldehyds katalysiert, bezeichnet man die Gesamtreaktion als oxidative Decarboxylierung von Pyruvat. Schritt 1 Schritt 1 Der Thiazolring des Thiaminpyrophosphats (TPP) gibt leicht ein Proton ab, wodurch ein Carbanion entsteht (Abb. A-7.4). Thiaminpyrophosphat (TPP), das Coenzym der Pyruvat-Dehydrogenase (E1), weist zwei heterozyklische Ringe auf. Für die Coenzym-Funktion ist der Thiazolring entscheidend. Das C-Atom, das in diesem Thiazolring zwischen dem Stickstoff- und dem Schwefelatom liegt, gibt leicht ein Proton ab, sodass ein negativ geladenes und sehr reaktives Carbanion entsteht (Abb. A-7.4). Dieses Carbanion leitet die PDH-Reaktion ein, indem es sich an den Carbonylkohlenstoff von Pyruvat anlagert und anschlieûend auf die Elektronen des Pyruvats einen kräftigen Elektronenzug ausübt. Dieser Elektronenzug wirkt sich insbesondere auf die negative Ladung der Carboxylgruppe aus, was zur Folge hat, dass sich die Carboxylgruppe in Form von CO2 ablöst. Dabei bleiben zwei Elektronen der Carboxylgruppe am TPP zurück. Parallel lagert sich ein Proton an den Sauerstoff der Carbonylgruppe an, und es bildet sich eine Doppelbindung zu TPP aus. Dadurch entsteht Hydroxyethyl-TPP (Abb. A-7.5). Der Hydroxyethylrest wird traditionell ¹aktivierter Acetaldehydª genannt, denn die Oxidationsstufe des Carbonylkohlenstoffs in HydroxyethylTPP entspricht der Oxidationsstufe des entsprechenden C-Atoms im Acetaldehyd. Dieses lagert sich an den Carbonylkohlenstoff von Pyruvat an und übt auf dessen Elektronen, insbesondere die der COOHGruppe, einen kräftigen Elektronenzug aus. Dabei löst sich CO2 ab. Weiteres Reaktionsprodukt ist Hydroxyethyl-TPP (Abb. A-7.5), dessen Hydroxyethylgruppe als ¹aktivierter Acetaldehydª bezeichnet wird. A-7.4 A-7.4 Das Carbanion des Thiaminpyrophosphats O CH2 CH3 CH2 N H3C N NH2 N CH2 O P O– O O P O– S R1 C H Thiaminpyrophosphat (TPP) R2 CH3 O– N S C Thiazolring des TPP als Carbanion (nach Ablösung eines H+) Rassow, Hauser, Netzker, Deutzmann, Duale Reihe, Biochemie (ISBN 3131253517), ã 2006 Georg Thieme Verlag KG 107 7.2 Die Pyruvat-Dehydrogenase (PDH) A Bildung von Hydroxyethyl-Thiaminpyrophosphat (an Enzymkomponente E1) A-7.5 S S S S + CO2 COO– O A-7.5 C E2 TPP E1 CH3 FAD E3 Pyruvat PDH HO C E2 TPP E1 CH3 FAD E3 Hydroxyethyl-TPP, „aktivierter Acetaldehyd“ Schritt 2 Schritt 2 Der aktivierte Acetaldehyd wird von TPP auf Liponamid, die fest gebundene prosthetische Gruppe der Dihydroliponamid-Acetyltransferase (E2), übertragen: n Die Disulfidgruppe des Liponamids, die vor dem Transfer im oxidierten Zustand vorliegt, öffnet sich. n An eines der beiden Schwefelatome lagert sich der Acetaldehyd an. Das andere Schwefelatom nimmt zusammen mit einem Proton die beiden überzähligen Elektronen auf, die bei der Abspaltung des CO2 am TPP zurück geblieben waren. Der aktivierte Acetaldehyd wird auf Liponamid ± prosthetische Gruppe der Dihydroliponamid-Acetyltransferase (E2) ± übertragen und zur Acetylgruppe oxidiert (Abb. A-7.6). Der Acetaldehyd wird in diesem Moment zu einer Acetylgruppe oxidiert (Abb. A-7.6). In der Acetylgruppe entspricht die Oxidationsstufe des Carbonylkohlenstoffs der Oxidationsstufe des entsprechenden C-Atoms in Acetat (d. h. in Essigsäure). Somit kann man sagen, dass in diesem Reaktionsschritt ein Acetaldehyd zu Acetat oxidiert wird. Das Acetat liegt allerdings nicht frei, sondern in Form eines Thioesters vor. Übertragung des Hydroxyethylrests auf Liponamid und Oxidation zu einem Acetylrest A-7.6 O oxidierte Form des Liponamids H3 C C A-7.6 reduzierte Form des Liponamids S S S Acetyl- HS gruppe HO C E2 TPP CH3 Hydroxyethylgruppe E1 FAD E3 PDH E2 TPP E1 FAD E3 Oxidation des Substrats zur Acetylgruppe Schritt 3 Schritt 3 Liponamid ist ein lang gestrecktes Molekül, das man sich wie einen langen Arm vorstellen kann. Dieser lange Arm überträgt die Acetylgruppe auf Coenzym A (CoA). Acetyl-CoA (= aktivierte Essigsäure) entsteht also an der Dihydroliponamid-Acetyltransferase (E2). Das Liponamid enthält daraufhin anstelle der ursprünglichen Disulfidgruppe zwei SH-Gruppen (Abb. A-7.7). Liponamid, das Coenzym des E2, überträgt die Acetylgruppe auf Coenzym A (CoA) (Abb. A-7.7) und wird dadurch reduziert. Rassow, Hauser, Netzker, Deutzmann, Duale Reihe, Biochemie (ISBN 3131253517), ã 2006 Georg Thieme Verlag KG 108 A 7 Die Reaktionen der Pyruvat-Dehydrogenase und des Citratzyklus A-7.7 Übertragung der Acetylgruppe auf Coenzym A A-7.7 O H3C C Dihydroliponamid reduzierte Form des Liponamids S HS HS O HS + H3C C S CoA Acetyl-CoA HS E2 TPP E1 CoA FAD E2 TPP E1 E3 FAD E3 Schritt 4 Schritt 4 Das reduzierte Liponamid des E2 wird von E3 durch Reaktion mit der prosthetischen Gruppe FAD oxidiert und so regeneriert. FADH2 überträgt die 2 Elektronen auf NAD+, sodass NADH entsteht (Abb. A-7.8). Um seine beiden SH-Gruppen zu oxidieren und die Disulfidbindung zu regenerieren, schwenkt der Liponamid-Arm zur Dihydroliponamid-Dehydrogenase (E3). Hier werden die beiden SH-Gruppen durch Reaktion mit der prosthetischen Gruppe FAD oxidiert. Dabei entsteht FADH2, das die beiden übertragenen Elektronen an NAD+ weitergibt (Abb. A-7.8). Das Reaktionsprodukt NADH enthält nun die beiden überzähligen Elektronen, die ursprünglich bei der Abspaltung des CO2 am TPP zurück geblieben waren. Liponamid steht nun für einen neuen Reaktionszyklus zur Verfügung. A-7.8 A-7.8 Regeneration der Disulfidbindung im Liponamid und Bildung von NADH Dihydroliponamid SH SH S S S S + NADH + H+ NAD+ E2 TPP E1 FAD E3 E2 TPP E1 FADH2 E3 E2 TPP E1 FAD E3 Reduktion des FAD Bilanz Bilanz E Merke E Merke. In einem Reaktionszyklus der PDH entstehen ein CO2, ein AcetylCoA und ein NADH. E Exkurs E Exkurs. Enzyme mit PDH-ähnlichen Reaktionsmechanismen Im Stoffwechsel gibt es mehrere Enzyme, deren Reaktionsmechanismus dem der PDH sehr ähnlich ist und die auch die gleichen Coenzyme benötigen. Zu den Enzymen dieses Reaktionstyps gehören n die verzweigtkettige á-Ketosäure-Dehydrogenase, ein Enzym, das am Abbau verzweigtkettiger Aminosäuren beteiligt ist, n die Transketolase des Pentosephosphatweges, n die á-Ketoglutarat-Dehydrogenase (2-Oxoglutarat-Dehydrogenase), die eine Reaktion des Citratzyklus katalysiert (S. 115). Rassow, Hauser, Netzker, Deutzmann, Duale Reihe, Biochemie (ISBN 3131253517), ã 2006 Georg Thieme Verlag KG