Chiralität und Leben
Werbung
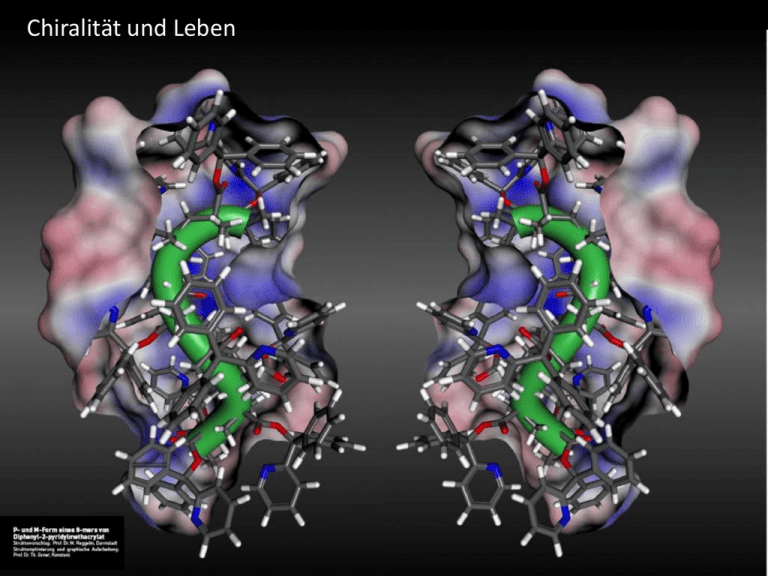
Chiralität und Leben Symmetrie: „Ebenmaß“ Geometrie: Bestimmte Operationen bilden Objekt auf sich selbst ab (dabei bleibt es quasi unverändert) • • • • • Rotationssymmetrie Achsensymmetrie - Spiegelsymmetrie Punktsymmetrie Translationssymmetrie Kugelsymmetrie Physik: Bestimmte Transformationen lassen eine physikalische Entität unverändert. Mit Symmetrien sind Erhaltungsgrößen verbunden – Noether-Theorem Translationsinvarianz Impulserhaltung Zeitinvarianz Energieerhaltung Rotationsinvarinanz Drehimpulserhaltung Moleküle und Symmetrie Die meisten organischen Moleküle existieren in Form von Isomeren Isomerie: Gleiche Summenformel – unterschiedliche räumliche Strukturen Butan: 𝐶4 𝐻10 Zwei Isomere mit unterschiedlichen physikalischen und chemischen Eigenschaften. Siedetemperatur 0.5° und -12° C Alkane ... • • • mit 15 Kohlenstoffatomen bringen es auf 4347 Isomere mit 25 Kohlenstoffatomen bringen es auf 36797588 Isomere und mit 40 Kohlenstoffatomen bringen es gar auf 62491178805831 Isomere. Spiegelsymmetrie Optisch aktive Substanzen In anorganischen Reaktionen werden rechts – und linkshändische Moleküle im Mittel gleich oft erzeugt. 1808 Louis Malus Polarisation 1813 Jean-Baptiste Biot opt. Aktivität 1843 Louis Pasteur Racematspaltung 1902 Emil Fischer (Nobelpreis 1902) Stereochemie der Kohlenwasserstoffe Chiralität Ein Gegenstand, der mit seinem Spiegelbild nicht zur Deckung gebracht werden kann, wird als chiral bezeichnet. Objekte, die sich mit ihrem Spiegelbild zur Deckung bringen lassen, werden als achiral bezeichnet. Moleküle, die sich zueinander wie Bild und Spiegelbild verhalten und sich nicht zur Deckung bringen lassen, nennt man Enantiomere (aus dem Griechischen enantio + meros: entgegengesetzte Teile). Chirale Moleküle besitzen • keine Symmetrieebene (Spiegelebene) im Molekül und • kein Symmetriezentrum (Spiegelpunkt). Verbindungen, welche die Ebene des polarisierten Lichtes drehen, bezeichnet man als optisch aktiv. Chirales Molekül Natrium-Ammonium-Tartrat (1847, Louis Pasteur) Nichtchirales Molekül Alle 20 proteinogenen Aminosäuren kommen nur in links-händischer Form in Lebewesen vor • Alle diese Aminosäuren sind mit Ausnahme von Glycin chiral • Bei ihnen handelt es sich Ausnahmslos um 𝛼-Aminosäuren (d.h. die Aminogruppe hängt am 2. Kohlenstoffatom) Die räumliche Struktur von biologisch erzeugten Proteinen muß nicht unbedíngt chiral sein. Die Struktur bestimmt aber ganz wesentlich deren biologische Funktion. Das betrifft insbesondere die Wirkung von Enzymen und anderen Wirkstoffen, die Enantiomere bilden. L=laevus=Links D=dexter=Rechts Beispiel: Thalidomid D-Thalidomid macht schläfrig L-Thalidomid führt zu massiven Mißbildungen von Feten Thalidomid wurde Ende der 50ziger und Anfang der 60ziger Jahre als Racemid verkauft mit dramatischen Folgen... DNA - Desoxribonukleinsäure „Rechts-händige“ B- und Z-DNA kommen in der Natur (Lebewesen) vor „Links-händige“ B- und Z-DNA kommen in der Natur nicht (Lebewesen) vor Kohlenhydrate (Zucker) In der Natur kommt fast ausschließlich D-Glukose vor. In Lebewesen kommen rechtshändische Kohlenwasserstoffe vor Die Biosynthese sowie die enzymatischen Abbaureaktionsketten, die in den Zellen wirken, sind auf D-Kohlenhydrate ausgerichtet. Lebewesen Aminosäuren linkshändisch Desoxribonukleinsäuren rechtshändisch Kohlenhydrate rechtshändisch „Homochiralität biologischer Moleküle“ CHIRALITÄTSPROBLEM Theorien zur Erklärung des Chiralitätsproblems Beobachtung: In allen Urey-Miller-Experimenten entstanden immer racemische Biomoleküle (d.h. z.B. L- und D-Aminosäuren in gleicher Konzentration) Zufall Lokal Theorie Determiniert Universal Es ist reiner Zufall, der nur jeweils eine „Sorte“ von Biomolekülen preferiert hat. Dieser „Zufall“ hat irgendwann während der Chemischen Evolution stattgefunden. Es ist kein Zufall, sondern die Preferenz ist durch Naturgesetze vorgegeben (z.B. Paritätsverletzung der Schwachen Wechselwirkung). Universelle Lösung? Paritätsverletzung bei schwach wechselwirkenden Prozessen Wu-Experiment 1957 Chien-Shiung Wu (1912-1997) Tsung Dao Lee + Chen Ning Yang Nobelpreis 1957 • Man erwartet, daß die Elektronen sowohl in Kernspinrichtung als auch entgegengesetzt emittiert werden • Der Spin ist ein axialer Vektor, der gegenüber einer Raumspiegelung invariant ist – Drehimpuls dreht sich aber um - Spiegelung: Rechtsschraube -> Linksschraube • Experiment: Elektronen werden bevorzugt entgegengesetzt zum Kernspin emittiert -> Verletzung der Spiegelsymmetrie Frage: Kann die Verletzung der Spiegelinvarianz bei schwacher Wechselwirkung bis auf die molekulare Ebene durchschlagen? Weitere Beobachtungen zum Chiralitätsproblem Untersuchung kohliger Chondrite: Beispiel Murchinson (Australien, 1969) • Es wurden mehr als 80 unterschiedliche Aminosäuren entdeckt, wobei nur wenige davon auch in irdischen Proteinen vorkommen • Detailuntersuchungen haben gezeigt, daß manche Aminosäuren (z.B. Isovalin) in nicht-racemischer Mischung vorkommen -> Chiralitätsexzess (L-Form bis zu 9% häufiger als R-Form) Fragen: • Durch welche abiotischen Prozesse kommt es zu diesem Chiralitätsexzess? • Inwieweit überträgt sich ein Chiralitätsexzess bei biochemischen Reaktionen auf die Reaktionsprodukte? -> Isovalin+Glycoaldehyd+Formaldehyd -> Threose (Zucker) Auch der entstehende Zucker zeigte einen Überschuß an der L-Form. Warum??? Das Chiralitätsproblem ist weiterhin ungelöst