Erfolgreiche Optimierung einer Chemotherapie mittels
Werbung

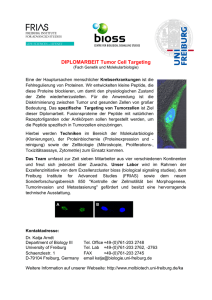
FO RT B I LDU N G Chemosensitivitätsprüfung ZIRKULIERENDE TUMORZELLEN Erfolgreiche Optimierung einer Chemotherapie mittels Chemosensitivitätsprüfung an zirkulierenden Tumorzellen C. Weigl1, C. Rabenstein1, U. Pachmann1, K. Pachmann1,2. Im hier vorgestellten Fall wird gezeigt, wie die chemotherapeutische Behandlung einer 73-jährigen Patientin mit beidseitigem Ovarialkarzinom mittels Chemosensitivitätstestung begleitet, überwacht und individuell angepasst werden konnte. Die Sensitivitätstests erfolgten an im Blut zirkulierenden Tumorzellen. Da diese die aktuellen Eigenschaften des Primärtumors widerspiegeln, können die daraus gewonnenen Daten erfolgreich auf die chemotherapeutische Behandlung der Patientin und das systemische Verhalten des Tumors extrapoliert werden. Damit hätte in diesem Fall nicht nur eine Progression der Krankheit unter schlecht wirksamen Chemotherapeutika frühzeitig entdeckt werden können, die zirkulierenden Tumorzellen halfen auch bei der anschließenden Auswahl eines wirksamen Medikamentes. Einleitung Die Chemotherapie ist nach wie vor eine der drei Säulen der Behandlung von Karzinomen. Zur Auswahl der eingesetzten Medikamente stehen dem Arzt nur statistisch abgeleitete Daten über deren Wirksamkeit aus vorangegangenen Studien zur Verfügung [1]. Hieraus lässt sich nicht zwangsläufig ein optimales Ansprechen für den einzelnen Patienten ableiten. Wird ein Patient mit weniger wirksamen Medikamenten therapiert, muss er die erheblichen Nebenwirkungen einer Chemotherapie ertragen, ohne den bestmöglichen therapeutischen Erfolg daraus zu ziehen. Ein vielversprechender Ansatz ist es, die Chemosensitivität der Tumorzellen für jeden Patienten vor einer entsprechenden Behandlung individuell zu bestimmen. Es gibt Ansätze in der Brustkrebsbehandlung, das Ansprechen auf eine neoadjuvante Medikation als in vivo Chemosensitivitätstest heranzuziehen [2-4]. Da neoadjuvante Chemotherapien bei manchen Brustkrebstypen in einem hohen Prozentsatz zu einer pathologisch kompletten Remission führen, werden sie immer häufiger auch bei operablen Tumoren der Brust eingesetzt [2]. Allerdings wird dadurch nicht immer das rezidivfreie Überleben verbessert. Es gibt Hinweise, dass eine neo-adjuvante Therapie bei Patientinnen mit triple-negativem Tumor zu höheren Rezidiv-Raten führen kann als eine adjuvante Therapie [5]. Eine neue Möglichkeit, die Chemosensitivität des Tumors zu bestimmen, basiert auf dem Einsatz von zirkulierenden Tumorzellen [6], im folgenden CETCs (circulating epithelial tumor cells) genannt. Diese CETCs werden vom Primärtumor während seines Wachstums kontinuierlich in Lymphund Blutgefäße abgegeben [7]. Der große diagnostische Vorteil dieser zirkulierenden Tumorzellen besteht darin, dass sie die Eigenschaften der Gesamttumorlast im Körper widerspiegeln [8]. Tumorverdächtige Zellen, welche in einer Patienten-Blutprobe identifiziert werden, können direkt auf ihre Sensitivität für die jeweils geplanten Medikamente untersucht werden. In dem folgenden Fall soll dargestellt werden, welche Vorteile diese Methode für die individuelle Behandlung haben könnte. Methoden Die Tumorzellen aus Patientenblut wurden, wie bereits publiziert [9], lediglich durch die Lyse der roten Blutzellen und einen Zentrifugationsschritt aufbereitet. Dafür wurde 1 ml Blut mit 15 ml Lysepuffer für 15 min im Kühlschrank inkubiert und anschließend bei 700 g abzentrifugiert. Tumorzellen wurden über ihre epithelialen Eigenschaften mittels EpCAM (epithelial cell adhesion molecule; CD326) – ein anti-epithelialer Antikörper konjugiert mit Fluoresceinisothiocyanat (FITC) – erfasst. Absterbende Zellen wurden mittels Propidiumjodid, wodurch nur der Kern von Zellen mit einer permeablen Membran, die sich in der Absterbephase befinden, angefärbt wurde, identifiziert. 100 μl der Zellsuspension wurden anschließend unter Zellkulturbedingungen mit den in Frage kommenden Medikamenten inkubiert. Zum Test der Effektivität des Medikamentes wurden alle weißen Blutzellen des Pellets aus 100 µl Blut verschiedenen Konzentrationen des zu untersuchenden Medikaments ausgesetzt. Die mittlere Konzentration entsprach der Tagesdosis, berechnet auf 5 Liter Blut, zusätzlich wurden die 10fache und die 1/10fache Konzentration getestet. Als Vergleich wurde ein Kontrollansatz ohne Medikamente gemessen. Die Zellen wurden unter diesen Bedingungen für bis zu neun Stunden inkubiert, wobei der zytotoxische Effekt nach jeweils drei, sechs und neun rbeitsgruppe Transfusionsmedizinisches Zentrum A Bayreuth (Arge. TZB) 2 Universitätsklinikum Jena 1 www.journalonko.de 285 JOURNAL ONKOLOGIE 4/2014 Leberprogress 11 Progress EoC 10 7 6 x CarbPl Pax 100.000 9 Die Ergebnisse zeigten bereits, im Gegensatz zur Messung vom 17.03.2010, bei den ersten Tests von 21.06.2010 ein verringertes Ansprechen der Zellen auf Carboplatin und Paclitaxel. Im weiteren Verlauf sinkt 8 6 5 4 3 1 2 1.000.000 Fallbericht 6 x CarbPl Pax pegyliertes Doxorubicin 10.000 1.000 100 23.01.2011 15.10.2010 07.07.2010 100 90 80 70 60 50 40 30 20 10 0 Carbo Pac Jan. 2011 Dez. 2010 Nov. 2010 Okt. 2010 Sep. 2010 Jul. 2010 Aug. 2010 Jun. 2010 Mai 2010 Apr. 2010 Feb. 2010 Doxo Mrz. 2010 b) 29.03.2010 10.09.2009 10 Nov. 2009 Die Ergebnisse dieses Vorgehens und ihre klinische Relevanz sollen im Fall einer 73-jährigen, weiblichen Patientin mit beidseitigem Ovarialkarzinom (Figo IV mit Leber und Milzherden ED 16.09.2009) dargestellt werden. Nach der operativen Teilsanierung vom 19.10.2009 begann der erste Behandlungszyklus der Chemotherapie am 19.11.2009 mit einer Kombination aus Carboplatin und Paclitaxel im Abstand von jeweils drei Wochen. Zusätzlich erfolgte zu jedem Behandlungszyklus eine Bestimmung der CETCs aus dem Blut der Patientin. Die Werte der einzelnen Bestimmungen sind in Abbildung 1a dargestellt. Während dieser ersten Chemotherapie schwankten die CETC-Werte, gemessen nach jedem Behandlungszyklus, deutlich. Nach einem anfänglichen Anstieg bis zum dritten Zyklus auf 2.720 Da die Patientin eine weitere Operation ablehnte, wurde am 21.06.2010 eine erneute Behandlung mit Carboplatin und Paclitaxel begonnen, wobei man am vorhergehenden Schema festhielt. Vor Beginn dieser folgenden Chemotherapie wurden keine CETCWerte bestimmt. Die nächste Messung stammt vom 12.07.2010, vor dem zweiten Zyklus des neuen Therapieblocks. Zusätzlich wurden am 12.07.2010, 23.08.2010, 30.11.2010 und am 11.01.2011 Chemosensitivitätstestungen nach dem oben beschriebenen Verfahren durchgeführt. Neben den bereits eingesetzten Medikamenten wurde Doxorubicin, normalerweise ein Medikament der Second-Line-Therapie, in die Tests miteinbezogen. EoC a) 19.12.2009 Zur quantitativen Analyse der Zellen half das Image Analysis System des scan^R (Olympus Hamburg, Deutschland) zur wiederholten Auswertung jeweils des gleichen Areals. Ansprechrate (%) 286 Jan. 2010 Die Anzahl der lebenden und toten CETCs wurde zu jedem Zeitpunkt sowohl im Vergleichsansatz wie auch in den verschiedenen Konzentrationen der Medikamentenansätze bestimmt. Aus dem Quotienten zwischen den einzelnen Ansätzen mit dem Vergleichsansatz wurde der Anteil der durch das Medikament zerstörten CETCs berechnet. einer 100%igen Wirkung überzeugen. Carboplatin hatte eine Chemosensitivität von 83%, Paclitaxel nur 53%. Die Klinik zeigte einen partiellen Erfolg dieser Behandlung. So konnte am 17.03.2010 eine Regredienz der vorliegenden intrahepatischen Metastasierung sowie eine deutliche Regredienz der Metastasierung der Milz festgestellt werden. Allerdings trat an anderer Stelle ebenfalls eine progrediente, plumpe Darstellung der linken Nebenniere auf. Therapiebegleitend wurde am 17.03.2010 die Chemosensitivität der eingesetzten Medikamente an den CETCs bestimmt (Abb. 1b). Die Ergebnisse sprachen für den in der Klinik beobachteten Krankheitsverlauf. Keines der Medikamente konnte mit Dez. 2009 1. Lebende Leukozyten ohne Fluoreszenzfärbung; nur im Durchlicht sichtbar 2. Tote Leukozyten mit permeabler Membran, durch die Propidiumjodid in die Zelle eindringen kann und daraus resultierende rote Fluoreszenz im Kern 3. Lebende epitheliale (und damit Tumor-) Zellen; nur durch den FITCkonjugierten EpCAM-Antikörper mit grüner Fluoreszenz angefärbt 4. Tote Tumorzellen, die sowohl eine grüne EpCAM-Färbung wie auch eine rote Propidiumjodid-Kernfärbung aufwiesen. CETCs/ml Blut fielen sie vor dem vierten Zyklus wieder auf 700 CETCs/ ml Blut ab. Darauf folgten 2.270 CETCs/ml Blut nach Zyklus vier und 1.220 CETCs/ml Blut nach Zyklus 5. Nach dem sechsten Zyklus, also nach Ende dieser ersten Therapie, zeigten die CETCs einen Spitzenwert von 7.800 CETCs/ml Blut. Beobachtet man den kompletten CETC-Verlauf dieser ersten Chemotherapie zeigt sich insgesamt ein sägezahnartiger Anstieg von zu Beginn 250 Zellen/ml Blut auf 7.800 Zellen/ml Blut zum Ende. ED Stunden bestimmt wurde. Es wurde nach folgenden Kriterien unterschieden: ZIRKULIERENDE TUMORZELLEN Chemosensitivitätsprüfung Anzahl Zellen pro ml Blut FO RTB IL DUN G Abb. 1: a) Verlauf der zirkulierenden Tumorzellen, b) Prozentuale Sensitivität der CETCs im Verlauf der Therapie. ED=Erstdiagnose, EoC=Zyklusende Chemosensitivitätsprüfung ZIRKULIERENDE TUMORZELLEN die Paclitaxel-Wirkung sogar nahezu auf 0%. Die Wirkung von Carboplatin verbesserte sich in den folgenden Messungen nicht ausreichend um das Fortschreiten der Tumorerkrankung aufzuhalten (siehe Abb. 1b). Vergleicht man hierzu die CETCs wird ein deutlicher Zusammenhang sichtbar. Auf den ersten Therapiezyklus sprach der Tumor noch relativ gut an. Die zirkulierenden Tumorzellen wurden auf einen relativ niedrigen Wert gesenkt. Daraufhin stiegen sie allerdings in den folgenden Messungen wieder fast exponentiell an, sogar höher als nach der ersten Chemotherapie. Die klinische Untersuchung vom 14.09.2010 zeigte eine Progredienz mit einer ausgedehnten abdominalen Metastase sowie Leber- Milz- und Lymphknoten-Metastasen. Weitere Veränderungen waren vereinbar mit einer ausgeprägten mesenterialen Metastasierung sowie einer Peritonealkarzinose. Wegen fortschreitender Progression des Tumors wurde die Therapie am 15.11.2010 abgebrochen und zum 30.11.2010 auf pegyliertes Doxorubicin (Caelyx®) umgestellt. Die Therapie wurde 14 tägig bis 17.01.2011 gegeben. Da dieses Medikament sich in fast allen Chemosensitivitätstests durch eine nahezu 100%ige Wirksamkeit auszeichnete, ist die folgende Verbesserung des Krankheitsprozesses nachvollziehbar. Die CETCs sanken am 11.01.2011 wieder erst auf einen Wert von 4.150 Zellen/ml Blut und am 31.01.2011 auf 490 Zellen/ml Blut. Allerdings wurde nach Ende der Therapie am 02.03.2011 erneut ein Leberprogress bei der Patientin festgestellt. Diskussion In mehreren Publikationen wurde gezeigt, dass die zirkulierenden Tumorzellen zur effektiven Bestimmung des Krankheitsverlaufs genutzt werden können [10-12]. Der hier vorgestellte Fall zeigt sowohl, wie eine zusätzliche Chemosensitivitätsprüfung an den CETCs eine laufende Chemotherapie noch wirkungsvoller optimieren könnte, als auch den Zusammenhang zwischen dem Ansprechen der CETCs auf Medikamente in der Chemosensitivität und dem klinischen Ansprechen. Im vorliegenden Fall wurden sowohl die Verlaufsbestimmung der CETCs für das Therapiemonitoring wie auch die Chemosensitivitätsprüfung durchgeführt. Innerhalb der ersten, sechszyklischen Chemotherapie zeigte sich ein sägezahnförmiger, insgesamt jedoch stetig steigender CETC-Verlauf. Diagnostisch wurde gegen Ende dieses ersten Behandlungsabschnitts eine teilweise Regredienz eines Teils der Metastasen festgestellt. An anderen Stellen war ein Progress nicht auszuschließen. In diesem Fall konnte die erste Chemotherapie die Tumorzellen nicht komplett eliminieren. Dieser Krankheitsverlauf lässt sich eventuell mit der gemessenen Chemosensitivität der eingesetzten Medikamente erklären. Danach waren initial 83% der im Körper vorhandenen Tumorzellen sensitiv auf Carboplation, 53% auf Paclitaxel. Damit wurden möglicherweise an manchen Tumorherden Erfolge erzielt, an anderen Herden ergab sich jedoch offenbar keine Wirkung. Durch Elimination der empfindlichen Tumorzellen konnten die resistenten Zellen eventuell besser wachsen. Somit kam es trotz der Regredienz an einigen Stellen zum Progress an anderen, mit einer steigenden Tendenz in der Anzahl CETCs und anschließender genereller Verschlechterung des Krankheitsbildes. Ein mögliches Self-Seeding durch zirkulierende Tumorzellen könnte ebenfalls die Krankheitsentwicklung erklären. Kim et al. konnten im Mausmodell zeigen, dass im Blut zirkulierende Tumorzellen wieder in den Primärtumor oder vorliegende Metastasen einwandern und sich dort festsetzen können [13]. Möglicherweise wurden aus den regredienten Tumorherden vitale Zellen ausgeschwemmt, die an anderen Stellen im Körper neue Metastasen gebildet haben. In der darauf folgenden Behandlungsphase zeigte sich erneut ein deutlicher Anstieg der CETCs. Die Klinik bestätigte ebenfalls einen Progress der Krankheit. Diese Ergebnisse entsprachen der Resistenz der Tumorzellen im Chemosensitivitätstest gegen die eingesetzten Medikamente. Von den beiden eingesetzten Medikamenten FO RT B I LDU N G zeigte Paclitaxel an den CETCs so gut wie keine Wirkung. In allen vier Versuchen wurden durch das Medikament im Durchschnitt nicht mehr als 10% der Zellen abgetötet. Carboplatin zeigte eine etwas bessere Wirkung. Die klinischen Untersuchungsdaten wie auch das Ergebnis der Sensitivitätstestung legen den Schluss nahe, dass diese Medikamentenkombination in der zweiten Chemotherapie nicht mehr in der Lage war, den Tumor effektiv zu bekämpfen. Zusätzlich zu den beiden Chemotherapeutika wurde noch das Medikament Doxorubicin während des Krankheitsverlaufs auf seine Wirksamkeit getestet. Erstaunlicherweise wiesen die vier Chemosensitivitätstests für Doxorubicin eine fast 100%ige Wirksamkeit auf. Wegen des Krankheitsprogresses am Ende der Carboplatin/Paclitaxel-Therapie wurde die Medikation auf pegyliertes Doxorubicin umgestellt. Darunter reduzierte sich die Zahl der CETCs deutlich. Diese Tendenz setzte sich fort. Damit zeigte das pegylierte Doxorubicin die durch die Chemosensitivitätsprüfung bestimmte Wirkung auch in vivo. Nach Ende der pegylierten Doxorubicintherapie erlitt die Patientin erneut einen Leberprogress. Möglicherweise hätte die Patientin von einer längeren Therapie mit Doxorubicin weiter profitiert. Ein weiterer Vorteil der Chemosensitivitätstets an CETCs besteht darin, dass die Sensitivität eventueller Mikrometastasen, aus welchen ebenfalls zirkulierende Tumorzellen in die Blutbahn abgeben, durch den Sensitivitätstest miterfasst werden können [14]. Wird daher eine Therapie nach den Ergebnissen dieser Tests ausgelegt, werden diese oft unentdeckten Metastasen möglicherweise ebenfalls wirksam bekämpft. Eine chemosensitivitätskonforme Behandlung von Patienten erscheint daher erstrebenswert. Bereits die ersten Sensitivitätstests unter der zweiten Chemotherapie belegten die überlegene Wirkung von pegylierten Doxorubicin deutlich. Möglicherweise hätte eine frühere Gabe des pegylierten Doxorubicin den Progress der Krankheit aufhalten oder zumindest verlangsamen können. www.journalonko.de 287 FO RTB IL DUN G Fazit Mit diesem Fall konnten wir die Vorteile einer therapieunterstützenden Chemosensitivitätstestung an CETCs darstellen. Es könnten die wirksamsten Medikamente ausgewählt werden, um dem Patienten die Nebenwirkungen einer wirkungsärmeren Chemotherapie zu ersparen. Der behandelnde Arzt muss seine Therapieentscheidung nicht mehr nur auf statistische Studiendaten gründen, sondern kann die eingesetzten Medikamente individuell auf den Patienten zuschneiden. AUTO R Christian Weigl Transfusionsmedizinisches Zentrum Bayreuth Kurpromenade 2 95448 Bayreuth ZIRKULIERENDE TUMORZELLEN Chemosensitivitätsprüfung A B S TR AC T C. Weigl1, C. Rabenstein1, U. Pachmann1, K. Pachmann1,2 The case reported here demonstrates how the chemotherapy of a 73-year-old woman with ovarian carcinoma was monitored and might have been optimized through repeated testing of tumor chemosensitivity on circulating epithelial tumor cells (CETCs) from peripheral blood. Since the characteristics of the CETCs reflect the features of the primary tumor, the obtained results can be used for the systemic chemotherapy. Therefore, not only the progression of the disease under insufficient chemotherapeutic drugs could have been early detected in our case, the CETCs also contributed to find more effective agents. 1 Arbeitsgemeinschaft TZB, 2Universitätsklinikum Jena Keywords: circulating epithelial tumor cells, CETCs, chemosensitivity 5.Fisher CS, Ma CX, Gillanders WE, et al. 10.Pachmann K, Camara O, Kohlhase A, et al. As- Neoadjuvant Chemotherapy Is Associated sessing the Efficacy of Targeted Therapy Using with Improved Survival Compared with Circulating Epithelial Tumor Cells (CETC): The Adjuvant Chemotherapy in Patients with Example of SERM Therapy Monitoring as a Triple-Negative Breast Cancer Only after Unique Tool to Individualize Therapy. J Can- Complete Pathologic Response. Ann Surg cer Res Clin Oncol 2011; 137(5):821-828, Oncol 2012; 19(1):253-258. doi:10.1245/ Tel: 0921/850 200 E-Mail: [email protected] Literatur 288 1.Bonadonna G, Moliterni A, Zambetti M, et s10434-011-1877-y. doi:10.1007/s00432-010-0942-4. 11. Pierga JY, Bidard FC, Mathiot C, et al. Cir- 6.Rudiger N, Stein ER, Schill E, et al. Chemo- culating Tumor Cell Detection Predicts sensitivity Testing of Circulating Epithelial Early Metastatic Relapse After Neoadjuvant Tumor Cells (CETC) in Vitro: Correlation to Chemotherapy in Large Operable and Lo- in Vivo Sensitivity and Clinical Outcome. cally Advanced Breast Cancer in a Phase II JCT 2013; 4(2):597-605, doi:10.4236/ Randomized Trial. Clin Cancer Res 2008; jct.2013.42077. 14(21):7004-7010. doi: 10.1158/1078- al. 30 years’ follow up of randomised studies 7.Camara O, Rengsberger M, Egbe A, et al. of adjuvant CMF in operable breast cancer: The relevance of circulating epithelial tu- 12.Pachmann K, Camara O, Kroll T, et al. Efficacy cohort study. BMJ 2005; 330(7485):217-0. 0432.CCR-08-0030. mor cells (CETC) for therapy monitoring control of therapy using circulating epithelial 2. Fisher B, Bryant J, Wolmark N, et al. Effect during neoadjuvant (primary systemic) tumor cells (CETC) as “Liquid Biopsy”: Trastu- of preoperative chemotherapy on the out- chemotherapy in breast cancer. Ann Oncol zumab in HER2/neu-positive breast carcinoma. come of women with operable breast can- 2007; 18(9):1484-1492. doi:10.1093/an- J Cancer Res Clin Oncol 2011; 137(9):1317- cer. J Clin Oncol 1998; 16(8):2672-2685. nonc/mdm206. 1327. doi:10.1007/s00432-011-1000-6. 3. Spanheimer PM, Carr JC, Thomas A, et al. 8.Ashworth TR. A case of cancer in which 13. Kim MY, Oskarsson T, Acharyya S, et The response to neoadjuvant chemothe- cells similar to those in the tumours were al. Tumor Self-Seeding by Circulating rapy predicts clinical outcome and incre- seen in the blood after death. Aust Med J Cancer Cells 2009; 139(7):1315-1326. ases breast conservation in advanced bre- 1869; 14(3):146-149. ast cancer. Am J Surg 2013; 206(1):2-7. doi:10.1016/j.cell.2009.11.025. 9. Pachmann K, Clement JH, Schneider 14. Hekimian K, Meisezahl S, Trompelt K, CP, et al. Standardized quantification of et al. Epithelial Cell Dissemination and 4.Shannon C, Smith I. Is there still a role for circulating peripheral tumor cells from Readhesion: Analysis of Factors Contri- neoadjuvant therapy in breast cancer?. Crit lung and breast cancer. Clin Chem Lab buting to Metastasis Formation in Breast Rev Oncol Hematol 2003; 45(1):77-90. Med 2005; Cancer. ISRN Oncol 2012; 2012:601810. doi:10.1016/S1040-8428(02)00091-4. CCLM.2005.107. doi:10.1016/j.amjsurg.2012.10.025. JOURNAL ONKOLOGIE 4/2014 43(6):617-27. doi:10.1515/ doi:10.5402/2012/601810.