Diagnostik und Therapie in der Nuklearmedizin
Werbung
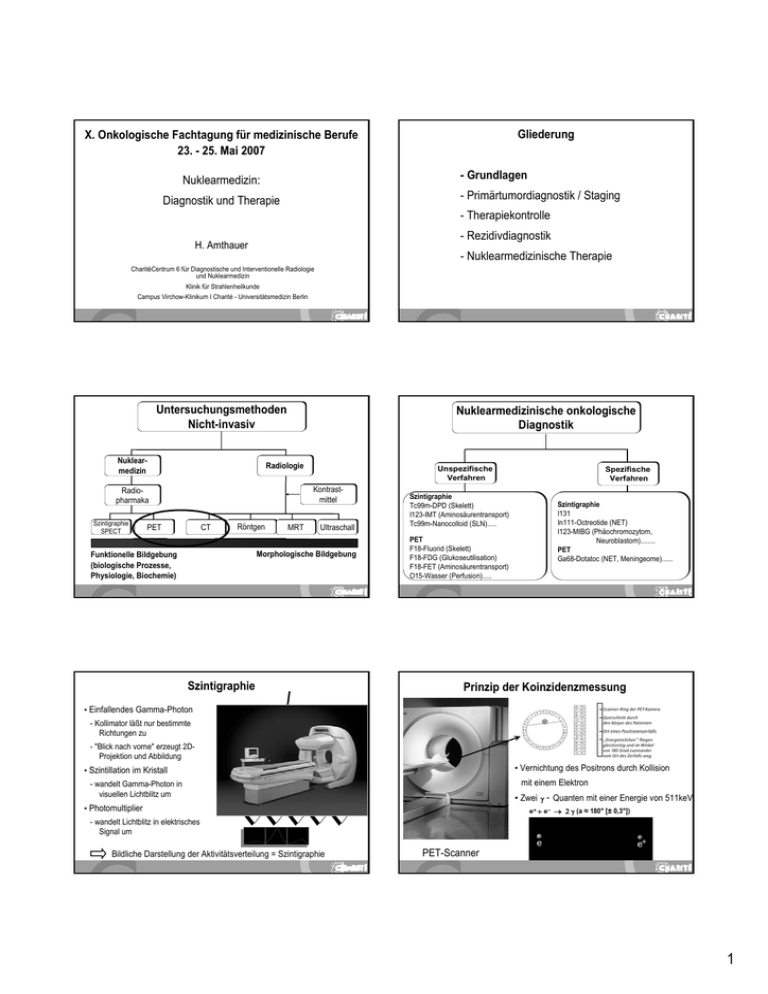
Gliederung X. Onkologische Fachtagung für medizinische Berufe 23. - 25. Mai 2007 - Grundlagen Nuklearmedizin: - Primärtumordiagnostik / Staging Diagnostik und Therapie - Therapiekontrolle - Rezidivdiagnostik H. Amthauer - Nuklearmedizinische Therapie CharitéCentrum 6 für Diagnostische und Interventionelle Radiologie und Nuklearmedizin Klinik für Strahlenheilkunde Campus Virchow-Klinikum I Charité - Universitätsmedizin Berlin Untersuchungsmethoden Nicht-invasiv Nuklearmedizin Nuklearmedizinische onkologische Diagnostik Radiologie Kontrastmittel Radiopharmaka Szintigraphie SPECT Unspezifische Verfahren PET CT Röntgen MRT Ultraschall Morphologische Bildgebung Funktionelle Bildgebung (biologische Prozesse, Physiologie, Biochemie) Szintigraphie Szintigraphie Tc99m-DPD (Skelett) I123-IMT (Aminosäurentransport) Tc99m-Nanocolloid (SLN)..... PET F18-Fluorid (Skelett) F18-FDG (Glukoseutilisation) F18-FET (Aminosäurentransport) O15-Wasser (Perfusion)..... Spezifische Verfahren Szintigraphie I131 In111-Octreotide (NET) I123-MIBG (Phäochromozytom, Neuroblastom)........ PET Ga68-Dotatoc (NET, Meningeome)...... Prinzip der Koinzidenzmessung • Einfallendes Gamma-Photon - Kollimator läßt nur bestimmte Richtungen zu - "Blick nach vorne" erzeugt 2DProjektion und Abbildung • Vernichtung des Positrons durch Kollision • Szintillation im Kristall mit einem Elektron - wandelt Gamma-Photon in visuellen Lichtblitz um • Zwei γ - Quanten mit einer Energie von 511keV • Photomultiplier e+ + e− → 2 γ (a ≈ 180° [± 0,3°]) - wandelt Lichtblitz in elektrisches Signal um Bildliche Darstellung der Aktivitätsverteilung = Szintigraphie PET-Scanner 1 Vergleich Szintigraphie und PET Tomographische Bildgebung Funktion vs. Anatomie • 56 j. Patientin • ED Mammakarzinom 03/2005 • Frage nach ossären Metastasen Komplementäre Charakteristika Vorteile PET: - höhere Sensitivität - Möglichkeit der Quantifizierung - 3D-Darstellung PET CT / MRT Sensitivität picomolar (10-12 M) milli-/mikromolar (10-2/10-6 M) Räumliche Auflösung > 3,5 mm (18F) < 1 mm Potenzielle Synergien R 3D-MIP L PET mit F18-Fluorid R anterior L L posterior R Skelettszintigraphie mit Tc99m-DPD PET-CT PET-CT CT PET „Washer and Drier“ Strahlenexposition in Deutschland Effektive Jahresdosis der Bevölkerung durch ionisierende Strahlung Effektive Dosen der Bild gebenden Verfahren 2 Gliederung Statistische Änderung der Lebenserwartung Ionisierende Strahlung vs. andere Risiken des täglichen Lebens - Grundlagen Lebenserwartung (Tage) Ursache Alkoholismus Ledig bleiben Männer Rauchen Ledig bleiben Frauen Rauchen 30% Übergewicht Passivrauchen -432 -350 -240 -1600 -1425 -130 -50 Strahlung 1 mSv pro Jahr, lebenslang 10 mSv einmalig 1 mSv einmalig - Primärtumordiagnostik / Staging - Therapiekontrolle - Rezidivdiagnostik - Nuklearmedizinische Therapie -19 -3 -0,5 Anlegen von Sicherheitsgurten Verfügbarkeit von Notarztwagen +50 +125 Lungenkarzinome 18F-FDG-PET • 44.000 Erkrankungen/Jahr in Deutschland Otto Heinrich Warburg (1883-1970) 1931 Nobelpreis für Medizin Professur für Physiologie Charité - Humboldt-Universität zu Berlin • Hauptursache: kontinuierliche Belastung durch Rauchen Glukose Plasma FDG Sarcoplasma Glucoso-6-Phosphat Glykolyse • Frühberentung: 31.000/Jahr GLUT 1-7 Hexokinase Phosphorylierung ATP, Pyruvat Ribose, NADPH Glykolyse Ribose, NADPH ATP, Pyruvat Nicht-kleinzelliges Lungenkarzinom Stage TNM Überleben IA T1 N0 M0 67% IB IIA T2 N0 M0 T1 N1 M0 T2 N1M0 T3 N0 M0 57% 55% IIB IIIA IIIB IV T3 N1 M0 T3 N2 M0 T4 N0-2 M0 T1-4 N3 M0 Tn Nn M1 • Arbeitsunfähigkeitstage: 17 Millionen FDG-6-Phosphat Pentosephosphatweg 39% • 85-90% der Patienten versterben an der Erkrankung Nicht-kleinzelliges Lungenkarzinom - TNM Staging Frage: Lymphknoten- bzw. Fernmetastasen? 23% 5% 1% Mountain et al. Chest 1997 Lababede et al. Chest 1999 3 FDG-PET-CT: Lungenkarzinom FDG-PET-CT: Lungenkarzinom 66j. Pat., Plattenepithelkarzinom pT2b ED 09/03 Gliederung FDG-PET-CT: Lungenkarzinom Fazit - Grundlagen - Primärtumordiagnostik / Staging PET-CT verbessert die diagnostische Schärfe - Therapiekontrolle • Änderung des Therapiemanagements in 30% - Rezidivdiagnostik • Vermeidung nichtkurativer Thoraxoperationen in 21% - Nuklearmedizinische Therapie Wechalekar et al. Clinical Radiology 2005 PLUS Study, Lancet 2002 Therapiekontrolle mit FDG: Rationale • FDG-Aufnahme ~ Proliferationsaktivität Glukose - Energielieferant und Quelle für die de novo Synthese von Aminosäuren, Lipiden und Nukleinsäuren Hodgkin Lymphome • Inzidenz 6/100.000/a • 2 Altersgipfel: 20-35 Jahre u. 50-55 Jahre HD9 • FDG-Aufnahme ~ Anzahl vitaler Tumorzellen • FDG-Metabolismus ist quantifizierbar Reduzierung der FDG Aufnahme ~ Untergang von Tumorzellen • männl. / weibl. = 2/1 komplette Remission partielle Remission Progress Tod während Therapie FFTF 24 Monate Überleben >24 Monate 2xCOPP/ ABVD (n=235) in % 83 1 13 3 72 89 4xBEACOPP baseline (n=241) in % 88 2 9 <1 81 94 8xBEACOPP escalated (n=231) in % 95 1 2 2 89 96 Quelle: DHSG-Köln, Sieber et al. Ann Oncol 2000 4 Therapiekontrolle - maligne Lymphome Therapiekontrolle - maligne Lymphome Initialuntersuchung 19 jährige Patientin, Morbus Hodgkin, Stadium IIA, Verlaufsuntersuchung: Z.n. Behandlung mit 2 Zyklen Polychemotherapie residuelle RF HD 15 Studie - M. Hodgkin Vitalität ? Therapiekontrolle: Sarkome im Kindesalter FDG-PET Befunde und Therapieempfehlung (Stand 4/2006: n=210 Patienten) Residuelle Raumforderung: 10-Jahres Überlebensrate nach Stadien (%) I II III IV Rhabdomyosarkom 85 75 70 20 Osteosarkom 95 70 50 30 Ewingsarkom 70 60 45 25 PET negativ 170 / 210 Patienten für 81% der Pat. Toxizitätsreduktion DHSG Dietlein et al., 2006 Therapiekontrolle Visuell SUV-Analyse Applizierte Aktivität [Bq] / Körpergewicht [g] SUV max Aktivitätskonzentration im Gewebe [Bq/g] • Responder: 74% 80 95% CI [0.66;0.81] 60 • Non Responder: 45% 40 95% CI [0.24;0.66]; p: 0.004 * in [%] Standard Uptake Value (SUV) SUV= SUV-Analyse (Initial - Verlauf) 100 Restaging Follow-up SUV Reduc. max reduction in % Initialstaging Therapiekontrolle - Sarkome 20 N= n=5 Non Responder 3 non response 11 Boxplot of SUV max reduction in responding vs. non-responding tumours during therapy. SUVmax: 6.2 14 j. Mädchen mit Rhabdomyosarkom der Ulna links SUVmax: Initial 3,2 Verlauf 2.9 n=12 response Responder PET 2003 Studie • CUT OFF 59% Vorhersage des Ansprechens auf die Therapie (Sens.: 1.00; Spec.: 0.93) PET 2003 Studie 5 Gliederung Kolorektale Karzinome - Grundlagen - Primärtumordiagnostik / Staging - Therapiekontrolle - Rezidivdiagnostik - Nuklearmedizinische Therapie FDG-PET-CT: Indikationen Kolorektale Karzinome Tumorentitäten Fragestellungen Nicht-kleinzelliges Lungenkarzinom Staging, Monitoring, Rezidivnachweis Kolorektale Karzinome Monitoring, Rezidivnachweis • Informationszugewinn - Frühzeitige Erfassung und Lokalisierung eines Tumorrezidivs bzw. einer Metastasierung - Bei Lebermetastasierung: Therapieplanung (Chirurgie, lokal ablative Verfahren, lokale oder systemische Chemotherapie) Maligne Lymphome Malignes Melanom Initialstaging, Frühe Response, Residuelle RF Staging Pankreaskarzinom Dignitätsbeurteilung, Staging Oesophaguskarzinom Staging, Monitoring CUP Primärtumornachweis Amthauer et al. Nuklearmedizin 2006, Juweid et al. NEJM 2006 Hirneigene Tumore Biopsieort, höhergrad. Anteile • Rezidiverfassung - Bei klinischem oder Bild gebendem Verdacht auf ein Rezidiv bzw. Erhöhung des Tumormarkers CEA ohne Korrelat Schlag et al. Chirurg 2001 Gliederung Nuklearmedizinische onkologische Therapie - Grundlagen - Primärtumordiagnostik / Staging - Therapiekontrolle - Rezidivdiagnostik - Nuklearmedizinische Therapie Metabolisch Iod 131 Behandlung von diff. SD-Karzinomen Iod 131-MIBG Neuroblastome Re186 HEDP o. Sm153 EDTMP Schmerztherapie bei ossären Metastasen Rezeptor,- bzw. Antikörper vermittelt Perfusionsbasiert Yttrium 90 - Antikörper z.B. CD20 (NHL) Yttrium 90 Mikrosphären Yttrium 90 o. Lutetium 177 Rezeptor-Analoga Somatostatin-Rezeptor (NET) Intraart. Therapie von primären und sek. Lebertumoren 6 Nuklide für die Therapie t1/2 I-131 Emax [MeV] γ -Emission [keV] 0,6 637; 365 Richtlinie Strahlenschutz in der Medizin 6.6.2 „Patienten, die offene radioaktive Stoffe zu therapeutischen 8,1 d Y-90 Nuklearmedizinische Therapie 2,7 d 2,3 - Sm-153 46,3 h 0,81 103 Re-186 3,7 d 1,07 137 Lu-177 6,7 d 0,49 113; 210 Grundlage: Zwecken erhalten haben, sind nach der Verabreichung mindestens 48 Std. stationär aufzunehmen, um eine Verschleppung dieser Stoffe zu vermeiden.“ Die Neufassung der Richtlinie Strahlenschutz in der Medizin W. Kemmer, 1992 Schilddrüsenkarzinome Therapie papillärer und follikulärer Karzinome Inzidenz in Deutschland: 2-3 pro 100.000 Einwohner • Papillär: 50-80% • Thyreoidektomie und evtl. Neck-Dissection Ca. 90% differenzierte Schilddrüsenkarzinome • Follikulär: 20-40% • Medullär: 4-10% • Radiojodtherapie: • Anaplastisch: ca. 2% – Ablation von Restschilddrüsengewebe 10-Jahresüberlebenszeiten – Behandlung von Lymphknoten und 80-90% Fernmetastasen • Follikuläres Karzinom: 60-70% Iod 131 Kapsel für orale Gabe Non-Hodgkin Lymphom Radiojodtherapie bei papillärem Schilddrüsenkarzinom Chemo- und Immuntherapien verlieren an Wirksamkeit im Krankheitsverlauf 100 100 • 48-jähriger Patient, Dauer (Mon.) 16 11,2 9,6 3,2 90 CR 1 2 3 4 80 Patienten (%) • ED eines pap. SD-Karzinoms 04/2005 • Z.n. totaler Thyreoidektomie (T2 Nx Mx) 70 60 50 40 30 20 • 06/2005 Durchführung einer ablativen Radiojodtherapie mit 3700 MBq I-131 10 0 anterior anterior posterior posterior p < 0,05 90 80 70 60 57 46 50 24 40 30 20 10 0 0 • Frage: Restschilddrüsengewebe, Metastasen Ganzkörperaufnahmen nach Therapie mit I-131 – Behandlung von Tumorrezidiven Gesamtansprechrate (%) • Papilläres Karzinom: 1 2 Jahre 3 4 1. Rezidiv (n=57) 2. Rezidiv (n=46) 3. Rezidiv (n=24) Patienten mit Remission (n=110) nach 4 aufeinander folgenden Therapien Gesamtansprechen auf Rituximab im 1. bis 3. Rezidiv Gallagher et al. J Clin Oncol 4:1470-1480 (1986) McLaughlin et al. Sem Oncol 26:79-87 (1999) →Bedarf an neuen effektiven Therapieoptionen 7 Radioimmuntherapie bei Non-Hodgkin Lymphomen 90Yttrium-Ibritumomab-Tiuxetan (Zevalin®) – NHL sind von Natur aus sehr strahlensensibel Indikation: – Die Radiotherapie kann bei NHL in frühen Stadien kurativ sein 90Y-radiomarkiertes Zevalin® ist indiziert zur Behandlung von erwachsenen Patienten mit einem nach einer Behandlung mit Rituximab – Radioaktiv markierte Antikörper bringen die Strahlung zielgerichtet zum Tumor – Die Radioimmuntherapie kann sowohl Ziel- als auch Nachbarzellen vernichten (“Kreuzfeuer-Effekt”) und so auch große oder gering vaskularisierte Tumoren erreichen 90Yttrium-Ibritumomab-Tiuxetan Monoklonaler Antikörper rezidivierenden oder refraktären CD20-positiven follikulären Non-Hodgkin-Lymphom (NHL) vom B-Zell-Typ. Kontraindikationen: - Überempfindlichkeit gegenüber Ibritumomab-Tiuxetan, Yttrium-chlorid, anderen murinen Proteinen oder einem der sonstigen Bestandteile - Schwangerschaft und Stillzeit. Radioimmuntherapie im Vergleich zur Immun-, Chemo- und Strahlentherapie (Zevalin®) •Ibritumomab – Muriner monoklonaler Mutter-Antikörper von Rituximab •Tiuxetan Chelator Beta-Strahlung – An den Antikörper gebundener Chelator, starke harnstoffartige Bindung – Stabile Retention von 90Yttrium Chemotherapie Immuntherapie mit „kalten“ Antikörpern Perkutane Strahlentherapie Radioimmuntherapie Radioaktiv markierter Antikörper Radionuklid: 90Yttrium Dauerhafte Remissionen: Vergleich zur Vortherapie Beiträge der Zevalin-Therapie zum Fortschritt in der NHL-Behandlung – Einmaltherapie mit guter Verträglichkeit auch bei älteren Patienten Mediane Remissionsdauer vorherige Therapie – Induktion hoher CR-Raten mit Langzeitremissionen auch im Rezidiv 12 – Perspektiven: 28,1 Zevalin 0 6 12 18 24 30 Monate Schilder et al. Blood 104(11): 719a, Abstr. 2629 (2004) • frühzeitiger Einsatz bei follikulären Lymphomen (1st-line/Konsolidierung) • weitere CD20-positive NHL: – – MCL DLBCL • gezielte Strahlentherapie in der Konditionierung vor Stammzelltransplantation 8 Neuroendokrine Tumoren (NET) Somatostatin-Rezeptor-Szintigraphie • Inzidenz: 0,1 - 1/100000 • Geschlechtsverteilung: m/w 1:1 • mittleres Alter bei Diagnosestellung: - 42 J (funktioneller NET des Appendix) bis - 70 J (nonfunktioneller NET des Colon) • 5-J Überleben: 50,4 % +/- 6,4% in Abhängigkeit von: - Primärlokalisation - Metastasierung - Funktionalität - Differenzierungsgrad 70-jähriger Patient in gutem AZ und EZ seit ca. 6 Monaten bestehenden Blähungen und Flush-Symptomatik V.a. Neuroendokrinen Tumor Öberg et al., Ann Oncol 1996, Modlin and Sandor, Cancer 1997 Therapiestrategien bei NET Radiorezeptortherapie Indikation: • Kurative Therapie ist nur durch Resektion (R0) möglich • Palliative Therapiestrategien Ziele: Zytoreduktion / Proliferationshemmung Kontrolle von Hypersekretionssyndromen Initialstaging vor Y-90-DOTATOC Therapie Verlaufskontrolle nach 3 Monaten - Metastasierter NET, histologisch gesichert - nicht-kurativ resektables Tumorleiden - Progress der Tumorerkrankung unter vorangegangenen konventionellen Standard-Therapieregimen - Progress: Nachweis in zwei aufeinander folgenden Bild gebenden Staging-Untersuchungen innerhalb von 6 Monaten (MRT, CT, SR-Szintigraphie oder PET) Ergebnisse - Studie Y-90-DOTATOC Metastasierte Gastroenteropankreatische NET mit Progress der Erkrankung (n=21) - Aktivität (Durchschnitt: 10,1 GBq) 13% 6% 37 % 44% partial response minor response stable disease Median follow-up: 13 Monate progressive Y90-Dotatoc: Anwendungsbeobachtungsstudie 9 Radioembolisation Mikrosphären (20-40 µm) mit Yttrium-90 beladen Radioembolisation Patienten mit irresektablen kolorektalen Lebermetastasen nach 2./3.-Linien-Chemotherapie n=20 Pat. 67j. Pat. mit Z.n. CRC, bilobäre Leberfiliae, chemotherapeutisch ausbehandelt FDG-PET: Vor Therapie FDG-PET: 3 Monate nach Therapie response partial response (PR) 6 Wochen 12 Wochen 6 Monate (n = 20) (n=20) (n=15) 12 3 stable disease (SD) 4 4 2 0 progressive disease (PD) 4 11 5 Verstorben 0 2 8 Rühl et al. DGN 2007 10