Gruppeneigenschaften der Chalkogene Sauerstoff (O) Schwefel (S
Werbung
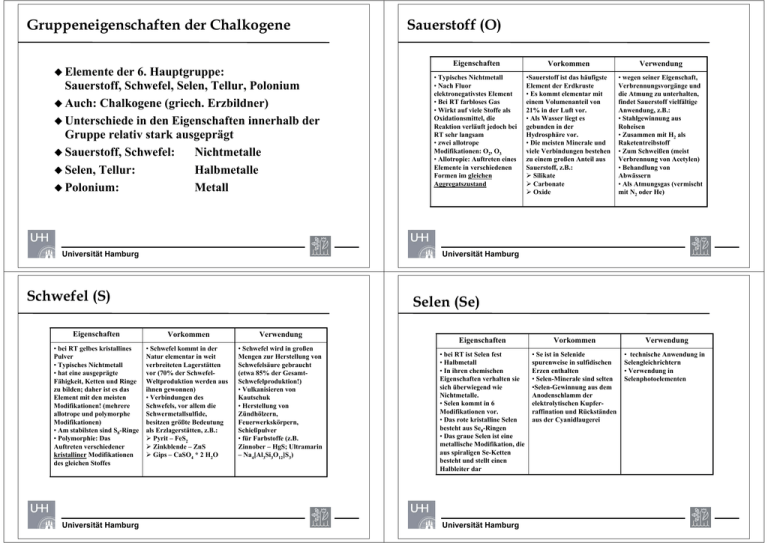
Gruppeneigenschaften der Chalkogene Elemente der 6. Hauptgruppe: Sauerstoff, Schwefel, Selen, Tellur, Polonium Auch: Chalkogene (griech. Erzbildner) Unterschiede in den Eigenschaften innerhalb der Gruppe relativ stark ausgeprägt Sauerstoff, Schwefel: Nichtmetalle Selen, Tellur: Halbmetalle Polonium: Metall Universität Hamburg Eigenschaften Vorkommen Verwendung • Typisches Nichtmetall • Nach Fluor elektronegativstes Element • Bei RT farbloses Gas • Wirkt auf viele Stoffe als Oxidationsmittel, die Reaktion verläuft jedoch bei RT sehr langsam • zwei allotrope Modifikationen: O2, O3 • Allotropie: Auftreten eines Elemente in verschiedenen Formen im gleichen Aggregatszustand •Sauerstoff ist das häufigste Element der Erdkruste • Es kommt elementar mit einem Volumenanteil von 21% in der Luft vor. • Als Wasser liegt es gebunden in der Hydrosphäre vor. • Die meisten Minerale und viele Verbindungen bestehen zu einem großen Anteil aus Sauerstoff, z.B.: ¾ Silikate ¾ Carbonate ¾ Oxide • wegen seiner Eigenschaft, Verbrennungsvorgänge und die Atmung zu unterhalten, findet Sauerstoff vielfältige Anwendung, z.B.: • Stahlgewinnung aus Roheisen • Zusammen mit H2 als Raketentreibstoff • Zum Schweißen (meist Verbrennung von Acetylen) • Behandlung von Abwässern • Als Atmungsgas (vermischt mit N2 oder He) Universität Hamburg Schwefel (S) Selen (Se) Eigenschaften Vorkommen Verwendung • bei RT gelbes kristallines Pulver • Typisches Nichtmetall • hat eine ausgeprägte Fähigkeit, Ketten und Ringe zu bilden; daher ist es das Element mit den meisten Modifikationen! (mehrere allotrope und polymorphe Modifikationen) • Am stabilsten sind S8-Ringe • Polymorphie: Das Auftreten verschiedener kristalliner Modifikationen des gleichen Stoffes • Schwefel kommt in der Natur elementar in weit verbreiteten Lagerstätten vor (70% der SchwefelWeltproduktion werden aus ihnen gewonnen) • Verbindungen des Schwefels, vor allem die Schwermetallsulfide, besitzen größte Bedeutung als Erzlagerstätten, z.B.: ¾ Pyrit – FeS2 ¾ Zinkblende – ZnS ¾ Gips – CaSO4 * 2 H2O • Schwefel wird in großen Mengen zur Herstellung von Schwefelsäure gebraucht (etwa 85% der GesamtSchwefelproduktion!) • Vulkanisieren von Kautschuk • Herstellung von Zündhölzern, Feuerwerkskörpern, Schießpulver • für Farbstoffe (z.B. Zinnober – HgS; Ultramarin – Na4[Al3Si3O12]S3) Universität Hamburg Sauerstoff (O) Eigenschaften Vorkommen • bei RT ist Selen fest • Halbmetall • In ihren chemischen Eigenschaften verhalten sie sich überwiegend wie Nichtmetalle. • Selen kommt in 6 Modifikationen vor. • Das rote kristalline Selen besteht aus Se8-Ringen • Das graue Selen ist eine metallische Modifikation, die aus spiraligen Se-Ketten besteht und stellt einen Halbleiter dar • Se ist in Selenide spurenweise in sulfidischen Erzen enthalten • Selen-Minerale sind selten •Selen-Gewinnung aus dem Anodenschlamm der elektrolytischen Kupferraffination und Rückständen aus der Cyanidlaugerei Universität Hamburg Verwendung • technische Anwendung in Selengleichrichtern • Verwendung in Selenphotoelementen Verbindungen des Sauerstoffs Tellur (Te) Eigenschaften • Bei RT silberweißer, metallischer Feststoff • Halbmetall • Tellur ist ein Halbleiter • Kristallisiert im gleichen Gitter wie graues Selen Vorkommen Verwendung • Sind als Telluride spurenweise in sulfidischen Erzen enthalten • Tellur-Minerale sind selten • Tellur kommt in geringen Mengen auch gediegen vor • Hauptausgangsmaterial für die Tellur-Gewinnung ist der bei der elektrolytischen Kupferraffination anfallende Anodenschlamm. • Dient u.a. als Legierungsbestandteil (< 1%) von Stählen und Legierungen, um mechanische Eigenschaften und Korrosionsbeständigkeit zu erhöhen • Ferrotellur (50-80% Tellur) wird als Stabilisator in der Eisengießerei eingesetzt Universität Hamburg O S H O S Schwefeltrioxid – SO3 O O H O O H O O S S Schwefelsäure – H2SO4 O H S O H O Schwefelwasserstoff – H2S Dischwefelsäure – H2S2O7 O H H O S O Universität Hamburg O H H O O H • Wichtigste Wasserstoffverbindung • Bindungen sind stark polar, es treten zwischen den H2O-Molekülen Wasserbindungen auf • • Wasser hat daher einen anormal hohen Schmelz- und Siedepunkt Gegenüber vielen Verbindungen wirkt H2O2 oxidierend • • Anormalie des Wassers: Beim Übergang vom flüssigen in den festen Zustand dehnt sich das Wasser unter Abnahme der Dichte aus. Das Dichtemaximum liegt bei 4°C (1g/cm3) H2O2 ist eine metastabile Verbindung und zersetzt sich bei höherer Temperatur • Wird heute überwiegend nach dem Anthrachinon-Verfahren hergestellt. Schwefelsäure O Schwefelige Säure – H2SO3 H Wasserstoffperoxid – H2O2 Universität Hamburg Verbindungen des Schwefels Schwefeldioxid – SO2 Wasser – H2O Schwefelsäure ist eines der wichtigsten großtechnischen Produkte Hauptmenge wird zur Herstellung von Kunstdünger verwendet O Farblose, ölige Flüssigkeit H O S O H Wirkt wasserziehend (Hygroskopie)! O Ist stark oxidierend! Wird heute fast ausschließlich durch das Kontaktverfahren hergestellt O O S O H O Universität Hamburg H2SO4 mittels Kontaktverfahren 2 SO2 + O2 → 2 SO3 Gleichgewicht geht zunehmender Temperatur in Richtung SO2 Bei Raumtemperatur reagieren SO2 und O2 aber nicht miteinander V2O5 + SO2 2 V2O4 + O2 → V2O4 + SO3 → 2 V2O5 SO3 + H2SO4 H2S2O7 + H2O → → Linde -Verfahren Gase (z.B. Sauerstoff) werden großtechnisch durch fraktionierende Destillation verflüssigter Luft gewonnen Luftverflüssigung nach Linde Damit die Reaktion bei günstiger Gleichgewichtslage mit gleichzeitig ausreichender Geschwindigkeit abläuft, werden Katalysatoren verwendet Beim Kontaktverfahren verwendet man V2O5 und Temperaturen um 500 °C H2S2O7 2 H2SO4 SO3 löst sich besser in Schwefelsäure als in Wasser. Beim Lösungsvorgang in Schwefelsäure entsteht Dischwefelsäure H2S2O7. Diese wird dann mit Wasser zu H2SO4 umgesetzt. Universität Hamburg Universität Hamburg











