Mikrowellen in der Organischen Synthese
Werbung

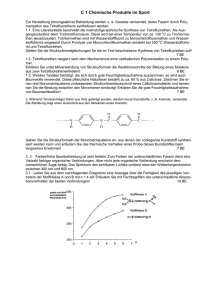
DOI: 10.1002/ciuz.201300610 Manche mögens heiß Mikrowellen in der Organischen Synthese D ORIS D ALLINGER ie meisten chemischen Reaktionen verlaufen bei Umgebungstemperatur (25 °C) nur sehr langsam, sodass in der organischen Synthesechemie Reaktionsgemische oft auf Temperaturen um 60-150 °C erwärmt werden müssen, um praktikable Reaktionszeiten zu erzielen. In der Praxis werden organische Synthesen im Labormaßstab meist in einem Lösungsmittel unter Rückflussbedingungen durchgeführt. Reaktionsmischungen werden dafür oft im Ölbad oder mittels Heizpilz erhitzt. Über den an sich naheliegenden Einsatz von Mikrowellenenergie zum Erhitzen organisch-chemischer Reaktionsgemische wurde erstmals 1986 von den Gruppen von Gedye und Giguere/Majetich berichtet [1]. Bei diesen Experimenten kamen zunächst herkömmliche Haushaltsmikrowellengeräte zum Einsatz, was zu Problemen bezüglich Sicherheit und Reproduzierbarkeit, bedingt durch das Fehlen geeigneter Systeme zur Temperatur- und Druckkontrolle, führte. Vor ungefähr 10 Jahren wurde mit dem Vertrieb wissenschaftlicher Labormikrowellengeräte begonnen, die speziell für die organische Synthesechemie entwickelt wurden. Damit einhergehend hat auch die Zahl der Publikationen zur Mikrowellen-unterstützten organischen Synthese (microwave-assisted organic synthesis, MAOS) seit den späten 90er Jahren drastisch zugenommen – mehr als 7000 Arbeiten auf dem Gebiet der organischen Synthese wurden bis jetzt veröffentlicht [2]. Als wesentliche Fortschritte gegenüber den Haushaltsmikrowellengeräten zählen eingebaute Magnetrührer, die direkte Temperaturkontrolle mithilfe faseroptischer Sonden oder IR-Sensoren und Software, die die Online-Steuerung von Temperatur und Druck durch Regulierung der Mikrowellenleistung ermöglicht. In mehr als 90 % der gegenwärtig publizierten Synthesen unter Einsatz von wissenschaftlichen Labormikrowellengeräten werden sogenannte „Single-mode“-Mikrowellenreaktoren in Kombination mit druckfest verschlossenen Reaktionsgefäßen verwendet (Abbildung 1). Ein typisches Heizprofil für ein Experiment unter geschlossen Gefäßbedingungen zeigt Abbildung 2: in diesem Fall wird Methanol außerordentlich schnell (in weniger als 50 Sekunden) bis 130 °C über den Siedepunkt auf 195 °C erhitzt. In diesem „Temperatur-kontrollierten“ Modus ist die Magnetronleistung an den Temperatursensor gekoppelt. Das heißt, das D Abb. 1 Beispiel eines „Single-mode“-Mikrowellenreaktors mit Autosampler und dazugehörigem verschlossenem 10 mL Glas-Reaktionsgefäß (Monowave 300, Anton Paar). Das Erhitzen mittels Mikrowellenenergie hat sich von einer Laborkuriosität zu einer etablierten Methode entwickelt und erfreut sich in den letzten 10 Jahren steigender Beliebtheit. Die drastische Verringerung der Reaktionszeiten ermöglicht, dass in vielen Fällen Ergebnisse innerhalb weniger Minuten vorliegen. Daher überrascht es nicht, dass viele akademische und industrielle Forschungsgruppen die Mikrowelle als fortschrittliche Technologie zur schnellen Reaktionsoptimierung, effizienten Synthese neuer Verbindungen oder Entdeckung und Untersuchung neuartiger chemischer Reaktionen nutzen. 356 © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim Chem. Unserer Zeit, 2013, 47, 356 – 366 MIKROWELLEN Gerät versucht so schnell wie möglich die eingestellte Temperatur bei hoher Leistung zu erreichen. Dann wird die Leistung soweit reduziert, um diese Temperatur konstant zu halten. ABB. 2 O RG A N I S C H E S Y N T H E S E T E M PE R AT U R , D R U C K U N D M I K ROW E L L E N L E I S T U N G … Mikrowellentheorie Wie funktioniert nun das Heizen mit Mikrowellenenergie? Konventionelles Heizen erfolgt unter Rückflussbedingungen (z.B. im Ölbad) durch den Wärmetransport über die Gefäßwand durch die klassischen Prinzipien der Wärmeübertragung: Wärmeleitung und Konvektion. Diese Methode der Energieübertragung ist relativ langsam und ineffizient; nachteilig kommt hinzu, dass die Temperatur des Reaktionsgefäßes meist höher ist als die des Reaktionsgemisches. Im Unterschied dazu wird unter Mikrowellenbestrahlung effizient von innen erhitzt („dielektrisches Erhitzen mit Mikrowellen“). Diesem Phänomen liegt die Fähigkeit eines bestimmten Stoffes (Solvens oder Reagens) zugrunde, Mikrowellenenergie zu absorbieren und in Wärme umzuwandeln. Da die verwendeten Reaktionsgefäße im Allgemeinen aus für Mikrowellen (nahezu) durchlässigem Material wie Glas oder Teflon bestehen, wird nur das Reaktionsgemisch – und nicht das Gefäß – erhitzt. Zwei Hauptmechanismen sind für die Wärmeerzeugung durch Mikrowellenbestrahlung verantwortlich: dipolare Polarisierung und Ionenleitung. Beim Bestrahlen mit Mikrowellenfrequenzen richten sich die Dipole oder Ionen der Probe im angelegten Feld aus. Dieses Feld oszilliert, und da das Dipol- oder Ionenfeld versucht, sich mit dem wechselnden elektrischen Feld neu auszurichten, wird durch Mo- … für das effiziente Mikrowellenheizen von Methanol (Kp 65 °C) auf 195 °C (31 bar) im geschlossenen Gefäß. lekularreibung und Dielektrizitätsverlust Energie in Form von Wärme frei. Die Fähigkeit einer bestimmten Verbindung, elektromagnetische Energie bei gegebener Frequenz und Temperatur in Wärme umzuwandeln, wird vom Verlustfaktor tan δ bestimmt. Eine effiziente Absorption und demzufolge ein rasches Aufheizen setzt voraus, dass tan δ bei der Standardfrequenz von Mikrowellenreaktoren (2,45 GHz) für das Reaktionsmedium groß ist. Die tan δ-Werte für einige gebräuchliche organische Lösungsmittel sind in Abbildung 3 M U LT I - V E R S U S S I N G L E- M O D E In Multimode-Geräten wird das Mikrowellenfeld chaotisch verteilt: Mikrowellen werden von den Wänden reflektiert und die so entstehenden Multimoden wechselwirken mit der Beschickung. Dieses Prinzip hat eine inhomogene Energieverteilung zur Folge. Aufgrund des normalerweise großen Innenraums ist die Felddichte gering, und um vernünftige Aufheizraten zu erzielen, ist deshalb eine hohe Mikrowellenleistung erforderlich. In den viel kleineren Innenräumen der Monomode-Reaktoren werden die Mikrowellen auf das in einem festen Abstand zur Strahlungsquelle montierte Reaktionsgefäß gerichtet, sodass eine stehende Welle entsteht (Wellen einer Mode wechselwirken mit dem Reaktionsgemisch). In diesen Geräten ist die Energieverteilung daher relativ homogen und die Felddichte hoch, weshalb eine geringere Mikrowellenleistung nötig ist. Der Hauptunterschied zwischen diesen beiden Reaktorsystemen besteht nun darin, dass in Multimode-Geräten mehrere Reaktionsgefäße gleichzeitig in Rotorsystemen bestrahlt werden können (Parallelsynthese), während in Monomode-Reaktoren immer nur ein Reaktionsgefäß bestrahlt werden kann. Chem. Unserer Zeit, 2013, 47, 356 – 366 Single-mode Multimode Antenne Magnetron Gefäß Feldrühre Wellenleiter Magnetron Gefäß www.chiuz.de Antenne Multimode Single-mode Anzahl Magnetrons 1-2 1 Leistung 1000-1600 W 300-850 W Felddichte niedrig hoch Energieverteilung inhomogen (Hot- und Coldspots) relativ homogen Mikrowellenfeld chaotisch (Reflexionen an Wand) stehende Welle (Wellen einer Mode) Reaktionsvolumina 0.3 mL - 2.5 L 60 µL - 50 mL Synthesemethode parallel (Rotorsysteme) sequenziell © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 357 Verwendung in einer Mikrowellen-beheizten Reaktion aus. Da oft entweder die Substrate oder einige der Reagentien/Katalysatoren polar sind, reichen somit die dielektrischen Eigenschaften des Reaktionsgemisches in den meisten Fällen für das Heizen durch Mikrowellen aus. Im Folgenden werden die wesentlichsten Vorteile, Konzepte und Prozesstechniken der Mikrowellen-assistierten organischen Synthese vorgestellt. Verkürzung der Reaktionszeit Abb. 3 Dielektrische Verlustfaktoren (tan δ) verschiedener Lösungsmittel (2,45 GHz, 20 °C). Daten aus Ref. [2a]. Üblicherweise wird bei organischen Synthesen unter Rückflussbedingungen die Reaktionstemperatur durch den Siedepunkt des Lösungsmittels bestimmt. Sind jedoch hohe Temperaturen notwendig, muss ein Lösungsmittel mit hohem Siedepunkt verwendet werden. Ungünstig dabei ist, dass dieses hochsiedende Lösungsmittel bei der Aufarbeitung wieder entfernt werden muss, was sich mitunter als schwierig erweist. zusammengestellt. Die Lösungsmittel werden allgemein als stark (tan δ > 0,5), mittel (tan δ = 0,1–0,5) und schwach Mikrowellen-absorbierend (tan δ < 0,1) eingestuft. Allerdings schließt ein niedriger tan δ-Wert ein Solvens nicht von der ABB. 4 R E A K T I O N S B E S C H L EU N I G U N G I N D E R S Y N T H E S E VO N 2 - M E T H Y L B E N Z I M I DA ZO L Bedingungen (T/p) ABB. 5 NH2 AcOH (1 M) N NH2 Bedingungen N H CONV CONV CONV MW MW MW MW Me Zeit 25 °C / 9 Wochen 60 °C / 3d 100 °C / 5h 130 °C / 2 bar 1h 160 °C / 4 bar 10 min 200 °C / 9 bar 3 min 270 °C / 29 bar 1s R E A K T I O N S B E S C H L E U N I G U N G VO N PA L L A D I U M - K ATA LYS I E R T E N K R E U Z KU PPLU N G E N Heck Reaktion OBu + NC O Pd/C, Et3N MeCN I Ölbad: 80 °C, 3 h MW: 155 °C, 2 min O OBu NC Suzuki Kreuzkupplung NO2 Cl + (HO)2B Pd, (PPh3), NaOH THF, H2O Cl NO2 Cl Ölbad: 66 °C, 18 h MW: 160 °C, 15 min Negishi Kreuzkupplung CN Cl + ClZn Me Pd/Bu3P.HBF4 THF, NMP CN Me Ölbad: 100 °C, 24 h MW: 175 °C, 10 min 358 © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim www.chiuz.de Chem. Unserer Zeit, 2013, 47, 356 – 366 MIKROWELLEN Im Gegensatz dazu ist die Reaktionstemperatur unter Mikrowellenbedingungen nicht auf den Siedepunkt des Lösungsmittels limitiert, wichtiger sind dessen dielektrische Eigenschaften. Die Verwendung von geschlossenen Gefäßen in Mikrowellenreaktoren erlaubt daher ein sehr rasches Aufheizen von Reaktionsmischungen auf Temperaturen weit über den Siedepunkt des Lösungsmittels unter atmosphärischen Bedingungen (Abbildung 2). Wendet man die Arrhenius-Gleichung [k = A exp(-Ea/RT)] an, wird deutlich, dass Synthesen, die unter Rückflussheizen mehrere Stunden erfordern, in wenigen Minuten oder gar Sekunden vollständigen Umsatz erreichen können [2]. Dazu gilt allgemein die Näherung: Eine Erhöhung der Temperatur um 10 °C führt zu einer Halbierung der Reaktionszeit. Ein eindrucksvolles Exempel hierfür ist die Synthese von 2-Methylbenzimidazol [3], dessen Grundkörper in einer Vielzahl von biologisch aktiven Substanzen zu finden ist (Abbildung 4). Bei Raumtemperatur (25 °C) benötigt die Reaktion von o-Phenylendiamin mit Essigsäure 9 Wochen, um einen vollständigen Umsatz zu erreichen. Unter konventionellen Rückflussbedingungen (~100 °C) dauert die Synthese noch immer 5 Stunden. Bei Erhitzen in einem Mikrowellenreaktor unter Verwendung von geschlossenen Gefäßen kann die Reaktionszeit bei 200 °C jedoch auf 3 Minuten verkürzt werden. Bei den maximal möglichen 270 °C (29 bar) des Reaktors beträgt die Reaktionszeit gar nur 1 Sekunde! Übergangsmetall-katalysierte C-C- oder C-HeteroatomKupplungsreaktionen zählen wohl zu den wichtigsten und am häufigsten untersuchten Umsetzungen in der Mikrowellen-unterstützten organischen Synthese [2, 4]. Unter Rückflussbedingungen benötigen diese Synthesen normalerweise Stunden, wenn nicht Tage, für einen vollständigen Umsatz. In Abbildung 5 sind drei Beispiele für Palladium-kataylsierte Kreuzkupplungen gezeigt. Sowohl für die Heck-, Negishi- als auch die Suzuki-Reaktion konnten die Reaktionszeiten von bis zu 24 Stunden unter Rückflussheizen im Ölbad auf wenige Minuten verkürzt werden, wenn die Synthesen mittels Mikrowellen beheizt wurden [5]. Die Mikrowellen-unterstützte Synthese bringt allerdings noch zusätzliche Vorteile: Häufig ist das unter herkömmlichen Bedingungen übliche Arbeiten unter Inertatmosphäre nicht notwendig. Entscheidende Beiträge in der Durchführung von Heck- und Suzuki-Reaktionen mit „homöopathischen“ Mengen (<10 ppm) an Pd-Katalysator wurden von der Arbeitsgruppe um Leadbeater geleistet [6]. ABB. 7 ABB. 6 VERBESSERUNG DER SYNTHESE … O 2 H Cl + R1 HO O RG A N I S C H E S Y N T H E S E R + R3 N HO N R3 Cl , Et3N 2 R1 R3 O O R3 R2 1 Cl Base N R1 MW, 90 °C 30 min N R3 Cl 3 O rt, 1 h HO N PdCl2(PPh3)2, CuI Et3N, THF O N O N 3 R O R3 R3 3 R2 O 4 N 24 Beispiele (12-74%) 5 … von 3,4,5-substituierten Isoxazolen durch verkürzte Reaktionszeit und erhöhte Ausbeuten. Verbesserte Ausbeuten Durch die exakte Temperaturmessung in Mikrowellenreaktoren und die generell viel höheren Reaktionstemperaturen werden gegenüber konventionell beheizten Reaktionen in vielen Fällen auch höhere Produktausbeuten und Reinheiten erzielt – aufgrund der Bildung von geringeren Mengen an Nebenprodukten [2]. Zusätzlich spielt das schnelle Aufheizen/Abkühlen und die Durchführung der Reaktionen bei optimierten Reaktionstemperaturen eine bedeutende Rolle. Ein Beispiel hierfür ist die von der Arbeitsgruppe Müller publizierte 3-Komponenten-Eintopf-Synthese von 3,4,5substituierten Isoxazolen (Abbildung 6) [7]. Im ersten Schritt wurden Alkynone 1 durch eine Sonogashira-Kupplung bei Raumtemperatur erhalten. Diese Reaktionssequenz wurde bereits im geschlossenen Mikrowellengefäß durchgeführt. Nach Zugabe von Hydroxyiminoylchloriden 2 und Triethylamin in dasselbe Gefäß reagierten die Alkynone mit den von 2 in situ generierten Nitriloxiden 3 weiter über eine 1,3-dipolare Cycloaddition zu den entsprechenden Isoxazolen 4. Der Cycloadditionsschritt konnte mittels Mikro- VERBESSERUNG DER SYNTHESE … NH2 3 O R1 CONV: AcOH, Rückfluss, 2-12 h + R NH2 N R1 N R2 3 O R2 MW: MeOH/AcOH, 160 °C, 5 min R CONV: 32-85% MW: >90% 6 … von Chinoxalinen durch verkürzte Reaktionszeit und erhöhte Ausbeuten. Chem. Unserer Zeit, 2013, 47, 356 – 366 www.chiuz.de © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 359 runter auch einige wirksame und selektive Kinase-Inhibitoren [8b]. wellen-Heizen signifikant beschleunigt werden: von bis zu 3 Tagen im Ölbad auf 30 Minuten. Ein Nachteil der langen Reaktionszeiten war die erhöhte Bildung von Furoxanoxid 5 als Nebenprodukt durch Dimerisierung des Nitriloxids 3. Somit wurden durch Mikrowellen-Heizen auch höhere Produktausbeuten erzielt, da unter konventionellen Bedingungen ca. 50 % mehr Nebenprodukt gebildet wurde. Auch in der Cyclokondensation von 1,2-Diaminen mit 1,2-Diketonen konnte unter Mikrowellenbedingungen bei 160 °C im geschlossenen Gefäß die Ausbeute erhöht werden [8]. Während Chinoxaline 6 in isolierten Ausbeuten von >90 % nach nur 5 Minuten Reaktionszeit erhalten wurden, waren unter Rückflussbedingungen 2-12 Stunden nötig, um die Produkte in nur 32-85 % herzustellen (Abbildung 7). In einem Drug Discovery Projekt wurden einige Hundert Chinoxaline unter den beschriebenen Mikrowellenbedingungen in exzellenten Ausbeuten synthetisiert, da- ABB. 8 Produktverteilung und Selektivität Da Mikrowellen-beheizte Reaktionen oft bei relativ hohen Temperaturen durchgeführt werden, können, im Vergleich zu konventionell beheizten Experimenten, veränderte Produktverteilungen und Selektivitäten beobachtet werden. Bei der Multikomponentenkondensation von 5-Aminopyrazolen 7, aromatischen Aldehyden 8 und cyklischen 1,3Diketonen 9 (Abbildung 8) unter stark basischen Bedingungen kam es zu einer Änderung des Reaktionsmechanismus je nachdem ob die Reaktion unter Rückfluss (80 °C) oder im geschlossen Gefäß in der Mikrowelle bei 150 °C durchgeführt wurde [9]. Unter Rückfluss wurden die bekannten trizyklischen Hantzsch-Dihydropyridine 11 generiert, wohingegen im Mikrowellenexperiment Pyrazolo-Chi- V E R Ä N D E R T E PRO D U K T V E R T E I LU N G I N M U LT I KO M P O N E N T E N R E A K T I O N E N 8 Ar O O H R1 + N N H 7 NH2 R1 EtOH, NaOEt R2 O Ar R2 N Hitze N H R2 9 N H OH R2 10 MW, 150 °C 20 min R1 Ar O Rückfluss, 80 °C 1-5 h H OH N H N R2 N R2 N H 12 O R2 11 Beispiele (40-75%) ABB. 9 O Ar R1 N N H R2 11 T H E R M O DY N A M I S C H E U N D K I N E T I S C H E KO N T RO L L E I N D E R B RO M I E R U N G VO N C H I N O LO N E N Ph Br Ph 14 0 °C, 17 h N Me NBS, MeCN N Me O O Ph Br 15 13 MW, 100 °C, 20 min 360 © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim www.chiuz.de N Me O Chem. Unserer Zeit, 2013, 47, 356 – 366 MIKROWELLEN nolizinone 12 durch eine Basen-vermittelte RingöffnungRezyklisierung des Intermediates 10 gebildet werden. Manchmal kann es bei hohen Temperaturen – die im Vergleich zu konventionellem Heizen durch Mikrowellenbestrahlung ohne großen Aufwand erzielt werden können – durchaus zu unerwarteten Produktbildungen kommen, die unter Standard-Rückflussbedingungen bei geringerer Temperatur nicht stattfinden. Wie die Temperatur die Selektivitäten beeinflussen kann, ist anhand der Bromierung von Chinolon 13 mit N-Bromsuccinimid (NBS) gezeigt (Abbildung 9) [10]. Führt man die Reaktion bei Raumtemperatur (4 h) durch, wird ein Gemisch aus 3-Brom- (14) und 6-Brom-Isomer (15) im Verhältnis von 83:17 erhalten. Eine Erhöhung der Temperatur auf 100 °C (20 min) durch Mikrowellen-Heizen im geschlossenen Gefäß erlaubt die selektive Synthese des 6-Brom-Isomers 15. Wird hingegen bei 0 °C für 17 Stunden bromiert, bildet sich bevorzugt das 3-Brom-Isomer im Verhältnis von 92:8. Höhere Temperaturen begünstigen in diesem Fall die Bildung des thermodynamisch stabileren Isomers 15. Allerdings muss hier angemerkt werden, dass das 3-Brom-Isomer 14 in dieser Synthese das Zielprodukt war. Unter Verwendung von Mikrowellenchemie konnte zwar eine ansonsten langsame Reaktion beschleunigt werden, jedoch führte dies zur Bildung eines unerwünschten Produktes! Hohe Temperaturen sind also nicht immer förderlich und obwohl Heizen mit Mikrowellen zwar zum Großteil eine erfolgreiche Methode ist, kann sie zweifellos nicht immer die Lösung aller synthetischer Probleme sein. Was muss zusätzlich zur thermodynamischen/kinetischen Kontrolle noch in der Mikrowellen-unterstützten organischen Synthese beachtet werden? Hohe Temperaturen führen meist ABB. 10 O RG A N I S C H E S Y N T H E S E nur zum Ziel, wenn die Stabilität der Substrate, Reagentien, Katalysatoren, Lösungsmittel und auch Produkte bei diesen Temperaturen gewährleistet ist. Höherer Durchsatz durch Automatisierung Geschwindigkeit ist ein entscheidender Faktor im Bereich der Arzneimittelforschung und Medizinalchemie. Der Einsatz von Mikrowellenreaktoren hat sich hier als sehr wertvolles Instrument – vorzugsweise zur Optimierung von Wirkstoffsynthesen und Herstellung von Produktbibliotheken – erwiesen. „Die erste Synthese nahezu aller neuen Verbindungen findet in einem Mikrowellenreaktor statt“ hat Jonathan Moseley von AstraZeneca UK schon 2008 postuliert [11]. Zur Automatisierung können in der Mikrowellentechnologie zwei Methoden angewandt werden: automatisiert sequenziell oder parallel. Von der sequenziellen Technik spricht man, wenn „Single-mode“-Reaktoren mit einem Autosampler ausgestattet sind, und die Gefäße Roboter-gesteuert transferiert werden (Abbildung 1). Die parallele Synthese wird in „Multimode“-Geräten in unterschiedlichen Rotorsystemen durchgeführt [2a]. Zusätzliche Automatisierung kann z. B. durch Roboter-gesteuertes Einwiegen, Pipettieren oder Verschließen und Öffnen des Reaktionsgefäßes eingeführt werden. Die sequenzielle Technik kam für die Optimierung der Biginelli-Multikomponentenreaktion (MCR) und darauffolgender Synthese einer kleinen Bibliothek von Dihydropyrimidinen 16 (Abbildung 10) zum Einsatz [12]. Da sich die Reaktionszeit von einigen Stunden unter Rückflussbedingungen auf nur 10 Minuten bei 120 °C unter Mikrowellen-Heizen reduziert, konnten mehr Parameter wie unterschiedliche Lösungsmittel und Katalysatoren, Molver- S Y N T H E S E VO N D I H Y D RO PY R I M I D I N - B I B L I OT H E K E N R1 O Biginelli MCR H EtS O NH2 + Me O HN R2 O Me3SiCl, MeCN MW, 120 °C, 10 min MW, 130 °C, 1 h N Me N R2 H + R3-B(OH)2 O 6 Beispiele (53-90%) O R3 N Me 5 Boronsäuren R1 N R2 H 17 O 30 Beispiele (57-88%) Chem. Unserer Zeit, 2013, 47, 356 – 366 EtS 16 Liebeskind-Srogl Pd(OAc)2, PPh3 CuTC, Dioxan R1 O www.chiuz.de Synthese von Dihydropyrimidin-Bibliotheken auf automatisiert-sequenzielle und parallele Weise. © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 361 ABB. 11 S Y N T H E S E E I N E R B E N Z Y L I D E N - OX I N D O L- B I B L I OT H E K … R2 O H Piperidin, EtOH R1 R1 R2 O + O MW, 140 °C, 10 min N H 18 20 19 N H 24 Beispiele (50-98%) a) b) … in einer 6 x 4 SiC-Mikrotiterplatte in einem 96-Positions-Rotorsystem (a). Die ausgezeichnete Temperaturhomogenität innerhalb der SiC-Platte wurde mit einer Wärmebildkamera bestätigt (b). ABB. 12 M E H R S T U F E N S Y N T H E S E VO N T R I A RY LC H I N O L I N E N … Cl I Br + Cl Me Me Me N Cl2Pd(dppf), THF aq. Cs2CO3 N Me Br + MW, 90 °C, 15 min N B(OH)2 21 Me Cl Cl Cl2Pd(dppf), THF aq. Cs2CO3 MW, 160 °C, 15 min (HO)2B N 78% Me N Me Me Cl Me O + B O Cl Me Cl2Pd(dppf), THF aq. Cs2CO3 Me MW, 160 °C, 30 min N N Me Me Cl N 73% 66% 22 … durch sequentielle Suzuki-Kreuzkupplungen mit nur einem Katalysator-Liganden-System. 362 © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim www.chiuz.de Chem. Unserer Zeit, 2013, 47, 356 – 366 MIKROWELLEN hältnisse der Substrate, Reagenskonzentration sowie Reaktionszeit und -temperatur im gleichen Zeitraum getestet werden. Die so erhaltenen sechs Dihydropyrimidine 14 mit einer Thioesterfunktionalität wurden im nächsten Schritt mit fünf unterschiedlichen Boronsäuren ein einer Palladiumkatalysierten C-C-bindungsknüpfenden Liebeskind-Srogl Reaktion zu 30 diversen Aroyl-dihydropyrimidinen 17 umgesetzt. Bei einer Reaktionszeit von 1 Stunde würde die Synthese einer 30-teiligen Substanzbibliothek 30 Stunden dauern, wenn automatisiert sequenziell gearbeitet würde. Werden die Produkte allerdings parallel in einem Rotorsystem hergestellt, ist nur ein einziges Mikrowellenexperiment von 1 Stunde Reaktionszeit von Nöten, was eine erhebliche Zeitersparnis mit sich bringt. Parallele Mikrowellensynthese kann in unterschiedlichen Formaten durchgeführt werden. Dafür sind unterschiedliche Rotorsysteme mit einer Vielzahl an Positionen (von 6–96) kommerziell erhältlich [2a]. Bei Verwendung von Mikrotiterplatten können sogar bis zu knapp 200 Reaktionen simultan ausgeführt werden. Um auch in Mikrotiterplatten vergleichbare Reaktionsbedingungen wie im geschlossenen Gefäß in „Single-mode“-Geräten zu schaffen, wurde ein Plattensystem mit einem Temperatur- und Drucklimit von 200 °C und 20 bar aus stark Mikrowellen-absorbierenden Silciumcarbid (SiC) entwickelt. Unter Verwendung von 5 mL Glas-Reaktionsgefäßen mit Schraubverschluss in einer Standard 6 × 4-Matrix wurden 24 Benzyliden-oxindole 20 durch eine Knoevenagel-Kondensation von sechs Oxindolen 18 mit vier Benzaldehyden 19 (Abbildung 11) in 10 Minuten in guten bis exzellenten Ausbeuten synthetisiert [13]. Eine Weiterentwicklung dieses SiC-Rotorsystems beinhaltet die Verwendung von Standard-HPLC/GC-Gefäßen, wobei der Transferschritt der Reaktionsmischung für die anschließende Analyse eliminiert wird, was wiederum eine höhere Zeiteffizienz mit sich bringt [14]. Mit generierten ABB. 13 O RG A N I S C H E S Y N T H E S E Substanzmengen von ca. 20–150 mg sind MikrotiterplattenRotorsysteme somit bestens geignet für die Hit-to-Lead(Weiterentwicklung eines Kanditatenmoleküls zu einer Leitverbindung) und Wirkstoff-Optimierungsphase bzw. für das Screening von Katalysatoren, Lösungsmittel und Substrat-Reaktivität. Mikrowellen: Heizmethode erster Wahl Im Wesentlichen kann jede Art von chemischer Umsetzung, die Wärme benötigt, unter Mikrowellen-Bedingungen durchgeführt werden. Die Einfachheit, mit der die Mikrowellen-Technologie genutzt werden kann, macht dieses nichtklassische Heizverfahren fast zu einem „Must-have“ in der modernen Synthesechemie. In der Vergangenheit wurden Mikrowellen-Bedingungen oft nur angewendet, wenn alle anderen Optionen, um eine bestimmte Reaktion durchzuführen, versagten, oder wenn eine Synthese extrem lange Reaktionszeiten oder hohe Temperaturen erforderte. Diese Vorgehensweise hat sich inzwischen erfreulicherweise geändert und synthetische Umsetzungen werden mittlerweile routinemäßig unter Verwendung von Mikrowellen-Bestrahlung durchgeführt. Die folgenden Beispiele zeigen deutlich, dass Mikrowellenchemie nicht mehr als letzter Ausweg gesehen wird, um sinnvolle Ausbeuten in angemessener Zeit zu erreichen. Wie erwähnt ist die Suzuki-Kreuzkupplung eine sehr beliebte Methode, um C-C-Bindungen zu knüpfen. Es gibt daher eine Reihe verschiedener Möglichkeiten um Mikrowellen-beheizte Suzuki-Reaktionen durchzuführen, die auch in zahlreichen anspruchsvollen Syntheseprojekten integriert wurden. Ein sehr elegantes Beispiel hierfür ist die von Wolkenberg et al. beschriebene Derivatisierung von tetrahalogenierten Chinolinen 21 durch sequentielle selektive Palladium-katalysierte Suzuki-Reaktionen (Abbildung 12) [15]. Ziel dieses Projektes war es, den Diversifizierungsschritt am Ende der Synthese durchzuführen. Üblicherweise kann M E H R S T U F E N - S Y N T H E S E D E S T R P C 3 - I N H I B I TO R S P Y R 3 ( 2 5 ) NHNH2 OEt CF3 O EtO + H2SO4, EtOH Rückfluss, 12 h, EtOH MW, 160 °C, 2 min O EtO2C NO2 EtO2C HO2C N Cl CF3 BOP, DIEA, DMF rt, 12 h + N Cl 24 Cyclohexen, Pd/C, EtOH MW, 160 °C, 2 min 23 CF3 N N N NO2 EtO2C 5% Pd/C, H2, EtOAc rt, 2 h CF3 NH2 Chem. Unserer Zeit, 2013, 47, 356 – 366 Cl N PCl3, MeCN MW, 150 °C, 5 min 25 www.chiuz.de O CONV: 25% MW: 57% Cl N H Cl Cl © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 363 eine Regio- und Chemoselektivität durch die Zuhilfenahme unterschiedlicher Katalysatoren und Liganden erreicht werden, in diesem Fall war dies jedoch mit einem einzigen Katalysator-Liganden-System möglich, indem nur die Reaktionstemperatur und -zeit variiert wurden. Dieser Syntheseweg beruht darauf, dass zwischen drei Halogeniden (Cl, Br, I) unterschieden werden kann und somit die Selektivität sowohl von der Reaktivität des Halogenids und den elektronischen Effekten als auch von dessen Position im Chinolinring 21 abhängt. Die erste Suzuki-Reaktion fand somit an der reaktivsten Stelle statt: an der 6-Iod-Position. Hierfür reichten 90 °C und 15 Minuten. Eine höhere Temperatur von 160 °C war für die 2. und 3. Kupplung nötig, wobei das Bromid in 3-Position innerhalb 15 Minuten zuerst reagierte, gefolgt vom Chlorid in 4-Position. Die Synthese von 22 konnte auch in einem Eintopfverfahren durch sequentielle Erwärmung einer einzigen Reaktionsmischung nach Zugabe der jeweiligen Boronsäure bzw. Boronsäurester und jeweils 10 mol% frischen Katalysators durchgeführt werden. In der 3-stufigen Synthese von Pyr3 (25), einem auf Pyrazol basierenden Inhibitor von TRPC3-Kanälen (canonical transient receptor potential), konnte durch MikrowellenHeizen nicht nur die Gesamtzeit der Synthese von zwei Tagen auf nur 40 Minuten verkürzt, sondern auch die Gesamtausbeute von 25 auf 57 % erhöht werden (Abbildung 13) [16]. Die Kondensation zu Pyrazol 23 und Reduktion der Nitrogruppe zum Amin mittels katalytischer Transferhydrierung gelangen zudem in einer Eintopfsynthese, wobei nach der ersten Reaktion einfach Cyclohexen und der Palladium-Katalysator in das abgekühlte Reaktionsgemisch gegeben und ein weiteres Mal erhitzt wurde. Anilin 24 konnte ohne Chromatographie-Aufreinigung durch einen Amidierungsschritt weiter zu Pyr3 (25) umgesetzt werden. ABB. 14 Für die Mikrowellensynthese wurden einige der Originalbedingungen durch Mikrowellen-kompatiblere ersetzt: Insbesondere die Vermeidung von gasförmigen Wasserstoff im Hydrierschritt erhöhte die Sicherheit und auch Praktikabilität. In der Totalsynthese von Rosiglitazon – ein blutzuckersenkender Wirkstoff für Diabetes Mellitus Typ II – wurde die Mikrowelle in vier von sechs Syntheseschritten eingesetzt (Abbildung 14), wodurch wiederum die Reaktionszeit von ca. 2 Tagen auf 1 Stunde verkürzt und auch die Ausbeuten verbessert wurden [17]. Im Vergleich zur konventionell beheizten Synthese benötigten auch hier die durch Mikrowellen-Heizen erhaltenen Intermediate keine langwierigen Aufreinigungsschritte wie Vakuumdestillation oder Säulenchromatographie. Ein noch eindrucksvolleres Beispiel ist die asymmetrische Totalsynthese des Pilzmetaboliten (-)-Stephacidin A, wobei von den 17 Reaktionsschritten 6 in der Mikrowelle durchgeführt wurden [18]. Problem der Maßstabsvergrößerung Die überwiegende Anzahl an publizierten Mikrowellen-unterstützten Reaktionen der letzten 25 Jahre beschreibt Synthesen im Milligramm- oder Gramm-Maßstab. Zum Teil ist dies auf die Popularität der „Single-mode“ Geräte zurückzuführen, die jedoch nur kleine Reaktionsvolumina (in der Regel 1–5 mL) im geschlossen Gefäß zulassen. Für die industrielle Verwertbarkeit dieser Technik ist es jedoch essentiell, die Skalierbarkeit dieser Reaktionen auf den Kilogramm-Maßstab und in weiterer Folge auf Produktionsmaßstab (Tonnen) zu gewährleisten. Durch die vergleichsweise begrenzte Eindringtiefe von Mikrowellenstrahlung in absorbierende Flüssigkeiten (typischerweise wenige Zentimeter) ist die Maßstabsvergröße- TOTA L S Y N T H E S E D E S B LU T Z U C K E R S E N K E N D E N W I R K S TO F F E S ROS I G L I TA ZO N O S + Cl H2N OH NH2 rt, 2 h H2 O 100 °C, 12 h S H2O HN N H O S H2 O MW, 140 °C, 10 min O F Cl N + Me H N OH + MW, 140 °C, 20 min N N Me CHO CONV: 82% MW: 90% DMF, NaH 80 °C, 8 h OH 140 °C, 15 h O N H O KOH, H2O, Toluen, TBAHS MW, 85 °C, 20 min N N Me MW: 92% CONV: 85% O O O Mg, MeOH, I2 S NH N 364 N Me Toluen, Piperidin, AcOH Rückfluss, 15 h NH rt, 3 h 95% Rosiglitazon CONV: 80% MW: 90% + O S CHO O © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim N N Me O Toluen, Piperidin, AcOH, SiO2 MW, 130 °C, 10 min S O N H O CONV: 85% MW: 93% www.chiuz.de Chem. Unserer Zeit, 2013, 47, 356 – 366 MIKROWELLEN rung (Scale-up) von Mikrowellen-unterstützten Synthesen eine große technische Herausforderung. Zwei unterschiedliche Ansätze wurden entwickelt: die Batch-Synthese und die kontinuierliche Durchfluss- bzw. Stop-Flow-Technik in größeren „Multimode“-Reaktoren. In der organischen Synthese kann eine Maßstabsvergrößerung mit kommerziell erhältlichen „Multimode“-Instrumenten in Batch entweder in einem einzelnen Reaktionsgefäß oder in den bereits genannten Rotorsystemen – mit jeweils bis zu ca. 1 L Gesamtvolumen – erfolgen [19]. Ein Nachteil der Paralleltechnik ist allerdings, dass ohne Automatisierung die Befüllung und Entleerung mehrerer Behälter sehr mühsam ist, insbesondere wenn Feststoffe beteiligt sind. Als Folge der offensichtlichen Limitierung des BatchVerfahrens gewann die Durchführung von Mikrowellenchemie unter Durchfluss- bzw. Stop-Flow-Bedingungen an Bedeutung, wobei die Reaktionsmischung z. B. durch eine Spule, die in der Mikrowellenkammer positioniert ist, gepumpt wird [19]. Jedoch ist auch diese Technik mit einem wesentlichen Manko behaftet: Heterogene Reaktionsgemische und hochviskose Flüssigkeiten sind generell inkompatibel. Dessen ungeachtet hat sich in den vergangenen Jahren eine beträchtliche Anzahl an Mikrowellen-Synthesen bereits ihren Weg in die Scale-up-Labors gebahnt [2a, 19]. Die Mikrowellen-Technologie wird schließlich zunehmend in der frühen Scale-up-Phase in einem 0,5 bis 5 kg-Maßstab – speziell für die Herstellung von Zwischenprodukten und Wirkstoffen – benötigt. Wünschenswert hierbei ist eine direkte Skalierbarkeit der Synthesen vom kleinen Maßstab – typischerweise durchgeführt in einem „Single-mode“-Instrument – auf einen Größeren in „Multimode“-Reaktoren. Bei Verwendung handelsüblicher Batch-Instrumente können typischerweise Produktmengen im Bereich von 50 bis 500 g pro Lauf hergestellt werden, was einer Tagesmenge von einigen Kilogramm entspräche [20]. Diese Maßstäbe werden auch von Mikrowellen-Durchflussreaktoren erreicht [20]. Mikrowelleneffekte: Mythos oder Wirklichkeit? Seit Beginn der Mikrowellensynthese führten die gegenüber Synthesen im Ölbad erhöhten Reaktionsgeschwindigkeiten und die manchmal abweichenden Produktverteilungen zu Spekulationen über „spezifische“ oder „nicht-thermische“ Mikrowelleneffekte [21]. Derartige Effekte wurden postuliert, wenn eine Synthese unter Mikrowellenbedingungen bei scheinbar gleicher Temperatur ein anderes Ergebnis lieferte als die entsprechende konventionell beheizte. Nichtthermischen Effekten wird zugeschrieben, dass sie von einer direkten – oft stabilisierenden – Wechselwirkung des elektromagnetischen Feldes mit bestimmten Molekülen, Zwischenprodukten oder sogar Übergangszuständen im Reaktionsmedium herrühren, die nicht mit einer Änderung der Reaktionstemperatur in Verbindung stehen. Die meisten Wissenschaftler sind sich heute jedoch einig, dass die Chem. Unserer Zeit, 2013, 47, 356 – 366 O RG A N I S C H E S Y N T H E S E Energie der Mikrowellenphotonen bei Weitem zu niedrig ist, um direkt molekulare Bindungen zu spalten. Daher können Mikrowellen keine chemischen Reaktionen durch direkte Absorption von elektromagnetischer Energie „induzieren“. In vielen Fällen, in denen spezifische/nicht-thermische Mikrowelleneffekte geltend gemacht wurden, konnte allerdings nach einer erneuten sorgfältigen Untersuchung gezeigt werden, dass vorwiegend experimentelle Artefakte – die aus fehlerhaften Temperaturmessungen und ineffizientem Rühren der Reaktionsmischung hervorgehen – für die ursprünglich beobachteten Phänomene verantwortlich waren [22]. Nach erheblichen Debatten stimmt man heute darin überein, dass der Grund für die beobachtete Geschwindigkeitserhöhung zumeist ein rein thermisches/kinetisches Phänomen infolge des schnellen Aufheizens und der hohen Reaktionstemperaturen (siehe Abb. 2) durch dielektrisches Mikrowellenheizen ist [22]. Zusammenfassung Das kontrollierte Mikrowellen-Heizen, besonders die Variante in geschlossenen Reaktionsgefäßen, bietet viele Vorzüge gegenüber traditionell beheizten Synthesen. Schnellere Reaktionszeiten, höhere Ausbeuten und bessere Reproduzierbarkeit zählen wohl zu den Wichtigsten. Außerdem kann die Mikrowellensynthese leicht an eine parallele oder automatisierte sequenzielle Arbeitsweise angepasst werden. Aufgrund der einfachen Handhabung der Mikrowellentechnologie und der Tatsache, dass man für eine bestimmte chemische Umwandlung binnen 5–10 Minuten ein aussagekräftiges Ergebnis („Ja“ oder „Nein“) erhalten kann, wird diese neuartige Heizmethode bereits an vielen Universitäten und in der Industrie vor allem zur schnellen Reaktionsoptimierung und zur effizienten Synthese neuer Verbindungen genutzt. Summary Controlled microwave heating, in particular using sealed-vessel systems, offers many advantages over traditionally heated syntheses. As most important ones are considered: reduced reaction times, higher yields and reproducibility. In addition, it can rapidly be adapted to a parallel or automated sequential processing format. Because of the convenience of microwave technology and the fact that a „yes or no answer“ for a particular chemical transformation can often be obtained within 5 to 10 minutes, this heating method is an efficient tool for many academic and industrial research groups. There it is primarily used for rapid reaction optimization and efficient synthesis of new chemical entities. Schlagwörter Mikrowellenbestrahlung, Hochtemperaturchemie, Reaktionsbeschleunigung, Kreuzkupplung, Mikrowelleneffekte www.chiuz.de © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 365 Literatur [1] a) R. Gedye, F. Smith, K. Westaway, H. Ali, L. Baldisera, L. Laberge und J. Rousell, Tetrahedron Lett. 1986, 27, 279; b) R. J. Giguere, T. L. Bray, S. M. Duncan und G. Majetich, Tetrahedron Lett. 1986, 27, 4945. [2] a) Microwaves in Organic Synthesis, 3. Aufl., (Hrsg.: A. De La Hoz und A. Loupy), Wiley-VCH, Weinheim, 2012; b) C. O. Kappe, A. Stadler und D. Dallinger, Microwaves in Organic and Medicinal Chemistry, 2. Aufl., Wiley-VCH, Weinheim, 2012; c) C. O. Kappe und D. Dallinger, Mol. Diversity 2009, 13, 71; d) S. Caddick und R. Fitzmaurice, Tetrahedron 2009, 65, 3325; e) C. O. Kappe, Chem. Soc. Rev. 2008, 37, 1127; f) C. O. Kappe, Angew. Chem., Int. Ed. 2004, 43, 6250. [3] M. Damm, T. N. Glasnov und C. O. Kappe, Org. Process Res. Dev. 2010, 14, 215. [4] P. Appukkuttan und E. Van der Eycken, Eur. J. Org. Chem. 2008, 1133. [5] a) T. N. Glasnov, S. Findenig und C. O. Kappe, Chem. Eur. J. 2009 15, 1001 ; b) P. Walla und C. O. Kappe, Chem. Commun. 2004, 564; c) T. N. Glasnov und C. O. Kappe, Adv. Synth. Catal. 2010, 352, 3089. [6] a) R. K. Arvela und N. E. Leadbeater, J. Org. Chem. 2005, 70, 1786; b) R. K. Arvela, N. E. Leadbeater, M. S. Sangi, V. A. Williams, P. Granados und R. S. Singer, J. Org. Chem. 2005, 70, 161. [7] B. Willy, F. Rominger und T. J. J. Müller, Synthesis 2008, 293. [8] a) Z. Zhao, D. D. Wisnoski, S. E. Wolkenberg, W. H. Leister, Y. Wang und C. W. Lindsley, Tetrahedron Lett. 2004, 45, 4873; b) C. O. Kappe und D. Dallinger, Nat. Rev. Drug Discovery 2006, 5, 55. [9] V. A. Chebanov, V. E. Saraev, S. M. Desenko, V. N. Chernenko, S. V. Shishkina, O. V. Shishkin, K. M. Kobzar und C. O. Kappe, Org. Lett. 2007, 10, 1691. [10] T. N. Glasnov, W. Stadlbauer und C. O. Kappe, J. Org. Chem. 2005, 70, 3864. [11] R. Van Noorden,Chemistry World 2008, 5(10), 40. [12] L. Pisani, H. Prokopcová , J. M. Kremsner und C. O. Kappe, J. Comb. Chem. 2007, 9, 415. [13] M. Treu, T. Karner, R. Kousek, H. Berger, M. Mayer, D. B. McConnell und A. Stadler J. Comb. Chem. 2008, 10, 863. [14] a) M. Damm und C. O. Kappe J. Comb. Chem. 2009, 11, 460; b) M. Damm und C. O. Kappe Mol. Diversity 2012, 16, 5. [15] M. B. Nolt, Z. Zhao und S. E. Wolkenberg, Tetrahedron Lett. 2008, 49, 3137. [16] T. N. Glasnov, K. Groschner und C. O. Kappe, ChemMedChem 2009, 4, 1816. 366 © 2013 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim [17] S. L. Gaonkar und H. Shimizu, Tetrahedron 2010, 66, 3314. [18] G. D. Artman III, A. W. Grubbs und R. M. Williams, J. Am. Chem. Soc. 2007, 129, 6336. [19] a) J. D. Moseley, Microwave Heating as a Tool for Sustainable Chemistry, (Hrsg.: N. E. Leadbeater) CRC Press, Taylor & Francis Group, Boca Raton, 2011, S. 105-147; b) C. R. Strauss, Org. Process Res. Dev. 2009, 13, 915; c) H. Lehmann, New Avenues to Efficient Chemical Synthesis, (Hrsg.: P. H. Seeberger und T. Blume), Springer-Verlag, Berlin, 2007; d) J. M. Kremsner; A. Stadler und C. O. Kappe, Top. Curr. Chem. 2006, 266, 233. [20] a) D. Dallinger, H.Lehmann, J. D. Moseley, A. Stadler und C. O. Kappe Org. Process Res. Dev. 2011, 15, 841; b) J. D. Moseley, P. Lenden, M. Lockwood, K. Ruda, J.-P. Sherlock, A. D. Thomson und J. P. Gilday, Org. Process Res. Dev. 2008, 12, 30. [21] a) A. De La Hoz, A. Diaz-Ortiz und A. Moreno, Chem. Soc. Rev. 2005, 34, 164; b) L. Perreux und A. Loupy, Tetrahedron 2001, 57, 9199. [22] C. O. Kappe, B. Pieber und D. Dallinger, Angew. Chem., Int. Ed. 2013, 52, 1088. Die Autorin www.chiuz.de Doris Dallinger, geboren 1976, studierte an der KarlFranzens-Universität Graz Chemie und promovierte in der Arbeitsgruppe von C. Oliver Kappe zum Thema der Mikrowellen-assistierten organischen Synthese und High-Throughput-Synthese. Nach Forschungsarbeiten als PostDoc im ChristianDoppler-Labor für Mikrowellenchemie trat sie 2011 in das Institut für Chemie an der Universität Graz als wissenschaftliche Mitarbeiterin (Senior Scientist) ein. Korrespondenzadresse: Dr. Doris Dallinger Institut für Chemie Karl-Franzens-Universität Graz Heinrichstrasse 28 A-8010 Graz E-Mail: [email protected] Chem. Unserer Zeit, 2013, 47, 356 – 366