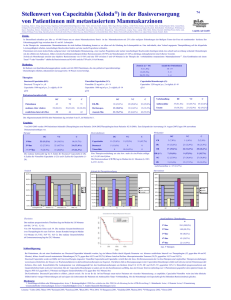
Wirksamkeit von Capecitabin bei rezidivierten Kopf-Hals
Werbung

Aus dem Klinikum Offenburg
Akademisches Lehrkrankenhaus der Albert-Ludwigs-Universität Freiburg i.Br.
Wirksamkeit von Capecitabin
bei rezidivierten Kopf-Hals-Tumoren
INAUGURAL-DISSERTATION
zur
Erlangung des Zahnmedizinischen Doktorgrades
der Medizinischen Fakultät
der Albert-Ludwigs-Universität
Freiburg i.Br.
Vorgelegt 2008
von Anne Julia Schottler
geboren in Hannover
Dekan
Prof. Dr. C. Peters
1.Gutachter
Prof. Dr. F. W. Hirsch
2.Gutachter
Prof. Dr. Dr. R. Schmelzeisen
Jahr der Promotion
2008
-1-
Inhaltsverzeichnis
1.
Einleitung……………………………………………………………………….4
1.1
Kopf- und Hals-Tumoren………………………………………………...…….4
Anatomie-Darstellung.…………………………………………………………5
1.1.1 Risikofaktoren...........................................................................................5
1.1.2 Histologie……………………………………………………………………….6
1.1.3 Tumorstaging…………………………………………………………………..6
1.1.4 TNM-Schema, Stadieneinteilung…………………………………………….8
1.1.5 Prognosen………………………………………………………………………9
1.1.6 Rezidive……………………………………………………………………….10
-2-
1.2
Therapiemöglichkeiten……………………………………………………..10
1.2.1 Chirurgische Therapie……………………………………………………….11
1.2.2 Radiotherapie…………………………………………………………………11
1.2.3 Chemotherapie…………………...…………………………………………..12
1.2.4 Simultane Chemoradiotherapie…………………………………………….14
1.2.5 Thyrosinkinaseinhibitoren…………………………………………………...14
1.2.6 Rezidive und Zweittumoren…………………………………………………15
1.3
Capecitabin…………………………………………………………………..15
Strukturformel von 5-FU und Capecitabin-Darstellung.………………….16
1.3.1
Pharmakokinetik……………………………………………………………..16
Enzymatische Aktivierung-Darstellung.…………………………………...17
1.3.2
Nebenwirkungen……………………………………………………………..18
-3-
1.3.3
Anwendung…………………………………………………………………..18
2.
Material und Methode..…………………………………………………….19
3.
Ergebnisse…………………………………………………………………...21
3.1
Nebenwirkungen...…………………………………………………………...26
4.
Diskussion…………………………………………………………………...28
5.
Zusammenfassung…………………………………………………………35
6.
Literaturverzeichnis………………………………………………………..36
7.
Danksagung…………………………………………………………………48
-4-
1. Einleitung
1.1 Kopf- und Hals-Tumoren
Kopf-Hals-Tumoren entsprechen im Jahre 2002 rund 6% der gesamten
Tumorerkrankungen weltweit [65]. In den letzten 30 Jahren fand eine Wende
bezüglich der Inzidenz und Letalität (jährlich 6/100000) maligner Erkrankungen
des Aerodigestivtraktes statt [6,50]. Bei den Frauen erfolgte ein kontinuierlicher
Anstieg von Neuerkrankungen, während sie bei den Männern konstant blieben.
Das veränderte Konsumverhalten in der westlichen Gesellschaft mit dem
„modern way of life“ und die gesteigerter Lebensqualität ist ein wesentlicher
Grund dafür [65]. Das Verhältnis der Prädilektion von Kopf-Hals-Tumoren liegt
im regionalem Durchschnitt bei 4:1 (Männer : Frauen) [6,50].
In Ländern mit großer Sonneneinstrahlung gibt es hohe Inzidenzen für
Plattenepithelkarzinome der Unterlippe:
Südaustralien 13/100000
Spanien
Ungarn
11/100000
21,2/ 100000
Die Inzidenzen in Europa und USA sind insgesamt niedrig: 1,8/ 100000 [65].
Die Mundhöhlenkarzinome treten meist zwischen dem 50. und 60. Lebensjahr
auf, die Oropharynxkarzinome im Alter von 60 bis 70 Jahren [65].
Zu den Kopf-Hals-Tumoren zählen Tumore im Bereich der Mundhöhle, des
Oropharynx, des Hypopharynx, des Larynx und der Nasennebenhöhlen (NNH).
Ebenso gehören in die Gruppe die Nasenpharynxkarzinome und die
Speicheldrüsentumoren.
Trotz
unterschiedlicher
Lokalisation
sind
die
Behandlungskonzepte
grundsätzlich gleich [68,69,82,84].
Tumore im vorderen Mundboden haben eine bessere Prognose als die sich
submukös im Hypopharynx ausbreitenden Tumore. Die Larynxkarzinome haben
durch häufige lokale Begrenzung eine bessere Prognose. Die NNH-Karzinome
mit einer Inzidenz von 1:100000 sind bekannt als Berufskrankheit in der Holz-,
-5-
Textil oder Uhrenindustrie durch Exposition mit Holzstaub, Propylalkohol und
Radium [1,44,76,87]. Die Nasenpharynxkarzinome kommen in fernöstlichen
Regionen im jüngeren Alter vor und sind prognostisch schwierig mit größerer
Tendenz zur Fernmetastasierung [2,14,25,35].
Anatomie
Darstellung 1 : paramedianer Sagitalschnitt im Bereich Kopf und Hals
1.1.1 Risikofaktoren
Die Risikofaktoren der Oropharynxskarzinome sind folgende Kanzerogene:
-Nikotin, Alkohol: mengenabhängige Kanzerogenität, zu 90% Auslöser von
Mundboden-Ca und Larynx-Ca
-Kautabak
-Schlechte Mundhygiene
-Vitaminmangel
-Eppstein-Barr-Virus
-6-
-Ionisierende Strahlung
-Immunsuppression
Berufliche Exposition:
- Benzpyren von Teerarbeitern
- Buchenstaub in der Holzindustrie
Sonnenexposition ist ein Risikofaktor der Lippenkarzinome.
1.1.2 Histologie
Histologisch
betrachtet
sind
über
90%
der
Kopf-Hals-Tumoren
Plattenepithelkarzinome.
Auf den lymphatischen Waldeyer’ Rachenring fallen 2,5%.
Zu den histologischen Formen zählen das Plattenepithelkarzinom, das
Adenokarzinom, das undifferenzierte Karzinom vom Nasopharynxstyp, die
adenoidzystischen Karzinome, die mukoepidermoiden Karzinome und auch
Lymphome, Melanome, Sarkome und extramedulläre Plasmazytome.
Zu den Präkanzerosen der Plattenepithelkarzinome gehören die Leukoplakien
mit folgenden Fomen und Entartungsraten nach WHO 2005:
Homogene Form :
Leucoplakia simplex
Inhomogene Form :
Leucoplakia verrucosa 24%
Leucoplakia errosiva
3%
38%
Die Erythroplakie gilt als Sonderform und ist zu 90% ein Carcinoma in situ [65].
1.1.3 Tumorstaging
Das Ziel des Tumorstaging ist die Abklärung des Primärtumors und der
lokoregionären Lymphknoten. Dafür stehen obligatorisch das CT- oder MRI-
-7-
Verfahren oder die Biopsie und die Panendoskopie zur Auswahl. Fakultativ
können
noch
die
Feinnadelaspiration,
die
Halssonographie,
das
Oesophagogramm oder eine Halslymphknotendissektion oder das PET bei
CUP-Syndrom hinzugezogen werden.
Das Erkennen von Fernmetastasen in der Lunge durch ein Thorax-Röntgen
oder im Knochen mit Hilfe einer Skelettszintigraphie und die Abklärung der
Leber durch die Abdomensonographie oder CT sind für das Tumorstaging
maßgeblich.
Zu den Zielen des Tumorstaging gehört auch das Erkennen von weiteren
Organerkrankungen
und
der
Ausschluss
eines
synchron
bestehenden
Zweittumors.
Eventuell muss das Tumorstaging durch endoskopische Eingriffe erweitert
werden.
-8-
1.1.4 TNM-Schema, Stadieneinteilung
TNM- Klassifikation von Lippen- und Mundhöhlenkarzinomen (UICC 2002)
Tx Primärtumor nicht beurteilbar / unbekannt
T1
Tumor ≤ 2cm
T2 Tumor > 2cm, ≤ 4cm
T3 Tumor > 4cm
T4 Tumor in benachbarte Strukturen (Knochen, Knorpel, Weichteile)
N0 keine regionären LK-Metastasen
N1 solitäre ipsilaterale LK-Metastasen ≤ 3cm
N2 LK > 3cm, ≤ 6cm
N3
N2a
solitäre ipsilaterale LK-Metastasen
N2b
multiple ipsilaterale LK-Metastasen
N2c
bilaterale / kontralaterale LK-Metastasen
LK-Metastasen > 6cm
M0 keine Fernmetastasen
M1 Fernmetastasen nachweisbar
Stadieneinteilung
Stadium I
T1
N0
M0
Stadium II
T2
N0
M0
Stadium III
T1-2
N1
M0
T3
N0-1
M0
T1-3
N2
M0
T4a
N0-2
M0
jedes T
N3
M0
T4b
jedes N
M0
jedes T
jedes N
M1
Stadium IVa
Stadium IVb
Stadium IVc
[65]
-9-
1.1.5 Prognosen
Die lokoregionäre Ausdehnung und die Tumorkontrolle sind maßgebend für die
Prognose. Folgende prognostische Faktoren wie Alter, Allgemeinzustand,
Ernährungszustand,
Begleiterkrankung,
Größe
des
Primärtumors
und
Lymphknotenstatus, histologischer und zytologischer Differenzierungsgrad,
Infiltrationstiefe des Tumors haben Auswirkungen auf die Überlebensrate.
Ebenso nehmen auch Lymphknotenkapseldurchbruch, Geschlecht (Frauen
haben bessere Überlebenschance) und das Vorhandensein und die Verbreitung
von Lymphknotenmetastasen Einfluss auf das Überleben der Patienten.
Je lateraler der Tumor lokalisiert ist, desto günstiger wirkt sich das auf die
Überlebenszeit aus.
Tumoren, welche im Zungengrund und an der posterioren Pharynxwand
lokalisiert sind, haben schlechtere Prognosen als solche in der Gaumen- und
Tonsillarregion [65].
Fasst man alle Tumoren zusammen, so wird eine 5-Jahres-Überlebensrate von
28% und eine krankheitsfreies Überlebensrate von 41% erreicht. 25% der
Langzeitüberlebenden tragen das Risiko der Bildung von Zweittumoren [65].
- 10 -
1.1.5 Rezidive
Die größte Anzahl der lokoregionären und distanten Rezidive kann innerhalb
von 2 Jahren nach der Primärtherapie beobachtet werden, so dass bereits nach
dieser Zeit der Einfluß der Tumorerkrankung auf das Überleben erkennbar wird.
Hierbei gibt es allerdings sehr große individuelle Schwankungen [65].
Bei der klinischen Diagnose eines lokalen Tumorrezidiv sind oftmals kurative
Therapiekonzepte kaum noch verfügbar. Die Therapie hat überwiegend
palliativen Charakter. In Abhängigkeit der Größe des Rezidivtumors und des
Allgemeinzustandes des Patienten werden meist umfangreiche chirurgische
Resektionen bzw. Rekonstruktionen zugunsten nichtchirurgischer, palliativ
intendierter Therapiemodalitäten vermieden. Die Tumorlokalisation, die Tumorgröße sowie eine R1- oder R2-Resektion werden in der Literatur als
wesentliche Ursache für das Auftreten lokaler Tumorrezidive angesehen [20].
1.2
Therapiemöglichkeiten
Etwa 30% aller Tumoren werden im Frühstadium (T1N0, T2N0) erkannt und zu
mehr als 90% der Fälle werden sie kurativ chirurgisch und/oder radiologisch
therapiert. Die 60% der intermediären (T2N1, T3N0) oder fortgeschrittenen (T34 N2-3 M0) Erkrankungen (in 10% der Fälle liegen Fernmetastasen vor) können
weniger als zu 30% kurativ therapiert werden.
Deshalb sollte nach multidisziplinärer Abklärung das für den Patienten optimale
Therapiekonzept
in
Abhängigkeit
von
Stadium
und
Ausdehnung
der
Erkrankung, der Physis des Patienten und der Erfahrung des behandelnden
Teams ausgewählt werden. Gleichzeitig wird eine kurative oder palliative
Behandlungsstrategie festgelegt [65].
- 11 -
1.2.1 Chirurgische Therapie
Grundsätzlich gilt bei der chirurgischen Therapie die R0-Resektion bzw. die
Resektion des Tumors „in sano“ mit histopathologisch nachgewiesener
Tumorfreiheit an den Resektionsrändern.
Zusätzlich
können
neben
der
plastisch-chirurgischen
Wiederherstellung
vereinzelt suspekte und vergrößerte Lymphknoten entfernt werden [63].
Die „neck dissection“ (radikal, modifiziert radikal, funktionell oder selektiv) ist
nicht als diagnostische, sondern als therapeutische Maßnahme gedacht,
befallene Lymphknoten zu entfernen. Dies kann mit unterschiedlicher
Radikalität vorgenommen werden. In der Regel wird die funktionelle neck
dissection, uni-oder bilateral als Therapie der Wahl durchgeführt. Aufgrund der
Nebenwirkungen wird keine prophylaktische neck dissection vorgenommen.
Bei Nachweis von regionären Lymphknotenmetastasen im Frühstadium kann
die chirurgische Dissektion auch durch perkutane Radiatio ersetzt werden
[57,66].
Die
Kombination
aus
selektiver
suprahyoidaler
neck
dissection
mit
anschließender Nachbestrahlung gilt als besonders effektiv [19].
1.2.2 Radiotherapie
Die folgenden Formen können zur Anwendung kommen:
-
postoperativ adjuvant (R0-Resektion)
-
additiv (R1-Resektion)
-
neoadjuvante Radio-/ Chemotherapie
-
palliative Radiatio ( Rezidivtherapie)
[17,19,52]
Die tumorizide Wirkung der Strahlentherapie ist von der Gesamtdosis abhängig,
welche jedoch durch die Gewebespätreaktion begrenzt ist [17,19,52].
- 12 -
Die Strahlentherapiedosen für Primärtumoren oder das Primärtumorbett
betragen 66-76 Gy. Diese Strahlendosis wird auch für positive Halslymphknoten
angewendet. Bei klinisch unauffällige Halslymphknoten reichen auch 45-50 Gy.
Durch hyperfraktionierte Therapiemethoden können kollaterale Schädigungen
in Form von akuten oder Gewebespätreaktion deutlich reduziert werden
[17,19,52].
1.2.3 Chemotherapie
In den letzten Jahren kam es zu einem deutlichen Umdenken bei der
Behandlung von Kopf-Hals-Tumoren durch die Chemotherapie. So beschränkte
sich früher die Chemotherapie lediglich auf die palliative Behandlung von
Metastasen und Tumorrezidiven. Die Chemotherapie heute wird auch zur
primären Behandlung von inoperablen Tumoren oder organerhaltenden
Therapie von Larynx- und Hypopharynxkarzinomen eingesetzt. Häufig wird sie
alternierend oder simultan mit der Radiotherapie kombiniert. Dadurch hat sich
eine signifikante Verlängerung der Überlebenszeiten ergeben [21,49].
Pignon konnte eine Erhöhung der Überlebenszeit um 8% nach 5 Jahren durch
Radiochemotherapie nachweisen [53].
Als typische Standardsubstanzen für die Monotherapie sind zu nennen:
-
Methotrexat ( rezidivierende + metastasierende HNO-Tumoren)
40-50 mg/m2 pro Woche
Remissionsrate: 30%
-
Cisplatin
100-120 mg/m2
Remissionsrate: 28%
-
Carboplatin
Remissionsrate: 26%
- 13 -
-
5-FU ( Fluoropyrimidine)
1000 mg/m2 als Dauerinfusion, d 1-4
Remissionsrate: 17%
-
Ifosamid
Remissionsrate: 26% , unvorbehandelt 43%
Weitere aktive Substanzen sind Cyclophosphamid, Doxorubicin und Bleomycin.
Die Responserate beträgt hier 10-30% [65].
Es
gibt
neue
gut
wirksame
Substanzen
wie
Paclitaxel,
Docetaxel
(Remissionsrate: 38%),Gemcitabin (Remissionsrate: 13-22%),
Topotecan (Remissionsrate: 14-22%), Vinorelbin (Remissionsrate: 22%) und
Oxaliplatin (Remissionsrate: 10%).
Die Kombinationstherapie ist häufig sinnvoll, da verschiedene Substanzen
synergistisch wirken oder sich gegenseitig in ihrer Wirkung verstärken.
Die neoadjuvante Chemotherapie, auch Induktionstherapie genannt, konnte in
vielen Studien durch hohe Ansprechraten und z. T. Komplettremissionen einen
neuen Weg aufzeigen. Hierdurch wurden sonst sehr radikale chirurgische
Eingriffe deutlich vereinfacht [27].
Außerdem konnte die Inzidenz von Fernmetastasen deutlich verringert werden.
Eine typische Zweier-Kombinationstherapie in der neoadjuvanten Form ist
Cisplatin und 5-FU. Diese konnte Ansprechraten von über 90% und komplette
Remissionen von ca. 40% aufzeigen [15,16].
Eine Dreier-Kombinationstherapie von Cisplatin, 5-FU und Docetaxel konnte
ebenfalls Ansprechraten von 90% bewirken. Die EORTC-Studie untersucht bei
inoperablen Patienten die Wirksamkeit der Induktionstherapie der Zweier- oder
Dreierkombination
hinsichtlich
der
verlängerten
progressionsfreien
Überlebensraten. Eine adjuvante Chemotherapie nach Chirurgie und Radiatio
- 14 -
zeigte keinen Überlebensvorteil und ist häufig wegen des Allgemeinzustandes
der Patienten nicht in ausreichender Intensität durchführbar [83].
Während
die
Induktionstherapie
eine
verminderte
Häufigkeit
von
Fernmetastasen aufzeigen konnte, blieb die Inzidenz der lokoregionären
Rezidive
unverändert.
Da
nun
für
einige
Chemotherapeutika
eine
strahlensensibilisierende Wirkung nachgewiesen wurde [67,84], kann durch
gleichzeitige Therapie mit Chemotherapie und Bestrahlung eine verbesserte
lokoregionäre Tumorkontrolle sowie die Reduktion der Fernmetastasierungsrate
erreicht werden [81].
Allerdings kommen teilweise schwere Nebenwirkungen vor, die eine geplante
Unterbrechung der Therapie notwendig machen.
1.2.4 Simultane Chemoradiotherapie
Ziel: - verbesserte lokoregionäre Tumorkontrolle
- Reduktion der Fernmetastasierungsrate
Konzepte: 1.) perkutane Radiotherapie + simultane
Monosubstanzchemotherapie
2.) unterbrochene Radiotherapie + intensivierte
Kombinationschemotherapie
3.) alternierende Radiochemotherapie
4.) Radiochemotherapie kombiniert mit
Hyperfraktionierung (kleinere Dosen, kürzere Intervalle) [81]
1.2.5 Thyrosinkinaseinhibitoren
- Cetuximab (C225): monoklonaler Antikörper hemmt den
EGFR (Epidermal-Growth-Factor-Rezeptor)
- 15 -
1.2.6 Rezidive und Zweittumore
Als Rezidivtherapie muss man zwischen einer erneuten chirurgischen
Maßnahme und
einer Radiotherapie,
wenn diese vorher nicht
initial
durchgeführt wurde, abwägen. Wenn zusätzlich eine Chemotherapie indiziert
ist, erscheint eine simultane Radiochemotherapie sinnvoll.
Häufig
kommt
es
durch
Feldkanzerogenisierung
der
Schleimhaut
zu
Ausweitung des Tumorgeschehens bzw. zu Zweittumoren. Diese sind bei 1040% der Patienten nachweisbar und sind die häufigsten Todesursachen bei
Patienten mit Kopf-Hals-Tumoren [65].
Bei
9-14%
der
Patienten
bestehen
diese
Zweittumore
bereits
bei
Diagnosestellung der Primärtumore. Ihre jährliche Inzidenz beträgt zwischen 4
und 7% und sie verteilen sich gleichmäßig auf Kopf-, Hals-, Lungen- und
Speiseröhrenkarzinome[65].
Für die lokoregionären Rezidive, genau wie für die Zweittumore, gibt es keine
einheitliche palliative Standardtherapie [65].
1.3 Capecitabin
Mehr als 40 Jahre lang sind die Fluoropyrimidine, mit 5-FU als ihr
Hauptvertreter, Standardtherapien für eine große Bandbreite von
„soliden“
Tumoren, Brust- und Colorectalcarcinome eingeschlossen, entweder als
Monotherapie
oder
in
Kombination
mit
anderen
Zytostatika
oder
Biomodulatoren verwendet worden [73].
Es gab bisher zwei Arten von systemischer 5-FU Therapiegabe.
Zum einen die i.v. Bolus 5-FU Exposition, die mit Myelosuppression und
gastrointestinalen Intoxikationen wie Diarrhöe und Stomatitis vergesellschaftet
sein konnte [32], und zum anderen eine 5-FU Gabe als kontinuierliche i.v.
Infusion,
welche
weniger
gastrointestinale
Intoxikationen
und
- 16 -
Myelosuppressionen aufwies, dafür aber mehr Inzidenzen der Hautintoxikation,
das sogenannten Hand-Fuß-Syndrom zeigte [11].
Strukturformel von 5-FU und Capecitabin
Fluoropyrimidin-basierte „Prodrugs“
Capecitabin
O
NH
F
H
CO
O
F
N
N
O
N
O
N
H3 C
O
5-FU
Capecitabin
OH
OH
Darstellung 2 : chemische Struktur-Formeln der Wirkstoffe
1.3.1 Pharmakokinetik
Die Wirkung von Xeloda wird über eine dreifache enzymatische Kaskade aktiv.
Um eine tumorselektive Wirkung zu erreichen, wird Xeloda über die
Thymidinphosphorylase (TP) aktiviert. TP zeigt eine signifikant höhere Aktivität
im tumurösen Gewebe als im gesunden Gewebe [46].
Die Kaskade läuft folgendermaßen ab:
Capecitabin (N4-pentyloxycarbonyl-5´-deoxy-5-fluorocytidine) ist ein nichtzytotoxisches Fluoropyrimidincarbamat, welches als eine oral eingenommene
Vorstufe („Prodrug“) rasch vom Magen-Darmtrakt aufgenommen wird, mit einer
- 17 -
maximalen Plasmakonzentration nach 90 Minuten. Die Plasmaproteinbindung
beträgt weniger als 60 %.
Capecitabin wird über mehrere enzymatische Schritte aktiviert, indem es
zunächst durch die hepatische Carboxylesterase zu 5´DFCR metabolisiert wird,
welches dann durch die Cytidin-Deaminase, die vornehmlich in der Leber und
im Tumorgewebe lokalisiert ist, zu 5´-DFUR umgewandelt wird. Die weitere
katalytische Aktivierung von 5`-DFUR zu 5-FU erfolgt dann durch die ThymidinPhosphorylase (TP). Die Enzyme, die in die katalytische Aktivierung involviert
sind, finden sich sowohl im Tumorgewebe als auch in gesundem Gewebe. Im
malignen Tumorgewebe ist die Aktivität signifikant höher [48].
Capecitabin
Enzymatische Aktivierung
Leber
100%
Capecitabin
Capecitabin
Tumor
CE
5´-DFCR
Darmmukosa
?
CyD
5´-DFUR
5´-DFCR
CyD
5´-DFUR
Thymidinphosphorylase (TP)
5-FU
5´-DFCR = 5´-Deoxy-5-Fluorocytidin; 5´-DFUR = 5´-Deoxy-5Fluorouridin; CyD = Cytidindeaminase; CE = Carboxylesterase
Darstellung 3 : Enzymatische Umwandlung von Capecitabin zu 5-FU
In den malignen Zellen liegt ein hoher Anteil an Thymidinphosphorylase
(„Tumor Assoziierter Angiogenese Faktor“) vor, weshalb das Tumorwachstum,
aggressives Invasionsverhalten und schlechte Prognose auch in Abhängigkeit
mit
der
Aktivität
der
Thymidinphosphorylase
Thymidinphosphorylase wirkt antiapoptotisch [40,45,74].
stehen.
Die
- 18 -
In Studien konnte die Tumorselektivität von Capecitabin bewiesen werden. Das
Konzentrationsverhältnis von 5-FU war in malignem Tumorgewebe vier Mal
höher als im Plasma [64].
Die Wirksamkeit von Capecitabin ist durch den intrazellulären Umbau zu 5-FU
mit herkömmlichen 5-FU vergleichbar [38]. Capecitabin konnte sogar eine
höhere Dosis-Wirkungs-Beziehung zeigen als 5-FU [36]. Auch vertragen die
Patienten Capecitabin eher besser und müssen deutlich seltener wegen
schwerer Nebenwirkungen behandelt werden [7].
1.3.2 Nebenwirkungen
Seltener als bei 5-FU sind insbesondere Durchfall, Übelkeit, Erbrechen und vor
allem Stomatitis [22]. Dennoch kann es auch unter Capecitabin zu schwerem
Durchfall kommen. Deutlich häufiger kam es bei der peroralen Medikation zum
Hand-Fuß-Syndrom. Die Symptome reichen von Taubheitsgefühl, Kribbeln und
Missempfindungen bis zu starken Schmerzen in Handflächen und Fusssohlen.
Es kann auch zu Geschwür- und Blasenbildung an Händen oder Füssen
kommen [7,22,86].
1.3.3 Anwendung
Capecitabin wird üblicherweise zweimal täglich, morgens und abends, innerhalb
von 30 Minuten nach einer Mahlzeit eingenommen. Je nach Dosierung muss
der Patient jeweils drei bis sieben Tabletten schlucken. Bei schweren
Nebenwirkungen muss die Therapie unterbrochen oder die Dosis reduziert
werden.
- 19 -
2. Material und Methode
Es handelt sich um eine retrospektive Nachuntersuchung aller konsekutiven
Patienten, die an Karzinomen im Kopf-Hals-Bereich im palliativen Stadium
erkrankt sind und mit Xeloda als Monotherapie behandelt wurden. Alle
Patienten wurden bereits durch eine oder mehrere Vortherapien mit
chirurgischer Intervention, Radiatio mit 55-63Gy, durchschnittlich 60,8 Gy, und
z.T. anderen Chemotherapeutika vorbehandelt. Als Chemotherapeutika wurden
verwendet:
Cisplatin
zu 72%
5-FU
zu 22%
Carboplatin
zu 11%
Gemcitabine
zu 5,5%
Mitomycin
zu 5,5%
Bei allen zeigte sich ein weiterer Fortschritt der Erkrankung durch lokoregionäre
Rezidive
oder Metastasierungen.
Einige
Patienten
entzogen
sich
der
konsequenten Nachuntersuchung (spätestens alle drei Monate) oder waren in
der Medikamenteneinnahme unzuverlässig. In solchen Fällen wurden die
Patienten nicht mit in die Studie aufgenommen, so dass insgesamt 34 Patienten
übrig blieben. Erst dann wurden die Akten weitergehend bearbeitet, um keine
vorselektierten Patienten-Gruppen zu bekommen.
Nun wurden die Patienten entsprechend einer Tabelle mit verschiedenen
Parametern nachuntersucht und zum Vergleich gegenübergestellt (Tabelle
siehe Anhang). Anschließend wurden die Patienten gemäß der Arbeiten von
van Cutsem [78] und Wagstaff [86] in Wirkungsgruppen zusammengestellt, die
den klinischen Verlauf beschrieben (SD, PR,PD).
Die Dauer der Behandlung mit Xeloda als Monotherapie entspricht der positiven
Wirkung der Therapie, die anhand des klinischen Befundes und des
laborchemischen Befundes (Tumormarker) kontrolliert wurde.
- 20 -
Wenn die Wirkung nachließ, wurde auf eine Kombination z.B. mit Oxaliplatin
oder auf eine andere Therapie umgestellt. Patienten, die Unverträglichkeiten
zeigten, die nicht durch leichte Dosismodulation gebessert werden konnten,
oder Patienten, die aus persönlichen Gründen die Therapie vorzeitig
abbrachen, wurden mit den Patienten zusammengefasst, die unter der
Monotherapie eine Progression der Krankheit zeigten. Diese Gruppe wurde als
PD (progressive disease) bezeichnet.
Die Patienten, die während der Monotherapie einen gleich bleibenden
Krankheitsverlauf zeigten, wurden zu SD (stable disease) gezählt.
Patienten, bei denen eine partielle Remission beobachtet werden konnte,
wurden als PR (partial remission) bezeichnet.
Es wurden nun die Gruppen absolut und in Prozent nach klinischer Wirkung
verglichen.
Nebenwirkungen der Therapie mit Capecitabin, wie z.B. eine palmare-plantare
Erythrodysästhesie,
rechtzeitigem
auch
Erkennen
Hand-Fuß-Syndrom
durch
Therapiepausen,
genannt,
wurden
bei
Dosisreduktionen
und
entsprechende Patientenaufklärung kontrolliert. So wurden die Dosierungen
individuell
modifiziert
und
damit
gewährleistet,
dass
der
Patient
die
Chemotherapie vollständig erhält und auf diese Weise ein maximaler
Behandlungserfolg erreicht werden konnte. Die Therapie wurde nie länger als
zwei Wochen pausiert und nach Abklingen der Symptome mit reduzierter Dosis
weiterbehandelt.
Als supportive Maßnahme (Antidot) verwendeten die Patienten eine 10%ige
Uridin-Salbe für Hand- und Fußflächen.
- 21 -
3. ERGEBNISSE
Es wurden alle Patienten nachuntersucht, die seit 1999 mit Capecitabin
(Xeloda®) bei Karzinomen im Kopf-Hals-Bereich behandelt wurden. In die
Studie wurden dann die Patienten eingeschlossen, die als Monotherapie mit
Capecitabin behandelt und lückenlos, d.h. spätestens alle 3 Monate,
nachuntersucht worden waren.
Alle Patienten wiesen wenigstens ein Karzinom im Kopf-Hals-Bereich auf. Von
den 34 Patienten besaßen 26 nur einen Tumor, während 8 Patienten eine
Kombination von zwei bis vier Tumoren gleichzeitig hatten
Die Diagnosen waren:
6
Oropharynx-Ca
5
Hypopharynx-Ca
4
Mundboden-Ca
2
Epipharynx-Ca
2
Tonsillen-Ca
2
Larynx-Ca
2
Adenoidzystisches Ca der Gl.Parotis
1
Parotis-Ca
1
Malignes pleomorphes Adenom der Gl. Submandibularis
1
Sinus piriformis-Ca
-Epiglottis-Ca + Zungengrund-Ca
-Zungengrund-Ca + Ösophagus-Ca
-Stimmband-Ca + Tonsillen-Ca
-Schilddrüsen-Ca + Parotis-Ca
-Mundboden-Ca + Oropharynx-Ca
-Tonsillen-Ca + Oropharynx-Ca + Larynx-Ca + Bronchial-Ca
-Oropharynx-Ca + Epipharynx-Ca + Gaumen-Ca + Zungengrund-Ca
-Zungengrund-Ca + Oro-, Hypo- und Laryx-Ca
- 22 -
Alle Patienten waren im Stadium eines lokoregionären Rezidivs oder im
Stadium der Metastasierung. Alle
Patienten waren nicht mehr in einer
kurativen, sondern in einer palliativ ausgelegten Therapie eingebunden.
Insgesamt sind 34 Patienten in die Studie mit aufgenommen worden. Darunter
befanden sich 4 Frauen mit 12% und 30 Männer, die einen Anteil von 88%
ausmachten.
Das Durchschnittsalter zu Beginn der Behandlung mit Xeloda betrug 62,2
Jahre, wobei der Jüngste 43 Jahre und die beiden Ältesten 80 Jahre alt waren.
(s. Abb. 1)
Es zeigte sich keinerlei Altersabhängigkeit in Bezug auf das Ansprechen der
Therapie mit Capecitabin.
Ebenso war die Verträglichkeit der Therapie altersunabhängig. Ein Unterschied
zwischen den Geschlechtern konnte nicht aufgezeigt werden.
Pat.-Alter bei Th.-Beginn
( Ø = 62,2 Jahre )
90
80
70
Alter in Jahren
60
50
40
30
20
10
0
1
2
3
4
5
6
7
8
9
10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34
Xeloda-Patienten
Frauen
Männer
Abb 1: Dargestellt sind die Alters- und Geschlechtsverteilung der mit Capecitabin behandelten
Patienten zu Therapiebeginn. Durchschnittlicher Therapiebeginn.
- 23 -
Die untersuchten Patienten ließen sich nach den Arbeiten von Van Cutsem [78]
und Wagstaff [86] in 4 Gruppen einteilen:
Stable Disease
(SD)
Partial Remission
(PR)
Progressive Disease
(PD)
Mixed Response
Dabei ist als Positivgruppe stable disease (SD) und partial remission (PR) und
als Negativgruppe progressive disease (PD) und Mixed response anzusehen.
Zu der Gruppe PD zählen sowohl Patienten, die nicht auf die Therapie
ansprachen, als auch die Patienten, die frühzeitig die Therapie abbrachen.
klin. Wirkung
Mixed-Resp.
PD
PR
SD
0
2
4
6
8
10
12
14
16
18
20
Abb 2: Dargestellt wird die absolute Anzahl der Patienten in den verschiedenen Gruppen der
klinischen Wirkung auf Capecitabin.
Von den 34 Patienten zeigten 24 Patienten eine positive Antwort auf die
Therapie mit Xeloda. Das macht 70,5% der gesamten untersuchten Patienten
- 24 -
aus. Davon entfielen auf die Gruppe mit SD 18 Patienten (52,9%) und 6
Patienten wiesen sogar eine partial remission (PR) auf. Dies entspricht 17,6%
aller Patienten in der Studie, die eine partielle Befundbesserung durch die
Capecitabin-Therapie erfahren haben. (s. Abb. 3)
Diese Ergebnisse beziehen sich auf einen Mindestzeitraum von 3 Monaten
nach Einnahme.
klin. Wirkung in %
Mixed-Resp.
PD
PR
SD
0,0
10,0
20,0
30,0
40,0
50,0
60,0
%
Abb 3: Dargestellt wird die klinische Wirkung von Capecitabin in den verschiedenen Gruppen in
% auf die Gesamtpatientenzahl.
Immer noch 44,1%, nämlich 15 Patienten, zeigten bei einem längeren
Beobachtungszeitraum
von
mindestens
6
Monaten
einen
positiven
Therapieverlauf. (s. Abb. 4)
Elf Patienten zeigten über 6 Monate ein stable disease (SD), dies entspricht
32,4%. Vier Patienten hatten über 6 Monate eine partielle Befundverbesserung
(PR), das macht 11,8%. Für den Zeitraum von 9 Monaten zeigten noch 11
- 25 -
Patienten einen stabilen Verlauf. Dies sind 32,4%. Für 12 Monate und länger
waren es noch 5 Patienten (14,7%).
Patient 29 zeigte einen extrem langen SD-Verlauf von über 23 Monaten.
Als andere Ausnahme ist Patient Nummer 9 anzusehen, der nach 2 Monaten
SD einen tendenziellen Tumorprogress aufwies und bei dem daraufhin die
Therapie modifiziert wurde.
Dauer der Xeloda-Therapie für Pat. mit SD oder PD
24
21
18
Monate
15
12
9
6
3
0
1
2
3
4
5
6
7
8
9
10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34
Patienten in Xeloda-Behandlung
Abb 4: Aufgeführt ist die Behandlungsdauer mit Capecitabin für die einzelnen Patienten - die
klinische Wirkung entspricht auch der mittleren Behandlungsdauer.
Die Patienten mit negativer Antwort auf die Xeloda -Therapie waren insgesamt
10 Patienten entsprechend 29,4%. (s. Abb. 3) Dadurch dass sie keine Wirkung
zeigten oder Nebenwirkungen auftraten, die zum Abbruch zwangen, war die
Behandlungsdauer in der Regel nur ≤ 3 Monate. (s. Abb 4)
Ein Patient zeigte eine gemischte Therapieantwort (mixed response). Dies
äußerte sich, indem die lokalen Halsschwellungen und die Tumormarker
rückläufig waren, jedoch zeitgleich ein Tumorprogress enoral feststellbar war.
- 26 -
Aufgrund der Tumorprogression wurde dieser Patient mit Mixed response in die
Gruppe des progressive disease (PD) eingerechnet. (s. Abb. 3)
Die mittlere Therapiedauer mit Capecitabin betrug 6,6 Monate. Für die
Patienten mit positivem Therapieansprechen betrug die mittlere Therapiedauer
8,5 Monate. (s. Abb. 4)
3.1 Nebenwirkungen
Von den 34 Patienten hatten 12 Patienten (35,3%) klinisch bedeutsame
Nebenwirkungen in unterschiedlichen Schweregraden nach WHO. (s. Abb. 5)
Nebenwirkungen aller Schweregrade nach WHO
Polyneuropathie
Asthma
Thrombozytopenie
Zytopenie
Thorakales Engegefühl
Soor
Mukositis
Übelkeit
Schwäche
Appetitlosigkeit
Hand-Fuß-Syndrom
0
1
2
3
4
5
6
7
Anzahl
Abb 5: Dargestellt wird die Anzahl der Patienten mit entsprechender Nebenwirkung (alle
Schweregrade WHO). 12 Patienten zeigten nennenswerte Nebenwirkungen auf die Behandlung
mit Capecitabin.
- 27 -
Meist traten die Nebenwirkungen in Kombination auf, wobei das Hand-FußSyndrom mit Abstand am häufigsten vorkam (18%). Sechs Patienten von den
12 Patienten zeigten diese für Xeloda als typisch beschriebene Nebenwirkung.
Davon waren 2 Patienten so stark betroffen, dass die Therapie abgebrochen
werden musste. Diese waren in der Gruppe der PD. Die anderen 4 Patienten
zeigten ein leichtes bis mäßiges Hand-Fuß-Syndrom auf. Bei 2 Patienten kam
das Hand-Fuß-Syndrom nach 5 bzw. 9 Monaten. Diese Patienten gehörten in
die Gruppe der SD. Das Hand-Fuß-Syndrom konnte in der Regel leicht durch
eine kurze Behandlungspause (im Mittel 1 Woche) mit anschließender
Dosisreduktion (um 25%) gebessert werden.
Appetitlosigkeit trat in 9% der Fälle als Nebenwirkung auf. Von Übelkeit,
Schwäche und Mukositis waren 6% der Patienten betroffen.
Hämatologische Veränderungen traten nur bei einem Patienten in Form einer
geringgradigen Thrombozytopenie auf. (s. Abb. 5)
Die Dosis wurde individuell modifiziert und damit gewährleistet, dass jeder
Patient die notwendige Chemotherapie möglichst vollständig erhält und auf
diese Weise der Benefit der Therapie erreicht wurde. In manchen Fällen gab es
eine Unterbrechung der Therapie. Als supportive Maßnahme verwendeten die
Patienten eine Uridin (10%) Salbe für Hand- und Fußflächen.
- 28 -
4. Diskussion
Für die Studie wurden Patienten verwendet, die nach chirurgischer Intervention
und
Radiochemotherapie
wegen
Karzinomen
im
Kopf-Hals-Bereich
lokoregionäre Rezidive aufwiesen oder Fernmetastasen zeigten und einem
fortgeschrittenen, palliativen Tumorstadium entsprachen. Alle Patienten zeigten
vor Therapiebeginn eine deutliche Tumorprogression.
Die Studie ist retrospektiv anhand der Patientenakten der hämatoonkologischen
und radioonkologischen und mittherapierenden HNO-Abteilung klinisch als auch
bildgebend und laborchemisch ausgewertet worden. Es wurden alle Patienten
in
gleicher
Weise
mit
Xeloda
als
Monotherapie
behandelt.
Diese
Vorgehensweise wurde ebenso in den Studien von Wagstaff [86] mit MammaCa Patienten und von Van Cutsem [78] mit Kolorektalcarcinomen in gleicher
Weise angewandt [42]. Da alle Patienten in Tumorprogression waren, ist ein
stable disease SD bereits durch Aufhalten des Krankheitsfortschrittes ein
Erfolg und zeigt damit einen Wirkungsnachweis der Capecitabintherapie, dies
auch vor dem Hintergrund, dass die Wirkung der Chemotherpie innerhalb von 6
Wochen anschlägt [33,78]. Die partielle Remission wurde nur dann registriert,
wenn über mehrere Wochen eine wirkliche Verbesserung der Tumorparameter
(CEA, Tumorgrößenregression durch CT, Sonographie oder HNO-Befund)
vorlag. Ein subjektiv verbessertes Wohlbefinden der Patienten als alleiniges
Kriterium wurde nicht berücksichtigt.
Capecitabin wurde so lange als Monotherapie angewendet bis ein Fortschreiten
der Krankheit ( progressive disease) oder inakzeptable Nebenwirkungen, die
nicht durch Dosisreduktion gebessert werden konnten, auftraten. Gleiches
Vorgehen zeigte Venturini in seiner Studie von 2007 [79].
Das Männer–Frauen Verhältnis, welches sich in vielen Studien auf 4:1 verteilt,
ist in dieser Studie aufgrund der geringen Frauenanzahl (4; siehe Abb.1) nicht
gewahrt. Dies könnte daran liegen, dass die Patienten aus einem überwiegend
ländlichen Einzugsbereich stammen und der Nikotinabusus dort bei Frauen
traditionell geringer ausfiel.
- 29 -
In keiner der Studien mit Kolorektal-Ca wurde zwischen Männern und Frauen
bei der Therapie unterschieden. Dies ließ sich anhand unserer Ergebnisse auch
für die Kopf-Hals-Tumoren nachvollziehen, da keinerlei Unterschiede zu
erkennen waren. Auch in der Studie von Bentzen von 2006, der in seiner Studie
Capecitabin bei Patienten mit metastasierten Kopf-Hals-Tumoren angewendet
hatte,
werden
keine
geschlechterbezogenen
Angaben
gemacht
bzw.
Unterschiede aufgezeigt [5].
In dieser Studie konnte ein durchschnittliches Alter der Patienten bei
Therapiebeginn mit Capecitabin von 62,2 Jahren ermittelt werden (siehe
Abb.1). Die durchschnittliche Inzidenz für Mundboden-Ca
liegt bei 50-60
Jahren, die der Oropharynx-Ca bei 60-70 Jahren [65]. So entspricht auch das
Durchschnittsalter dieser Studie dem der genannten Inzidenzen.
Aufgrund der Studie von Miwa et al. [46] wurde gezeigt, dass die
Thymidinphosphorylase (TP)-Aktivität in menschlichen Tumorzellen bei soliden
Tumoren signifikant höher ist als im gesunden Gewebe des gleichen
Individuums. Interindividuell bestehen durchaus große Differenzen bezüglich
der TP-Aktivität [55]. Das Verhältnis von der TP-Aktivität gesunder und
tumuröser Zellen ist für die soliden Tumoren als signifikant unterschiedlich
bewiesen worden [42,46].
Bei Tumoren wie Mamma-Ca, Kolorektal-Ca,
Ösophagiale-Ca und orale Plattenepithel-Ca konnte eine extrem höhere TPAktivität in den Tumorzellen nachgewiesen werden [46]. Daher liegt der Schluß
nahe,
dass
Xeloda
als
Prodrug
für
die
Behandlung
der
soliden
Oropharyngealen Tumoren, wie in dieser Studie zusammengestellt, ebenso
vergleichbare Wirksamkeit zeigen konnte.
In dieser Studie konnte beobachtet werden, dass 18 von 34 Patienten (52,9%)
mit SD (stable disease) auf die Therapie reagierten. Damit zeigt sich ein sehr
vergleichbares Ergebnis zu den Studien von Van Cutsem [78], der bei
kontinuierlicher Xelodagabe als Monotherapie bei metastasierten KolorektalCarcinomen eine SD von 51% aufzeigen konnte. Das gleiche Ergebnis von
51% SD konnte die Studiengruppe von Wagstaff et al. für die Monotherapie von
Xeloda bei fortgeschritten Mamma-Cacinom aufzeigen [86].
- 30 -
Eine neue Studie von Van Cutsem von 2004 konnte ebenfalls eine stable
disease Rate unter Capecitabin Monotherapie von 48,3% nachweisen [77].
Ebenso konnte Venturini [79] eine stable disease Rate von 46,7% aufzeigen.
Beide oben genannten SD-Raten liegen im Vergleich zu vorliegender Studie
(52,9%) geringfügig darunter. Die Studie von Gelman aus dem Jahr 2006 [29]
konnte eine SD-Rate von 57-63% aufzeigen. In ihrer Studie wurden Patienten
mit Capecitabin als Monotherapie behandelt, die bereits mit Taxanen
vorbehandelt wurden [29]. Auch in dieser Studie erhielten die Patienten
Vorbehandlungen mit Taxanen. Die Vorbehandlung mit Taxanen könnte die
leichte Erhöhung unserer SD-Werte im Vergleich zu denen von Van Cutsem
[77] und Venturini [79] erklären.
Patienten mit PR (partial remission) waren in 17,6% der Fälle der vorliegenden
Studie vorhanden. Ein Patient konnte diese partielle Besserung 23 Monate
halten. (s. Abb. 4)
Van Cutsem zeigte 2004 bei Coloractalen-Ca eine Response von 25,7% auf
[77]. Gleiches zeigte Wagstaff für das Ansprechen auf fortgeschrittene MammaCarcinomen
mit 25% PR [86]. Während bei diesen Studien die overall
response nur im Schnitt für vier Monate anhielt, zeigten in dieser Studie die
Patienten im Durchschnitt für 10 Monate eine partielle Remission. Die Studie
von Findlay von 2008 konnte bei mit Taxanen vortherapierten Patienten in der
Capecitabin Monotherapie eine overall response von 22,4% aufzeigen [26]. In
der vorliegenden Studie sind Patienten ebenfalls mit Taxanen vorbehandelt
gewesen und wiesen eine overall response von 17,6% auf.
Die Gruppe der Progressive Disease (PD) ist mit 26,5% höher als es in der
Studie von Wagstaff für Brust-Carcinomen gezeigt werden konnte. (s. Abb. 3)
Bei ihm liegt die Rate bei 16%. Dies mag darin begründet sein, dass die
meisten Patienten auf Xeloda innerhalb der ersten 6 Wochen [10,12,42,78] der
Therapie ansprechen und in unserer Studie in der Regel die klinischen
Wiedervorstellungstermine nach 10 bis 12 Wochen erfolgten und dann, wenn
kein Ansprechen erfolgte, die Therapie von einer Monotherapie auf eine
- 31 -
Kombination oder ein anderes Medikament umgestellt wurde. Dadurch ist
keines der Gruppenmitglieder der PD-Gruppe, d.h. ohne Wirkung auf Xeloda,
länger als 12 Wochen mit Capecitabin als Monotherapie behandelt worden. Sie
wurden durchschnittlich insgesamt nur 6 Wochen (1,4 Monate) behandelt. (s.
Abb. 4) Eine individuelle Therapieumstellung erfolgte zum Wohle des Patienten
sehr schnell. Auch in der Studie von Venturini von 2007 wurde das orale
Capecitabin so
lange gegeben bis ein Fortschreiten der Krankheit
nachvollzogen werden konnte [79].
Bei den Vergleichsstudien wurde die Monotherapie bei Nichtansprechen
trotzdem länger weiter geführt [86].
In einer Studie von Bentzen von 2006 [5] , die 50 Patienten mit Tumoren im
Kopf-Hals-Bereich auf ihr Ansprechen von einer Kominationstherapie mit
Paclitaxel und Capecitabin untersuchte, wird eine Rate von Patienten mit
progressive disease von 24% angegeben. Dies entspricht sehr genau unserer
Rate von 26,5% für progressive disease. (s. Abb. 3) Allerdings zeigte sich
diese Rate in unserer Studie mit Capecitabin-Monotherapie in höherer Dosis
von 1250mg/m².
Desweiteren
wurden
Nebenwirkungen,
Patienten,
die
Hand-Fuß-Syndrom
ihre
WHO
Therapie
Grad
aufgrund
3-4
oder
von
Asthma,
abgebrochen haben, ebenfalls in die Gruppe der PD mit eingerechnet. Zwei
Patienten von den 9 Patienten in der PD-Gruppe zeigten eine echte
Unverträglichkeit mit starkem HFS (WHO 3-4) bei gleichzeitig schneller
Tumorprogression, so dass diese Patienten bereits nach 4 Wochen in der
Therapie umgestellt werden mussten.
Ein Patient zeigte eine deutliche Normalisierung der Tumormarker (CEA) mit
subjektiv
klinischer
Besserung
(Schwellungsrückgang
im
Bereich
der
Halsweichteile), in der gleichen Zeit jedoch eine leichte Größenzunahme des
Tumors im Mundboden, so dass eine klare Zuordnung nicht möglich war und er
daher als mixed response in der Studie ausgewiesen wurde. Diese Zuordnung
ist in den Vergleichsstudien nicht zu finden [78,86]. Es wurde dieser Patient
wegen des Tumorprogress in die Gruppe der negativen Responder PD
- 32 -
eingerechnet. Auch in den jüngsten Studien von Venturini 2007 [79] und Findlay
[26] von 2008 wurde ein mixed response nicht angesprochen.
Die Patienten dieser Studie haben die Therapie mit Xeloda gut toleriert. Es
traten in der Studie keine therapiebedingten Todesfälle auf. Zwei Patienten
(5,9%) mussten die Therapie wegen Unverträglichkeit vorzeitig abbrechen.
Die Nebenwirkungsrate betrug für die Patienten der Studie 35,3%. (s. Abb. 5)
3 Patienten zeigten die WHO Grade 3 bis 4. Dies sind 8% und damit gut
vergleichbar mit der Studie von Venturini [79]. Wie in dieser und anderen
Studien vergleichbar [22] zeigte sich das Hand-Fuß-Syndrom (HFS) als die
häufigste Komplikation. Von allen Patienten hatten 18% das HFS als
Nebenwirkung mit unterschiedlicher Auswirkung. (s. Abb. 5)
Ershler konnte
2006 zeigen, dass das HFS durchschnittlich bei 13% der Patienten mit
Capecitabin-Therapie auftrat. Allerdings weisen die verschiedenen Studien eine
enorme Varianz von 0-42% auf [24]. In vorliegender Studie beträgt der
eigentliche
Anteil
von
Patienten
mit
HFS
an
allen
Patienten,
die
Nebenwirkungen zeigten, jedoch 50%. Dies ist durchaus vergleichbar mit der
Studie von Cathy Eng [20], die in 53% aller Fälle das HFS aufzeigen konnte.
Allerdings ist bei ihr der Ausprägungsgrad 3 mit 17% ausgegeben, während in
unserer Studie nur 5,9% das Stadium 3 zeigten. Die anderen Nebenwirkungen
wie Thrombozytopenie, Soor, Mukositis, Übelkeit und Fatigue sind nur gering
ausgeprägt und selten aufgetreten. Meist waren die Nebenwirkungen auch mit
anderen kombiniert (s. Abb 5).
Wenn Nebenwirkungen auftraten, konnten diese durch kurzes Pausieren und
leichte Dosisreduktion gebessert werden. In der Regel wurde die Dosis auf
1000mg/m² reduziert oder für 1 Woche pausiert. Unter dieser Dosisreduktion
besserten sich die Nebenwirkungen schnell und zuverlässig. Ershler konnte in
seiner Studie nachweisen, dass bei bis zu 50% der Patienten alleine eine
Dosisreduktion um 25% eine Besserung der gezeigten Nebenwirkungen zur
Folge hatte [24]. Dabei scheint vor allem das HFS dosisassoziiert. Ershler
verringerte die Rate an HFS von 20% auf 2% durch Reduktion der Tagesdosis
- 33 -
von 2x 1250 mg/ m² auf 2x 1000mg/m². Auch Bajetta et al. [3] konnte gleiche
Nebenwirkungsraten von 2% HFS aufzeigen bei einer Dosierung von 2x
1000mg/m². Die Ergebnisse waren jedoch mit denen von van Cutsem [77]
vergleichbar, obwohl dieser 2x 1250mg/m² pro Tag verabreicht hatte.
Zwei Drittel der Patienten (64,7%) zeigten keinerlei auf die Therapie
zurückzuführenden Nebenwirkungen, so dass man von einer gut tolerierten
Monotherapie mit Xeloda sprechen darf. (s. Abb. 5)
Das Ergebnis einer Studie ergab, dass die Patienten zu 89% die orale Therapie
der i. v. Gabe des Zytostatikums vorziehen [41]. Eine andere Studie, die die
Therapieerfolge in privater häuslicher Umgebung oder im Krankenhaus
vergleicht, besagt, dass sich die Lebensqualität bei der Therapie in gewohnter
häuslicher Atmosphäre verbesserte [51]. In einer nächsten Studie bekamen
Patienten nacheinander entweder erst oral und danach i.v. oder umgekehrt 5FU verabreicht [8]. Danach ließ man die Patienten selbst entscheiden, ob sie
die Therapie oral oder i.v. weiterführen wollten. Die meisten Patienten (84%)
entschieden sich für die orale Form der Therapie. Die wichtigsten Gründe dafür
waren die Tablettenform des Zytostatikums, die Möglichkeit der häuslichen
Therapiedurchführung und ein von der Therapie unabhängigen normalen Alltag
[8]. Die Studie von Topham et al. [75] kam zum Ergebnis, dass 87% der
Patienten einen kurzen Krankenhausbesuch und kurze Behandlungsdauer wie
eine 15-Minuten Infusion alle 3 Wochen bevorzugen. Der Großteil der
Probanden
entscheidet
sich
sogar
für
die
orale
Therapieform
ohne
Berücksichtigung der Wirksamkeit [8,41].
Die Patienten empfanden die Chemotherapie als gut tolerabel, da sie zum
einen oral verabreicht wurde und zum anderen zu Hause durchführbar war.
Ebenso war die Akzeptanz der Therapie durch die Selbstverantwortlichkeit im
Alltag deutlich höher als eine stationär durchgeführte Therapie. Diese
Zusammenhänge sind in vielen Studien belegt [5,35,45,68]. Außerdem ist die
Therapie sehr kosteneffektiv. Dies ist auch in den Studien von Fumoleau von
2003 [28] und Gelman von 2006 [29] in gleicher Weise beschrieben.
- 34 -
Diese Studie konnte ähnliche Wirksamkeit bei Kopf-Hals-Tumoren aufzeigen,
wie sie in vielen Studien bei der Therapie von Colorectal-Ca und Mamma-Ca
bewiesen wurden. Die Studie gibt daher Anlaß, für Kopf-Hals-Tumoren im
palliativen Stadium eine Capecitabin-Monotherapie durchaus in gleicher Weise
durchzuführen, wie bereits bei Mamma-Ca und Kolorektalen-Ca anerkannt.
Weitere Studien wären wünschenswert, um die Ergebnisse zu bestätigen und
die schwierige palliative Behandlung dieser Tumore zu optimieren.
- 35 -
5. Zusammenfassung
Die Studie konnte zeigen, dass die Monotherapie mit Xeloda bei Patienten mit
palliativen Kopf-Hals-Tumoren ähnlich gute Ergebnisse wie vergleichbare
Studien für Mammakarzinome und Kolorektalkarzinome zeigten. Diese
Therapien sind bereits anerkannt und entsprechend ist die CapecitabinTherapie zugelassen. Über 70% der Patienten zeigten unter Behandlung einen
Stillstand der Tumorprogression und teilweise sogar partielle Remissionen für
mindestens drei Monate. 44,1% konnten auch mehr als 6 Monate diese
Verbesserung aufzeigen.
Die Behandlung zeigt verhältnismäßig wenige Nebenwirkungen, die auch meist
durch leicht zu modifizierende Capecitabindosen gebessert werden konnten.
Die hier vorgelegten Daten bei der Behandlung von Kopf-Hals-Tumoren mit
Capecitabin entsprechen weitgehend den Daten der Vergleichsstudien, die die
Wirksamkeit der Therapie mit Capecitabin bei Mamma-Ca oder Kolon-Ca
aufzeigen konnten.
Die Ergebnisse bei der Behandlung von Kopf-Hals-Tumoren mit Capecitabin
zeigen die Wirksamkeit des Medikamentes Xeloda auch bei diesen Diagnosen.
Die Beobachtungen und Ergebnisse sollten Anlass zu einer großen,
kontrollierten Studie sein, die den Stellenwert der Substanz bei der Therapie
von Patienten eindeutig beweist.
Wahrscheinlich ist die zur Zeit immer noch diffizile palliative Behandlung von
Patienten mit Kopf-Hals-Tumoren zukünftig leichter und für die Patienten besser
verträglich mit Capecitabin durchzuführen.
- 36 -
6. Literaturverzeichnis
1.
Acheson E, Cowdell R, Jolles B. (1970) Nasal Cancer in the
Northhamtonshire bood and shoe industrsy. Br Med J, 1:385-393.
2.
Al-Sarraf M, Le Blanc M, Giri PG, Fu K, Cooper J, Vuong T, Forastiere A,
Adams G, Sakr W, Schuller D, Ensley J. (1998) Chemotherapy versus
radiotherapy in patients with advanced nasopharyngeal cancer: Phase
III randomized Intergroup study 0099. J Clin Oncol, 16:1310-1317.
3.
Bajetta E, Procopio G, Celio L et al. (2005) Safety and efficiacy of two
different doses of Capecitabine in the treatment of advanced breast
cancer in older women. J Clin Oncol, 23;2155-2161.
4.
Benson AB III. (1998) Therapy for advanced colorectal cancer. Semin
Oncol, 25(5suppl 11):2-11.
5.
Bentzen JD, Hansen HS. (2006) Phase II analysis of placitaxel and
Capecitabine in the treatment of recurrent or disseminated squamous
cell carcinoma of the head and neck region. Wiley Interscience Head
and Neck, Volume 29, Issue 1, Pages 47-51.
6.
Black R, Bray F, Ferlay J, Parkin D. (1997) Cancer incidence and motality
in the European Union. Cancer registry data and estimates of national
incidence for 1990. Eur J Cancer, 33:1075-1107.
7.
Blum JL. (2001) The Role of Capecitabine, an Oral, Enzymatically
Activated Fluoropyrimidine, in the Treatment of Metastatic Breast
Cancer. The Oncologist, Volume 6, Number 1
- 37 -
8.
Borner M, Schneithauer W, Twelves C et al. (2001) Answering
patients´needs: oral alternatives to intravenous therapy. Oncologist.,
6(suppl 4):12-16.
9.
Borner M, Schöffski P, de Wit R et al. (2002) Patient prereference and
pharmacokinetics
of
oral
modulated
UFT
versus
intravenous
fluorouracil and leucovorin: a randomised crossover trial in advanced
colorectal cancer. Eur J Cancer, 38:349-358.
10. Budman DR, Meropol NJ, Reigner B et al. (1998) Preliminary studies of a
novel oral fluoropyrimidine carbamate: capecitabine. J Clin Oncol,
16:1795-802.
11. Buroker TR, O´Connell MJ, Wieand HS et al. (1994) Randomized
comparison of two schedules of fluorouracil and leucovorin in the
treatment of advanced colorectal cancer. J Clin Oncol, 12:14-20.
12. Cassidy J, Dirix L, Bissett D et al. (1998) A phase I study of capecitabine in
combination with oral leukovorin in patients with intractable solid
tumors. Clin Cancer Res, 4:2755-61.
13. Cassidy J, Tabernero J, Twelves C et al. (2004) Capecitabine plus
oxaliplatin first-line therapy for patients with metastatic colorectal
cancer. J Clin Onol, 22:2084-2091.
14. Chan A, Teo P, Ngan R, Leung T, Lau W, Zee B, Leung S, Cheung F, Yeo
W, Yiu H, Chiu K, Chan D, Mok T, Yuen K, Kwan W, Choi P, Johnson
P. (2000) A phase III randomized trial comparing concurrent
chemotherapy-radiotherapy with radiotherapy alone in locoregionally
advanced nasopharyngeal carcinoma. Proc Am Soc Clin Oncol,
19:415a {abstract #1637}.
- 38 -
15. Colvevas AD, Norris CM, Tishler RB et al. (1999) Phase II trial of
docetaxel, cisplatin, fluorouracil and leucoverin as induction for
squamous cell carcinoma of the head and neck cancer. J Clin Oncol,
17:3503-3511.
16. Colvevas A, Tishler R, Fried M, Read R, DeFusco P, Norris C, Posner M.
(2000) A Phase I/II Study of Outpatient Docetaxel (Taxotere), Cisplatin,
5-FU and Leucovorin (OP-TPFL) as Induction Chemotherapy for
Patients with Squamous Cell Carcinoma of the Head and Neck
(SCCHN). Proc Am Soc Clin Oncol, 19:420a{abstract#1664}.
17. Dadian G, Riches PG, Henderson DC et al. (1993) Immun changes in
peripheral blood resulting from locally directed interleukin-2-therapy in
squamous cell carcinoma of the head and neck. Eur J Canc B Oral,
29b:29-34.
18. Danenberg K, Metzger R, Groshen S et al. (1997) Thymidylate synthase
(TP) and thymidine phosphorylase (TP) are prognostic indicators of
survival for colorectal cancer. Proc AM Soc Clin Oncol, 16:257a
(Abstract 914).
19. Dische S. (1994) Radiotherapy - new fractionation schemes. Semin Onocl,
21:304-310.
20. Eckardt A, Barth E , Janssen S, Wegener G. (2004) Tumorrezidive im
Mund-Kiefer-Gesichtsbereich. Springer Berlin/Heidelberg, Heft Volume
8, Number 4.
21. El-Sayed S, Nelson N. (1996) Adjuvant and adjunctive chemotherapy in
the management of squamous cell carcinoma of head and neck region:
A meta-analysis of prospective and randomized trials. J Clin Oncol,
14:838-847.
- 39 -
22. Eng
C,
Abbruzze
J.
®
Capecitabine(Xeloda )
(2003) The
Efficacy and
Monotherapie.
The
Expectations
American
Journal
of
of
Oncology Review, Vol 2, No 5 Supplement 3.
23. Endo M, Shinbori N, Fukase Y
phosphorylase
expression
et al. (1999) Induction of thymidine
and
enhancement
of
efficacy
of
Capecitabine or 5´-deoxy-5-flourouridine by cyclophosphamide in
mammary tumor models. Int J Cancer, 83:127-34.
24.
Ershler WB. (2006) Capecitabine Monotherapy: Safe and Effective
Treatment for Metastatic Breast Cancer. The Oncologist, 11:325-335.
25. Fandi A, Altun M, Azli N, Armund JP, Cvitkiovic E. (1994) Nasophatryngeal
cancer: epidemiology, staging, treatment. Semin Oncol, 21:382-397.
26. Findlay M, Minckwitz v G, Wardley A. (2008) Effective oral chemotherapy
for breast cancer: pillars of strength. Annals of Oncology, Volume 19,
No2:212-222.
27. Forastiere AA. (1991) Randomized trials of induction chemotherapy. A
critical review. Hematol Oncol Clin North Am, 5:725-736.
28. Fumoleau P, Largillier R, Clippe C et al. (2004) Multicentre, phase II study
evaluating capecitabine monotherapy in
patients anthracycline- and
taxane-pretreated metastatic breast cancer. Eur J Cancer, 40:536-542.
29. Gelmon K, Chan A, Harbeck N. (2006) The Role of Capecitabine in FirstLine Treatment for Patients with Metastatic Breast Cancer. The
Oncologist, 11:42-51.
- 40 -
30. Frings
S.
(1998)
Capecitabine
-
a
novel
oral
tumor-activated
fluoropyrimidine. Onkologie, 21:451-458.
31. Gieschke R, Reigner B, Blesch KS, Steimer JL. (2002) Population
pharmacogenetic analysis of the major metabolites of capecitabine. J
Pharmacokinet Pharmacodyn, 29:25-47.
32. Grem JL. 5-fluoropyrimidines. In: Chabner BA, Longo DL, editors. (1996)
Cancer Chemotherapy and Biotherapy: Principles and Practice 2nd ed.
Philadelphia: Lippincott-Raven, pp. 149-211.
33. Höhler T, Rödel C, Hölscher AH, Al-Batran S-E. (2007) Neoadjuvante und
palliative Therapie des Ösophagus- und Magenkarzinoms. Onkologie,
30(suppl 2):23-26.
34. Imazano Y, Takebayashi Y, Nishiyama K
et al. (1997) Correlation
between thymidine phosphorylase expression and prognosis in human
renal cell carcinoma. J Clin Oncol, 15:2570-8.
35. International Nasopharynx Cancer Study Group. (1996) VUMCA 1 trial:
Preliminary results of a randomized trial comparing neoadjuvant
chemotherapy (cisplatin, epirubicin, bleomycin) plus radiotherapy alone
in stage IV (≥N2, M0) undifferentiated nasopharyngeal carcinoma: a
positive effect on progression-free survival. Int J Radiat Oncol Biol
Phys, 35:463-469.
36. Ishikawa T, Fukase Y, Yamamoto T et al. (1998) Antitumor activities of a
novel fluoropyrimidine, N4-pentoxycarbonyl-5´-deoxy-5-fluorocytidine
(capecitabine). Biol Pharm Bull, 21:713-717.
- 41 -
37. Ishikawa T, Sekiguchi F, Fukase Y
et al. (1998) Positive correlation
between the efficacy of capecitabine and doxifluridine and the ratio of
thymidine phosphorylase to dihydropyrimidine dehydrogenase activities
in human cancer xenografts. Cancer Res., 58:685-690.
38. Ishikawa T, Utoh M, Sawada N et al. (1998) Tumor selective delivery of 5fluorouracil by Capecitabine, a new fluoropyrimidine carbamate, in
human cancer xenografts. Biochem Pharmaco.l, 55:1091-1097.
39. Ishitsuka H. (2000) Capecitabine: preclinical pharmacology studies. Invest
New Drugs, 18:343-54.
40. Kitazono M, Takebayashi Y, Ishitsuka K et al. (1998) Prevention of
hypoxia-induced
apoptosis
by
angiogenic
factor
thymidine
phosphorylase. Biochem Biophys Res Commun, 253:797-803.
41. Liu G, Franssen E, Fitch MI, et al. (1997) Patient preferences for oral
versus intravenous palliative chemotherapy. J Clin Oncol., 15:110-115.
42. Mackean M, Planting a, Twelves C
et al. (1998) Phase I and
pharmacologic study of intermittent twice-daily oral therapy wit
capecitabine in patients with advanced and/or metastatic cancer. J Clin
Oncol, 16:2977-85.
43. Maeda K, Cung Y-S, Ogawa Y et al. (1996) Thymidine phosphorylase/
platelet-derived endothelial cell growth factor expression associated
with hepatic metastasis in gastric carcinoma. Br J Cancer, 73:884-8.
44. Maier H, Dietz A, Gewelke U, Heller WD. (1992) Berufliche Exposition
gegenüber Schadstoffen und Krebsrisiko im Bereich der Mundhöhle,
Oropharynx, Hypopharynx, Larynx. Eine Fall-Kontrollstudie. Laryngo
Rhino Otol, 70:93-98.
- 42 -
45. Matsuura T, Kuratate I, Teramachi K, Osaki Y, Fukuda H. (1999)
Thymidine phosphorylase expression is associated with both increase
intratumoral microvessels and decrease of apoptosis in human
colorectal carcinomas. Cancer Res, 59:5037-5040.
46. Miwa M, Ura M, Nishida M et al. (1998) Design of a novel oral
fluoropyrimidin
carbamate,
Capecitabine,
which
generates
5-
fluorouracil selectively in tumors by enzymes concentrated in human
liver and cancer tissue. Eur J Cancer, 34:1274-1281.
47. Mizutani Y, Okada Y, Yoshida O. (1997) Expression of platelet-derived
endothelial cell growth factor in bladder carcinoma. Cancer, 79:1190-4.
48. Moghaddam A, Zhang H-T, Fan T-PD
et al. (1995) Thymidine
phosphorylase is angiogenic and promotes tumor growth. Proc Natl
Acad Sci USA, 92:998-1002.
49. Munro AJ. (1995) An overview of randomised controlled trials of adjuvant
chemotherapy in head and neck cancer. Br J Cancer, 71:83-91.
50. Parker S, Tong T, Bolden S, Wingo P. (1997) Cancer statistics, 1997. CA,
Cancer J Clin, 47:5-27.
51. Payne SA. (1992) A study of quality of life in cancer patients receiving
palliative chemotherapy. Soc Sci Med., 35:1505-1509.
52. Peters LJ, Ang KK, Thames HD Jr. (1988) Accelerated fractionation in the
radiation treatment of head and neck cancer. A critical comparison of
different strategies. Acta Oncol, 27:185-194.
- 43 -
53. Pignon JP, Bourhis J, Domenge C, Designé L on behalf of the MACH-NC
Collaborative Group. (2000) Chemotherapy added to locoregional
treatment for head and neck squamous-cell carcinoma: three metaanalysis of updated individual data. Lancet, 355:949-955.
54. Pinedo
HM,
Peters
GF.
(1988)
Fluorouacil:
biochemistry
and
pharmacology. J Clin Oncol., 6:1653-1664.
55.
Reichardt P. (2002) Hand-Fuß-Syndrom. Beilage in „Der Onkologe“ Band
8,Heft 5 Springer Verlag :4
56. Reynolds K, Farzaneh F, Collins WP et al. (1994) Association of ovarian
malignancy with expression of platelet-derived endothelial cell growth
factor. J Natl Cancer Inst, 86:1234-8.
57. Robbins KT, Medina JE, Wolfe GT, Levine PA, Sessions RB, Pruet CW.
(1991) Standardizing neck dissection terminology. Official report of the
Academy´s Committee for Head and Neck Surgery and Oncology. Arch
Otolaryngol Head Neck Surg, 117:601-605.
58. Sakaguchi H, Hirose R, Ichigo S, Tamaya T. (1999) Expression of plateletderived endothelial growth factor (PD-ECGF) and its mRNA in uterine
cervical cancer. Br J Cancer, 79:1249-54.
59. Sawada N, Fujimoto-Ouchi K, Ishikawa T, Tanaka Y, Ishitsuka H. (2002)
Antitumor activity of combination therapy with capecitabine plus
vironelbine, and capecitabine plus gemcitabine in human tumor
xenografts models. Proc Am Assoc Cancer Res., (Abstract 5388;
poster update).
- 44 -
60. Sawada N, Ishikawa T, Fukase Y, Nishida M, Yoshikubo T, Ishitsuka H.
(1998) Induction of thymidine phosphorylase activity and enhancement
of capecitabine efficacy by Taxol/Taxotere in human cancer xenografts.
Clin Cancer Res., 4:1013-19.
61. Sawada N, Ishikawa T, Sekiguchi F, Tanaka Y, Ishitsuka H. (1999) X-ray
irradiation induces thymidine phosphorylase and enhances the efficacy
of Capecitabine (Xeloda®) in human cancer xenografts. Clin Cancer
Res., 5:2948-53.
62. Schilsky RL, Bertucci D, Vogelzang NJ, Kindler HL, Ratain MJ. (2002)
Doseescalating study of capecitabine plus gemcitabine combination
therapy in patients with advanced cancer. J Clin Oncol, 20:582-587.
63. Sloan D, Goepfert H. (1991) Conventional therapy of head and neck
cancer. Hematol Oncol Clin North Am, 5:601-625.
64. Schüller J, Cassidy J, Dumont E et al. (2000) Preferential activation of
Capecitabine in tumor following oral abministration to colorectal cancer
patients. Cancer Chemother Pharmacol., 45:292-297.
65. Schmoll HJ ,Höffken K, Possinger K. (2006) Kompendium Internistische
Onkologie 4.Auflage Springer, : 3342-3381
66. Spiro RH, Strong EW, Shah JP. (1994) Classification of neck dissection:
Variations on a new theme. Am J Surg, 168:415-418.
67. Stupp R, Vokes EE. (1995) 5-FU plus radiation for head and neck cancer.
J Infus Chemother, 5:55-60.
68. Stupp R, Vokes EE. (1995) Progress in treatment of head and neck
cancer. Part1: Chemotherapie.Strahlenter Onkol, 171:12-17.
- 45 -
69. Stupp R, Vokes EE. (1995) Progress in treatment of head and neck
cancer. Part2: Chemoradiotherapie. Strahlenter Onkol, 171:140-148.
70. Takebayashi Y, Akiyama S, Akiba S
prognostic
significance
of
et al. (1996) Clinicopathological
an
angionetic
factor,
thymidine
phosphorylase, in human colorectal carcinoma. J Natl Cancer Inst,
88:1110-17.
71. Takebayashi Y, Miyadera K, Akiyama S
et al. (1996) Expressions of
thymidine phosphorylase in human gastric carcinoma. Jpn J Cancer
Res., 87:288-95.
72. Takebayashi Y, Yamada K, Miyadera K
et al. (1996) The activity ad
expression of thymidine phosphorylase in human solid tumors. Eur J
Cancer, 32A:1227-32.
73. Thuro HC. (2001) Capecitabin-first-line-Therapie bei Patienten mit
kolorektalen Karzinomen. Beilage in „Der Onkologe“, Band 7, Heft 3.
74. Toi M, Ohashi T, Takatsuka Y
adjuvant 5´-
et al. (1997)
Selective effects of
deoxy-5-flourouridine (5´-DFUR) treatment for thymidine
phosphorylase positive tumors in primary breast cancer. Proc AM Soc
Clin Oncol, 16:136a (Abstract 481).
75. Topham C, Moore J. (1997) Patient preferences for chemotherapy
schedules used in the treatment of advanced colorectal cancer- a pilot
study. Eur J Cancer Care, 6:291-294.
76. Vader J, Minder C. (1987) Die Sterblichkeit an Krebsen der Nasen- und
Nasennebenhöhlen ei Schweizer Schreinern. Schweiz Med Wschr,
117:481-486.
- 46 -
77.
Van Cutsem E, Hoff PM, Harper P et al. (2004) Oral capecitabine vs
intravenous 5-fluorouracil and leucovorin: integrated efficacy data and
novel analysis from two large, randomised, phase III trials. British J
Can, 90:1190-1197.
78. Van Cutsem E, Findlay M, Osterwalder B et al. (2000) Capecitabine, an
oral flouropyrimidine carbamate with substantial activity in advanced
colorectal cancer: results of randomized phase II study. J Clin Onol,
18:1337-45.
79.
Venturini M, Paridaens R, Rossner D et al. (2007) An Open-Label,
Multicenter Study of Outpatient Capecitabine Monotherapy in 631
Patients with Pretreated Advanced Breast Cancer. Oncology, 72:51-57.
80. Verweij J. (1999) Rational design of new tumoractivatedTM cytotoxic
agents. Oncology, 57(Suppl.1):9-15.
81. Vokes E. (1993) Interactions of chemotherapy and radiation. Semin Oncol,
20:70-79.
82. Vokes E, Athanasiadis I. (1996) Chemotherapy for squamous cell
carcinoma of head and neck cancer. The future is now. Ann Oncol,
7:15-29.
83. Vokes E, Kies M, Rosen F et al. (2000) Induction Chemotherapy Followed
by Concomitant Chemoradiotherapy for Stage IV Head and Neck
Cancer (HNC): An Attempt at Locoregional and Systematic Tumor
Control. Proc Am Soc Clin Oncol, 19:419a{abstract #1653}.
- 47 -
84. Vokes EE, Weichselbaum RR. (1990) Concomitant chemoradiotherapy:
Rationale and clinical experience in patients with solid tumors. J Clin
Oncol, 8:911-934.
85. Vokes EE, Weichselbaum RR, Lippmann SM, Hong WK. (1993) Medical
progress: Head and neck cancer. N Engl J Med, 328:184-194.
86. Wagstaff AJ, Ibbotson T, Goa KL. (2002) A Review of its Use in the
Management of Advanced Breast Cancer. Adis Drug Evaluation, Drugs
62 (15), Adis International Limited, Auckland, New Zealand 2002
87. Weickhard
U.
(1989)
Ionisierende
Schweiz.Unfallversicherungsanstalt,
Merkblatt 4.
Strahlung
1989.
Reihe
Luzern.
SUVA,
Arbeitsmedizin;
- 48 -
7. Danksagung
Mein großes und herzliches Dankeschön gilt….
…Herrn Chefarzt Prof. Dr. F. Hirsch für die
freundliche Überlassung des
Promotionsthemas und die gute fachliche Betreuung während der Arbeit
…Herrn Chefarzt Dr. A. Jakob für die Bereitstellung seiner Unterlagen und
fachliche Unterstützung
…Frau Birgit Rösch für die schnelle Herausgabe der Patientenakten
…meiner lieben Familie für die jahrelange Unterstützung im Studium und
intensive Teilnahme an meinem beruflichen Werdegang
…meinem lieben Mann für seine motivierende Unterstützung !