Elektrochemie
Werbung

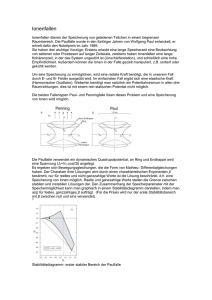
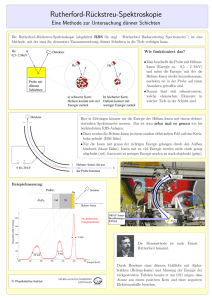
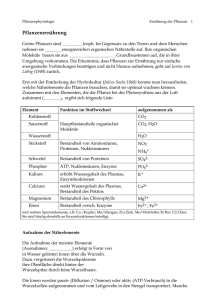
Technische Universität Dresden Institut für Werkstoffwissenschaft Professur für Anorganisch-Nichtmetallische Werkstoffe Praktikumsanleitung Elektrochemische Herstellung und Charakterisierung keramischer Deckschichten auf Ventilmetallen Praktikum zur Vorlesung Keramische Werkstoffe Ulrike Langklotz 1. Einleitung Einige Metalle wie Aluminium, Titan, Tantal, Niob oder Wolfram etc. sind in Gegenwart von Sauerstoff oder Wasser thermodynamisch instabil und zeigen ein großes Bestreben, sich mit Oxidschichten zu bedecken. An trockener Luft beispielsweise entstehen spontan homogene, dichte und weitgehend wasserfreie Passivschichten (d0,Al=2,8 – 3nm, d0,Ta= 1nm, d0,Nb=1,5nm, d0,W=1,5nm). Diese nativen Oxidschichten stellen ein Hindernis für den Transport von Ionen und Elektronen dar und verhindern damit ein weiteres Schichtwachstum. Diese Metalle werden „Ventilmetalle“ genannt. Die Bezeichnung als „Ventilmetalle“ geht auf eine Entdeckung des französischen Forschers Ducretet aus dem Jahre 1875 zurück. Er beobachtete das Phänomen, dass man auf Aluminium in einem elektrochemischen Verfahren bei anodischer Polung (PlusPol) eine Oxidsschicht erzeugen kann, welche den elektrischen Strom in diese Richtung sperrt. Dagegen ist bei einer kathodischen Polung (Minus-Pol) des Metalls unter H2-Entwicklung ein ungehinderter Stromfluss möglich. Das elektrochemische Verhalten von Ventilmetallen unterscheidet sich damit teils drastisch vom Verhalten von Nicht-Ventilmetallen (z.B. Edelmetalle, Eisen, …). Die Dicke der nativen Oxidfilme auf Ventilmetallen beträgt wenige Nanometer, die Schichten können jedoch künstlich bis auf einige µm verstärkt werden, z.B. durch anodische oder thermische Oxidation. Durch die Wahl des Oxidationsverfahrens und der Prozessparameter werden auch die Eigenschaften der Passivfilme modifiziert, so können gezielt geschlossene, poröse oder nanostrukturierte Oxidschichten erzeugt werden. Die Oxide zeigen die typischen Eigenschaften von Gläsern oder keramischen Werkstoffen wie große Härte, chemische Resistenz, geringe Lichtabsorption im Sichtbaren und extreme Behinderung des Transports von Ladung und Materie. Letztere Eigenschaft kennzeichnet diese Oxide also als ausgezeichnete Isolatoren. Eine Vielzahl technischer Anwendungen dieser Sondermetalle beruht auf der Präsenz und den Eigenschaften dieser dünnen oxidischen Deckschichten. So finden von anodischen Oxidschichten bedeckte Ventilmetalle Anwendung - im Fahrzeugbau sowie Luft- und Raumfahrt (Titanlegierungen, Aluminium), - als Verschleißschutzschichten (Hartanodisiertes Aluminium) - im Medizintechnikbereich (Titanlegierungen als Implantatwerkstoff), P A G - im Korrosionsschutz (Tantal, Niob, z.B. als Auskleidung chemischer Reaktoren) - in der Mikroelektronik (Aluminium-, Tantal-, Nioboxid als Isolatoren) - als Kondensatorwerkstoffe (Aluminium, Tantal, Niob: Material für Elkos) Die Anwendung von Ventilmetallen als Kondensatorwerkstoff wurde bereits 1896 von Charles Pollack vorgeschlagen. Da die einseitig stromsperrenden Oxidschichten eine sehr hohe Spannungsfestigkeit schon bei sehr dünnen Schichten aufweisen, kam er auf die Idee, solche Oxidschichten als Dielektrikum eines gepolten Kondensators mit hoher Kapazität in einem Gleichstromkreis auszunutzen. Aufgrund ihrer hohen Dielektrizitätskonstanten werden in der heutigen Industrie vor allem Tantal und Niobium für die Herstellung von Kondensatoren eingesetzt. Des Weiteren haben sich dünne Schichten dieser Oxide, die über Sputterprozesse hergestellt werden, in der Halbleiterindustrie als Sperrschichten für Mikrochips etabliert. Im Rahmen dieses Praktikumsversuches sollen die dielektrischen Eigenschaften der Oxidschichten von Ventilmetallen und ihre Fähigkeiten zur Ionenleitung über elektrochemische Methoden untersucht werden. 2 Allgemeine Grundlagen 2.1 Oxidationsverhalten und Leitfähigkeit In der Regel besitzen die oxidischen Deckschichten von Ventilmetallen bei Raumtemperatur ausschließlich eine ionische Leitfähigkeit, aber keine Elektronenleitfähigkeit. Damit unterscheiden sie sich deutlich von Oxidfilmen auf Nicht-Ventilmetallen, die i.d.R. ausgeprägt elektronenleitendes Verhalten zeigen. Es kann jedoch zu einer zusätzlichen Elektronenleitfähigkeit in den Oxidfilmen auf Ventilmetallen kommen, wenn sich die Lücke zwischen Valenz- und Leitungsband in den Oxidschichten verringert und in den Bereich der Halbleiter kommt. Genauso kann eine wachsende Anzahl von erlaubten Besetzungszuständen innerhalb der Bandlücke eine Elektronenleitung bewirken. So werden die Oxidschichten auf Niob, Titan und Wolfram mit Donorkonzentrationen von 1020 bis 1021 cm-3 zu den n-Halbleitern gerechnet. Experimentell lässt sich ohne größeren Aufwand nicht zwischen ionischer und elektronischer Leitfähigkeit unterscheiden. Auf die bei der Ionenleitung ablaufenden Vorgänge kann anschaulich bei der elektrochemischen Oxidation der Metalle in wässrigen Elektrolyten eingegangen werden. Grundsätzlich laufen in Anwesenheit eines wässrigen Elektrolyten die Oxidationsreaktionen entsprechend folgender Beispielgleichungen ab: 2 Al + 3 H2O 2 Ta + 5 H2O 2 Nb + 5 H2O Zr + 2 H2O Al2O3 + 6 H+ + 6 eTa2O5 + 10 H+ + 10 eNb2O5 + 10 H+ + 10 eZrO2 + 4 H+ + 4 e- Abbildung 1 zeigt das CV der anodischen Oxidation eines Ventilmetalls in einem wässrigen Elektrolyten. P A G 600x10-6 2 Stromdichte / A cm-2 500x10-6 400x10-6 3 300x10-6 U 200x10-6 4 100x10-6 1 U 0 -0.5 0.0 0.5 1.0 1.5 2.0 2.5 3.0 Potential gegen NHE / V Abb. 1 Cyclovoltammogramm von Tantal in 1N H2SO4 Durch die Präsenz einer nativen Oxidschicht auf der Oberfläche der Probe beginnt die anodische Oxidbildung nicht beim thermodynamischen Bildungspotential des Metalls (z.B. U0,Al= -1,6 ± 0,2V, U0,Ta= -0,7 ± 0,2V), sondern erst bei deutlich positiveren Werten. Damit die vorhandene Schicht weiterwachsen kann, müssen Kationen (MeX+) von der Metalloberfläche und Anionen (O2-) vom Elektrolyten aus durch die Schicht hindurch wandern. Der Ionentransport erfolgt dabei über einen Hopping-Prozess der Ionen. Jeder Sprung benötigt eine hohe Aktivierungsenergie, so dass eine Diffusion der Ionen allein auf Grund eines Gradienten des chemischen Potentials nicht in ausreichendem Umfang stattfindet. Es muss zusätzlich eine ausreichend große elektrische Feldstärke an der oxidbedeckten Elektrode anliegen. Solange die angelegte Feldstärke unterhalb eines kritischen Wertes liegt, bleibt die ionische Leitfähigkeit der Schichten sehr klein und es findet keine Oxidation statt. Es fließt dementsprechend nur ein vernachlässigbar geringer Strom (Bereich 1 des CVs). Die Feldstärke im Oxid ist über die Dicke des nativen Oxids mit dem an der Probe anliegenden elektrischen Potential verknüpft. Erreicht dieses das so genannte Schichtbildungspotential, können sich Ionen entsprechend ihrer Ladung im elektrischen Feld durch die Schicht hindurch bewegen. Die Folge ist ein Wachstum der Oxidschicht. Das material- und schichtdickenabhängige Schichtbildungspotential lässt sich im CV (Abbildung 2) am Anfang von Bereich 2 (Beginn des Anstiegs) ablesen. Das Maximum in Abschnitt 2 des Cyclovoltamogramms wird als Overshoot bezeichnet. Sein Zustandekommen kann mit der Injektion mobiler Ladungsträger in die vorhandene Oxidschicht erklärt werden. Unter dem Einfluss des elektrischen Feldes wandern die Ladungsträger, die zum einen aus dem Metall (Mex+) und zum anderen aus dem Elektrolyten (O2-) stammen, durch die Oxidschicht hindurch. Dadurch steigt die Stromdichte im CV stark an, da sie ein direktes Maß für die Anzahl freier Ladungsträger im Oxid ist. Die Ionen reagieren jedoch erst an den jeweils gegenüber liegenden Phasengrenzflächen mit entgegengesetzt geladenen Ionen zum Oxid (Abbildung 2). Dadurch nimmt die Anzahl an Ladungsträgern im Oxid schlagartig drastisch ab, was sich im Absinken der Stromdichte äußert. Als Folge dieser Oxidbildungsreaktion nimmt die Schichtdicke zu und die effektive elektrische Feldstärke über die Schicht ab. P A G Abb. 2 Schematische Darstellung der Ionenwanderung während der elektrochemischen Oxidschichtbildung auf einem Ventilmetall in wässriger Lösung unter Berücksichtigung der verschiedenen Atomradien des Aluminiums im Fall von metallischer und ionischer Bindung. Nach der Ladungsträgerinjektion mit Overshoot erfolgt ein dem anliegenden Potential direkt proportionales Oxidwachstum. Das zeigt sich in Abschnitt 3 des CVs als ein weitgehend potentialunabhängiges Stromplateau, das fast ausschließlich von der Art des Metalls abhängig ist und durch den konstanten Strom von Metall- und Oxidionen durch die wachsende Oxidschicht hervorgerufen wird. Zusätzliche anodische Sauerstoffentwicklung durch Elektrolyse des wässrigen Elektrolyts findet unter den dargestellten Bedingungen nicht statt. Im Rücklauf des CVs wird das anliegende Potential wieder auf den Anfangswert verringert (Bereich 4). Typisch für alle Ventilmetalle ist hier ein starker Abfall der messbaren Stromdichte. Das elektrische Feld in der Oxidschicht wird durch das Absenken des Potentials geringer und reicht nicht mehr aus, um den Transport weiterer Ionen durch das Oxid zu bewirken. Bedingt durch die noch hohe Konzentration an mobilen Ladungsträgern in der Schicht hört der Stromabfall nicht abrupt, sondern innerhalb eines endlichen Zeitraums auf. 2.2 Das Hochfeldmodell Ansätze zur modellhaften Beschreibung der anodischen Oxidbildung an Ventilmetallen gehen zurück auf die Arbeiten von GÜNTHER SCHULZE und BETZ aus den Jahren 1931-38, die mit galvanostatischen und potentiostatischen Messverfahren die Ionenleitfähigkeit der Oxidschichten auf Al und Ta untersuchten. Sie entdeckten, dass der Ionenstrom exponentiell von der Feldstärke E im Oxid abhängt. VERWEY und später MOTT und CABRERA entwickelten das Hochfeldmodell als einen Ansatz zur Beschreibung des anodischen Oxidwachstums auf Ventilmetallen. Dieses Modell besagt im Wesentlichen, dass sich zu jedem Elektrodenpotential direkt proportional eine bestimmte Dicke der Oxidschicht ausbildet. Es eignet sich darüber hinaus zur Beschreibung der ionischen Leitfähigkeit bei einer Vielfalt von Festkörpern, z.B. NaCl, Al2O3 oder TiO2. Das Hochfeldmodell beschreibt das Oxidwachstum als Folge von Ionentransport durch die bestehende Oxidschicht über eine Reihe von feldunterstützten, thermisch aktivierten Sprüngen. Die Ionen (Mex+, O2-) befinden sich im Kristallgitter auf Minima der potentiellen Energie, wie normalen Gitterpositionen oder Zwischengitterplätzen. Ionen können über die Barriere mit der Aktivierungsenergie W zum nächsten Minimum über eine Sprungdistanz a springen. Die nachfolgende Abbildung 3 zeigt schematisch die von den Ionen bei der Wanderung zu überwindenden Energiebarrieren W innerhalb einer Oxidschicht. Ohne ein elektrisches Feld ist P A G die Aktivierungsenergie über die gesamte Schichtdicke hinweg konstant und zu hoch, um eine Ionenwanderung durch Diffusion zu bewirken. Durch Anlegen eines elektrischen Feldes E in der Größenordnung von 106–107 V cm-1 kommt es in der Oxidschicht zu einem Potentialabfall ox, der die Aktivierungsenergie um den Betrag azFox/d absenkt. Bei der kritischen Feldstärke Ekrit ist Ladungstransport in Form einer Ionenwanderung ermöglicht, wie im vorhergehenden Abschnitt diskutiert. Dann sind Stromdichten in Größenordnungen einiger 100 µA cm-2 messbar, die ein Wachstum der Oxidschicht anzeigen. a a a a zFox d Energie Ohne Feld zFox a d Mit Feld zF ox x Abstand x (0,1nm-Bereich) Abb. 3 Einfluss eines elektrischen Feldes auf die Aktivierungsenergie beim Transport von Ionen (Me x+ und O2-) durch eine Oxidschicht Abbildung ist nur schematisch !! Die Ionenbewegung laut Hochfeldgesetzlässt sich durch folgende Gleichung beschreiben: W a z F ox (1 ) a z F ox i a e RT exp exp R T d R T d Term 1…… ……. Term 2………. (1) …………Term 3………… mit a : Sprungdistanz der Ionen z : Ladungszahl der Ionen F : Faraday-Konstante ox : Potentialdifferenz über der Oxidschicht d : Dicke der Oxidschicht R : Allgemeine Gaskonstante Die Stromdichte i ist ein Maß für die Anzahl der beweglichen Ladungsträger im Oxid, d.h. vereinfacht die Anzahl der migrierenden Ionen. Diese Stromdichte hängt zunächst von der Häufigkeit der erfolgreichen Sprünge der Ionen in der Schicht ab (Term 1 in Gleichung (1)). Die Anzahl erfolgreicher Sprünge hängt wiederum von der Sprungdistanz a, der Zahl der Sprungversuche , der Ladungsdichte und einem Boltzmann-Faktor mit der Aktivierungsenergie W, ab. P A G Der Wert für a hängt zusätzlich von der Form der Energiebarriere ab. Für die Ladungsdichte gilt c z F, mit c der Konzentration der beweglichen Ladungsträger. Für den Fall, dass im Festkörper sowohl Anionen und Kationen wandern können, müssen i und in ihre kationischen (i+, +) und ihre anionischen Anteile (i-, -) zerlegt werden: i = i+ + i- und = + + - Die Terme 2 und 3 beschreiben die Verringerung der Aktivierungsenergie durch das zusätzlich anliegende elektrische Feld um den Betrag azFox/d, wie bereits erwähnt. Dabei gibt das Verhältnis ox/d = E die elektrische Feldstärke an. Die Konstante bezeichnet man auch als Durchtrittsfaktor, sie gibt das Verhältnis der transportierten Kationen und Anionen im Oxid (0< < 1) an. Der Durchtrittsfaktor beschreibt die Symmetrie der Barriere und hat für den symmetrischen Fall den Wert 0.5. Für homogene Oxidschichten auf Ventilmetallen genügt eine eindimensionale Beschreibung der Ionenbewegung, da hier die Richtung des elektrischen Feldvektors senkrecht zur Oberfläche ist. Gleichung (1) ähnelt formal der BUTLER-VOLMER-Gleichung für die Durchtrittsreaktion an der Phasengrenze. Wie bei dieser kann bei hohen Feldstärken die Bewegung der Ionen in Gegenrichtung zum Feld vernachlässigt werden. Damit entfällt Term 3, und die Gleichung vereinfacht sich zu: a z F ox W i a exp exp R T d R T (2) Führt man die beiden Konstanten i0 und ein, entspricht Gleichung (2) dem empirisch gefundenen Hochfeldgesetz: Hochfeldgesetz: ox i i0 exp d (3) a zF W mit i0 a exp und R T R T Nach Gleichung 3 ist die Stromdichte i konstant für ein konstantes Verhältnis ox/d. Daraus folgt, dass die Dicke einer Oxidschicht linear mit dem anliegenden Elektrodenpotential ansteigen sollte: d k ox (4) Der Proportionalitätsfaktor k wird Schichtbildungsfaktor genannt und ist eine wichtige Kenngröße zur Beschreibung der anodischen Oxidation von Ventilmetallen. Allerdings zeigt k ebenfalls eine Abhängigkeit von den Anodisierbedingungen (Elektrolyt, Prozessführung, Temperatur, …), was die Bestimmung dieser Größe für verschiedene Werkstoffe und experimentelle Bedingungen notwendig macht. 2.3 Kapazitive Eigenschaften der Oxidschichten Wie in Abschnitt 1 erwähnt, finden die Oxide ausgewählter Ventilmetalle (vor allem Aluminium, Tantal und Niob) Verwendung als Dielektrika in Kondensatoren. Im einfachsten Fall besteht ein Kondensator aus zwei parallel zueinander angeordneten Elektroden, die räumlich durch ein Dielektrikum voneinander getrennt sind. Seine Kapazität ist direkt P A G proportional zu seiner Fläche und umgekehrt proportional zum Abstand der Elektroden. Eine wichtige Kenngröße des zwischen den Elektroden befindlichen Dielektrikums stellt die relative Dielektrizitätszahl (r) dar. Sie ist das Maß für die kapazitiven Eigenschaften dieses Materials. Dieser Zusammenhang wird durch die Kondensatorgleichung beschrieben: C r 0 A d (5) mit C : Kapazität [A s / V] A : Fläche der Elektroden [m2] d : Dicke des Dielektrikums [m] 0 : absolute Dielektrizitätskonstante [F m-1] r : relative Dielektrizitätskonstante [ - ] Das elektrochemische System aus Metall-Metalloxid in einem leitfähigen Elektrolyten kann vereinfacht als ein solcher Kondensator betrachtet werden. Zur Ermittlung der Kapazität der Oxidfilme auf Ventilmetallen wird in diesem Versuch die elektrochemische Impedanzspektroskopie (EIS) genutzt. Bei dieser Messung wird das elektrochemische System mit einer Wechselspannung variierter Frequenz beaufschlagt, der resultierende Wechselstrom gemessen und aus beiden Größen die frequenzabhängige Impedanz der Schicht bestimmt. Die Impedanz ist der komplexe Widerstand, der sich aus ohmschen (Wirkwiderstand) und nichtohmschen (Blindwiderstand) Anteilen zusammensetzt. Ein charakteristisches Impedanzspektrum eines oxidbedeckten Ventilmetalls in der so genannten Bode-Darstellung ist in Abbildung 4 zu sehen. Abb.4: Typisches EIS eines Ventilmetalls in Kontakt mit Elektrolyt, mit entsprechendem Ersatzschaltbild und Zuordnung der Frequenzbereiche. Es ist charakterisiert durch ohmsches Verhalten im Hoch- und Niederfrequenzbereich, was auf die ohmschen Widerstände des Elektrolyten (<104Hz) und des Oxids (>10-3Hz) zurückzuführen ist. Der mittlere Frequenzbereich wird durch kapazitives Verhalten dominiert, zu erkennen am Phasenwinkel von -90° sowie dem linearen Anstieg der Impedanz. Durch Auswertung dieses kapazitiven Bereiches kann die Kapazität des Oxidfilms, Cox, aus Gleichung (6) berechnet werden: P A G | Z | 90 1 1 C 2 f C (6) mit: |Z|=-90° = Impedanzbetrag bei maximaler Phasenverschiebung = Kreisfrequenz C = Oxidkapazität f = Frequenz Wenn zusätzlich die Dicke der Oxidschicht bekannt ist, kann die materialspezifische Dielektrizitätskonstante nach Gleichung (5) ermittelt werden. In Abhängigkeit von der Art des Ventilmetalls besitzen die sich ausbildenden Oxidschichten unterschiedliche dielektrische Eigenschaften (r) und Durchbruchsspannungen- bzw. Feldstärken, bei denen eine elektrolytische Sauerstoffbildung einsetzt. Im Fall von Tantal können diese Spannungen bis zu mehreren hundert Volt betragen. Bei anderen Ventilmetallen dagegen setzt die Sauerstoffentwicklung bereits bei deutlich geringeren Spannungen ein. Dieses Verhalten steht für eine geringere Durchschlagsfestigkeit der Oxidschichten und schränkt die Eignung dieser Materialien als Kondensatorwerkstoffe deutlich ein. 3. Experimentelles Der Versuch ist als „Schauversuch“ konzeptioniert, die Ausführung liegt entsprechend beim Praktikumsbetreuer. Trotzdem sollen die Versuchsdurchführung und die experimentellen Bedingungen im Folgenden kurz beschrieben werden. Der Versuchsaufbau besteht aus einer elektrochemischen Messzelle in 3-Elektrodenanordnung. Für Potentialkontrolle, Strom- und Impedanzmessungen steht ein Potentiostat zur Verfügung. 3.1.1 Elektrochemische Oxidation eines Ventilmetalls Ein 0,5mm dicker Draht aus Tantal wird in der Messzelle als Arbeitselektrode geschaltet. Als Elektrolyt dient Essigsäure-Natriumacetatpuffer (ca. 1M, pH = 5.9). Die anodische Oxidation erfolgt durch Cyclovoltammetrie, wobei in abgestufter Form 5 CVs in folgender Reihe aufgenommen werden: Startpotential: -0,5V (vs. Ag/AgCl-Elektrode) Endpotentiale: 2V, 4V, 6V, 8V und 9,5V (vs. Ag/AgCl-Elektrode) Vorschubrate: 100 mVs-1 3.1.2 Bestimmung der Kapazität der Oxidschichten Direkt nach jedem CV wird ein Impedanzspektrum der frisch entstandenen Oxidschicht aufgenommen. Die Einstellungen für die Impedanzspektren sind bei allen 5 Messungen gleich: Frequenz: 100kHz - 0,1Hz Gleichspannung: 1V Wechselspannung: 10mV P A G Hinweise zur Auswertung Die Schichtdickenbestimmung der Oxidfilme erfolgt über Coulometrie. Zunächst ist die umgesetzte Ladung durch Integration der Fläche unter den gemessenen CVs zu bestimmen. Entsprechend dem Faradayschen Gesetz kann aus der Ladungsmenge die Schichtdicke berechnet werden: (7) Q idt nzF d Q Vm A z F (8) mit Q i t Vm A z F Umgesetzte Ladung Stromdichte Zeit Molares Volumen der Oxide Elektrodenfläche Umgesetzte Elektronen entsprechend Reaktionsgleichung Faraday-Konstante Die Berechnungen sind unter Zuhilfenahme von Excel und den bekannten Beziehungen für numerische Integrationen vorzunehmen. Die Kapazitäten sind aus den Impedanzspektren zu berechnen. Die Impedanz |Z| bei maximaler Verschiebung des Phasenwinkels fmax wird direkt aus dem Spektrum abgelesen. Aus diesem Wert ermittelt man anschließend die Kapazität der Oxidschicht C nach Gleichung (6). Für die Auswertung aller fünf EIS ist die Frequenz fmax zu benutzen, die aus dem Spektrum des 2VOxidfilms abgelesen wurde. 3.1.2 Relevante Daten zu Ventilmetallen und ihren Oxiden Ta/Ta2O5 Ti/TiO2 Al/Al2O3 Nb/Nb2O5 Zr/ZrO2 3.1.3 - M / g/mol 442 80 102 266 123 k / nm/V 1,3 – 2,4 1,3 – 2,8 0,8 – 2,0 2,1 – 3,7 1,7 – 3,0 r 28 56 11 43 20 / g/cm³ 8,2 4,2 3,2 4,8 5,7 0 / VSSE -0,9 -0,9 -1,7 -0,6 -1,5 Praktikumsschwerpunkte 3-Elektroden-Anordnung bei elektrochemischen Messungen Faradaysches Gesetz Cyclovoltammogramm Funktionsweise eines Kondensators Was ist Impedanz? Was ist eine Kapazität? Was ist ein Dielektrikum? P A G