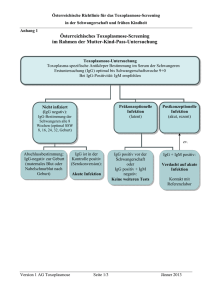
Diagnostik und Therapie bei Parvovirus B19 und Zytomegalievirus
Werbung

Labor Prof. Gisela Enders Stuttgart Diagnostik und Therapie bei Parvovirus B19 und Zytomegalievirus Infektionen in der Schwangerschaft Rainer Bald Leitender Arzt Pränatalmedizin Klinik für Frauenheilkunde und Geburtshilfe im Klinikum Leverkusen Martin Enders Labor Prof. G. Enders und Partner Samstag, 5. November 11 Parvovirus B19 (B19V) Samstag, 5. November 11 Parvovirus B19 - Erreger und Epidemiologie • ss-DNA Virus ohne Hülle • Weltweit verbreitet, Tröpfcheninfektion • Haupt-Zielzellen: Vorläuferzellen der Erythropoiese • Klinik: postnatal 30% asymptomatische Infektion, Ringelröteln/Exanthem, Arthropathien • Ca. 60-70% der Schwangeren sind seropositiv • Infektionsquelle: Kinder 3-10 Jahre, (Blutprodukte) • Intrauterine Transmision ➠ Abort, Anämie, Hydrops Samstag, 5. November 11 B19V-bedingtes Hydrops- und Abortrisiko in Abh. vom Gestationsalter bei mütterlicher Infektion GA (SSW) Risiko für Hydrops Risiko für Abort / IUFT Transmissionsrate Anteil asym. Infektionen < 13 3,9 % (2/51) 7,8 % (4/51) ? ? 13-20 11,9 % (8/67) 6,0 % (4/67) ? ? >20 0 % (0/118) 0 % (0/118) >50 % Hoch Total 4,2 % (10/236) 3,4 % (8/236) 30-50 % ? Hoch Enders M et al. JCV 2010 Samstag, 5. November 11 Intervall zwischen mütterlicher B19V- Infektion und Auftreten Hydrops fetalis Anzahl Fälle [n] N=40 Hydropsfälle ?, <5% Wochen nach Erkrankungsbeginn Enders M et al., Prenat Diagn 2004 Samstag, 5. November 11 B19: Virusstruktur und Antigene mit diagnostischer Bedeutung Kapsid 95% VP2 (58 kD); 5% VP1 (83 kD): à Neutralisation; Zelleintritt; Hemmung der Hämatopoese (VP2) Nicht-Strukturprotein (NS1): Zytotoxizität (Apoptose); Replikation; Transkription Broliden K et al. J Intern Med. 2006 Samstag, 5. November 11 B19V Diagnostik: Methoden Testformat Einsatz • B19V IgG- und IgM-AK Immunoassay (IA), ImmunfluoreszenzTest Routinediagnostik - Immunstatus - Akute Infektion • Epitop-spez. IgG-AK Immunoassay, Line-Blot • Antigen-spez. IgG-AK (NS-1) Line-Blot Serologische Zusatzdiagnostik (Eingrenzung des Infektionszeitpunktes) NAT z.B. Real-time PCR (Taqman, LightCycler) Zusatzdiagnostik in Schwangerschaft; Pränataldiagnostik Antikörpernachweis Erregernachweis • Nukleinsäurenachweis (B19V nicht in RoutineZellkultur anzüchtbar) Samstag, 5. November 11 Antikörperbildung u. Virämie bei Schwangeren mit akuter B19 Infektion B19-DNA B19-IgM VP2-IgG (konformelle Epitope); VP1-IgG NS-1 VP2-IgG lin. Enders M et al. JCV 2006 Samstag, 5. November 11 Parvovirusinfektion Samstag, 5. November 11 Algorithmus zur Immunitätsabklärung in der Schwangerschaft nach Kontakt Immunstatus der Mutter IgM(-) ; IgG(-) IgM(+) ; IgG(+) IgM(-) ; IgG(+) Keine Immunität Kontrolle n. 2-3 Wochen V.a. akute/kürzliche B19 Infektion Frühere Infektion mit B19, Schutz ist anzunehmen IgM(+) ; IgG(+): Akute Infektion IgM(-) ; IgG(-): Keine Infektion, keine Immunität Samstag, 5. November 11 2. Blutprobe zur Bestätigung; Ggf. PCR bzw. Zusatzteste bei unklaren Befunden bzw. Eingrenzung des Infektionszeitpunktes Algorithmus zur Immunitätsabklärung in der Schwangerschaft bei Exanthem Immunstatus der Mutter IgM(-) ; IgG(-) IgM(+) ; IgG(+) IgM(-) ; IgG(+) Exanthem nicht B19bedingt V.a. akute / kürzliche B19 Infektion Ausschluss einer akuten Infektion mit Parvovirus B19, Schutz ist anzunehmen 2. Blutprobe zur Bestätigung; Ggf. PCR und serologische Zusatzteste bei unklaren Befunden bzw. zur Eingrenzung des Infektionszeitpunktes Samstag, 5. November 11 Algorithmus zur Immunitätsabklärung in der Schwangerschaft bei Anämie / Hydrops / IUFT Immunstatus der Mutter IgM(-) ; IgG(-) Hydrops / IUFT nicht B19-bedingt Samstag, 5. November 11 IgM(+) ; IgG(+) IgM(-) ; IgG(+) CAVE – IgM kann bereits wieder unter die Nachweisgrenze abgefallen sein. ➠ Zusatzteste inklusive PCR zur Eingrenzung des Infektionszeitpunktes anfordern; ➠ bzw. invasive Diagnostik/Therapie oder postmortal Erregernachweis in fetalen Geweben anstreben B19V Diagnose beim Feten • Erregernachweis vorrangig – Goldstandard ist der quantitative Nachweis von B19V DNA (mittels PCR) • In der Regel hohe Viruslast im Fruchtwasser bzw. Fetalblut nachweisbar (>106 cop/ml) • IgM Bestimmung im Nabelschnurblut hat eine sehr geringe Sensitivität (<30%) Samstag, 5. November 11 Verschiedene sonographische Hinweise allerdings unspezifisch •Parvo B 19, CMV, Röteln, Toxoplasmose, Malaria, Lues ..... Hydrops Periventrikulitis Anämie AV-Klappeninsuffizienz Hydrops placentae AV-Klappeninsuffizienz Samstag, 5. November 11 Intrauterine Therapie 1963 wurde die RH-Inkompatibilität die erste intrauterin behandelbare fetale Erkrankung, nachdem Liley1 die erste intrauterine intraperitoneale Transfusion durchführte 1. Liley AW. Iintrauterine Transfusion of Foetus in haemolytic disease. Br Med J 1963; 2:1107. Samstag, 5. November 11 Cordocentese 1986 bis heute Samstag, 5. November 11 Intraarterielle/intravenöse Transfusion 18+5 SSW Samstag, 5. November 11 G1P0, 20+4 SSW 20+4 SSW, Aszites, Perikarderguss, Vmax. in der ACM hoch, Freitag Nachmittag Samstag, 5. November 11 Samstag, 5. November 11 Samstag, 5. November 11 Parvo B 19 Infektion, 20+4 SSW Hb P1 Hb Pe 14,0 11,7 9,3 7,0 12,1 13,3 12,7 11,9 10,8 4,7 7,9 7,6 6,5 6,0 2,3 9,1 8,9 5,1 6,6 5,3 3,8 0 1,1 20+4 Samstag, 5. November 11 21+0 21+6 22+3 23+0 23+5 24+5 25+5 Samstag, 5. November 11 Parvo B 19 Infektion, 20+4 SSW Thrombos P1 Thrombos P2 500 487,0 464,0 488,0 501,0 489,0 474,0 443,0 493,0 400 300 200 100 0 33,0 8,0 20,0 20+4 Samstag, 5. November 11 21+0 12,0 21+3 21+6 54,0 22+3 22,0 23+0 46,0 23+5 53,0 24+5 Abschätzen der fetalen Anämie Invasiv •Serielle Cordocentesen Nicht invasiv •Ultraschall •Dopplerultraschall Samstag, 5. November 11 Nicht invasive Methoden zur Beurteilung der fetalen Anämie Brass et. al. 1988 zeigten erstmals einen Zusammenhang zwischen der systolischen Geschwindigkeit in der ACM und dem Hämatokrit Mari et al. 1995 maßen die „peak flow velocity“ in der Arteria cerebri media und korrelierten diese mit dem fetalen Hämatokrit Samstag, 5. November 11 ACM Vmax: Korrekte Messung Samstag, 5. November 11 0° 41 ° 73,1 cm/s 45,9 cm/s Vmax - Werte der ACM und Hb-Werte o keine/milde Anämie ▲ mäßige/schwere Anämie ● Hydrops nach Mari, 2000 Samstag, 5. November 11 Oepkes et al 2006, NEJM ACM V max Samstag, 5. November 11 Sensitivität Spezifität Exaktheit 88 % 82 % 85 % Anämie - Ultraschall Samstag, 5. November 11 Klappeninsuffizienz Klappeninsuffizienz Samstag, 5. November 11 Hb 0,9 g/dl Hb 4,6 g/dl Kardiomegalie Klappeninsuffizienz Hb 4,6 g/dl Hb 1,2 g/dl Hb 1,7 g/dl Hb 1,6 g/dl Samstag, 5. November 11 Hb 1,2 g/dl Hb 1,8 g/dl Vor Transfusion; HB: 4,3 g/dl Nach Transfusion; HB: 8,4 g/dl Samstag, 5. November 11 Probleme der ACM • Falsch positiv Raten von 10-18% (moderate bis schwere Anämie) werden berichtet10,11,13 • Nach 35 Schwangerschaftswochen nehmen die „falsch positiv Raten“ deutlich zu12 • Messung in fetaler Ruhe • Fetale Atembewegungen • Falsch negative Raten von > 20% durch Druck der Schallsonde auf den fetalen Kopf 10 Zimmerman, R, Carpenter, RJ Jr, Durig, P, Mari, G. Longitudinal measurement of peak systolic velocity in the fetal middle cerebral artery for monitoring pregnancies complicated by red cell alloimmunisation: a prospective multicentre trial with intention-to-treat. BJOG 2002; 109:746. 11 Oepkes, D, Seaward, PG, Vandenbussche, FP, et al. Doppler ultrasonography versus amniocentesis to predict fetal anemia. N Engl J Med 2006; 355:156. 12 Sallout, BI, Fung, KF, Wen, SW, et al. The effect of fetal behavioral states on middle cerebral artery peak systolic velocity. Am J Obstet Gynecol 2004; 191:1283. 13 Shono, M, Shono, H, Ito, Y, et al. The effect of behavioral states on fetal heart rate and middle cerebral artery flow-velocity waveforms in normal full-term fetuses. Int J Gynaecol Obstet 1997; 58:275. Samstag, 5. November 11 B19-Infektion in der Schwangerschaft – Fortschritte (Erfahrungen 1987–2008, Enders/Bald) • Fetales Risiko (Hydrops fetalis, Verlustrate) ➠ kleiner als früher beschrieben (prosp. Studien) • Bisher kein erhöhtes Missbildungsrisiko festgestellt ➠ keine Indikation für SS-Abbruch • Verbesserte nicht-invasive Anämiediagnostik (Farbdoppler) • fetale Therapie mit Erythrozyten- und Thrombozytenkonzentraten schnelle Therapie senkt fetale Verlustrate • Bisher keine Auffälligkeiten bei Neugeborenen, die intrauterin therapiert wurden bis auf eine Studie von Nagel 2010: •neuromotorische Spätfolgen bei (5/16) intrauterin transfundierten Kindern entdeckt im Alter von 6 Monaten bis 7 Jahre Samstag, 5. November 11 Zytomegalievirus (CMV) c Samstag, 5. November 11 Zytomegalievirus (CMV) - Erreger und Epidemiologie • ds-DNA Virus mit Hülle • Breiter Zelltropismus • Primärinfektion ➠ Persistenz • Rekurrenz (endogene Reaktivierung oder Reinfektion) ➠ erneute Virämie und Virusausscheidung • Weltweit verbreitet, Schmierinfektion • Ca. 40-50% der Schwangeren sind seropositiv (BRD) • Infektionsquelle: Kinder <3 (6) Jahren, Sexualpartner • Intrauterine Transmission ➠ Hör- und Sehstörungen, Intelligenzminderung, spastische Paresen u.a. Samstag, 5. November 11 Transmissions- und Schädigungsrate in Abh. von der Art der mütterlichen CMV-Infektion CMV-Primärinfektion: Risiko für fetale CMV-Infektion 30–70% (abh. vom GA) Symptomatisch bei Entbindung: 13% Spätschäden: 40%–58% CMV-Rekurrenz: Risiko für fetale CMV-Infektion bei präkonzeptioneller Immunität <1,0% Asymptomatisch bei Entbindung: 87% Spätschäden: 13,5% (v.a. Hördefekte) Symptomatisch bei Entbindung: ? Spätschäden: ? FAZIT: >80% der mütterlichen CMV Primär-infektionen sind ohne negative Folgen für das Kind modifiziert nach Dollard SC et al., Rev Med Virol 2007 Samstag, 5. November 11 Transmissionsrate in Abh. vom Zeitpunkt der mütterlichen CMV-Primärinfektion Nachweis fetaler/kongenitaler CMV-Infektion Infektionszeitpunkt (SSW) Präkonzeptionell % 95 % CI 4 / 24 16.7 4.7–37.4 Perikonzeptionell (1 Wo. vor LP ➠ 4+6) 10 / 29 34.5 17.9–54.3 1. Trimenon (5+0 ➠ 13+6) 25 / 83 30.1 20.5–41.2 2. Trimenon (14+0 ➠ 25+6) 29 / 76 38.2 27.3–50.0 3. Trimenon (≥26+0) 26 / 36 72.2 54.8–85.8 94 /248 37.9 31.8–44.3 Total (1–10 Wo. vor LP) n / total Enders G. et al. JCV 2011 Samstag, 5. November 11 CMV: Virusstruktur und Antigene mit diagnostischer Bedeutung Virus-Hülle (Phospholipidmembran) c >20 Glycoproteine, Neutralisierende Epitope: gB (UL55); gH (UL75) Matrix (Tegument) >27 Proteine, meist phosphoryliert und hoch immunogen: pp150 (UL32); pp65 (UL83) =15% der Virion-Masse!; Nukleokapsid (Ikosaeder) aus 6 Strukturproteinen Genom: ds DNA, ca. 235 kbp Samstag, 5. November 11 CMV-Diagnostik: Methoden Testformate Einsatz • CMV IgG- und IgM-AK Immunoassay (z.B. EIA) Routinediagnostik • IgG-Avidität Immunoassay, Immunoblot (IB) Antikörpernachweis • Anti-gB IgG-AK IB, EIA • Neutralisierende AK Neutralisationstest Serologische Zusatzdiagnostik zur Eingrenzung des Infektionszeitpunktes Erregernachweis • Virusanzucht • Nukleinsäurenachweis Samstag, 5. November 11 Schnell-Zellkulturtest Standard Zellkultur NAT (z.B. PCR) Nachweis einer intrauterinen Infektion (prä- und postnatal) Antikörpertiter / IgG-Aviditätsindex CMV-Primärinfektion Frühere Infektion IgM IgG IgG Avidität NT gB-IgG langpersistierende IgM-Ak negativ NT = Neutralisierende Antikörper Samstag, 5. November 11 CMV-Rekurrenz CMV Diagnostik in Schwangerschaft • Bestimmung des Immunstatus • nach Kontakt • bei erhöhtem Expositionsrisiko • als Screening (zu Beginn der Schwangerschaft; seriell ?) • Symptome (! Erstinfektion in > 80% asymptomatisch) • Fieber, Kopfschmerzen, Respirationstrakt-Symptome • Lymphknotenschwellungen, Exanthem • Abgeschlagenheit, Hepatitis (GOT/GPT), Thrombozytopenie • Auffälliger Ultraschall Samstag, 5. November 11 Befundbewertung serologischer CMV Basisteste IgG negativ IgM negativ v Patientin ist empfänglich IgG positiv IgM negativ (IgG Avidität hoch) v Schutz vor Primärinfektion ➠ Keine weiteren serologischen Kontrollen, beachte: CMV Rekurrenz ➠ CAVE: Schließt fetale CMV Infektion nicht aus IgM positiv v Mögliche Ursachen: 1. CMV Primärinfektion: Hohes fetales Risiko 2. CMV Rekurrenz: Geringes fetales Risiko 3. Lang persistierende IgM Ak ➠ „Kein“ fetales 4. Falsch positive IgM Ak ➠ Risiko ! Samstag, 5. November 11 ➠ Beratung zur Prophylaxe und Kontrolle der CMV IgG Ak alle 8-(10) Wochen bei erhöhtem Expositionsrisiko CMV Diagnose beim Feten Indikation zur invasiven Pränataldiagnostik (PD): • Serolog. gesicherte CMV-Primärinfektion 1./2. Trimenon • Auffälliger Ultraschall (und Mutter CMV IgG positiv) Vorrangig Erregernachweis: • Fruchtwasser: CMV-PCR und Schnellzell-Kultur • Immediate Early-AG-Zelltest • Fetalblut: CMV-PCR und IgM-AK-Test • klinisch-chemische Marker Prädiktiver Wert der invasiven PD: • negativer Vorhersagewert >96% • positiver Samstag, 5. November 11 Vorhersagewert >99% Enders G. et al. Prenat Diagn. 2001 Einfluss des Zeitpunktes der Amniozentese auf die Aussagekraft des CMV Nachweises Zeit zw. mütterl. Infektion und AC Sensitivität (SZK+ZK+nPCR) Spezifität (SZK+ZK+nPCR) ≤8 Wo. 50,0 % (5/10) 100 % (4/4) 9–12 Wo. 76,2 % (16/21) 100 % (20/20) ≥13 Wo. 91,3 % (21/23) 100 % (24/24) Revello et Gerna, JCV 2004 SSW bei AC Sensitivität (PCR+ZK) Spezifität (PCR+ZK) ≤21 66,7 % (12/18) 100 % (76/76) >21 96,2 % (25/26) 100 % (46/46) Enders G et al. Prenat Diagn 2001 Samstag, 5. November 11 Prognostische Marker für kindliche Schädigung bei CMV-infizierten Feten • Auffällige Befunde in der „Bildgebung“ – Ultraschall – MRT (ZNS-Auffälligkeiten) • Virusspezifische Marker im Fetalblut – Nachweis einer hohen Viruslast – Nachweis CMV-spez. IgM-AK in hoher Konzentration • Nicht-virusspezifische Marker im Fetalblut – Thrombozytenzahl erniedrigt – µGT erhöht – beta2-Microglobulin erhöht Samstag, 5. November 11 Enders G et al., Prenat Diagn 2001 Benoist G. et al, AJOG 2008 Picone O. et al., Prenat Diagn 2008 Guerra B et al., AJOG 2008 Fabbri E. et al. BJOG 2010 Cytomegalie-Infektion Moll, Rheder, Schoner Institut für Pathologie Universität Marburg Samstag, 5. November 11 Symptomatische cong. CMV Infektion ! Mikrozephalie, Petechien Stagno, Remington, 2005, Petechien Samstag, 5. November 11 Hintergrund Samstag, 5. November 11 Schlüsselerlebnis Samstag, 5. November 11 31+1 SSW, NIHF unklarer Ursache Samstag, 5. November 11 Patientin 901795, NIHF 31+1 Hydrops fetalis (Aszites), Polyhydramnie, ACM 72,1cm/s 31+1 Aszites, Hepatosplenomegalie, moderate Anämie, Polyhydramnie 1. IUT (Hb 8,2 ➙ 12,1 g/dl), Aszitespunktion (353 ml), 31+1 Thrombozyten 151 x 10 9/l 31+2 Aszites, Hautödem, Hepatosplenomegalie, Polyhydramnie 31+5 EP 1120 ml, Aszites nachgelaufen Samstag, 5. November 11 32+1 Labor Prof Enders, Stuttgart : Frische CMV-Infektion 32+5 1. Cytotect CP Gabe i.v. (Fet) 34+0 2. Cytotect CP Gabe i.v. (Fet) 34+1 Kein Aszites, Demissio 38+6 Geburt durch elektive Sectio im Perinatalzentrum Samstag, 5. November 11 Untersuchung durch die Kinderklinik: Augenhintergrund o.B. Ausscheidung von CMV-Viren (wenig) im Urin Im Liquorpunktat keine Viren nachweisbar Behandlung mit Gancicovir ® Kind, derzeit über 5 Jahre alt Aussage des behandelnden Kinderarztes und der Kinderklinik „.... ist völlig unauffällig“ Samstag, 5. November 11 CMV-Infektion Bekanntheitsgrad ist immer noch gering •bei Ärzten •bei medizinischen Berufen •in der Öffentlichkeit Bedeutung •Häufigste infektiöse Ursache mentaler Retardierung und nicht erblicher Taubheit •Nicht selten unsachgemäße/insuffiziente Beratung •der Schwangeren mit Überbewertung des Risikos •Schwangerschaftsabbruch •der Eltern eines asymptomatisch kongenital infizierten Kindes • fehlender Hinweis auf mögliche Spätschäden • Hörschäden werden erst spät entdeckt Samstag, 5. November 11 972245, 38 Jahre, G2P1 • 25+3 SSW, Serokonversion (Labor Prof. Enders), unauffällige Biometrie, hyperechogener Darm. • Randständige NS-Insertion an der Hinterwandplazenta • 25+4SSW, 1. Cordocentese und 1. IUTT bei Thrombozytopenie, 1. Cytotect CP Gabe (i.v.) • Fetale Therapie mit Valcyte® 2-0-2 (bis 32+2) • 26+4 SSW, Amniozentese und 2. IUTT • 27+4 SSW, 3. IUTT, 1. IUT • 29+4 SSW, 4. IUTT und 2. Cytotect CP-Gabe (i.v.) • 31+4 SSW, 5. IUTT, 2. IUT Samstag, 5. November 11 972245, 38 Jahre, G2P1 ® Therapie auf 32+2 SSW Reduktion der Valcyte • 2-0-0 bis zur Geburt (Erhaltungsdosis) • 32+4 SSW, 6. IUTT, 3. IUT • 35+4 SSW, 4. IUT • Fet seit 32+2 SSW CMV-Virus negativ • Entbindung durch RE-Sectio • Post partale Therapie mit Valcyte® über 2 Wochen ab 3 Lebenstag • Hörscreening unauffällig Samstag, 5. November 11 972245, 38 Jahre, G2P1 Samstag, 5. November 11 Samstag, 5. November 11 Samstag, 5. November 11 Samstag, 5. November 11 Symptomatische intrauterine CMV-Infektion: Antenatale Therapie mit CMV-Hyperimmunglobulin und Ganciclovir nach Primärinfektion im 1. Trimester Valcyte: 2-0-2 2-0-0 Partus neg Samstag, 5. November 11 Samstag, 5. November 11 972245, 38 Jahre, G2P1 • Im Alter von 10 Wochen hohe Ausscheidung von CMV-Viren im Urin nachweisbar • Beratung der Eltern (Risiko für Hörstörungen ist von 10% auf 4-5% reduzierbar durch Ganciclovir) •Keine eindeutige Therapieempfehlung •Im Alter von 6 Monaten • extreme Schwerhörigkeit auf einem Ohr (Grenze 100 Dezibel) •anderes Ohr (noch) unauffällig. Rat zur Ganciclovir-Therapie über mindestens 6 Monate Samstag, 5. November 11 Labordiagnostik, Ultraschalldiagnostik und MRT Samstag, 5. November 11 Klinische Manifestationen beim Neugeborenen mit kong. CMV-Infektion bei Geburt 13% aller kongenital infizierten Kinder davon Mortalität (erste 6 LW.): ~4% Art der Symptome bei Geburt (% der Überlebenden) Systemische (meist transiente): ZNS Symptomatik (bei 72% ein bis mehrere Symptome: Frühgeburt (<38 SSW) 34% Mikrozephalie ~40% geringes Geburtsgewicht 47% Intracranielle Verkalkungen ~43% Petechien ~54% neurologische Auffälligkeiten ~26% Thrombozytopenie ~54% Lethargie/Trinkschwäche ~25% Hepatosplenomegalie Ikterus Pneumonie Samstag, 5. November 11 44-47% 36% ~11% Krämpfe ~7% Hördefekte ~41% Chorioretinitis ~11% CMV-HIG zur Prävention kongenitaler CMV-Infektionen (nach Nigro) •Die Gabe von HIG an Mütter mit Serokonversion reduziert signifikant das Risiko einer Virustransmission auf den Feten •Die Gabe von HIG an Mütter mit intrauterin infizierten Feten reduziert signifikant das Risiko einer symptomatischen Erkrankung bei Geburt aber • Der beste Weg der Applikation (an die Mutter, an den Feten, in das Fruchtwasser) blieb unklar • Die Studie war nicht randomisiert und die Zahl der Patientinnen war klein Samstag, 5. November 11 CMV-HIG vor Behandlung von intrauterin infizierten Feten (nach Nigro) •Es gab keine Daten über die HIG-Konzentration in den verschiedenen Kompartimenten (Mutter, Fet, Fruchtwasser) •Es wurden die verschiedenen Wege der Applikation nicht verglichen (Gabe über die Mutter, Gabe an den Feten oder in das Fruchtwasser) •Es gibt keine Aussage zur Behandlung der Plazenta (durch HIG oder durch Virostatika) •Die Kosten des HIG ist bei Gabe an die Mutter unvergleichlich größer, als bei Gabe an den Feten (6.000-12.000 € gegenüber 500-1.000 €) Samstag, 5. November 11 CMV-Therapie - Fragen • Wie verteilt sich CMV Hyperimmunglobulin in verschiedenen Kompartimenten nach der Applikation? • Übertritt (aktiv/passiv) von der Mutter auf den Feten? • bei Gabe an den Feten • Rücktransport (aktiv/passiv) in die Mutter? • Ist die Cordozentese im Rahmen der Behandlung sinnvoll? • Ist eine „antivirale Therapie“ möglich und sinnvoll? Samstag, 5. November 11 CMV-Therapie - unbelegte Thesen • HIG wird aktiv von der Mutter über die Plazenta auf den Feten übertragen und dort konzentriert • Immunglobuline werden aus dem Fruchtwasser aktiv über den FC-Rezeptor im Darm des Feten in seinen Kreislauf aufgenommen • CMV-Hyperimmunglobulin diffundiert passiv aus dem fetalen Kompartiment in das mütterliche Kompatiment • Eine Cordozentese im Rahmen einer CMVTherapie bringt keinen Nutzen und ist ein unnötiges, hohes Risiko für den Feten Samstag, 5. November 11 Ergebnisse – Fall 1: Mutter: CMV Primärinfektion 3./4. SSW, Ø Symptome PCR pos., 2.900 cop/ml IgM pos., Index 11,0 (N<0.9) Thromb.: 173 Tsd./µl PCR pos., 15.000 cop/ml IgM pos., Index 11,7 Fetalblut Nabelschnurblut mütterliches Blut ~850 U/kg Dosis 200 U/kg maternaleSamstag, 5. November 11 fetale HIG-Appl. ~450 U/kg ~1200 U/kg M. Enders, Labor Enders, R. Bald, Leverkusen, 2010 „Reverser“ Transport via Plazenta von CMV-Hyperimmuneglobulin ? SSW 1 mother G. Enders, Stuttgart, R. Bald, Leverkusen 2009 2 fetus CMV-IgG [mPEIU/ml] gB-IgG [index] CMV-IgG [mPEIU/ml] gB-IgG [index] 20+3 1580 1,3 - - 21+2 - - <200 0,2 21+2 1. intravascular fetal application of Cytotect (500E) 21+2 1480 1,2 22+2 - - 4,4 1611 22+2 2. intravascular fetal application of Cytotect (500E) 24+2 2139 1,3 1CMV 1306 3,1 5,9 primary infection of mother between 10. and 15. week 2detection of fetal infection in 21+2 weeks (amniotic fluid and fetal blood: CMV DNA positive) gB-IgG = anti-CMV-gB IgG EIA (index<0,9 = negative) CMV-IgG <200mPEIU/ml neg. Samstag, 5. November 11 Kein Nachweis von CMV-gB IgG Ak im Fetalblut nach intramnialer CMV Hyperimmunglobulingabe SSW vor 14 nach vor 17 G. Enders, Stuttgart, R. Bald, Leverkusen 2010 Mütterl. Blut§ Fetalblut Fruchtwasser gB-IgG [Index] gB-IgG [Index] gB-IgG [Index] 0,2 1. CMV HIG Gabe an Mutter; 200 U/kg KG 6,8 2,8 2. CMV HIG Gabe an Mutter; 200 U/kg KG nach 7,6 vor 19 0,2 1. intraamniale CMV HIG Gabe an Fetus; 3500 U/kg KG nach 3,3 vor 1,1 23 nach §Schwangere 0,5 (negativ) 1. intravasale CMV HIG Gabe an Fetus; 1000 U/kg KG 9,5 mit CMV Primärinfektion im ersten Trimester Samstag, 5. November 11 2,6 gB-IgG = anti-CMV-gB IgG EIA (index< 0,9 = negative) Schlussfolgerungen 1. Die hochdosierte Gabe von HIG an die Mutter (< 26. SSW) führt nicht zu messbaren anti-CMV gBIgG Spiegeln in der fetalen Zirkulation •Keine passive Immunisierung des Feten •Keine antivirale / immunmodulat. Wirkung im fetalen Kompartiment 2. Nach hochdosierter intrauteriner i.v. Applikation sind anti-CMV gB-IgG über mindestens 4 Wochen in der fetalen Zirkulation nachweisbar •Bislang keine Studien zur fetalen i.v.-Gabe - klinischer Nutzen •Kein reverser Transport vom Feten zur Mutter Samstag, 5. November 11 CMV-Therapie - Probleme • Eine fetale antivirale Therapie erbringt keinen Nutzen? • Eine antivirale fetale Therapie ist teratogen? • Eine antivirale Terapie ist mutagen? Samstag, 5. November 11 Veröffentlichte Fakten Teratogenität • in Tierversuchen wurden teratogene Effekte bei hohen Dosierungen beobachtet aber Aciclovir: eine Studie mit 20 Probandinnen (zweites und drittes Trimenon) zeigte keine teratogenen Effekte Ganciclovir: 4 Fallberichte (2 im ersten Trimenon) zeigte keine teratogenen Effecte Brady, RC et al.: Pediatr Infect Dis J 2002 Miller, BW: Transplantation 1995 Pescovitz, M: Transplantation 1999 Puliyanda, DP: Transpl Infect Dis 2005 Samstag, 5. November 11 Therapie mit Valganciclovir und CMV-Hyperimmunglobuline (HIG) SSW 1 mother GCV-level [mg/l] peak) 21+2 2 fetus (trough/ - G. Enders, Stuttgart, R. Bald, Leverkusen 2009 GCV-Spiegel [mg/l] peak) (trough/ - virusload [copies/ml] 880.000 21+2 1.fetal HIG-application (500E) 22+2 2.fetal HIG-application (500E) 22+4 Valcyte to the mother (1x900mg/day) 22+6 0,04/ 2,36 -/ 2,49 500.000 24+2 0,03/ 2,24 -/ 2,30 200.000 24+2 3.fetal HIG-application (600E) 24+6 Valcyte to the mother (2x900mg/day) 26+2 -/ 4,10 -/ 3,90 10.000 28+2 0,39/ - 1,52/ - 6.800 1CMV Samstag, 5. November 11 primary infection of mother between 10. and 15. week 2detection of fetal infection in 21+2 weeks CMV-DNA (in-house) cop x 103/ml Valganciclovir und HIG intravasal CMV-DNA copies im Fetalblut 900 675 HIG Valganciclovir 450 880 510 500 225 200 10 6,8 0 26+2 28+2 30+2 0 21+2 Samstag, 5. November 11 22+2 22+6 24+2 Periventrikulitis 22+6 SSW Samstag, 5. November 11 Samstag, 5. November 11 Vorteile der Cordocentese • CMV assoziierte Thrombozytopenie und Anämie können diagnostiziert und behandelt werden • Fetale Viruslast, Medikamentenspiegel und CMVHIG Spiegel können bestimmt werden und • das Risiko einer Cordozentese wird häufig überschätzt bei über 57 Patientinnen, die wegen einer pränatalen CMV-Infection behandelt wurden, führten wir mehr als 115 Cordocentesen durch (HIG intravasal) ohne assoziierte Komplikationen oder IUFT Samstag, 5. November 11 Samstag, 5. November 11 Abdel-Fattah, SA, Bhat, A, Illanes, S, et al. TORCH test for fetal medicine indications: only CMV is necessary in the United Kingdom. Prenat Diagn 2005; 25:1028. Samstag, 5. November 11 Samstag, 5. November 11