studien im fokus - Deutsches Ärzteblatt
Werbung
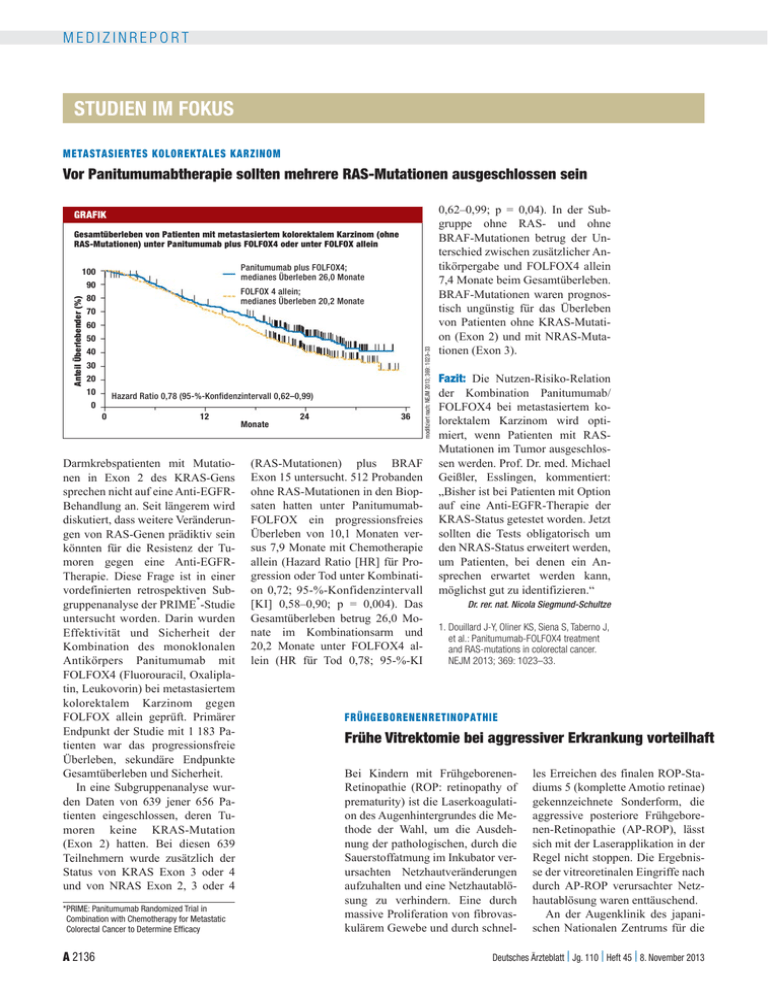
MEDIZINREPORT STUDIEN IM FOKUS METASTASIERTES KOLOREKTALES KARZINOM Vor Panitumumabtherapie sollten mehrere RAS-Mutationen ausgeschlossen sein GRAFIK Gesamtüberleben von Patienten mit metastasiertem kolorektalem Karzinom (ohne RAS-Mutationen) unter Panitumumab plus FOLFOX4 oder unter FOLFOX allein Panitumumab plus FOLFOX4; medianes Überleben 26,0 Monate 100 FOLFOX 4 allein; medianes Überleben 20,2 Monate 80 70 60 50 40 30 20 10 Hazard Ratio 0,78 (95-%-Konfidenzintervall 0,62–0,99) 0 0 12 24 36 Monate Darmkrebspatienten mit Mutationen in Exon 2 des KRAS-Gens sprechen nicht auf eine Anti-EGFRBehandlung an. Seit längerem wird diskutiert, dass weitere Veränderungen von RAS-Genen prädiktiv sein könnten für die Resistenz der Tumoren gegen eine Anti-EGFRTherapie. Diese Frage ist in einer vordefinierten retrospektiven Subgruppenanalyse der PRIME*-Studie untersucht worden. Darin wurden Effektivität und Sicherheit der Kombination des monoklonalen Antikörpers Panitumumab mit FOLFOX4 (Fluorouracil, Oxaliplatin, Leukovorin) bei metastasiertem kolorektalem Karzinom gegen FOLFOX allein geprüft. Primärer Endpunkt der Studie mit 1 183 Patienten war das progressionsfreie Überleben, sekundäre Endpunkte Gesamtüberleben und Sicherheit. In eine Subgruppenanalyse wurden Daten von 639 jener 656 Patienten eingeschlossen, deren Tumoren keine KRAS-Mutation (Exon 2) hatten. Bei diesen 639 Teilnehmern wurde zusätzlich der Status von KRAS Exon 3 oder 4 und von NRAS Exon 2, 3 oder 4 *PRIME: Panitumumab Randomized Trial in Combination with Chemotherapy for Metastatic Colorectal Cancer to Determine Efficacy A 2136 (RAS-Mutationen) plus BRAF Exon 15 untersucht. 512 Probanden ohne RAS-Mutationen in den Biopsaten hatten unter PanitumumabFOLFOX ein progressionsfreies Überleben von 10,1 Monaten versus 7,9 Monate mit Chemotherapie allein (Hazard Ratio [HR] für Progression oder Tod unter Kombination 0,72; 95-%-Konfidenzintervall [KI] 0,58–0,90; p = 0,004). Das Gesamtüberleben betrug 26,0 Monate im Kombinationsarm und 20,2 Monate unter FOLFOX4 allein (HR für Tod 0,78; 95-%-KI modifiziert nach: NEJM 2013; 369: 1023–33 Anteil Überlebender (%) 90 0,62–0,99; p = 0,04). In der Subgruppe ohne RAS- und ohne BRAF-Mutationen betrug der Unterschied zwischen zusätzlicher Antikörpergabe und FOLFOX4 allein 7,4 Monate beim Gesamtüberleben. BRAF-Mutationen waren prognostisch ungünstig für das Überleben von Patienten ohne KRAS-Mutation (Exon 2) und mit NRAS-Mutationen (Exon 3). Fazit: Die Nutzen-Risiko-Relation der Kombination Panitumumab/ FOLFOX4 bei metastasiertem kolorektalem Karzinom wird optimiert, wenn Patienten mit RASMutationen im Tumor ausgeschlossen werden. Prof. Dr. med. Michael Geißler, Esslingen, kommentiert: „Bisher ist bei Patienten mit Option auf eine Anti-EGFR-Therapie der KRAS-Status getestet worden. Jetzt sollten die Tests obligatorisch um den NRAS-Status erweitert werden, um Patienten, bei denen ein Ansprechen erwartet werden kann, möglichst gut zu identifizieren.“ Dr. rer. nat. Nicola Siegmund-Schultze 1. Douillard J-Y, Oliner KS, Siena S, Taberno J, et al.: Panitumumab-FOLFOX4 treatment and RAS-mutations in colorectal cancer. NEJM 2013; 369: 1023–33. FRÜHGEBORENENRETINOPATHIE Frühe Vitrektomie bei aggressiver Erkrankung vorteilhaft Bei Kindern mit FrühgeborenenRetinopathie (ROP: retinopathy of prematurity) ist die Laserkoagulation des Augenhintergrundes die Methode der Wahl, um die Ausdehnung der pathologischen, durch die Sauerstoffatmung im Inkubator verursachten Netzhautveränderungen aufzuhalten und eine Netzhautablösung zu verhindern. Eine durch massive Proliferation von fibrovaskulärem Gewebe und durch schnel- les Erreichen des finalen ROP-Stadiums 5 (komplette Amotio retinae) gekennzeichnete Sonderform, die aggressive posteriore Frühgeborenen-Retinopathie (AP-ROP), lässt sich mit der Laserapplikation in der Regel nicht stoppen. Die Ergebnisse der vitreoretinalen Eingriffe nach durch AP-ROP verursachter Netzhautablösung waren enttäuschend. An der Augenklinik des japanischen Nationalen Zentrums für die Deutsches Ärzteblatt | Jg. 110 | Heft 45 | 8. November 2013 MEDIZINREPORT Gesundheit und Entwicklung von Kindern in Tokio wurde bei Frühgeborenen mit dieser Retinopathieform früher als üblich, nämlich bei ersten Zeichen für eine Traktionsamotio, vitrektomiert. Dabei wird gleichzeitig auch die Linse des betroffenen Auges entfernt, deren refraktive Funktion später Kontaktlinsen übernehmen. 103 Augen wurden vitrektomiert. Die Patienten hatten zum Operationszeitpunkt ein durchschnittliches postmenstruales Alter von 37 Wochen, waren durchschnittlich nach 24 Schwangerschaftswochen auf die Welt gekommen und wogen 706 Gramm. Bei 32 Patienten war im Laufe der Nachkontrolle eine Messung des Visus möglich; es wurden Sehschärfen zwischen 20/2 000 und 20/40 ermittelt. Immerhin fast 70 % dieser Augen hatten einen Visus von 20/250 oder besser. Vielleicht noch wichtiger für die visuelle Langzeitprognose ist die Frage, ob sich eine regelrechte Fovea – das für die Sehschärfe entscheidende Zentrum der Makula – ausbilden kann. Dies war bei all jenen Augen der Fall, bei denen operiert wurde, bevor die fibrovaskulären Veränderungen die Glaskörperbasis oder die Linsenoberfläche erreicht hatten. Fazit: Bei einer besonders aggressiven Form der ROP kann durch frühzeitige Vitrektomie bei einigen Patienten ein fast altersentsprechender Visus erreicht werden. Welchen Stellenwert die frühe Vitrektomie bei dieser Variante der Frühgeborenenretinopathie bekommen wird, wenn mehr Daten zu Alternativen wie der Anti-VEGF-Therapie (Injektion von Bevacizumab zum Beispiel) vorliegen, bleibe abzuwarten, so die Autoren. Dr. med. Ronald D. Gerste 1. Azuma N, et al.: Visual outcomes after early vitreous surgery for aggressive posterior retinopathy of prematurity. JAMA Ophthalmol 2013; 131: 1309–13. ABSTOSSUNG VON NIERENTRANSPLANTATEN C1q-bindende Antikörper lassen Abstoßungsrisiko gut abschätzen Abstoßungen von Organtransplantaten zu verhindern, ist ein wesentliches Ziel der Nachsorge von Patienten. Dabei wird die Immunantwort auf das Allotransplantat beobachtet durch die Suche nach HLA-Antikörpern, meist durch Festphasenassays wie die Luminex-Technologie: HLA-Antigene werden auf Mikropartikeln fixiert und die Bindung von Antikörpern aus dem Organempfängerserum über Fluoreszenzsignale nachgewiesen. Die Bewertung der Ergebnisse dieser sehr sensitiven MethoGRAFIK 1,0 0,8 0,6 0,4 grau hinterlegt: 95-%-Konfidenzintervalle 0,2 0,0 0 1 4 5 2 3 Jahre nach Transplantation Deutsches Ärzteblatt | Jg. 110 | Heft 45 | 8. November 2013 6 7 modifiziert nach: NEJM 2013 ; 369: 1215–26 Wahrscheinlichkeit des Transplantatüberlebens Überleben von Nierentransplantaten in Abhängigkeit von donorspezifischen Antikörpern (DSA) und C1qDSA-Status de kann schwierig sein, weil in positiven Seren eine Vielzahl von Spezifitäten nachgewiesen wird, ohne dass sich daraus erkennen ließe, welche Anti-HLA-Antikörper dem Transplantat schaden könnten und eine Anpassung der Abstoßungsprophylaxe zur Folge haben sollten. Deshalb wird versucht, das Monitoring durch eine funktionelle Differenzierung der Antikörper zu verbessern. Eine Forschergruppe hat in einer Population von 1 016 Nierenempfängern untersucht, ob das Auftreten von C1q-bindenden, donorspezifischen Antikörpern (C1qDSA) prognostische Bedeutung für das Auftreten von Abstoßungen hat (1). Die Bindung von Antikörpern an C1q ist der erste Schritt der klassischen Aktivierung der Komplementkaskade (C). Die Forscher verwendeten ebenfalls die LuminexTechnologie, allerdings mit der Erweiterung, dass die C1q-Bindung der DSA nachgewiesen wurde. Von allen Subgruppen fand sich bei Patienten mit C1qDSA binnen 5 Jahren das schlechteste Transplantatüberleben, nämlich 54 %. Dagegen funktionierten in der Gruppe der Patienten mit nichtkomplementbindenden DSA im selben Zeitraum 93 % der Nieren und in der Gruppe ohne DSA 94 % der Transplantate (p < 0,001 für beide Vergleiche). Komplementbindende DSA waren mit einem mehr als vierfach erhöhten Risiko für einen Transplantatverlust assoziiert (Hazard Ratio 4,78; 95-%-Konfidenzintervall 2,69–8,49), stärkeren Gewebeschäden mit ausgeprägter mikrovaskulärer Entzündung und Ablagerungen von C4d in den Kapillaren des Transplantats. Ein weiteres Ergebnis der Studie war, dass C1qDSA größere prognostische Bedeutung haben als C4dDSA, und die Integration des Parameters „C1qDSA“ in einen Score zur Abschätzung des Abstoßungsrisikos erhöhte signifikant dessen Vorhersagekraft. Fazit: Das Auftreten von C1q-bindenden, donorspezifischen Antikörpern bei Nierenempfängern ist mit einem stark erhöhten Abstoßungsrisiko assoziiert. Die Bedeutung für das Routinemonitoring müsse geprüft werden, heißt es im Kommentar (2). In Protokolle klinischer Studien sollten Tests auf C1qDSA aber künftig aufgenommen werden. Dr. rer. nat. Nicola Siegmund-Schultze 1. Loupy A, et al.: Complementbindung anti-HLA antibodies and kidney-allograft survival. NEJM 2013 ; 369: 1215–26. 2. Racusen LC, et al.: C1q-binding antibodies in kidney transplantation. NEJM 2013; 369: 1266–7. A 2137








