Erkrankungen des Magens
Werbung

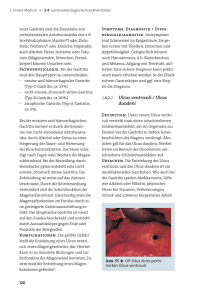
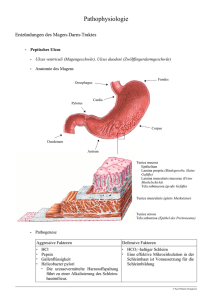
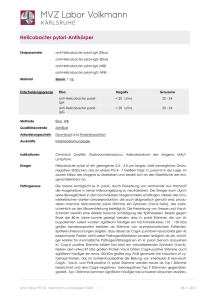
Erkrankungen des Magens 02.11.2012 Marko Lehmann Andreas Stallmach Lernziele Gastritis (akut/chronisch/Sonderformen) Ulkuskrankheit Gutartige Tumoren Malignome (Bestandteil des Onkologieblocks) Reizmagensyndrom Die Beschwerdesymptomatik erlaubt keine Differenzierung zwischen Ulkus, Magenfrühkarzinom oder Reizmagen ! > 4 Wochen bestehende oder rezidivierende Oberbauchbeschwerden müssen zu einer ENDOSKOPIE veranlassen! Reizmagen (funktionelle Dyspepsie) Beschwerden > 3 Monate ohne strukturelle oder biochemische Läsion Typische Symptome – epigastrischer Schmerz, Druck-, Völlegefühl, frühe Sättigung, Übelkeit/Brechreiz – Sodbrennen, geblähter Leib, Aufstoßen wechselnde Symptomkombination u. fluktuierende Intensität zunehmend bei psychischer Belastung 3 Typen (Rom II-Kriterien) – Dysmotilitäts-Typ / Ulkus-Typ / Reflux-Typ Reizmagen Pathomechanismus – viszerale Hyperalgesie, Motilitätsstörungen, autonome Neuropathie, Aerophagie Epidemiologie – Dyspepsie 20-30%, 50% gehen zum Arzt, – 50% der Beschwerden - funktionell – m=w Assoziierte Erkrankungen – Reizdarm, Kopf-/Rückenschmerzen, funktionelle Herzbeschwerden, Schlafstörung, psych. KH Reizmagen-Diagnostik u. Therapie Diagnostik (Ausschlußdiagnostik!) Anamnese/Klinische Untersuchung Gastroskopie + H.p.-Status Labor: BSG/CrP, BB, Fermente, Lipase, Kreatinin, UStatus Sonographie Abdomen / Koloskopieindikation großzügig „Umgebungsdiagnostik!“ Therapie - Aufklärung PPI-Versuch 4-6 Wochen Prokinetika (MCP, Domperidon) Antidepressiva Iberogast-Tr. , Dimeticon Psychotherapie/autogenes Training Gastritis Entzündliche Reaktion der Magenschleimhaut keine typische Klinik oder Endoskopie Diagnosestellung aus der Histologie ! Akute GastritisÄtiopathogenese – exogene Noxen Alkohol, reizende Speisen Medikamente (ASS/NSAR; Zytostatika) Verätzungen, Gallensäuren (v.a. nach MagenOp) – Stress Hypoxie (Trauma/Verbrennungen/Schock) perioperativ – lokale Schäden Magensonde, Radiatio – bakterielle Entzündungen H. pylori, toxinbild. Staphylokokken, Salmonellen Therapie Weglassen der Noxen passagere Nahrungskarenz oft keine spezifische Medikation nötig – Antazida/Protonenpumpenhemmer (PPI) – Antiemetika: Metoclopramid (MCP hexal®, Cerucal® 3x1 oder 3x30Tr.), Dimenhydrenat (Vomex A®) Prophylaxe mit PPI – bei streßbedingten Läsionen, NSAR, Chemother. Chronische Gastritis (alte Klassifikation - einfach - A/B/C-Gastritis) (v.a. nach Magen-Op mit Pylorusresektion) (Typ A) - Gastritis = Autoimmungastritis (5%) – chronisch-atrophische Corpusgastritis – deszendierende Ausbreitung von der Cardia – Autoantikörper PCA-Ak (=Parietal) -Zelle u. gegen Protonenpumpen (H+/K+-ATPase) 90% positiv, intrinsic factor Ak 70% positiv Folge: Hypo- bis Achlorhydrie u. Vit. B12-Mangel – aber Hypergastrinämie (normale Antrummukosa) Autoimmungastritis Klinik Achlorhydrie allein stumm Endoskopisch keine verlässlichen Zeichen (Atrophie -> durchscheinende Gefäße) Histologisch Mukosaatrophie intrinsic factor-Mangel Vitamin B12-Mangel perniziöse Anämie Therapie: Vit. B12-Gaben 1000µg parenteral Aufsättigung dann alle 8-12 Wochen Chronische H.p.-Gastritis Klinik – akute Infektion mit unspezifischer Dyspepsie – fast nie erfaßt/ Mehrzahl asymptomatisch – weiter Symptome abh. von Folgeerkrankungen Assoziierte Erkrankungen (bei ca. 15%) – Ulcus duodeni (10%) – Ulcus ventriculi (1%) – Magenkarzinom (1:3000, Präkanzerose) – MALT-Lymphom des Magens (1:40000) – Riesenfaltengastritis Chronische H.p.-Gastritis Diagnostik – Endoskopie mit Biopsien aus Antrum und Corpus – nichtinvasive H. pylori-Tests (C13Atemgas) Helicobacter pylori- Infektion Epidemiologie Übertragung fäkal-oral o. oral-oral Faustregel Prävalenz ~ Lebensalter Infektion im Kindesalter – akut dyspeptisches Krankheitsbild – Ausheilung oder chronische Gastritis ohne Therapie lebenslang persistierend Helicobacter pylori Verteilungsmuster der Gastritis Antrumgastritis • Gastritis beim Duodenalulkus Corpusgastritis • Gastritis beim Magenulkus Ulkus H. pylori befällt Regionen mit einer intestinalen Metaplasie; dies führt zu einer Entzündung (chronischen Duodenitis) und schließlich zum Duodenalulkus. Therapie wann? Nein, beim asymptomatischen Patienten umstritten bei funktioneller Dyspepsie ja bei Folgekrankheiten – symptomatische H.p.-Gastritis – chronisch-atrophische-Gastritis (korpusdomionante Form (Ca-Risiko) – Ulkuskrankheit – erhöhtes Karzinomrisiko (+ Familienanamnese/H.p.-Gastritis im Magenstumpf nach Teilresektion) – niedrigmalignes Malt-Lymphom – nach Resektion eines Frühkarzinoms auf Wunsch des Patienten Therapie wie ? Triple-Therapie „Italienische“ Tripel-Th. – PPI (2 x Standarddosis) + – Clarithromycin (2 x 250mg) – + Metronidazol (2 x 400mg) über 7 Tage „Französische“ Tripel Therapie – PPI (2 x Standarddosis) + – Clarithromycin (2 x 500mg) + – Amoxycillin (2 x 1000 mg) über 7 Tage Sonderformen der chronischen Gastritis Eosinophile Gastritis granulomatöse Gastritis – M. Crohn, Tbc, M. Whipple, Sarkoidose kollagene Gastritis (Einzelfall) Endoskopisches Bild Riesenfaltenmagen Faltendicke > 10 mm foveoläre Hyperplasie - Morbus Menetrier glanduläre Hyperplasie - Hypergastrinämie helicobacterassoz. Gastritis mit Riesenfalten Komplikationen - Diarrhoe, enterales Eiweißverlustsyndrom - erhöhtes Karzinomrisiko (2-15%) Differentialdiagnose (Endosono + Histologie) Lymphom/Magenszirrhus/Fundusvarizen Morbus Menetrier Ulcus ventriculi et duodeni Epidemiologie Inzidenz Ulcus ventriculi 50/100 000 E. pro Jahr Ulcus duodeni 150/100 000 E. pro Jahr insgesamt abnehmend m: w = 3:1 Ulc. duodeni / m = w Ulc. ventriculi Ulcus ventriculi et duodeni Erosion – Defekt der Mukosa, der Lamina muscularis mucosae nicht durchdringt Ulkus – umschriebener Substanzdefekt, der die Lamina muscul. mucosae durchdringt, meist tiefer Ätiopathogenese Helicobacter pylori – 95% U. duodeni / 70% d. U. ventriculi – U. duodeni -> H.p. besiedelte gastrale Metaplasie NSAR-/ASS-induzierte Ulzera – 4 faches Ulkusrisiko unter NSAR – hemmen protektive Prostaglandine – Glukokortikosteroide 1,1 x, aber mit NSAR 15 x erhöhtes Ulkusrisiko akutes Streßulkus (siehe Gastritis) selten Zollinger-Ellison-Syndrom, Hyperparathyreoidismus Ulkuskrankheit - Klinik Keine Diagnose aufgrund der Klinik ! (bis 1/3 asymptomatisch) körperliche Untersuchung: epigastrischer Druckschmerz Im Einzelfall typisch Ulcus ventriculi – Sofortschmerz nach Nahrungsaufnahme oder nahrungsunabhängige Schmerzen Ulcus duodeni – Spät-, Nacht- und Nüchternschmerz im Epigastrium – Besserung mit Nahrungsaufnahme Ulus duodeni und Ulcus ventriculi werden endoskopisch diagnostiziert (Sensitivität! Biopsien!) Röntgenologische Untersuchungen sind heute obsolet und nur speziellen Fragestellungen vorbehalten) Im Gegensatz zum Ulcus duodeni muß die Abheilung des Ulcus ventriculi nach 6-8 Wochen endoskopisch und bioptisch kontrolliert werden (incl. Biopsien auch aus der Ulcusnarbe). da bei U. ventr. immer Differentialdiagnose zum Magenkarzinom besteht. Ulcera duodeni sind nur in 0,035% maligne (Pankreaskarzinom, malignes Lymphom, Schleimhaut-MTS, primäres Duodenalkarzinom) und müssen deshalb nicht bioptiert werden Ulcus duodeni NSAR-induzierte Ulzera Ulkuskrankheit - Therapie H. pylori - Eradikation, – ohne Therapie - Rezidiv U. duodeni 80-90% U. ventriculi 50% Weglassen der Noxen – (NSAR, Rauchen, Streß) symptomatische Therapie – 1. Wahl - Protonenpumpenhemmer – 2. Wahl - H2-Rezeptorantagonisten (H2-Blocker) Ulkus - Komplikationen Blutung – 20%, gehäuft bei NSAR-/Streßulzera Penetration – z.B. in das Pancreas, Rückenschmerzen Perforation – akutes Abdomen, freie Luft subphrenisch - Op ! Stenose – narbige Magenausgangsstenose/Bulbusstenose Entleerungsstörung (Aufstoßen, Erbrechen) Forrest - Klassifikation Blutungsaktivität Rezidivblutung Forrest Ia Arteriell spritzend 90% Forrest Ib Sickernde Blutung 30% Forrest IIa Sichtbarer Gefäßstumpf 50-100% Forrest IIb Koagelbedecktes Ulkus 20% Forrest IIc Hämatinbelegtes Ulkus <5% Forrest III Fibrinbelegtes Ulkus <5% Gutartige Neubildungen Echte Neoplasien Epitheliale Tu. Tubuläres Adenom tubulopapilläres A. papilläres Adenom Pylorusdrüsenadenom Endokrine Tu. Karzinoid Mesenchymale Tu. Leiomyom (GIST) Hämangiom Lipom Fibrom Tumorähnliche Läsionen Nichtadenomatöse Heterotopien Sonderformen Polypen hyperplastischer P. heterotopes Pancreas foveoläre Hyperplasie Entzündl-fibrom. P. heterotopes Brunnerom Corpusdrüsenzysten juveniler P. Adenomatöser Magenpolyp Hyperplastischer Magenpolyp Gastrointestinale Stromatumoren (GIST) Vorzugsweise Magen u. Dünndarm Inzidenz 1-2: 100.000 Histologie: Spindelzell-70%, Epitheloidzell-20%, gemischt Immunhistochemie: c-Kit = CD 117: 95% positiv CD 34 60-70% positiv Malignes Potential Diagnostik: meist asymptomatisch, ÖGD, EUS, EUS-FNP Sono-Kriterien: echoarm, aber auch echoreiche Bezirke/Verkalkungen Prognose - abh. von Größe und Mitosezahl Therapie: 1. OP (<1cm im Magen evtl. beobachten) 2. Imatinib (GlivecR) = Tyrosinkinaseinhibitor) bei MTS 400-600 mg/Tag p.o. Was tun gegen dyspeptische Beschwerden nach Völlerei? Franke et al. J Gastrointestin Liver Dis 2008; 17: 27-31