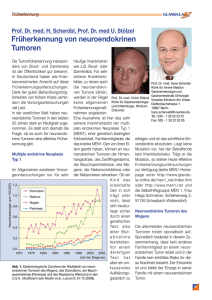
Publik - Netzwerk Neuroendokrine Tumoren (NeT)
Werbung

Netzwerk Neuroendokrine Tumoren (NeT) e.V. www.karzinoid.info www.neuroendokrine-tumoren.de Publik: Erstes Treffen der Regionalgruppe Lübeck Einladung zum 3. Treffen der „Regionalgruppe Rhein-Main” des Netzwerks NeT e. V. Engere Zusammenarbeit zwischen Netzwerk NeT e.V. Erlangen und Bundesorganisation Selbsthilfe NeuroEndokrine Tumoren e.V. Berlin Neue Patientenbroschüre: Mehr Wissen über Neuroendokrine Tumoren Behandlungszentren: Gründung der Arbeitsgruppe „Neuroendokrine Tumore” am Universitätsklinikum Kiel Biotherapie: Stellenwert und Fortschritte der Biotherapie bei (neuro-)endokrinen Tumoren des MagenDarmtraktes Veranstaltungen: Berichte vom 3. überregionalen Neuroendokrinen Tumor-Tag in Mainz Bericht über die Saarländisch-Pfälzische Internistengesellschaft Erfahrungsberichte: Eine Transarterielle Chemoembolisation – Erlebnisbericht eines Patienten Mit etwas Glück optimaler Verlauf – Leben 20 Jahre nach Operation eines neuroendokrinen Tumors 9-07 Aus dem Inhalt Publik Erstes Treffen der Regionalgruppe Lübeck 3 Einladung zum 3. Treffen der „Regionalgruppe Rhein-Main” des Netzwerks NeT e. V. 4 Engere Zusammenarbeit zwischen Netzwerk NeT e.V. Erlangen und Bundesorganisation Selbsthilfe NeuroEndokrine Tumoren e.V. Berlin 5 Netzwerk NeT wieder auf zahlreichen Kongressen vertreten 7 Neue Patientenbroschüre Mehr Wissen über Neuroendokrine Tumoren 6 8 Behandlungszentren Gründung der Arbeitsgruppe „Neuroendokrine Tumore” am Universtitätsklinikum Schleswig-Holstein 9 Biotherapie Stellenwert und Fortschritte der Biotherapie bei (neuro-)endokrinen Tumoren des Magen-Darmtraktes 16 11 Veranstaltungen 3. Überregionaler Neuroendokriner Tumor-Tag, 24.-26. Nov. 2006 in Mainz Außergewöhnliche Resonanz – Bericht vom 3. Überregionalen Neuroendokrinen Tumor-Tag vom 24.-26. November 2006 in Mainz 16 Neue Diagnoseverfahren bei neuroendokrinen Tumoren 20 Behandlungsmöglichkeiten bei Lebermetastasen von neuroendokrinen Tumoren – Operation, Lebertransplantation und andere Methoden aus internistischer Sicht 24 Neue und bewährte medikamentöse Therapieoptionen 27 Indikation, Planung und Durchführung der Radiopeptidtherapie mit 90Yttrium-DOTATOC 30 Erfolg mit kleinen Schnitten? –Minimal-invasive Chirurgie bei neuroendokrinen Tumoren 32 Behandlung jenseits der Schulmedizin – Über alternative und unterstützende Methoden 36 Das breite Spektrum der NET-Probleme 37 Renommierter Internisten-Kongress mit Kardinal Lehmann 39 20 30 Erfahrungsberichte Eine Transarterielle Chemoembolisation 40 Mit etwas Glück optimaler Verlauf – Leben 20 Jahre nach Operation eines neuroendokrinen Tumors 43 39 Editorial Liebe Patientinnen und Patienten, nun ist es endlich wieder soweit. Zeitgerecht zum Münchner NET-Tag möchten wir Ihnen die neue Ausgabe der GlandulaNeT präsentieren. In diesem Jahr haben sich zahlreiche Veränderungen eingestellt. Prof. Hensen hat die Herausgabe der GlandulaNeT an mich übergeben. Ich habe diese Aufgabe sehr gerne übernommen. Meine Haupttätigkeit an meinem neuen Wirkungsort in Berlin seit Mai dieses Jahres ist den Patientinnen und Patienten mit neuroendokrinen Tumoren gewidmet und zahlreichen damit verbundenen Aufgaben im klinischen und wissenschaftlichen Bereich. Unverändert ist es das Bestreben, über die vielfältigen Aktivitäten in Deutschland zu diesem Themengebiet zu berichten. Mittlerweile haben sich durch das Engagement einzelner Patientinnen und Patienten unter Beteiligung der sie betreuenden Ärzte neue Regionalgruppen gegründet. Nicht zuletzt bewirken auch die Veranstaltungen an verschiedenen Kliniken und die interdisziplinären Fortbildungen zu NET eine steigende Wahrnehmung dieser seltenen Krankheit und eine Verbesserung von deren Diagnostik und Behandlung. Das Jahr hat uns leider auch traurige Ereignisse beschert. Unser Vorstandsmitglied Frau Ingeborg Schäfer ist viel zu früh von uns gegangen. Sie hat durch unermüdlichen Einsatz vielen Patienten mit Ihrem Rat zur Seite gestanden, auf zahlreichen medizinischen Kongressen auf das Netzwerk aufmerksam gemacht und damit einen ganz wesentlichen Beitrag für das Netzwerk NeT geleistet. Sie wird gedanklich für uns stets mit dem Netzwerk verbunden bleiben. Durch den Einsatz der Vorstandsmitglieder des Netzwerks NeT und der Bundesorganisation Selbsthilfe NeuroEndokrine Tumoren e. V. mit Sitz in Berlin hat eine erste Annäherung beider Selbsthilfeorganisationen stattgefunden. Ziel ist die Bündelung von Aktivitäten. Wir berichten in dieser Ausgabe der GlandulaNeT über ein erstes Treffen beider Organisationen in Berlin. Gerne nehme ich Ihre Anregungen für die folgenden Ausgaben der GlandulaNeT entgegen. Die nächste Ausgabe ist für April 2008 geplant. Herzlichst Ihre PD Dr. Marianne Pavel Herausgeberin der GlandulaNeT Unsere neue Ansprechpartnerin im Netzwerk-Büro Seit dem 30. Juli dieses Jahres hat unser Netzwerk-Büro in Erlangen eine neue Mitarbeiterin: Frau Martina Friedl. Sie tritt damit die Nachfolge von Frau Hummel an, die sich beruflich neu orientiert hat. Frau Friedl sorgt nun für den reibungslosen Ablauf aller organisatorischen Angelegenheiten rund um das Netzwerk. Außerdem steht sie den Mitgliedern bei Fragen auch telefonisch zur Verfügung. Bitte beachten Sie: Die Bürozeiten haben sich etwas geändert. Martina Friedl Das Telefon ist nun Montag bis Donnerstag von 8 bis 12 Uhr besetzt. Unser neuer Redakteur Seit September diesen Jahres werden die Zeitschriften „GlandulaNeT“ und „Glandula“ von einem neuen Redakteur betreut: Herrn Christian Schulze Kalthoff. Er tritt die Nachfolge von Frau Brigitte Söllner an, der wir alles Gute für ihre weitere berufliche Laufbahn wünschen. Herr Schulze Kalthoff hat Politische Wissenschaften und Psychologie mit Schwerpunkt auf „Psychiatrische Pharmakologie“ studiert. Christian Schulze Kalthoff Als Journalist kann er auf vielfältige Tätigkeiten bei Tageszeitungen, Magazinen und neuen Medien zurückblicken. Dabei hat er auch häufig medizinische Themen bearbeitet. „Die große Herausforderung bei meiner neuen Aufgabe sehe ich darin, komplexe medizinische Themen verständlich und spannend darzustellen“, so der 38jährige. Unser neuer Redakteur ist stets offen für Anregungen, Informationen sowie Themen- und Verbesserungsvorschläge. Sie erreichen ihn per Post unter der Adresse des Netzwerk-Büros (Netzwerk Neuroendokrine Tumoren e.V., z.Hd. Herrn Christian Schulze Kalthoff, Waldstraße 34, 91054 Erlangen) oder per E-Mail: [email protected] Moderate Anpassung des jährlichen Mitgliedsbeitrages Sie wissen es selbst: Fast alles wird im Lauf der Jahre teurer. Auch wir vom Netzwerk bleiben leider von Preiserhöhungen für Mieten, Materialien, Gehälter etc. nicht verschont. Gleichzeitig deuten sich Einbußen bei den Zuschüssen von Firmen und Krankenkassen an. Außerdem wollen wir als Selbsthilfegruppe im Dienste der Patienten natürlich so weit wie möglich unabhängig bleiben. Der Beitrag lag nun lange Zeit bei Euro 15,-, was im Vergleich zu ähnlichen Vereinen extrem niedrig ist. Auf der Mitgliederversammlung des Netzwerks für Hypophysen- und Nebennierenerkrankungen e.V. wurde mit großer Mehrheit eine moderate Erhöhung auf Euro 20,- ab Januar 2008 beschlossen. Dies gilt ebenfalls für die Mitglieder des Netzwerks Neuroendokrine Tumoren e.V. Natürlich ist es uns bewusst, dass wir auch sozial schwache Mitglieder haben, für die selbst eine Erhöhung um Euro 5,- schmerzhaft ist. Wenn Sie zu dieser Gruppe gehören, können Sie sich mit einem formlosen schriftlichen Antrag von der Erhöhung befreien lassen. Termine Treffen der Regionalgruppe München Bitte merken Sie sich die folgenden Termine vor: •Donnerstag, 24.04.2008 •Donnerstag, 16.10.2008 Beginn ist jeweils 19.00 Uhr. Veranstaltungsort: Klinikum der Universität München Großhadern, Marchioninistraße 15, 81377 München, Konferenzraum 1 (1. Stock bis FG, dann bei FG links in den Direktionstrakt) Ansprechpartner: Herr Blas, Dr. Edgar Wittmann, PD Dr. Christoph Auernhammer Publik Erstes Treffen der Regionalgruppe Lübeck Am Samstag, den 27. Januar 2007, hatte die neugegründete Lübecker Regionalgruppe ins “HAUS DER SENIOREN” in Bad Schwartau eingeladen. Insgesamt 13 Betroffene und deren Angehörige aus dem Raum Lübeck, südliches Ostholstein und aus dem Westen des Landes, aus Heide, waren erschienen. Alle Teilnehmerinnen und Teilnehmer betonten in der Aussprache über ihre Krankheiten und Therapien, daß eine Selbsthilfegruppe von großem Nutzen sei. Besonders wichtig seien auch die sich aufbauenden Kontakte zwischen den Betroffenen. Für medizinische Fragen stand die betreuende Ärztin Frau Dr. Nehara Begum von der Chirurgie der UniKlinik-Lübeck zur Verfügung. Herr Schmid, Frau Spiekermann und Herr Dr. phil.Klopsch Hervorgehoben sei noch, daß die seltene Krankheit MEN-1 bei einer Anwesenden bestand. Gerade auch von dieser Krankheit Betroffene werden um Kontaktaufnahme gebeten. Auch Neuerkrankte an neuroendokrinen Tumoren mögen mit uns Kontakt aufnehmen. Infos über: Frau Spiekermann, Tel.: 0451 - 28 14 56 Herrn Schmid, Tel.: 0451 - 2 79 22 Herrn Dr. phil. Klopsch Tel.: 04504 - 56 24 Termine Nächstes Treffen der Regionalgruppe Lübeck Termine der Regionalgruppe Erlangen Am Samstag, den 08.12.2007, von 15:00 Uhr – 18:00 Uhr findet unser nächstes Treffen der Selbsthilfegruppe Lübeck im „Haus der Senioren”, Eutiner Straße 4b in 23611 Bad Schwartau, statt. An diesem Tag stellt sich ein Homöopath vor. Frau Dr. Begum hält einen kleinen Vortrag und beantwortet Fragen der Anwesenden. Wir laden Sie herzlich ein, an unseren Patiententreffen in Erlangen teilzunehmen. Bitte merken Sie sich die folgenden Termine vor: In einer vorweihnachtlichen Atmosphäre, bei Kaffee und Kuchen, lassen wir unser letztes Treffen in diesem Jahr ausklingen. Auskünfte erteilen: Frau Spiekermann Tel: 0451 - 28 14 56 Herr Schmid Tel: 0451 - 2 79 22 Herr Dr. phil. Klopsch Tel: 04504 - 56 24 •Donnerstag, 20.03.2008 •Donnerstag, 19.06.2008 •Donnerstag, 16.10.2008 •Donnerstag, 19.03.2009 •Donnerstag, 18.06.2009 •Donnerstag, 15.10.2009 Beginn ist jeweils 18.00 Uhr. Veranstaltungsort: Nichtopera­tives Zentrum der Universitätsklinik Erlangen, Ulmenweg 18. Den Besprechungsraum können Sie an der Information erfragen. Da Terminänderungen nicht ausgeschlossen sind, wenden Sie sich bitte eine Woche vorher an das Netzwerk-Büro. Wir freuen uns auf Ihr Kommen H.-D. Allmendinger, Hemhofen Publik Einladung zum 3. Treffen der „Regionalgruppe Rhein-Main“ des Netzwerks NeT e.V. Donnerstag, 22. November 17:30 – 19:30 Uhr, Mainz Sehr geehrte Netzwerk-Mitglieder, nach den überaus erfolgreichen ersten beiden Treffen der „Regionalgruppe Rhein-Main“ des Netzwerks NeT e.V., welches auf sehr reges Interesse gestoßen ist, möchten wir Sie gerne zum 3. gemeinsamen Treffen am Donnerstag, den 22. November 2007, von 17:30 – 19:30 Uhr im Hilton Hotel Mainz/Goldsaal einladen. Aus terminlichen Gründen mussten wir den eigentlich vorgesehenen Termin um eine Woche vorziehen, da wir Sie gerne zu einer gemeinsamen Informationsveranstaltung des Interdisziplinären Endokrinen- und Neuroendokrinen Tumorforums (IENET) des Klinikums der JohannesGutenberg-Universität Mainz einladen möchten. Hier werden alle Vertreter des Zentrums (Internisten, Chirurgen, Radiologen, Strahlentherapeuten und Nuklearmediziner) aus ihrem Bereich über aktuelle diagnostische und therapeutische Möglichkeiten bei der Behandlung neuroendokriner Tumoren berichten und Ihnen wiederum ausreichend Gelegenheit für Fragen und eine interaktive Diskussion geben. Über Ihr zahlreiches Kommen würden wir uns freuen. Herzlich sind natürlich auch alle anderen interessierten Personen bei der Informationsveranstaltung willkommen. Eine Anmeldung ist nicht erforderlich. Ebenso fällt keine Teilnahmegebühr an. Das Programm wird den Mitgliedern der Regionalgruppe mit der Post zugesandt. Interessierte können dies gerne auch unter unten angegebener Kontaktadresse anfordern. weiteren Patienten aus der Region und dem Patientenvertreter der Regionalgruppe, Herrn Günther Nockemann, können Sie wie üblich bei der Netzwerk-Geschäftsstelle erfragen: Als Ansprechpartner bei evtl. Rückfragen stehen Ihnen wie gewohnt von ärztlicher Seite Herr Prof. Dr. med. Matthias M. Weber und Herr Dr. med. Christian Fottner gerne zur Verfügung. Kontaktadressen von Univ.-Prof. Dr. med. M. M. Weber Dr. med. C. Fottner Schwerpunkt Endokrinologie und Stoffwechselerkrankungen I. Medizinische Klinik und Poliklinik Klinikum der Johannes Gutenberg Netzwerk NeT e. V. Waldstraße 34 91054 Erlangen Tel. : 09131/81 50 46 Wir freuen uns auf Ihr zahlreiches Kommen! Mit freundlichen Grüßen, Liebe Netzwerk-Mitglieder, bereits seit mehreren Jahren bekommt jedes neue Mitglied zusammen mit seinem Begrüßungsschreiben einen Fragebogen. Leider wurde er bislang nur von wenigen ausgefüllt. Die Informationen der Fragebögen sind allerdings für den internen Gebrauch und die Arbeit des Netzwerks von großer Bedeutung. Betroffene Patienten können auch, natürlich streng anonym, in Studien einbezogen werden. Selbstverständlich werden alle Daten absolut vertraulich behandelt. Sollten Sie Ihren Fragebogen nicht oder nicht mehr haben, können Sie ihn ganz problemlos bei uns anfordern. Ein kurzer Anruf bei der Geschäftsstelle genügt. Telefonnummer: 09131-815046. Adresse für schriftliche Anforderung: Netzwerk Hypophysenund Nebennierenerkrankungen e.V., Waldstraße 34, 91054 Erlangen Publik Engere Zusammenarbeit zwischen Netzwerk NeT e.V. Erlangen und Bundesorganisation Selbsthilfe NeuroEndokrine Tumoren e.V. Berlin Treffen von Vereinsvertretern in Berlin am 15. Aug. 2007 Netzwerk NeT e.V. Erlangen und BS-NET e.V. Berlin sind beide Patientenorganisationen, die auf die Vermittlung von Informationen und die Beratung von Betroffenen und Ärzten ausgerichtet sind. Ziel des Treffens in Berlins war es deshalb, die Möglichkeiten einer intensiveren Zusammenarbeit – bis hin zu einer eventuellen Verschmelzung der beiden Vereine – zu diskutieren und nächste Schritte vorzubereiten. Nachdem bereits in der ersten Jahreshälfte 2007 zwischen den Vorstandvorsitzenden beider Vereine, Herrn Prof. Dr. Johannes Hensen (Netzwerk NeT e.V.) und Herrn Prof. Dr. Rudolf Arnold (BS-NET e.V.) sowie weiteren Vertretern der BS-NET e.V., Gespräche zur künftigen Zusammenarbeit der Vereine stattgefunden hatten, sollte nun ein vertiefter Austausch erfolgen. Hierzu trafen sich am 15. August 2007 in Berlin die Netzwerk-NeTe.V.-Vorstandsmitglieder Frau PD Dr. Marianne Pavel, Frau Rosemarie Oehme, Herr Martin Michael sowie Herr Dr. Edgar Wittmann mit den BS-NET-e.V.-Vorstandsmitgliedern Frau Inge Engel und Herr Benjamin Aydin sowie den Regionalgruppenleitern Frau Regina Hanack und Herrn Wolfgang Rösch. Zu Beginn des Treffens wurden zunächst der Aufbau und die Aktivitäten der beiden Vereine von den jeweiligen Vertretern detailliert dargestellt. Die Bundesorganisation Selbsthilfe NET e.V. wurde im Mai 2001 gegründet und hat derzeit 270 Mitglieder. Hauptaktivitäten sind die Öffentlichkeitsarbeit mit intensiver Direktberatung sowie die Information der Mitglieder über Rundbriefe. Daneben werden in Zusammenarbeit mit der Charité in Berlin Patiententage organisiert und Mitglieder und Betroffene in vier Regionalgruppen (Berlin-Brandenburg, Minden, Dresden, Köln) betreut. Das Netzwerk NeT e.V. existiert im Rahmen des Netzwerks Hypophysen- und Nebennierenerkrankungen seit Januar 2000, als eigenständiger Verein seit 2005, und verfügt derzeit über rund 300 Mitglieder. Schwerpunkte der Arbeit sind die Förderung des Austausches unter Betroffenen, sowie zwischen Patienten Diskussion mit den Vertretern des BS-NeT e.V. Publik und Ärzten. Dies wird durch die Bereitstellung von entsprechendem Informationsmaterial, die Beteiligung an ärztlichen Kongressen und der Veranstaltung eines jährlichen überregionalen NET-Patiententages unterstützt. Eine besondere Rolle spielt die GLANDULANeT, die Zeitschrift des Netzwerks, die aktuelle Therapiekonzepte und Forschungsansätze vorstellt und als Plattform für Erfahrungsberichte dient. Daneben stehen fünf Regionalgruppen (Erlangen, München, Regensburg, Mainz, Lübeck) für den unmittelbaren Kontakt von Betroffenen zur Verfügung. Vor dem Hintergrund der offensichtlich weitgehend gleich gerichteten Zielsetzungen beider Vereine wurden daraufhin Möglichkeiten einer Intensivierung der Zusammenarbeit diskutiert. Diese können z.B. in Form des vermehrten Austausches von Informationsmaterialien, in der gemeinsamen Gestaltung einer Ausgabe der GLANDULANeT-Zeitschrift (mit Beiträgen aus beiden Vereinen), oder in der gemeinsamen Vorbereitung und Durchführung von Patientenveranstaltungen bestehen. Daneben käme eine Zusam- Frau PD Dr. Pavel und Herr Dr. Wittmann präsentierten die Aktivitäten des Netzwerk NeT e.V. menarbeit bei den Regionalgruppen in Frage, indem etwa zur Gründung neuer Regionalgruppen die Mitglieder beider Vereine eingeladen werden können. Es wurde deshalb beschlossen, diese Felder der Kooperation weiter zu konkretisieren und eine entsprechende Zusammenarbeit vorzubereiten. Darüber hinaus wurde diskutiert, inwieweit eine eventuelle Verschmelzung der beiden Vereine anzustreben ist, und welche Vorteile und Konsequenzen sich hieraus ergeben könnten. Dies betrifft z.B. die Bildung eines gemeinsamen wissenschaftlichen Beirats, aber auch formale Aspekte wie die Erarbeitung einer gemeinsamen Satzung oder organisatorische Themen wie die gemeinsame Nutzung von Geschäftsstellen. Zu diesen weitergehenden Themen ist das Votum der jeweiligen Mitgliederversammlungen notwendig. Für das Netzwerk NeT e.V. wird dies auf der Mitgliederversammlung Anfang November 2007 geschehen. E. W. Nachruf auf Frau Ingeborg Schäfer Mit großer Trauer mussten wir am 13.3.2007 von unserem Vorstandsmitglied Frau Ingeborg Schäfer Abschied nehmen. Seit der Gründung des eigenständigen Netzwerkes Neuroendokrine Tumoren (NeT) gehörte Frau Schäfer dem Vorstand an. In ihrem Wirken und ihrem Einsatz war sie von Anfang an sehr aktiv. Sie besuchte viele medizinische Kongresse und machte mit Informationsmaterial auf diese seltene Krankheit aufmerksam. Ihr Engagement bewirkte einen beachtlichen Zuwachs an Mitgliedern. Als Ansprechpartnerin hat sie jederzeit ihre eigenen Erfahrungen weitergegeben und anderen Betroffenen Mut gemacht, mit ihrer Erkrankung zu leben. Wir vermissen Frau Schäfer sehr und werden ihr stets ein ehrendes Gedenken bewahren. Rosemarie Oehme für den Vorstand des Netzwerk NeT Netzwerk NeT wieder auf zahlreichen Medizin-Kongressen vertreten Durch die Teilnahme des Netzwerks NeT an diesen Veranstaltungen bieten sich vielfältige Möglichkeiten, die Unterstützung der Patienten und den Kontakt zu den Ärzten zu verbessern. Das Interesse an unserem Verein, den verteilten Informationsbroschüren und der GlandulaNeT ist dabei immer sehr groß. Besonders geschätzt wird sowohl von Patienten wie auch von Ärzten, dass hier direkt von Betroffenen kompetent Auskunft über die Erkrankung gegeben wird. Frau Schäfer im Gespräch mit Prof. Th. Schneider, Chefarzt der Med. Klinik 2, Klinikum Fürth. Bis zum Februar 2007 setzte sich unser Vorstandsmitglied Frau Ingeborg Schäfer auch auf medizinischen Kongressen unermüdlich für das Netzwerk NeT ein. So wurde unser Verein von Frau Schäfer, unterstützt von ihrem Ehemann, im Jahr 2006 bis Anfang 2007 auf zahlreichen Kongressen und vertreten. Wir verweisen auf die früheren Ausgaben der GlandulaNeT. Ergänzend seien hier genannt: • 61. Jahrestagung der Deutschen Gesellschaft für Verdauungs- und Stoffwechselkrankheiten (DGVS), 13.-16.9.2006 Frau Schäfer am AdP-Infostand beim Symposium „Pankreaskarzinom 2006” in München. • 51. Jahreskongress der Saarländischen-Pfälzischen Internistengesellschaft e. V., Saalbau, Neustadt a. d. Weinstraße 22.-24.2.2007 Nun wird diese Aufgabe von Herrn Dr. Edgar Wittmann wahrgenommen, der sich auch auf vielen anderen Feldern für das Netzwerk engagiert. Im Laufe des Jahres 2007 hat er, zusammen mit seiner Frau, den Infostand des Netzwerk NeT bei folgenden Kongressen betreut: • 51. Symposium der Deutschen Gesellschaft für Endokrinologie, Salzburg 07.-10.3.2007 Beim 50. Symposium der DGE, März 2006 in Essen, besuchte Professor Hensen (links) in einer Vortragspause Frau Schäfer und ihren Mann (Mitte), der sie unterstütze, am NeT-Infostand. • Neuroendokrine Tumoren des GastroEnteroPankreatischen Systems: Diagnostik und Therapie 2007–Standards und Ausblick, Veranstaltung des Interdisziplinären Tumorkolloquiums Neuroendokrine Tumoren, Klinikum München-Großhadern, 28.3.2007 • 113. Kongress der Deutschen Gesellschaft für Innere Medizin (DGIM) Wiesbaden 14.-18.4.2007 • Aktuelle Möglichkeiten der Krebsbehandlung, Informationstag für Patienten und Angehörige, Veranstalter: lebensmut e.V., Klinikum MünchenGroß­hadern, 15.9.2007 E. W. Beim DGIM-Kongress in Wiesbaden besuchte Herr Prof. Dr. Hensen zusammen mit seiner Frau auch den Infostand des Netzwerk NeT, der von Herrn Dr. Wittmann und seiner Frau betreut wurde. Publik Mehr Wissen über Neuroendokrine Tumoren Neue Patientenbroschüre „Neuroendokrine Tumoren“ und Internetseite „www.leben-mit-net.de“ Neue Informationsmöglichkeiten stehen seit kurzem Patienten mit neuroendokrinen Tumoren (NET) zur Verfügung. Die neue Patientenbroschüre „Neuroendokrine Tumoren“, die von Herrn Professor R. Arnold inhaltlich völlig überarbeitet und aktualisiert wurde, wird von Novartis Oncology in Zusammenarbeit mit dem Netzwerk NeT e.V., der Bundesorganisation Selbsthilfe NET e.V., der Arbeitsgemeinschaft NET der Deutschen Gesellschaft für Endokrinologie und Tyco Healthcare herausgegeben. über Novartis Pharma GmbH, GE Oncology, Roonstr 25, 90429 Nürnberg angefordert werden. Außerdem finden Sie auf unserer Homepage (www.neuroendokrine-tumoren.de) eine frei zugängliche PDF-Version. Seit kurzem existiert auch ein Internet-Angebot für Patienten mit NET, das von Lifeline – einem der größten Medizinportal-Anbieter – in Kooperation mit Novartis Oncology Die neue Patientenbroschüre enthält jetzt noch mehr ausführliche Informationen zum Theme NeT. Der 80-seitige, reich bebilderte Ratgeber gibt einen Überblick zu Art und Häufigkeit der verschiedenen Tumorformen und den damit verbundenen Beschwerden. Auch seltene Formen werden erläutert. Ein Schwerpunkt wird auf die Diagnostik und Behandlungsmöglichkeiten von NET gelegt. Abgerundet wird das Heft mit einem Patienteninterview, Ausschnitten aus interessanten, bereits in der GlandulaNeT veröffentlichten Erfahrungsberichten und einer Sammlung von Internetund Kontakt-Adressen. Da sich die Broschüre an Patienten richtet, wurde Wert auf eine verständliche Sprache gelegt. Fachbegriffe werden im Text erklärt und können alphabetisch im ausführlichen Glossar nachgeschlagen werden. Alles in allem ein empfehlenswerter Ratgeber, der die wichtigsten Infos in kompakter Aufbereitung enthält. Diese Broschüre kann kostenlos Thematisch zur Broschüre passend wurde von der Fa. Novartis ebenfalls die neue Website „www.leben-mit-net” eingerichtet. bereitgestellt wird. Unter der Adresse www.leben-mit-net.de werden vielfältige Informationen zur Erkrankung, Diagnose und Therapie, Erfahrungsberichte sowie informative Links angeboten. Inhaltlich orientiert sich www.leben-mit-net.de an der Patientenbroschüre „Neuroendokrine Tumoren“, die ebenfalls kosten- los auf der Internetseite als pdf-Version heruntergeladen werden kann. In Kürze wird auch ein ärztlicher Expertenrat aktiv sein, an den sich Patienten mit Fragen wenden können. Christian Schulze Kalthoff Behandlungszentren Hilfe für die „maßgeschneiderte Therapie” Gründung der Arbeitsgruppe „Neuroendokrine Tumore” am Universitätsklinikum Schleswig-Holstein/Campus Kiel Prof. Dr. med. G. Klöppel Direktor des Instituts für Pathologie und Pathologische Anatomie Priv.-Doz. Dr. med. H.-J. Klomp Geschäftsführender Oberarzt der Klinik für allgemeine Chirurgie und Thoraxchirurgie Fachübergreifender Ansatz – Auch „Nichtstun” kann sinnvoll sein Ein weiteres NET-Zentrum soll die Hilfsmöglichkeiten für betroffene Patienten bereichern. Am 21.6.2006 wurde am Universitätsklinikum Schleswig-Holstein/Campus Kiel die Arbeitsgruppe „Neuroendokrine Tumore” (AG-NET) gegründet. Das Universitätsklinikum Schleswig-Holstein greift damit eine Initiative der Deutschen Gesellschaft für Endokrinologie auf, welche zur Gründung des deutschen Registers für Neuroendokrine Gastrointestinale Tumore (NET-Register) in Berlin geführt hat. Der Vorstand des NET-Registers koordiniert die Tätigkeiten der inzwischen bundesweit recht zahlreichen NET-Zentren. Die AG-NET ist Mitglied des deutschen NET-Registers. Hintergrund dieser Bemühungen ist das Bestreben, die Versorgung be- Dr. med U. Lützen Stellv. Direktor der Klinik für Nuklearmedizin troffener Patienten zu verbessern. Im Gegensatz zu häufigen Erkrankungen, wie Diabetes mellitus oder Bluthochdruck muss man davon ausgehen, dass die Kenntnisse über die seltenen neuroendokrinen Tumoren außerhalb spezialisierter Zentren oftmals nicht ausreichend sind. Solche Zentren ermöglichen auch einen interdisziplinären Ansatz, d. h. dass sich Ärzte aus verschiedenen Fachgebieten mit den Befunden des Patienten beschäftigen, um eine für ihn „maßgeschneiderte” Therapie zu ermöglichen. So nahe liegend ein solcher interdisziplinärer, also fächerübergreifender Ansatz auch ist – er kann leicht scheitern, wenn Gespräche nicht in bestimmte Strukturen eingebunden sind. Als Patient sollte man wissen: Jeder Facharzt, der mit einem seltenen, möglicherweise unterschiedlich behandelbaren Krankheitsbild konfrontiert wird, wird spontan die Prof. Dr. med. H. Mönig Stellv. Direktor der Klinik für Allgemeine Innere Medizin eigene Behandlungsmethode in den Vordergrund stellen. Dies ist verständlich und ergibt sich schon aus der einfachen Tatsache, dass er diese Therapie eben genau kennt. Mit den anderen Behandlungsmöglichkeiten ist er hingegen weniger vertraut. Gerade bei neuroendokrinen Tumoren ist es aber unbedingt erforderlich, dass derjenige, der einen Patienten vorrangig behandelt, „über den Tellerrand schaut” und das Gespräch mit den Kollegen der benachbarten Fachgebiete sucht. Die beste Therapie kann unter Umständen auch einmal den Verzicht auf eine Therapie bedeuten. Das ist vor allem dann der Fall, wenn der erwartete Verlauf der Erkrankung so günstig ist, dass man befürchten muss, durch eingreifende Maßnahmen mehr zu schaden als zu nutzen. Ein solcher Behandlungsverzicht erfordert natürlich neben einem umfangreichen Wissen auf Behandlungszentren diesem Fachgebiet eine besonders intensive Auseinandersetzung mit den Vorstellungen, Wünschen und Ängsten des Patienten oder der Patientin. Leider wird nur allzu oft aus der Erwartung heraus, dass der Patient ein „Nichtstun” nicht akzeptieren werde, diese Möglichkeit gar nicht in Betracht gezogen. Und dies, selbst wenn sie nach der aktuellen wissenschaftlichen Erkenntnislage durchaus angebracht und im Interesse des Patienten Abb. 1: Ablaufschema des sog. „NET-Konsils” wäre. Sinn und Zweck der Gründung der AG-NET am UK S-H/ Falls gewünscht, wird die weitere Campus Kiel war es somit, diesen Betreuung inklusive Meldung des interdisziplinären Ansatz nicht mehr Patienten an das NET-Register von dem Zufall zu überlassen, sondern der AG-NET übernommen. Der ersdie Strukturen dafür fest zu etablie- te Schritt ist immer, dass eine mögren. Die ersten Erfahrungen mit die- lichst genaue pathologisch-anatosem Vorhaben sind außerordentlich mische Zuordnung erfolgt. Unter positiv. pathologischer Anatomie versteht Wir haben dafür die Konstruktion man die Lehre von krankhaften des sog. „NET-Konsils” geschaffen. Veränderungen im Körper. Dabei Es funktioniert folgendermaßen (sie- sind wir in Kiel in der glücklichen he Abb. 1): Lage, mit Herrn Prof. Klöppel und Wer immer auf dem Campus mit seiner Arbeitsgruppe eine intereinem neuroendokrinen Tumor national anerkannte Spitzenpathokonfrontiert wird, ist aufgefordert, logie zur Seite zu haben, welche diesen Patienten im NET-Konsil vor- sich als aktiver Teil der AG-NET zustellen. Er braucht dafür nur eine begreift. einfach zu merkende Telefonnum- Als zusätzliche Aufgabe hat sich die mer zu wählen (597-5000) und die AG-NET die regelmäßige FortbilPatientendaten anzugeben. Diese dung zum Thema neuroendokrine Angaben werden dann an einen Tumore gestellt; eine erste FortMitarbeiter der AG-NET weitergelei- bildung erfolgte am 11.1.2007 im tet, der die anfragende Klinik berät. Rahmen des Qualitätszirkels OnEr sorgt dann dafür, dass der Fall kologie (Krebswissenschaft) und im Rahmen eines interdisziplinären wurde mit großem Interesse auch Gesprächs vorgestellt und eine ent- seitens der niedergelassenen Kolsprechende Empfehlung formuliert leginnen und Kollegen aufgenomwird. men. 10 Derzeit sind folgende Institutionen und Kliniken an der AG-NET beteiligt: • Klinik für Allgemeine Innere Medizin • Klinik für Allgemeine Chirurgie und Thoraxchirurgie • Institut für Allgemeine Pathologie und Pathologische Anatomie • Klinik für Nuklearmedizin Für Fragen auch aus dem überregionalen Raum sind wir immer ansprechbar. Kontaktadresse: Prof. Dr. H. Mönig UKS-H/Campus Kiel Klinik für Allgemeine Innere Medizin Schittenhelmstr. 12 24105 Kiel Tel.: 0431-597-1393 Fax: 0431-597-1302 E-Mail: [email protected] Biotherapie Stellenwert und Fortschritte der Biotherapie bei (neuro-)endokrinen Tumoren des Magen-Darmtraktes Einleitung Neuroendokrine Tumore (NET) sind seltene und überwiegend geringgradig bösartige Neubildungen. Sie können im menschlichen Organismus überall dort auftreten, wo auch normale, d.h. im Wachstumsverhalten nicht veränderte, endokrine Zellen vorkommen. Der Begriff „neuroendokrin” bezieht sich auf biologische Ähnlichkeiten der hormonabgebenden endokrinen Zellen mit Nervenzellen (=Neuronen), die statt der Hormone sog. Neurotransmitter an ihre Umgebung abgeben. Beide, Hormone wie Neurotransmitter, dienen im gesunden Organismus als Botenstoffe der Kommunikation von Zellen untereinander. Im Gegensatz zu Neuronen, die überwiegend mit benachbarten Zellen kommunizieren, geben endokrine Zellen ihre Hormone allerdings an den Blutkreislauf ab, um so Zielzellen im gesamten Körper erreichen zu können. Endokrine Zellen kommen am häufigsten aber nicht in kompakten Organen wie z.B. der Schilddrüse vor, sondern sie liegen eingestreut zwischen anderen Oberflächenzellen (Epithelien) vor allem des Bronchialund des Magen-Darmtraktes. Dies wird als das diffuse endokrine System bezeichnet. Die Vielfalt der von den Zellen des diffusen endokrinen Systems abgegebenen Botenstoffe (Hormone und sog. biogene Amine als Entsprechung der Neurotransmitter) lässt eine Unterteilung in verschiedenen Untergruppen zu, die durch das jeweilige Sekretionsprodukt charakterisiert werden und mit verschiedenen Buchstaben be- zeichnet werden (z.B. A-Zellen, BZellen, EC-Zellen usw.). Ein besonders typisches Merkmal der von diesen Zellen abgeleiteten neuroendokrinen Tumore (NET) ist die zumindest teilweise erhaltene Fähigkeit zur Hormonsynthese und -abgabe an den Kreislauf. Mindestens 75% der NET befinden sich im Magen-Darmtrakt, v.a. in der Bauchspeicheldrüse (Pankreas; ca. 20-30%) und im Dünndarm (Jejunum und Ileum: ca. 30%); sie stehen im Fokus des Artikels. Im Gegensatz zur normalen Situation, in der die endokrinen Zellen ihr Hormon jedoch nur unter bestimmten, streng regulierten und kontrollierten Bedingungen abgeben, ist dies bei den Tumorzellen jedoch meist nicht mehr der Fall, was zu einer unkontrollierten Hormonfreisetzung führt. In Abhängigkeit vom Ausmaß des abgegebenen Hormonüberschusses, der Abbaukapazität derselben und dem Ausmaß an subjektiv bemerkbaren Beschwerden führt dies bei etwa 30 bis 50% der Patienten mit einem NET zu einem bemerkbaren Beschwerdebild: dem sog. hormonellen Hypersekretionssyndrom bzw. dem klinischen Bild der Funktionalität. Dabei können sehr verschiedene Hypersekretionssyndrome bzw. funktionelle Syndrome voneinander unterschieden werden (siehe Tabelle1). Bei einem Teil der NET können die Tumorzellen aber das hergestellte Hormon nicht mehr abgeben und Syndrom/Tumor abgesonderte Hormone Klinik Karzinoid-Syndrom Serotonin Flush (85%) Durchfälle (75%) Karzinoidherzerkrankung (25%) Bronchospasmus (<10%) Zollinger-EllisonSyndrom (ZES)/ Gastrinom Gastrin wiederkehrende Magen-Darm-Geschwüre (v.a. mehrfach an atypischen Orten) Durchfälle Insulinom Insulin Whipple´sche Trias (Unterzuckerung) Nüchternhypoglykämie (Unterzuckerung nach ca. fünfstündigem Nahrungsverzicht) Neuroglykopenie mit Symptomen adrenerger Gegenregulation (vielfältige Störungen von Gehirnfunktionen) Reversibilität nach Glukosegabe Glukagonom Glukagon Diabetes mellitus nekrolytisches migratorisches Erythem (Hautausschlag) Anämie (Mangel an roten Blutkörperchen) Verner-MorrisonSyndrom/ VIPom vasoaktives intestinales Peptid (VIP) wässrige Durchfälle Hypokaliämie (Kaliummangel) Achlorhydrie (Fehlen von Magensäure) Tabelle 1: Hypersekretionssyndrome bei NET 11 Biotherapie bei einem weiteren Teil der Tumore scheinen die Zellen trotz der endokrinen Abstammung mit den entsprechenden biologischen Charakteristika kein Hormon mehr herzustellen. Solche Tumore, die sich auch klinisch nicht durch das Auftreten hormonbedingter Symptome bemerkbar machen, werden als nonfunktionell bezeichnet. Biotherapie – was ist das? Zur Behandlung von Tumorerkrankungen bestehen prinzipiell verschiedene Strategien. So gilt insbesondere auch für NET, dass eine Heilung, d.h. anhaltende Tumorfreiheit, nur durch Entfernung aller Tumore, üblicherweise durch eine Operation, erreicht werden kann. Kann keine Heilung durch eine Operation erreicht werden, müssen andere Therapieansätze verfolgt werden, z.B. Chemotherapie, bei der Zellgifte gegen die Tumorzellen zum Einsatz kommen. Eine andere Alternative bei den meist eher langsam fortschreitenden NET ist die so genannte Biotherapie, bei der biologisch im menschlichen Organsimus vorkommende Stoffe bzw. ihre Analoga (synthetisch hergestellte Stoffe mit gleicher Wirkung) verwendet werden. Die Biotherapeutika, zu denen für NET Somatostatinanaloga und Interferon-alpha gehören, können einerseits zur Symptomkon­ trolle bei funktionellen NET und an­ dererseits zur Wachstumskontrolle sowohl bei funktionellen als auch bei nonfunktionellen NET eingesetzt werden. Somatostatin und seine Analoga Bereits im gesunden Organismus spielt die Balance zwischen Stimu12 lation der Hormonabgabe und ihrer Kontrolle mittels Abgabehemmung eine wesentliche Rolle. Ein bedeutendes Hormon, das diese Kontrolle übernimmt ist das Somatostatin, das von den so genannten D-Zellen abgegeben wird. Somatostatin bindet an seine Bindungsstellen auf anderen endokrinen Zellen und NETZellen, den sog. Somatostatinrezeptoren, die auch in der nuklearmedizinischen Diagnostik eine große Rolle spielen. Es gibt fünf verschiedene Somatostatinrezeptorsubtypen, von denen derzeit dem Subtyp 2 bei den NET die größte Bedeutung zugesprochen wird. Somatostatinbindung an den Rezeptor löst verschiedene Signalanhäufungen in der jeweiligen Zelle aus, die letztlich über unterschiedliche Mechanismen eine deutliche Hemmung der Hormonproduk­tion bzw. –abgabe bewirken. Darüber hinaus gibt es auch aus Zellkultur- und Tiermodellen gute Belege dafür, dass die Somatostatinbindung an seine Rezeptoren auch Zellwachstumshemmung und sogar Zelltod (Apoptose) insbesondere der NET-Zellen aus­ lösen kann. Da das vom Körper selbst synthetisierte Somatostatin nur eine sehr kurze Verweildauer (Halbwertszeit) im Blutkreislauf aufweist und daher nur eine sehr kurze Wirkdauer zeigt, sind Analoga hergestellt worden. Sie haben eine vergleichbare Rezeptorbindungsfähigkeit mit deutlich verlängerten Halbwertszeiten im Organismus. In der Behandlung von NET werden daher die Somatostatinanaloga angewendet. Octreotid (Sandostatin®, Sandostatin LAR®) und Lanreotid (Somatuline®, Somatuline Autogel®) sind die in Deutschland erhältlichen Präparate. Voraussetzung für eine Wirksamkeit der Somatostatinanaloga ist die Expression (Ausbildung) der Somatostatinrezeptoren vom Subtyp 2 in ausreichender Dichte auf den Tumorzellen. Ein bislang nur im Rahmen klinischer Studien untersuchtes Somatostatinanalogon, das SOM230, bindet nicht nur an den Rezeptorsubtyp 2, sondern auch an die Subtypen 1,3 und 5, so dass hiermit in Zukunft auch NET, die die entsprechenden Rezeptoren ausbilden, behandelt werden können. Somatostatinanaloga in der Behandlung des hormonellen Hypersekretionssyndroms Die medikamentösen Behandlungsmöglichkeiten bei hormonellen Hypersekretionssyndromen (Hypersekretion= krankhaft gesteigerte Substanzabgabe durch Zellen bzw. Drüsen) sind vielfältig, wie in Tabelle 2 dargestellt. Somatostatinanaloga stellen bei nahezu allen hormonellen Hypersekretionssyndromen eine Behandlungsoption dar (siehe Abbildung 1), im Falle des Karzinoidsyndroms, dem mit Abstand häufigsten Hypersekretionssyndrom, sogar die führende Behandlungsstrategie. Auch beim Glukagonom (NET des Verdauungstraktes) und beim VIPom (WDHA-Syndrom) sind Somatostatinanaloga die Behandlungsmethode der ersten Wahl. Somatostatinanaloga sind besonders wirksam in der Reduktion der Durchfallshäufigkeit und -intensität (Diarrhöen) und der Reduktion der Häufigkeit und Dauer von Flushanfällen (vorübergehende Hautrötung). Allerdings zeigt sich insbesondere bei den Durchfällen die Wirkung nur in knapp der Hälfte aller Behandelten bereits innerhalb der ersten drei Monate in vollem Umfang. Man kann aber da- Syndrom Behandlungsmöglichkeiten Karzinoidsyndrom Somatostatinanaloga Interferon-a Loperamid ggf. 5HT3-Antagonisten (z.B. Tropisetron) Gastrinom/ZES Protonenpumpeninhibitoren (PPI) ggf. Somatostatinanaloga Insulinom KATP-Kanalöffner (Diazoxid) ggf. Somatostatinanaloga Glukagonom Somatostatinanaloga ggf. orale Antidiabetika oder Insulin VIPom Somatostatinanaloga + Antidiarrhoika GHRHom Somatostatinanaloga ACTHom 11b-Hydroxylaseinhibitoren (z.B. Metyrapon) Tabelle 2: Behandlungsmöglichkeiten der hormonellen Hypersekretionssyndrome bei NET Abb. 1: Antisymptomatische Wirkung der Biotherapie bei NET. mit rechnen, daß nach einem Jahr etwa 60 bis 80% der Patienten eine deutliche Besserung auch bei den Durchfällen verspüren. Dabei gibt es keinen wesentlichen Unterschied zwischen Octreotid und Lanreotid. Üblicherweise wird mit einer 2 bis 3 mal täglichen subkutanen (d.h. in das Fettgewebe unter der Haut gespritzten) Injektion begonnen. Bei Wirksamkeit wird heutzutage in aller Regel auf langwirksame Depotpräparate (Sandostatin LAR®, Somatuline Autogel®) umgestellt, die in vierwöchentlichen Abständen injiziert werden. Sandostatin LAR® wird dabei intramuskulär in aller Regel im Bereich des Gesäßmuskels, Somatuline Autogel® tief subkutan injiziert (ist in Deutschland seit diesem Jahr für funktionelle NET des MagenDarmtrakts zugelassen). Die Rolle des bei hormonellen Hypersekretionssyndromen prinzipiell ebenfalls wirksamen SOM 230 (Pasireotid) wird derzeit in klinischen Studien untersucht; das Präparat ist noch nicht im Handel erhältlich. Auch hier befindet sich ein Verzögerungspräparat in Entwicklung bzw. in klinischen Studien. Unerwünschte Arzneimittelwirkungen (= Nebenwirkungen) sind insgesamt selten und in aller Regel milde. Sie können folgende Beschwerden beinhalten: Bauchschmerzen, Blähungen, Fettstühle, vorübergehende Verstärkung der Diarrhöen (sehr selten) sowie milde Störungen der Nährstoff- und Kalorienaufnahme. Langfristig können sich Gallengrieß (Sludge) und Gallensteine ausbilden, die aber nur extrem selten zu Cholezystitis (Gallenblasenentzündung) oder Cholangitis (Gallengangsentzündung) führen. Weitere nur selten bedeutsam werdende Nebenwirkungen sind Vitamin-B12-Mangel, eine gestörte Glukosetoleranz mit Störungen des Blutzuckerspiegels bis hin zu mildem Diabetes mellitus und sehr selten ein verlangsamter Puls (Bradykardie). Ein gelegentlich auftretender milder Haarausfall bildet sich bei Beendigung der Therapie in der Regel voll zurück. Somatostatinanaloga zur Wachstumskontrolle von NET Die Erfolge von Somatstatinanaloga zur Kontrolle des Tumorwachstums von NET sind sehr begrenzt (siehe Abbildung 2). Eine Verkleinerung oder gar komplette Rückbildung von Tumoren ist nur in sehr wenigen Einzelfällen beschrieben worden, insbesondere unter Verwendung sehr hoher Dosierungen. Aus Zell13 Diagnostik Biotherapie kulturuntersuchungen und Tiermodellen haben sich aber Hinweise auf eine Wachstumshemmung ergeben. Deshalb ist die Frage, in welchem Ausmaß Somatostatinanaloga ein fortschreitendes Tumorwachstum (= Progress) zum Stillstand bringen können (= Krankheitsstabilisierung, „stable disease”) derzeit Gegenstand mehrerer deutscher und internationaler klinischer Studien. Bisherige Studien lassen einen Erfolg in ca. 30 bis 60% der Fälle erwarten; allerdings ist derzeit nicht mit Sicherheit abzuschätzen, wie lange ein solcher durch Somatostatinanaloga erreichter Wachstumsstillstand anhält. Im Rahmen der so genannten PROMID-Studie (Placebo-kontrollierte, randomisierte – also nach Zufallsbedingungen zugeordnete Therapie – klinische Studie zur antiproliferativen Wirksamkeit von Octreotid bei MidgutNET; antiproliferativ = gegen eine Gewebevermehrung gerichtet) wird der Einsatz von Octreotid bei chirurgisch nicht komplett entfernten NET des Dünndarms bzw. nicht operablen Metastasen solcher NET untersucht. Studienzentrum hierfür ist die Klinik für Innere Medizin, Schwerpunkt Gastroenterologie, Endokrinologie und Stoffwechsel der Philipps-Universität in Marburg. Die ENET-1-Studie vergleicht die Wirksamkeit von Octreotid mit der einer Chemotherapie bei nachweislich wachsenden (progredienten) NET des Vorderdarmbereichs (d.h. Lunge, Magen, Bauchspeicheldrüse); Studienzentrum hierfür ist das Studiensekretariat der Medizinischen Klinik mit Schwerpunkt für Hepatologie und Gastroenterologie, Interdisziplinäres Stoffwechselzentrum, Endokrinologie und Diabetes der Charité, Campus Virchow Klinikum der Universitätsmedizin in Berlin. 14 Abb. 2: Antiproliferative Wirkung der Biotherapie bei NET. Interferon-alpha zur Behandlung des KarzinoidSyndroms und zur Wachstumskontrolle Interferon-alpha ist ein körpereigener Botenstoff, der v.a. im Rahmen von entzündlichen Prozessen von Leukozyten (weiße Blutkörperchen, Abwehrzellen) abgegeben wird, ein sog. Zytokin. Dieses Zytokin hat auf Tumorzellen einen das Wachstum hemmenden, z.T. sogar tödlichen Effekt; insbesondere bei NET-Zellen sind Einflüsse auf das Tumorwachstum und die damit verbundene Zellteilung aber auch auf die Neubildung von Tumor-versorgenden Blutgefäßen (= Angiogenese) beschrieben worden (siehe Abbildung 2). Darüber hinaus kann Interferon-alpha auch eine Verminderung der Hormonhypersekretion beim Karzinoidsyndrom bewirken und hat hier insbesondere auch einen Stellenwert neben den Somatostatinanaloga (siehe Abbildung 1). V.a. bei besonders ausgeprägtem Karzinoidsyndrom, wo die einfache Therapie mit Somatostatin­analoga nicht zu einer ausreichenden Symp­ tomkontrolle führt, kann die Kombination mit Interferon-alpha zu einem befriedigenden Therapieerfolg füh- ren. Interferon-alpha kann aber auch alleine (als Monotherapie) zur Symptomkontrolle bei Karzinoidsyndrom eingesetzt werden. Interferon-alpha wird hierzu üblicherweise 3 Mal wöchentlich subkutan injiziert. Zur Vorbeugung von Nebenwirkungen (siehe nächster Absatz) können ca. 30 Minuten vorher 500 bis 1000 mg Paracetamol eingenommen werden. Es existieren auch für Interferon-alpha längerwirksame Verzögerungspräparate (so genannte pegylierte Interferone: PegIntron®, Pegasys®), die nur einmal pro Woche injiziert werden müssen. Interferon-alpha hat andere unerwünschte Arzneimittelwirkungen als die Somatostatinanaloga, die auch einer anderen Überwachung (= Monitoring) bedürfen. Häufig treten Fieber und Schüttelfrost nach der Injektion auf, sowie Rötung und seltener Schmerzen an der Injektionsstelle, Kopf- oder/und Muskelschmerzen, Müdigkeit, Abgeschlagenheit, Husten und andere grippeartige Symptome. Das liegt daran, dass Interferon-alpha als körpereigenes Zytokin auch bei einer Grippeerkrankung vermehrt ausgeschüttet wird und dann eben auch die genannten Beschwerden auslösen kann. Durch Paracetamol-Einnahme vor Interfe- Weiterführende Fachliteratur Biotherapie roninjektion können diese allerdings sehr gut kontrolliert werden. Außer den genannten Beschwerden sind auch Haarausfall, Hautausschlag, Durchfälle, gelegentlich auch Übelkeit und Blutbildveränderungen, die regelmäßige Kontrollen beim Hausarzt erforderlich machen, möglich. Ferner können so genannte Autoimmunerkrankungen z.B. der Schilddrüse, der Leber oder andere wieder aktiviert werden, was die Bedeutung der ärztlichen Kontrolle unterstreicht. Auch hier sind gegebenenfalls entsprechende Laborkontrollen durch die behandelnden Ärzte erforderlich. Von großer Bedeutung ist das mögliche Auftreten von seelischen Stimmungsschwankungen bis hin zu depressiven Verstimmungen. Hier ist in der Regel die Beendigung der Therapie angezeigt, im Einzelfall kann auch eine begleitende stimmungsaufhellende (antidepressive) Medikation durch den Psychiater erwogen werden. Ähnlich wie die Somatostatinanaloga hat Interferon nur eine sehr begrenzte Wirksamkeit im Hinblick auf Tumorverkleinerung. Die Wirksamkeit im Hinblick auf eine Erkrankungsstabilisierung („stable disease”) ist jedoch in etwa der von Somatostatinanaloga vergleichbar mit einer Stabilisierung in etwa 30 bis 60 % der Fälle unter Inkaufnahme des größeren Nebenwirkungsspektrums als bei Somatostatinanaloga. Kombinationsbiotherapie zur Wachstumskontrolle? 1. Faiss S, Pape UF, Böhmig M, et al. Prospective, randomized, multicenter trial on the antiproliferative effect of lanreotide, interferon-alfa, and their combination for therapy of metastatic neuroendocrine gastroenteropancreatic tumors - The International Lanreotide and Interferon-alfa Study Group. J Clin Oncol 2003; 21:2689-96 2. Pape UF, Wiedenmann B. Adding interferon-alpha to octreotide slows tumour progression compared with octreotide alone but evidence is lacking for improved survival in people with disseminated midgut carcinoid tumours. Cancer Treat Rev 2003; 29:565-569 3. Plöckinger U, Rindi G, Arnold R, Eriksson B, Krenning EP, de Herder WW, Goede A, Caplin M, Öberg K, Reubi JC, Nilsson O, Delle Fave G, Ruszniewski P, Ahlman H, Wiedenmann B. Guidelines for the diagnosis and treatment of neuroendocrine gastrointestinal tumors. Neuroendocrinology 2004; 80:394-424 4. Wiedenmann B, Höffken (Hrsg.). Neuroendokrine Tumoren. Onkologe 2004; 10:559-639 5. Öberg K, Kvols L, Caplin M, Delle Fave G, de Herder W, Rindi G, Ruszniewski P, Woltering EA, Wiedenmann B. Consensus report on the use of somatostatin analogs for the management of neuroendocrine tumors of the gastroenteropancreatic system. Ann Oncol 2004; 15:966-973 6. Plöckinger U, Wiedenmann B. Neuroendokrine Tumoren des Gastrointestinaltrakts. Z Gastroenterol 2004; 42:517-526 7. Arnold R, Rinke A, Klose KJ, Muller HH, Wied M, Zamzow K, Schmidt C, Schade-Brittinger C, Barth P, Moll R, Koller M, Unterhalt M, Hiddemann W, Schmidt-Lauber M, Pavel M, Arnold CN. Octreotide versus octreotide plus interferon-alpha in endocrine gastroenteropancreatic tumors: a randomized trial. Clin Gastroenterol Hepatol 2005; 3:761-771 8. Plöckinger U. Neuroendokrine Tumoren des Gastrointestinaltraktes. Gastroenterologie up2date 2006; 2:233-256 im Einzelfall wirksam sein kann, ist auch die Frage untersucht worden, ob eine Kombination der beiden Substanzen, die jeweils nur begrenzt wirksam sind, bei der Wachstumskontrolle von NET, zur Hemmung des Tumorwachstums effektiv ist. Zusammenfassend haben die Untersuchungen zu dieser Frage die Wirksamkeit der Kombination bei mittels Monotherapie nicht (mehr) ausreichend kontrollierten Symptomen bestätigt, eine eindeutig bessere Wirkung gegen das Tumorwachstum konnte aber nicht belegt werden. Deshalb hat die Kombination dieser beiden Substanzen derzeit keinen festen Platz in der antiproliferativen Therapie zur Wachstumskontrolle von NET. Zusammenfassung Während die Kombination von Somatostatinanaloga und Interferonalpha zur Beschwerdelinderung bei mittels längerer Einfachtherapie (Monotherapie) nicht beherrschbarem Hypersekretionssyndrom Somatostatinanaloga und Interferon-alpha stehen zur Symptombekämpfung und mit Einschränkung auch zur Wachstumskontrolle bei meist langsam wachsenden sog. niedriggradig bösartigen NET zur Verfügung. Insbesondere in der Behandlung der hormonellen Hypersekretionssyndrome sind sie fester und unverzichtbarer Bestandteil der erfolgreichen Therapie. Ihre Rolle bei der antiproliferativen Behandlung wird durch derzeit noch laufende klinische Untersuchungen weiter geklärt werden. Autorenanschrift: Dr. med. Ulrich-Frank Pape Prof. Dr. med. Bertram Wiedenmann Med. Klinik m. S. Hepatologie und Gastroenterologie Charité, Campus Virchow Klinikum Universitätsmedizin Berlin Augustenburger Platz 1 13353 Berlin 15 Veranstaltungen Außergewöhnliche Resonanz – Bericht vom 3. Überregionalen Neuroendokrinen Tumor-Tag vom 24.-26. November 2006 in Mainz Nach dem überaus erfolgreichen 2. Informationstag in Nürnberg im November 2005 fand der 3. Überregionale Neuroendokrine Tumor-Tag vom 24.-26. November 2006 in Mainz statt. Lagen zwischen dem 1. Neuroendokrinen TumorTag in Herzogenaurach und dem 2. in Nürnberg mehr als fünf Jahre, so gab es jetzt schon nach einem Jahr die nächste überregionale Informationsveranstaltung für Patienten, Angehörige, Ärzte und andere Interessierte. Organisiert wurde die Veranstaltung von den Mitarbeitern im Vorstand des Netzwerks Neuroendokrine Tumoren (NeT e.V.), die lokale Organisation erfolgte diesmal durch Prof. Dr. M.M. Weber und Dr. C. Fottner vom Schwerpunkt Endokrinologie und Stoffwechselerkrankungen der I. Medizinischen Klinik und Poliklinik, in Zusammenarbeit mit dem Interdisziplinären Endokrinen und Neuroendokrinen Tumorforum (IENET) des Universitätsklinikums Mainz, welches Prof. Weber als Sprecher vertritt. Unterstützt wurde die Veranstaltung dankenswerterweise erneut von Novartis Oncology (Frau Dr. Grassmann). Der kürzere Abstand zum 2. Informationstag spiegelt das große Interesse und Engagement der Betroffenen und Mitglieder im Verein NeT e.V. wider. Darüber hinaus war angesichts des immer rascher fortschreitenden medizinischen Fortschrittes, natürlich auch im Bereich der Diagnostik und Therapie neuroendokriner Tumoren, für genug Gesprächsstoff gesorgt – insbesondere für die verschiedenen Expertenvorträge, Workshops und Diskussionsrunden. Nicht zuletzt sollte die Veranstaltung dazu dienen, die Seltenheit und Vielfalt der neuroendokrinen Tumoren auch Hausärzten und anderen ärztlichen Kollegen nahe zu bringen, damit eine frühe Diagnose dieser Erkrankung gefördert wird. 16 Die Resonanz auf den Tumor-Tag war außergewöhnlich groß. Insgesamt haben über 125 Patienten, Angehörige und Ärzte teilgenommen, die zum Teil hunderte Kilometer weit angereist sind. Das große Interesse an der Veranstaltung zeigt sich auch an der großen Resonanz in der regionalen und überregionalen Presse, die mehrfach und ausführlich über die Tagung berichtet hat. Damit wurde nicht unwesentlich zur weiteren Aufklärung über diese seltene Tumorvariante beigetragen. Quelle: Allgemeine Zeitung Mainz Es wurde bei der Organisation des Programms an das bewährte Format angeknüpft. Auch diesmal bot man an jedem der drei Tage einen eigenen Schwerpunkt: • 24.11.06: Mitgliederversammlung • 25.11.06: Vorträge und Workshops • 26.11.06: Erfahrungsaustausch unter Patienten Freitagabend - Mitgliederversammlung Netzwerk Neuroendokrine Tumoren (NeT) e.V. Der erste Abend der Veranstaltung war wie gewohnt der Mitgliederversammlung des Netzwerks Neuroendokrine Tumoren e.V. gewidmet. Nachdem sich die Teilnehmer am diesjährigen Veranstaltungsort, dem Hotel DorintNovotel Mainz, eingefunden hatten, trafen sich der Vorstand und die bis dahin bereits angereisten Mitglieder des Netzwerks NeT, um sich intern zu besprechen. Darüber hinaus fiel hier der Startschuss zur Gründung der „Regionalgruppe Rhein-Main” des Netzwerks NeT e.V., die von Patienten mit Hilfe der Mainzer Experten neu gegründet wurde. „Dies war ein wichtiger Schritt, Veranstaltungen um die Belange der Betroffenen wirksamer zu vertreten, sowie den Gedanken- und Informationsaustausch zu fördern”, erläuterte Prof. Weber. Beschlossen wurde der Abend dann in geselliger Runde beim gemeinsamen Abendessen. Samstag - Vorträge und Workshops Bereits um 8:00 Uhr fanden sich die ersten Teilnehmer und Vertreter der regionalen und überregionalen Presse im Vortragssaal ein, und bis zum Beginn der Veranstaltung war der Saal restlos belegt. Nachdem der rege Teilnehmerandrang von den Mitarbeitern des Netzwerks dank der wie gewohnt professionellen Organisation problemlos bewältigt wurde, stand einem pünktlichen Beginn der Veranstaltung nichts mehr im Wege. Zunächst wurden die Angereisten von den wissenschaftlichen Leitern der Veranstaltung, Herrn Prof. Dr. J. Hensen und Herrn Prof. Dr. M.M. Weber, begrüßt. Dabei wurde nicht versäumt, sich bei allen Mitarbeitern des Netzwerks, die durch ihre tatkräftige Unterstützung zum Gelingen der Tagung Prof. Dr. Hensen beigetragen haben, persönlich zu bedanken,. „Ohne die unermüdliche ehrenamtliche Mithilfe wäre eine solch große Veranstaltung wie der überregionale NET-Tag sicher nicht möglich”, meinte Prof. Hensen in seinem Grußwort und übergab das Mikrofon an die teilweise aus ganz Deutschland angereisten Experten. Als erstes startete Prof. Dr. Weber die wissenschaftliche Vortragsreihe mit einer Präsentation zum Überblick und zur Einteilung neuroendokriner Tumoren. Dieser einleitende Vortrag sollte einen Überblick über die Diagnostik und Therapie dieser unterschiedlich auftreProf. Dr. Weber tenden Erkrankung geben und zu den folgenden Einzelvorträgen überleiten. Dabei ging Prof. Weber insbesondere auch auf die neue so genannte TNM-Klassifikation neuroendokriner Tumoren ein, die erstmals, vergleichbar mit den bereits für nahezu alle anderen bösartigen Tumoren existierenden Klassifikationen, eine präzise Klassifikation und Stadieneinteilung ermöglicht. Da neuroendokrine Tumoren bezüglich ihrer biologischen Aktivität aber auch bezüglich ihres Wachstumsverhaltens und ihrer Prognose eine sehr uneinheitliche Gruppe von Tumorerkrankungen darstellen, muß für jede Untergruppe eine entsprechende Einteilung vorgenommen werden. Dies bietet eventuell für die Zukunft die Möglichkeit einer stadienabhängigen einheitlichen Therapie dieser seltenen Tumoren. In der Folge schlossen sich weitere hochinteressante Referate der medizinischen Experten aus den Bereichen der Endokrinologie, Chirurgie, Nuklearmedizin und Radiologie an. Im Anschluss haben wir die für Patienten interessantesten Vorträge in weitgehend volDr. Hörsch ler Länge veröffentlicht. In diesem Zusammenhang möchten wir den Autoren unseren herzlichen Dank aussprechen, dass sie uns ihre Texte zur Verfügung gestellt haben. Herr Privatdozent Dr. Dieter Hörsch berichtete in seinem Referat über neue Methoden in der Diagnostik neuroendokriner Tumoren. Einen großen Schwerpunkt legte er dabei auf die bildgebenden Methoden und deren aktuelle technische Verbesserungen (Seite 20). Als weiterer Internist sprach Herr Privatdozent Dr. Christoph Auernhammer aus München über Behandlungsmöglichkeiten bei isoliertem Leberbefall. Besonders die Ausführungen über moderne Therapie17 Veranstaltungen verfahren wie der Radiofrequenzablation stießen auf großes Interesse, was sich auch in den Berichten der Zeitungen widerspiegelt (das komplette Referat finden Sie auf Seite 24). gab einen entsprechenden Überblick über die aktuell in Deutschland laufenden Studien und Kontaktadressen. Den kompletten Text finden Sie auf S. 27. Weitere besondere Schwerpunkte der Veranstaltung waren unter anderem Vorträge von Dr. A. Helisch zur DOTATOC-Therapie (S. 30) und von Prof. Dr. T.J. Musholt zu chirurgischen Therapiemöglichkeiten (S. 32). Prof. Dr. Schmidberger sprach zu möglichen Indikationen für die Strahlentherapie. Quelle: Wormser Zeitung Auf nicht weniger großes Interesse stieß, wie jedes Jahr, der Bericht zu „Neuen und bewährten medikamentösen Therapieansätzen“ bei der Behandlung von neuroendokrinen Tumoren von Frau Privatdozentin Dr. Marianne Pavel. Neben den bewährten medikamentösen Dr. Pavel Therapieoptionen wie den Somatostatinanaloga und Interferon insbesondere zur Behandlung von Tumoren herrührenden Hormonsyndromen, ging Frau Dr. Pavel hier insbesondere auf neue Somatostatinanaloga wie etwa Pasireotid (SOM230) ein. Sie erläuterte aber auch moderne Hemmstoffe der Gefäßneubildung (so genannte Angiogenesehemmer), Hemmstoffe des Wachstums von Tumor – und Gefäßzellen (im Sinne einer molekular-zielgerichteten Therapie) und neue Chemotherapeutika. Frau Dr. Pavel betonte hier, dass diese bisher noch wenig erprobten Medikamente in erster Linie bei Tumorwachstum, einer unzureichenden Symptomkontrolle und insbesondere bei Versagen etablierter Therapieoptionen und fehlender Option einer Radionuklidtherapie erwogen werden sollten. Um weitere Erfahrungen mit diesen erfolgversprechenden Substanzen sammeln zu können, sollte der Einsatz jedoch im Rahmen kontrollierter klinischer Studien erfolgen, meinte die Referentin und 18 Im Anschluss an jeden Expertenvortrag bot sich den Zuhörern die Gelegenheit, Fragen an die Vortragenden zu stellen. Daraus entwickelte sich eine lebhafte Fragen- und Diskussionsrunde, was das rege Interesse der Angereisten widerspiegelte. Um diesem Rechnung zu tragen, stand nach Abschluss der Vorträge eine eigene Diskussionsrunde auf dem Programm, bei der die Möglichkeit bestand, allen Referenten weitere Fragen zu stellen. Nach Abschluss der Expertenrunde hatten die Besucher dann die Qual der Wahl: In vier Parallelveranstaltungen wurden verschiedene Gebiete der neuroendokrinen Tumoren in Workshops vorgestellt. Hier bot sich den Interessierten beispielsweise die Möglichkeit, sich im Workshop von Prof. Dr. Hensen über alternative und unterstützende Behandlungsmethoden zu informieren (ausführlicher Bericht: siehe S. 36). Dr. Fottner bot einen Workshop über familiäre endokrine und neuroendokrine Tumorerkrankungen an, bei denen insbesondere auf die verschiedenen erblichen Tumorsyndrome, aber auch auf andere Krankheitsbilder wie das von-Hippel-Lindau-Syndrom und hereditäre Paragangliom-Syndrome eingegangen wurde. Sie gehen mit dem gehäuften Auftreten von endokrinen und neuroendokrinen Tumoren einher. Veranstaltungen Das wichtige Thema der Krankheitsbewältigung war ein weiteres Thema des Workshops, der von Frau Dr. Hensen geleitet wurde. Prof. Dr. Musholt bot die Möglichkeit, seinen Vortrag über chirurgische Therapieoptionen bei neuroendokrinen Tumoren in einem eigenen Workshop in kleinen Gruppengesprächen zu vertiefen. Schnell entwickelten sich in den offenen Gesprächsrunden lebhafte Diskussionen der Teilnehmer und ein reger Erfahrungsaustausch. und Erlebnisse mit ihrer Krankheit miteinander auszutauschen. Da neuroendokrine Tumoren seltene Erkrankungen mit einem breiten Spektrum sind, können die Mitglieder des Netzwerk NeT gerade auch bei solchen überregionalen Veranstaltungen voneinander lernen, neue Kontakte knüpfen und Unterstützung finden. Sonntag - Erfahrungsaustausch unter Patienten Der dritte Tag bot den Teilnehmern der Veranstaltung die Möglichkeit, sich über ihre eigenen Erfahrungen Mit dem Erfahrungsaustausch der Patienten untereinander kam der gelungene 3. Überregionale Neuroendokrine Tumor-Tag schließlich zu seinem Abschluss. Wir können bereits jetzt wieder gespannt auf die nächste Veranstaltung in dieser Reihe sein. Der nächste überregionale Tumor-Tag wird vom 9. bis zum 11. November in München stattfinden. Für die Organisatoren des 3. überregionalen Neuroendokrinen Tumortages in Mainz, Dr. med. Christian Fottner Prof. Dr. med. Matthias M. Weber Dr. med. Klaus P. Kreisselmeier Dr. med. Christian Fottner Prof. Dr. med. Matthias M. Weber Schwerpunkt Endokrinologie und Stoffwechselerkrankungen, I. Medizinische Klinik und Poliklinik Klinikum der Johannes Gutenberg Universität Mainz Langenbeckstrasse 1, 55101 Mainz Tel.: 06131/17-7260 e-mail: [email protected] 19 Veranstaltungen 3. Überregionaler Neuroendokriner Tumor-Tag vom 24.-26. November 2006 in Mainz Neue Diagnoseverfahren bei neuroendokrinen Tumoren Die Diagnose von neuroendokrinen Tumoren (NET) beinhaltet die richtige und umfassende Erkenntnis über Art und Ausbreitung der Erkrankung. Gerade bei den seltenen neuroendokrinen Tumoren ist die richtige Diagnose das wichtigste Werkzeug um den weiteren Verlauf der Erkrankung günstig beeinflussen zu können oder eine Heilung herbeizuführen. Die Diagnose eines neuroendokrinen Tumors soll vor allem folgende Fragen beantworten: • Wo sitzt der Ausgangstumor (Primärtumor oder Primarius) • Wie ausgedehnt ist der Primär­ tumor • Gibt es Tochtergeschwülste (Metastasen) und wo sind sie lokalisiert • Wie gutartig oder bösartig ist der Tumor • Produziert der Tumor Substanzen, die zu funktionellen Störungen führen können (z.B. Karzinoidkrisen) • Ist das Risiko für Zweittumore erhöht oder besteht eine familiäre Belastung Die Ausdehnung des Tumors und eventueller Tochtergeschwülste wird üblicherweise in einem System festgehalten (TNM-System; wobei T die Ausdehnung des Primärtumors, N das Vorliegen von Lymphknotenmetastasen und M das Vorliegen von Fernmetastasen beschreibt) sowie in einer feingeweblichen Einteilung des Tumors nach Bös20 artigkeit, (betrifft die Wachstumsgeschwindigkeit und die Neigung Tochtergeschwülste zu bilden). Für die neuroendokrinen Tumoren ist ein eigenes TNM-System in Arbeit und liegt für NETs des Magens, des Zwölffingerdarms und der Bauchspeicheldrüse vor. Das Grading (Differenzierungsgrad) erfolgt nach der so genannten WHO-Nomenklatur oder dem TNM System. Die Erfassung der Tumorausdehnung und Grad der Bösartigkeit wird auch als Staging bezeichnet. Da das richtige Staging von NETs über die Therapie entscheidet und auch Prognosen über den Krankheitsverlauf zulässt, kommt den diagnostischen Verfahren bei NETs zusammen mit der Fachkompetenz der behandelnden Ärzte eine richtungsweisende und gelegentlich lebensentscheidende Bedeutung zu. Die Standardverfahren zur Diagnose von NETs beinhalten sonographische Methoden, interventionelle oder chirurgische Probenentnahmen mit nachfolgender feingeweblicher Untersuchung (z.B. Endoskopie), nuklearmedizinische Verfahren wie die Octreotid-Szintigraphie (OctreoScan) und radiologische Methoden wie CT und MRT. Laborchemische Methoden, wie z.B. die Bestimmung von Chromogranin A und Serotonin als Tumormarker, wurden bereits in mehrfach in den letzten Ausgaben der GlandulaNeT behandelt. Neue Diagnoseverfahren sollten gegenüber diesen verbreiteten und etablierten Methoden einen Vorteil aufweisen hinsichtlich der richtigen Tumorerkennung (Sensitivität) oder der genaueren Charakterisierung von nicht entartetem Gewebe (Spezifität). Weitere Vorteile können Schnelligkeit und Vollständigkeit (z.B. Ganzkörperuntersuchung) einer Untersuchungsmethode oder die verminderte Belastung der Patienten sein, was bei den langandauernden Verläufen der Erkrankung von besonderer Wichtigkeit ist. In den letzten Jahren wurden im Bereich der Sonographie und insbesondere in der Nuklearmedizin neue Techniken für die Diagnose von Tumorerkrankungen entwickelt, die auch für die genauere Diagnose der NETs eine zunehmend größere Rolle spielen. Neue Entwicklungen im Ultraschall Der transabdominelle Ultraschall ist eine einfache und wenig belastende Methode zur Diagnose von NETs und der Verlaufsbeurteilung. Die Genauigkeit der Methode hängt von der Lokalisation des Tumors, der Erfahrung des Untersuchers und der Qualität der Darstellung ab. Hochqualitative Geräte verfügen heutzutage über eine Reihe von Möglichkeiten, die Darstellung der Tumore zu verbessern. Einerseits können Verfahren die Abbildungsqualität und den Kontrast zwischen verschiedenen Körpergeweben verbessern (zum Beispiel durch „tissue harmonic ima- Veranstaltungen Abb. 1: Die KM-verstärkte Sonographie kann Lebermetastasen sichtbar machen. ging” oder „spatial compound imaging”), zum anderen konnte die Darstellung des Blutflusses im Gewebe durch die Doppler-Technik weiter verbessert und verfeinert werden. Dadurch können versteckte Tumore besser erkannt werden und Raumforderungen sind besser auf die Durchblutung zu untersuchen, die bei Tochtergeschwülsten von NETs meist verstärkt ist. Die wichtigste Neuerung auf dem Gebiet des Ultraschalls ist jedoch die Einführung von verbesserten Kontrastmitteln. Durch diese Kontrastmittel kann der Blutfluss auch in kleinen Raumforderungen sichtbar gemacht werden. Zudem kann eine Aussage über die Art der Durchblutung aufgrund der Kontrastmittelanflutung gemacht werden. Durch die kontrastmittelverstärkte Sonographie können auch Raumforderungen in der Lunge, die nah an der Thoraxwand liegen besser erkannt werden (Abbildung 1). Für Tumore in der Speiseröhre, dem Magen, dem Zwölffingerdarm, der Bauchspeicheldrüse sowie der Gallengänge ist der Ultraschall durch eine am Endoskop befestigte Sonde die Methode der Wahl (Endosonographie). Diese Methode kann mit Schallköpfen durchgeführt werden, die einen Rundumblick erlauben oder einen kleineren Ausschnitt darstellen. Diese letzteren Sektorscanner können mit einer Punktionsnadel bestückt werden, die auch die Punktion zur Gewebe-Entnahme, und nachfolgende feingewebliche Untersuchung von kleinen suspekten Läsionen (Raumforderungen, das heißt meist fremdes Gewebe in einem Organ) erlaubt. Schwierigkeiten machen bei der Endosonographie oft kleine Tumoren in der Wand des Zwölffingerdarms, die bei Gastrinomen auftreten können. Hierfür gibt es jedoch mittlerweile kleine Ultraschallsonden, die mit einem Endoskop eingeführt werden können und somit die Kombination zwischen einer Spiegelung des Zwölffingerdarms und gezielter Ultraschalluntersuchung verdächtiger Bezirke erlauben. Diese Mini-Sonden sind zudem extrem hochauflösend und können dadurch auch sehr kleine Tumoren erkennen. Für alle diese Methoden gilt, dass die Erfahrung des Untersuchers die wichtigste Rolle bei der Befunderhebung spielt. Ultraschallmethoden verschiedener Art haben sich in der Diagnose von Erkrankungen außerordentlich bewährt. Ultraschall wird jedoch möglicherweise in Zukunft auch eine Rolle bei der Behandlung von Tumorerkrankungen spielen. Sehr hochenergetischer Ultraschall kann, wenn er durch eine Kernspinuntersuchung gezielt auf erkranktes Gewebe gerichtet und fokussiert wird, dieses ohne äußere Verletzungen zerstören. Hier gibt es vor allem in 21 Veranstaltungen China interessante Entwicklungen, die zur Zeit in Studien überprüft werden. Neue Entwicklungen in der Nuklearmedizin Ultraschall und radiologische Verfahren wie CT und Kernspin stellen neuroendokrine Tumoren durch unterschiedliche Eigenschaften wie Dichte, Durchblutung oder Schallreflexion dar. Meist werden bestimmte Körperregionen zur Darstellung ausgewählt, wie der Oberbauch bei der Abbildung von Lebermetastasen im CT oder Kernspintomogramm. Ein völlig anderes Prinzip kommt in der nuklearmedizinischen Diagnostik zur Anwendung. Hierbei werden NETs (aber auch andere Tumore) durch die verstärkte Aufnahme bzw. Bindung von speziellen, radioaktiv markierten Molekülen (so genannten Peptiden), die an die Zelloberfläche binden, nachgewiesen („SchlüsselSchloß-Prinzip“). Da die meisten NETs Somatostatin-Rezeptoren verstärkt exprimieren (= an der Oberfläche tragen) ist die Darstellung von NETs durch 111Indium- oder 99mTechnetium-markierte Somatostatinanaloga (Octreotid, Octreotid-Szinigraphie, OctreoScan) ein etabliertes Verfahren, um mit hoher Empfindlichkeit und Genauigkeit NETs darzustellen. Ein weiterer Vorteil des Verfahrens ist die Erfassung und Darstellung des gesamten Körpers und der Nachweis zellulärer Funktionen, in diesem Fall die Exprimierung von Somatostatinrezeptoren auf der Zelloberfläche. Eine wesentliche Weiterentwicklung der nuklearmedizinischen Verfahren für die noch exaktere Diagnose von Tumorerkrankungen ist die Positronen-Emissions-Tomographie (PET). 22 Vor Therapie 3 Monate nach Therapie Abb.2: Das FDG-PET ist bei schnell wachsenden neuroendokrinen Tumoren positiv. Bei diesem Verfahren werden Positronenstrahlen, die von bestimmten Molekülen ausgesendet werden, in Lichtsignale umgewandelt und dargestellt. Am gebräuchlichsten ist die Fluor-18-2-Deoxy-FluorGlukose-PET (auch als FDG-PET oder Zucker-PET bezeichnet). Hierbei macht man sich die verstärkte Aufnahme und Umwandlung von Glukose in Krebszellen zunutze, um Tumoren anhand ihres erhöhten Zuckerverbrauchs darzustellen. NETs haben jedoch meist nur einen gering erhöhten Zuckerstoffwechsel und sind dadurch im FDG-PET nur schwer nachweisbar oder nur, wenn sie schnell wachsen (Abbildung 2). Eine ganz neue Entwicklung ist die Rezeptor-PET/CT, die heute das bei weitem empfindlichste und schonendste Verfahren zur Ganzkörperdiagnostik bei neuroendokrinen Tumoren darstellt. Hierbei wird ein kurzlebiger Positronenstrahler, 68Gallium (Halbwertszeit nur 68 Minuten, d.h. geringe Strahlenbelastung für den Patienten) an bestimmte, so genannte Somatostatinrezeptor-bindende Peptide gekoppelt. Dies ermöglicht die Darstellung von Somatostatin-Rezeptor-tragenden NETs mit einer wesentlich höheren Sensitivität als die Octreotid-Szintigraphie. Hier hat sich vor allem 68Gallium-DOTANOC zur Darstellung von NETs bewährt, das eine sehr kontrastreiche Darstellung mit einer hohen Auflösung verbindet, wodurch auch kleinste Tumoren im Millimeterbereich nachgewiesen werden können. Die Kombination einer Gallium-68-DOTA-NOC PET mit einem Ganzkörper-CT in einem Gerät (so genannte PET/CT) erlaubt die genaue anatomische Zuordnung von PET-Befunden, wodurch zwei Fliegen mit einer Klappe geschlagen werden: hohe Empfindlichkeit (Sensitivität) zum Tumor- bzw. Metastasennachweis und genaue Körperdarstellung mit sofortiger Zuordnung verdächtiger Befunde. So können zum Beispiel kleine Lymphknoten, die im normalen CT nicht weiter auffällig wären, wenn sie im PET aufleuchten, als befallene Lymphknotenmetastasen erkannt werden (Abbildung 3 A). Gleiches gilt für kleine Knochenmetastasen Veranstaltungen PET SUV 22 GP-337156/05-08 CT 6 mm kleiner neuroendokriner Pankreastumor (CUP), operativ bestätigt PET/CT A B Abb.3: Im 68Gallium-PET/CT sichtbare Lymphknotenund Knochenmetastasen. (Abbildung 3 B) oder versteckte kleine Primärtumore (so genanntes CUP-Syndrom, d.h. unbekannter Primärtumor, Abbildung 4). Besonders bewährt hat sich die Gallium-68-DOTA-NOC-PET/CT (oder kurz Rezeptor-PET/CT) bei folgenden Fragestellungen: • Erstdiagnose von NETs, um eine genaue Abbildung der Tumorausbreitung zu erhalten und dadurch die optimale Therapie festzulegen • bei unbekanntem Primärtumor durch die verbesserte Darstellung (höhere Sensitivität) im Vergleich zu den Standardverfahren • nach einer operativen Entfernung des Tumors, um ein Rezidiv (erneutes Auftreten) frühzeitig zu erkennen (Tumornachsorge) • bei Verdacht auf kleine Tochtergeschwülste (Nachweis von kleinen Metastasen, z.B. in Lymphknoten oder im Knochen) • um eine Peptidrezeptor-vermittelte Radionuklidtherapie (PRRT, nuklearmedizinische Radio-Rezeptortherapie) zu planen und zu überwachen Abb. 4: Im 68Gallium-PET/CT sichtbarer Primärtumor, der durch andere Diagnoseverfahren nicht sichtbar gemacht werden konnte. • bei Verdacht auf Zweittumoren (in Kombination mit einem FDGPET) • um Hinweise auf die Funktionalität der Tumore anhand des Rezeptorbesatzes zu erhalten. Nicht alle NETs können mit einem Gallium-68-DOTA-NOC PET dargestellt werden. Daher wird intensiv nach weiteren Methoden gesucht, um diese rund 20 % von neuroendokrinen Tumoren genauso gut abzubilden wie die Somatostatinrezeptor-tragenden NETs. Das Peptid Bombesin, dessen Rezeptoren auf vielen verschiedenen Tumoren vorhanden sind, wird zur Zeit von unserer Arbeitsgruppe auf seine Eignung untersucht, im PET/CT für die Diagnostik von NETs eingesetzt zu werden. Weitere Peptide wie das Peptid GLP-1, dessen Rezeptoren vor allem auf Insulinomen exprimiert werden oder Minigastrin für die Diagnostik und möglicherweise Therapie von medullären, das heißt Calcitonin-exprimierenden Schilddrüsenkarzinomen, sind ebenfalls Kandidaten für eine verbesserte Darstellung aller NETs, denn schließlich hängt die exakte Planung einer Therapie von Patienten mit NETs vor allem von einem entscheidenden Schritt ab – einer möglichst genauen und präzisen Diagnose. Als Patient können sie also in Zukunft weitere entscheidende Optimierungen bei den Diagnoseverfahren erwarten, die sich hoffentlich dann auch in einer verbesserten Therapie ihrer Erkrankung niederschlagen werden. Priv. Doz. Dr. med. Dieter Hörsch Zentrum für Neuroendokrine Tumore Bad Berka Klinik für Innere Medizin, Gastroenterologie, Onkologie, Endokrinologie Zentralklinik Bad Berka Prof. Dr. med. Richard P. Baum Zentrum für Neuroendokrine Tumore Bad Berka Klinik für Nuklearmedizin/ PET Zentrum Zentralklinik Bad Berka Robert-Koch Allee 9 99437 Bad Berka 23 Veranstaltungen 3. Überregionaler Neuroendokriner Tumor-Tag vom 24.-26. November 2006 in Mainz Behandlungsmöglichkeiten bei Lebermetastasen von neuroendokrinen Tumoren – Operation, Lebertransplantation und andere Methoden aus internistischer Sicht Allgemeines Therapiekonzept Das vorrangig angestrebte Therapieziel bei neuroendokrinen Tumoren ist immer die vollständige operative Entfernung des Tumors. Häufig sind zum Zeitpunkt der Diagnosestellung jedoch bereits Tumor­ absiedlungen in der Leber (= intrahepatische Metastasen) oder auch ausserhalb der Leber (= extrahepatische Metastasen) bekannt. Auch für die Behandlung von Lebermetastasen steht prinzipiell eine Vielfalt von lokalen, also direkt an der Leber angreifenden Therapiemöglichkeiten zur Verfügung, welche die Operation mit Leberteilentfernung oder lokal-ablative (= den Tumor lokal abtragende) Therapieverfahren wie Radiofrequenzablation (RFA), Transarterielle Chemoembolisation (TACE) und Selektive Intraarterielle Radiotherapie (SIRT) umfassen. Ergänzend stehen als systemische (= am ganzen Körper wirkende) Therapiemöglichkeiten die Biotherapie mit Somatostatinanaloga (Octreotid oder Lanreotid) oder Interferona, die klassische Chemotherapie oder die Peptidvermittelte RadioRezeptor-Therapie (PRRT) zur Verfügung. Außerdem entwickelt sich als neuer viel versprechender Therapieansatz die so genannte „targeted therapy“ (= zielgerichtete spezifische Therapie) mit spezifischen Medikamenten. In Abhängigkeit von 24 Anzahl und Größe der Metastasen und dem individuellen Krankheitsverlauf sollte eine individuelle Therapieempfehlung gemeinsam von Ärzten verschiedener Fachdisziplinen erarbeitet werden. Operation von Lebermetastasen Bei allen neuroendokrinen Tumoren mit Lebermetastasierung sollte zunächst immer die Möglichkeit einer Metastasenchirurgie und Leberteilentfernung diskutiert werden. Hinsichtlich der Radikalität der Leberchirurgie ergeben sich natürliche Grenzen durch die Funktion der Leber als Stoffwechselorgan mit vielen lebenswichtigen Funktionen. Es muss deshalb genügend gesundes Lebergewebe bei der Operation belassen werden. Klassischerweise kann die operative Entfernung von einzelnen Leberbereichen (Lebersegmentresektion) bzw. des rechten oder linken Leberlappens ( = Hemihepatektomie) erfolgen – dies kommt nur für 10–20% aller Pa­tienten mit Lebermetastasierung in Frage. Durch spezielle neue Operationstechniken und durch die Kombination von Metastasenchirurgie und Radiofrequenzablation (siehe Absatz lokal-ablative Therapieverfahren) konnte in den letzten Jahren das Ausmaß und Häufigkeit der Metastasenchirurgie erweitert werden. Mit dieser neuen Strategie kommt ein Eingriff für 30 – 50 % aller Patienten mit Lebermetastasierung in Frage. Mehrere Studien zeigen, dass die 5-Jahres-Überlebensrate durch eine „aggressive Metastasenchirurgie“ wahrscheinlich verbessert wird und bei 60 – 70 % liegt; bei funktionell aktiven neuroendokrinen Tumoren kommt es auch zur Symptomfreiheit in 70 – 90 % der behandelten Fälle. Da eine bekannte Lebermetastasierung jedoch Ausdruck einer den ganzen Körper betreffenden Systemerkrankung ist und neben den in der Bildgebung sichtbaren Metastasen meist noch unsichtbare Mikrometastasen vorliegen, ist von einer solchen Operation nur selten eine völlige Heilung zu erwarten. Trotz kompletter Entfernung aller sichtbaren Metastasen in der Operation kommt es bei über 80 % aller Patienten innerhalb von fünf Jahren zu einem erneuten Auftreten des Tumors. Eine regelmäßige alle drei bis sechs Monate stattfindende Tumornachsorge ist deshalb auch nach operativer Entfernung aller (sichtbaren) Tumorherde unbedingt notwendig. Lebertransplantation Die Lebertransplantation ist ein etabliertes Therapieverfahren bei Patienten mit Leberzirrhose, aku- Veranstaltungen tem Leberversagen, Gallenwegserkrankungen und bei Patienten mit Leberzelltumor. Patienten mit Lebermetastasen bei verschiedenen Ursprungstumoren stellen dagegen weniger als 1 % aller Patienten mit Lebertransplantation dar. Die Lebertransplantation bei Patienten mit neuroendokrinen Tumoren und Lebermetastasen ist kein etabliertes Verfahren und wird kontrovers diskutiert. Bei bisher weltweit etwa 200 publizierten Patienten mit neuroendokrinen Tumoren und Lebermetastasen konnte nach Lebertransplantation eine 5-Jahres-Überlebensrate von 40 – 80 % erreicht werden; innerhalb von 5 Jahren kommt es bei über 75 % aller Patienten zur erneuten Tumorbildung. Somit erscheinen die Ergebnisse der Lebertransplantation nicht von vornherein besser als die der Operation bei Lebermetastasen; hinzu kommt bei der Lebertransplantation eine hohe 1-Jahres-Mortalität (= Sterblichkeit) von mindestens 10 %. Eine Transplantation kann deshalb nur im Einzelfall im Rahmen von klinischen Studien angeboten werden – neue strikte Auswahlkriterien für diesen Eingriff sollen helfen, die Ergebnisse langfristig zu verbessern. Lokal-ablative Verfahren Die Radiofrequenzablation ist für einzelne oder wenige (< 5) Lebermetastasen mit einem Durchmesser < 3 – 5 cm geeignet. Hierbei werden die einzelnen Lebermetastasen mit einer dünnen Nadel punktiert; d.h. die Nadelspitze wird in die Lebermetastase eingestochen - dies erfolgt unter Bildkontrolle mittels Ultraschall oder Computertomographie. Über die Nadelspitze wird die Lebermetastasen bei neuroendokrinen Tumoren Operation möglich? operabel 10 – 20% (konservativer Ansatz) 30 – 50% (maximaler Ansatz) nicht operabel 80 – 90% (konservativer Ansatz) 50 – 70% (maximaler Ansatz) ein Leberlappen beide Leberlappen Segmentresektion Hemihepatektomie „One-step”-Operation „Two-step”-Operation Lebermetastase auf eine Temperatur von bis zu 100 Grad Celsius erhitzt und dadurch ein Absterben der Tumorzellen erzeugt. Die Radiofrequenzablation kann entweder bei lokaler Betäubung oder in Vollnarkose durchgeführt werden; die Radiofrequenzablation ist durch die Haut oder während einer Operation direkt an der Leber möglich. Es handelt sich um eine effektive Methode zur lokalen Tumorkontrolle; so kommt es innerhalb eines Jahres nur bei 3 - 4 % der Patienten zu einem Lokalrezidiv (= erneutes Auftreten des Tumors an der gleichen Stelle). Allerdings ist aufgrund der Systemerkrankung (siehe Absatz Operation) im längeren Zeitverlauf häufig mit dem Auftreten neuer Lebermetastasen an anderer Stelle zu rechnen. Die transarterielle Embolisation (TAE) oder Chemoembolisation (TACE) ist für multiple, also mehrfache (> 5) Lebermetastasen jeder Größe geeignet, solange mindestens 30 % gesundes Lebergewebe noch erhalten sind. Hierbei wird die medikamentöse Therapie lokal-ablative Therapie Radiorezeptor-Therapie Debulking-Operation evtl. Lebertransplantation Blutversorgung der Lebermetastasen durch gezielte Embolisation (= Verschluss eines Blutgefässes durch Verstopfung) der zuführenden Leberarterie unterbrochen; durch die Unterbrechung der Blutversorgung kommt es zu einem Sauerstoff- und Nährstoffmagel und dadurch zu einem teilweisen Absterben und zur Wachstumsbehinderung der Lebermetastasen. Bei Durchführung der TAE wird zunächst die Arteria femoralis (= Beinarterie) in der Leistenregion punktiert, ähnlich wie bei einer Herzkatheteruntersuchung. Ein dünner Katheter wird dann unter Röntgenkontrolle bis zur Arteria hepatica (= Leberarterie) vorgeschoben und einzelne Seitenäste der Leberarterie, die den Tumor mit Blut versorgen, werden durch Einspritzen von Mikropartikeln ausgewählt embolisiert. Bei der TACE wird den Mikropartikeln vor der Injektion noch ein Chemotherapeutikum zugemischt, das dann in hoher Konzentration die Tumorzellen erreicht. Durch die TAE und TACE kann in etwa 50 % eine Tumorverkleinerung und bei der 25 Veranstaltungen grossen Mehrzahl der behandelten Patienten eine Symptomverbesserung erreicht werden. Der optimale Zeitpunkt für die TAE/TACE im Krankheitsverlauf ist unklar – jedoch profitieren auch Patienten mit weit fortgeschrittener Tumorerkrankung häufig noch von einer TAE oder TACE. Die selektive intraarterielle Radiotherapie (SIRT) ist wie die TAE für multiple Lebermetastasen jeder Grösse geeignet, solange mindestens 30 % gesundes Lebergewebe noch erhalten sind. Das Grundprinzip besteht wie bei der TAE in der Embolisation kleinster Seitenäste der Leberarterie, welche die Lebermetastasen mit Blut versorgen. Zum Verschluss der Blutgefässe werden kleinste 20-40 µm große, mit einer bestimmten Strahlung beladene Mikropartikel benutzt. Es kommt zum Absterben des Tumorgewebes durch die Unterbrechung der Blutversorgung der Lebermetastasen und durch die zeitgleiche interne Bestrahlung der Lebermetasen mit hoher Tumordosis. Während die SIRT für Patienten mit bösartigen Leberzelltumoren oder Lebermetastasen bei Darmkrebs zugelassen ist, liegen bisher nur limitierte Erfahrungen bei Patienten mit neuroendokrinen Tumoren vor. Ob die Behandlungsergebnisse bei SIRT besser sind als bei TAE lässt sich derzeit noch nicht abschließend beurteilen. Die Behandlung mit SIRT sollte derzeit im Rahmen von klinischen Studien erfolgen. stehen meist mehrere alternative chirurgisch eingreifende und medi­ kamentöse Therapieformen zur Auswahl, die vom behandelnden Arzt mit dem Pa­tienten gemeinsam besprochen werden müssen. Durch eine individuelle Therapieplanung kann eine Verbesserung des Langzeitüberlebens und der Lebensqualität der betroffenen Patienten erreicht werden. Zusammenfassung und Ausblick Auch bei Lebermetastasierung muss zunächst immer die Operabilität überprüft werden. Die Indikation zur Operation und/oder Radiofrequenzablation bei Lebermetastasen hat sich in den letzten Jahren erweitert. Eine „aggressive“ Metastasenchirurgie bringt wahrscheinlich einen Überlebensvorteil mit sich; eine dauerhafte Heilung ist jedoch häufig nicht zu erreichen – eine regelmäßige Nachsorge ist deshalb immer zwingend notwendig. Die Lebertransplantation stellt bisher keine etablierte Therapieoption von Lebermetastasen bei neuroendokrinen Tumoren dar. Aufgrund der Vielfalt der Therapieoptionen PD Dr. med. C. J. Auernhammer. Medizinische Klinik II, Standort Großhadern, Klinikum der LudwigMaximilians-Universität München, Marchioninistrasse 15, 81377 München. Tel. 089 / 7095 – 3003, E-mail: Christoph.Auernhammer@ med.uni-muenchen.de Besuchen Sie unsere Internet-Foren! Wir haben es in der letzten Ausgabe bereits angeprochen: Im Internet bieten wir Ihnen die Möglichkeit, sich schnell und umfassend mit anderen Betroffenen auszutauschen. Dabei stehen Ihnen Foren zu verschiedenen Themen zur Verfügung. Neben „Ankündigungen” und einem „Allgemeinen Forum” sind dies im Einzelnen „Karzinoid”, „Gastrinom”, „Insulinom”, „Lebermetastasen”, „Diagnostik”, „Therapie” und „Andere Neuroendo­ krine Tumoren”. Zusätzlich ist Platz für Wünsche, Kritik und Anregungen zu diesem Angebot und zur Website allgemein. Die Anmeldung ist ganz unkompliziert und mit wenigen Angaben möglich. Die Adresse: http://www.glandula-online.de/karzinoid/forum/phpBB2net/ index.php – oder Sie klicken einfach auf der Startseite www.neuroendokrine-tumoren.de die Rubrik „Forum” an. Wir freuen uns auf Ihre rege Teilnahme! 26 Veranstaltungen 3. Überregionaler Neuroendokriner Tumor-Tag vom 24.-26. November 2006 in Mainz Neue und bewährte medikamentöse Therapieoptionen Die Behandlung von Patienten mit Neuroendokrinen Tumoren (NET) ist sehr individuell. Es stehen verschiedene Behandlungsmöglichkeiten zur Verfügung. Diese sind entweder im gesamten Körper wirksam (so genannte systemische Therapie) oder richten sich gezielt gegen Lebermetastasen. Treten Absiedlungen des Tumors außerhalb der Leber auf, ist den systemischen Ansätzen der Vorzug zu geben. Systemische Therapien werden über Injektionen in die Bauchdecke oder über einen Venenzugang verabreicht. Die am häufigsten eingesetzten Therapien sind Somatostatinanaloga (Octreotid, Lanreotid) und Interferon-alpha. Beide Substanzgruppen wurden Mitte der 80er Jahre in die Behandlung der NET eingeführt und haben bei der Mehrheit der Patienten durch Hemmung der Hormonausschüttung und der damit verbundenen Reduktion von Flush und Durchfällen zu einer wesentlichen Verbesserung der Lebensqualität geführt. So werden durch Einsatz von Somatostatinabkömmlingen in 70-90 % die Beschwerden des Karzinoid-Syndroms (Flush, Durchfall, gegebenenfalls asthmaähnliche Zustände) gebessert, durch Interferon-alpha in 40 -70 %. Eine Hemmung des Tumorwachstums ist dagegen selten und wird bei Einsatz von ­Somatostatinabkömmlingen in ca. 5 %, unter Interferon-alpha in bis zu 12 % der Patienten berichtet. In Studien, die den Einsatz von Somatostatinanaloga (Octreotid, Lanreotid) und Interferon-alpha, allein oder zusammen verabreicht, untersucht haben, hat sich keine Überlegenheit der Kombinationstherapie gegen­ über der Einzelgabe der Substanzen gezeigt. Die Frage, inwieweit Somatostatinanaloga das Wachstum von NET hemmen, ist noch offen und wird in klinischen Studien mit einem „Scheinmedikament“ (Placebo) derzeit noch untersucht. Insgesamt betrachtet ist davon auszugehen, dass jeder zweite bis dritte Patient noch nach einem Jahr Behandlung von Somatostatinabkömmlingen oder Interferon-alpha profitiert. Dabei ist Wachstumshemmung als ein Behandlungserfolg zu betrachten. Etabliert ist außerdem der Einsatz einer Chemotherapie bei NET der Bauchspreicheldrüse und bei schlecht differenzierten NET unabhängig von der Lokalisation. Letztere wachsen aggressiv und unterscheiden sich in ihrem Wachstumsverhalten nicht von anderen bösartigen Tumoren. Dabei hat sich die Kombination von den chemotherapeutischen Substanzen Streptozotocin und 5-Fluorouracil bei wachsenden Bauchspeicheldrüsentumoren bewährt. Etwa 40-50% der Patienten profitieren von dieser Therapie für 12-24 Monate, in Einzelfällen auch länger. Bei aggressiv wachsenden NET ist der Einsatz der Substanzen Cisplatin und Etoposid Standard. Die Ansprechrate bewegt sich dabei zwischen 46 und 67%. Oftmals kommt es jedoch schon innerhalb eines Jahres zum erneuten Tumorwachstum. Neben der so genannten Biotherapie (Somatostatinabkömmlinge und Interferon-alpha) und der Chemotherapie kommen die Radionuklidtherapie und an der Leber lokal wirkende Strategien, wie Chemoembolisation, zum Einsatz. Zur Bedeutung der Radionuklidtherapie wird auf den Artikel von PD Dr. Helisch (siehe S. 30), Mainz, zur Bedeutung der lokalen Verfahren auf den Artikel von PD Dr. Auernhammer (siehe S. 24), München, dieser Ausgabe verwiesen. Sollten die genannten Therapieverfahren nicht hinreichend sein, können neuartige Methoden in Betracht gezogen werden (s. Abb. 1). Neue Behandlungsmöglichkeiten sind konkret zu erwägen • bei Tumorwachstum • bei unzureichender Symptomkontrolle • bei Versagen etablierter Therapien (Octreotid und/oder alpha-Interferon bzw. Chemotherapie) • bei fehlender Option einer Radionuklidtherapie (negatives Somatostatinrezeptor-Szintigramm) 27 Veranstaltungen (EPT: =endokriner Pankreastumor) Abb.1 Zu den neuen Therapieoptionen gehören neue Somatostatinanaloga, z. B. Pasireotid (SOM230), Hemmstoffe der Gefäßneubildung (Angiogenesehemmer), Hemmstoffe der Tumorzellen und/ oder Gefäßzellen (molekular-zielgerichtete Therapien) und neue Chemotherapeutika. Pasireotid wirkt an vier von fünf Bindungsstellen (Rezeptoren) für Somatostatin, während Octreotid vorzugsweise über zwei Bindungsstellen wirkt. Über die Rezeptoren werden hemmende Signale vermittelt, wie Hemmung der Hormonausschüttung und des Tumorwachstums. Die zur Zeit nur in klinischen Studien einsetzbare Substanz Pasireotid führte bei gut einem Viertel der Patienten, die bereits mit Octreotid vorbehandelt waren und noch Beschwerden des KarzinoidSyndorms aufwiesen, zu einer Beschwerdelinderung mit Rückgang von Durchfällen und Flushanfällen. Bei 20 - 30 % der Patienten traten Begleiterscheinungen wie Müdig28 keit, Gewichtsverlust, Übelkeit und Bauchschmerzen auf. Einige Beschwerden können möglicherweise auch durch die Erkrankung selbst bedingt sein. In einer laufenden Studie unter Leitung der Universitätsklinik in Essen (PD Dr. S. Petersenn) werden verschiedene Dosierungen eines Depotpräparats von Pasireotid bei Karzinoid-Syndrom hinsichtlich Verstoffwechslung und Verträglichkeit erprobt. Ob die neue Substanz stärker hemmend auf das Tumorwachstum wirkt, ist noch unklar. Ansätze zur Hemmung des Gefäßwachstums von Tumoren umfassen den Einsatz von Substanzen, die einen Gefäßwachstumsfaktor im Blut wegfangen (Anti-VEGF, Bevacizumab), Hemmstoffe, die die Andockstelle selbst blockieren, sowie Hemmstoffe, die die Vermittlung von Signalen an der Andockstelle für den Wachstumsfaktor unterbinden (VEGF-Rezeptortyrosinkinasehemmer). Diese Ansätze erscheinen erfolgversprechend, da NET einerseits sehr gefäßreich sind, andererseits den Wachstumsfaktor für Gefäße in über 80 % der Fälle selbst bilden. Die genannten Sub­ stanzen wurden in kleinen Studien, zum Teil in Kombination mit Octreotid oder Interferon-alpha, bereits bei Patienten mit neuroendokrinen Tumoren eingesetzt. Erfolgversprechend ist auch der Einsatz in Kombination mit einer Chemotherapie bei endokrinen Tumoren der Bauchspeicheldrüse (EPT). So führte der Einsatz des Chemotherapeutikums Temozolomid, welches als Tablette eingenommen werden kann, gemeinsam mit dem Gefäßhemmstoff Anti-VEGF zu einer Tumorverkleinerung bei 24 % der Patienten mit EPT. Häufig (in 70-90 % der Fälle) lag auch ein stabiler Tumorbefund vor. Da NET auch spontan zu Wachstumsstillständen neigen, bleibt offen, inwieweit die Substanzen tatsächlich eine Wachstumshemmung des Tumors bewirken. Weitere Zielstrukturen von anderen Wachstumsfaktoren stellen außerdem mögliche Behandlungsansätze dar. Eine Substanz, die sich gegen die Andockstelle für den Epidermalen Wachstumsfaktor (EGF, epidermal growth factor) richtet, wurde bei 96 Patienten mit wachsenden NET eingesetzt. 25 % der Patienten mit endokrinen Tumoren der Bauchspeicheldrüse und 37 % der Patienten mit NET im Darmbereich profitierten von der Behandlung, überwiegend mit einem Stillstand des Tumorwachstums. Einen Vertreter der Substanzen, die sowohl an der Tumorzelle als auch an der Gefäßzelle wirken, stellt die Substanz Sunitinib dar. Es wurde bei über 100 Patienten mit NET eingesetzt. Tumorverkleinerungen wurden wiederum bei 15 % der Pati- Veranstaltungen enten mit EPT beobachtet, Wachstumsstillstände bei über 70 % der Patienten, dagegen bei über 90 % der Patienten mit Lokalisation des Ursprungstumors im Darmtrakt. Auch hier ist unklar, inwieweit die Tumorstillstände durch die Sub­ stanz tatsächlich verursacht sind. Aus diesem Grund wurde kürzlich eine klinische Studie international initiiert, die den Stellenwert der Substanz im Vergleich zu Placebo untersuchen soll. Die Kombination einer Behandlung von Octreotid mit einer Substanz, die eine zentrale Schaltstelle sowohl in der Tumor- als auch der Gefäßzelle blockiert, stellt die Substanz Everolimus (RAD001) dar. Nach ersten Untersuchungen war eine Rückbildung des Tumors bei 18 % der Behandelten mit EPT und 13 % der Patienten mit Tumoren im Darmtrakt zu verzeichnen. Abermals zeigte sich häufig ein Wachstumsstillstand der Tumore. Diese Untersuchung war Ausgangspunkt für insgesamt drei klinische Studien bei NET. Eine Studie bei EPT ist bereits abgeschlossen und befindet sich in der Auswertungsphase. Eine weitere Studie bei Patienten mit Karzinoid-Syndrom wird derzeit in Kombination mit Octreotid weltweit durchgeführt; eine dritte bei EPT im Vergleich zu Placebo ist kurz vor der Initiierung. Insgesamt sind unter Einsatz der neuen Therapien Tumorrückbildungen zwar selten, Wachstumsstillstände jedoch häufig. Die Ansprechraten können durch Kombination mit anderen Therapieprinzipien (Octreotid, Chemotherapeutika) erhöht werden. Weitere Studien sind erforderlich, um den genauen Stellenwert dieser neuen Behandlungsmethoden herauszustellen. Da­ bei ist die Beurteilung des Tumorverlaufs vor Therapiebeginn von Bedeutung. Nähere Informationen erhalten Sie bei der Verfasserin des Artikels. PD Dr. med. M. Pavel Leiterin des Schwerpunkts Neuroendokrine Tumore der Med. Klinik mit S. Hepatologie und Gastroenterologie Interdisziplinäres Stoffwechselzentrum Augustenburgerplatz 1 13353 Berlin Tel: 030/ 450 553032 Email: [email protected] Glossar Chemotherapie: Behandlung von Krebs mit Medikamenten, die die Tumorzellen zerstören Flush: Anfallsartige Gesichtsrötung Somatostatinanaloga: Medikamente, die Abkömmlinge des natürlichen Somatostatins sind und die unkontrollierte Hormonfreisetzung über Somatostatinrezeptoren (siehe dort) auf der Tumorzelle hemmen Somatostatinrezeptoren: Andockstellen für das Hormon Somatostatin auf der Oberfläche von Tumorzellen. Somatostatinrezeptoren kommen auch im normalen Gewebe vor, aber ihre Dichte ist an der Tumorzelloberfläche stark erhöht. 29 Veranstaltungen 3. Überregionaler Neuroendokriner Tumor-Tag vom 24.-26. November 2006 in Mainz Indikation, Planung und Durchführung der Radiopeptidtherapie mit 90Yttrium-DOTATOC Seit mehreren Jahren werden in der Klinik für Nuklearmedizin der Johannes-Gutenberg-Universität Mainz Radiopeptidtherapien mit 90Yttrium-DOTATOC bei Patienten mit metastasierten neuroendokrinen Tumoren durchführt. Die Therapie-Substanz besteht aus einem radioaktiven und einem nicht-radioaktiven Anteil, die stabil miteinander verbunden sind. Der nichtradioaktive Anteil erkennt spezielle Strukturen auf der Zell­oberfläche der neuroendokrinen Tumoren bzw. Metastasen, so genannte Somatostatin-Rezeptoren. Die spezifische Therapie-Wirkung erfolgt dann im Sinne einer inneren Bestrahlung dieser Tumor-Manifestationen. Poten­ziell kritische Organe dieser Therapie sind die Nieren und das Knochenmark. Voraussetzung für die Planung dieser nuklearmedizinischen Therapien ist eine inoperable Befund-Konstellation, die nach Anwendung nichtradioaktiver Therapieformen (z.B. Sandostatin, Interferon oder transarterieller Chemotherapien) weiter fortschreitet. Zudem muss eine möglichst hohe Somatostatin-Rezeptor-Dichte mittels 111Indium-Octreotide-Szintigraphie oder 68Gallium-DOTATOC-PET nachgewiesen sein (Abb. 1 und 2). Die Patienten müssen eine normale Nierenfunktion und eine ausreichende Knochenmarkreserve aufweisen. Bei Patienten mit grenzwertiger Nierenfunktion oder eher ungünstig angesiedelten Metastasen (z.B. diffus 30 in Lunge und Skelett, Abbildung 3) bieten wir eine Kalkulation der Organ- und Tumordosis vor Therapiebeginn an (so genannte Dosimetrie). Ziel ist dabei auch, den Nutzen und das potenzielle Risiko dieser Therapie für den individuellen Patienten besser einschätzen zu können. Abb. 1: (111Indium-Octreotid-Szintigraphie): Nach rein szintigraphischen Kriterien gut für die Radiopeptidtherapie geeigneter Patient mit intensiv Somatostatin-Rezeptorpositiven Herden im Bereich des Pankreas. Abb. 2: (111Indium-Octreotid-Szintigraphie): Szintigraphisch ungeeigneter Patient ohne Nachweis einer gesteigerten Somatostatin-Rezeptor-Dichte. Veranstaltungen Die Radiopeptidtherapie mit 90Yttrium-DOTATOC wird stationär in der Klinik für Nuklearmedizin durchgeführt, hierfür werden die Patienten vier Tage auf unserer Therapiestation aufgenommen (siehe Abb. 4). Am Tag der stationären Aufnahme erfolgt eine Kontrolle wichtiger Laborparameter, wie z.B. Blutbild, Nieren- und Leberwerte sowie eine nuklearmedizinische Bestimmung der Nierenfunktion (MAG3-Clearance). Am zweiten Tag wird dann die Radiopeptidtherapie mit 90Yttrium-DOTATOC gemäß des Protokolls der Deutschen Gesellschaft für Nuklearmedizin und der Deutschen Gesellschaft für Endokrinologie durchgeführt. Begleitende Aminosäure-Infusionen verringern hierbei die Strahlenbelastung der Nieren. Am Entlassungstag wird ein so genanntes Bremsstrahlen-Szintigramm zur Kontrolle der Verteilung des 90Yttrium-DOTATOC erstellt. Nach der Therapie sind dann regelmäßige ambulante Kontrollen des Blutbildes, der Leber- und Nierenwerte erforderlich, nach drei Monaten erfolgt zusätzlich eine Bildgebung mittels Computertomographie (CT) und 111Indium-OctreotideSzintigraphie oder 68Gallium-DOTATOC-PET, um die Notwendigkeit bzw. Möglichkeit einer erneuten Radiopeptidtherapie mit 90Yttrium-DOTATOC zu prüfen. Zusammenfassend ist die Radiopeptidtherapie mit 90Yttrium-DOTATOC für geeignete Patienten eine vielversprechende Therapie-Option, die Wirksamkeit und der längerfristige Verlauf im Anschluss an die Therapie werden derzeit untersucht. Abb. 3: (111Indium-Octreotid-Szintigraphie): Diffuse Metastasen im Knochen und der Lunge, zusätzliche Absiedlungen in der Leber und im Abdomen. Abb. 4: Blick in ein Patientenzimmer auf unserer nuklearmedizinischen Therapiestation. Dr. med. Andreas Helisch Leitender Oberarzt Klinik und Poliklinik für Nuklearmedizin Klinikum der Johannes-GutenbergUniversität Mainz Langenbeckstraße 1, 55101 Mainz Tel.: 06131/17-2984 e-mail:[email protected]. uni-mainz.de 31 3. Überregionaler Neuroendokriner Tumor-Tag vom 24.-26. November 2006 in Mainz Erfolg mit kleinen Schnitten? Minimal-invasive Chirurgie bei neuroendokrinen Tumoren Die Bezeichnung neuroendokriner Tumor (NET) beschreibt die Eigenschaft der Tumorzellen, sowohl Ähnlichkeit mit Nervenzellen („Neuronen“) als auch mit hormonbildenden („endokrinen“) Zellen zu besitzen. Neuroendokrine Tumore sind seltene gut- oder bösartige Neubildungen verschiedenster Organsysteme. Treten sie in Abschnitten des Magen-Darm-Traktes (Gastrointestinaltrakt: Magen, Dünndarm, Dickdarm) oder der Bauchspeicheldrüse (Pankreas) auf, werden sie auch GEP-NET abgekürzt. NET kommen aber ebenfalls in der Nebenniere oder in Nervenzellen des sympathischen und parasympathischen (vegetativen) Nervensystems vor, zum Beispiel als Tumoren des (Nerven-)Grenzstranges neben der Hauptschlagader (Abb. 1A). Sie treten nicht nur im Bauchraum auf: das medulläre oder C-Zell-Karzinom der Schilddrüse ist ebenfalls ein neuroendokriner Tumor (Abb. 1B). Viele NET produzieren Hormone, welche Symptome wie Durchfälle, Hitzewallungen, niedrigen Blutdruck oder Bluthochdruck verursachen oder sogar lebensbedrohende Unterzuckerungen auslösen können. Manchmal kann die Diagnose eines GEP-NET (häufig auch „Karzinoid“ genannt) aufgrund des so genannten „Karzinoid-Syndroms“ gestellt werden; in diesen Fällen liegen in aller Regel bereits hormon-produzierende Tumorabsiedlungen (Toch32 tergeschwülste = „Metastasen“) in der Leber vor. Durch die Hormonbildung werden typische Symptome verursacht wie plötzliche Hitzewallungen mit Rötung von Gesicht und Oberkörper („Flush“), Erweiterungen kleinster Hautgefäße („Teleangiektasien“), Durchfälle und Herzbeschwerden. Neuroendokrine Tumore ohne Hormonbildung werden dagegen aufgrund fehlender Symptome leider häufig erst spät erkannt. Nicht selten werden bei Ultraschall- oder CT-Untersuchungen wegen anderer Erkrankungen Lebermetastasen entdeckt und ein NET stellt sich bei weiterer Suche als die Quelle der Tumorabsiedlungen heraus. Je nach Organbefall und Wachstumsverhalten des Tumors sind unterschiedliche Behandlungen erforderlich; häufig stellt die Operation die Erstmaßnahme dar. Ziel ist dann, die Geschwulst vollständig zu entfernen oder – falls dies nicht möglich ist – die Tumormasse zu verkleinern. Abhängig davon, ob es sich um einen möglicherweise bösartigen oder sicher gutartigen Tumor handelt, muss die Entfernung mit einem größeren Sicherheitsabstand erfolgen. Bei Bösartigkeit („Malignität“) muss ein Sicherheitsabstand zum Tumor eingehalten werden, um eine Aussaat von Tumorzellen, welche möglicherweise ein erneutes Tumorwachstum verursachen können, zu Abb. 1 verhindern. Keinesfalls sollte während der Operation die (bindegewebige) Kapsel des Tumors verletzt oder in den Tumor hineingeschnitten werden. Vor einer chirurgischen NET-Therapie sollte geklärt werden, wie groß der Tumor ist bzw. welche Beziehung er zu den Nachbarorganen Veranstaltungen hat. Ob nur ein Tumor vorhanden ist oder ggf. mehrere an unterschiedlichen Stellen in einem Organ (Abb. 1C) oder in verschiedenen Organen vorliegen, hat ebenso Einfluss auf das operative Vorgehen. Trotz umfangreicher und modernster bildgebender Diagnostik (CT, Kernspin [MRT], Szintigraphie etc.) können die unterschiedlichen Lokalisationen der NET nicht immer bereits vor dem chirurgischen Eingriff entdeckt werden. Der erfahrene Chirurg sucht dann während der Operation den Tumor und seine Absiedlungen an den typischen Stellen durch Tasten, Ultraschall, Diaphanoskopie ( = Durchleuchten von Körperteilen mittels sichtbarem Licht, Abb. 2). Bei hormon-produzierenden NET ist häufig eine besondere Vorbehandlung vor der Operation oder Nachbehandlung nach der Operation notwendig, um die sich mit dem Eingriff plötzlich verändernde hormonelle Situation abzudämpfen. So benötigen Patienten mit einem Insulin-produzierenden Tumor in der Bauchspeicheldrüse („Insulinom“) vor der Operation häufig Zuckerlösungen als Infusionen. Tumoren der Nebenniere oder des Nervengrenzstranges wiederum schütten häufig den Blutdruck steigernde Stresshormone aus. Vor einer Operation muss diese Hormonproduktion durch Medikamente blockiert werden, da es sonst unter der Narkose zu lebensgefährlichen Blutdruckkrisen kommen kann. Trotz einer solchen Vorbehandlung achtet der Chirurg dennoch darauf, diese Tumoren während des Eingriffes möglichst wenig zu berühren, um nicht eine plötzliche Hormonausschüttung zu provozieren. Abb. 2: Diaphanoskopie des Duodenums mittels intraoperativer Endoskopie. Ist ein NET bereits so ausgedehnt, dass er nicht vollständig entfernt werden kann, ist ein chirurgischer Eingriff möglicherweise dennoch sinnvoll: die Masse der Tumorzellen und damit der ausgeschütteten Hormone kann so verringert werden („Debulking“), dass der Patient keine Beschwerden oder zumindest nur noch erträgliche Symptome zurückbehält. Des Weiteren kann eine Verringerung der Tumormasse vor Beginn weiterer Therapien mit Medikamenten wie DOTATOC oder Interferon sinnvoll sein, da die Sub­ stanzen auf die wenigen verbliebenen Tumorreste besser einwir-­ ken können. Debulking-Operationen können auch verhindern, dass weiteres Tumorwachstum Engstellen in Hohlorganen mit sich bringt: GEPNET können Gallenwege oder den Darm verengen oder ein Abfließen des Bauchspeicheldrüsensekretes verhindern. Schließlich ist für den Chirurgen von besonderem Interesse, ob ggf. eine vererbliche NET-Erkrankung vorliegt. In diesen Fällen besteht nämlich eine hohe Wahrscheinlichkeit, dass mehrere Tumore unabhängig voneinander entstanden sind oder dass nach Jahren wieder neue NET auftreten können. Besteht der Verdacht auf eine erbliche Erkrankung, wird während der Operation intensiv nach weiteren Tumoren gesucht. Ist die Art der Erberkrankung durch Erbgut-Untersuchungen belegt, werden die Familienmitglieder getestet, gegebenenfalls auch untersucht und frühzeitig operiert. In vielen Gebieten der chirurgischen Therapie haben sich in den vergangenen Jahren so genannte endoskopische oder minimal-invasive Eingriffe („Schlüsselloch-Chirurgie“) zunehmend durchgesetzt, welche an den sehr kleinen Hautschnitten erkennbar sind. Über Kunststoffhülsen werden feine Instrumente und eine Kamera („Endoskop“) in den Bauch des Patienten eingeführt. Der Chirurg sieht dann das Operationsfeld per Video-Übertragung. Neben den kosmetischen Vorteilen entstehen in einer solchen Operation weniger Gewebeschäden, so dass der Eingriff für den Patienten weniger belastend und schmerzhaft verläuft. Auch wenn die Vorteile dieser neuen operativen Verfahren überzeugen, kann die Schlüsselloch-Chirurgie jedoch nicht in jedem Falle angewendet werden. Ein wesentlicher Nachteil dieser Techniken ist nämlich, dass der Chirurg seine Hände nicht mehr zum Abtasten der Organe während der Operation („digitale Palpation“) ver33 wenden kann, denn gerade bei den sehr schwer aufzufindenden NET liefert der Tastsinn entscheidende Informationen (Abb. 3). Zudem wird bei bereits bekannt bösartigen Tumoren ein offener Zugang - also ein normaler Bauchschnitt – empfohlen. Es ist nämlich nicht belegt, ob der Krebs und insbesondere seine kleinen Absiedlungen in Lymphknoten oder anderen Geweben in der Tumorumgebung mit der minimal-invasiven Methode genauso gründlich entfernt werden können wie beim normalen offenen Eingriff. Bei großen Geschwulsten, selbst bei gutartigen, ist eine Schlüsselloch-Chirurgie nicht sinnvoll, da der Tumor wegen einer möglichen Aussaat von Tumorzellen nicht im Körper zerschnitten werden darf, um durch den kleinen Hautschnitt zu passen. Entsprechend ist das minimal-invasive Vorgehen zur NETBehandlung in jedem Einzelfall abzuwägen und mit dem Patienten zu besprechen. Bewährt haben sich endoskopische Verfahren zur Entfernung von NET bei: • Tumoren der Nebenniere (Phäochromozytom) • Grenzstrangtumoren (Paragangliom) • bestimmten Magentumoren •einzelnen neuroendokrinen Tumoren der Bauchspeicheldrüse (Pankreas) •Tumoren des Dickdarms (Colon) und des Blinddarms (Appendix) Für die Nebenniere sind minimalinvasive Operationen bei Tumoren, welche kleiner als 6-8 cm sind und keine erkennbaren Hinweise auf eine Bösartigkeit liefern, zum bevorzugten Verfahren geworden („Gold Standard“). Sowohl die rechte als 34 Abb. 3: Digitale Palpation des Pankreaskopfes. auch die linke Nebenniere lassen sich auf diese Weise durch die Bauchdecke oder durch einen Zugang vom Rücken bzw. der Seite aus ohne Eröffnung der eigentlichen Bauchhöhle entfernen. Bei sicher gutartigen kleinen Tumoren kann hierbei versucht werden, einen Teil des Nebennierengewebes mit seiner lebenswichtigen Hormonproduktion zu erhalten. Dies ist insbesondere bei jungen Patienten mit vererblichen NET-Erkrankungen von Vorteil, da in diesen Fällen häufig bereits ein Tumor in beiden Nebennieren vorliegt oder deren Auftreten im weiteren Leben erwartet werden kann. Auch hormonbildende Tumore des so genannten Grenzstranges - eines Anteils des vegetativen Nervensystems - welcher im Bauchraum neben der Hauptschlagader (Aorta) gelegen ist, können gegebenenfalls durch minimal-invasive Eingriffe in spezialisierten Zentren entfernt werden. Weniger häufig ist eine endoskopische Entfernung von NET des Verdauungstraktes möglich. Neuroendokrine Tumore des Magens (Abb. 1D), welche als knollenartige Vorwölbungen („Polypen“) in Erscheinung treten, können manchmal im Rahmen einer Magenspiegelung vollständig abgetragen werden, solange sie eine bestimmte Größe nicht überschreiten und keine Absiedlung von Tumorzellen in den angrenzenden Lymphknoten vorliegt. Schlüsselloch-Chirurgie bei bestimmten neuroendokrinen Tumoren der Bauchspeicheldrüse (z.B. Insulinom) wird bisher nur sehr selten in weltweit wenigen spezialisierten Zentren durchgeführt. Dabei hat nur eine geringe Anzahl von Chirurgen mehr als 20 solcher Eingriffe durchgeführt. Bei diesen ausgewählten Fällen sind die Ergebnisse hinsichtlich der Komplikationen mit offenen Bauchschnitten vergleichbar. In jedem dritten bis sechsten der minimal-invasiv begonnenen Eingriffe muss jedoch zu einem offenen Verfahren gewechselt werden, z.B. da der Tumor ohne Tastsinn des Chi­ rurgen nicht auffindbar ist. In anderen Fällen kommt aufgrund der Lokalisation des Tumors (z.B. im darmnahen Bereich [„PankreasKopf“] der Bauchspeicheldrüse nahe an den Gallenwegen) oder bei vermuteter Bösartigkeit, aber auch bei Vorliegen mehrerer Tumoren (Abb. 1D) ein minimal-invasives Vorgehen nicht in Frage. Insbesondere bei einer familiären/vererblichen Grunderkrankung wie der Multiplen Endokrinen Neoplasie Typ 1 (MEN1) sollte die gesamte Bauchspeicheldrüse und der Zwölffingerdarm („Duodenum“) freigelegt und vom Chirurgen sorgfältig durchsucht werden, um nicht kleinere Tumore zu übersehen (Abb. 4). Zusammenfassend ist somit ein minimal-invasives Vorgehen Veranstaltungen Abb. 4: Insulinome des Pankreas bei MEN1 bei NET der Bauchspeicheldrüse nur für sehr wenige Patienten geeignet, und Langzeitergebnisse der so operierten Patienten müssen noch abgewartet werden. Im Gegensatz zu Hormon-bildenden Tumoren der Bauchspeicheldrüse - wie z.B. dem Insulinom und Gastrinom - führen nicht-hormon-bildende NET des Pankreas erst spät zu Symptomen, so dass die Erkrankung häufig erst in einem fortgeschrittenen Stadium erkannt wird. Nicht selten liegen in diesen Fällen große Tumore vor, die bereits in benachbarte Organe hineingewachsen sind oder bereits Absiedlungen in die Leber oder in Lymphknoten des Bauchraumes gesetzt haben (Abb. 1E). Im Gegensatz zum Pankreaskarzinom - also dem „normalen“ Krebs der Bauchspeicheldrüse, der von den so genannten exokrinen (verdauungssaft-produzierenden) Zellen ausgeht – ist selbst bei fortgeschrittenen NET der Bauchspeicheldrüse eine operative Entfernung des gesamten oder nahezu gesamten Tumors zumeist sinnvoll. Diese Eingriffe sind nicht minimal-invasiv möglich, sondern stellen ausgedehnte Operationen dar, welche mehrere Organsysteme betreffen können. GEP-NET des Dünndarms, des Blinddarms und des Dickdarms werden leider in der Regel recht spät als Zufallsbefund erkannt, nicht selten im Rahmen einer NotfallOperation wie bei einem Verdacht auf Blinddarmentzündung („Appendizitis“) oder auf Darmverschluss. Obwohl kleine NET des Darms prinzipiell minimal-invasiv entfernt werden könnten, erfolgt dies aufgrund der vor der Operation unbekannten Diagnose bzw. der akuten Situation zumeist nicht. Bei bösartigen NET wird zunächst immer angestrebt, nicht nur den Tumor selbst, sondern auch die häufig Absiedlungen enthaltenden umgebenden Lymphknoten sowie alle einer Operation zugänglichen Metastasen vollständig zu entfernen. Hierzu zählen insbesondere Absiedlungen neuroendokriner Tumore in der Leber (siehe zu diesem Thema auch den Artikel „Behandlungsmöglichkeiten von Lebermetastasen bei NET” S. 24). Dem Chirurgen sind jedoch aufgrund der lebenswichtigen Funktion der Leber, die (im Gegensatz zur Nierenfunktion) nicht künstlich über einen längeren Zeitraum ersetzt werden kann, natürliche Grenzen gesetzt. Wenn durch eine Operation nicht ausreichend funktionsfähiges Lebergewebe erhalten werden könnte oder wenn aus anderen Gründen (Begleiterkrankungen) ein belastender chi­ rurgischer Eingriff nicht möglich ist, stehen heutzutage alternative Therapien zur Verfügung. Eine gezielte Zerstörung einzelner Tumorherde („lokale Ablation“) in der Leber ist möglich, z.B. durch Radiofrequenzablation oder Chemoembolisation. Auch Radio-Nuklidtherapien und Chemotherapien werden statt oder ergänzend zur chirurgischen Therapie eingesetzt. Abschliessend soll betont werden, dass bei neuroendokrinen Tumoren aufgrund der Komplexität der Erkrankungsbilder, der Vielzahl an Therapiemöglichkeiten und der vielen Umstände, welche bei jedem einzelnen Patienten bedacht werden müssen, auch der spezialisierte endokrine Chirurg nicht als Einzelner handelt. Die Beratung des einzelnen Falles in einem Team von Spezialisten unterschiedlicher Disziplinen (Endokrinologen, Nuklearmediziner, ggf. Kinderärzte, endokrinspezialisierte Chirurgen, Radiologen, Pathologen, Humangenetiker) im Rahmen von NET-Konferenzen sehen wir als einen idealen Weg zur optimalen Betreuung des betroffenen Patienten. Prof. Dr. med. Thomas J. Musholt, Petra B. Musholt Endokrine Chirurgie Klinik für Allgemein – und Abdominalchirurgie Klinikum der Johannes-GutenbergUniversität Mainz Langenbeckstrasse 1, 55101 Mainz Tel.: 06131/17-7179 e-mail: [email protected]. uni-mainz.de 35 Veranstaltungen 3. Überregionaler Neuroendokriner Tumor-Tag vom 24.-26. November 2006 in Mainz Behandlung jenseits der Schulmedizin – Über alternative und unterstützende Methoden Der Workshop „Alternative und unterstützende Behandlungsmethoden”, einer von vieren, fand das größte Interesse. Herr Professor Dr. med. Hensen verstand es, die ca. 50 Teilnehmerinnen und Teilnehmer mit Humor und Charme für die Thematik zu begeistern. Erfahrungen Nach einer kurzen Einführung in das Thema bat er um Erfahrungsberichte zu alternativen und unterstützenden Behandlungsmethoden. Es kamen zahlreiche Beiträge zu folgenden Bereichen: • Akupunktur • Blutwäsche • Entspannungsübungen • Meditation/Visualisierung • Ernährung/Nahrungser gänzung • Fussreflexzonenmassage •heilpraktische Verfahren und Naturheilverfahren, z.B. auch nach Kneipp • Homöopathie • Hyperthermie • Reiki • Misteltherapie • spirituelles Heilen • Sport Dem Placebo auf der Spur Professor Hensen erläuterte kurz jeweils Konzepte und geschichtliche Hintergünde einiger weit verbreiteter alternativer Behandlungsmethoden. 36 Insbesondere am Beispiel der Akupunktur und der Homöopathie erklärte er wissenschaftliche Erkenntnisse zum Placeboeffekt. Ihm ist häufig im Rahmen so genannter randomisierter Doppelblindstudien auf die Spur zu kommen. Hier wissen weder Patient noch Mediziner, ob ein Placebo, also ein Scheinmedikament, oder ein wirksames Präparat verabreicht wird. Erfahrungen zeigen nämlich, dass der Mediziner den Patienten oft unbewusst beeinflusst, wenn er ihm wissentlich ein unwirksames Präparat gibt. Hensen verdeutlichte, dass auch so genannte Placebos unter schulmedizinisch-wissenschaftlichen Gesichtspunkten eine deutliche Wirksamkeit aufweisen können. Damit wolle er aber keinesfalls sagen, dass alternative und heilpraktische Verfahren nicht auch aufgrund der Wirkstoffe oder Methoden heilsam oder lindernd sein könnten. Bei den meisten Verfahren sei die Wirksamkeit wissenschaftlich zwar nicht nachgewiesen, sie seien aber sehr wohl oft hilfreich. Resümee Wichtig sei, dass jeder Betroffene herausfinde, welche Verfahren für ihn persönlich die Geeignetsten seien. Jeder könne für sich außerdem ergänzend etwas tun. Dazu gehören etwa gesunde Ernährung, Sport und Bewegung, Entspannung, ein regelmäßiger Tagesablauf und das Bemühen, Ordnung in sein Leben zu bringen. Viele der angesprochenen Verfahren könnten ergänzend zu schulmedizinischen Behandlungsmethoden durchaus zur Heilung beitragen. Das Motto sei dabei: Wer heilt, hat Recht – was heilsam ist, ist zu befürworten. Berichterstatter: Heribert Meyer Veranstaltungen 3. Überregionaler Neuroendokriner Tumor-Tag vom 24.-26. November 2006 in Mainz Das breite Spektrum der NET-Probleme Zu Beginn des Workshops zeigt Prof. Musholt einen Diavortrag über Beispiel-Patienten, die von neuroendokrinen Tumoren (NET) betroffen sind. Dabei zeigt sich, dass viel Überlegung vor der Operation, viel Kenntnis für eine optimale Narkose und Erfahrung in der Weiterbetreuung nach der Operation notwendig sind. Im Beispiel wird über drei Brüder einer PGL-1 Familie berichtet, die an NET des Halses, des Brustkorbes und des Bauches operiert werden mussten. Beim vererbbaren PGL-1, Paraganglioma-Syndrom 1, entstehen aus Geweben des vegetativen (also nicht willentlich beeinflussbaren) Nervensystemes zumeist gutartige Tumoren an der Kreuzung der Halsschlagader, an der Nebenniere und am Grenzstrang, einer Nervenstruktur entlang der Wirbelsäule. Wie bei vielen NET ist es insbesondere die Hormonbildung durch die Tumoren, die die Chirurgen vor schwierige Aufgaben stellt. Demonstriert wird, dass trotz aller allgemeinen medizinischen Regeln für jeden Patienten eine individuelle Operationsstrategie entwickelt werden muss. Durch den Diavortrag neugierig gemacht, fragt eine Workshop-Teilnehmerin nach, welche Tumoren Hormone bilden und welche Probleme sich daraus ergeben. Prof. Musholt erläutert, dass insbesondere Tumoren der Nebenniere und des Grenzstranges Stresshormone wie Noradrenalin, Adrenalin etc. bilden. Jeder kennt die Wirkung die- ser Hormone am eigenen Leibe, wenn man unter Stress steht: das Herz schlägt schneller, der Blutdruck steigt, man bekommt einen roten Kopf, heiße Wangen und kalte Hände, leidet an Kopfschmerzen. Werden Tumoren wie Phäochromozytome nicht vor einer Operation erkannt und durch Medikamente die Hormonausschüttung blockiert, kann es in der Narkose zu nicht beherrschbaren Blutdruckkrisen und Schlaganfällen kommen. Nun ist Gelegenheit, den Spezialisten zur eigenen Krankengeschichte zu befragen. Im Workshop in Mainz zeigt sich dabei das breite Spektrum an Problemen, mit welchen sich NET-Patienten konfrontiert sehen: Ein junger Mann leidet an einem NET des Pankreaskopfes, der direkt an den Dünndarm angrenzende Teil der Bauchspeicheldrüse, mit Absiedelungen in der Leber. Er hat bereits Experten-Meinungen eingeholt und stellt gezielte Fragen: Wann kann ein Pankreaskopf-Tumor herausgeschält werden und wann muss er reseziert werden (Entfernung eines Pankreasteils)? Wie häufig sind Fistelbildungen? Soll man Absiedlungen eines bösartigen Tumors (Metastasen) der Leber einzeitig oder zweizeitig operieren? Prof. Musholt erläutert, dass Tumorgröße und das Einwachsen in den Pankreasgang, über den der Ver- dauungssaft in den Darm abfließt, oder in angrenzende Organe über das Ausmaß der Operation bis hin zur so genannten Whipple-Operation entscheiden. Bei der WhippleOperation wird das Pankreas ganz oder teilweise entfernt. Je näher zum Pankreasgang operiert werden muss, desto höher die Gefahr einer Fistel, d.h., das aggressive säureähnliche Pankreas-Sekret verdaut Bauchspeicheldrüsen-Gewebe und Binde- und Fettgewebe der Umgebung und führt zu Entzündungen im Bauchraum. In ca. 10-30 % der Pankreas-Operationen entstehen Fisteln. Absaugungen (Drainagen) lassen das Sekret dann nach außen abfließen. Hier berichtet eine weitere Patientin, dass die nach ihrer Bauchspeicheldrüsen-Operation entstandene Fistel nach zwei Wochen abgeheilt war. Weiterhin erläutert Prof. Musholt, dass in Fällen von weit verstreuten Tochtergeschwülsten in der Leber mindestens 30 % der Leber mit den entsprechenden versorgenden Gefäßen zurückbleiben muss. Die lebenswichtigen Leberfunktionen wie Blutentgiftung und Aufrechterhaltung der Blutgerinnung können - anders als bei der Niere – nämlich nicht dauerhaft durch eine Dialyse aufrecht erhalten werden. Da die Leber jedoch die Fähigkeit zum „Nachwachsen” besitzt, kann in Einzelfällen zweizeitig operiert wer37 Veranstaltungen den, d.h., verbliebene Metastasen können in einem zweiten Eingriff nach Monaten entfernt werden. Eine Patientin mit einem NET des Dünndarms berichtet, dass sie aus Furcht vor dauerhaften Durchfällen bisher vor einer Operation zurückschreckt. Entscheidend ist, so Prof. Musholt, wie viel Anteile vom Dickdarm während des chirurgischen Eingriffes mit entfernt werden müssen. Da der Dickdarm dem Darminhalt Flüssigkeit entzieht, kann bei der Entfernung eines großen Dickdarm-Anteiles diese Funktion nicht mehr aufrechterhalten werden, und es kann zu Durchfällen kommen. Eine weitere Patientin leidet an einem Insulinom, einem seltenen Pankreastumor, und Tochtergeschwülsten in der Leber. Sie berichtet über ihren langjährigen Krankheitsverlauf und fragt, ob sich Tumor oder Metastasen wieder „redifferenzieren” können, also erneut beginnen, Insulin zu produzieren. Prof. Musholt antwortet, dass es bei NET kaum etwas gibt, mit dem man nicht rechnen muss, aber dass Tumoren im Zeitverlauf eher dazu neigen, zu „entdifferenzieren”, also ihre ursprünglichen, gewebetypischen Eigenschaften wie die Produktion von Insulin dauerhaft verlieren. Nach einem Unfall mit Schlag auf den Bauch sei zufällig ein Tumor im Bauchraum bei ihr entdeckt worden, berichtet eine Teilnehmerin. Die Operation in einem städtischen Krankenhaus musste wegen starker Blutungen abgebrochen werden, der Tumor konnte nicht entfernt werden. Sie sei mittlerweile eine insulinpflichtige Diabetikerin und habe Leistungsabfälle nach bestimmten 38 Mahlzeiten. Es entwickelt sich eine lebhafte Diskussion unter den Patienten, dass eine Portion Glück dazugehöre, als NET-Patient von Beginn an in Expertenhand zu gelangen. So ist vielen Hausärzten nicht bekannt, dass spezialisierte Zentren zur Verfügung stehen, in denen Endokrinologen, Radiologen, Nuklearmediziner, Endokrine Chirurgen etc. betroffene Patienten gemeinsam betreuen oder dass in Mainz die deutschlandweit einzige Professur für Endokrine Chirurgie eingerichtet ist. Zuletzt schlägt die Internistin und Laborärztin Frau Dr. Musholt der Patientin vor, die behandelnde Diabetologin nach neueren Laboruntersuchungen und Behandlungsmethoden zu fragen. Der nächste Workshop-Teilnehmer leidet seit vielen Jahren an einem faustgroßen, unter Interferon zum Stillstand gekommenen neuroendokrinen Tumor des Beckens mit Einwachsen in Beckengefäße und -nerven. Aufgrund der verdrängenden Darmverlegung wurde vor sieben Jahren ein doppelläufiges Colostoma (künstlicher Darmausgang) angelegt. Das Problem ist, dass ca. alle vier Wochen die Bildung von „Kotsteinen” im Enddarm große Beschwerden verursacht. Die Frage an Prof. Musholt lautet deshalb, ob das Colostoma nicht zurückverlegt werden kann. Aber solange die Ursache der Darmverlegung nicht behoben werden kann, ist eine Wiederherstellung der natürlichen Passage nicht sinnvoll. Prof. Musholt erklärt, dass die „Kotsteine” durch Absonderung von Schleim und abgeschilferte Schleimhaut in den leeren Restdarm entstehen und rät, mit einem Stomatherapeuten zu besprechen, ob der Patient nicht eine regelmäßige Spülung des ab- führenden Stoma-Schenkels durchführen kann. Zuletzt berichtet eine MEN2A-Patientin über die Erfahrungen ihrer Familie mit der genetischen Testung, der chirurgischen Behandlung und der Tumornachsorge ihrer Familie an der Uniklinik in Mainz. Bei der Multiplen Endokrinen Neoplasie (MEN2A) handelt es sich um ein vererbbares Tumorleiden, bei dem verschiedene neuroendokrine Tumoren auftreten. Die Patientin war mit einem fortgeschrittenen Schilddrüsenkrebs aufgefallen. Von Prof. Musholt waren dann in einer achtstündigen Operation der Tumor und sämtliche Lymphknoten des Halses entfernt worden. Die genetische Testung der Familie zeigte, dass auch der Sohn und zwei Enkelkinder die MEN2A-Veranlagung in sich trugen. Dadurch konnte der bereits bestehende Krebs des symptomlosen Sohnes operiert werden. Bei dessen acht bzw. neun Jahre alten Kindern erfolgte eine so genannte „prophylaktische” Operation, d.h., die Schilddrüse wurde entfernt, damit sich erst gar kein bösartiger Tumor entwickeln kann, und die fehlenden Schilddrüsenhormone werden durch eine tägliche Tablette ersetzt. Allerdings zeigte die feingewebliche Untersuchung, dass bei dem älteren Jungen bereits ein Krebs bestand, der somit jetzt geheilt ist. Die Großmutter berichtet nun, dass in ihrer Heimat im Saarland die zeitnahe Durchführung der Tumornachsorge-Untersuchung wegen der fehlenden Spezialisten für MEN2A ein Problem darstellt. Die Familie wird daher auch weiterhin in Betreuung bei der Endokrinologie und Endokrinen Chirurgie in Mainz bleiben. Dr. Petra B. Musholt Veranstaltungen Bericht über die Teilnahme des Netzwerks NeT e.V. an der 51. Jahrestagung der Saarländisch-Pfälzischen Internistengesellschaft vom 22.-24. Februar 2007 in Neustadt i. d. Pfalz Renommierter Internisten-Kongress mit Kardinal Lehmann Vom 22. bis 24. Februar fand in Neustadt an der Weinstrasse unter der Präsidentschaft von Prof. Dr. Weber der Jahreskongress der Saarländisch-Pfälzischen Internistengesellschaft e.V. (SPIG) statt. Die Tagung, welche in diesem Jahr unter dem Motto „Innere Medizin im Spannungsfeld zwischen Allgemeinmedizin und Spezialisierung“ stand, hat sich als größter internistischer Kongress für die Region Saarland und Rheinland-Pfalz etabliert. Sie fand bereits zum 51. Mal statt. Neben zahlreichen internistischen Fachreferaten und Seminaren bot der Kongress auch eine wichtige Plattform für interessierte Angehörige und Patientenselbsthilfegruppen wie zum Beispiel für das Netzwerk NeT e.V.. Es war mit einem eigenen Stand auf der gesamten dreitägigen Veranstaltung anwesend. Nur durch den selbstlosen und unermüdlichen Einsatz der Netzwerk-Mitarbeiter, Frau Ingeborg Schäfer und Herr Prof. Weber am Stand des Netzwerks NeT. Zusammen mit ihrem Ehemann beantwortete Frau Schäfer allen Interessierten ihre Fragen und stand sowohl Ärzten als auch Patienten mit Rat und Tat sowie Informationsmaterial zur Verfügung. oft auch trotz der eigenen gesundheitlichen Beschwerden, gelingt es so, wertvolle Kontakte zu knüpfen. Auch kann so die Aufmerksamkeit bei den ärztlichen Kollegen aus der Klinik und Praxis für das Netzwerk und diese seltenen und immer noch oft übersehenen Erkrankungen geweckt werden. Dieser Einsatz, letztendlich stellvertretend für alle Patienten mit neuroendokrinen Tumorerkrankungen, ist nicht hoch genug zu bewerten. begleitung. Als Hauptredner referierte der Bischof von Mainz und Vorsitzender der Deutschen Bischofskonferenz Karl Kardinal Lehmann zu moraltheologischen Überlegungen zur Leidminderung und Lebensverlängerung in der modernen Medizin. Ausführliche Informationen zum Vortrag von Kardinal Lehmann können bei Interesse unter der unten angegebenen Kontaktadresse angefordert werden. „Als Tagungspräsident war es mir ein besonderes Anliegen auf diesem Kongress auch auf die Probleme von Patienten, Angehörigen und behandelnden Ärzten im Umgang mit schwerst- und todkranken Menschen aufmerksam zu machen und neue fachübergreifende Wege in diesem Grenzbereich der Medizin aufzuzeigen“ so Prof. Karl Kardinal Lehmann bei seinem viel beachteten Plenarvortrag Weber. Ein be- „Der Mensch in Leid und Leiden” auf dem Eröffnungssymposium sonderer Schwer- der Saarländisch-Pfälzischen Internistentagung. punkt auf der diesjährigen Tagung war daher auch Dr. med. Christian Fottner das Vorsymposium zum Thema der Schwerpunkt Endokrinologie und Palliativmedizin (lindernde Medizin). Stoffwechselerkrankungen, In dieser sehr prominent besetzten I. Medizinische Klinik und Poliklinik Veranstaltung sprach neben Vertre- Klinikum der Johannes-Gutenbergtern von Hospiz- und PalliativmeUniversität Mainz dizin auch der Vorsitzende Richter Langenbeckstrasse 1, 55101 Mainz am Bundesgerichtshof a. D. Herr Tel.: 06131/17-7260 Kutzer über rechtliche Aspekte der e-mail:[email protected]. Patientenautonomie und Sterbeuni-mainz.de 39 Erfahrungsberichte Eine Transarterielle Chemoembolisation – Erlebnisbericht eines Patienten Diagnose und medikamentöse Behandlung Im April 1996 wurde bei mir anlässlich einer Darmoperation ein neuroendokriner Tumor diagnostiziert. Bei einer anschließenden Untersuchung der Leber sind zwei etwa 1,2 cm große Metastasen festgestellt worden. Inzwischen sind einige weitere Metastasen entstanden, und die Größte ist, trotz Behandlung mit Sandostatin, auf etwa 4 cm Durchmesser angewachsen. Zunächst wurde versucht, das weitere Wachstum der Metastasen mit Interferon zu bremsen. Doch waren die Nebenwirkungen dieses Medikamentes bei mir so ausgeprägt, dass ich es nach einem halben Jahr absetzen musste. Danach sollte eine Yttrium DOTATOC-Therapie durchgeführt werden. Nach einer ambulanten Untersuchung in der Zentralklinik Bad Berka bekam ich den Bescheid, dass diese Therapie bei mir nicht möglich ist. Das Somatostatin-Analogon, welches das radioaktive Ittrium-Isotop zu den Metastasen transportieren soll, dockt an den Tumorzellen nicht ausreichend intensiv an. Um die Tumormasse in der Leber zu reduzieren, wurde mir danach eine „Transarterielle Chemoembolisation“ (TACE) empfohlen. Bei diesem Verfahren wird von der Leiste aus ein Katheter durch die Arterie bis in die Leber und dort möglichst nahe an die zu behandelnde Metastase eingeführt. Dann wird durch diesen ein Zellgift eingespritzt und diese Arterie danach verschlossen. Da die Metastasen in der Leber zu fast 40 100 % über die Arterie versorgt werden, und das gesunde Lebergewebe nur zu 25 % (die übrige Versorgung des gesunden Gewebes erfolgt über die Pfortader), sammelt sich das Zellgift vorwiegend in den Metastasen. Zusätzlich wird durch die verschlossene Arterie die weitere Versorgung der Metastasen mit Sauerstoff und Nährstoffen behindert. Ende September 2006 fand dann ein Vorgespräch bei Prof. Dr. Uder in der Radiologie der Uniklinik Erlangen statt. Zur Vorbereitung darauf habe ich den Beitrag von Prof. Dr. Wagner in der GlandulaNeT 7/2006 (Seite 39) gelesen. Er beschreibt dort nicht nur die Therapie TACE, sondern auch die „selektive interne Radiotherapie“ (SIRT). Auch bei dieser Therapie wird ein Katheter über die Arterie bis zur Leber eingeführt, dann aber ein radioaktiver Strahler (Yttrium-90) eingespritzt, der das Tumorgewebe zerstören soll. Von beiden Therapien sind in dem Beitrag von Prof. Dr. Wagner Bilder einer Leber jeweils vor und nach der Behandlung zu sehen. Vor der Behandlung waren in beiden Bildern der Leber etwa gleich viel und gleich große Metastasen zu erkennen. Nach einer TACE-Behandlung war eine Metastase weniger vorhanden. Um weiter Metastasen zu behandeln sind dann mehrere Sitzungen notwendig. In der nach dem SIRT-Verfahren behandelten Leber sind nach einer Therapie keine Metastasen mehr zu erkennen. Die Aussicht, nach einer Behandlung von allen Metastasen in meiner Leber befreit zu sein, hat mich dazu bewogen, auch die SIRT-Therapie in Erwägung zu ziehen. Leider hat Herr Prof. Dr. Wagner im Anschluss an seinen Vortrag in der ­ Glandula NeT nur erwähnt, dass Komplikationen und Nebenwirkungen auftreten können, ohne zu konkretisieren. Da die Yttrium DOTATOC-Therapie nach den Ergebnissen der Untersuchungen in Bad Berka für mich nicht durchführbar war, SIRT aber dasselbe Isotop Yttrium-90 als Strahler verwendet, fragte ich bei dem Vorgespräch Herrn Prof. Dr. Uder nach den Komplikationen und Nebenwirkungen dieser Therapie. Danach vereinbarten wir einen Termin für eine TACE-Behandlung. Im Krankenhaus Am 11.10.06 meldete ich mich pünktlich um 9 Uhr auf der Station Henning im nichtoperativen Zentrum der Universitätsklinik in Erlangen. Da noch kein geeignetes Bett für mich frei war, hatte ich Zeit, den Speisezettel zu lesen. Cordon bleu und fränkischer Schweinebraten waren als die nächsten beiden Mittagsmahlzeiten angekündigt. Kurz vor 12 kamen auch die Wagen aus der Küche auf der Station an und mit ihnen der Duft von Cordon bleu. Gleichzeitig sprach mich eine Schwester an und sagte mir, jetzt sei wenigstens vorübergehend ein Bett und ein Zimmer frei. Ich holte meinen Koffer und sie zeigte mir den Weg. Im Zimmer angekommen bat sie mich um meinen linken Arm. Nicht mal fünf Minuten später saß Erfahrungsberichte ich mit einem Stück dünnen Stoff bekleidet, in den zwei Löcher für die Arme geschnitten waren, und der am Rücken mit drei angenähten Stoffstücken zusammengebunden war, am Bettenrand und vor mir ein fahrbares Gestell, an dem eine Wasserflasche und ein Plastiksack hingen, die über einen Schlauch mit einem Zugang im Arm verbunden waren. Da wurde mir langsam klar, dass es an diesem Tag für mich kein Cordon bleu mehr gibt. Die ganzen beiden Tage vergingen ähnlich turbulent und endeten damit, dass ich nach der Entlassung am zweiten Tag abends gegen 19 Uhr nochmals beim Pförtner nach meiner fehlenden linken Sandale fragte. Sie war auf dem Rücktransport vom Bettenhaus zum nichtoperativen Zentrum unbemerkt vom Wagen gefallen. Der unbekannte Finder hat sie kurz vorher beim Pförtner abgegeben. Damit hatte ich wieder alles, was ich am Tage vorher mitgebracht hatte. Grund für manche Überraschungen war, dass ich bei dem Vorgespräch bei Prof. Dr. Uder nicht abgewartet habe, bis er mir den Ablauf des Eingriffes vollständig erklärt hat. Nachdem ich die Therapie SIRT ins Gespräch brachte, wurde nur noch über die beiden Therapien gesprochen. Deswegen erfuhr ich nicht, dass der Patient nach dem Eingriff 24 Stunden lang weder im Bett sitzen noch vom Bett aufstehen darf. Auch ein Patient, der kurz vorher die gleiche Therapie mitgemacht hat, und den ich nach seinen Erlebnissen gefragt habe, hat mich darüber nicht aufgeklärt. Ich habe mir vorgenommen, bei solchen Gesprächen in Zukunft erst dann Fragen zu stellen, wenn ich dazu aufgefordert werde. Gegen 16 Uhr sollte ich in die Interventionelle Radiologie kommen. Vorher musste ich alles, was nicht fest am Köper angewachsen war, ablegen. Daher sind auch alle folgenden Zeitangaben nur geschätzt. Ein Arzt in der Ausbildung hat mich begleitet. Dort angekommen erfuhren wir, dass noch mindestens eine Stunde vergehen wird, bis meine Therapie beginnen kann. Wir nutzten die Zeit, um die Eingangsuntersuchung nachzuholen. Allerdings waren einige Untersuchungen nicht möglich, da wir im Flur auf zwei Stühlen warteten. Etwa um 17 Uhr wurden wir in den Behandlungsraum gerufen. Dort wartete bereits das Team, bestehend aus Prof. Dr. Uder, einem Oberarzt und einer Assistentin auf uns. Ich durfte mich auf eine Liege legen. Danach wurde die vorgesehene Zugangsstelle zur Arterie rasiert, desinfiziert und vermutlich ein Schmerzmittel injiziert. Nachdem ich beim Versuch, die Arterie anzuschneiden einen leichten Schmerz gespürt und offensichtlich leicht gezuckt habe, wurde nochmals ein vermutlich etwas stärkeres Schmerzmittel gespritzt. Danach habe ich während der gesamten Behandlungsdauer keinerlei Schmerzen mehr gespürt. In den ersten Teil der Arterie wird, wohl zur Schonung, ein dünner Plastikschlauch eingeführt. Beim Einführen des Katheters spürt man manchmal ein leichtes Kribbeln. Unter Sichtkontrolle wird der Katheter möglichst nahe an die zu behandelnde Metastase vorgeschoben. In meinem Fall scheint er die Metastase gut erreicht zu haben, jedenfalls meine ich einmal gehört zu haben, ich wäre der ideale Patient für diese Therapie. Im Anschluss an das Einspritzen des Zellgiftes wird die Arterie ver- schlossen. Als Patient fühlt man dabei lediglich den Temperaturunterschied zwischen der Körpertemperatur und der Temperatur der eingespritzten Flüssigkeit, ähnlich wie beim CT, wenn das Kontrastmittel eingespritzt wird. Danach wird der Katheter und der Plastikschlauch aus der Arterie entfernt, die Schnittstelle, ähnlich wie nach dem Ziehen der Nadel nach einer Blutentnahme, jedoch mindestens 10 Minuten lang abgedrückt und schließlich ein Druckverband angelegt. Dann wurde ich noch von der Liege in ein Krankenbett gehoben und auf dem Flur abgestellt. Der mich begleitende Arzt bestellte noch den Transport zur Station Henning und bat die Nachtschwester, auch hin und wieder nach mir zu schauen. Auf der Uhr im Flur war es inzwischen 18:30 Uhr. Nach einer guten Stunde kam der Transportdienst und brachte mich zur Station zurück. Gegen Mitternacht wachte ich einmal wegen Bauchschmerzen auf. Da ich nach einer Stunde noch nicht wieder eingeschlafen war, ließ ich mir ein Schmerzmittel geben und schlief dann bis zum Morgen durch. Abgesehen davon, dass ich nicht aufstehen durfte, ging es mir gut. Am Nachmittag kamen zwei Krankenschwestern und wollten den Druckverband entfernen. Dazu musste die Binde immer wieder unter meinem Rücken auf die andere Seite durchgegeben werden. Um dies den Krankenschwestern zu erleichtern machte ich eine Brücke, so dass ich nur noch mit der Schulter und den Fersen auf der Matratze lag. Doch ich hatte die Länge der Binde unterschätzt. Nach kurzer Zeit hatte ich starke Schmerzen in den Beinen, die mit jeder Sekunde, die ich in dieser Stellung wei41 Erfahrungsberichte ter verharren wollte, schnell größer wurden. Kurz nachdem die Binde entfernt war und ich mich von der Anstrengung erholen wollte, wurde mir plötzlich sehr übel und ich war froh, dass ich das Cordon bleu nicht essen durfte. Bevor die beiden Schwestern aus dem Zimmer gingen. sagten sie noch zu mir, dass sie noch nicht wüssten, wann die CT gemacht werden könne. In diesem Augenblick dachte ich an das Kontrastmittel, und mein Magen fing jetzt an zu rotieren Noch nie hatte ich Probleme damit, das Kontrastmittel in der vorgegebenen Zeit zu trinken. Aber allein der Gedanke daran, dass ich das jetzt trinken müsste, gab mir den Rest. Zum Glück redete niemand mehr von der CT. Nach einer kurzen Untersuchung erhielt ich die Erlaubnis, noch am selben Abend abreisen zu dürfen. 42 Resümee An dieser Stelle möchte ich mich ganz herzlich bei Prof. Dr. Uder und seinem Team bedanken. Ich muss zugeben, dass ich zu Beginn der Behandlung schon etwas nervös war. Aber die ruhige und sachliche Art miteinander zu reden, miteinander die bessere von zwei möglichen Lösungen zu finden und ohne Hektik und trotzdem zügig zum Ziel zu gelangen hat viel dazu beigetragen, dass meine Nervosität bald dem Gefühl weichen musste, bei ihm und seinem Team in guten und kompetenten Händen zu sein. Nach zwei Tagen waren auch die letzten Nachwirkungen des Klinik­ aufenthaltes überwunden. Nun hatte ich das Gefühl, als wäre ich zwei Jahre jünger geworden. Ich hatte wieder Lust Dinge zu tun, die ich im Laufe der letzten Jahre aufgegeben hatte. Und bis heute ist dieser Zustand so erfreulich geblieben. H.-D. Allmendinger Erfahrungsberichte Mit etwas Glück optimaler Verlauf - Leben 20 Jahre nach Operation eines neuroendokrinen Tumors Nicht immer müssen zunächst erlebte Negativerfahrungen den Gesamtverlauf einer Krankheit prägen. In der GlandulaNeT Nr. 3/2002 (S. 13) schilderte Bernhard Zach seinen Krankheitsverlauf. Er erlebte so manche Fehler, Rückschläge und Enttäuschungen. Doch heute kommt er zu einem überraschend positiven Fazit ... Beginn der Stabilisierung In der GlandulaNeT 3/2002 wurde mein Krankheitsverlauf bereits vorgestellt. Der Bericht endete damit, dass ich mich einer fünften Yttrium-DOTATOC-Sitzung, einer mit radioaktiver Substanz arbeitenden Therapie, unterziehen werde. Die weitere Entwicklung schien noch ungewiss. Nun ist glücklicherweise festzustellen, dass der Verlauf seit dieser Behandlung durchaus positiv war. Die fünfte Radionuklidtherapie habe ich gut vertragen. Die kritischen Blutwerte liegen noch alle im Normbereich. Seit 2001 wurden keine neuen Herde bzw. kein Wachstum bei den bekannten Herden festgestellt. „Optimal gelaufen“ 2002 stand mein Bericht unter der Überschrift „Manches hätte besser laufen können“. Heute, im Rückblick auf 20 Jahre Leben mit bekanntem NET, möchte ich den Verlauf meiner Krankheit eher so beschreiben: „Durch Glück und Zufall ist alles optimal gelaufen.“ Soweit ich informiert bin, gibt es nur wenige Patienten, die sich 20 Jahre nach einer NET- Operation der Lunge bzw. 13 Jahre nach einer Rezidivoperation (Operation eines Rückfalls) über eine recht zufriedenstellende Lebensqualität freuen können. Im Rückblick sind die Jahre seit 1994 durchaus positiv verlaufen, obwohl die Prognose nach der letzten Operation gar nicht gut aussah. Glück bei der Ärztewahl Ich glaube, dass ich das vor allem dem Fortschritt der modernen Medizin zu verdanken habe. Bei mir war allerdings insofern etwas Glück im Spiel, dass ich gerade zu diesen Ärzten gekommen bin, die diese neuen Therapiemöglichkeiten kannten. Ich möchte mich auch an dieser Stelle recht herzlich bei allen Ärzten bedanken, die mir zu noch recht guter Lebensqualität verholfen haben. Meiner Ansicht nach waren dabei folgende Ärzte von entscheidender Bedeutung: • Ein Glücksfall war sicher, dass das Rezidiv von einem hervorragenden Chirurgen operiert wurde, der die ausgedehnten Metastasen in einer Sitzung weitestgehend beseitigen konnte. Die Operation wurde in der Thoraxchirurgischen Klinik in Wangen im Allgäu von Chefarzt Dr. Holdt durchgeführt. • Nur durch Zufall bin ich zu Prof. Dr. Eilles am Klinikum der Universität Regensburg (Abteilung für Nuklearmedizin) gekommen, der mir schon 1998 die Radionuklidtherapie in Basel vermittelte. Diese Therapie war wohl damals nur wenigen Ärzten bekannt. Sie war erfolgreich und zeigt in meinem Fall bisher keine negativen Nebenwirkungen. • Ein weiterer Zufall bzw. Glücksfall war auch, dass ich in Basel von einem Arzt die Adresse von Privat-Dozentin Dr. med. Marianne Pavel bekommen habe. Ich kann hierzu nur die Erfahrungen des Leserbriefs (Glandula 8-06, G. M.) bestärken, dass Frau PD Dr. Pavel durch ihr umfassendes Wissen und auch durch ihren enormen Einsatz den NeT-Patienten eine sehr große Hilfe ist. • Eine wichtige Rolle spielte natürlich auch mein Hausarzt, Dr. Schneider, der mit den anderen Ärzten sehr gut kooperiert. Dadurch sind mir oft weite Fahrten, etwa zur Bestimmung von Laborwerten, erspart geblieben. Gründung einer Regionalgruppe geplant In Bezug auf meine Krankheitsgeschichte, kann ich mich dem Leserbriefschreiber G. M. nur anschließen: Ich habe allen Grund zur Dankbarkeit. Deshalb habe ich mich auch entschlossen, eine Regionalgruppe „Bayrischer Wald“ in 43 Erfahrungsberichte Regensburg zu gründen (siehe Hinweis in der Ausgabe 8/06 der GlandulaNeT). Ich möchte damit meine doch schon recht lange Erfahrung als NeT-Patient anderen Betroffenen zukommen lassen. Erfreulicherweise hat sich auch für diese Gruppe ein Spezialist auf diesem Gebiet, Dr. Philipp Hahn (Uniklinik Regensburg), bereit erklärt, uns zu unterstützen. Durch diese Art von Selbsthilfegruppen, wie sie beim Netzwerk üblich sind, können Betroffene nicht nur Erfahrungen austauschen, sondern sie werden auch stets auf dem neuesten Stand über Diagnose- und Therapiemöglichkeiten gehalten. Sicher hat nicht jeder Patient so viel Glück und vielleicht auch nicht so viel Zeit, dass er durch Zufälle an die richtigen Stellen gelangt. Bernhard Zach Regionalgruppe Regensburg Bitte geänderte Tel.-Nr. beachten: 09941- 60 65 14 44 Liebe Leserinnen und Leser, damit wir Ihren Brief oder Beitrag in der nächsten GlandulaNeT abdrucken können, beachten Sie bitte: Redaktionsschluss für Ausgabe 10/2008 ist der 15. Februar 2008 Impressum: GLANDULANeT ist die Mitgliederzeitschrift der bundesweiten Selbsthilfe-Organisation „Netzwerk Neuroendokrine Tumoren (NeT) e.V.“, Sitz Erlangen. Die Zeitschrift erscheint zweimal jährlich. Internet-Adresse: http://www.karzinoid.info oder http://www.neuroendokrine-tumoren.de Herausgeberin: PD Dr. med. M. Pavel, Leiterin des Schwerpunkts Neuroendokrine Tumore der Med. Klinik mit S. Hepatologie und Gastroenterologie, Interdisziplinäres Stoffwechselzentrum, Augustenburgerplatz 1, 13353 Berlin, Email: [email protected] Redaktion: Christian Schulze Kalthoff, Weintraubengasse 10, 90403 Nürnberg ([email protected]) Fotos: privat Layout und Gestaltung: Klaus Dursch, Fürth Druck: Druckerei Raum, Oberasbach Redaktionsanschrift: Redaktion GLANDULANeT, Netzwerk Neuroendokrine Tumoren (NeT) e.V., Waldstraße 34, 91054 Erlangen, Tel. 09131/815046, Fax 09131/815047, E-Mail: [email protected] Diese Zeitschrift und alle in ihr enthaltenen Beiträge sind urheberrechtlich geschützt, Nachdruck nur mit Genehmigung und Quellenangabe. Jede beruflich (gewerblich) genutzte Fotokopie verpflichtet zur Gebührenzahlung an die VG Wort, 80336 München, Goethestraße 49. Keine Haftung für unverlangt eingesandte Manuskripte. Namentlich gekennzeichnete Beiträge geben nicht in jedem Fall die Meinung von Redaktion und Herausgeber wieder. Wichtiger Hinweis: Medizin und Wissenschaft unterliegen ständigen Entwicklungen. Autoren, Herausgeber und Redaktion verwenden größ­tmögliche Sorgfalt, daß vor allem die Angaben zu Behandlung und medikamentöser Therapie dem aktuellen Wissensstand entsprechen. Eine Gewähr für die Richtigkeit der Angaben ist jedoch ausdrücklich ausgeschlossen. Jeder Benutzer muss im Zuge seiner Sorgfaltspflicht die Angaben anhand der Beipackzettel verwendeter Präparate und ggf. auch durch Hinzuziehung eines Spezialisten überprüfen und ggf. korrigieren. Jede Medikamentenangabe und/oder Dosierung erfolgt ausschließlich auf Gefahr des Anwenders. Mit Namen gekennzeichnete Beiträge geben nicht unbedingt die Meinung des wissenschaftlichen Beirats des Netzwerks oder der Redaktion wieder. Die Herausgabe der GlandulaNeT wird gesponsert von