Ein Enzym mit enger Verwandtschaft zu humanen
Werbung

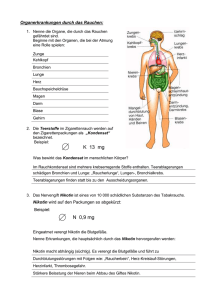
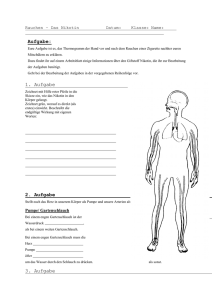
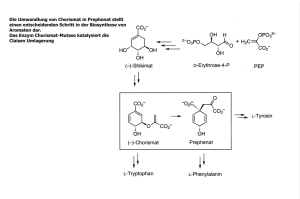
Jahrbuch 2009/2010 | Bartunik, Hans D. | Ein Enzym mit enger Verw andtschaft zu humanen Monoaminoxidasen ermöglicht Bodenbakterium ein Leben von Nikotin Ein Enzym mit enger Verwandtschaft zu humanen Monoaminoxidasen ermöglicht Bodenbakterium ein Leben von Nikotin An enzyme structurally closely related to human monoamine oxidases enables a soil bacterium to live on nicotine Bartunik, Hans D. Max-Planck-Arbeitsgruppen für strukturelle Molekularbiologie am DESY, Hamburg Korrespondierender Autor E-Mail: [email protected] Zusammenfassung Das Bodenbakterium Arthrobacter nicotinovorans „ernährt“ sich von Nikotin. Der Abbau von L-Nikotin und DNikotin erfolgt durch zw ei genetisch nicht verw andte Flavoenzyme, 6HLNO und 6HDNO. Ihre Kristallstrukturen bieten eine Erklärung für die Stereospezifizität der Enzymkatalyse. 6HLNO zeigt in Struktur und Funktionsw eise enge Verw andtschaft zu humanen Monoaminoxidasen (MAO), die eine zentrale Rolle beim Abbau von Neurotransmittern spielen. Die Strukturanalyse von 6HLNO-Reaktionsintermediaten und des Inhibitionsmechanismus erw eitert die Grundlagen für eine mögliche Entw icklung neuer MAO-W irkstoffe. Summary The soil bacterium Arthrobacter nicotinovorans grow s on nicotine. Degradation of L-nicotine and D-nicotine involves tw o genetically unrelated flavoenzymes, 6HLNO and 6HDNO. Their crystal structures may explain the stereospecificity of their enzymatic reactions. 6HLNO by its structure and mechanism is closely related to human monoamine oxidases (MAO), w hich play central roles in degradation of neurotransmitters. Structural analysis of 6HLNO reaction intermediates and the inhibition mechanism extends the basis for possible development of new leads for MAO. Nikotinabbau durch zwei verschiedene Enzyme mit spiegelbildlicher Reaktionsweise Nikotin, das in Tabakpflanzen nahezu vollständig in der (linksdrehenden) L-Form vorliegt und als Insektizid fungiert, dient einer Reihe von Bakterienarten als alleinige Nahrungsquelle, um aus dem Abbau des Alkaloids ihren Bedarf an Kohlenstoff und Stickstoff zu decken [1]. Im Bodenbakterium Arthrobacter nicotinovorans beginnt der Nikotinabbau mit der Hydroxylierung des Pyridinrings an C6. Im darauf folgenden Schritt, der für LNikotin durch 6-Hydroxy-L-Nikotin-Oxidase (6HLNO) und für D-Nikotin durch 6-Hydroxy-D-Nikotin-Oxidase (6HDNO) katalysiert w ird, w ird der Pyrrolidinring zum Myosmin-Intermediat oxidiert. Anschließende Ringöffnung durch Hydrolyse führt zum Produkt 6-Hydroxy-Pseudooxynikotin (Abb. 1). Im menschlichen Körper, der Nikotin (auch) durch Passivrauchen und in vergleichbarer Menge durch Nahrung (bestimmte Gemüse, Tee) aufnimmt, © 2010 Max-Planck-Gesellschaft w w w .mpg.de 1/4 Jahrbuch 2009/2010 | Bartunik, Hans D. | Ein Enzym mit enger Verw andtschaft zu humanen Monoaminoxidasen ermöglicht Bodenbakterium ein Leben von Nikotin beginnt der Abbau von Nikotin zu einem hohen Prozentsatz mit einem direkten Angriff auf den Pyrrolidinring, dessen Oxidation durch die Enzyme Cytochrom-P450 und Aldehydoxidase zur Bildung von Cotinin führen [2]. Nik otina bba u durch Arthroba cte r nicotinovora ns. © MP I-Arbe itsgruppe n für struk ture lle Mole k ula rbiologie a m DESY; a us [3] 6HLNO und 6HDNO sind Flavoenzyme, die mithilfe von FAD-Kofaktoren ein und dieselbe Reaktion an den stereomeren Substraten katalysieren. Die beiden Enzyme w eisen jedoch völlig verschiedene Sequenzen und Konformationen auf. Die Kristallstrukturanalyse von 6HLNO im Komplex mit 6-Hydroxy-L-Nikotin (Abb. 2) zeigt d a s L-Substrat in einer Orientierung relativ zum Isoalloxazinring des Kofaktors, die Hydridtransfer vom Pyrrolidin-Kohlenstoffatom C2’, dem chiralen Zentrum, zum FAD als ersten Reaktionsschritt ermöglicht [3]. Auf der experimentellen Grundlage dieser Komplexstruktur und der Struktur des freien 6HDNO [4] w urde ein Modell der Substratbindung an 6HDNO entw ickelt, das – bis auf eine Spiegelung an der Ebene des Isoalloxazinrings –eine identische Orientierung des D-Substrats relativ zum Kofaktor zeigt. Arthrobacter nicotinovorans setzt also zw ei genetisch nicht verw andte Proteine mit unterschiedlicher Gesamtstruktur und chemisch induzierter Symmetriebeziehung in der Orientierung der spiegelbildlichen Substrate zum Flavinring des Kofaktors ein, um absolute Stereospezifizität der Katalyse zu erreichen. In w eiteren Experimenten gelang es unter Einsatz von Tieftemperaturverfahren, den gesamten Verlauf der Enzymreaktion in 6HLNO-Kristallen vom Andocken des Substrats an die aktive Stelle (Michaelis-Zustand) über das Myosmin-Intermediat bis zur Bildung des Keton-Produkts Pseudooxynikotin in einer Serie von Kristallstrukturen hoher Auflösung zu verfolgen. In Verbindung mit früheren NMR-Messungen w urde damit eine experimentelle Grundlage zur Aufklärung des vollständigen Strukturmechanismus einer Flavooxidase auf molekularer Ebene geschaffen. © 2010 Max-Planck-Gesellschaft w w w .mpg.de 2/4 Jahrbuch 2009/2010 | Bartunik, Hans D. | Ein Enzym mit enger Verw andtschaft zu humanen Monoaminoxidasen ermöglicht Bodenbakterium ein Leben von Nikotin Krista llstruk tur de r 6-Hydrox y-L-Nik otin-O x ida se im Kom ple x m it de m Substra t L-Nik otin. Die Abbildung ze igt e ine Unte re inhe it de s hom odim e re n Enzym s, da s a us de r FADbinde nde n Dom ä ne (cya n) und de r Substra t-binde nde n Dom ä ne m it zwe i Unte rdom ä ne n (S1: rot; S2: la chsfa rbe n) a ufge ba ut ist. Da s Substra t (grün) binde t a n da s a k tive Ze ntrum a n de r Re-Se ite de s FAD-Kofa k tors (ge lb). Die Funk tion e ine s a n S1 ge bunde ne n P hospholipids (gra u) ist noch unbe k a nnt. © MP I-Arbe itsgruppe n für struk ture lle Mole k ula rbiologie a m DESY; a us [3] Enge Verwandtschaft von 6HLNO mit MAO-A und MAO-B Die Aufklärung der Kristallstruktur von 6HLNO [3] zeigte eine enge Verw andtschaft zu einem Humanenzym auf, das am Nikotinabbau nicht direkt beteiligt ist, aber durch Nikotinabbauprodukte inhibiert w ird und am Entstehen der Nikotinabhängigkeit beteiligt ist [5]. Dieses Enzym, die in zw ei Isoformen vorliegende Monoaminoxidase (MAO-A und MAO-B), spielt eine zentrale Rolle bei der Kontrolle der Konzentration von Neurotransmittern w ie Dopamin und Serotonin in der Zelle. MAO-Inhibitoren sind von Bedeutung für die Behandlung einer Reihe von neurologischen Erkrankungen, die insbesondere Parkinson, Alzheimer und me n t a le Störungen einschließen. MAO unterscheidet sich im dreidimensionalen Aufbau von 6HLNO im Wesentlichen durch eine zusätzliche Helix am C-terminalen Ende, die der Verankerung in der mitochondrialen Membran dient. Die aktiven Zentren w eisen ähnliche Lagen und Architekturen auf. Kristallstrukturen zeigten, dass 6HLNO auch die MAO-Substrate Dopamin und Serotonin binden kann. Angesichts der engen Verw andtschaft der Struktur-Funktionsbeziehungen beider Aminoxidasen ist die Kenntnis des genauen Reaktionsw egs und intermediärer Bindungsstellen im 6HLNO-Molekül von potenziellem Interesse für eine mögliche gerichtete Entw icklung von MAO-Inhibitoren. Originalveröffentlichungen Nach Erw eiterungen suchenBilderw eiterungChanneltickerDateilisteHTML- Erw eiterungJobtickerKalendererw eiterungLinkerw eiterungMPG.PuRe-ReferenzMitarbeiter © 2010 Max-Planck-Gesellschaft w w w .mpg.de (Employee 3/4 Jahrbuch 2009/2010 | Bartunik, Hans D. | Ein Enzym mit enger Verw andtschaft zu humanen Monoaminoxidasen ermöglicht Bodenbakterium ein Leben von Nikotin Editor)Personenerw eiterungPublikationserw eiterungTeaser mit BildTextblockerw eiterungVeranstaltungstickererw eiterungVideoerw eiterungVideolistenerw eiterungYouTubeErw eiterung [1] R. Brandsch: Microbiology and biochemistry of nicotine degradation. Applied Microbiology and Biotechnology 69, 493-498 (2006). [2] J. Hukkanen, P. Jacob, N. L. Benowitz: Metabolism and disposition kinetics of nicotine. Pharmacological Review s 57, 79-115 (2005). [3] G. S. Kachalova, G. P. Bourenkov, T. Mengesdorf, S. Schenk, H. R. Maun, M. Burghammer, C. Riekel, K. Decker, H. D. Bartunik: Crystal structure analysis of free and substrate-bound 6-hydroxy-L-nicotine oxidase from Arthrobacter nicotinov orans. Journal of Molecular Biology 396(3), 785-99(2010). [4] J. W. A. Koetter, G. E. Schulz: Crystal structure of 6-hydroxy-D-nicotine oxidase from Arthrobacter nicotinov orans. Journal of Molecular Biology 352, 418-428 (2005). [5] T. P. George, A. H. Weinberger: Monoamine oxidase inhibition for tobacco pharmacotherapy. Clinical Pharmacology & Therapeutics 83, 619-621 (2008). © 2010 Max-Planck-Gesellschaft w w w .mpg.de 4/4