Interpretation von Geschwindigkeitskonstanten nahe der
Werbung

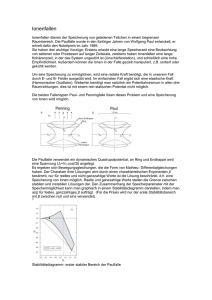
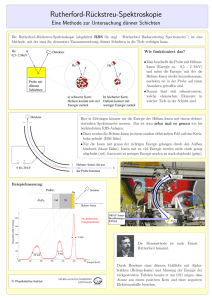
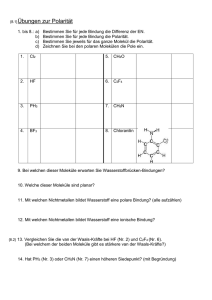
Die Geschwindigkeitskonstante einer diffusionskontrollierten Reaktion • Marian Smoluchowski (18721917) entwickelte 1917 ein theoretisches Modell für die Beschreibung der Koagulation kolloidaler Teilchen in Elektrolytlösungen. • Dieses Modell ist auch auf andere diffusionskontrollierte Prozesse übertragbar. • kdc=diffusionskontrollierte Geschwindigkeitskonstante, kann mit der Smoluchowski-Gleichung berechnet werde. A B P k dc Smoluchowski-Theorie, von Debye auf Reaktionen in Lösung angewendet: kdc 4 N L d12 DA DB Stoßdurchmesser d12=rA+rB A und B nähern sich einander aus dem Unendlichen: Die Reaktion erfolgt sofort, wenn der Abstand d12 erreicht ist. Diese einfache Form der Gleichung gilt nur, wenn keine WechselwirkungsEnergien zwischen den Molekülen zu berücksichtigen sind. Diffusionskoeffizienten • Der Diffusionskoeffizient ist umgekehrt proportional der Viskosität des LM • Stokes-Einstein Gleichung: kB T DA 6 rA Viskosität des Lösungsmittels • Somit ist bei einer diffusionskontrollierten Reaktion die Reaktionsgeschwindigkeit abhängig von der Viskosität des LM • Solche Geschwindigkeitskonstanten und deren Temperaturabhängigkeit sagen NICHTS aus über die Eigenschaften des aktivierten Komplexes! • Falls sich eine Reaktion der diffusionskontrollierten Grenze nähert, ist ihre Geschwindigkeitskonstante nicht mehr leicht zu interpretieren. diffusionskontrollierte Reaktionen > < aktivierungskontrollierte Reaktionen Interpretation von Geschwindigkeitskonstanten nahe der diffusionskontrollierten Grenze • Zweistufiges Schema: – 1. Diffusion der reagierenden Teilchen zueinander und voneinander weg – 2. Reaktion innerhalb des Lösungsmittelkäfigs A B dc k kdc AB P Q kr LM-Käfig Steady-state approximation: AB const d A v k dc A B k dc AB dt d AB 0 k r AB k dc AB k dc A B dt AB k dc A B k r k dc k dc k dc k dc A B v k dc A B k dc A B k dc k r k dc k r k dc kexp k dc k r k r k dc Für sehr großes kr gilt: kexp →kdc Ionenreaktionen in Lösungen • Die elektrostatischen Kräfte zwischen Ionen beeinflussen bestimmte Eigenschaften wie Aktivitätskoeffizienten und elektr. Leitfähigkeit • sowie die Geschwindigkeitskonstanten bei Ionenreaktionen • Auch die Dielektrizitätskonstante (=dielektrische Leitfähigkeit) des LM spielt eine wichtige Rolle, da mit abnehmendem ε die elektrostatischen Kräfte zwischen den Ionen zunehmen. Einfluss der Dielektrizitätskonstante ε des Lösungsmittels • Zwei Ionen A und B befinden sich im Abstand r zueinander. Die elektrostatische Kraft zwischen diesen Ionen ist (Coulomb‘sches Gesetz): z A zB e2 F 40 r 2 = dielektrische Leitfähigkeit oder Dielektrizitätskonstante • Um diesen Abstand um die Strecke -dr zu vermindern, müssen wir die folgende Arbeit aufwenden: z A zB e2 dw dr 2 40 r • Um zwei Ionen aus unendlicher Entfernung auf ihren Stoßdurchmesser dAB zu bringen, muss folgender Betrag an (elektrostatischer) Arbeit aufgebracht werden: w d AB z A z B e dr z A zB e 2 40 r 40 d AB 2 w zählt mit zum Arbeitsaufwand bei der Bildung des Aktivierten Komplexes! positiv, wenn zA und zB gleiches Vorzeichen haben: Aktivierungsenergie erhöht negativ, wenn zA und zB ungleiches Vorzeichen haben: Aktivierungsenergie verringert 2 G kB T k exp h RT 2 z z e NL A B G GN GE GN 40 d AB elektrostatisch nicht-elektrostatisch z A zB e2 N L G 40 d AB z A zB e2 N L kB T ln k ln ln k N RT 40 d AB RT h N • ln k sollte demnach eine lineare Funktion von 1/ε sein, wenn die Geschwindigkeit einer bestimmten Reaktion in einer Reihe von LM mit unterschiedlichem ε bestimmt wird. • Experimentelle Befunde stimmen gut damit überein. Erst bei kleinen Werten von ε tritt Abweichung von der Geraden auf (durch Ionenassoziation). Einfluss gelöster Salze • Beispiel: Bimolekulare Reaktion z z • Die beiden Ionen A A und B B reagieren miteinander • Die Reaktion verläuft über den aktivierten Komplex AB z A z B A B zA z.B. Fe3+ + I- zB AB P (FeI)2+ z A zB Fe2+ + ½ I2 Da Ionen vorliegen, muss die Quasi Gleichgewichtskonstante K durch Aktivitäten ausgedrückt werden: zA zB a (AB) K a A aB Az A B zB A B In die Reaktionsgeschwindigkeit geht jedoch die Konzentration des aktivierten Komplexes ein, nicht seine Aktivität! (AB) zA zB A B K A B zA zB d AzA v k A z A B z B (AB) z A z B dt kB T h A B kB T K A B h zA zB A B kB T kK h H kB T A B k exp h RT S exp R • Nach der Debye-Hückel-Theorie gilt für wässrige Lösungen bei 298 K (Debye-Hückelsches Grenzgesetz für verdünnte Lösungen) log i 0.509 zi2 I 1 I ci zi2 2 i Die Summierung erstreckt sich über alle Ionenarten in der Lösung, nicht nur über die reagierenden Ionen! Brønsted‘sche Gleichung k K kB T A B h A B kB T log k log K log h k T 2 log K B 0.509 z A2 0.509 z B2 0.509 z A z B I h kB T log k log K 1.018 z A z B I h kI 1.018 z A z B I log k I 0 kI für eine wässrige Lösung bei 298 K gegen log Trägt man k I 0 Die Quadratwurzel der Ionenstärke auf, so erhält man eine Gerade, deren Steigung nahezu gleich dem Produkt der Ionenladungen der reagierenden Ionen ist. Änderung der Reaktionsgeschwindigkeitskonstante mit der Ionenstärke = Primärer kinetischer Salzeffekt • Wenn zA und zB dasselbe Vorzeichen haben, dann ist die Steigung der Geraden positiv, die Reaktionsgeschwindigkeit nimmt mit steigender Ionenstärke zu • Wenn zA und zB unterschiedliches Vorzeichen haben, dann ist die Steigung der Geraden negativ, die Reaktionsgeschwindigkeit nimmt mit steigender Ionenstärke ab • Ist einer der Reaktionsteilnehmer ungeladen, dann ist die Reaktionsgeschwindigkeit unabhängig von der Ionenstärke Quelle: Moore/Hummel Rohrzuckerinversion • Die Saccharose hydrolisiert in wässriger Lösung protonenkatalysiert zu D-(+)- Glucose und D-(-)-Fructose. Die Sauerstoffbrücke wird in einem vorgelagerten Gleichgewicht protoniert und schließlich hydrolytisch gespalten: • SH+ + H2O → G + F + H+ • Einer der Reaktionsteilnehmer (H2O) ist ungeladen. Kontrolle der experimentellen Bedingungen • Enthält das System nur die reagierenden Ionen, so ändert sich während der Reaktion die Ionenstärke oft beträchtlich. • Dementsprechend ändert sich der Wert der Geschwindigkeitskonstante während der Reaktion. • Um zuverlässige Werte für die Geschwindigkeitskonstanten von Ionenreaktionen zu bekommen, setzt man der Reaktionsmischung einen Überschuss eines inerten Salzes zu (schwach koordinierende Ionen wie NaNO3 oder NaClO4 oder Natrium-Trifluoromethansulfonat) • Dadurch bleibt die Ionenstärke während der Reaktion praktisch konstant. Geltungsbereich der Brønsted‘schen Gleichung: • Nur bei Konzentrationen erfüllt, die auch im Geltungsbereich der Debye-Hückel Theorie liegen. • Bei höheren Konzentrationen treten Ionenassoziationen auf. • Es ist dann nicht mehr möglich, alle Salzeffekte in dem einfachen Faktor für die Ionenstärke zusammenzufassen! Kinetische Isotopieeffekte • Können sehr hilfreich sein, wenn die Frage auftritt, ob während des Aktivierungsprozesses eine Bindung zu Wasserstoff oder einem anderen leichten Element gebrochen wird oder nicht. • Betrachten wir eine Bindung zwischen einer Gruppe R und einem Atom A. Während der Reaktion erfolge der Bruch dieser Bindung. • Wie unterscheidet sich die Geschwindigkeitskonstante dieser Reaktion von der einer analogen Reaktion, bei der A durch A* (= schwereres Isotop desselben Elements) ersetzt ist? Die Chemische Bindung, betrachtet als quantenmechanischer harmonischer Oszillator • Harmonischer Oszillator bedeutet: Rückstellkraft proportional zur Auslenkung • Beschleunigung proportional zur Auslenkung und dieser entgegengesetzt • Die Energieniveaus des Oszillators sind: 1 En n h 2 Schwingungsquantenzahl • Anders als in der klassischen Mechanik kann der Oszillator seine Energie nie ganz abgeben • Das niedrigste Schwingungsniveau liegt bei n=0 Nullpunktsenergie Harmonischer Oszillator: h E0 2 x x0 cos t Auslenkung Amplitude Kreisfrequenz 2 1 k' 2 Kraftkonstante (Federkonstante) reduzierte Masse Das Spektrum des harmonischen Oszillators besteht nur aus einer einzigen Frequenz, Diese ist (wie in der klassischen Mechanik) unabhängig von der Amplitude (Energie) der Schwingung mR m A mR m A Der Auslenkung aus der Ruhelage r – r0 wirkt die harmonische Kraft F entgegen: F = - k‘ (r – r0) • A sei H (Wasserstoff) • A* sei D (Deuterium) mR>>mH mR>>mD R H mH R D mD • Die Kraftkonstante k‘ ist unabhängig vom Isotop, daher gilt: 1 k' 2 mH RH mD 2 RD mH 1 k' 2 mD • Der Unterschied in den Aktivierungsenergien kann gleichgesetzt werden dem Unterschied zwischen den Grundzuständen, • wenn im ÜZ die R-H bzw. R-D Bindung nicht mehr existiert und daher die Übergangszustände die gleiche Energie haben E E N L (E E ) H a D a D 0 E0H E0D H 0 E aD EaH Ea k A exp RT EaD EaH kH exp kD RT N L ( E0H E0D ) exp RT kH N L h R H R D exp kD 2 RT RH 2 RD RH RD 2 h R H h R D 2 1 N L kH exp exp kD 2 RT Für eine C-H Bindung (aliphatisch) ist die StreckSchwingungsfrequenz 8.7x1013 s-1 Bei 298 K ergibt sich daher kH 7.8 kD Primärer kinetischer Isotopieeffekt: Wenn die Bindung zum Isotop gespalten wird Für H/D ist der Effekt am größten, für C-12/C-13 beträgt er nur ca. 4% 1 1 NL 2 2 RT Hinweise auf die Struktur des Übergangszustandes • Wird die R-H bzw. R-D Bindung im ÜZ nicht ganz sondern nur teilweise gebrochen, so ist der kinetische Isotopieeffekt kleiner als berechnet. • Der Effekt ist auch dann kleiner, wenn sich im ÜZ eine neue Bindung von H (bzw. D) zu einer zweiten an der Reaktion teilnehmenden Spezies abzuzeichnen beginnt. • Ist die neue Bindung viel stärker als die alte, so kann man sogar einen inversen kinetischen Isotopieeffekt beobachten! • Regel: Substitution durch ein schwereres Isotop favorisiert die Spezies mit der stärkeren Bindung in jedem Gleichgewicht, einschließlich des Quasi-Gleichgewichts des ÜZ mit den Edukten. Bindung R-H bzw. R-D stärker im Edukt als im ÜZ: Reaktion durch Ersatz von H durch D verlangsamt Bindung R-H bzw. R-D stärker im ÜZ als im Edukt: Reaktion durch Ersatz von H durch D beschleunigt (weil höhere Konzentration an aktiviertem Komplex)