7.8 Spezifische Wärmekapazität von Gasen Für Gase gibt es zwei
Werbung

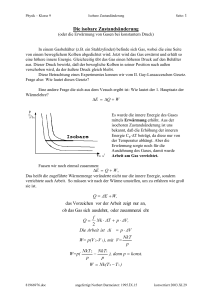
Fach: Physik/ L. Wenzl | Datum: 7.8 Spezifische Wärmekapazität von Gasen Für Gase gibt es zwei spezifische Wärmekapzitäten: cv und cp. cv ist die spezif. Wärmekapazität bei konstantem Volumen cpist die spezif. Wärmekapazität bei konstantem Druck Es gilt stets: In Abb. 1 a wird das Volumen konstant gehalten, bei Erwärmung steigen Temperatur T und Druck p. Die geswamte zugeführte Wärme erhöht die innere Energie U des Gases. In Abb. 1 b wird der Kolben freigegeben, so dass sich das Gas ausdehnen kann, der Druck p bleibt konstant. Das Gas dehnt sich aus und verrichtet gegen die Gewichtskraft die Arbeit W. Deshalb erhöht nur ein Teil der zugeführten Wärme die innere Energie U des Gases. Um in beiden Fällen gleiche Temperaturerhöhung zu erfahren, ist deshalb bei konstantem Druck (Fall b) mehr Wärme erforderlich als bei konstantem Volumen (Fall a). Da sich Festkörper und Flüssigkeiten bei Erwärmung nur rel. wenig ausdehnen, wird bei ihnen in der Praxis zischen cp und cv nicht unterschieden. Beispiel: Wie viel Wärme ist notwendig, um ein Klassenzimmer mit 10 m Länge, 10 m Breit und 3,0 m Höhe von 14,0° C auf 21,0° C zu erwärmen? ( Da die Fenster, Türen usw. nicht luftdicht sind, ist von einem konstanten Druck auszugehen. Luft hat eine Dichte von ρ = 1,29 kg/m3. Geg.: Ges.: