Inhalt - Zeitschrift für Chemotherapie
Werbung

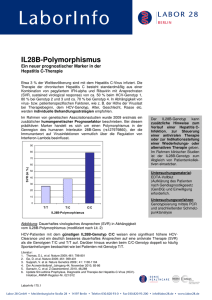
be w w e e .d in n i nl rl 4 tzc 01 . w r2 st gi o ZEITSCHRIFT FÜR ISSN 0722/5067 e Re Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie Übersicht Glykopeptide – neue Präparate bieten erweiterte therapeutische Möglichkeiten Vancomycin (diverse Generika), das erste Glykopeptid-Antibiotikum, wurde bereits Mitte des vergangenen Jahrhunderts als Stoffwechselprodukt eines Actinomyceten (Streptomyces bzw. Amycolatopsis orientalis) entdeckt und als Therapeutikum von Eli Lilly in den USA entwickelt. Mit der zunehmenden Entwicklung der Penicillin-Resistenz wurde es in den letzten Jahrzehnten ein immer häufiger angewandtes Arzneimittel zur Behandlung von Infektionen durch Methicillin-resistente Staphylococcus aureus und andere grampositive Erreger. Als zweite wichtige Indikation ist die oral zu behandelnde, durch Clostridium difficile verursachte Diarrhö zu nennen, die ebenfalls seit Jahrzehnten etabliert ist. Nach wie vor ist Vancomycin ein Mittel der Wahl bei diesen Infektionen, obwohl eine abnehmende Empfindlichkeit der Erreger seit langem beschrieben wurde. Die Bemühungen, dieser Entwicklung durch höhere Dosierungen zu begegnen, werden durch das nephro- und ototoxische Potenzial des Antibiotikums limitiert. Ein Bedarf an Alternativen ist offensichtlich. Die erste verfügbare Alternative zu Vancomycin war Teicoplanin (TARGOCID), das ebenfalls von einem Mikroorganismus gebildet wird. Es handelt sich um ein Gemisch von fünf verschiedenen Komponenten, die im Gegensatz zu Vancomycin lipophile Seitenketten (C10 -Acylrest) aufweisen. Es kann sich über diesen Strukturanteil in der bakteriellen Zellmembran verankern, wodurch einige Unterschiede im Resistenzmuster erklärt werden können. 1988 in Europa eingeführt ist es heute in zahlreichen Ländern - aber nicht in den USA - zugelassen. Anders als Vancomycin fördert es nicht die Histaminfreisetzung („red man Syndrom“) und zeigt damit eine bessere Verträglichkeit. Inhalt Januar/Februar 2015 - 36. Jahrg. 1/2015 Übersicht — Glykopeptide – neue Präparate Seite 1-3 Infektiologische Merksätze — Empfehlungen zum Jahresauftakt Seite 3 Neueinführungen — Daclatasvir — Ledipasvir plus Sofosbuvir Seite 3-4 Seite 4-6 Hepatitis C – Strukturproteine und alle neuen Virustatika Seite 6-7 Pneumonien — Ambulant erworbene Pneumonie: Mono- oder Kombinationstherapie? Seite 7-8 — Invasive Pneumokokken-Infektionen: Vortherapie beachten Seite 8 Endokarditis – Ohne Prophylaxe mehr Infektionen? – MRSA-Infektionen: Reserve-Therapie Seite 8-9 Seite 9 Nebenwirkungen – Makrolide bei Neugeborenen – mehr Pylorusstenosen – Daptomycin: Mehr Myopathien durch Statine? – Neue Daten zur Verträglichkeit von Amoxicillin Halbsynthetische Lipoglykopeptide Mit den halbsynthetischen Glykopeptiden Telavancin (VIBATIV), [siehe ZCT 2014;35(3):26-28], Dalbavancin (XYDALBA) und Oritavancin (ORBACTIV), wird die Gruppe der Glykopeptid-antibiotika zur Zeit erheblich ausgeweitet. Da sie alle einen lipophilen Substituenten besitzen, werden sie auch als Lipoglykopeptide bezeichnet (siehe Tabelle S. 2).1 Telavancin und Oritavancin sind Vancomycin-Derivate, während Dalbavancin durch chemische Modifikation von Teicoplanin gewonnen wurde. Das zuständige Komitee (CHMP) bei der Europäischen Behörde EMA hat vor wenigen Wochen die Zulassung von XYDALBA und ORBACTIV empfohlen. Seite 9 Seite 9-10 Seite 10 Obwohl diese Antibiotika erst kürzlich zugelassen wurden oder ihre Einführung in Europa kurz bevorsteht, sind bereits etliche Jahre seit ihrer Erstbeschreibung vergangen. So wurde Telavancin (TD-6424) schon 2003 erwähnt und mit der Entwicklung von Dalbavancin (BI-397) und Oritavancin (LY333328) wurde bereits in den 1990er Jahren begonnen. Im Jahr 2009 wurde die Zulassung für ein Oritavancin-basiertes Präparat bei der EMA gestoppt, da nicht genug Daten zur therapeutischen Wirksamkeit und Reinheit des Produktes vorlagen. Diese drei neu zugelassenen Arzneimittel sind damit ein weiterer Hinweis auf die „Antibiotikalücke“, die durch die nachlassenden Aktivitäten der pharmazeutischen Industrie auf diesem Gebiet entstanden ist. Aufgrund 1 Januar /Februar 2015 - 36. Jahrg. Zeitschrift für Chemotherapie Tabelle: Glykopeptid-Antibiotika Antibiotikum Handelsname (Europa) Handelsname (USA) Eliminationshalbwertzeit (h) Proteinbindung (%) Dosierung Verträglichkeit, Toxizität Vancomycin diverse Generika diverse Generika 4 – 6 (-11) 55 Infusion (mindestens über 60 min): 2 x tgl. 1,0 g „Red man Syndrom“ durch Histaminfreisetzung; nephro- und ototoxisch Teicoplanin TARGOCID (in den USA nicht im Handel) 100 – 170 88 – 91 Infusion (30 min): initial: 2 x tgl. 6 - 12 mg/kg, dann 1 x tgl. (auch i.m. möglich) nephro- und ototoxisch; embryotoxisch im Tierexperiment Telavancin VIBATIV VIBATIV 8 90 Infusion (60 min) 1 x tgl. 10 mg/kg nephrotoxisch; teratogen im Tierexperiment Dalbavancin XYDALBA (EMA:12/2014) DALVANCE (FDA: 5/2014) 346 93 Infusion (30 min): 1 x 1,0 g i.v., nach einer Woche 1 x 0,5 g i.v. offenbar gut verträglich, nicht abschliessend beurteilbar Oritavancin ORBACTIV (EMA: 1/2015) ORBACTIV (FDA: 8/2014) 245 85 Infusion (180 min): 1 x 1,2 g offenbar gut verträglich, nicht abschliessend beurteilbar des erheblichen Bedarfs und angesichts der fortschreitenden Resistenzentwicklung sowie einem Mangel an echten Innovationen werden ältere Substanzen reaktiviert. Antibakterielle Wirkung, Resistenz Man kann die Glykopeptide nach ihrer Struktur in vier oder fünf Klassen einordnen, demnach gehört Vancomycin zur Klasse I und Teicoplanin zur Klasse IV. Beides sind Naturstoffe; gemeinsam ist die Heptapeptid-Grundstruktur.1 Dieser Teil des Moleküls bindet an die C-terminale Peptidstruktur D-Ala-D-Ala der Peptidoglykan-Vorstufen (Lipid II), aus denen die Bakterienzelle die Zellwand synthetisiert. Die Funktion der entscheidenden Enzyme der Peptidoglykan-Synthese, der Transglycosylase und der Transpeptidase, wird behindert, weil ihr Substrat blockiert ist. Obwohl Glykopeptide damit - ähnlich wie die ß-Laktamantibiotika - in die Zellwandsynthese eingreifen, findet keine direkte Hemmung der Enzyme statt, sondern eine Bindung an das Substrat; damit besteht ein wesentlicher Unterschied zwischen den beiden Antibiotikagruppen. Dies hat Konsequenzen für die Resistenzentwicklung und die Frage einer möglichen Kreuzresistenz. Bei genauer Betrachtung gibt es relevante Unterschiede zwischen den einzelnen Glykopeptiden. Mehrere Mechanismen sind bekannt, durch die ein Erreger Vancomycin-resistent werden kann. Bei den VISA (Vancomycin-intermediär resistente S. aureus)-Stämmen ist die Zellwand deutlich verdickt, die Antibio- 2 tika erreichen dann ihren Wirkort nicht. Bei diesen Bakterienstämmen kann Dalbavancin noch wirksam sein, weil es ähnlich wie Vancomycin dimerisiert und es zusätzlich über die C12-Seitenkette so in der Zellmembran verankert ist, dass es die Aktivität der Zellwand synthetisierenden Enzyme hemmen kann.1,2 Bei einer anderen Art von Resistenz ist das Lipid II so verändert, dass die meisten Glykopeptide nicht mehr binden können. Der Peptidoglykanbaustein Lipid II wird im Zytoplasma synthetisiert, in der Zytoplasmamembran verankert und dann zum weiteren Aufbau der Zellwandschichten benutzt. Resistenz gegen Glykopeptide wird durch geringe Modifikationen erreicht: durch Umwandlung des endständigen DAlanins in D-Laktat (VanA, VanB, VanD Stämme) oder D-Serin (VanC, VanE, VanL). Diese Stämme sind hochresistent (VRE, Vancomycin-resistente Enterokokken; VRSA, Vancomycin-resistente S. aureus), weil die Antibiotika nicht mehr ausreichend an das veränderte Substrat binden können. Die Gene, die diese Resistenz vermitteln (vanA) wurden primär in Enterokokken nachgewiesen und sind bei S. aureus zur Zeit noch selten. Bei diesen Stämmen besitzt Oritavancin als einziges der Glykopeptide noch Aktivität. Es lagert sich über einen lipophilen 4-Chlorbiphenylrest in die Membran ein, es bildet Dimere und bindet fest genug auch an die modifizierten Lipid-II-Bauteile, um die Synthese der Zellwand zu blockieren; daneben kommt es zu einer Störung der Membranfunktion. 3,4 Pharmakokinetische Eigenschaften Die Glykopeptid-Antibiotika werden nach oraler Gabe nicht resorbiert und müssen zur systemischen Therapie parenteral verabreicht werden. Eine orale Gabe von Vancomycin oder Teicoplanin bei der intestinalen C. difficile-Infektion ist möglich. Die Proteinbindung ist bei allen Derivaten höher als bei Vancomycin (55%) und liegt in einem Bereich zwischen 85% (Oritavancin) und 93% (Dalbavancin). Der wesentliche Unterschied besteht in der Geschwindigkeit der Elimination (s. Tabelle). Während Vancomycin mit einer Halbwertzeit von ca. 6 Stunden rasch eliminiert wird und mindestens zweimal täglich verabreicht werden muss, werden die anderen Glykopeptide langsamer ausgeschieden. Teicoplanin und Telavancin müssen einmal täglich infundiert werden, für Dalbavancin ist eine Infusion pro Woche und für Oritavancin eine einmalige Infusion ausreichend. Dies gilt derzeit für die Therapie von Hautund Weichgewebsinfektionen, nicht jedoch für andere Arten von Infektionen, wie Pneumonie oder Sepsis [vgl. ZCT 2014: 35 (6): 59]. Die theoretischen Voraussetzungen sind jedoch erfüllt, um auch Knocheninfektionen zum Beispiel mit Dalbavancin zu behandeln. Bei niedrigen Hemmkonzentrationen von 0,06 µg/ml für S. aureus wurden nach Infusion einer Dosis von 1,0g Konzentrationen im Knochen von etwa 6 µg/g gemessen. 5 Januar /Februar 2015 - 36. Jahrg. Zeitschrift für Chemotherapie Verträglichkeit Zu den therapeutischen Problemen von Vancomycin und Teicoplanin gehören das nephro- und ototoxische Potenzial dieser Antibiotika. Auch das neuere Telavancin ist nephrotoxisch, während dies bei den beiden anderen halbsynthetischen Substanzen nicht relevant zu sein scheint. In einer Vergleichsstudie zwischen Vancomycin und Oritavancin waren leichte gastrointestinale Reaktionen (Erbrechen, Diarrhö) und ZNSSymptome (Kopfschmerzen, Schwindel) die häufigsten Nebenwirkungen. Zwischen den beiden Arzneimitteln war kein Unterschied in der Häufigkeit erkennbar. Ein sehr ähnliches Resultat wurde in den klinischen Studien mit Dalbavancin registriert. Eine abschließende Beurteilung der unerwünschten Wirkungen und insbesondere möglicher seltener Risiken dieser Antibiotika kann zurzeit noch nicht erfolgen. Erst der weitere klinische Einsatz wird zeigen, ob zum Beispiel Hypersensitivitätsreaktionen insbesondere bei den Präparaten mit langer Verweildauer im Organismus zum Problem werden könnten. ZUSAMMENFASSUNG: Die vergrößerte Palette von Glykopeptid-Antibiotika erweitert die therapeutischen Optionen bei Infektionen durch grampositive Bakterien. Vorteilhaft ist die erhöhte antibakterielle Aktivität, die sich zum Teil auch auf Erreger erstreckt, die gegen Vancomycin (diverse Generika) resistent sind. Ein weiterer Vorteil der beiden neueren Präparate Dalbavancin (XYDALBA) und Oritavancin (ORBACTIV) ist die langsame Elimination, die es ermöglicht zumindest Haut- und Weichgewebsinfektionen mit nur einer Infusion pro Woche bzw. mit einer Einmaltherapie zu behandeln. Vancomycin, Teicoplanin (TARGOCID) und Telavancin (VIBATIV) besitzen ein nephro- und ototoxisches Potenzial. Eine abschließende Beurteilung der Verträglichkeit von Dalbavancin und Oritavancin ist derzeit aufgrund mangelnder klinischer Daten noch nicht möglich. Nephro- und ototoxische Effekte scheinen mit diesen Substanzen nicht relevant zu sein. 1. BUTLER, M.S. et al. J Antibiotics 2014; 67:631-644 2. ROECKER, A. M. & POPE, S.D. Expert Opin Pharmacother 2008; 9:1745-1754 3. ZHANEL, G.G. et al. Clin Inf Dis 2012; 54 (Suppl 3): S214-S219 4. MÜNCH, D. et al. Antimicrob Agents Chemother 2015 (ahead of print) k „Merksätze“ der Infektiologie o 1. 2. 3. 4. 5. 6. 7. 8. r r e l i e r Ohne Händewaschen sind auch Kittel und Häubchen entbehrlich. Wenn man die Temperatur nicht misst, findet man auch kein Fieber. Fieber ist keine Meronem-Mangelkrankheit. Das Fehlen einer Diagnose lässt sich nicht durch eine Dreifach-Kombination ersetzen. Je breiter das Spektrum, desto größer die Lücken. Bei Verdacht auf Sepsis ist ein Rektalabstrich sinnlos. Je länger der Probentransport, desto schwerer die Harnwegsinfektion. Campylobacter wächst nicht auf Salmonellen-Spezialagar. nach Schmitt, H. J., Consilium infectiorum 2007; 17: 1 Ab Ausgabe 2 der ZCT 2015 erscheint an dieser Stelle die Rubrik „Mikrobiologie in Klinik und Praxis – Epidemiologie und Fortschritte der Diagnostik“. Neueinführungen dene neue Wirkstoffe zur Behandlung der chronischen Hepatitis C in der klinischen Prüfung.1,2 Daclatasvir – die erste Substanz einer neuen Wirkstoffgruppe gegen Hepatitis C-Viren Antivirale Aktivität Als Ergebnis eines screenings von mehr als 1 Million Substanzen wurde eine neue Klasse von Wirkstoffen entdeckt, die eine bemerkenswert hohe Aktivität gegen das Hepatitis C-Virus (HCV) aufweisen. In Zellkulturversuchen wurde beobachtet, dass die Ausgangssubstanz BMS-824 spontan dimerisierte, was zu der gezielten Synthese symmetrischer Moleküle Anlass gab. Während die ersten Stoffe in diesem Entwicklungsprogramm eine antivirale Aktivität im mikro- und nanomolaren Bereich zeigten, konnten bei den Weiterentwicklungen Aktivitäten sogar im pikomolaren Bereich festgestellt werden.1 Das seit einigen Monaten verfügbare Daclatasvir (DAKLINZA) stellt einen vorläufigen Abschluss dieser Entwicklung beim Hersteller Bristol-Myers Squibb dar. Es ist wohl einer der potentesten antiviralen Wirkstoffe, die bisher beschrieben wurden. Analoge Präparate befinden sich bei anderen Firmen in der klinischen Entwicklung. Insgesamt sind derzeit mehr als 50 verschieStrukturformel Daclatasvir Daclatasvir ist ein Inhibitor des multifunktionalen viralen Proteins NS5A, das ein wesentlicher Bestandteil des HCV-Replikationskomplexes ist. Es handelt sich um ein Phosphoprotein ohne enzymatische Aktivität. Daclatasvir hemmt durch Beeinflussung dieses Proteins sowohl die virale RNA-Replikation als auch den Zusammenbau neuer Viruspartikel (assembly). Die Hemmung erfolgt hochselektiv bereits in sehr niedrigen Konzentrationen. Trotz der hohen antiviralen Potenz ist die Resistenzbarriere niedrig, dies gilt insbesondere für den Genotyp 1a, dem weltweit häufigsten Genotyp. In vitro ist die Aktivität gegen Viren vom Genotyp 1b etwa fünffach höher, als gegen die des 1a Genotyps. Auch bei der klinischen Prüfung des Virustatikums in Kombination mit Peginterferon (PEGASYS) und Ribavirin (COPEGUS) wurde beim Genotyp 1a häufiger Resistenzentwicklung beobachtet als beim Typ 1b. Eine Monotherapie mit Daclatasvir ist nicht sinnvoll. Es eignet sich besonders als Kombinationspartner mit anderen Wirkstoffen mit direkter Aktivität gegen HCV, wie zum Beispiel dem Polymerase-Inhibitor Sofosbuvir (SOVALDI). 3 (= BMS-790052) Das symmetrische Molekül weist im Zentrum eine Biphenylstruktur auf (MM 738,9 Da). 5. DUNNE, M.W. et al. Antimicrob Agents Chemother 2015 (ahead of print) 3 Zeitschrift für Chemotherapie Januar /Februar 2015 - 36. Jahrg. Pharmakokinetische Eigenschaften Daclatasvir wird nach oraler Einnahme rasch resorbiert, eine leichte Mahlzeit hat keinen wesentlichen Einfluss auf die Bioverfügbarkeit. Bei einmal täglicher Einnahme von 60 mg wurde ein steady-state nach vier Tagen erreicht. In der Tabelle wurden einige pharmakokinetische Daten zusammengefasst. Daclatasvir ist ein Substrat von Cytochrom 3A4 (CYP3A4) und besitzt eine schwache, induktive Wirkung auf dieses Enzym. Es hemmt die Transportproteine PGlykoprotein (P-gp), OATP1B1 und BCRP. Pharmakokinetische Daten von Daclatasvir Tabelle: Parameter Mittelwert Cmax (mg/l) 1,5 Cmin (mg/l) 0,2 Tmax (h) 1 bis 2 AUC0-24 (mg/l x h) 14,1 Verteilungsvolumen (l) 47 Plasmaproteinbindung (%) 99 Metabolismus CYP3A4 Renale Elimination (unverändert) ca. 6% t1/2 (h) 12 - 15 Clearance (l/h) 4,2 mod. nach DAKLINZA, Summary of Product Characteristics2 Therapeutische Wirksamkeit Daclatasvir ist zur Behandlung der chronischen Infektion mit dem Hepatitis C-Virus (HCV) bei Erwachsenen in einer Dosierung von 60 mg einmal täglich zugelassen. Daclatasvir muss in Kombination mit anderen Wirkstoffen mit direkter Aktivität gegen HCV angewandt werden. Die Dauer der Behandlung und auch die Kombinationspartner richten sich nach dem Genotyp des HCV und einer eventuell erfolgten Vorbehandlung. Darüber hinaus wird zum Beispiel bei einer Leberzirrhose länger behandelt; andererseits kann die Dauer reduziert werden, wenn positive Prognosefaktoren, wie ein IL28B-CC-Genotyp, vorliegen. Detaillierte Empfehlungen werden von der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS) publiziert und fortlaufend aktualisiert.4 Zunächst konnte gezeigt werden, dass durch Daclatasvir ein zusätzlicher therapeutischer Nutzen erzielt werden kann, wenn es als Ergänzung zu der früher üblichen Standardkombination von Peginterferon alpha-2a und Ribavirin gegeben wird. Diese beiden Therapeutika haben bekanntlich eine indi- 4 rekte, im Detail nicht geklärte Wirkung auf die virale Vermehrung. Die Möglichkeiten von Daclatasvir werden jedoch erst deutlich, wenn es mit anderen direkt wirksamen Virustatika kombiniert wird. Die Wirksamkeit und Sicherheit von Daclatasvir in Kombination mit Sofosbuvir (400 mg einmal täglich) mit oder ohne Ribavirin bei der Behandlung einer chronischen Infektion mit HCV wurden in mehreren Studien untersucht. Ein dauerhaftes virologisches Ansprechen nach 12 Behandlungswochen (SVR12) wurde von 99% der Patienten mit HCV-Genotyp 1, von 96% der Patienten mit Genotyp 2 und von 89% der Patienten mit Genotyp 3 erreicht. Die Dreifach-Kombination aus Daclatasvir, Sofosbuvir und Ribavirin wird bei Patienten mit Infektionen durch den Genotyp 3 empfohlen, die zusätzlich eine kompensierte Zirrhose aufweisen oder vorbehandelt sind. Bei Patienten mit dem Genotyp 4 kann Daclatasvir auch mit dem früher üblichen Standardregime aus Ribavirin und Peginterferon kombiniert werden. Für Patienten, die mit den Genotypen 5 oder 6 infiziert sind, liegen keine Empfehlungen vor. 2,5,6 Unerwünschte Wirkungen, Interaktionen, Toxizität Weil Daclatasvir immer in Kombination mit anderen Arzneimitteln eingesetzt wird, lässt sich die Verträglichkeit aus den klinischen Studien nur mit Einschränkungen ableiten. Als häufigste Ereignisse, die während der Therapie beobachtet wurden, sind zum Beispiel Müdigkeit, Kopfschmerzen und Pruritus zu nennen. Diese Symptome können jedoch auch krankheitsbedingt sein oder durch die anderen gleichzeitig verabreichten Substanzen verursacht werden. Eine Verschlechterung der Verträglichkeit des Peginterferon/Ribavirin-Regimes durch Daclatasvir ist aus Placebo-kontrollierten Studien nicht abzuleiten. Dies ist ein wesentlicher Unterschied zu den Proteaseinhibitoren Boceprevir (VICTRELIS) und Telaprevir (INCIVO). Dalclatasvir ist kontraindiziert bei gleichzeitiger Gabe von potenten CYP3A4- oder P-gp-Induktoren, wie zum Beispiel Rifampicin (EREMFAT), Carbamazepin (diverse Generika) oder Johanniskraut-Präparaten, da diese zu einer Reduktion der Plasmaspiegel und gegebenenfalls zu einer Einschränkung des Therapieerfolgs führen können. Daclatasvir zeigte in der toxikologischen Prüfung ein teratogenes Potenzial. Bei Ratten betrafen die Fehlbildungen hauptsächlich Gehirn, Schädel, Augen, Ohren, Nase, Lippen, Gaumen oder Extremitäten. Das Arzneimittel darf daher nicht von Frauen im gebärfähigen Alter eingenommen wer- den, wenn keine empfängnisverhütenden Maßnahmen durchgeführt werden. Therapiekosten Der Apothekenverkaufspreis für eine Packung DAKLINZA mit 28 Tabletten beträgt 13.325,25 Euro. Wenn das Arzneimittel mit dem noch teureren SOVALDI (19.999,46 Euro) kombiniert wird, resultieren Tagestherapiekosten von fast 1.200 Euro oder 100.000 Euro für die Gesamtbehandlung über zwölf Wochen. ZUSAMMENFASSUNG: Daclatasvir (DAKLINZA) ist das erste Arzneimittel aus der Gruppe der NS5A-Inhibitoren, das zur Behandlung der chronischen Hepatitis C in Kombination mit anderen Arzneimitteln zugelassen ist. Als NS5A wird ein nichtstrukturelles Protein bezeichnet, das ein wesentlicher Bestandteil des HCV-Replikationskomplexes ist. Trotz hoher antiviraler Aktivität von Daclatasvir ist die genetische Resistenzbarriere gering, es wird daher vorzugsweise mit dem Polymerase-(NS5B)Inhibitor Sofosbuvir (SOVALDI) kombiniert. Diese einmal täglich, oral einzunehmende Kombination führt vergleichsweise rasch zu einem dauerhaften virologischen Ansprechen. Die Verträglichkeit der Kombination ist gut. Angesichts der begrenzten Anzahl von Patienten, die bisher behandelt wurden, ist eine Aussage zu sehr selten auftretenden unerwünschten Wirkungen allerdings noch nicht möglich. Da die Substanz im Tierexperiment teratogen ist, muss eine Schwangerschaft während der Therapie sicher verhütet werden. 1. BELDA, O., TARGETT-ADAMS, P. Virus Res 2012; 170:1-14 2. DAKLINZA, SPC (Zusammenfassung der Merkmale des Arzneimittels); www.ema.europa.eu 3. AGHEMO, A., DE FRANCESCO, R. Gut 2014 (ahead of print) 4. DGVS, Aktuelle Empfehlung zur Therapie der chronischen Hepatitis C www.dgvs. de/leitlinien/aktuelle-empfehlungen/ 5. SULKOWSKI, M.S. et al. N Engl J Med 2014; 370:211-221 6. FEENEY, E.R. und CHUNG, R.T Brit Med. J 2014; 349:g3308 Ledipasvir plus Sofosbuvir – ein Kombinationspräparat zur oralen Therapie der chronischen Hepatitis C Die Kombination aus Daclatasvir (DAKLINZA) und Sofosbuvir (SOVALDI) er- Januar /Februar 2015 - 36. Jahrg. Zeitschrift für Chemotherapie wies sich als ein wirksames und verträgliches Regime zur einmal täglichen, oralen Behandlung der chronischen Hepatitis C (vgl. ZCT 2015; 36:3-4).1 Die Studie zeigte, dass offensichtlich die Kombination aus einem NS5A-Inhibitor (Daclatasvir) und einem Polymerase-(NS5B)-Inhibitor (Sofosbuvir) auch bei erfolglos mit Protease-Inhibitoren vorbehandelten Patienten gut wirksam ist. Die beiden Arzneimittel wurden von verschiedenen Herstellern entwickelt (Sofosbuvir: Gilead; Daclatasvir: Bristol-Myers Squibb). Es ist daher nicht überraschend, dass von beiden Firmen Kombinationspräparate mit „eigenen“ Wirkstoffen produziert werden. Bristol-Myers Squibb entwickelt unter anderem den Proteaseinhibitor Asunaprevir (in Europa noch nicht im Handel), der mit Daclatasvir kombiniert werden kann. Von Gilead wurde vor einigen Monaten ein fixes Kombinationspräparat unter dem Namen HARVONI in den Handel gebracht, das den NS5A-Inibitor Ledipasvir (= GS-5885) und Sofosbuvir vereint. Da Sofosbuvir bereits in einer früheren Ausgabe dieser Zeitschrift beschrieben wurde (vgl. www.zct-berlin.de, Antiinfektiva/Neueinführungen), soll in diesem Beitrag auf die Eigenschaften des Ledipasvir fokussiert werden, einer Substanz, die als Monotherapeutikum nicht verfügbar ist. Empfindlichkeit gegenüber Ledipasvir war beim Genotyp 1a und 1b mit der primären NS5A-Substitution Y93H verbunden. Darüber hinaus entwickelte sich in den Replikons des Genotyps 1a eine Q30E-Substitution. Ledipasvir war uneingeschränkt aktiv gegen die mit Sofosbuvir-Resistenz assoziierte Substitution S282T in NS5B, während alle mit Ledipasvir-Resistenz assoziierten Substitutionen in NS5A uneingeschränkt empfindlich gegenüber Sofosbuvir waren. 2 Pharmakokinetische Eigenschaften Die Angaben zur Pharmakokinetik von Ledipasvir in der Tabelle beziehen sich auf die Anwendung in Kombination mit Sofosbuvir. Demnach wird Ledipasvir nach oraler Einnahme rasch und unabhängig von der Nahrungsaufnahme resorbiert und größtenteils, zu etwa 70%, unverändert biliär eliminiert. Im Vergleich zu Daclatasvir sind die Plasmakonzentrationen von Ledipasvir niedriger und die Eliminationshalbwertzeit länger. In vitro wurde keine nachweisbare Metabolisierung von Ledipasvir über humane Cytochrom-abhängige Monooxygenasen beobachtet. Es liegen Hinweise auf eine langsame oxidative Metabolisierung durch einen unbekannten Mechanismus vor. 2 C-Virus (HCV) bei Erwachsenen in einer Dosierung von 90 mg / 400 mg einmal täglich zugelassen. In drei klinischen Studien, die im April 2014 im New England Journal of Medicine erschienen, wurden insgesamt fast 2.000 Patienten mit chronischer Hepatitis C (Genotyp 1a oder 1b) behandelt, von denen 93% bis 99% ein anhaltendes virologisches Ansprechen zeigten. 3 In den ION1- und ION-2-Studien war die Wirksamkeit nach 12 Wochen sehr ähnlich wie nach 24 Wochen. Es machte ebenfalls keinen Unterschied, ob zusätzlich Ribavirin (COPEGUS u.a.) verabreicht wurde oder nicht. Bei nicht vorbehandelten Patienten ohne Leberzirrhose war eine 8-wöchige Therapie der 12-wöchigen Behandlung gleichwertig. Allerdings waren die Rückfallraten höher bei kürzerer Therapiedauer (8 Wochen: 5%; 12 Wochen: 2%; 24 Wochen: 0,2%). Das gute Behandlungsergebnis war unabhängig vom Genotyp (1a vs. 1b). Ein mehr als 94%iges Ansprechen wurde auch erzielt bei Patienten, bei denen zuvor eine Interferon-basierte Therapie nicht gewirkt hatte. Lediglich bei Patienten mit Leberzirrhose wurde mit 88% eine relativ geringere Ansprechrate ermittelt. Weitere Daten zeigen, dass ähnlich hohe Behandlungserfolge auch bei Infektionen mit den HCV-Genotypen 2 und 3 möglich sind. 3,4 Chemische Struktur, antivirale Aktivität Tabelle: Pharmakokinetische Daten von Ledipasvir Unerwünschte Wirkungen, Interaktionen, Toxizität Ledipasvir besitzt eine ähnliche Struktur wie Daclatasvir, der einzige andere bisher zugelassene Stoff aus dieser Arzneimittelklasse (s. Abbildung). Parameter Mittelwert Cmax (mg/l) 0,3 Tmax (h) 4 AUC0-24 (mg/l x h) 7,3 Ledipasvir hemmt das Hepatitis C-Virus ähnlich wie Daclatasvir - bereits in niedrigen pikomolaren Konzentrationen durch Beeinflussung des viralen Proteins NS5A, das ein wesentlicher Bestandteil des HCV-Replikationskomplexes ist. In vitro wurde eine Hemmung bereits bei 31 (Genotyp 1a) bzw. 4 pM (Genotyp 1b) beobachtet (EC50 -Werte). Im Vergleich dazu sind für den PolymeraseInhibitor Sofosbuvir mehr als 1000-fach höhere Konzentrationen notwendig (40 und 110 nM). In Zellkulturen wurden HCV-Replikons mit reduzierter Empfindlichkeit gegenüber Ledipasvir selektiert. Die reduzierte Plasmaproteinbindung (%) > 99,8 Metabolismus unbekannt Renale Elimination (unverändert) ca. 1% t1/2 (h) 47 Nach den bisherigen Erfahrungen zeichnet sich HARVONI durch eine gute Verträglichkeit aus. Zu den häufigsten unerwünschten Ereignissen, die während der klinischen Prüfung registriert wurden, gehörten Müdigkeit, Kopfschmerzen und Erbrechen. Von 539 Patienten, die dieses Kombinationspräparat in den klinischen Studien 12 Wochen lang ohne weitere Medikation erhielten, brachen nur zwei Teilnehmer die Studie wegen unerwünschter Wirkungen ab. 3 Strukturformel Ledipasvir mod. nach SPC HARVONI 2 Therapeutische Wirksamkeit Das Kombinationspräparat aus Sofosbuvir und Ledipasvir ist zur Behandlung der chronischen Infektion mit dem Hepatitis (= GS-5885; MM 889,0 Da) Das Molekül besitzt im Vergleich zu Daclatasvir einen ähnlichen, jedoch nicht streng symmetrischen Aufbau mit einer zentralen DifluorfluorenStruktur. Ledipasvir und Sofosbuvir sind Substrate der Transporterproteine P-gp und BCRP. Potente P-gp-Induktoren [z.B. Rifampicin (EREMFAT), Carbamazepin (diverse Generika) oder Johanniskraut-Präparate], können zu einer Abnahme der Plasmakonzentrationen von Ledipasvir führen und sollten daher nicht zusammen mit HARVONI verabreicht werden. Klinisch bedeutsame Wechselwirkungen mit Ledipasvir/Sofosbuvir, die über CYP450- oder UGT1A1Enzyme vermittelt werden, sind nicht zu erwarten. 2 Im Gegensatz zu Daclatasvir zeigten weder Ledipasvir noch Sofosbuvir in den routinemäßig durchgeführten reproduktionstoxikologischen Studien an Ratten und Kaninchen ein teratogenes Potenzial. 5 Januar /Februar 2015 - 36. Jahrg. Zeitschrift für Chemotherapie Therapiekosten Der Apothekenverkaufspreis für eine Packung HARVONI mit 28 Filmtabletten beträgt 22.260,88 Euro. ZUSAMMENFASSUNG: Das Kombinationspräparat HARVONI enthält die Wirkstoffe Ledipasvir und Sofosbuvir zur Behandlung der chronischen Hepatitis C. Diese einmal täglich, oral einzunehmende Kombination führt vergleichsweise rasch zu einem dauerhaften virologischen Ansprechen. Die Verträglichkeit der Kombination ist gut. Angesichts der begrenzten Anzahl von Patienten, die bisher behandelt wurden, ist eine Aussage zu sehr selten auftretenden unerwünschten Wirkungen allerdings noch nicht möglich. Weitere Arzneimittel zur oralen Behandlung einer chronischen Hepatitis C werden in den nächsten Monaten in den Handel kommen. Es bleibt abzuwarten, welche Präparate sich letztlich durchsetzen werden. 1. SULKOWSKI, M.S. et al. N Engl J Med 2014; 370:211-221 2. HARVONI, SPC (Zusammenfassung der Merkmale des Arzneimittels); www.ema.europa.eu 3. HOOFNAGLE, J.H., SHERKER, A.H. N Engl J Med 2014; 370:1552-1553 4. ASSELAH, T., MARCELLIN, P. Liver Int 2015; 35 (Suppl. 1):56-64 Hepatitis C Virustatika zur oralen Behandlung der Hepatitis C In dieser Ausgabe der Zeitschrift für Chemotherapie werden zwei neue Virustatika beschrieben, die seit kurzem für die Therapie der chronischen Hepatitis C zur Verfügung stehen. Die rasante Entwicklung auf diesem Gebiet hält seit Jahren an, nun wurde mit HARVONI (Sofosbuvir/Ledipasvir) ein erstes Kombinationspräparat zur oralen, Interferon-freien Behandlung der Hepatitis C zugelassen. Eine Alternative stellt die Kombination aus den beiden Monopräparaten Sofosbuvir (SOVALDI) und Daclatasvir (DAKLINZA) dar (vgl. ZCT 2014; 35:16). Erst vor einigen Wochen hat der Ausschuss für Humanarzneimittel der Europäischen Arzneimittelbehörde EMA (CHMP) Zulassungsempfehlungen für zwei weitere Präparate zur Therapie der Hepatitis C ausgesprochen: Dasabuvir, ein Hemmstoff der RNA-Polymerase NS5B (EXVIERA) und eine Fixkombination aus Ombitasvir plus Paritaprevir plus Ritonavir (VIEKIRAX). Ombitasvir ist ein Hemmstoff des viralen Proteins NS5A, Paritaprevir hemmt die virale Protease. Die Abbildung auf S. 7 gibt einen Überblick über die Proteine des Hepatitis C-Virus und die Zuordnung der entsprechenden Arzneistoffe. In einigen Teilbereichen besteht sicher noch weiterer Bedarf zur Optimierung der Behandlung. Als die Kombination aus Peginterferon alpha (PEGASYS) und Ribavirin (COPEGUS) noch die Standardtherapie darstellte, galten Infektionen durch die HCV Genotypen 1 und 4 als „schwierig“ zu behandeln, während die Genotypen 2 und 3 geringere Probleme machten. Mit den neueren Therapeutika hat sich die Situation geändert: Die Patienten mit einer HCV Genotyp 3-Infektion stellen nun die am schwierigsten zu behandelnden Patienten dar, bei denen in Abhängigkeit vom Ausmaß einer bestehenden Fibrose und einer Vorbehandlung mit Interferon die Kombination aus Sofosbuvir und Ribavirin nicht ausreichend erfolgreich war.1,2 In der untenstehenden Tabelle wurden die neueren Wirkstoffe zusammengestellt, die bisher im Handel sind oder deren Zulassung unmittelbar bevorsteht. Bei der breiten Anwendung außerhalb der klinischen Studien wird sich zeigen müssen, wie sehr Abstriche bei den hohen Erfolgsraten gemacht werden müssen. Die Compliance der Patienten wird ein wesentlicher Aspekt sein, der beachtet werden muss, um Rückfälle zu vermeiden. Auch die Frage möglicher Arzneimittelinteraktionen wird sich erst bei häufigerer Anwendung und weiterer Untersuchungen besser beantworten lassen. Schließlich bleibt das Problem schwerwiegender unerwünschter Wirkungen offen, da alle neuen Verbindungen nur bei einer begrenzten Tabelle: Virustatika zur Behandlung der chronischen Hepatitis C Arzneimittelgruppe Abkürzung für das virale Zielprotein * Freiname Handelsname Hersteller Genotypen Resistenzbarriere ZCT Heft ProteaseInhibitoren NS3/4A Boceprevir VICTRELIS Merck (MSD) 1 niedrig 5 / 2011 Telaprevir INCIVO Janssen (J&J) 1 niedrig 6 / 2011 Simeprevir OLYSIO Janssen (J&J) 1, 4 niedrig 5 / 2014 Asunaprevir SUNVEPRA** BMS 1, 4 niedrig Paritaprevir in: VIEKIRAX Abbvie 1-4, 6 PolymeraseInhibitoren (Nukleotidanaloga) NS5B Sofosbuvir SOVALDI Gilead alle PolymeraseInhibitoren (nicht-nukleosidisch) NS5B Dasabuvir EXVIERA Abbvie 1 BMS 1, 3-6 niedrig Inhibitoren des Replikationskomplexes NS5A Beclabuvir 2 / 2014 Daclatasvir*** DAKLINZA BMS alle niedrig 1 / 2015 Ledipasvir*** in: HARVONI Gilead alle niedrig 1 / 2105 Ombitasvir in: VIEKIRAX Abbvie alle niedrig * beim Hepatitis C-Virus werden strukturelle (z. B. Hüllproteine) und nichtstrukturelle (NS) Proteine unterschieden ** Handelsname in Japan; Asunaprevir ist in Europa noch nicht im Handel *** Anwendung zusammen mit Sofosbuvir; HARVONI ist ein fixes Kombinationspräparat aus Sofosbuvir und Ledipasvir 6 hoch Januar /Februar 2015 - 36. Jahrg. Zeitschrift für Chemotherapie Anzahl von Patienten geprüft wurden. Von Interesse wird auch sein, in wieweit die sich abzeichnende Konkurrenzsituation zu einer Reduktion des sehr hohen Preisniveaus der neuen Präparate führt. 1. PETTA, S. und CRAXI, A. Liver Int 2015; 35 (Suppl.1 ): 4-10 2. LAWITZ, E. et al. N Engl J Med 2013; 368:1878-1887 Pneumonien Ambulant erworbene Pneumonie: Mono- oder Kombinationstherapie? Die ambulant erworbene Pneumonie ist eine erhebliche Belastung für das Gesundheitswesen, da diese Infektion mit einer relativ hohen Rate an stationär behandelten Patienten und einer hohen Letalität einhergeht. In Deutschland werden im Mittel um die 250.000 Patienten jährlich mit einer ambulant erworbenen Pneumonie in den Krankenhäusern behandelt und die Letalität bewegt sich konstant zwischen 12 und 14%. Die optimale Behandlung, insbesondere die Frage, ob eine Monotherapie ausreicht oder eine Kombinationstherapie besser ist, wird kontrovers diskutiert. Während in den nordamerikanischen Leitlinien immer eine Erfassung der atypischen Erreger in Form einer Kombination aus Betalaktamplus Makrolid-Antibiotikum bzw. mittels Fluorchinolonen empfohlen wird, beharren die europäischen Leitlinien konsequent auf der Monotherapie mit einem BetalaktamAntibiotikum. In der vorliegenden Schweizer Studie wurde versucht, diese Frage zu klären. In einer prospektiven offenen randomisierten Studie vom Januar 2009 bis Januar 2013 wurden 602 Patienten in sechs Schweizer Krankenhäusern der Akut-Versorgung eingeschlossen, von denen letztlich 580 Patienten ausgewertet werden konnten. Die Patienten erhielten in randomisierter Zuteilung Co-Amoxiclav (AUGMENTAN u.a.) in einer Dosierung von 1,2 g viermal täglich oder Cefuroxim (ELOBACT u. a.) 1,5 g dreimal täglich i. v., wobei in der Kombinationsgruppe Clarithromycin (KLACID u. a.) in einer Dosis von 2 x 500 mg i.v. oder oral hinzugegeben wurde. Diagnostisch wurden Blutkulturen, Sputum und Pleuraflüssigkeit mikrobiologisch analysiert sowie das Legionellen-Antigen im Urin bestimmt. Ein Rachenabstrich wurde am ersten Tag zum Nachweis von C. pneumoniae und M. pneumoniae mittels PCR vorgenommen. Die Schwere der Erkrankung wurde mittels Pneumonia Severity Index (PSI) sowie CURB-65-Index bestimmt. Das mediane Lebensalter der Patienten (291 im Monotherapie-Arm und 289 in der Kombinationsgruppe) lag bei 76 Jahren. 351 (60,5%) wiesen mindestens eine oder mehr Grunderkrankungen auf. Der mittlere PSI-Index betrug 84,5; 54% der Patienten hatten einen CURB-65-Index von ≥ 2. Bei 180 Patienten (31,0%) wurde eine bakteriologische Ätio- logie gesichert, davon hatten 48 Patienten (8,3%) eine Bakteriämie. Streptococcus pneumoniae war mit etwa 15% der häufigste Erreger im Monotherapie-Arm und in der Vergleichsgruppe. 12 Patienten (4,1%) in der Monotherapie-Gruppe wiesen eine L. pneumophila-Infektion auf im Vergleich zu vier Patienten (1,4%) im Kombinationsarm. Die Mehrzahl der Patienten in beiden Gruppen (77% und 74,4%) wurde mit Co-Amoxiclav behandelt. Der primäre Endpunkt der Studie war die klinische Stabilität zum Tag 7 der Behandlung, die von 120 Patienten (41,2%) in der Monotherapie-Gruppe nicht erreicht wurde im Vergleich zu 33,6% im Kombinationsarm. Die absolute Differenz betrug 7,6%, was statistisch zu dem Ergebnis führte, dass die Monotherapie gegenüber der Kombinationstherapie primär nicht unterlegen war. Auch bezüglich der Letalität am Tag 30 (4,8% in der Monotherapie-Gruppe versus 3,4% in der KombinationstherapieGruppe) wie auch zum Tag 90 (8,2% versus 6,9%) ergaben sich keine signifikanten Unterschiede. In den Subgruppen-Analysen zeigte sich eine signifikante Überlegenheit der Kombinationstherapie bei den Patienten mit einer Infektion durch atypische Erreger (p = 0,02). Auch bei den Patienten mit einer schwerergradigen Pneumonie (PSI IV oder CURB-65 2 bis 5) zeigte sich eine deutliche Tendenz zugunsten der Kombinationsbehandlung. Auffällig war auch, dass bis zum Tag 30 mehr Patienten im MonotherapieArm wieder in die Klinik eingewiesen werden mussten (7,9% versus 3,1%). 7 Zeitschrift für Chemotherapie FOLGERUNG DER AUTOREN: Prinzipiell erwies sich die Monotherapie mit einem Betalaktam-Antibiotikum im Vergleich zu einer Kombination aus Betalaktam plus Makrolid als nicht unterlegen in der Therapie der leichten bis mittelschweren ambulant erworbenen Pneumonie bei stationär behandelten Patienten. Allerdings sollte bei höherem Schweregrad (PSI Kategorie IV/V oder CURB-65-Score >2) eine Kombinationstherapie bevorzugt werden. Das gleiche gilt auch für Patienten mit einer Infektion durch atypische Erreger, insbesondere durch Legionella pneumophila. GARIN, N. et al. JAMA 2014; 174:1894-1901 Invasive Pneumokokken-Infektionen: Vorangegangene Antibiotika-Therapie beachten Invasive Pneumokokken-Infektionen sind eine bedrohliche Infektion, die mit einer erhöhten Letalität einhergehen. In den USA wird von etwa 43.500 Infektionen mit 5.000 Todesfällen ausgegangen. Eine frühe und wirksame antimikrobielle Therapie ist für die Prognose des Krankheitsbildes von großer Bedeutung. Aus älteren Studien gibt es Hinweise, dass eine vorangegangene Antibiotika-Therapie in den letzten drei Monaten vor der akuten Manifestation der Infektion mit einer erhöhten Resistenz der Erreger einhergehen kann. Eine sehr erfahrene Arbeitsgruppe aus Toronto in Kanada analysierte diese Frage erneut in einer prospektiven Studie in den Jahren 2002 bis 2011. In diesen 10 Jahren wurden insgesamt 4.490 Patienten mit einer invasiven Pneumokokken-Infektion identifiziert, bei 90% (4.062) lagen ausreichende klinische Informationen und auch mikrobiologische Empfindlichkeitsdaten vor. Das mediane Alter der Patienten betrug 57 Jahre und 45% waren Frauen. Bei 4% kam es zu den Infektionen während eines Krankenhausaufenthaltes und 5% der Patienten lebten in Pflegeheimen. 88% der Patienten waren hospitalisiert und 28% benötigten eine intensivmedizinische Versorgung unmittelbar nach der Krankenhausaufnahme. 21% der 4.062 Isolate waren Erythromycin-resistent, 1 % wiesen eine Unempfindlichkeit gegenüber Fluorchinolonen auf, 16% waren Penicillin-resistent und 6% hatten eine Resistenz gegenüber Ceftriaxon (ROCEPHIN u.a.). Zwischen 2002 und 2011 stieg die Resistenz gegenüber Erythromycin von 14% auf 32% an. Die Resistenz gegenüber Penicillin blieb mit 16% auf 17% weitgehend stabil, das Gleiche galt auch für die sehr niedrige Resistenz gegenüber Levofloxacin (TAVANIC u.a.). Bei 29% der Patienten war in den drei Mo- 8 Januar /Februar 2015 - 36. Jahrg. naten vor der akuten Infektion eine antibiotische Behandlung vorangegangen. Diese betraf bei 349 Patienten Makrolide, bei 436 Patienten Fluorchinolone, in 322 Fällen Penicilline und bei 311 Patienten Cephalosporine. In einer Multivarianzanalyse war eine vorangegangene Therapie mit Makroliden, Cephalosporinen und Penicillinen assoziiert mit einer signifikant erhöhten Resistenz der nachgewiesenen Pneumokokken. Insbesondere die Vorbehandlung innerhalb des letzten Monats vor der akuten Erkrankung war mit einer vermehrten Resistenz verbunden. Für die Makrolide konnte ein besonders lang anhaltender Zeitraum vom Abschluss der Vorbehandlung bis zum Nachweis von resistenten Pneumokokken gezeigt werden. FOLGERUNG DER AUTOREN: Die anamnestische Erfassung einer antibiotischen Vorbehandlung bei Patienten mit akuten invasiven Pneumokokken-Infektionen ist außerordentlich wichtig, da ein eindeutiger Zusammenhang besteht zwischen einer antibiotischen Behandlung innerhalb der letzten ein bis drei Monate und dem Nachweis von resistenten Pneumokokken. Insbesondere eine Makrolid-Vorbehandlung innerhalb der letzten drei Monate muss an eine Resistenzentwicklung denken lassen. KUSTER, S. P. et al. Clin Infect Dis 2014;59:944-952 Endokarditis Bakterielle Endokarditis: Ohne Prophylaxe mehr Erkrankungen? Die bakterielle Endokarditis ist eine seltene Infektion, die jedoch mit einer hohen Morbidität und Letalität assoziiert ist. Orale Viridans-Streptokokken werden als häufige Erreger zwischen 35% bis 45% in vielen Studien nachgewiesen. Eine antibiotische Prophylaxe vor einem invasiven zahnärztlichen Eingriff ist bis vor einigen Jahren prinzipiell empfohlen und durchgeführt worden. Hintergrund dieser Prophylaxe ist eine Bakteriämie zu vermeiden, die bei disponierten Patienten eine bakterielle Klappeninfektion auslösen kann. Indikationen für eine perioperative Prophylaxe sind eine vorangegangene abgelaufene Infektion der Herzklappen, Existenz von prothetischen Herzklappen oder nicht beseitigte zyanotische kongenitale Herzfehler. Patienten mit abgelaufenem rheumatischen Fieber, pathologischen Herzgeräuschen oder Hinweisen auf ein Klappenvitium haben ebenfalls ein erhöhtes Risiko. Diese wurde zumeist mit 3 g Amoxicillin (AMOXYPEN u. a.) oder mit 600 mg Clindamycin (SOBELIN u. a.) als einmalige orale Gabe vor dem Eingriff durchgeführt. Da die Evidenz für diese Maßnahme in der Literatur bisher nicht überzeugend dargelegt war, empfahl die nationale Gesundheitsbehörde in Großbritannien im März 2008 bei allen Patienten auf diese Prophylaxe zu verzichten. In einer umfangreichen retrospektiven Analyse untersuchten Autoren aus der Universität von Sheffield die Datenlage bezüglich der antibiotischen Prophylaxe von Januar 2004 bis März 2013 und erfassten auch die Anzahl der Patienten mit einer primären Diagnose einer bakteriellen Endokarditis vom Januar 2000 bis zum März 2013.1 Die Ergebnisse zeigten, dass die Verschreibungen einer antibiotischen Prophylaxe von im Mittel 10.900 monatlich im Zeitraum bis März 2008 abfiel auf 2.236 pro Monat im Zeitraum von April 2008 bis März 2013. In den letzten sechs Monaten der Studie war der Rückgang der Verschreibungen mit nur 1.307 pro Monat noch eindrucksvoller. Die Mehrzahl der Verschreibungen betraf Amoxicillin und wurde überwiegend zu 90% durch Zahnärzte vorgenommen. Insgesamt 19.804 Patienten mit der primären Diagnose einer bakteriellen Endokarditis wurden zwischen Januar 2000 und März 2013 ermittelt. Hinsichtlich der Inzidenz einer Endokarditis konnten die Autoren bis zum März 2008 einen geringen jährlichen Anstieg beobachten. Dieser Anstieg änderte sich jedoch signifikant nach der Empfehlung der nationalen Gesundheitsbehörde mit einer monatlichen Zunahme von 0,11 Erkrankungen pro 10 Millionen Einwohner. Bis zum März 2013 berichteten die Autoren, dass monatlich 34,9 Fälle einer bakteriellen Endokarditis mehr auftraten im Vergleich zu der Periode vor März 2008. Von Bedeutung war, dass dieser signifikante Trend nicht nur bei Patienten mit hohem Risiko, sondern auch bei der Patientengruppe mit mittlerem Risiko nachweisbar war. In der Diskussion ihrer Daten weisen die Autoren ausdrücklich darauf hin, dass in einer ersten Studie 2 mit einer Analyse nach zwei Jahren dieser signifikante Trend nicht nachweisbar war und dieser erst in der vorliegenden Analyse über fünf Jahre deutlich wurde. FOLGERUNG DER AUTOREN: In einer retrospektiven Fünf-Jahres-Analyse vor und nach der Empfehlung der nationalen britischen Gesundheitsbehörde, auf eine Endokarditis-Prophylaxe zu verzichten, wurde zwar eine signifikante eindrucksvolle Abnahme der Prophylaxe-Verschreibungen festgestellt, jedoch auf der anderen Seite auch ein signifikanter Anstieg der Inzidenz der bakteriellen Endokarditis. Die Autoren weisen aber vorsichtigerweise auch darauf hin, dass andere Faktoren (bessere Diagnostik u.a.) einen Einfluss auf ihre Ergebnisse haben könnten. Januar /Februar 2015 - 36. Jahrg. Zeitschrift für Chemotherapie 1. DAYER, M. J. et al. Lancet 2014; online Nov. 2014 2. Thornhill, M. M. et al. Brit Med J 2011; 342:d2392 Reserve-Therapie bei komplizierten Endokarditiden durch MRSA Die antibiotische Therapie einer bakteriellen Endokarditis durch Methicillin-resistente Staphylococcus aureus (MRSA) wird auf der Basis der gegenwärtigen internationalen Leitlinien vorwiegend mit Vancomycin (VANCOMYCIN CP u.a.) oder Daptomycin (CUBICIN) durchgeführt. Insbesondere bei der Endokarditis der Klappen des linken Herzens ist diese Therapie häufig nicht erfolgreich und Alternativbehandlungen werden notwendig. In vitro-Untersuchungen deuten darauf hin, dass Fosfomycin (INFECTOFOS) über eine schnelle bakterizide Aktivität gegen grampositive Erreger verfügt mittels Hemmung der frühen Phase der Peptidoglykan-Synthese in der bakteriellen Zellwand. Wegen der schnellen Resistenzentwicklung einer Monotherapie mit Fosfomycin muss diese Substanz in der Regel mit anderen Antibiotika kombiniert werden. Eine spanische Autorengruppe hat auf der Basis ihrer günstigen in vitro-Daten von Fosfomycin mit dem Carbapenem-Antibiotikum Imipenem (ZIENAM u. a.) diese Kombination bei schwerkranken Patienten mit nachgewiesener Endokarditis bzw. Bakteriämie durch MRSA eingesetzt. Insgesamt 16 Patienten, davon 12 mit einer Endokarditis an linksseitigen Herzklappen, zwei mit einer Infektion einer Gefäßprothese und zwei mit komplizierten Bakteriämien, wurden nach nicht erfolgreicher vorangegangener Behandlung mit Vancomycin und Daptomycin prospektiv in die Studie aufgenommen. Das mediane Lebensalter betrug 67,5 Jahre, 13 Patienten litten an chronischen Grunderkrankungen wie Leberzirrhose, Niereninsuffizienz und Diabetes mellitus sowie Tumoren. Alle MRSA-Isolate waren empfindlich gegenüber Vancomycin und Daptomycin, die Fosfomycin-MHK-Werte lagen durchweg bei weniger als 32 µg/ml und vier Isolate wiesen MHK-Werte gegenüber Imipenem im sensiblen Bereich auf. Die Kombinationstherapie über im Median 28 Tage bestand in 2 g Fosfomycin alle sechs Stunden täglich intravenös plus Imipenem 1g alle sechs Stunden täglich ebenfalls intravenös. Am primären Endpunkt der Studie – 72 Stunden nach Beginn der Therapie – waren sämtliche Blutkulturen negativ. Eine Durchbruchsbakteriämie wurde unter der Behandlung nicht beobachtet. Am klinischen Endpunkt, 45 Tage nach Beendigung der antibiotischen Therapie waren 11 der 16 Patienten erfolgreich behandelt, fünf waren verstorben. In vier der fünf Todesfälle waren andere Ursachen und nicht die Infektion für den ungünstigen Verlauf verantwortlich. Als wesentliche Unverträglichkeitsreaktion wurde bei drei Patienten mit einer Leberzirrhose eine erhebliche Natrium-Belastung beobachtet, die letztlich bei einem Patienten für den tödlichen Verlauf mitverantwortlich war. FOLGERUNG DER AUTOREN: Die Aussagekraft dieser Studie ist sicherlich limitiert wegen der recht kleinen Patientenzahl. Allerdings sind die relativ günstigen Therapieergebnisse der Kombination aus Fosfomycin (INFECTOFOS) mit Imipenem (ZIENAM) als Reservetherapie bei nicht erfolgreicher Vorbehandlung einer Linksherz-Endokarditis recht ermutigend. Eine inzwischen gestartete prospektive Vergleichsstudie soll den Stellenwert dieser Kombination weiter untersuchen. DEL RIO, A. et al. Clin Infect Dis 2014; 59:1105-1112 Nebenwirkungen Makrolide und Pylorusstenose – deutliche Risikoerhöhung in den ersten zwei Lebenswochen Neben ihrer antibakteriellen Aktivität besitzen Makrolid-Antibiotika weitere pharmakologische Wirkungen. Es ist bekannt, dass sie Motilin-Rezeptoren im Gastrointestinaltrakt stimulieren können. Dies wird zum Beispiel bei der Behandlung der Gastroparese mit Makroliden ausgenutzt. Bei Neugeborenen verursacht die Stimulation der glatten Muskulatur wahrscheinlich eine Pylorushypertrophie und Stenose. Auf das erhöhte Risiko einer infantilen hypertrophen Pylorusstenose (IHPS) nach Makrolidbehandlung bei Säuglingen hatten bereits frühere Untersuchungen hingewiesen. Unklarheiten bestehen jedoch noch hinsichtlich der sensiblen Entwicklungsphase und inwieweit eine mütterliche Einnahme auch zu diesen kindlichen Veränderungen führen kann, da Makrolide in der Muttermilch vorhanden sind und auf den Säugling übergehen. Eine Gruppe von Epidemiologen untersuchte in Dänemark erneut die Zusammenhänge und analysierte die Daten von etwa einer Million Kindern, die zwischen 1996 und 2001 geboren worden waren. Eine Behandlung innerhalb der ersten zwei Lebenswochen führte zu einem etwa 30fachen Anstieg der IHPS-Inzidenz. Dies entspricht einer Zunahme der Erkrankung von 2,4% und stimmt mit den früheren Resultaten überein. Auch in einem späteren Zeitraum (14 bis 120 Tage nach der Geburt) war noch ein erhöhtes Risiko erkennbar (ca. 3,2-fach). Die mütterliche Einnahme eines Makrolidantibiotikums innerhalb von zwei Wochen nach der Geburt war mit einer ähnlichen Risikoerhöhung assoziiert (3,5fach). Bei Makrolidgebrauch in der späten Schwangerschaft war dagegen keine signifikante Erhöhung des Risikos zu ermitteln. FOLGERUNG DER AUTROEN: Eine Behandlung von Neugeborenen mit Makrolid-Antibiotika ist in den ersten beiden Lebenswochen mit einem deutlich erhöhten Risiko für eine Pylorushypertrophie assoziiert. Falls die stillende Mutter während dieser Zeit mit einem Makrolid behandelt wird, ist ebenfalls eine geringe Assoziation nachweisbar. Auf Makrolide sollte bei Neugeborenen verzichtet werden. Problematisch ist die Situation, wenn das Kind an Keuchhusten erkrankt ist. Bei Pertussis sind Makrolide die Mittel der ersten Wahl, ohne Antibiotikatherapie kann diese Infektion bei Säuglingen zum Tode führen. LUND, M. et al. Brit Med J 2014; 348: g1908 Verstärken Statine die myotoxische Wirkung von Daptomycin? Daptomycin (CUBICIN) kann Myopathien verursachen vgl. www.zct-berlin.de, „Neueinführungen, Daptomycin“). Eine Kontrolle der Creatin-Phosphokinase (CPK) wird daher empfohlen. Über mögliche synergistische Wirkungen zwischen Daptomycin und anderen potenziell myotoxischen Arzneistoffen ist wenig bekannt. In den USA wurden daher in einer retrospektiven Studie die Daten von 49 Patienten ausgewertet, die während einer Behandlung mit Daptomycin gleichzeitig ein Statin-haltiges Arzneimittel bekamen. Diese wurden mit einer Gruppe von 171 Patienten verglichen, die keine Statine während einer Daptomycin-Therapie erhielten. Myalgien traten bei 6,1% der Patienten auf, die gleichzeitig mit Statinen behandelt wurden (3 von 49), dagegen nur bei 2,9% (5 von 171), die nur das Lipopeptidantibiotikum erhalten hatten. Ein ähnlicher Unterschied wurde hinsichtlich der CPK-Erhöhung gefunden: Werte von > 1000 U/L traten bei etwa 10% bzw. 5% der Patienten auf. Auch die Abbruchrate war in der Kombinationsgruppe höher (6,1% vs. 3,5%); nach Absetzen des Antibiotikums waren sowohl die Symptome als auch die Laborwerte reversibel. Trotz deutlicher Differenzen zwischen den Gruppen waren die Ergebnisse nach üblichen Kriterien statis- 9 Zeitschrift für Chemotherapie Januar /Februar 2015 - 36. Jahrg. tisch nicht signifikant unterschiedlich. Weitere, prospektive Untersuchungen an größeren Patientengruppen sind notwendig, um die Risiken einer kombinierten Gabe besser abschätzen zu können. FOLGERUNG DER AUTOREN: Myopathien waren nach der Gabe von Daptomycin (CUBICIN) häufiger, wenn die Patienten gleichzeitig mit Statinen behandelt wurden. Die Unterschiede waren allerdings nicht statistisch signifikant. BLAND, C.M. et al. Antimicrob Agents Chemother 2014; 58:5726-5731 Neue Daten zur Verträglichkeit von Amoxicillin im Vergleich zu Placebo Amoxicillin (diverse Generika) zählt mit Abstand zu den am häufigsten verordneten Antibiotika. Die unerwünschten Wirkungen des Arzneimittels gelten als gut bekannt, genaue Angaben zur Häufigkeit von gastrointestinalen Nebenwirkungen oder Hautreaktionen sind jedoch kaum verfügbar. Daher scheint es auf den ersten Blick sinnvoll zu sein, jene Studien genauer auszuwerten, in denen Amoxicillin mit einer Placebo-Medikation verglichen wurde. Allerdings ist das Ergebnis einer aktuell publizierten Metaanalyse eher enttäuschend. Wissenschaftler aus Australien identifizierten aus zunächst 730 Veröffentlichungen insgesamt 45 Studien mit ausreichender Qualität, in denen Amoxicillin alleine oder in Kombination mit Clavulansäure (diverse Generika) untersucht wurde. Die Publikationen stammen aus den Jahren 1977 bis 2013, im Mittel wurden die Arzneimittel sieben Tage lang gegeben, insgesamt wurden die Daten von mehr als 10.000 Patienten erfasst, von denen etwa die Hälfte mit Amoxicillin behandelt wurde. Leider wurden nur in insgesamt 25 Studien die Nebenwirkungen detailliert genug beschrieben, um sie auswerten zu können. Auch in diesen Fällen wurde meist nicht genau genug angegeben, wie die unerwünschten Wirkungen erfasst und registriert wurden. Zu den wichtigsten Nachteilen dieser Auswertung zählt die Tatsache, dass sehr unterschiedliche Studien zusammengefasst wurden. Sie wurden zum Beispiel bei Kindern oder Erwachsenen durchgeführt und zu den Indikationen zählten Infektionen der Atemwege, Behandlung oder Prophylaxe von Dentalinfektionen oder die Anwendung bei gynäkologischen Infektionen. Die Anzahl der Patienten pro Gruppe schwankte zwischen 10 und knapp 1000. In einer der umfangreichsten Untersuchungen wurde 10 der Effekt von Amoxicillin als Teil einer umfassenden Behandlung von schwer unterernährten Kindern in Malawi (Afrika) geprüft. Es liegt nahe, dass aus solchen Daten kaum Rückschlüsse auf das Nebenwirkungsprofil der Arzneimittel generell gezogen werden können. Die Auswertung kam zu dem Ergebnis, dass das Risiko für eine Diarrhö oder Candidiasis durch eine Amoxicillin-Therapie signifikant erhöht war. Andere bekannte Nebenwirkungen des Antibiotikums, wie Hautausschlag, Juckreiz, Übelkeit, Erbrechen waren nicht signifikant häufiger im Vergleich zu Placebo. FOLGERUNG DER AUTOREN: Die Veröffentlichung macht deutlich, dass durch eine Metaanalyse die Datenlage häufig nicht verbessert wird, sondern aufgrund der Heterogenität der zugrunde liegenden Daten die Informationen eher unschärfer werden. Eine detaillierte Auswertung der Einzelstudien und kritische Interpretation der Ergebnisse sind häufig sinnvoller. GILLIES, M. et al. CMAJ 2015; 187:E21-31 Impressum Kündigung des Abonnements jeweils drei Monate zum Jahresende. Die gewählten Produktbezeichnungen sagen nichts über die Schutzrechte der Warenzeichen aus. Zeitschrift für Chemotherapie Eichenallee 36a, 14050 Berlin Herausgeber: Prof. Dr. med. H. Lode Mitherausgeber: Prof. Dr. med. R. Stahlmann 1980 Zeitschrift für Chemotherapie (H. Lode), Berlin Redaktion: Prof. Dr. med. H. Lode (verantwortlich), Prof. Dr. med. R. Stahlmann, Frau R. Schoeller-Wiley (Fachärztin), Prof. Dr. med. W. R. Heizmann, München, Prof. Dr. M. Kresken, Bonn, Frau Nadja Engelhardt (Redaktionsassistentin). Die Zeitschrift für Chemotherapie erscheint zweimonatlich. Bezug nur im Abonnement. Jahresbezugspreise für Ärzte, Apotheker und Einzelpersonen 36,- Euro, für Studenten und Pensionäre 27,- Euro (Nachweis erforderlich), für Firmen, Behörden und andere Institutionen mit Mehrfachlesern 66,- Euro. Alle Rechte weltweit vorbehalten. Diese Publikation darf auch nicht auszugsweise ohne schriftliche Einwilligung des Copyright-Eigentümers auf irgendeine Weise und in irgendeiner Sprache vervielfältigt werden. Obwohl die in dieser Publikation enthaltenen Informationen mit großer Sorgfalt zusammengestellt und auf Richtigkeit geprüft wurden, übernehmen weder die Verfasser, der Herausgeber, die Angestellten oder ihre Vertreter die Verantwortung dafür, dass die Information ihre Gültigkeit behalten, noch haften sie für Irrtümer, Auslassungen oder Ungenauigkeiten in dieser Publikation, die durch Fahrlässigkeiten oder andere Ursachen entstanden sind sowie für alle sich hieraus ergebenden Folgen. Abonnement-Bestellschein Als Abonnent erhalten Sie sechs ZCT-Ausgaben zum jährlichen Bezugspreis von • 36, - Euro • 27, - Euro ermäßigt für Studenten und Pensionäre • 66, - Euro für Mehrfachleser • 48, - Euro für Sendungen ins Ausland • 24, - Euro für die PDF-Datei der Zeitschrift per E-Mail Vor- und Zuname Anschrift Datum und Unterschrift Bitte senden Sie Ihre Bestellung an den Verlag ZCT, Eichenallee 36a, D-14050 Berlin, per E-Mail an [email protected] oder per Fax an 030-312 47 42 (schriftl. Widerruf ist innerhalb eines Monats möglich). Wir bedanken uns für Ihr Interesse!