Ausgabe als PDF - Klinik St. Anna
Werbung

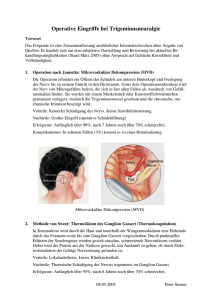
FÜR SIE AUSGESUCHT Trigeminusneuralgie: Gesichtsschmerzen Einseitige Gesichtsschmerzen im Versorgungsbereich des Nervus trigeminus sind seit Jahrhunderten in der medizinischen Literatur bekannt. Die erste Beschreibung der Trigeminusneuralgie scheint von Arethaeus von Kappadokien im 2. Jahrhundert v. Chr. zu stammen [1]. Neunhundert Jahre später beschrieb Avicenna zwei Gesichtssyndrome. In dem einen Fall die typische Beschreibung einer Fazialisparese, Gesichtslähmung, im zweiten Teil die charakteristische Symptomatik einer Trigeminusneuralgie [2]. Formen von Trigeminusneuralgie Die idiopathische Form des Typs 1 zeichnet sich durch spontane episodische lancierende, für Sekunden anhaltende Schmerzen aus. Für idiopathische Trigeminusneuralgie Typ 2 sind anhaltende, pulsierende, oder brennende Schmerzen über mehr als die Hälfte der Zeit typisch. Andere Formen der Trigeminusneuralgie können als Folge einseitiger Schädigung des Nerven durch Trauma oder einen operativen Eingriff bzw. eines entzündlichen Prozesses (Herpes Zoster) auftreten. Ursache Derzeit wird als pathophysiologische Grundlage der klassischen Trigeminusneuralgie ein GefässNerven-Konflikt angenommen [3]. Dabei wird der Nervus trigeminus bzw. der Austrittspunkt des Nerven am Hirnstamm typischerweise durch eine Schlinge der Arteria cerebelli superior bzw. der Arteria cerebelli inferior anterior (AICA) komprimiert. Die durch den Druck und Pulsation der Gefässschlinge entstandene Entmarkung des peripheren Verlaufes des Nervus trigeminus am Hirnstamm soll die paroxysmalen Anfälle verursachen. Diagnose Die Diagnose der Trigeminusneuralgie erfolgt immer auf Grundlage der Anamnese des Patienten. Dabei werden agonisierende, paroxysmale, lancierende Schmerzen in einem oder mehreren Ästen des Nervus trigeminus angegeben, ausgelöst durch Aktivitäten wie Kauen, Sprechen, Schlucken, Berührung des Gesichtes oder Zähneputzen. Schmerzfreie Intervalle sind üblich und können Tage, Wochen oder Monate, gelegentlich auch Jahre anhalten. Die Anamnese kann mehrere Monate bis mehrere Jahrzehnte erfassen. Operative Diagnostik Die Diagnosestellung erfolgt hauptsächlich aufgrund der erhobenen Anamnese. Die heutige apparative Diagnostik erfolgt ausschliesslich durch die kernspintomographische Untersuchung des Schädels. Die Untersuchung sollte primär eine pathologische Raumforderung, die zu einer Kompression des Hirnstammes bzw. des Nervus trigeminus führt, ausschliessen. Gleichzeitig kann ein demyelinisierender Prozess im Bereich des Kerngebietes im Rahmen einer Multiplen Sklerose dokumentiert werden. Der Nachweis eines Gefäss-Nerven-Konfliktes zeigt bei der Bildgebung eine Spezifität für Patienten mit Typ 1 und Typ 2 mit 91- bzw. 66-prozentiger Sicherheit. Wird anhand der klinischen Symptomatik die Diagnose einer Trigeminusneuralgie gestellt, ist der fehlende Nachweis eines Gefäss-Nerven-Konfliktes im MRT für die Indikationsstellung der Therapie zu vernachlässigen. Formen der Therapie Erst zu Beginn des 20. Jahrhunderts wurde über die medikamentöse Therapie, Chemoneurolyse, Rhizotomie, Manipulationen des Nervus trigeminus und Radiotherapie als mögliche Behandlung der Trigeminusneuralgie berichtet. Die erste Einführung antikonvulsiver Medikamente als mögliche Behandlungsmodalität der Trigeminusneuralgie erfolgte durch Bergouignan im Jahr 1942 [10]. Die Wirkung des Carbamazepine in der Behandlung der Trigeminusneuralgie wurde mit grosser Effizienz durch Bloom untersucht [11]. Carbamazepine ist auch heute noch in der Behandlung der Trigeminusneuralgie das erste Medikament der Wahl mit einer annähernden Kontrolle der Beschwerden bis auf 90 Prozent. In neuerer Zeit wird das Gabapentin häufiger favorisiert. Die primäre Wirkung einer Muskelrelaxanz für die Behandlung der Trigeminusneuralgie wurde 1966 durch King entdeckt [6]. Die noch heute angewendete perkutane Thermokoagulation durch Insertion einer Nadel durch das Foramen ovale wurde durch Härtel [7] veröffentlicht und später durch Putnam und Hampton [8] sowie Kuhlenkampf 1942 verfeinert [9]. Auf Grundlage der durch Reethi [10] eingeführten Elektrokoagulation basiert die Weiterführung der Methode durch Kirchner 1931 [11]. Die radio-frequente Thermokoagulation der präganglionären Trigeminusfasern im Cavum meckeli führten Sweet und Wespsic 1974 ein [12]. Diese Methode wird auch heute in bestimmten Fällen der Trigeminusneuralgie angewendet. Die perkutane Ballonkompression, eingeführt durch Mullan und Lichtor 1983 [13], ist eine weitere Methode der Deafferenzierung des Nervus trigeminus. Ein alternativer chirurgischer Zugang zur partiellen Durchtrennung des Nervus trigeminus via lateral subokzipitale Kraniotomie wurde durch Dandy propagiert [14]. Erst 1967 explorierte Peter Jannetta die hintere Schädelgrube unter Verwendung des Operationsmikroskopes und erneuerte die Behandlung durch die Beschreibung der mikrovaskulären Dekompression des Nervus trigeminus [15]. Die Einführung der fokussierten stereotaktischen Radiation (Gamma-Knife) zur Behandlung der Trigeminusneuralgie erfolgte durch Leksel [16]. Fazit der Behandlungsmethoden Die medikamentöse Therapie der Trigeminusneuralgie ist und bleibt die erste Wahl der Behandlung. Bei Versagen dieser Therapie bzw. nicht vertretbaren Nebenwirkungen scheint die mikrovaskuläre Dekompression nach Jannetta die beste Wahl zur Behandlung der Trigeminusneuralgie zu sein, wobei die perkutane Deafferenzierung durch Thermokoagulation den Risiko-Patienten vorbehalten bleiben sollte. Im Allgemeinen wird die erfolgte Schmerzfreiheit über fünf Jahre nach mikrovaskulärer Dekompression mit über 84 Prozent angegeben, somit beträgt die Rezidiv-Rate ca. 26 Prozent. Eigene Erfahrungen Das eigene Patientenkollektiv umfasst mehr als 340 Patienten. Eine mikrovaskuläre Dekompression des Nervus trigeminus wurde bei 210 Patienten vorgenommen. In über 90 Prozent der Fälle waren der 2. Ast bzw. und/oder der 3. Ast des Nervus trigeminus betroffen. Nur 10 Prozent der Patienten gaben primär Schmerzen hauptsächlich im 1. Ast an. Intraoperativ konnte bei 81 Prozent der Patienten ein Gefäss-Nerven-Konflikt nachgewiesen und durch die mikrovaskuläre Dekompression behoben werden. Über 85 Prozent der Patienten in dieser Gruppe waren auch nach fünf Jahren beschwerdefrei. Die restlichen Patienten (hauptsächlich Risikopatienten bzw. Patienten ohne Nachweis eines Gefäss-Nerven-Konfliktes oder bei Trigeminusneuralgie aufgrund einer MultipleSklerose-Erkrankung) wurden durch die Thermokoaguation behandelt. Dieser Eingriff musste durchschnittlich nach zweieinhalb bis drei Jahren wiederholt werden. Abbildungen zur mikrovaskulären Dekompression des Nervus trigeminus Abbildung 1 Abbildung 2 Abbildung 3 Literatur: 1. Rose FC. Trigeminalneuralgia. Arch Neurol 1999;56:1163–1164. Die erste vollständige Beschreibung der Trigeminusneuralgie erfolgte durch John Locke im Jahre 1677. 2. Amelie NO. Avicenna and trigeminal neuralgia. J Neurol Sci 1965;102:105–107. 3. Jannetta PJ. Arterial compression of the trigeminal nerve at the pons in patients with trigeminalneuralgia. J Neurosurg 1967; 26 (Suppl):159–162. 4. Bergouignan M. Cures de neurologies essentielles par le dephenyl hydantoinate de sounde. Rev Laryngeol Otol Rhinol 1942;63:34–41. 5. Blom S: trigeminal neuralgia. Its treatment with a new anti-convolsant drug. Lancet 1962;1:839–849. 6. King RB. The value of nephenesin carbamate in the control of pain in patient with tic douloureux. J. Neurosurg 1966;25:153–158. 7. Härtel F. Über die intrakranielle Injektionsbehandlung der Trigeminusneuralgie. Med Klinik 1914;10:582–584. 8. Putnam TJ, Humpton AO. A technic of injection into the gasserian ganglion under roentgenographic control. Arch Eurol Psychiat 1936;35:92–98. 9. Stookey B, Ransohoff J. Trigeminal neuralgia: Its History and Treatment. Springfield IL: Charles C: Thomas, 1959. 10. Willkinns RH. Trigeminal neuralgia historical overview. In: Burchiell K. Surgical management of pain. New York: Thieme 2002;288–301. 11. Kirchner M. Zur Elektrochirurgie. Aich Klin Chir 1931;167:761–768 12. Seet WH, Wespic JG. Controlled thermocoagulation of trigeminal ganglion and rootlets for differential destruction of pain fiber 1. Trigeminal Neuralgia. J. Neurosurg 1974;40:143–156. 13. Mullan S, Lichtor T. Percutaneus microcompression of the trigeminal ganglion for trigeminal neuralgia. J Neurosurg 1983;59: 1007–1012. 14. Apfelbaum RI. Neurovascular decompression: the procedure of choice? Clin Neurosurg 2000;6: 473–498. 15. Jannetta PJ. Arterial compression of the trigeminal nerv at the pons in patient with trigeminal neuralgia. J Neurosurg 1967; 26(Suppl):159–162. 16. Leksel L. Steriotacic radiosurgery in trigeminal neuralgia. Acta Chir Skant 1971;137:311–314. Autor: Prof. Dr. med. Abolghassem Sepehrnia Facharzt für Neurochirurgie, Spezialist für Schädelbasischirurgie Klinik St. Anna Ärztehaus Lützelmatt (Trakt L) St. Anna-Strasse 32 6006 Luzern T +41 41 918 00 00 F +41 41 918 00 01 E-Mail Zur Online Visitenkarte www.neurochirurgie-sepehrnia.de Neue Paradigmen in der Bildgebung des Schädel-Hirn-Traumas Jedes Jahr erleiden etwa 3000–5000 Menschen in der Schweiz ein Trauma mit Hirnverletzung. Etwa 75 % davon erleiden eine leichte traumatische Hirnverletzung (MTBI), etwa 715 Menschen erlitten 2010 ein schweres Hirntrauma. Bisher beschränkte sich die Bildgebung im Fall eines akuten Schädel-Hirn-Traumas fast ausschliesslich auf die CT, da hiermit sowohl knöcherne Verletzungen als auch grössere frische Hirnblutungen abgeklärt werden können. Neuere Techniken in der MRI zeigen subtilere Veränderungen des Parenchyms und ermöglichen so prognostische Aussagen vor allem bei geringen Traumata. Bildgebende Diagnostik des SHT Das leichte Schädel-Hirn-Trauma (MTBI – Mild Traumatic Brain Injury) ist charakterisiert durch eine Bewusstlosigkeit unter 30 Min., einen GCS (Glasgow Coma Scale) von 13–15 bei der medizinischen Untersuchung und eine Amnesie von unter 24 Stunden. Während sich die meisten Patienten mit MTBI problemlos erholen, zeigt eine Subgruppe auch nach Jahren anhaltende Ausfälle. Diese Patienten sollten daher frühzeitig einer geeigneten Therapie zugeführt werden, um Folgeschäden zu minimieren. Die von der SUVA herausgegebenen Leitlinien für die Schweiz empfehlen bei Patienten mit MTBI die Durchführung einer CT für alle Patienten mit einem GCS von 13 oder 14 [1]. Bei Patienten mit einem GCS von 15 wird dagegen je nach Risiko entweder eine CT oder eine klinische Überwachung empfohlen, wobei die CT vor allem aus Strahlenschutzgründen abgelehnt wird. Die MRI stellt bei kooperativen Patienten eine strahlenfreie Alternative dar, welche Blutungen, insbesondere relevante Subarachnoidalhämatome, sensitiver darstellt als die CT Neue bildgebende Methoden Bei Patienten mit GCS 15, geringem Risiko und negativer CT ist die Wahrscheinlichkeit einer relevanten intrakraniellen Läsion extrem gering [2]. Bei persistierenden Beschwerden wird jedoch die Durchführung einer MRI empfohlen, da eine erneute CT-Kontrolle in der Regel keine Veränderungen zeigt. Moderne Techniken der MRI wie die suszeptibilitätsgewichtete Bildgebung (SWI) sind gegenüber der CT um ein Vielfaches empfindlicher für minimale Parenchymblutungen (Abbildung 1). Allerdings weisen Personen, die aktiv Kontaktsportarten betreiben, häufig minimale Traumata auf, an die sich der Patient selbst nicht erinnert [3]. Dies gilt auch für Fussballspieler, die häufige Kopfbälle spielen. Kleine Parenchymblutungen müssen daher nicht immer von dem aktuellen Trauma stammen. Dies erhöht die Bedeutung einer Bildgebung früh nach dem Trauma, da zu diesem Zeitpunkt frische Blutungen noch von älteren bereits vorbestehenden Blutungen unterschieden werden können. Letztere haben aktuell keine Relevanz, sind jedoch prognostisch bedeutsam, da sie mit einem erhöhten Demenzrisiko verbunden sind. Neben der Blutungsdarstellung können in der MRI mit der sogenannten Diffusionstensor-Bildgebung (DTI) die Nervenfasern bzw. die Bahnen innerhalb des Gehirns dargestellt werden (Abbildung 2). Patienten ohne Veränderungen in der CT nach MTBI zeigten eine erhöhte Diffusion in den Faserstrukturen der Hemisphären, was auf mikroskopische Schädigungen der Bahnen hinweist. Ausgeprägte Läsionen zeigen auch eine umschriebene Diffusionsstörung, vergleichbar zu punktförmigen Infarkten des Parenchyms. Neben der Erkennung der akuten Verletzungen ohne Strahlenbelastung ermöglicht die MRI in der frühen und subakuten Phase nach dem Trauma eine Aussage über die Prognose. So hatten Patienten mit normaler CT jedoch mehr als 3 Microblutungen oder axonalen Scherverletzungen in der DTI eine signifikant schlechtere Prognose in klinischen Tests 3 Monate nach dem Trauma. Die prognostische Bedeutung dieser minimalen Veränderungen war dabei ähnlich ausgeprägt wie eine traumatische Subarachnoidalblutung [4]. Fazit Zusammenfassend können mit der MRI relevante Veränderungen frühzeitig erkannt werden, welche der bisherigen Diagnostik mittels CT entgangen sind. Insbesondere bei Patienten mit unklarem Trauma, jedoch aktuell gutem Zustand sollte die Indikation zur MRI frühzeitig gestellt werden, um minimale Schädigungen zu erkennen und eine geeignete Rehabilitation einzuleiten. Teamwork zum Wohl des Patienten Planung und Operation gehen bei der minimal-invasiven Chirurgie Hand in Hand zwischen Chirurg und interventionellem Radiologen. Dank flexiblen Anästhesie- und OP-Teams kann konventionelle Chirurgie mit Hightech-Intervention zum Nutzen des Patienten verschmolzen werden. Am Ende des Eingriffs wird mit einer abschliessenden 3D-Bildgebung die Qualität überprüft und dokumentiert, bevor der Patient aus der Narkose erwacht. Dank minimal-invasiver Chirurgie folgt dem „grossen Trauma“ der Fraktur das „kleine Trauma“ der Operation. Abbildungen: Abbildung 1: CT (oben) und MRI (unten) mit blutungssensitiver Hämosequenz eines Patienten mit diffuser axonaler Schädigung (DAI). Während die CT keine Veränderungen zeigt, finden sich in der MRI zahlreiche Mikroblutungen (Pfeile) an der Mark-Rindengrenze und im subcorticalen Marklager der Hemisphären als Zeichen der Scherverletzung. Abbildung 2: Schädel-MRI eines Patienten mit Status nach MTBI. In der FLAIR-Sequenz (a) zeigt sich eine kleine Parenchymblutung rechts frontal (Pfeilspitzen), in der T2*-gewichteten blutungssensitiven Hämosequenz (b) kann darüber hinaus noch eine kleine Blutung rechts occipital erkannt werden. In der Diffusions-Tensorbildgebung (c) mit Traktographie (d) zeigt sich ein Abbruch der Sehbahn auf Höhe dieser Blutung auf der rechten Seite (breiter Pfeil in d), während sich die gesunde Sehbahn links bis an die Sehrinde verfolgen lässt (kleine Pfeile in d) Literatur 1. Johannes und Schaumann-von Stosch. Leichte traumatische Hirnverletzung: Empfehlungen für die Akutversorgung. Suva Medical 2010 (2010) – http://www.suva.ch/artikel-lthv.pdf 2. Af Geijerstam und Britton. Mild head injury: reliability of early computed tomographic findings in triage for admission. Emergency Medicine Journal (2005) vol. 22 (2) pp. 103–7 3. Koerte et al. A review of neuroimaging findings in repetitive brain trauma. Brain Pathol (2015) vol. 25 (3) pp. 318–49 4. Yuh et al. Magnetic resonance imaging improves 3-month outcome prediction in mild traumatic brain injury. Ann Neurol (2013) vol. 73 (2) pp. 224–35 Autor: PD Dr. med. Arne Fischmann Facharzt Radiologie Institut für Radiologie und Nuklearmedizin St. Anna-Strasse 32 6006 Luzern T +41 41 208 30 30 F +41 41 208 30 23 E-Mail [email protected] Zur Online Visitenkarte WIR HEISSEN HERZLICH WILLKOMMEN Neuer zugelassener Arzt an der Klinik St. Anna für Orthopädische Chirurgie und Traumatologie des Bewegungsapparates, Spezialist für Fusschirurgie Wir heissen Dr. med. Christian Sommer als zugelassenen Arzt an der Klinik St. Anna per 1. Februar 2015 herzlich willkommen. Er ist schon seit mehreren Jahren Belegarzt an der damaligen swissana clinic, die seit August zur Privatklinikgruppe Hirslanden gestossen ist und seit Januar neu Hirslanden Klinik Meggen heisst. Berufliche Tätigkeiten während der letzten Jahre: 2000 Facharzttitel FMH für Orthopädische Chirurgie und Traumatologie des Bewegungsapparates 2000 - 2002 Oberarzt Schulthessklinik Zürich, Orthopädische Abteilung 2003 Praxiseröffnung und Aufnahme Belegarzttätigkeit an der Klinik St. Anna Luzern, Subspezialität Fusschirurgie 2007 Eröffnung der FussClinic an der Haldenstrasse 6 in Luzern 2008 Sprechstundentätigkeit am Bethesda Spital in Basel 2008 Belegarzt an der privaten swissana clinic in Meggen 2009 Belegarzt an der Privatklinik Pyramide am See in Zürich Zusätzliche Tätigkeiten Mitgliedschaften in folgenden Institutionen: Verbindung Schweizer Ärztinnen und Ärzte (FMH) Gesellschaft für Chirurgie und Medizin des Fusses (SFAS) Schweizerische Gesellschaft für Orthopädie und Traumatologie (SGOT) Schweizerische Gesellschaft für Physikalische Medizin und Rehabilitation Schweizerische Gesellschaft für Sportmedizin Schweizerische Gesellschaft für Rheumatologie Schweizerische Belegärzte-Vereinigung American Orthopaedic Foot and Ankle Society European Society of Foot and Ankle Surgeons Gesellschaft für Fusschirurgie (GFFC) Deutsche Assoziation für Fuss & Sprunggelenk e.V. D.A.F. Vereinigung Süddeutscher Orthopäden e.V. Gesellschaft der orthopädischen Chirurgen der Innerschweiz (ISO) Rheumaliga Luzern/Obwalden AerzteGesellschaft des Kantons Zürich (AGZ) Vereinigung Gesellschaft der Sanitätsoffiziere Autor: Dr. med. Christian Sommer Facharzt Orthopädische Chirurgie und Traumatologie des Bewegungsapparates FussClinic Haldenstrasse 6 6006 Luzern T +41 41 418 70 00 F +41 41 418 70 01 E-Mail Zur Online Visitenkarte www.fussclinic.ch Neuer zugelassener Arzt an der Klinik St. Anna für Hals-Nasen-OhrenKrankheiten Wir heissen Dr. med. Markus Reber als neuen zugelassenen Arzt an der Klinik St. Anna per 1. April 2015 herzlich willkommen. Er ist Facharzt für HNO-Krankheiten, Hals- und Gesichtschirurgie. Seine Kernkompetenzen sind: Nasen- und Nasennebenhöhlenchirurgie Konservative und operative Therapie von Schnarchen und Schlafapnoesyndrom Hals-Ultraschall und ultraschallgesteuerte Punktionen Das HNO Zentrum Affoltern am Albis liegt etwa auf halbem Weg zwischen Zürich und Luzern, direkt am Bahnhof und an der Autobahnausfahrt, daher ideal für Pendler zwischen der Zentralschweiz und Zürich gelegen. Diesen wird bei Bedarf Gelegenheit geboten, in Luzern an einer hervorragenden und bekannten Klinik operieren zu können. Dank der Belegarzttätigkeit vieler HNO-Ärzte an der Hirslanden Klinik St. Anna ist hier ein ausgezeichnetes Equipment und Know-how vorhanden. Berufliche Tätigkeiten während der letzten Jahre: Bis 2012 Hals-Nasen-Ohren-ärztliche Praxis in Luzern 2012 - 2013 Spital Zollikerberg Seit 2014 Hals-Nasen-Ohren-Praxis in Affoltern am Albis 2015 ab 1. April zugelassener Arzt an der Hirslanden Klinik St. Anna Zusätzliche Tätigkeiten Mitgliedschaften in folgenden Institutionen: Verbindung Schweizer Ärztinnen und Ärzte (FMH) Schweizerische Gesellschaft für Oto-Rhino-Laryngologie, Hals- und Gesichtschirurgie Gesellschaft der Zürcher Hals-Nasen-Ohren-Ärz Autor: Dr. med. Markus Reber Facharzt Hals-Nasen-Ohren-Krankheiten und Innere Medizin HNO Zentrum Affoltern am Albis Obstgartenstrasse 5 8910 Affoltern a. Albis T +41 44 763 14 14 F +41 44 763 14 15 E-Mail [email protected] Zur Online-Visitenkarte www.hno-aaa.ch ST. ANNA AKTUELL Baugesuch für zwei provisorische OPS-Säle Auf Grund der engen Platzverhältnisse und im Hinblick auf die Errichtung der Neubauten der Trakte A+ und E Hof sind im Innenhof provisorische Trakte mit zwei weiteren OPS-Sälen geplant. Das Baugesuch wird Ende Mai bei der Stadt Luzern eingereicht. Das Baugespann dazu kennzeichnet die Umrisse und wird ebenfalls Ende Mai errichtet. Ende Juli 2013 reichte die Klinik das Baugesuch für die Neubauten ein, das eine umfassende Modernisierung der wichtigsten Infrastruktur (Notfall, Operationssäle, Aufwachraum Radiologie und Zentralsterilisation) ermöglicht. Einsprachen verzögerten bis anhin den Baustart. Manetsch Meyer Architekten AG dipl. Architekten ETH SIA - Seebahnstrasse 85 8003 Zuürich +41 44 466 80 50 | Mai 2015 IN SERIE Bewegung als Therapiealternative bei Depression - Sollten wir nicht mit dem Patienten spazieren gehen? Obwohl die Depression zu den häufigsten Erkrankungen gehört und jeder fünfte Schweizer im Laufe des Lebens eine depressive Episode erlebt, ist die Behandlung in vielen Fällen unzureichend. Neben der Psychotherapie und der Pharmakotherapie spielen sogenannte Lifestyle-Interventionen, insbesondere die Anleitung zur körperlichen Aktivität, eine wichtige Rolle. Die Depression ist eine affektive Störung, welche durch gedrückte Stimmung und Verminderung von Antrieb und Aktivität gekennzeichnet ist. Laut Behandlungsempfehlungen der Schweizerischen Gesellschaft für Angst und Depression sollten die Behandlungsalternativen entsprechend der Schwere der Symptomatik, in Abhängigkeit vom Krankheitsverlauf und der Patientenpräferenz, gewählt werden. Dazu zählen eine aktiv-abwartende Begleitung („watchful waiting“) bei leichter Depression, Psycho- oder Pharmakotherapie bei Verschlechterung der Symptomatik und eine Kombinationstherapie bei der schweren Depression [1]. In der Schweiz leiden jährlich etwa 5,2 % der Bevölkerung an einer Depression, was geschätzte Kosten von 11 Milliarden Franken nach sich zieht [2]. Der Zusammenhang zwischen Bewegung und Stimmung zeigt sich schon in der Sprache – man „lässt den Kopf hängen“ oder „bewahrt Haltung“. Auch weisen immer mehr Daten darauf hin, dass sich durch körperliche Aktivität im Rahmen der Neuroplastizität positive Effekte im Gehirn entwickeln. Patienten mit depressiver Symptomatik zeigen häufig neben den psychischen Symptomen auch körperliche Beschwerden, die sich häufig gegenseitig verstärken und nicht klar voneinander trennen lassen. So führt die Depression häufig zu einer reduzierten körperlichen Aktivität, während andererseits Übergewicht und fehlende Aktivität das Risiko einer Depression verstärken [3]. Bewegung als therapeutische Alternative Die Anleitung zur sportlichen Aktivität bildet daher einen wichtigen Baustein in der Behandlung der Depression. Patienten mit Depression können durch Bewegungsangebote die Gefühle von Schwere und Antriebslosigkeit überwinden, ohne dass sie sich verbal damit auseinandersetzen müssen. Dabei verspüren sie schon allein durch die Überwindung und den Trainingseffekt Erfolgserlebnisse. Zusätzlich entwickeln die Kranken ein neues Körpergefühl, was zu einer besseren Wahrnehmung und zu neuem Vertrauen in sich selber führt. Wie bei anderen Therapieformen müssen die Patienten für die Mitarbeit gewonnen werden, wobei eine vertrauensvolle therapeutische Beziehung die wichtigste Rolle spielt. Der Arzt darf dabei die resignierte Haltung des Patienten nicht aufnehmen, sondern sollte sein Vertrauen in die Fähigkeiten des Patienten betonen und ihn beharrlich motivieren, bis sich durch Erfolgserlebnisse eine Eigenmotivation einstellt. Diese Erfolge lassen sich auch wissenschaftlich belegen: Ein kontrolliertes Training über mehrere Monate hatte einen vergleichbaren Effekt zu Psychopharmaka (SSRI) auf der Hamilton-DepressionsSkala HAM-D [4]. Ein Training von 12 Wochen kann den HAM-D um durchschnittlich 6 Punkte oder 47% senken, wobei 20% der Patienten mit leichter oder mittlerer Depression allein durch Training in Remission kamen. Dabei ist intensiveres Training wirksamer als solches mit niedriger Intensität [5]. Zusätzlich kann die Bewegung mit anderen Therapiemethoden kombiniert werden: So zeigte eine systematische Literaturanalyse einen signifikanten Vorteil der sportlichen Aktivität als Zusatz zu einer regulären Psycho- und Pharmakotherapie, sowohl auf die Schwere der Depression als auch auf die Zahl der Remissionen [6]. Ein Cochrane-Review zeigte allerdings nur für Krafttraining einen geringen Effekt auf die Fehltage bei der Arbeit, während Ausdauertraining keinen Vorteil gegenüber Entspannungsmethoden brachte [7]. Die Evidenz für die Wirksamkeit der körperlichen Aktivität ist dabei höher als für andere LebensstilInterventionen, wie beispielsweise Ernährung – insbesondere mediterrane Diät und Vollwert-Kost, Meditation, Haustiere oder Alkohol- und Tabakabstinenz [8]. Da viele Patienten mit Depression an einem metabolischen Syndrom leiden, kann sportliche Aktivität synergistische Effekte auslösen [9]. Neben dem positiven Effekt der körperlichen Aktivität selbst wirkt die Bewegung in der Gemeinschaft der oft vorhandenen Isolation entgegen. Viele Sportarten und Aktivitäten sind an Gruppen gebunden. Da Patienten mit Depression häufig ein reduziertes soziales Netz haben, kann die Sportgruppe oder der Verein eine geeignete Lösung bieten. Hinweise für die Praxis Patienten mit depressiver Symptomatik sollten in jedem Fall zu körperlicher Aktivität ermutigt werden, einerseits um der Depression selbst entgegenzuwirken, zum anderen zur Vermeidung von Komorbiditäten. In einer vertrauensvollen therapeutischen Beziehung sollte dabei gemeinsam mit dem Patienten eine individuell passende Art der Bewegung gesucht werden. Insbesondere für Hausärzte bietet sich die Anleitung zur Bewegung an, sowohl in Ergänzung zur Standardtherapie, aber auch als Alternative, wenn eine Pharmakotherapie abgelehnt wird. WEITERE INFORMATIONEN Buchtipp: John J. Ratey, Eric Hagerman: Superfaktor Bewegung: Das Beste für Ihr Gehirn! Auf http://brainsciencepodcast.com/bsp/111-exercise findet sich ein etwa 40 Min. langes Interview (auf Englisch) mit Prof. John J. Ratey über den Einfluss der Bewegung auf die Plastizität des Gehirns. Literaturhinweise: www.medline.ch/include_php/previewdoc.php?file_id=6831 Baer, N., Schuler, D., Füglister-Dousse, S. & Moreau-Gruet, F. (2013). Depressionen in der Schweiz. Daten zur Epidemiologie, Behandlung und sozial-beruflichen Integration (Obsan Bericht 56). Neuchâtel: Schweizerisches Gesundheitsobservatorium. Baer, N., Schuler, D., Füglister-Dousse, S. & Moreau-Gruet, F. (2013). Depressionen in der Schweiz. Daten zur Epidemiologie, Behandlung und sozial-beruflichen Integration (Obsan Bericht 56). Neuchâtel: Schweizerisches Gesundheitsobservatorium. Blumenthal et al. Effects of exercise training on older patients with major depression. Archives of internal medicine (1999) vol. 159 (19) pp. 2349–2356 Dunn et al. Exercise treatment for depression: efficacy and dose response. Am J Prev Med (2005) vol. 28 (1) pp. 1–8 Mura et al. Exercise as an add-on strategy for the treatment of major depressive disorder: a systematic review. CNS Spectr. (2014) vol. 19 (6) pp. 496–508 Nieuwenhuijsen et al. Interventions to improve return to work in depressed people. The Cochrane Library (2014) McIntyre et al. The Canadian Network for Mood and Anxiety Treatments (CANMAT) task force recommendations for the management of patients with mood disorders and comorbid metabolic disorders. Ann Clin Psychiatry (2012) vol. 24 (1) pp. 69–81 McIntyre et al. The Canadian Network for Mood and Anxiety Treatments (CANMAT) task force recommendations for the management of patients with mood disorders and comorbid metabolic disorders. Ann Clin Psychiatry (2012) vol. 24 (1) pp. 69–81 Autorin: Dr. med. Katarzyna Fischmann Fachärztin Psychiatrie und Psychotherapie Praxis Fischmann GmbH Zinggentorstrasse 1a1 6006 Luzern T +41 41 266 03 51 F +41 41 266 03 52 E-Mail Zur Online Visitenkarte www.praxis-fischmann.ch 13 FRAGEN AN ST. Anna Ärzte und Ärztinnen im persönlichen Gespräch: Seitenwechsel - Klinikmitarbeiter im persönlichen Gespräch 1. Manche Leute bezeichnen Patienten als Kunden. Wie sehen Sie das? Inwiefern ist für Sie der Patient Kunde? Der Pflegedienst ist ein Dienstleistungsbetrieb für verschiedene Kunden. Die Leistungen, die wir erbringen, sind immer im Sinne des Patienten, abgestimmt nach dessen individueller Situation. Patienten sind für mich aber Patienten, ich nenne sie nicht Kunden. 2. Was ist Ihr höchstes Ziel für den Patienten betreffend Pflege? Wie tragen Sie zum Wohl des Patienten bei? Mein höchstes Ziel ist es, wenn sich unsere Patienten gut versorgt, wohl und aufgehoben fühlen. Zentral für mich ist eine bestmögliche individuelle Pflegequalität durch kompetentes Pflegepersonal gewährleisten zu können. Wir bieten entsprechende Weiterbildung an, um diesem Anspruch gerecht zu werden. Ich leiste meinen Beitrag dazu, indem ich eine offene Feedbackkultur lebe, das Personal adäquat rekrutiere und die Personen für ihre Funktionen gezielt auswähle. 3. Sie sind letztlich verantwortlich, dass der Patient eine gute Pflege erhält. Was ist für Sie gute Pflege? Gute Pflege ist für mich individuelle Pflege, die nach dem Willen des Patienten ausgeführt wird. Also eine Pflege, die er braucht und wünscht. Wir Pflegefachpersonen kompensieren die Selbstpflegedefizite, sind Berater, Seelsorger, Zuhörer. 4. Wer noch ausser dem Patienten ist Kunde für Sie? Dies sind unsere Belegärzte, angestellten Ärzte und zuweisenden Ärzte, wie auch die Angehörigen und Besucher der Patienten, ebenso unsere Lieferanten. Aber auch die Öffentlichkeit hat im Sinne eines globalen Partners Kundencharakter. 5. Haben Sie auch Kontakt zu den zuweisenden Ärzten? Inwiefern und was ist Ihnen dabei wichtig? Ja teilweise, jedoch läuft dieser Kontakt primär über die Belegärzte und die Patientendisposition. Der direkte Kontakt erfolgt bei unseren Events für die Zuweiser, wie das Zuweiserfest oder das Patronatskonzert, bei Ärzte-Befragungen und über den Kontakt zu den Ärzten in der Geschäftsleitung. Es lohnt sich für die Zuweiser über diese Kontaktkanäle ihre Bedürfnisse und Wünsche zu äussern, auf die wir gerne eingehen und auf die wir angewiesen sind. Es ist uns wichtig eine möglichst gute Transparenz der Anliegen zu haben, insbesondere für die Patientenplanung. 6. Die Medizin wird immer teurer – welche Ausgaben nehmen im Bereich der Pflege zu, weshalb? Als Dienstleistungsbereich nehmen die Personalkosten in der Pflege einen grossen Anteil ein. Dieser Teil nimmt zu, da die Betreuung mit steigendem Alter der Patienten und häufiger Polymorbidität aufwändiger wird. Material und Medikamente werden immer besser und somit auch teurer. 7. Was sind die Herausforderungen in der Pflege für die Zukunft? Fachkräfte für eine adäquate Patientenbetreuung zu finden und zu behalten, ist die Herausforderung jetzt und in der Zukunft. Es besteht ein Dilemma zwischen Fachkräftemangel und Zunahme der Komplexität des Patientengutes. Viele Experten sind in der Behandlung eines Patienten involviert, das Gremium wird immer interdisziplinärer, weil die Behandlung immer spezialisierter wird. Somit sind mehrere Personen in der Betreuung involviert. 8. Weshalb haben Sie die Klinik St. Anna als Arbeitsort ausgewählt? Ich war schon als Lernende im Praktikum hier. Seit 2002 bin ich im St. Anna, aber immer mit wechselnden Funktionen. Angefangen habe ich als Dipl. Pflegefachfrau, dann war ich stellvertretende Stationsleiterin, dann Stationsleiterin und schliesslich wurde ich Bereichsleiterin. Die verschiedenen Funktionen habe ich immer mit berufsbegleitender Weiterbildung gekoppelt. Das St. Anna bietet mit den vielen interdisziplinären Stationen viel Lernpotential und ein grosses Lernfeld. Mir gefällt die Grösse der Institution, die ein familiäres Flair aufrechterhält und Mitbestimmung wie auch Umsetzung unserer Ziele zulässt. Mich beeindruckt die medizinische und pflegerische Kompetenz der Klinik St. Anna. 9. Weshalb haben Sie sich den Pflegeberuf ausgewählt und was ist Ihre Herausforderung als Pflegedirektorin? Den Beruf habe ich ausgewählt, weil ich Menschen, die Hilfe benötigen, unterstützen möchte, weil der Beruf viele soziale Kontakte mit sich bringt und weil mich Interaktionen mit Menschen interessieren. Zudem fand ich Anatomie und Physiologie des Körpers spannend. In der Rolle der Pflegedirektorin gefällt mir der Mix zwischen Managen, Planen und dennoch Kontakt zu den verschiedenen Kundengruppen zu haben. Einmal pro Monat arbeite ich für ca. einen Tag auf einer Station, um in der Praxis zu bleiben und die Probleme des Pflegealltags wahrzunehmen. 10. Wenn Sie selber Patient wären – würden Sie sich im St. Anna behandeln lassen? Ja, jederzeit. Wir haben sehr gute Ärzte, Fachpersonen und Infrastruktur. Als ich einmal selber als Notfallpatientin in Sportbekleidung eingeliefert wurde, erlebte ich – beinahe unerkannt – die Aufklärung, die Beratung, der Dienstleistungsgedanke, ja die ganze Philosophie unserer Klinik am eigenen Leib. 11. Work-Life-Balance ist ein viel gehörtes Schlagwort. Wie erreichen Sie Ihre Balance? Für mich ist Work ein wesentlicher Bestandteil von Life. Mein Job ist mein Traumberuf, viele meiner Bedürfnisse und Wünsche sind mit meinem Beruf erfüllt. Es gelingt mir immer gut nach einem Arbeitstag abzuschalten. Als Ausgleich treibe ich Sport oder bin mit Freunden und Familie zusammen. Zurzeit mache ich berufsbegleitend eine Ausbildung, für mich auch ein Ausgleich. 12. Das Jahresmotto vom St. Anna ist «Unsere Klinik – Ein Orchester». Welches Instrument spielen Sie? Je nach Situation z.B. die Pauke, auf die ich manchmal schlagen muss. Oder die Trompete, die mit dem Orchester mitspielt und ihre Rolle als Teil des Gesamten akzeptiert. Mir am nächsten kommt jedoch das Horn, welches auf Ordnung und Präzision bedacht ist. Mit seiner Liebe zum Detail arbeitet es eher im Hintergrund, plant und berechnet exakt seinen Einsatz im Voraus. 13. Welches Buch liegt auf Ihrem Nachttisch? Da ich zurzeit an meiner Masterarbeit schreibe, sind dies vor allem Fachbücher: Personalmanagement, Umgang mit Generation Y, HR-Strategie 2010. Mein Thema ist Magnetspital – welche Magnetwirkung und Marketingstrategien braucht es, um dem Fachkräftemangel entgegenzuwirken. Autor: Erika Rohrer Geschäftsleitungsmitglied, Pflegedirektorin Klinik St. Anna St. Anna-Strasse 32 6006 Luzern T +41 41 208 34 38 F +41 41 208 34 39 E-Mail