Prochiralität
Werbung
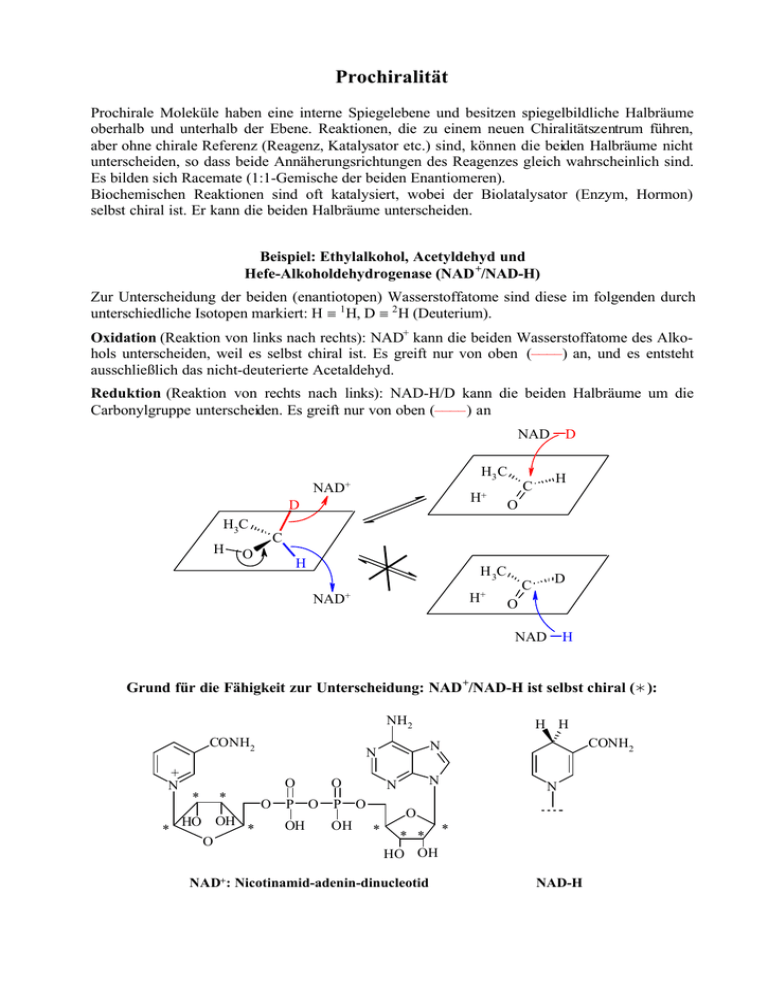
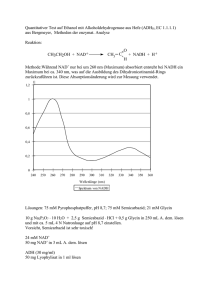
Prochiralität Prochirale Moleküle haben eine interne Spiegelebene und besitzen spiegelbildliche Halbräume oberhalb und unterhalb der Ebene. Reaktionen, die zu einem neuen Chiralitätszentrum führen, aber ohne chirale Referenz (Reagenz, Katalysator etc.) sind, können die beiden Halbräume nicht unterscheiden, so dass beide Annäherungsrichtungen des Reagenzes gleich wahrscheinlich sind. Es bilden sich Racemate (1:1-Gemische der beiden Enantiomeren). Biochemischen Reaktionen sind oft katalysiert, wobei der Biolatalysator (Enzym, Hormon) selbst chiral ist. Er kann die beiden Halbräume unterscheiden. Beispiel: Ethylalkohol, Acetyldehyd und Hefe-Alkoholdehydrogenase (NAD +/NAD-H) Zur Unterscheidung der beiden (enantiotopen) Wasserstoffatome sind diese im folgenden durch unterschiedliche Isotopen markiert: H ≡ 1 H, D ≡ 2 H (Deuterium). Oxidation (Reaktion von links nach rechts): NAD+ kann die beiden Wasserstoffatome des Alkohols unterscheiden, weil es selbst chiral ist. Es greift nur von oben (––––) an, und es entsteht ausschließlich das nicht-deuterierte Acetaldehyd. Reduktion (Reaktion von rechts nach links): NAD-H/D kann die beiden Halbräume um die Carbonylgruppe unterscheiden. Es greift nur von oben (––––) an NAD H3 C NAD+ H+ D H3C H D H C O C O H H 3C H+ NAD+ D C O NAD H Grund für die Fähigkeit zur Unterscheidung: NAD +/NAD-H ist selbst chiral (Ú ): NH2 CONH2 + N * HO OH * * O O P OH O O P OH N N O CONH2 N N O * H H N O * * * HO OH NAD+: Nicotinamid-adenin-dinucleotid * NAD-H