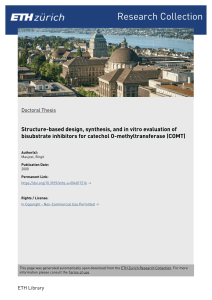
Opicapon
Werbung

Pharmazeutische Chemie - Opicapon Opicapon (Ongentys®) Levodopa, die direkte biogenetische Vorstufe des Dopamins, ist nach wie vor der Goldstandard in der Therapie des Morbus Parkinson. Die Catechol-O-MethylTransferase (COMT) ist neben der Dopa-Decarboxylase (DDC) das zweite Schlüsselenzym im Metabolismus des Levodopas. Durch eine COMT-Hemmung wird insbesondere die periphere Inaktivierung unterbunden und die Bioverfügbarkeit des Levodopas erhöht. Letztlich resultiert eine gesteigerte Levodopa-Aufnahme ins Gehirn. Die COMT-Hemmung durch entsprechende Inhibitoren hat sich zusätzlich zur DDC-Hemmung als effektive Maßnahme erwiesen, um die LevodopaKonzentration im Gehirn signifikant zu steigern (Männistö und Kaakkola 1999, Tai und Wu 2002, Bonifácio et al. 2007). Abbildung 1: der neue COMT-Hemmer Opicapon Opicapon (Ongentys®) ist nach Tolcapon und Entacapon endlich ein weiterer, neuer COMT-Inhibitor (Strukturformel s. Abbildung 1). Tolcapon (Tasmar®) war in 1997 der erste Vertreter dieser Arzneistoffklasse, wurde aber bereits 1998 wegen seiner Lebertoxizität teilweise sogar mit Todesfolge sowie anderer Organschädigungen wieder vom Markt genommen (nicht in den USA) (Assal et al. 1998). Mittlerweile ist Tolcapon aber wieder bei uns zugelassen, gilt aber wegen der Hepatotoxizität und der damit verbundenen regelmäßigen Leberwertkontrollen nur als Mittel der zweiten Wahl nach Entacapon (Fachinformation Tasmar® 2015). Ersetzt wurde Tolcapon durch das 1998 zugelassene und bereits erwähnte Entacapon (Comtess®), das als Zusatz für Parkinson-Kranke zugelassen ist, die mit Levodopa plus DopaDecarboxylase-Hemmer (DDCI) (Benserazid oder Carbidopa) allein nicht klar kommen (Fachinformation Comtess® 2015). Entacapon ist zusätzlich als FAM unter dem Namen Stalevo® auch in einer Fixkombination bestehend aus Levodopa, dem DDCI Carbidopa und eben Entacapon erhältlich (Strukturformeln Entacapon und Tolcapon s. Abbildung 2). Abbildung 2: die beiden bisher bekannten COMT-Hemmer mit Zulassung: Entacapon (Comtess®) seit 1998; Tolcapon (Tasmar®) Zulassung 1997, Marktrücknahme wegen lebensbedrohlicher Lebertoxizität 1998, mittlerweile wieder zugelassen. 1 CA 6.10.2016 Pharmazeutische Chemie - Opicapon Der neue COMT-Hemmer Opicapon besitzt ein ähnliches Anwendungsgebiet. Auch dieser darf nur als Zusatztherapie bei Parkinsonpatienten mit motorischen „End-ofdose“-Fluktuationen, die eine Kombination aus Levodopa und DDCI erhalten und bei denen mit dieser Zweier-Kombination keine Stabilisierung erreicht werden kann, eingesetzt werden. Ein deutlicher Nachteil des Entacapons ist, dass es sehr häufig eingenommen werden muss, bei jeder Levodopa/DDCI-Gabe bis hin zu einer Maximaldosis von zehnmal täglich einer 200mg-Filmtablette (Fachinformation Comtess® 2016). Die Ongentys®-Hartkapseln werden demgegenüber compliancefördernd nur einmal täglich vorzugsweise beim Zubettgehen mindestens eine Stunde vor oder nach der Levodopa-DDCI-Kombination eingenommen (Fachinformation Ongentys® 2016). Im Vergleich zur Einnahme ohne Mahlzeit, verringert die Einnahme zusammen mit einer fettreichen Mahlzeit die Bioverfügbarkeit signifikant (Almeida et al. 2013). Die Catechol-O-Methyl-Transferase kommt sowohl ubiquitär in der Peripherie als auch im Gehirn vor. Sie tritt in zwei Formen auf, in der Peripherie liegt vor allem die lösliche Form S-COMT vor, im Gehirn dagegen dominiert die membrangebundene Form MB-COMT. Die COMT ist ein Mg2+-abhängiges Enzym, das unspezifisch die Methylierung der 3‘-Hydroxyl-Gruppe des Catechol-Ringes und damit die Inaktivierung biologisch aktiver, aber auch potentiell toxischer Catechol-Derivate oder anderer hydroxylierter Substanzen katalysiert (s. Abbildung 3). Als Methyl-GruppenDonor und Kofaktor fungiert S-Adenosyl-Methionin, das durch den Methyl-Transfer zum S-Adenosyl-Homocystein wird. Substrate der COMT sind u.a. Levodopa, Catecholamine wie Dopamin, Noradrenalin und Adrenalin und ihre hydroxylierten Metaboliten sowie Ascorbinsäure (Männistö und Kaakkola 1999, Tai und Wu 2002, Bonifácio et al. 2007). Abbildung 3: die allgemeine COMT-Reaktion: Der COMT-katalysierte Transfer einer Methyl-Gruppe vom Kofaktor SAdenosyl-Methionin auf die 3‘-Hydroxyl-Gruppe eines Catechol-Substrates Für den Fall der Gabe einer Kombination bestehend aus Levodopa und einem DDCI ist für das Levodopa der Metabolisierungsweg über die Dopa-Decarboxylase zum Dopamin blockiert. Dadurch wird die COMT für das Levodopa zum wichtigsten metabolisierenden Enzym, das dessen Inaktivierung sowohl im Gehirn als auch in der Peripherie zum 3-O-Methyldopa katalysiert (s. Abbildung 4A) (Bonifácio et al. 2007, Fachinformation Ongentys® 2016). Anders als Tolcapon, das die Blut-HirnSchranke überwindet und die COMT sowohl in der Peripherie als auch im Gehirn hemmt, ist das neue Opicapon genauso wie Entacapon ein lediglich peripher wirksamer COMT-Hemmer, der nicht ins Gehirn vordringt. Allerdings erhöht Opicapon bei Patienten, die Levodopa zusammen mit den peripheren DDCI Carbidopa oder Benserazid einnehmen, signifikant die systemische Levodopa-Exposition um etwa das Doppelte bei gleichen cmax-Werten und die Levodopa-Exposition im dorsalen Striatum und der Substantia nigra um etwa das 1,4- bis 1,7-fache, reduziert gleichzeitig signifikant die Bildung des Levodopa2 CA 6.10.2016 Pharmazeutische Chemie - Opicapon Metaboliten 3-O-Methyldopa und führt zu einem verbesserten Ansprechen auf das Levodopa (s. Abbildung 4B) (Bonifácio et al. 2014 und 2015, Fabbri et al 2016, Fachinformation Ongentys® 2016, Scott 2016). Abbildung 4: A) Bei einer Levodopa/DDCI-Kombination wird der Dopa-Decarboxylase-Abbau des Levodopas gehemmt. Dadurch kann der Abbau über die COMT entscheidend werden und das in der Peripherie vorhandene Levodopa inaktivieren, so dass es kaum ins ZNS gelangt. B) Bei einer zusätzlichen Gabe eines peripheren COMT-Hemmers wie dem neuen Opicapon wird dann auch dieser Abbauweg blockiert, Levodopa wird nicht mehr vollständig peripher abgebaut und gelangt über die Blut-Hirn-Schranke ins ZNS. 3 CA 6.10.2016 Pharmazeutische Chemie - Opicapon Die beiden bekannten COMT-Hemmer Entacapon und Tolcapon sowie das neue Opicapon gehören strukturell zur selben Klasse innerhalb der vielen Substanzklassen, die als COMT-Hemmer bekannt sind. Es sind NitrocatecholDerivate, die ihren Ursprung Ende der 1980er Jahre haben, als zwei Gruppen bei Orion und Hoffman-La Roche unabhängig voneinander neue Serien disubstituierter Catechole entwickelten, die an der ortho-Position einer der beiden Hydroxyl-Gruppen eine elektronenziehende Gruppe besaßen (s Abbildung 5). Abbildung 5: Nitrocatechole als COMT-Hemmer 4 CA 6.10.2016 Pharmazeutische Chemie - Opicapon Einer der ersten Nitrocatechol-Inhibitoren der ersten Generation war 3,5Dinitrocatechol (OR-486), dessen inhibitorische Aktivität mit IC50 = 12nM zwei bis drei Zehnerpotenzen größer ist als die der bis dahin bekannten Pyrogallol- und CatecholInhibitoren (Bäckström et al. 1989, Bonifácio et al. 2007). Aus Struktur-WirkungsAnalysen weiß man, dass die ortho-ständige Nitro-Gruppe essentiell für eine große Inhibitor-Aktivität ist. Nachfolgende Entwicklungen konzentrierten sich dann auf den Austausch der zweiten, entfernter von den Hydroxyl-Gruppen positionierten Nitro-Gruppe, um vor allem die pharmakokinetischen Eigenschaften zu verbessern. Insbesondere Arylketone und Vinyl-Derivate rückten in den Focus (Bäckström et al. 1989, Borgulya et al. 1989). So entstanden die COMT-Inhibitoren der zweiten Generation. Das Arylketon Tolcapon sowie das Cyanovinyl-Derivat Entacapon gehören zu dieser zweiten Generation, die mit einer hohen Affinität (subnanomolare K i) vollständig reversibel an die COMT binden und keine Aktivität zu anderen Enzymen des Catecholamin-Metabolismus besitzen (Prous et al. 1994, Borguly et al. 1991, Lotta et al. 1995). Entacapon ist das reine E-Isomer (das Z-Isomer kann nur als aktiver Hauptmetabolit nachgewiesen werden) und ein ausschließlich peripher wirksamer COMT-Hemmer, der zwar eine große inhibitorische Aktivität besitzt, aber gekennzeichnet ist durch eine sehr kurze Wirkdauer, die sich in den sehr kurzen Dosirungsintervallen von bis zu zehnmal täglichen Gaben wiederspiegelt. Zudem werden für therapeutische Effekte sehr hohe Dosierungen nötig (bis zu 10 x 200mg) (Keranen et al. 1994). Die Effektivität und Wirksamkeit des Entacapons wurde mehrfach in Frage gestellt (Parashos et al. 2004). Im Gegensatz zum Entacapon ist das neuerdings wieder verfügbare, aber wegen seiner Hepatotoxizität hinter Entacapon nur als zweite Wahl anzusehende Tolcapon ein equipotenter Hemmer sowohl der peripheren S-COMT als auch der zentralen MB-COMT und besitzt zudem eine längere Wirkdauer als Entacapon. Lange Jahre war also Entacapon mit seiner kurzen Wirkdauer, seinen hohen Dosierungen insbesondere wegen der schlechten peroralen Bioverfügbarkeit der einzige in der Parkinson-Therapie einsetzbare COMT-Hemmer. Opicapon, ein hydrophiles und damit nur peripher wirksames Nitrocatechol der dritten Generation, ist keine Weiterentwicklung der Zweitgenerationen-Hemmer Entacapon und Tolcapon, sondern unabhängig davon entstanden. Untersuchungen zeigten, dass der Prototyp der Drittgenerationen-Hemmer, das unsubstituierte 1,2,4Oxadiazolylpyridin-N-oxid-Derivat eine dem Tolcapon vergleichbare Aktivität besitzt bei gleichzeitig verminderter Toxizität (Kiss et al. 2010). Intensive SARUntersuchungen wurden durchgeführt, um die gastrointestinale Absorption und die Dauer der COMT-Hemmung zu verbessern und das geringe toxische Potential dieser Substanzklasse beizubehalten. Es konnte gezeigt werden, dass Pyridin-N-OxidDerivate mit kleinen lipophilen Resten (wie beim Opicapon die Methyl-und ChlorSubstituenten) ein besseres inhibitorisches Profil aufweisen als die Inhibitoren der zweiten Generation (Kiss et al. 2010, Kiss und Soares-da Silva 2014). Opicapon besitzt eine sehr große Bindungsaffinität zur COMT. Der Opicapon-COMTKomplex besitzt eine Dissoziationskonstante im subpicomolaren Bereich (K d = 0,19pM) (Rocha et al. 2013). Daraus resultiert eine starke Bindung ans Enzym und eine sehr langsame Dissoziation vom Enzym, was zu einer deutlich verlängerten Wirkdauer gegenüber den Zweitgenerationen-Hemmern Entacapon und Tolcapon führt. Während für Entacapon die S-COMT-Aktivität (gemessen bei gesunden Erwachsenen) 8 Stunden nach Entacapon-Gabe wieder ihr ursprüngliches Niveau erreicht, dauert es beim Tolcapon schon 18 Stunden. Beim Opicapon dagegen 5 CA 6.10.2016 Pharmazeutische Chemie - Opicapon dauert die S-COMT-Hemmung länger als 24 Stunden an. 24 Stunden nach der letzten Opicapon-Applikation wird bei subtherapeutischen Dosierungen von 5 bis 30mg noch eine S-COMT-Hemmung von 42,8 bis 64,9% verzeichnet (Rocha et al. 2013). Bei einer therapeutischen Dosierung von 50mg pro Tag beträgt die S-COMTHemmung nach 24 Stunden immer noch über 90% und ermöglicht eine einmal täglich Gabe (Fachinformation Ongentys® 2016). Dementsprechend stellt der Drittgenerationen-COMT-Hemmer Opicapon mit einer einmal täglichen Applikation einen therapeutischen Fortschritt gegenüber den Zweitgenerationen-Hemmern Entacapon (Applikation bei jeder Levodopa-Gabe bis zu zehnmal täglich 200mg) und Tolcapon (Applikation dreimal täglich 100mg) dar - gerade wenn man an die Patientencompliance bei fortgeschrittenem Parkinson mit oftmals komplizierten und häufigen Arzneimitteleinnahmen und -zeitpunkten denkt. Die S-COMT-Hemmung durch Opicapon zeigt in vivo eine Halbwertszeit von etwa 100 Stunden und ist damit wesentlich länger als überhaupt Opicapon oder einer seiner Metaboliten im Plasma nachgewiesen werden können (Rocha et al. 2013). Durch die geringe Lipophilie des Opicapons, die schon ein Überwinden der Blut-HirnSchranke verhindert, scheint auch die gastrointestinale Resorption beeinträchtigt. Opicapon weist lediglich eine Resorptionsquote von ca. 20% auf. Allerdings wird es rasch resorbiert mit tmax-Werten von 1 bis 2,5 Stunden nach wiederholter Gabe. Die Eliminationshalbwertszeit des Opicapons liegt bei nur 0,7 bis 3,2 Stunden (Hauptmetabolit ist das inaktive Opicaponsulfat, weiterhin kommt es zu Methylierung (COMT!), Glucuronidierung und Reduktion) (Fachinformation Ongentys® 2016). Aufgrund der kurzen Halbwertszeit des Opicapons im Plasma, wonach es praktisch nach acht Stunden komplett metabolisiert ist, wird noch einmal klar, dass die lange Wirkdauer des Opicapons nicht das Resultat der langen Verweildauer im Kreislauf ist, sondern tatsächlich auf den extrem langsam dissoziierenden Opicapon-COMTKomplex mit einer Halbwertszeit von ca. 100 Stunden zurückzuführen ist (Rocha t al. 2013). Die katalytischen Eigenschaften sowie die Mechanismen der Hemmung der COMT sind ausführlich untersucht worden (z.B. Chen et al. 2005). Es existieren zudem einige Kristallstrukturen der COMT im Komplex mit Inhibitoren der ersten und zweiten Generation (Ma et al. 2013). Die 3-Nitrocatechol-Einheit ist über die drei Generationen der COMT-Hemmer unverändert geblieben und essentiell für eine inhibitorische Wirkung, da sie die Substratbindungsstelle besetzt und den Inhibitor dort quasi fest verankert. Die Nitrocatechol-Einheit ragt tief in das aktive Zentrum der COMT und wird über Wasserstoffbrückenbindungen zur Carboxyl-Gruppe der Glutaminsäure an Position 199 (Glu199) und zur Ɛ-Aminogruppe des Lysins an Position 144 (Lys144) fixiert (s. Abbildung 6). Zusätzlich wird der Phenyl-Ring des Catechol-Systems über π-πWechselwirkungen mit dem Indol-Ringsystem des Tryptophans an Position 38 (Trp38) gebunden. Dieses Tryptophan ist für eine hohe Bindungsaffinität der Catechole enorm wichtig, da z.B. schon eine einzelne Substitution des Tryptophans durch ein Arginin die Affinität der Catechole um das 10- bis 1000-fache reduziert. Das Mg2+-Ion wird über eine octahedrale Koordination im aktiven Zentrum fixiert. Koordinative Bindungen bestehen zu drei Aminosäuren (die Asparaginsäuren Asp141 und Asp169 sowie Asparagin Asn170) und einem Wassermolekül. Die zwei freien Koordinationsstellen werden durch die beiden Hydroxyl-Gruppen des Catechols besetzt (s. Abbildung 6). Somit sind nicht nur die betreffenden Aminosäuren sondern auch das Mg2+-Ion für die Verankerung des Catechols im aktiven Zentrum verantwortlich. Zusätzlich zur Fixierung des Substrates bzw. des 6 CA 6.10.2016 Pharmazeutische Chemie - Opicapon Inhibitors hat das Mg2+-Ion noch eine weitere Funktion, indem es den pK s-Wert der Lysin an Position 144 und des Catechols erniedrigt. Bei einem physiologischen pHWert von 7,4 wird die Ɛ-Aminogruppe des Lys144 deprotoniert vorliegen und als normale katalytische Base fungieren und somit das Proton der räumlich angrenzenden Catechol-3-Hydroxyl-Gruppe anziehen. Dieser Proton-Transfer von der Hydroxyl-Gruppe des Catechols zur Ɛ-NH2-Gruppe von Lys144 ist der erste Schritt innerhalb der enzymatischen O-Methylierung. Sobald die Hydroxyl-Gruppe deprotoniert ist, greift das neu gebildete nucleophile Hydroxylat-Anion des Catechols die elektrophile Methylsulfonium-Gruppe des Kofaktors S-Adenosylmethionin und der Methyltransfer schreitet über einen SN2-Übergangszustand voran (s. Abbildung 6) (Bonifácio et al. 2007). Abbildung 6: Die Opicapon-Methylierung an der 3‘-Hydroxyl-Gruppe des Catechol-Teils durch die COMT: Auch der eigentlich reversible COMT-Inhibitor Opicapon ist eigentlich ein Substrat der COMT und wird durch das Enzym methyliert. Was macht aber nun den Unterschied zwischen einem gewöhnlichen CatecholSubstrat und einem Catechol-Inhibitor im aktiven Zentrum der COMT aus? Es ist zum einen sicherlich die Stabilität der Bindung des Substrates bzw. Inhibitors im aktiven Zentrum der COMT. Auch beim Opicapon wird durch die COMT und deren Kofaktor S-Adenosylmethionin die 3-Hydroxyl-Gruppe des Catechol-Ringes methyliert. Allerdings schreitet diese Reaktion beim Opicapon sehr langsam voran, die Dissoziation des inaktiven O-methylierten Opicapons aus dem aktiven Zentrum der COMT ist nochmals viel langsamer, so dass das Enzym für eine lange Zeit quasi dauerhaft - blockiert ist. - Trotzdem bleibt festzuhalten: auch die NitrocatecholHemmer der COMT und auch das Opicapon sind nach wie vor Substrate der COMT, die genauso methyliert werden wie z.B. das Levodopa (s. Abbildung 6). - Nach Dissoziation des Produktes, also des methylierten Opicapons, liegt die COMT nicht in einem funktionsfähigen Zustand vor. Nach Transfer der Methyl-Gruppe muss der demethylierte Kofaktor, das S-Adenosylhomocystein durch einen neuen Kofaktor, das S-Adenosylmethionin ersetzt werden, bevor der katalytische Zyklus des Enzyms komplettiert ist. Dieser Austausch des Kofaktors dürfte relativ langsam ablaufen, da der Kofaktor tief im Enzym lokalisiert ist und eine umfangreiche dreidimensionale Konformationsänderung des Enzyms erforderlich ist. Es wird vermutet, dass solange noch zirkulierendes Opicapon vorhanden ist - dieses wieder viel schneller an das verbrauchte und noch nicht regenerierte Enzym bindet als der Austausch des 7 CA 6.10.2016 Pharmazeutische Chemie - Opicapon Kofaktors stattfindet. Ein solcher ternärer Opicapon-COMT-S-AdenosylhomocysteinKomplex wäre sehr stabil mit einer Dissoziations-Halbwertszeit von ca. 100 Stunden, wäre aber nicht mehr katalytisch aktiv und hätte die Fähigkeit verloren, Methylierungen durchzuführen (Bonifácio, et al 2012, Rocha et al. 2013). Abbildung 6: Ein Nitrocatechol (blau) gebunden im aktiven Zentrum der COMT (rot): Zunächst erfolgt ein Protontransfer von der zu methylierenden Hydroxal-Gruppe des Nitrocatechols zur Ɛ-Amino-Gruppe des Lsyins144, das deprotoniert vorliegt und somit als normale Base fungiert. Durch den Transfer des Protons auf die Amino-Gruppe resultiert ein nucleophiles Hydroxylat-Anion, das die räumlich benachbarte elektrophile Methylsulfonium-Gruppe des Kofaktors S-Adenosylmethionin (grün) angreift, wodurch nachfolgend der Methyltransfer über einen SN2-Übergangszustand abläuft. 8 CA 6.10.2016 Pharmazeutische Chemie - Opicapon Für die Nitrocatechole ist es auf molekularer Ebene sicherlich zunächst die zusätzliche Nitro-Gruppe am Catechol-Ring, die aus einem COMT-Substrat einen COMT-Inhibitor macht. Einerseits führt die Nitro-Gruppe natürlich, wie oben bereits erwähnt, durch eine H-Brücke zu einer zusätzlichen Fixierung des Inhibitors und erschwert damit die Dissoziation des Inhibitors vom aktiven Zentrum. Wichtiger aber scheinen die elektronischen Verhältnisse im Catechol-Ring des Inhibitors zu sein. Die elektronenziehende Nitro-Gruppe scheint vermutlich durch eine Delokalisierung der negativen Ladung des Hydroxylat-Anions dieses zu stabilisieren und den Methyltransfer zu verlangsamen. Beim Opicapon scheint zusätzlich der Oxadiazolpyridin-N-Oxid-Substituent die Reaktivität des HydroxylatAnions drastisch zu senken und zwar etwa in dem Maße wie es eine einfache weitere Nitro-Gruppe an dieser Position des Catechol-Ringes macht (Lotta et al. 1992, Bonifácio et al. 2007). Denkbar ist natürlich auch unter Einbeziehung des Oxydiazol-Ringes ein Tautomer des Opicapons, bei dem die Elektronendichte im Catechol-Ring noch einmal deutlich verringert ist aufgrund einer 1,4-Chinonmethidartigen Struktur des Catechol-Ringes und einer möglichen Konjugation der Doppelbindungen über alle drei Ringe (s. Abbildung 7). Abbildung 7: Opicapon (links) und sein mögliches Tautomer (rechts), bei dem die Elektronendichte im Catechol-Ring aufgrund der p-chinoiden Struktur stark reduziert ist. Zusätzlich zur elektronenziehenden Nitro-Gruppe im Catechol-Ring spielt natürlich auch die Seitenkette an Position 5 des Catechol-Ringes eine entscheidende Rolle für die inhibitorische Aktivität einer Substanz. Beim Entacapon wird die vinylische Seitenkette nur durch hydophobe Wechselwirkungen mit den sogenannten „gatekeeper“-Aminosäuren, den beiden Tryptophanen Trp38 und 143, dem Prolin Pro174 und dem Leucin Leu198, fixiert und der Catechol-Ring so in der richtigen Orientierung gehalten. Es scheint plausibel, dass beim Opicapon der Oxadiazolpyridin-N-oxid-Molekülteil deutlich stärkere (elektrostatische) Wechselwirkungen und Bindungen mit dem aktiven Zentrum (insbesondere auch durch den elektrischen Dipol im Molekül, das N-Oxid) eingehen kann. Literatur: Almeida, L. et al. Clin Pharmacokinet 2013, 52, 139 Assal, F. et al. Lancet 1998, 352, 958 Bäckström, R. et al. J Med Chem 1989, 32, 841 Bonifácio, M.J. et al. CNS Drug Rev 2007, 13, 352 9 CA 6.10.2016 Pharmazeutische Chemie - Opicapon Bonifácio, M.J. et al. Parkinsonism Relat Disord 2012, 18 (S2), S125 Bonifácio, M.J. et al. Neuropharmacology 2014, 77, 334 Bonifácio, M.J. et al. Br J Pharmacol 2015, 172, 1739 Borgulya, J. Helv Chim Acta 1989, 72, 952 Borgulya, J. et al. Drugs Future 1991, 16, 719 Chen, D. et al. Biochem Pharmacol 2005, 69, 1523 Fabbri, M. et al. Neurodegener Dis Manag 2016, 6, 349 Fachinformation Comtess® 2015, Orion Corporation Fachinformation Ongentys® 2016, Bial-Portela & Ca, S.A. Fachinformation Tasmar® 2015, Meda AB Keranen, T. et al. J Clin Pharmacol 1994, 46, 151 Kiss, L.E. et al. J Med Chem 2010, 53, 3396 Kiss, L.E. und Soares-da Silva, P. J Med Chem 2014, 57, 8692 Lotta, T. et al. Biochemistry 199534, 4202 Lotta, T. et al. J Comput Aided Mol Des 1992, 6, 253 Ma, Z. et al. Br J Clin Pharmacol 2013, 77, 410 Männistö, P.T. und Kaakkola, S. Pharmacol Rev 1999, 51, 593 Parashos, S.A. et al. Clin Neuropharmacol 2004, 27, 119 Prous, J. et al. Drugs Future 1994, 19, 641 Rocha, J.F. et al. Br J Clin Pharmacol 2013, 76, 763 Scott, L.J. Drugs 2016, 76, 1293 Tai, C.H. und Wu, R.M. Acta Med Okayama 2002, 56, 1 10 CA 6.10.2016