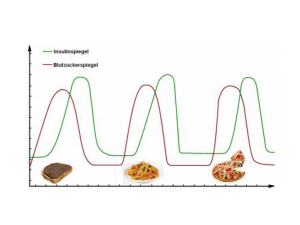
pdf-Datei - kantiriederer.ch
Werbung

EINE STUDIE ÜBER DEN EFFEKT VON SACCHAROSE UND KÜNSTL KÜNSTLICHEN ICHEN ZUCKERERSATZSTOFFEN AAUF UF DEN KÖRPER MATURAARBEIT VON SAMUEL WIELER BETREUT VON RAPHAEL RIEDERER KANTONSSCHULE ANTO SCHAFFHAUSEN 2015 ABSTRACT In dieser Maturaarbeit werden, wie der Titel bereits offenlegt, die Auswirkungen von künstlichen Süssungsmittel auf unseren Körper im Vergleich mit gewöhnlichem Haushaltszucker (Saccharose) untersucht. Der Schwerpunkt liegt vor allem auf Blutzucker, Insulin, Nahrungsaufnahme, Appetit und Sättigungsgefühl. Dafür wurden drei Testflüssigkeiten festgelegt, welche alle gleich süss sein sollten: eine Saccharose-Wasser Lösung, eine Aspartam-Wasser Lösung und ein Coca Cola Zero. So wurde der Zuckerersatz Aspartam einmal isoliert und einmal in einem Gemisch aus Zuckerersatzstoffen betrachtet. Schlussendlich gab es drei Testdurchläufe (jede Lösung wurde einmal getestet) an drei verschiedenen Tagen. Um den Blutzucker- und Insulinspiegel messen zu können, wurde jeweils vor und 20, 30, 60, 90, 120 Minuten nach Einnahme der zu testenden Lösung venös eine Ampulle Blut entnommen. Um den Appetit und das Sättigungsgefühl zu untersuchen, mussten mir die Probanden stündlich über Appetit und Sättigung berichten. Zusätzlich schrieben sich die Probanden auf, was sie den ganzen Tag assen, womit die Kalorienzufuhr berechnet werden konnte. Es galt herauszufinden, ob der Mensch auf ein Gemisch aus Zuckerersatzstoffen möglicherweise anders reagiert, als auf einen einzelnen Süssstoff, um somit das Gemisch als schädlicher oder weniger schädlich einzustufen. Des Weiteren stellte sich die Frage, ob der süsse Geschmack allein ausreicht, um die Insulinsekretion des Pankreas anzuregen oder ob ausschliesslich der Blutzuckerspiegel die Sekretion steuert. Insgesamt wurden sieben Probanden mit einem Durchschnittsalter von 29 ± 14 Jahren und einem durchschnittlichen Gewicht von 79 ± 19 kg untersucht. Darunter sind zwei weiblich. Die Probanden unterscheiden sich stark voneinander. Alter, Gewicht und Aktivitätsgrad sind von Proband zu Proband verschieden. Das zeigt sich auch darin, dass jedes Individuum anders auf die Testsubstanzen reagiert hat. Es konnte festgestellt werden, dass Aspartam in isolierter Form weder den Blutzuckerspiegel, noch die Insulinkonzentration beeinflusst. Das Gemisch im Coca Cola Zero hat jedoch einen seltsamen Effekt auf Blutzucker-und Insulinspiegel, welcher möglicherweise auf das Gemisch chemischer Substanzen im Coca Cola Zero zurückzuführen ist. Der Appetit vor dem Mittagessen ist im 2. und 3. Testdurchlauf grösser als nach Saccharose. Trotzdem essen die Probanden während des Untersuchungszeitraums gleichviel (Aspartam) bzw. weniger (Coca Cola Zero). Nach dem Mittagessen im 2. und 3. Durchlauf fühlen sich die Probanden trotzdem satter. Aber die Probanden kriegen im Verlauf des Nachmittages schneller wieder hunger bzw. Appetit und essen dadurch mehr Snacks zwischendurch. Meine Ergebnisse lassen vermuten, dass ein Gemisch aus künstlichen Süssungsmittel, in Verbindung mit weiteren chemischen Substanzen, andere, eher schädlichere Effekte auf unseren Körper hat, als ein Zuckerersatzstoff in isolierter Form. Inhalt 1 Motivation Einleitung ....................................................................................................................................... 7 1.1 Glucosekreislauf ..................................................................................................................... 7 1.1.1 Zellatmung ...................................................................................................................... 7 1.1.3 Glykogensynthese ......................................................................................................... 14 1.1.2 1.1.4 1.2 Lipogenese .................................................................................................................... 14 Insulin ................................................................................................................................... 16 1.2.1 Insulinproduktion .......................................................................................................... 16 1.2.3 Insulinrezeptor und Signalweiterleitung mittels Kinasen-Kaskaden ............................ 19 1.2.2 1.2.4 1.2.5 1.2.6 1.3 Insulinsekretion............................................................................................................. 18 Insulinwirkungen ........................................................................................................... 20 Fehlfunktionen und Krankheiten .................................................................................. 21 Gegenspieler ................................................................................................................. 23 Künstliche Zuckerersatzstoffe .............................................................................................. 24 1.3.1 Kategorisierung süssender Stoffe ................................................................................. 25 1.3.3 Effekt auf den Metabolismus ........................................................................................ 27 1.3.2 2 Cori-Zyklus..................................................................................................................... 10 Der süsse Geschmack.................................................................................................... 26 Material und Methoden .............................................................................................................. 28 2.1 Süsskraft der Testflüssigkeit ................................................................................................. 28 2.3 Nachweis von Insulin ............................................................................................................ 30 2.2 2.4 Appetit, Sättigung und Nahrungsaufnahme......................................................................... 28 Mercodia Insulin ELISA ......................................................................................................... 32 2.4.1 Testprinzip..................................................................................................................... 32 2.4.3 Grenzen des Verfahrens ............................................................................................... 33 2.4.2 2.4.4 2.4.5 Inhalt ............................................................................................................................. 33 Erwartete Werte ........................................................................................................... 34 Spezifität ....................................................................................................................... 34 3 2.4.6 Praktikumsbericht ......................................................................................................... 34 2.4.8 Berechnung der Resultate ............................................................................................ 37 2.4.7 3 Resultate ...................................................................................................................................... 38 3.1 Die Probanden ...................................................................................................................... 38 3.3 Das Verhalten der Insulinkonzentration .............................................................................. 40 3.2 3.4 3.5 4 3.6 Das Blutzuckergedächtnis..................................................................................................... 47 4.7 9 Das Sättigungsgefühl ............................................................................................................ 44 4.3 4.6 8 Der Appetit ........................................................................................................................... 42 Probanden ............................................................................................................................ 46 4.5 7 Nahrungszufuhr .................................................................................................................... 41 4.1 4.4 6 Das Verhalten des Blutzuckerspiegels .................................................................................. 38 Diskussion .................................................................................................................................... 46 4.2 5 Umrechnungsfaktor ...................................................................................................... 36 4.8 Homeostatic Model Assessment .......................................................................................... 46 Korrelation von Blutzucker-und Insulinkonzentration ......................................................... 48 Chi Quadrat Test ................................................................................................................... 49 Das Verhalten des Blutzuckerspiegels .................................................................................. 50 Das Verhalten der Insulinkonzentration .............................................................................. 55 Nahrungszufuhr, Appetit und Sättigung............................................................................... 58 Ausblick ........................................................................................................................................ 61 Dank ............................................................................................................................................. 61 Glossar ......................................................................................................................................... 62 Quellenverzeichnis ....................................................................................................................... 64 8.1 8.2 Literatur ................................................................................................................................ 64 Internet ................................................................................................................................. 64 Abbildungs-und Tabellenverzeichnis ........................................................................................... 64 9.1 Diagramme ........................................................................................................................... 64 9.3 Abbildungen ......................................................................................................................... 66 9.2 Tabellen ................................................................................................................................ 65 10 Anhang ......................................................................................................................................... 67 4 10.1 Rohdaten und Messwerte .................................................................................................... 67 10.1.1 Blutzucker [mmol/l] ...................................................................................................... 67 10.1.3 Nahrungszufuhr [kJ] ...................................................................................................... 70 10.1.2 Insulin [mU/l] ................................................................................................................ 68 5 MOTIVATION Mittlerweilen ist die Liste der künstlichen Zuckerersatzstoffe unüberschaubar geworden. Cyclamat, Xylit, Aspartam u.a. finden wir immer häufiger in allen möglichen Lebensmitteln und diese künstlich gesüssten Produkte sind beliebt. Der Mensch entwickelte in den letzten gut 70 Jahren ein enormes Ernährungsbewusstsein. Jeder will sich so gesund ernähren wie möglich, aber trotzdem nicht auf den süssen Geschmack verzichten. Mittlerweilen gibt es alle möglichen Süssgetränke in einer „Zero“ Version. Coca Cola Zero, Sprite Zero oder Fanta Zero. Diese Zero-Getränke scheinen die perfekte Lösung zu sein. Ein Getränk das dem Original geschmacklich extrem nahe ist, aber kein Zucker enthält. Jedes Mal, wenn ich einkaufen gehe, gibt es wieder ein neues kalorienarmes Produkt in den Regalen. Die Süssungsmittel machen es möglich. Dennoch sind viele Leute und auch die Wissenschaft misstrauisch. Viele Gerüchte über diese Süssstoffe machen die Runde. Sie regen den Appetit an. Manch einer behauptet sogar, sie seien krebserregend. Ich habe mich gefragt, was wirklich dahinter steckt und wollte mehr wissen. Wie kommt man auf das Ergebnis, dass diese künstlichen Süssstoffe krebserregend seine sollen? Verursachen sie wirklich einen grösseren Appetit und sind sie überhaupt gesund für unseren Körper? Man untersucht den Effekt von künstlichen Süssungsmittel häufig an Mäusen. Dabei gibt man den Mäusen so viel von diesen Zuckerersatzstoffen, dass sie förmlich darin ertrinken. Folglich erkranken die Tiere an einem Tumor. So viele künstliche Zuckerersatzstoffe kann ein Mensch kaum konsumieren. Soweit ich mich ins Thema eingelesen hatte, wurde der krebserregende Effekt an Menschen noch nie nachgewiesen. Dennoch ist diesen chemischen Substanzen nicht zu trauen. Sie werfen eine Menge Fragen auf. Ich wollte mehr wissen und widmete meine Maturaarbeit diesem Thema. 6 1 EINLEITUNG 1.1 Glucosekreislauf So wie ein Auto Diesel oder Benzin benötigt, um zu funktionieren, braucht der Mensch Energie in Form von Nahrung um zu überleben. Ein Grossteil der Nahrung besteht aus einer er Vielfalt von Kohlenhydraten, vorkommend als Einfach- oder Mehrfachzucker. zucker. Der bedeutendstes Energieträger ist Glucose C6H12O6 ein in Einfachzucker, am besten bekannt als Traubenzucker. Ohne Glucose kann unser Körper nicht funktionieren. Das beste Beispiel hierfür ist das Gehirn, welches ausschliesslich mit Energie in Form von Glucose versorgt werden kann. Im folgenden Kapitel möchte ich zeigen, welche zentrale ntrale Rolle Einfachzucker für unser Leben spielt, indem ich seine Funktionen und Verwendun Verwendungen etwas genauer und kritisch erläutere. H H C H C H H C C H C O OH OH OH OH OH C O H Strukturisomere von Glucose C6H12O6 1.1.1 Zellatmung Würde man sagen, dass die Verwendung von Glucose im Körper sehr mannigfaltig ist, so hätte man nur beschränkt recht. echt. Denn das, was eine so vielseitige Verwendung findet findet,, ist das Molekül ATP (Adenosintriphosphat). Es ist das Produkt der Zellatmung, gilt als die universelle Zellenergie und ist daher für den Menschen unverzichtbar. Sei es die Kontraktion der Muskeln oder gar die kleinste intrazelluläre re Bewegung auf dem Cytoskelett; ATP liefert die dafür nötige Energie, indem eine von drei Phosphatgruppen abgespalten wird wird. Dabei wird Energie frei, die der menschliche Körper gelernt hat zu nutzen. Die Produkte sind unte unten zu sehen. ATP ⇄ ADP + P + Energie Was hat das aber nun mit der Glucose zu tun? Die Antwort liegt in einem der zentralsten zen biochemischen Prozesse des Körpers: der Zellatmung. Sie ist in drei Schritte unterteilbar. 1.1.1.1 Glykolyse im Cytoplasma ytoplasma1 Durch Umformen und Anhängen nhängen von zwei Phosphatgruppen an Glucose O entsteht Fructose-1,6-Bisphosphat. phosphat. Hier wird Energie investiert. Nun folgt die Phase der Energiegewinnung. giegewinnung. Dieses energiereichere und instabilere C6Molekül zerfällt in zwei identische C3-Körper. Durch deren Oxidation entstehen schlussendlich zwei Mol Pyruvat (C3H4O3), wobei gleichzeitig NAD+ zu NADH + H+ reduziert wird. Diese Reduktion wird spä später noch von H3C COO - Strukturformel Pyruvat C3H4O3 grosser Bedeutung sein! 1 Prof. Dr. Jürgen Markl et. al. (Klett 2010), Klett Markl Biologie 1. Auflage, S. 108 7 Abbildung 1:: Die Glykolyse vereinfacht dargestellt. Ein schwarzer Punkt ist stellvertretend für ein Kohlenstoffatom. C6H12O6 + 2(ADP+P) P) + 2NAD+ → 2 C3H4O3 + 2(NADH+H 2(NADH +) + 2ATP 1.1.1.2 Citratzyklus in der Mitochondrienmatrix2 Bevor Pyruvat in den Citratzyklus geschleust wird, oxidiert es zu einem C2-Körper Körper (Acetylrest bzw. aktivierte Essigsäure), wobei ein Molekül CO2 abgetrennt und erneut NAD+ zu NADH + H+ reduziert wird Diesen Vorgang, welcher dem Citratzyklus noch vorausgeht, nennt man Pyruvatoxidation Pyruvatoxidation. Zeitgleich bindet der Acetylrest an das Coenzym A (CoA) und bildet das Molekül Acetyl-CoA, Acetyl das wohl wichtigste Zwischenprodukt im Zellstof Zellstoffwechsel der dreii Hauptnährstoffe Kohlenhydrate, Proteine und Fette. Verbunden mit CoA CoA, hat der Acetylrest eine besondere Bereitschaft, sich mit den Enzymkomplexen des Citratzyklus zu verbinden. Eingeschleust in den Citratzyklus Citratzyklus, trennt sich die aktivierte Essigsäure vom CoA und bindet an Oxalacetat (C4). Es entsteht Citrat (C6). In den nun folgenden zyklischen enzymatischen schen Reaktionen wird Citrat unter Abspaltung von zwei CO C 2- Molekülen zu Oxalacetat oxidiert oxidiert. Das heisst, der Acetylrest aus dem Acetyl-CoA CoA oxidiert zu zwei CO2-Molekülen. Oxidationsmittel ist das bereits bekannte Molekül NAD+ und zusätzlich FAD. Sie werden dabei zu NADH + H+ und nd FADH2 reduziert. Das Kohlenstoffgerüst der anfänglichen Glucose ist somit vollständig verarbeitet tet worden. 2 Pyruvat + 8 NAD+ + 2FAD + 2(ADP+P) 2 → 8(NADH+H+) + 2FADH2 +2ATP + 6CO2 Prof. Dr. Jürgen Markl et. al. (Klett 2010), Klett Markl Biologie 1. Auflage, S. 110 8 1.1.1.3 Atmungskette in der inneren Mitochondrienmembran3 In diesem letzten Schritt der Zellatmung wird mit Abstand am meisten Energie erzeugt. In den beiden vorherigen Schritten wurde immer wieder NAD+ zu NADH + H+ und FAD+ zu FADH2 reduziert. Die Elektronen, welche diese Reduktionsäquivalente aufgenommen haben, könne können an einen Proteinkomplex in der inneren Abbildung 2: Mitochindrium Mitochondrienmembran (1) abge gegeben werden. Insgesamt gibt es vier Arten von diesen Komplexen in der inneren Mitochondrienmembran, welche zusammen eine ne Elektronentransportkette bilden bilden.. Die Elektronen werden von Komplex zu Komplex weitergegeben. Dabei wirken die Elektronen wie eine Protonenpumpe. Denn jedes Mal, wenn ein Elektron einen solchen Komplex passi passiert, ert, gibt es Energie ab. Dadurch kann jedes Mal ein H+-Atom von der Mitochondrienmatrix (4) durch einen der vier Komplexe in den Intermembranraum Interme (3) transportiert werden.. So entsteht ein Ladungsunte Ladungsunterschied rschied zwischen der Matrix (4, ( negativ) und dem Intermembranraum (3, positiv). Der Ladungsausgleich geschieht ebenfalls wieder an einem tunnelartigen lartigen Protein in der Membran; der ATP-Synthase. Die H+-Ionen können die Membran durch diese Synthase passieren. Bei diesem Ladungsausgleich wird erneut Energie frei, welche den drehbaren Kopf der ATP-Synthase Synthase antreibt, womit die Energie auf ADP + P übertragen werden kann kann, und sie sich zu ATP verbinden. Zeitgleich steigt das Redoxpotential von Komplex zu Komplex, da das Elektron immer energieärmer wird. Hat es den vierten Komplex erreicht, kann das Elektron in die Matrix abgegeben werden, wo es an folgender Reaktion teilnimmt: 4H+ + O2 + 4e- → 2H2O Dadurch, dass die H+-Ionen immer an ein anderes Molekül gebunden werden,, wird eine Knallgasreaktion (Wasserstoff reagiert mit Sauerstoff), bei der sehr viel Energie auf einmal frei würde, verhindert. Erst ganz am Schluss wird diese Reaktion zugelassen. So lautet die gesamthafte Reaktion der Atmungskette wie folgt: 10(NADH + H+) + 2FADH2 + 6O2 + 34(ADP+P) → 10NAD+ + 2FAD + 34ATP + 12H2O Bei jedem dieser drei Schritte, hritte, die in sich sehr kompliziert sind, entsteht Energie, unter anderem in Form von ATP. Glucose hat jedoch seine Hauptrolle ganz am Anfang der Zellatmung, da sie Ausgangsstoff für die Glykolyse und somit für die gesamte Zellatmung ist. Ohne C6H12O6 läuft nicht einmal mehr die Glykolyse. Pyruvat, Endprodukt der Glykolyse und Ausgangsstoff für den Citratzyklus, ratzyklus, würde nicht mehr synthetisiert werden. Der Citratzyklus steht still, wodurch kein NAD+ und FAD+ reduziert werden kann. Die Atmung Atmungskette skette kann nicht mehr mit genügend Elektronen 3 Prof. Dr. Jürgen Markl et. al. (Klett 2010), Klett Markl Biologie 1. Auflage, S. 111 9 versorgt werden, was zur Folge hat, dass kein ATP mehr aufgebaut werden kann. Die gesamte Zellatmung und die damit verbundene Energiegewinnung käme zum Erliegen und das bloss, weil ein Molekül fehlt: Glucose. 1.1.1.4 Gesamtreaktion Zellatmung C6H12O6 + 6O2 + 38 (ADP +P) → 6H2O + 6CO2 + 38ATP Aus einem Mol Glucose entstehen also 38 Mol Adenosintriphosphat. 1.1.2 Cori-Zyklus4 Der Cori-Zyklus beschreibt im Grunde den Glucose-Lactat Kreislauf zwischen der Skelettmuskulatur und der Leber. Auch für die Skelettmuskulatur ist Glucose der bevorzugte Brennstoff. Anders als in der Zellatmung können die Reaktionen in den Skelettmuskeln unter anaeroben Bedingungen (Sauerstoffmangel) ablaufen. Die anaerobe Glykolyse unterscheidet sich kaum von jener in der Zellatmung. Aber das unter diesen anaeroben Bedingungen anfallende Pyruvat in den Skelettmuskeln kann nicht in den Citratzyklus eingeschleust werden, da kein NAD+ und FAD mehr vorhanden ist, sondern muss zu Lactat (Milchsäure) reduziert werden. Diesen Vorgang nennt man Milchsäuregärung. Wir alle kennen das Gefühl, wenn unsere Muskeln vor lauter Anstrengung zu schmerzen beginnen und brennen. Das ist auf das Lactat zurückzuführen, das in den Muskeln anfällt. Dieses Lactat muss also abtransportiert werden. Es gelangt über das Blut in die Leber, wo mittels Gluconeogenese wieder ursprüngliche Glucose erzeugt werden kann. 1.1.2.1 Anaerober Abbau von Pyruvat Wenn wir uns körperlich verausgaben, brauchen wir mehr Energie, als wenn wir nur gemütlich auf einem Stuhl sitzen. Wir benötigen also mehr ATP als im Ruhezustand. Die Zellatmung muss mehr Energie (ATP) produzieren. Dies ist aber nur möglich, wenn genügend Sauerstoff im Körper vorhanden ist. Denn die Elektronen aus der Atmungskette müssen zum Schluss auf folgende, bereits bekannte Reaktion übertragen werden, damit eine Knallgasreaktion verhindert werden kann: 4H+ + O2 + 4e- → 2H2O Florian Horn et. al. (Thieme 2012), Biochemie des Menschen: Das Lehrbuch für das Medizinstudium 5. Auflage, S. 94-96, S. 101-106 4 10 Als Konsequenz daraus atmen wir viel stärker, um weiterhin genug ATP produzieren zu können. Aber was geschieht nun, wenn wir zu wenig Sauerstoff bereitstellen können? Weil die Elektronen aus der Atmungskette nicht mehr auf den Sauerstoff übertragen werden können, wird die ATP-Synthase nicht mehr angetrieben, wodurch die ATP-Synthese zum Erliegen kommt. Unmittelbar vor der Atmungskette kann weder NADH + H+ noch FADH2 seine Elektronen an die Membranproteine der inneren Mitochondrienmembran abgeben. Es liegen also immer mehr NADH + H+ und FADH2 in reduzierter Form vor und die Menge an NAD+ und FAD+ nimmt stetig ab. Somit fehlen die nötigen Oxidationsmittel für den Citratzyklus und die Glykolyse, wodurch diese enorm wichtigen Reaktionen stark beeinträchtigt werden. Für den Fall, dass die Zellatmung nicht mehr genügend Energie liefern kann, hat der Körper bzw. die Muskeln noch eine Alternativmethode, eine Art Notfallplan, um Energie zu produzieren: die Milchsäuregärung. Sie erlaubt dem Körper, auch ohne Sauerstoff ATP zu synthetisieren. Trotz des Sauerstoffmangels kann die Glykolyse wie gewohnt ablaufen. Es entstehen ATP und Pyruvat. Aufgrund des Sauerstoffmangels und den oben aufgezählten Gründen wird das Pyruvat nicht in den Citratzyklus eingeschleust sondern zu Lactat reduziert. Dabei dient NADH + H+ als Reduktionsmittel und oxidiert zu NAD+. ATP entsteht hier nur dank der Glykolyse. Durch die eigentliche Milchsäuregärung ,das heisst, wenn Pyruvat wird zu Lactat reduziert wird, entsteht Energie in Form von NAD+. Die Gärung hat im Gegensatz zur Zellatmung einige Nachteile. Zum einen ist die Gärung ineffizienter. Damit gleich viel ATP entsteht wie bei der Zellatmung braucht es 19-mal mehr Glucose. Zum anderen muss das anfallende Lactat schnellst möglich aus den Muskeln abtransportiert werden, da es sonst zu einer Übersäuerung der Muskeln kommt und wir derart Schmerzen empfinden, dass wir unsere Aktivität abbrechen müssen. Der Mensch ist jedoch nicht in der Lage, dauerhaft auf diese Weise ATP zu generieren. Denn unter hoher und längerer Belastung wie beispielsweise bei einem 100 Meter Sprint kann das anfallende Lactat nicht genügend schnell abtransportiert werden. H3C OH O H O - Strukturformel Pyruvat C3H4O3 11 Abbildung 3: Glykolyse und Milchsäuregärung 12 1.1.2.2 Gluconeogenese5 Das bei der Milchsäuregärung entstehende Lactat gelangt über die Blutbahn in die Leber. Was nun folgt, zeigt ein weiteres Mal, wie wichtig die Glucose für den Menschen ist. Die Gluconeogenese (gr. neo = neu, genesis = Erzeugung) ist die endogene Biosynthese von Glucose aus Nicht-Zuckern – Lactat, Aminosäuren und Glycerin – und findet vor or allem im Zytosol statt. Man könnte sie als eine Umkehrung der Glykolyse beschreiben. Denn die Nicht Nicht-Zucker Zucker werden immer zuerst in Pyruvat umgewandelt (Glycerin und einige Aminosäuren müssen nicht in Pyruvat umgewandelt werden, sondern in andere Zwischen Zwischenprodukte produkte der Gluconeogenese, wie beispielsweise Oxalacetat). Dann folgt eine Reihe von Reaktionen, an denen viele Enzyme beteiligt sind und am Schluss der Gluconeogenese liegt wieder Gluc Glucose ose vor. Die Glucose gelangt ins Blut, damit der Körper mit ausreichend nd Energie versorgt werden kann. Anders als die Glykolyse ist die Gluconeogenese eine endogene Reaktion. Es wird also Energie gebraucht und nicht produziert. Die Gluconeogenese ist demnach keine exakte Umkehrung der Glykolyse. Die meisten Reaktionen der G Glykolyse lykolyse sind zwar reversibel, die drei Schlüsselreaktionen, Schlüsselreaktionen bei welchen in der Glykolyse Energie entsteht, sind jedoch irreversibel und müssen durch energieaufwendige Alternativen ersetzt werden werden.. Diese drei Schritte bilden dann auch in der Gluconeogenese die Schlüsselreaktionen. Abbildung 4:: Drei verschiedene Einstiegsmöglichkeiten für die Gluconeogenese 5 Florian Horn et. al. (Thieme 2012), Biochemie des Menschen Menschen: Das Lehrbuch für das Medizinstudium edizinstudium 5. Auflage, S. 94-96, S. 101-106 5 13 1.1.3 Glykogensynthese Das Glykogen dient unserem Organism Organismus als Speicher für Glucose, welcher schnell mobilisiert werden kann. Anders als bei den Pflanzen, die ihre Energie in Form von Stärke speichern, dient bei uns Menschen das Glykogen als Speicher. Der menschliche Körper ist in der Lage, 400 g Glucose zu speichern. Da Glucose aber osmotisch ak aktiv tiv ist (zieht Wasser in die Zelle), wird es in Form von Glykogen gespeichert. Da es sich in Wasser nicht löst, ist dieses Molekül osmotisch nicht aktiv. aktiv Glykogen ist ein verzweigtes Polysaccharid (Vielfachzucker), das aus Glucose Glucose-Einheiten Einheiten aufgebaut ist, die aneinander gehängt wurden. Auch in der Glykogensynthese wird die Glucose wie in der Glykolyse zuerst phosphoryliert, damit sie in einen angeregten Zustand kommt, in welchem sie schneller und besser reagiert. rt. Die Glykogen Glykogen-Synthase Synthase (Verzweigungsenzym) hängt hä die einzelnen Glucosemoleküle aneinander. Umgekehrt gibt es natürlich auch das Entzweigungsenzym, das di die Glucosemoleküle wieder voneinander trennt. Sind die Verzweigungen aufgehoben, ist die Glucose wieder im ursprünglichen Zustand und gelangt in die Blutbahn. Die beiden Enzyme werden unter anderem von drei sehr speziellen und zentralen Hormone Hormonen beeinflusst, auf die ich bald zu sprechen komme: Insulin, Adrenalin und Glucagon. Abbildung 5: Das Polysaccharid Glykogen 1.1.4 Lipogenese6 Die Lipogenese beschreibt den Vorgang der Fettproduktion. Dabei werden dr drei ei Fettsäuren mit einem Glycerol verknüpft. Es entsteht ein Triacylglycerin (TAG). TAG’s sind genau wie Glykogen Energiespeicher. TAG‘s haben jedoch eine viel höhere Energ Energiedichte iedichte und machen bei Normalgewichtigen 12% des Körpergewichtes aus. Die Fettdepots reichen aus, um einige Wochen über die Runden zu kommen, wobei die Glykogenspeicher nach 24 Stunden leer sind. Was aber hat die Glucose mit der Fettproduktion zu tun? Der Fettaufbau im Fettgewebe kann aus zwei Gründen nur ablaufen, wenn genügend Glucose im Körper ist: Florian Horn et. al. (Thieme 2012), Biochemie des Menschen Menschen:: Das Lehrbuch für das Medizinstudium 5. Auflage, S. 141-146 & https://de.wikibooks.org/wiki/Biochemie_und_Pathobiochemie:_Triacylglycerinbiosynthe https://de.wikibooks.org/wiki/Biochemie_und_Pathobiochemie:_Triacylglycerinbiosynthese se 6 14 1. Es braucht Insulin, damit die Glucose in die Fettzellen aufgenommen werden kann. 2. Es wird ein Zwischenprodukt (Glyceron (Glyceron-3-Phosphat) Phosphat) der Glykolyse benötigt. Ohne Glucose läuft die Lipogenese also nicht ab. Glyceron Glyceron-3-Phosphat Phosphat wird zu Glycerin-3-Phosphat Glycerin reduziert und kann dann in weiteren Schritten mit drei Fettsäuren verknüpft werden. Di Die Glucose hat also im Fettstoffwechsel eine grosse Bedeutung. Betrachtet man das Glucosemolekül, dann würde man nicht vermuten, dass einmal ein TGA daraus entsteht. Abbildung 6:: Ein Triacylglycerin aus einem Glycerinkopf und drei Fettsäuren 15 1.2 Insulin Wenn wir essen, dann werden bereits im Mund die Kohlenhydrate (Mehrfachzucker, wie zum Beispiel Stärke aus den Kartoffeln) ein Stück weit verdaut. Durch das Verdauungsenzym α-Amylase, das sich im Speichel befindet, werden die Kohlenhydrate gespalten. Das kann man sehr schön feststellen, wenn man Brot etwas länger kaut. Mit der Zeit beginnt es, süss zu schmecken. Das liegt an der Spaltung der Kohlenhydrate durch α-Amylase in Maltose, ein Disaccharid (Zweifachzucker). Der Grossteil der Kohlenhydrate wird im Verdauungstrakt zu Glucose verdaut. Die Glucosemoleküle können aus dem Verdauungstrakt diffundieren und gelangen so ins Blut. Vorläufig geschieht nichts geringeres, als dass sich die Konzentration von Glucose im Blut erhöht. Mit anderen Worten: Der Blutzuckerspiegel steigt an. Solange sich die Glucose-Moleküle im Blut befindet, nützen sie uns nicht viel, denn der Energiegewinnungsprozess läuft in den Zellen ab. Hier kommt Insulin ins Spiel. Eines der absolut wichtigsten Hormone in unserem Körper und das einzige, welches den Blutzucker senken kann. Insulin (vom lateinischen „insula“, was Insel bedeutet) hat seinen Namen von seinem Ursprung. Es wird im endokrinen Teil der Bauchspeicheldrüse, in den β-Zellen der Langerhansschen Inseln, produziert. Das Peptidhormon besteht aus einer A-Kette aus 21 Aminosäuren und einer B-Kette aus 30 Aminosäuren. Die Ketten halten durch zwei Disulfidbrücken zusammen. Eine dritte Disulfidbrücke innerhalb der A-Kette stabilisiert das Molekül. Insulin sorgt dafür, dass die Glucose in die Zelle aufgenommen werden kann und unterbricht gleichzeitig glucoseliefernde Prozesse im Körper, indem es deren Enzyme hemmt. Was alles geschehen muss, bis die Glucose schlussendlich in der Zelle für die Energiegewinnung bereit steht, werde ich in folgendem Kapitel erläutern. 1.2.1 Insulinproduktion7 Die Biosynthese von Insulin im Zellinnern verläuft, wie bei allen Eiweissen, nach den Grundsätzen der Genexpression. Zuerst wird das Insulingen im Zellkern in eine mRNA transkribiert und gespleisst. Diese messenger-RNA wird an den Ribosomen ins Prä-Proinsulin translatiert. Danach werden überflüssige Stellen vom Prä-Proinsulin entfernt und durch die charakteristische Faltung der Aminosäurenkette können die Disulfidbrücken gebildet werden. So entsteht das Proinsulin. Es unterscheidet sich noch vom Insulinhormon, da eine dritte Aminosäurensequenz, das C-Peptid aus 35 Aminosäuren, die A-Kette und die B-Kette miteinander verbindet. Der letzte Schritt der Synthese findet im Golgi-Apparat statt. Hier wird enzymatisch das C-Peptid vom Proinsulin abgespalten. Das „reife“ Insulinhormon sowie das C-Peptid werden vom Golgi-Apparat in Sekretgranula (Vesikel, die Speicher-und Sekretstoffe enthalten) verpackt. Auch wenn das C-Peptid keine physiologische Wirkung hat, wird es nicht abgebaut, sondern in äquimolarem Verhältnis zusammen mit dem Insulin in den Blutkreislauf sekretiert. Diese Tatsache macht man sich zu Nutze, da man so indirekt Gertrud Rehner et. al. (Spektrum Akademischer Verlag, 2010), Biochemie der Ernährung 3. Auflage, S. 141-144 & Florian Horn et. al. (Thieme 2012), Biochemie des Menschen: Das Lehrbuch für das Medizinstudium 5. Auflage, S. 350-351 7 16 die Menge Insulin im Blut bestimmen kann, die vom Pankreas sezerniert wurde. Auch bei Diabetikern, die mit exogenem Insulin nachhelfen müssen, kann anhand der C-Peptid Konzentration bestimmt werden, wie viel Insulin vom eigenen Körper noch produziert und sezerniert wird. Biosynthese des Insulins: 1. 2. 3. 4. Transkription des Insulingens (DNA) in eine mRNA Translation der mRNA in eine Aminosäurensequenz → Prä-Proinsulin Faltung und Bildung der Disulfidbrücken → Proinsulin Entfernung des C-Peptids → Insulin Abbildung 7: Biosynthese des Insulins 17 1.2.2 Insulinsekretion8 Interessant wird es, wenn man sich die Frage stellt, welches die Bedingungen für eine Insulinausschüttung sind. Es ist dies nämlich eine Erhöhung des Blutzuckerspiegels. Die Sekretion beginnt bei einer Blutzuckerkonzentration von 2-3 mmol/l und nimmt bis zu einer Konzentration von 15 mmol/l zu. Untersuchungen der letzten Jahre lassen stark vermuten, dass die Erhöhung der Blutglucosekonzentration ein intrazelluläres Signal in den β- Zellen auslöst. Dieses Signal ermöglicht Abbildung 8: Auslösen der Insulinsekretion durch Glucose schlussendlich die Verschmelzung der Sekretgranula mit der Zellmembran der β-Zellen, wodurch deren Inhalt (Insulin und C-Peptid) per Exocytose in das Blut abgegeben werden. Man geht davon aus, dass die β-Zellen eine Art Glucosesensor in Form eines Glucose-Transporters (GLUT 2) besitzt. Dieses Transportprotein in der Zellmembran befördert die Glucose, proportional zu deren Konzentration, ins Zellinnere. Der erste Schritt, der die intrazelluläre Metabolisierung der Glucose einleitet, ist eine Phosphorylierung der Glucose. Auch die Phosphorylierung (mittels des Enzyms Glucokinase) geschieht proportional zur Glucosekonzentration. Nach der Phosphorylierung im Zellinnern durchläuft die Glucose den üblichen Prozesse der Energiegewinnung (Kapitel 1.1.1). Je nach Glucoseangebot entsteht so mehr oder minder viel ATP. Je höher der Glucoseeintritt in die Zelle, desto grösser die ATP-Konzentration im Zellinnern. Diese erhöhte ATP-Menge hat zur Folge, dass ATP-sensitive Kalium-Kanäle inhibitiert werden. Der K+-Ausstrom wird somit gestoppt und die Membran wird depolarisiert. Durch das veränderte Membranpotenzial öffnen sich spannungsgesteuerte Calcium-Kanäle, die einen Ca2+-Einstrom ermöglichen. Eine der spezifischen Zellantworten auf eine Erhöhung der intrazellulären Ca2+-Konzentration ist das Auslösen der Exocytose. Die insulin- und C-Peptid-haltigen Sekretgranula verschmelzen mit der Zellmembran der β-Zellen und geben ihren Inhalt in den extrazellulären Raum ab. 8 Gertrud Rehner et. al. (Spektrum Akademischer Verlag, 2010), Biochemie der Ernährung 3. Auflage, S. 144-146 18 Zusammengefasst ergibt das folgenden Ablauf: 1. 2. 3. 4. 5. 6. 7. Glucosetransport ins Zellinnere durch GLUT 2 Phosphorylierung der Glucosemoleküle ATP-Produktion Inhibition der K+-Kanäle durch steigende ATP-Konzentration. K+-Ausstrom wird gestoppt. Depolarisation der Membran Spannungsgesteuerte Ca2+-Kanäle werden aktiviert. Ca2+-Einstrom. Durch Calcium-Ionen wird die Excytose ausgelöst. Die Sekretgranula verschmelzen mit der Plasmamembran. 8. Insulin und C-Peptid gelangen in die Blutbahn. 1.2.3 Insulinrezeptor und Signalweiterleitung mittels Kinasen-Kaskaden9 Das Peptidhormon Insulin hat ein sehr breites Wirkungsspektrum. Die Wirkungen sind organspezifisch. Je nach Zelle, löst Insulin ein anderes Signal aus, was schlussendlich zu vielen verschiedenen Wirkungen führt. Auch in ihrer Dauer unterscheiden sie sich. Manche haben den Umfang einiger Sekunden oder Minuten, während andere Wirkungen mehrere Stunden andauern können. Trotz des breiten Wirkungsspektrums löst Insulin, durch das Andocken an den Insulinrezeptor, im Zellinnern immer dieselbe Reaktion aus. Im Folgenden wird diese Reaktion genauer erläutert. Der Insulinrezeptor ist ein Typ-1-Rezeptor. Wie alle Typ-1-Rezeptoren besteht auch der Insulinrezeptor aus zwei identischen α-Untereinheiten, die sich vollständig im Extrazellulärraum befinden und zwei ebenfalls identischen β-Untereinheiten, die sich durch die Membran hindurch bis ins Zellinnere erstrecken. Typisch für einen Typ-1-Rezeptor ist auch die Signalweiterleitung im Zellinnern, welche über eine Tyrosinkinase-Aktivität verläuft. An die β-Untereinheiten sind Tyrosinkinasen angehängt. Tyrosin ist eine Aminosäure. Kinasen sind nichts Geringeres als Enzyme, die Phosphatgruppen transportieren und auf andere Proteine übertragen können. Durch das Anhängen einer Phosphatgruppe an ein Protein wird dessen Wirkung und Funktion stark verändert. Auf diesem Grundsatz pflanzen sich beinahe alle Signale im Zellinnern fort. Wenn nun Insulin an die α-Untereinheiten bindet, dann wird das an die β-Untereinheiten weitergeleitet, TyrosinKinase Abbildung 9: Insulinrezeptor und Signalweiterleitung Gertrud Rehner et. al. (Spektrum Akademischer Verlag, 2010), Biochemie der Ernährung 3. Auflage, S. 146-149,S. 28-29 & Florian Horn et. al. (Thieme 2012), Biochemie des Menschen: Das Lehrbuch für das Medizinstudium 5. Auflage, S. 339-340, S. 352-353, 9 19 worauf sich diese verformen. Durch diese Verformung beginnen die Tyrosinkinasen, ihre eigenen Tyrosinreste zu phosphorylieren. Das nennt sich Autophosphorylierung. Die phosphorylierten Tyrosinreste sind nun in der Lage ein zelluläres Signalproteine zu phosphorylieren. Im Fall des Insulinrezeptors ist dies das Insulin-Rezeptor-Substrat-1 (IRS-1). Das IRS-1 in phosphorylierter Form kann nun alle möglichen Enzyme und Substrate phosphorylieren. Je nach phosphoryliertem Enzym bzw. Substrat hat das einen völlig anderen Effekt. Insulinwirkung: 1. Insulin dockt an die α-Untereinheit des Insulinrezeptors. Dadurch verformen sich die βUntereinheiten innerhalb der Zelle. 2. Autophosphorylierung. Die Tyrosinkinasen phosphorylieren ihre eigenen Tyrosinreste. 3. Zelluläres Signalprotein (IRS-1) wird an den Tyrosinkinasen phosphoryliert. 4. Es folgen Kinasen-Kaskaden, die je nach Enzym und Substrat verschiedenste Wirkungen haben können. Unter einer Kinasen-Kaskade versteht man eine Folge von Phosphorylierungen. Die Phosphatgruppe wird in der Zelle von Enzym zu Enzym weitergegeben. 1.2.4 Insulinwirkungen10 Die Grundlage für alle Insulinwirkungen ist die Aktivierung bzw. Hemmung von Enzymen durch Kinasen-Kaskaden. Der Ursprung ist immer die Autophosphorylierung der Tyrosinkinasen des Insulinrezeptors. Von hier aus können alle möglichen Enzyme phosphoryliert werden. Folglich sind die wichtigsten Beispiele aufgelistet: GLUT 4 Wie bereits erwähnt, senkt Insulin den Blutzuckerspiegel. Dies erreicht das Hormon, indem es die Glucoseaufnahme der Zellen dosisproportional zum Blutzuckerspiegel fördert. Neben der Leber sind Muskel- und Fettgewebe die bedeutendsten Glucoseverbraucher. Aber wie funktioniert das genau? Man weiss heute, dass im Golgikompartiment ein inaktiver Pool von Glucose-Carriern vorhanden ist. Carrier-Proteine sind Membranproteine, die den Durchtritt von Molekülen durch die Membran vereinfachen. Glucose-Carrier-Proteine ermöglichen es den Glucosemolekülen, die Zellmembran zu passieren. Dieses Carrier-Protein ist in diesem Fall der Glucosetransporter 4 (GLUT 4). Die intrazelluläre Signalweiterleitung verursacht im Zellkern eine Translokation. Das Chromosom enthält nun andere Informationen als vorher. Die Folge: Der GLUT 4-Pool wird aktiviert und die Carrier lagern sich in die Zellmembran ein. Das ermöglicht eine vermehrte Glucose-Aufnahme in die Zellen. Gertrud Rehner et. al. (Spektrum Akademischer Verlag, 2010), Biochemie der Ernährung 3. Auflage, S. 146-149 & Florian Horn et. al. (Thieme 2012), Biochemie des Menschen: Das Lehrbuch für das Medizinstudium 5. Auflage, S. 352-353 10 20 Effekt auf die Leber Im Energiestoffwechsel ist die Leber das wichtigste und aktivste Organ. Die Leber unterscheidet sich von anderen Organen, da sie Glucose insulinunabhängig aufnimmt. Dennoch hat Insulin einen Einfluss auf die Glykogensynthese. Insulin bewirkt in der Leber, dass vermehrt Glykogen gebildet und gleichzeitig weniger Glykogen in Glucose gespaltet wird. Auch dieser Effekt geschieht aufgrund der Kinase-Kaskade im Zellinnern. Bindet Insulin an den Insulinrezeptor, wird das für die Glykogensynthese zuständige Enzym (Glykogen-Synthase) phosphoryliert und dadurch aktiviert. Das bewerkstelligt eine erhöhte Glykogensynthese. Andere Kinasen-Kaskaden verursachen zeitgleich eine Aktivierung wichtiger Enzyme der Glykolyse (Phosphofructokinase), wodurch vermehrt Glucose abgebaut wird. Die Enzyme der Gluconeogenese werden durch die intrazellulären Phosphorylierungsreaktionen gehemmt, was den Unterbruch einer glucoseliefernden Reaktion bedeutet. Der Effekt von Insulin auf den Kohlenhydratstoffwechsel lässt sich folgendermassen Zusammenfassen: Insulin fördert die Glucoseaufnahme (GLUT 4), den intrazellulären Glucoseabbau(Glykolyse) und den intrazellulären Umbau (Glykogensynthese). Gleichzeitig unterbricht er glucoseliefernde Prozesse wie beispielsweise Die Gluconeogenese. Fettstoffwechsel Insulin hat auch einen bedeutenden Effekt auf den Fettstoffwechsel. Durch GLUT 4 wird mehr Glucose in die Fettzellen aufgenommen. Gleichzeitig werden durch die oben erwähnten KinasenKaskaden (mehrere Phosphorylierungsreaktionen) genau die Enzyme (Pyruvat-Dehydrogenase, Acetyl-CoA-Carboxylase) aktiviert, die das Pyruvat so verstoffwechseln, dass es zu Malonyl-CoA verarbeitet wird. Malonyl-CoA dient als Vorstufe für die Biosynthese von Fettsäuren, die dann später mit Glycerol zu TAG’s werden. Auf dieselbe Art und Weise hemmt Insulin die Enzyme, die an der Lipolyse beteiligt sind. Die Lipolyse ist die Umkehrung der Lipogenese. Insulin ist das einzige Hormon, das die Lipogenese fördert und gleichzeitig unser Fett in den Fettzellen festhält, indem es den Abbau von TAG’s hemmt. 1.2.5 Fehlfunktionen und Krankheiten Ich möchte diese Möglichkeit nutzen, um die Krankheiten, die einer Fehlfunktion oder gar dem vollständigen Versagen von Insulin zu Grunde liegen, etwas kritisch zu betrachten. Die häufigsten Erkrankungen sind: Diabetes Mellitus (Typ 1 & Typ 2; im Volksmunde auch Zuckerkrankheit) Insulinom (Tumor aus endokrinen Zellen, die vermehrt Insulin produzieren. Macht sich Insulinresistenz (Vorstufe von Diabetes) durch wiederkehrende Unterzuckerung bemerkbar.) Hyperinsulinismus (erhöhte Insulinkonzentration im Blut) 21 Ich will gar nicht weiter darüber berichten, welche Erkrankungen das sind und wie sie wirken, sondern vielmehr darauf eingehen, wie sie entstehen. Der Volksmund glaubt nämlich, dass der Auslöser für diese Fehlfunktionen (vor allem Diabetes) der erhöhte Zuckerkonsum (und folglich ein erhöhter Blutzucker) ist. Das ist nicht falsch. Es ist wahr, dass in den letzten 100 Jahren der Zuckerkonsum drastisch angestiegen ist. Alle denkbaren Süssgetränke und Süssigkeiten wurden von der Zuckerindustrie clever vermarktet. Die Leute konnten nicht ahnen, was das für Folgen haben könnte. Man kannte die Krankheiten kaum, und plötzlich gehörten die „Zuckerkrankheiten“ zu den häufigsten Erkrankungen überhaupt. Man weiss heute, dass der übermässige Zuckerkonsum bzw. allgemein die ungesunde Ernährung nur eine von vielen Ursachen ist. Auch die Menge an Nahrungsmitteln, die der Mensch konsumiert, ist drastisch gestiegen. Vergleicht man Portionsgrössen von heute mit jenen von früher, wird man sich dessen bewusst. Der „Popcorn-Eimer“ im Kino oder das 5 dl Coca Cola im Restaurant waren einst kleine Tüten Popcorn und ein 2-3 dl Glas mit Wasser. Durch die Ernährungsgewohnheiten von heute werden unsere β-Zellen viel stärker beansprucht als früher. Fakt ist, dass die Lebensmittel von heute viel raffinierter und reiner sind als noch vor 100 Jahren. Dadurch schmecken sie intensiver. Unser Körper leidet jedoch darunter. Ich ziele hier auf den glykämischen Index. Dieser ist ein Mass dafür, wie stark ein Kohlenhydrat den Blutzuckerspiegel ansteigen lässt. Die raffinierten Lebensmittel haben einen höheren glykämischen Index, was bedeutet, dass die den Blutzucker stärker ansteigen lassen. Die β-Zellen sind stark gefordert. Früher verhielt sich der Blutzucker um einiges gleichmässiger und ruhiger. Die β-Zellen blieben verschont. Folgende Grafik soll diesen Sachverhalt wiedergeben: Heute Früher Abbildung 10: Der Blutzuckerverlauf früher und heute 22 Ein weiterer Grund für die unzähligen Erkrankungen ist die Bequemlichkeit der heutigen Gesellschaft. Der Mensch muss sich weniger bewegen als früher. Auto und öffentliche Verkehrsmittel machen uns mobil und wir können innert kürzester Zeit ohne jegliche Anstrengung von A nach B reisen. Im Winter ist es überall beheizt und bequem. Man bleibt lieber drinnen als hinaus in die Kälte zu gehen. Die Gesellschaft will jedoch nicht glauben respektive akzeptieren, dass der Mensch selbst an der Zunahme der oben erwähnten Krankheiten schuld ist. Man gibt den Krankheiten und der Genetik die Schuld. Nach dem Motto; „Wir können nichts dagegen tun und sind unserem Körper hilflos ausgeliefert.“ Dabei liegt es einzig und allein in unserer Hand. Die Pharmaindustrie profitiert natürlich von dieser Einstellung der Menschen. Medikamente, die heilende Wirkungen haben sollten, lassen sich dadurch gut verkaufen. Zucker wird von vielen Leuten immer wieder als „Gift“ bezeichnet und in gewisser Weise haben sie Recht! Es wird immer wieder vergessen, dass unser Körper keinen Zucker (Mono-und Dissaccharide), wie er in vielen Lebensmitteln enthalten ist, mit der Nahrung aufnehmen muss. Wie bereits erwähnt, können wir aus den Mehrfachzuckern den für uns wichtigsten Einfachzucker Glucose selbst herstellen. Es lassen sich unter anderem die folgenden Punkte als Ursachenbündel für die erhöhte Anzahl an Zuckerkranken zusammenfassen: Unausgewogene und ungesunde Ernährung (hoher Zuckerkonsum, zu grosse Portionen) Zunehmende Bequemlichkeit und mangelhafte Bewegung Raffiniertere Lebensmittel Die Wissenschaft weiss bis heute nicht, welches die Auslöser einer Diabetes Mellitus Typ 2Erkrankung sind. 1.2.6 Gegenspieler Es gibt nur ein Hormon, das den Blutzucker senken kann, aber dafür eine Menge, welche das Gegenteil bewirken. Fällt der Blutzuckerspiegel unter einen kritischen Wert von ca. 4 mmol/l, wird die Insulinproduktion drastisch reduziert und es kommt zu einer Erhöhung des Blutzuckers durch: Adrenalin Kortisol Glucagon Somatostatin 23 1.3 Künstliche Zuckerersatzstoffe11 Der erste künstliche Zuckerersatz war Saccharin, erstmals synthetisiert um 1897. Im ersten und zweiten Weltkrieg war er aufgrund des Zuckermangels und seiner niedrigen Produktionskosten weit verbreitet. Nach den Kriegen stieg der Lebensstandard und die Wirtschaft konnte sich erholen. Der Zucker wurde plötzlich bezahlbar und somit in Unmengen konsumiert. Die Zahl der Übergewichtigen und Fettleibigen stieg drastisch an. Von hier an war die Verwendung von Saccharin nicht mehr kostenbedingt, sondern man nutzte Saccharin, um kalorienreduzierte Lebensmittel herzustellen. Der Zucker wurde durch Saccharin ersetzt. Der Markt mit kalorienreduzierten Produkten boomte. Leider verleiht Saccharin den Produkten einen bitteren Nachgeschmack. Die Leute wollten alternative Substanzen, die süss schmecken, jedoch keine Kalorien enthalten. Mit Cyclamat erreichte man in den 1950er Jahren einen Durchbruch. Zusammen mit Saccharin entstand eine sehr angenehme Süsse. Man mischte die beiden Zuckerersatzstoffe zusammen und mischte weitere Substanzen dazu. So entstand die Produktreihe „Sweet ’n’ Low“, welche vor allem in den USA ein grosser Erfolg wurde. Die Süssungsmittel-Industrie erlitt einen Schock, als Cyclamat verboten wurde. Laut der „Food and Drug Aministration (FDA)“ sollte Cyclamat krebserregend sein. In allen anderen Ländern ausser den USA wird Cyclamat heute noch verwendet. Der nächste Schritt war die Entdeckung von Aspartam in den 1980er Jahren. Lebensmittel wurden zum ersten Mal mit „light“ beschriftet. Diese drei Substanzen Saccharin, Cyclamat und Aspartam bilden die „erste Generation“ künstlicher Süssstoffe. Alle folgenden (Acesulfam-K, Sucralose etc.) formen die „neue Generation“ der Süssungsmittel. 11 M. R. Weihrauch (Review, 2004), Artifical sweeteners – do they bear a carcinogenic risk? 24 1.3.1 Kategorisierung süssender Stoffe12 Die süss schmeckenden Stoffe lassen sich in drei Kategorien einordnen: Zucker (im Sinne von Zuckerstoffen) Süssstoffe Zuckeraustauschstoffe (Zuckeralkohole) Süssende Substanzen Kohlenhydrate (mit Energie) Süssstoffe (ohne Energie) Einfachzucker Zweifachzucker Mischungen Zuckeralkohole Natürlich künstlich Fructose Lactose Stärkezucker Xylit Thaumatin Cyclamat Glucose Saccharose Maltose Glucosesirup Sorbit Laktit Stevioside Miraculin Maltit Isomalt Zuckerstoffe Zuckeraustauschstoffe Saccharin Acesulfam-K Aspartam Süssstoffe Süssungsmittel Tabelle 1: Kategorisierung süssender Stoffe Folgende Differenzierungen sind wichtig: Zuckerstoffe und Zuckeraustauschstoffe (auch bekannt als mehrwertige Alkohole) verleihen einem Lebensmittel Masse und Volumen, Struktur, Geschmack und Mundgefühl. Süssstoffe dagegen geben einem Lebensmittel lediglich einen süssen Geschmack. Daraus folgt ihr Gebrauch in der Lebensmittelindustrie: Zuckerstoffe v.a. in Backwaren, Süsswaren, Getränken und Obsterzeugnissen als Zuckeraustauschstoffe v.a. in zuckerfreien Backwaren, Süsswaren, Dessertspeisen und Geschmacksverstärker, Feuchthaltemittel, Überzugsmittel und auch Konservierungsmittel Kaugummi als Geschmacksverstärker, Feuchthaltemittel, Trennmittel, Überzugsmittel und auch Konservierungsmittel Süssstoffe v.a. in Getränken, zuckerfreien Süsswaren, Dessertspeisen, Kaugummi und in kalorienverminderten Lebensmitteln ausschliesslich als Süssungsmittel. Dazu muss man erwähnen, dass gerade der Gebrauch von Süssungsmitteln gesetzlich geregelt ist. Je nach dem, mit welchen anderen Substanzen die Süssungsmittel gemischt werden, variiert die zugelassene Menge. K. Rosenplenter et. al. (Behr’s Verlag, 2007), Handbuch Süssungsmittel: Eigenschaften und Anwendung, 2. Auflage, S. 2-5 12 25 1.3.2 Der süsse Geschmack13 Es soll die Frage geklärt werden, weshalb die Zuckerersatzstoffe süss schmecken, obwohl sich ihre Struktur stark von derjenigen der Glucose unterscheidet. Die Wahrnehmung des Geschmackes im Mund findet hauptsächlich über die Zunge statt, während sich im Rachenraum nur sehr wenige Geschmackspapillen befinden. Auf der Zunge befinden sich Geschmackspapillen. Es gibt 3 Abbildung 11: Die Geschmackspapille verschiedene Arten von Geschmackspapillen. Sie unterscheiden sich in ihrer Form und in der Anzahl an Geschmacksknospen. In den Papillen befinden sich die Geschmacksknospen. Etwa 100 Zellen einer Geschmacksknospe sind die eigentlichen Sinneszellen, die als Geschmacksrezeptoren fungieren und schlussendlich mit den Geschmacksstoffen in Verbindung treten. Folglich sind Substanzen nur schmeckbar, wenn sie die Geschmacksrezeptorzellen reizen, sprich an deren Rezeptor andocken können. Die Sinneszellen sind mit afferenten Nervenfasern in Verbindung. Nach neueren Forschungen stellte man fest, dass die Süssrezeptoren eine Vielzahl von unterschiedlichen Stoffen detektieren können, auch wenn sich diese in ihrem Bau stark voneinander unterscheiden. Die angeführten Quellen unterscheiden sich dennoch. Die einen behaupten, dass die Süssstoffe und die Zuckerstoffe über den gleichen Weg erkannt werden und andere behaupten wiederrum, dass sie über unterschiedliche Wege zu einem süssen Geschmack führen. Aber auch wenn man behauptet, dass es unterschiedliche Vorgänge sind, haben diese trotzdem Gemeinsamkeiten und funktionieren nach demselben Prinzip: K. Rosenplenter et. al. (Behr’s Verlag, 2007), Handbuch Süssungsmittel: Eigenschaften und Anwendung, 2. Auflage, S. 16-17 & Christine Knopf (Diplomarbeit, 2000), Beziehung zwischen Struktur und Geschmack bei Aspartam und seinen Analogen, S. 2-12 & HC. Pape et. al. (Thieme, 2014), Physiologie, 7. Auflage, S.805-808 13 26 Durch das Andocken des süss schmeckenden Stoffes wird im Inneren der Sinneszelle ein G G-Protein aktiviert. Dieses aktivierte G-Protein Protein ist in der Lage, weitere Enzyme zu aktivieren, wodurch wod sich Calcium-Speicher im Inneren der Sinneszelle „öffnen“. Gleichzeitig steigt die ATP-Konzentration. ATP Steigende Ca2+-und ATP-Konzentration Konzentrationen depolarisieren die Membran der Sinneszelle. Spannungsgesteuerte Kanäle auf Seiten der Präsynapse öffnen sich und die Ca2+-Ionen und ATPMoleküle können ihre Wirkung als Transmitter entfalten. Die Folge ist eine Depolarisierung der postsynaptischen Membran.. Schlussendlich entsteht ein Aktionspotenzial in der afferenten Nervenfaser. Das Signal, in Form eines Aktionspotenzials Aktionspotenzials, wird an das zentrale Nervensystem weitergeleitet. Schlussendlich nehmen wir einen süssen Geschmack wahr. Abbildung 12:: Entstehung eines süssen Geschmackes 1.3.3 Effekt auf den Metabolismus14 Süssungsmittel haben keinen Einfluss auf den Blutzuckerspiegel bzw. auf die Insulinsekretion. Der in diesem Fall verwendete Zuckerersatz Aspartam hat keinen krebsfördernden Effekt beim Menschen. Auch wenn die Zuckerersatzstoffe süss schmecken, erhöhen sie den Blutzucker Blutzucker-und den Insulinspiegel nicht. Stephen D. Anton et. al. (Elsevier, 2010), Effects of Stevia, Aspartame and Sucrose on food intake, satiety and postprandial glucose an insulin levels 14 27 2 MATERIAL UND METHODEN Mein Ziel ist es, zu zeigen, wie sich künstliche Zuckerersatztstoffe auf unseren Körper auswirken. Ich führte hierfür folgenden Versuch mit insgesamt 7 Probanden durch: Jeder Proband musste drei verschiedene Testflüssigkeiten an drei verschiedenen Tagen zu sich nehmen. Jede Flüssigkeit hat ein Volumen von 500 ml und ist jeweils mit einem anderen Stoff gesüsst: eine Saccharose-Wasser Lösung, eine Aspartam-Wasser Lösung und ein Coca Cola Zero. Letzteres ist mit einem Gemisch aus Süssstoffen (Cyclamat, Acesulfam-K und Aspartam) versehen. Das entspricht viel eher der Realität, als die Aspartam-Wasser Lösung, denn der Grossteil der künstlich gesüssten Getränke ist mit mehr als nur einem Zuckerersatz versehen. Um herauszufinden, welche Einflüsse diese künstlichen Süssstoffe auf unseren Körper haben, wurde vor dem Einnehmen der zu testenden Flüssigkeit und 20, 30, 60, 90 und 120 Minuten danach von jedem Proband venös Blut genommen. Ich hatte also am Schluss insgesamt 126 Proben um herauszufinden, wie sich Blutzucker-und Insulinspiegel nach der Einnahme der drei verschiedenen Testflüssigkeiten verhalten. Weiter untersuchte ich, wie sich der Appetit, das Sättigungsgefühl und die Nahrungsaufnahme der Probanden an den drei Testtagen verhielten. 2.1 Süsskraft der Testflüssigkeit Damit mein Versuch möglichst realitätsgetreu und nachvollziehbar ist, kann ich die Flüssigkeiten nicht irgendwie süssen! Ich versuche also, alle Flüssigkeiten gleich stark zu süssen, so dass sie alle gleich süss schmecken. Da Coca Cola Zero gleich süss ist, wie das gewöhnliche Coca Cola, nehme ich für das Saccharose-Wassergemisch die Zuckerkonzentration von Coca Cola. Es ist bekannt, dass Aspartam 180-200-mal so stark süsst wie Saccharose. Daraus lässt sich berechnen, wie viel Aspartam ich zufügen muss. Das gibt dann folgende Mengen: 53 g Saccharose auf 500 ml Wasser und 0.265 g Aspartam auf 500 ml Wasser. Wie viel Süssstoffe Coca Cola Zero enthält, ist mir leider nicht bekannt. 2.2 Appetit, Sättigung und Nahrungsaufnahme Um vergleichen zu können, wie viel die Probanden an den drei Testtagen assen, zählte ich die jeweils aufgenommenen Kalorien. Um Appetit und Sättigung zu untersuchen, mussten die Probanden an den Testtagen eine Scorecard wie folgt ausfüllen: 1. 2. 3. 4. Unmittelbar vor dem Mittagessen Unmittelbar nach dem Mittagessen 30 Minuten nach dem Mittagessen Jede Stunde bis 18 Uhr 28 Abbildung 13: Sättigungs-und Appetit-Scorecard So weiss ich am Schluss, wie satt resp. hungrig sie sich fühlen. Diese Fragen im Verlauf des Tages betrachtet, geben mir Auskunft darüber, wie lange ihr Sättigungsgefühl anhält und wie sich ihr Appetit verhält. Zusammen mit der Nahrungsaufnahme lassen sich dann genauere Schlüsse ziehen, aber dazu später mehr. 10 9 8 Hungry 7 full 6 satisfied 5 4 eat now 3 Mean 1&4 2 Mean 2&3 1 0 vor nach 30 min 1h 2h 3h 4h Diagramm 1: Veranschaulichung der Ähnlichkeit der einzelnen Kurvenverläufe von Sättigung und Appetit Beim Auswerten sämtlicher Werte habe ich folgende Beobachtung gemacht: Die Antworten auf die Frage, wie hungrig die Probanden sind (1. How hungry do you feel? Kurve „hungry“) und wie viel sie noch essen könnten (4. How much do you think you can eat now? Kurve „eat now“) sind in den meisten Fällen identisch, weshalb ich für die weiteren Auswertungen den Mittelwert dieser beiden Werte (Mean 1&4) verwende. Ebenso fasse ich die Werte der Fragen 2 und 3 zusammen (Mean 2&3). Wenn man sich die Fragen auf der Scorecard genauer anschaut, dann fällt auf, dass die Antworten auf die Frage 3 dieselben sind, wie die Antworten auf die Frage 4, bloss umgedreht. Während bei 29 der 3. Frage „I can’t eat another bite“ ganz rechts steht, befindet sich „Nothing at all“ bei der 4. Frage ganz links. Die 3. und die 4. Frage sind also einfach spiegelverkehrt, sagen aber beide aus, wie viel der Proband noch essen könnte. Aus diesem Grund verzichte ich beim Auswerten auf die 3. Frage, wodurch auch die weitere Betrachtung des Wertes „Mean 2&3“ hinfällig wird. Somit habe ich noch folgende drei Fragen auszuwerten: 1. Wie hungrig fühlst du dich? 2. Wie voll fühlst du dich? 4. Wie viel könntest du jetzt noch essen? Appetit Sättigung Appetit Wie dem Diagramm oben zu entnehmen ist, sind die drei Kurven „hungry“, „eat now“ und „Mean 1&4“ bis auf den ersten Wert deckungsgleich. Da dieses Diagramm Werte einer umfassenden Stichprobe enthält und dadurch aussagekräftig ist, werde ich mit den Werten „Mean 1&4“ weiterarbeiten. Ausserdem wird beide Male nach dem Appetit gefragt. Mit den Mittelwerten dieser zwei Fragen erhalte ich Kurven, die den Appetit im Verlauf des Tages sehr gut veranschaulichen. Die Diagramme sehen dann zusammen mit den Werten der Frage 2 (Sättigung) folgendermassen aus: 10 9 8 7 6 Appetit 5 Sättigung 4 3 2 1 0 1 2 3 4 5 6 7 Diagramm 2: Die verwertbaren Kurven von Appetit und Sättigung 2.3 Nachweis von Insulin Insulin im Blut ist mittels eines „Direct ELISA (Enzyme-Linked-Immuno-Sorbent-Assay)“, auch Sandwich ELISA genannt, nachzuweisen. Dieses Verfahren basiert auf den Grundlagen der Immunbiologie und funktioniert folgendermassen: 1. Ausgangsposition Die Innenwände der Vertiefungen der Mikrotiterplatte sind mit spezifischen monoklonalen Antikörpern beschichtet. In meinem Fall sind es Insulin-Antikörper einer Maus. 30 2. Zufügen Das zu testende Serum wird in die Vertiefungen gegeben. Falls vorhanden, binden die Antigene aus dem Serum an die Antikörper in der Vertiefung. Das kann später nachgewiesen werden. Ich teste also, ob Insulin-Antigene, sprich Insulin, in meinem Serum enthalten ist. 3. Auswaschen Die Testflüssigkeit wird ausgeleert und ausgewaschen. Die Bindung zwischen Antikörper und Antigen hält diesen Krafteinwirkungen stand. Hat das Antigen nicht an den Antikörper gebunden, wird es in diesem Vorgang ausgewaschen. 4. Reporterenzym / Konjugat Es wird derselbe monoklonale Antikörper in die Vertiefung gegeben mit dem Unterschied, dass dieser an ein Reporterenzym gebunden ist. Dieses Enzym hat die Eigenschaft, dass es sich verfärbt, wenn es mit dem richtigen Substrat in Verbindung kommt. Eine solche Konstellation aus Antikörper und eines zweiten funktionalen Moleküls (Reporterenzym) nennt man Konjugat. 5. Auswaschen Die Vertiefungen werden erneut ausgewaschen. Entweder befindet sich jetzt ein Komplex aus Antikörper der Beschichtung, Antigen und reporterenzymgebundener Antikörper in der Vertiefung oder falls anfänglicher Antikörper und Antigen nicht aufeinander gepasst haben nur der spezifische monoklonale Antikörper, der noch immer an der Innenwand "klebt". 6. Verfärbung durch Substrat Das Substrat wird zugefügt. Wenn das Reporterenzym präsent ist, wird sich die Testflüssigkeit in der Vertiefung verfärben. Das Reporterenzym ist aber nur vorhanden, wenn auch das nachzuweisende Antigen in der Vertiefung ist. Diese Verfärbung geschieht also nur, wenn das nachzuweisende Antigen im Serum ist. Anderenfalls gibt es keine Verfärbung. Wenn man die Intensität der Verfärbung misst, kann man bestimmen, wie hoch die Konzentration der Antigene (in meinem Fall Insulin) ist. Zufügen von Serum Auswaschen Nachzuweisendes Antigen anwesend Nachzuweisendes Antigen abwesend Die Anziehungskräfte von Antikörper und Antigen halten den einwirkenden Kräften stand. Der Komplex bleibt in der Vertiefung Das Serum und all seine Bestandteile werden ausgewaschen. Nur die Antikörperbeschichtung bleibt in der Vertiefung zurück Antikörper der Beschichtung verbinden sich mit den Antigenen im Serum. Es entsteht ein AntikörperAntigen-Komplex Antikörper der Beschichtung können nicht binden. Es entsteht kein AntikörperAntigen-Komplex 31 Reporterenzym / Konjugat Auswaschen Substrat Antikörper mit verfärblichem Enzym kann an das Antigen binden. Hier entsteht dieses Sandwich: Antikörper, Antigen, reporterenzymgebundener Antikörper. Auch dieses Mal sind Die Antikörper-AntigenBindungen genug stark, um den Kräften standzuhalten. Der Komplex bleibt in der Vertiefung. Antikörper mit verfärblichem Enzym kann nicht binden, da kein Antigen anwesend ist Reporterenzym bzw. das funktionale Molekül des Konjugats bindet mit dem Substrat und die Vertiefung verfärbt sich Es kommt zu keiner Verfärbung. 2.4 Mercodia Insulin ELISA15 Der Antikörper mit dem Reporterenzym wird ausgewaschen, da er nirgens binden konnte. Wieder bleibt nur die Antikörperbeschichtung zurück Tabelle 2: ELISA zusammengefasst 2.4.1 Testprinzip Mercodia Insulin ELISA ist ein enzymatischer, zweiseitiger Immunoassay mit einer Festphase. Der Test basiert auf der direkten Sandwich-Technik, in welcher zwei monoklonale Antikörper gegen ein bestimmtes Antigen im Insulinmolekül gerichtet sind. Während der Inkubation reagiert das Insulin in der Probe mit den Insulin-Antikörpern im Peroxidase-Konjugat und den Insulin-Antikörpern welche auf der Mikrotiterplatte gebunden sind. Unter einem Konjugat versteht man einen Antikörper, der mit einem zweiten funktionalen Molekül als Markierung verbunden ist. Eine einfache Waschung entfernt die ungebundenen, enzymatisch gekennzeichneten Antikörper. Das gebundene Konjugat wird durch 3,3’und 5,5’- Tetramethylbenzidine (TMB) sichtbar gemacht. Durch Zugabe von Säure wird die Reaktion gestoppt. Der dadurch erhaltene Endpunkt wird nun spektrophotometrisch abgelesen. 15 Mercodia Insulin ELISA Gebrauchsinformationen 32 2.4.2 Inhalt Beschichtete Mikrotiterplatte Maus Anti-Insulin monoklonal 1 Platte Kalibratoren 1,2,3,4,5 5 Fläschchen 96 Vertiefungen 8 Streifen gebrauchsfertig Die unbenutzten Mikrotiterstreifen können in der mit Klebstreifen wiederverschlossenen Originalverpackung 2 Monate lang aufbewahrt werden. Rekombinantes Humaninsulin Gelbfärbung 1000 μl gebrauchsfertig Konzentrationen sind auf dem Fläschchen angegeben. Kalibrator 0 Gelbfärbung Konzentration 0 mU/l 1 Fläschchen 5 ml gebrauchsfertig Enzym Konjugat 11x Reporterenzym Monoklonales Anti-Insulin der Maus. 1 Fläschchen 1.2 ml Zubereitung siehe Enzym Konjugat Puffer Blaufärbung 1 Fläschchen 12 ml gebrauchsfertig Wasch Puffer 21x 1 Flasche 50 ml Substrat TMB Farblose Lösung Achtung: lichtempfindlich! 1 Flasche 50 ml Zubereitung siehe Praktikumsbericht 1 Fläschchen 7 ml Stopp Lösung 0.5 M H2SO4 2.4.3 Grenzen des Verfahrens Praktikumsbericht gebrauchtfertig gebrauchsfertig Tabelle 3: Inhalte des Mercodia Insulin ELISA Kit Proben von Individuen, die einer Insulinbehandlung unterzogen wurden, können den Test stören, da in diesen Insulin-Antikörper vorhanden sind. Hämolysierte Proben (Blutproben, in welchen sich die roten Blutkörperchen aufgelöst haben) beeinträchtigen den Versuch nicht. Hämolyse in Serum- und Plasmaproben kann jedoch einen Abbau von Insulin verursachen, der zu falsch erniedrigten Werten führen kann. Dieser ELISA hat eine obere und untere Messwertgrenze. Werte ausserhalb dieses Bereiches können nicht mehr gemessen werden. Der Bereich reicht von 3 mU/l bis 17 mU/l 33 2.4.4 Erwartete Werte Anhand von Referenzwerten des Labors für Endokrinologie und Diabetologie der Universität Zürich habe ich folgende Insulinkonzentrationen erwartet:: Die Werte von augenscheinlich gesunden und fastenden fastende Personen erreichten einen Mittelwert telwert von 9.2 mU/l und einen Medianwert von 6.9 mU/l. Die Spannweite betrug 2–25 25 mU/l bezogen auf die zentralen 95% der beobachteten Werte. Diese Werte basieren auf jahrelanger langer Erfahrung des Universitätslabors. 2.4.5 Spezifität Dieser Insulin Elisa Kit von Mercodia ist, was die Kreuzreaktionen mit Proinsulinen anbelangt, sehr genau und reagiert mit diesen in einem Bereich, der ohne weiteres vernachlässigbar ist (<0.5 %). Insulinpräparate präparate jedoch verfälschen die Werte enorm, da diese stark mit den Antikörpern der Mikrotiterplatte tte reagieren. Das ist aber ein gutes Zeichen, denn das zeigt, dass diese Präparate dem Humaninsulin sehr ähnlich sind. Die folgenden Kreuzreaktionen werden in der Gebrauchsinformation angegeben: C-Peptide <0.01 % Proinsulin <0.01 % Mausinsulin 0.3 % Schweine-Insulin nsulin 374 % Schaf-Insulin Rinder-Insulin 2.4.6 Praktikumsbericht 48 % 31 % Tabelle 4:: Kreuzreaktionen Die Blutentnahme wurde im Kantonsspital Schaffhausen ausen durchgeführt. Den Insulin-Elisa Insulin durfte ich im Labor für Endokrinologie und Diabetologie der Universität Zürich durchführen. 1. Süsse Lösung trinken Die Probanden trinken die Flüs Flüssigkeit und starten danach ihre Stoppuhren. 2. Blutentnahme Nach den angegebenen Zeitpunkten wird Blut genommen. Da das Serum des Blutes für den ELISA benötigt wird, muss eine grössere Menge Blut venös entnommen werden. Ein Röhrchen mit 8,5 ml Inhalt reicht aus. 3. Blutzucker messen Der Blutzuckerspiegel tzuckerspiegel lässt sich mit einem Blutzuckermessgerät und dem Blut aus den Röhrchen einwandfrei messen. 4. Blutgerinnung Röhrchen 30 Minuten bei Raumtem Raumtemperatur stehen lassen, damit das Blut gerinnen kann. Abbildung 14: Blutserum und Blutzellen durch Zentrifugation getrennt 34 5. Serumgewinnung Das Blut wird bei 3‘900 900 Umdrehungen pro Minute für 6 Minuten zentrifugiert. 6. Vorbereitung der Enzym Konjugat 1x Lösung Man mische 10 ml Enzym Konjugat Puffer mit 1 ml Enzyme Konjugat 11x (elffache ( Konzentration. ation. So erhält man eine Enzym Konjugat 1x Lösung (einfach kkonzentriert) 7. Vorbereitung der Was Wasch Lösung 1x Man mische 20 ml Wasch ch P Puffer uffer 21x mit destilliertem Wasser. Mit diesem Mischverhältnis erhält man die gewollte Was Wasch Lösung 1x 8. Kalibratoren 25 μl von jedem Kalibrator alibrator in die dafür vorgesehene Vertiefung pipettieren. Die Calibrators müssen doppelt gemessen werden! 9. Proben 25 μl von jeder Blutserumprobe in die daf dafür ür vorgesehene Vertiefung pipettieren. 10. Enzym Konjugat 1x Lösung Zugabe von 100 μl Enzyme Konjugat 1x Lösung in jede Vertiefung 11. Inkubation Inkubation auf einem Schüttler (700 (700-900 900 rpm) für eine Stunde bei Raumtemperatur (18(18 25°C). In dieser Zeit verbinden sich die Antigene des Humaninsulins aus den Blutseren mit den Antikörpern ikörpern der beschichteten Mikrotiterplatte. 12. Waschen mit Wasch Lösung 1x Reaktionsvolumen verwerfen, durch Umdrehen der Mikrotiterplatte latte über einem Ausgussbecken. 300 μL Wasch Lösung 1x in jede Vertiefung geben. Wasch Lösung 1x verwerfen und mehrmals kräftig gegen saugfähiges Papier schlagen, um überschüssige Flüssigkeit zu entfernen. 66-mal wiederholen. Längere Einwirkzeiten während dieser Waschprozedur vermeiden. 13. TBM Substrat Zugabe von 200 μl TBM Substrat in die Vertiefungen Abbildung 15: Auswaschen der Vertiefungen 35 14. Inkubation 15 Minuten bei Raumtemperatur inkubieren lassen. In dieser Zeit verfärben sich die Vertiefungen je nach Insulinko Insulinkonzentration unterschiedlich stark. 15. Stopp Lösung Zugabe von 50 μL Stopp Lösung in jede Vertiefung. Um eine gute Mischung von Substrat und Stopp Lösung zu gewährleisten, wird empfohlen, die Platte für 5 Sekunden auf den Schüttler zu stellen 16. Absorption mit Photometer messen Messen der Absorption bei 450 nm (Wellenlänge) und auswerten. Das Resultat sollte innerhalb von 30 Minuten abgelesen werden. Abbildung 16: Unterschiedlich starke Verfärbungen je nach Insulinkonzentration 2.4.7 Umrechnungsfaktor 1 μg/l = 23 mU/l 1mU/l = 6.0 pmol/l mmol/l = 18 mg/dl 36 2.4.8 Berechnung der Resultate Kalibratorkurve Linear Regression 2.5 450 Blank 2 1.5 1 0.5 0 0 50 100 150 200 Konzentrationen der Kalibratoren [mU/l] 250 Diagramm 3: Kalibratorkurve Auf der X-Achse sind die Konzentrationen der Kalibratoren eingetragen und auf der Y-Achse die dabei gemessenen Absorptionen: Konzentration der Kalibratoren [mU/l] 0 3 9.74 29.8 104 Absorption 0 0.0285 0.1135 0.401 1.176 Jede Verfärbung wird relativ zu diesen Standardwerten beziehungsweise zu der Standardkurve berechnet. Die Standardkurve (hier ist es eine Trendkurve durch die erhaltenen Punkte) ist dem Diagramm oben zu entnehmen. Die von Excel berechnete Funktionsgleichung der Standardkurve wird nach „x“ aufgelöst, da auf der X-Achse die Konzentrationen eingetragen, sind und die will man herausfinden. Nun setzt man die vom Photometer gemessene Absorption in die Funktionsgleichung ein und man erhält die dazugehörige Insulinkonzentration. 37 3 RESULTATE 3.1 Die Probanden P1 Geschlecht Alter Gewicht (kg) BMI Grösse (cm) Blutdruck W 44 68 24 168 118-71 W P2 P3 M P4 M P5 M P6 M P7 M 20 50 18 165 108-81 46 104 32 178 168-103 16 75 22 186 124-74 183 124-73 43 17 18 100 71 85 30 181 21 25 184 125-75 125-71 Tabelle 5: Angaben zu den Probanden Ich hatte für meinen Feldversuch 7 Probanden gefunden. Wie man der Tabelle entnehmen kann, unterscheiden sich die Probanden stark voneinander, und das war auch mein Ziel. 3.2 Das Verhalten des Blutzuckerspiegels Anhand der Blutproben konnte ich folgende Blutzuckerkonzentrationen messen: 9.00 Blutzucker [mmol/l] 8.00 7.00 Saccharose 6.00 Aspartam Coke Zero 5.00 4.00 3.00 0 30 60 Zeit [min] 90 120 Diagramm 4: Durchschnittlicher Blutzuckerspiegel aller Probanden 38 Zeit Saccharose 0 STABW Aspartam STABW Coke Zero STABW 5.11 0.38 5.30 0.39 5.49 0.41 Saccharose: 20 7.79 30 1.00 5.29 0.52 5.57 0.43 6.57 1.86 5.34 0.68 5.50 0.54 60 4.89 90 1.03 5.24 0.36 5.51 0.26 4.76 120 0.66 5.07 0.33 5.36 0.42 5.17 0.54 5.19 0.32 5.54 0.48 Tabelle 6: Durchschnittlicher Blutzuckerspiegel und Standardabweichungen (STABW) Nach 20 Minuten war der Blutzucker am höchsten. Danach wird die Blutglucose in die Zelle aufgenommen, worauf der Blutzuckerspiegel unter den Nüchternwert fällt. Nach 120 Minuten hat sich der Blutzuckerspiegel wieder auf dem Nüchternlevel eingependelt. Aspartam: Die Kurve verläuft beinahe waagrecht. Coca Cola Zero: Die Kurve entspricht bis auf einen vernachlässigbaren Ausschlag (nach 30min) der parallelen Verschiebung der Aspartamkurve nach oben. Standardabweichungen: Die Standardabweichungen sind im Durchlauf mit Saccharose am grössten. 39 3.3 Das Verhalten der Insulinkonzentration Nachdem die Blutproben zentrifgiert wurden, konnte ich anhand der Blutseren und eines ELISAs die folgenden Insulinkonzentrationen messen: 40.00 35.00 30.00 Insulin [mU/l] 25.00 Saccharose 20.00 Aspartam 15.00 Coke Zero 10.00 5.00 0.00 Zeit Saccharose STABW Aspartam STABW Coke Zero STABW Saccharose: 0 0 30 60 90 Zeit [min] 120 Diagramm 5: Durchschnittliche Insulinkonzentration aller Probanden 4.89 4.95 3.21 3.35 5.45 2.84 20 29.29 19.33 3.43 2.37 7.13 4.41 30 29.60 23.87 3.65 3.01 6.97 4.68 60 11.75 90 8.38 4.08 4.19 4.89 2.96 4.93 5.07 3.49 2.23 6.27 4.32 120 5.94 5.51 3.76 3.67 7.27 4.11 Tabelle 7: Durchschnittliche Insulinkonzentrationen und Standardabweichungen (STABW) Die Insulinkonzentration steigt zu Beginn stark an und bleibt für einen Moment (ca. 5-10 Minuten) auf diesem Niveau. Danach wird das Insulin von den Zellen aufgenommen und abgebaut, wodurch die Konzentration auf den nüchternen Insulinwert fällt. Aspartam: Die Kurve verhält sich waagrecht ohne irgendwelche signifikante Ausreisser. 40 Coca Cola Zero: Die Insulinkonzentration im Blut nach Einnahme von Coca Cola Zero unterliegt seltsamen Schwankungen. Zuerst folgt eine Ausschüttung von Insulin ins Blut, wodurch die Insulinkonzentration auf ein erstes Maximum ansteigt. Bei 60 Minuten knickt die Kurve ein und die Insulinkonzentration fällt unter den Nüchternwert. Von hier an steigt sie linear an. Standardabweichungen: Auch bei den Insulinkonzentrationen sind die Abweichungen im 1. Testdurchlauf deutlich am höchsten. Im Vergleich zu Aspartam und Coca Cola Zero sind die Standardabweichungen im Durchlauf mit Saccharose stark erhöht. 3.4 Nahrungszufuhr Die Probanden haben sich an den drei Testtagen notiert, was sie gegessen hatten. Somit konnte ich ermitteln, wie viel Kalorien sie gegessen hatten. 10000 9000 8000 7000 Energie [kJ] 6000 5000 4000 3000 2000 1000 0 Abend Snack Mittag Saccharose: Saccharose Aspartam Coke Zero 1197 2475 2686 3839 3281 3714 3161 2192 2917 Diagramm 6: Durchschnittliche Nahrungszufuhr in Kilojoule aller Probanden Insgesamt: 8‘317 kJ (= 1‘986 kcal). An der Nahrungsaufnahme ist nichts Aussergewöhnliches festzustellen, als die Probanden die Saccharose-Wasser Lösung zu sich nahmen. Die knappen 8'400 (=2‘000 kcal) entsprechen der Referenzmenge für einen Erwachsenen. Das Mittagessen war etwas grösser als das Abendessen und die kleinen Mahlzeiten zwischendurch sind durchaus angemessen. Aspartam: Insgesamt: 9‘351 kJ (=2‘233 kcal). Nach der Einnahme der Aspartamlösung assen die Probanden im Vergleich zu den anderen Testtagen am meisten. Das sind immerhin 1‘034 kJ (=247 kcal) mehr, als sie nach der Saccharose zu sich genommen haben und 1‘550 kJ (=371 kcal) mehr als nach dem halben Liter Coca Cola Zero. Die Hauptmahlzeiten Mittag-und Abendessen sind bei Saccharose und 41 Aspartam beinahe identisch. Es fällt auf, dass vor allem zwischendurch (Snacks) mehr gegessen wurde. Coca Cola Zero: Insgesamt: 7‘794 kJ (=1‘862 kcal). Am dritten und letzten Tag, als die Probanden das Coca Cola Zero tranken, assen sie am wenigsten. Am Mittag und am Abend wurde weniger konsumiert, als im ersten und zweiten Testdurchlauf. Zwischendurch assen die Probanden noch mehr, als sie es am zweiten Testtag nach Aspartam taten. 3.5 Der Appetit Durch Berichte der Probanden über ihren Appetit im Verlauf des Tages konnte ich folgende Kurven zeichnen: 10.0 8.0 6.0 Saccharose 4.0 Coke Zero Aspartam 2.0 0.0 Zeit Saccharose Aspartam Coke Zero Saccharose: vor vor nach 30 min 1h 2h 3h 4h Diagramm 7: Durchschnittlicher Appetit aller Probanden im Tagesverlauf 3.2 3.4 3.3 nach 2.0 1.5 1.1 30 min 1.8 1.1 1.1 1h 2.1 1.3 1.6 2h 2.0 1.7 1.9 3h 2.7 4h 2.0 2.3 2.6 2.5 2.9 Tabelle 8: Durchschnittliche Standardabweichungen beim Appetit Wie dem Diagramm zu entnehmen ist, hatten die Probanden im Durchlauf mit Saccharose keine Probleme mit dem Appetit. Vor dem Essen war er weder ausserordentlich gross noch extrem klein. Nach dem Essen fühlten sich die Probanden satt und im Verlauf des Nachmittages stieg der Appetit wieder an. Aspartam: 42 Wie man sieht, ist der Appetit vor dem Essen grösser, als bei der Saccharose. In den ein bis zwei Stunden nach dem Essen bleibt der Appetit, im Vergleich zur Saccharose, länger klein. Im Verlauf des Nachmittags steigt er jedoch ein wenig schneller und stärker an. Im Grossen und Ganzen verhält sich der Appetit am Nachmittag jedoch gleich wie im ersten Testdurchlauf. Coca Cola Zero: Offensichtlich war der Appetit, im Vergleich zu Saccharose und Aspartam, vor dem Essen am grössten. Nach dem Mittagessen hatten die Probanden den kleinsten Appetit von allen drei Testdurchläufen. Das hielt jedoch nicht lange an. Im Gegenteil. Der Appetit stieg stark an und wurde sehr schnell sehr viel grösser als in den ersten zwei Durchläufen. Will man eine Aussage darüber machen, an welchem Tag die Probanden den grössten Appetit verspürten, so muss man dafür die Fläche unter den Kurven berechnen. ä ℎ = ( + 2 Saccharose Aspartam Coke Zero × ∆ ) Fläche 1184 1089 1179 Tabelle 9: Fläche unter den Appetitkurven Je grösser diese Fläche ist, desto grösser ist der Appetit. Somit kann man aussagen, dass die Probanden am ersten und dritten Testtag am meisten Appetit hatten, während sie im Durchlauf mit Aspartam weniger Appetit hatten. 43 3.6 Das Sättigungsgefühl Anhand einer Scorecard konnte ich das Sättigungsgefühl der Probanden untersuchen. 10.0 9.0 8.0 7.0 6.0 Saccharose 4.0 Coke Zero 5.0 Aspartam 3.0 2.0 1.0 0.0 Zeit vor nach 30 min 1h 2h 3h 4h Diagramm 8: Durchschnittliches Sättigungsgefühl aller Probanden im Tagesverlauf inkl. Standardabweichungen Saccharose vor Aspartam Coke Zero 1.5 3.4 3.3 nach 3.4 1.6 1.2 30 min 3.1 1.1 0.9 1h 3.1 1.2 1.6 2h 2.8 1.6 1.9 3h 2.8 4h 1.9 2.4 2.5 2.6 2.8 Tabelle 10: Durchschnittliche Standardabweichungen beim Sättigungsgefühl Saccharose: Die Probanden hatten im ersten Testdurchlauf ein gewöhnliches Sättigungsgefühl. Sie haben sich weder extrem voll noch extrem leer gefühlt. Das Sättigungsgefühl machte sich erst 30 Minuten nach dem Essen bemerkt. Im Verlauf des Nachmittags liess dieses Gefühl nach und die Probanden wurden allmählich wieder hungrig. Aspartam: Im Vergleich zu den anderen zwei Testdurchläufen fühlten sich die Testpersonen im Testdurchlauf mit Aspartam vor dem Essen ein wenig satter. Nach dem Essen fühlten sie sich dann deutlich satter. Und das Sättigungsgefühl hielt auch deutlich länger an, so dass sich die Probanden lange nach dem Essen noch satt fühlten. Coca Cola Zero: Nachdem die Probanden den halben Liter Coca Cola Zero getrunken hatten, waren sie im Vergleich mit den ersten zwei Durchläufen am hungrigsten. Dafür fühlten sie sich nach dem Essen am 44 sattesten. Dieses Sättigungsgefühl verschwand jedoch genauso schnell wieder, wie es kam. Die Sättigungskurve von Coca Cola Zero fällt stark, bis unter die Kurven von Aspartam und Saccharose. Auch hier lässt sich dieselbe Methode anwenden, um zu bestimmen, an welchem Tag die Probanden am sattesten waren. Je grösser die Fläche unter der Kurve, desto grosser war das Sättigungsgefühl. Saccharose Aspartam Coke Zero Fläche 1827 2102 1927 Tabelle 11: Flächen unter den Sättigungskurven Im Testdurchlauf mit Aspartam fühlten sich die Probanden insgesamt am sattesten. An zweiter Stelle steht der 3. Durchlauf mit Coca Cola Zero und nach Saccharose hatten die Probanden das kleinste Sättigungsgefühl. 45 4 DISKUSSION Bevor ich beginne, genauer auf die Resultate einzugehen und diese zu erklären, möchte ich folgendes anmerken: Aufgrund der Informationen meiner Probanden gehe ich davon aus, dass die Resultate aus dem Durchlauf mit Saccharose mit denen aus dem Alltag korrelieren. Vor allem was Nahrungszufuhr, Sättigung und Appetit betrifft. Natürlich hätte ich die Probanden auffordern können, die Scorecard zusätzlich an einem ganz normalen Tag auszufüllen und mir zu berichten, was sie gegessen hatten. Da ich aber untersuche, wie sich künstliche Süssstoffe im Vergleich zu Haushaltszucker auf den Körper auswirken, hat dies nur im entfernteren Sinne mit meiner Maturaarbeit zu tun. Ich muss an dieser Stelle noch erwähnen, dass meine Stichprobe aus 7 Probanden sehr klein ist. Mit einer Basis aus Messewerten von 7 Probanden lassen sich keine signifikanten Statistiken erstellen. Um statistisch relevante Aussagen machen zu können, muss eine Studie eine viel grössere Stichprobe behandeln. Ich kann lediglich Vermutungen aufstellen, und diese mit meinen Messwerten versuchen zu begründen. 4.1 Probanden An dieser Stelle möchte ich erwähnen, dass meine Probanden kerngesund sind. Da der BMI Muskeln und Fett nicht unterscheidet und den Körperbau ebenfalls nicht berücksichtigt, ist auf diesen in dem Fall kein Verlass. Keiner meiner Probanden hat auch nur im entferntesten Adipositas! Sie treiben alle regelmässig Sport und ernähren sich ausgewogen. 4.2 Homeostatic Model Assessment16 In der folgenden Tabelle sind die sogenannten HOMA (Homeostatic Model Assessment) eingetragen. Diese HOMA Werte sind ein Methode, mit welcher man die Insulinresistenz und die Beta-Zell Funktion messen kann. Man muss jedoch dazu sagen, dass diese Werte einen stark mathematischen Charakter haben und deshalb die Werte mit Vorsicht zu geniessen sind! Die Formeln sind unten zu sehen. Es werden jeweils nur die Nüchternwerte (n.Glucose und n.Insulin) für die Berechnung gebraucht. Die Nüchtern-Werte allein genügen also, um zu ermitteln, ob jemand eine Insulinresistenz hat und wie gut seine Beta-Zellen funktionieren. = . × . 22,5 = 20 × . . − 3,5 % Der HOMA IR (Insulinresistenz) besagt, dass wenn der Wert die Grenze von 2,7 überschreitet, ist es wahrscheinlich, dass die Person eine Insulinresistenz vorweist. Je höher der HOMA IR, desto wahrscheinlicher ist es also, dass eine Insulinresistenz vorliegt. 16 National Center for Biotechnology Information: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3152191/ 46 Der HOMA -Zelle gibt (in Prozent) an, wie gut die Beta-Zellen funktionieren bzw. wie stark sie ausgelastet sind. Hier ist ein hoher Wert ein Zeichen dafür, dass die Beta-Zellen viel Insulin ausschütten. Werte bis zu 65% sind liegen im gesunden Bereich. Proband 1 Proband 2 Proband 3 Proband 4 Proband 5 Proband 6 Proband 7 Nüchtern Blutzucker Nüchtern Insulin HOMA IR HOMA b-Cell (%) 5.00 1.48 0.33 19.69 4.85 2.66 0.57 39.45 5.70 12.27 3.11 111.57 5.61 2.49 0.62 23.57 5.26 3.61 0.84 41.14 5.40 3.76 0.90 39.60 5.58 5.35 1.33 51.48 Tabelle 12: Homeostatic Model Assessment Wie man der Tabelle entnehmen kann, sind alle Probanden weit von einer Insulinresistenz entfernt und haben gesunde und funktionierende Beta-Zellen, bis auf einen einzigen Probanden. Dieser Proband hat einen erhöhten HOMA IR und einen im Vergleich mit den restlichen Probanden hohen HOMA -Zelle. Was heisst das nun? Man muss diese Werte miteinander in Verbindung bringen, denn sie hängen stark voneinander ab. Proband 3 hat einen gewöhnlichen Nüchternblutzucker, jedoch eine erhöhte Nüchterninsulinkonzentration. Diese erhöhte Nüchtern-Insulinkonzentration stimmt mit dem erhöhten HOMA IR und ebenfalls erhöhten HOMA -Zelle überein. Aufgrund der Tendenz einer Insulinresistenz muss die β-Zelle mehr Insulin produzieren und ausschütten, damit der Blutzucker gesenkt werden kann, denn die Zellen reagieren weniger auf Insulin wie diejenigen eines gesunden Menschen. Um den Blutzucker auf ein gewisses Niveau zu senken, braucht es bei einer Person mit einer Insulinresistenz mehr Insulin als bei einer gesunden Person. In diesem Zusammenhang soll gesund bedeuten, dass die medizinischen Werte im Normalbereich liegen. Die drei Werte von Proband 3 (nüchtern Insulin, HOMA IR, HOMA -Zelle) lassen eine Insulinresistenz vermuten. Der Körper schafft es, durch eine erhöhte Insulinsekretion den Blutzucker auf ein gesundes Level zu senken. Auch wenn man die Insulinkonzentrationen in den drei Versuchen mit den Mittelwerten vergleicht, sind sie deutlich höher (siehe Kapitel 10.1.2). 4.3 Das Blutzuckergedächtnis17 Um sicher zu gehen, ob und wie ausgeprägt der Proband 3 insulinresistent ist, müsste dieser den HbA1C Test machen. HbA1C ist ein Glykohämoglobin, das heisst eine Form von Hämoglobin, an das Glukose gebunden ist. Der Anteil des HbA1C am gesamten Hämoglobin (Hb) lässt sich mit einer Blutuntersuchung feststellen. Dieser erlaubt eine Aussage über den Blutzuckerspiegel der vergangene Wochen und ist somit einiges aussagekräftiger als meine Messungen. Diesen Test lege ich dieser Person ans Herzen. Florian Horn et. al. (Thieme 2012), Biochemie des Menschen: Das Lehrbuch für das Medizinstudium 5. Auflage, S.523 17 47 4.4 Korrelation von Blutzucker-und Insulinkonzentration Der Korrelationskoeffizient (auch Korrelationswert) ist ein dimensionsloses Mass, das angibt, wie sehr zwei Merkmale linear zusammenhängen. Er kann Werte von -1 bis 1 annehmen, wobei bei einem Wert von 1 (bzw. -1) ein vollständiger linearer Zusammenhang besteht. Je näher sich der Korrelationswert bei null befindet, desto kleiner ist der lineare Zusammenhang der zwei Merkmale. Diese Merkmale sind in dem Fall der Blutzucker und die Insulinkonzentration im Blut. Proband 1 Saccharose -0.14 Proband 2 Aspartam 0.90 Proband 3 Proband 6 0.13 0.59 0.77 -0.63 0.95 -0.60 0.75 Proband 7 0.03 0.34 0.85 Proband 5 -0.09 0.02 0.97 Proband 4 0.05 Coca Cola Zero 0.30 0.66 -0.01 0.83 0.63 Tabelle 13: Korrelationskoeffizienten Die rot markierten Werte sind diejenigen, welche eine auffallend kleine Korrelation aufweisen. Alle diese Werte sind auf Ausreisser zurückzuführen. Alle anderen Korrelationswerte zeugen von einer guten Korrelation von Blutzucker und Insulin. Im Durchlauf mit Saccharose korrelieren Blutzucker und Insulin sehr gut miteinander. Mit Ausnahme von Proband 1. Das könnte daran liegen, dass ihre Zellen so sensitiv auf Insulin reagieren, dass die kleinste Menge bereits zu einer Glucoseaufnahme der Zellen führt. Dadurch wird der verzögerte Effekt von Insulin geschwächt, auf dem Papier jedoch verstärkt: Proband 1 Blutzucker (mmol/l) Insulin (mU/l) 0 4.8 0.94 20 6.3 3.02 30 4.7 19.81 60 3.9 7.64 90 3.8 120 5.57 4.4 1.13 Tabelle 14: Blutzucker und Insulin von Proband 1 im ersten Testdurchlauf Man kann erkennen, dass in den ersten 30 Minuten die Blutzuckerkonzentration ansteigt und gleich wieder sinkt, während der Insulinspiegel stetig ansteigt. Deshalb ist die Korrelation so klein. In den Versuchen mit Aspartam und Coca Cola Zero häufen sich die niedrigen Korrelationen. Diese Tatsache ist möglicherweise auf die Homöostase zurückzuführen. Insulin und seine Gegenspieler versuchen den Blutzucker auf einem Niveau zu halten. Dies geschieht jedoch unter gewissen Schwankungen und Unregelmässigkeiten, was zu einer geringen Korrelation von Insulin und Blutzucker führt. Die hohen Korrelationswerte im 2. Und 3. Durchlauf sind also eher zufälligen Ursprungs. 48 4.5 Chi Quadrat Test Da das ELISA-Verfahren ein sehr schwieriges Verfahren ist, können sehr schnell Ungenauigkeiten bei den Messungen auftauchen. Der Chi Quadrat Test ist ein statistisches Mittel, welches ich verwende, um herauszufinden, ob ein Ausreisser irrtümlich entstand ist oder ob er im Bereich der erwarteten Schranken liegt. Am Ende erhalte ich eine Wahrscheinlichkeit, die Irrtumswahrscheinlichkeit p. Je höher diese ist, umso eher ist der Ausreisser irrtümlichen Ursprungs. Aspartam Erwartung 0 20 3.21 Gemessen 3.11 3.43 30 60 3.65 26.51 4.08 3.40 90 3.49 3.40 120 3.76 5.19 3.58 Tabelle 15: Literaturwerte Insulinkonzentration nach künstlichen Zuckerersatzstoffen 18 Nullhypothese: Der Ausreisser (Proband 7, Aspartam, 20 Minuten) ist kein Zufall sondern liegt im erwarteten Schwankungsbereich. ℎ Proband 7 Chi Werte 0 ( = 0.003 20 155.431 30 ℎ 0.018 60 − 0.116 ) 90 0.826 120 Summe 0.008 156.402 Tabelle 16: Chi Quadrat Test Proband 7 Man kann deutlich erkennen, dass der rot markierte Wert aus der Reihe tanzt. Nach dem Aufsummieren erhält man einen Chi Quadrat Wert, der extrem hoch ist und ausschliesslich auf den Ausreisser nach 20 Minuten zurückzuführen ist. p Chi Werte 0,005 0,68 0,01 0,87 0,025 1,24 0,05 1,64 0,1 0,5 2,20 5,35 0,9 0,95 0,975 0,99 0,995 10,64 12,59 14,45 16,81 18,55 Tabelle 17: Chi Quadrat Verteilung für den Freiheitsgrad 6 19 Es liegt also mit beinahe 100 prozentiger Wahrscheinlichkeit ein Irrtum vor. Ich muss diese Insulinkonzentration durch einen Literatur-bzw. Mittelwert ersetzen. Was wird das für einen Einfluss auf meine Teststatistik haben? Folgende Diagramme veranschaulichen dies. 18 Stephen D. Anton et. al. (Elsevier, 2010), Effects of Stevia, Aspartame and Sucrose on food intake, satiety and postprandial glucose an insulin levels 19 https://de.wikibooks.org/wiki/Statistik:_Tabelle_der_Chi-Quadrat-Verteilung 49 0 30 60 Zeit [min] 90 Insulin [mU/l] Insulin [mU/l] 10.00 8.00 6.00 4.00 2.00 0.00 120 10.00 8.00 6.00 4.00 2.00 0.00 Diagramm 9: Korrigierte Insulinkurve 0 30 60 Zeit [min] 90 120 Diagramm 10: Ursprüngliche Insulinkurve 4.6 Das Verhalten des Blutzuckerspiegels Auf der Basis meiner Messwerte versuche ich in den folgenden Kapitel Blutzucker, Insulin, Nahrungsaufnahme, Appetit und Sättigung in Verbindung zu bringen. 9.00 Blutzucker [mmol/l] 8.00 7.00 Saccharose 6.00 Aspartam Coke Zero 5.00 4.00 3.00 0 Zeit 30 0 min 60 90 Zeit [min] 120 Diagramm 11:Blutzuckerspiegel mit Standardabweichung 20 min 30 min 60 min 90 min 120 min Saccharose 5.11 7.79 6.57 4.89 4.76 5.17 Maximum 5.6 9.4 9 6.4 5.6 5.8 Minimum Standardabweichung 4.60 0.38 6.30 1.00 4.50 1.86 3.60 1.03 3.80 0.66 4.40 0.54 50 Aspartam 5.30 5.29 5.34 5.24 5.07 5.19 Maximum 5.9 6.2 6.2 5.7 5.7 5.7 Minimum 4.90 4.70 4.30 4.70 4.80 4.70 Standardabweichung 0.39 0.52 0.68 0.36 0.33 0.32 Coke Zero 5.49 5.57 5.50 5.51 5.36 5.54 Maximum 6 6.2 6.2 5.8 5.9 6.5 Minimum Standardabweichung 4.80 0.41 4.90 0.43 4.70 0.54 5.10 0.26 4.50 0.42 5.10 0.48 Tabelle 18: Mittelwerte, Minima, Maxima und Standardabweichung der Blutzuckerkonzentration Die Standardabweichung ist ein Mass für die Streuung der Testresultate. Sie beschreibt den Bereich, in dem sich 68% aller Werte befinden. Saccharose: Aufgrund meiner Recherche habe ich herausfinden können, welche Zeitpunkte für meine Feldversuche die geeignetsten und aussagekräftigsten sind. Viele Publikationen benutzen genau dieselben Zeitpunkte, wenn Blutzucker oder Insulin gemessen wird20. Nach 20 Minuten erwartet man das Maximum. Danach sinkt der Blutzucker aufgrund einer Insulinausschüttung und sollte nach 120 Minuten wieder den Nüchternwert erreichen. Das stimmt für die Saccharosekurve ziemlich genau. Meine Kurve ist mit jenen der Publikationen praktisch äquivalent. Was jedoch auffällt, sind die hohen Standardabweichungen. Nach 30 Minuten ist die Streuung am grössten. Das könnte bedeutet, dass der Blutzuckerspiegel bei den einen schneller und effektiver gesenkt wird, als bei den anderen. Die ebenfalls hohe Streuung nach 20 Minuten lässt vermuten, dass bei denselben Probanden der Blutzucker gar nicht erst so sehr ansteigt. Wie bereits erwähnt sind meine Probanden sehr unterschiedlich: männlich-weiblich, sportlich-passiv, die Essgewohnheiten, genetische Variabilität etc. Diese Faktoren haben alle einen Einfluss darauf, wie effektiv ein Individuum auf Kohlenhydrate reagiert. Stephen D.Anton et. al. (Elsevier, 2010), Effects of Stevia, Aspartame and Sucrose on food intake, satiety and postprandial glucose an insulin levels 20 51 Aspartam: Da Aspartam ein künstlicher Süssstoff ist, ist es kein Kohlenhydrat. Es gibt also keinen Grund, weshalb der Blutzucker ansteigen sollte. Aspartam hatte keinen Einfluss auf den Blutzuckerspiegel. pro 100 g pro Stück (0,05g) 1564 kJ 0,8 kJ (0,2 kcal) (368kcal) 92 g 0.046 g 0g 0g 0g 0g Brennwert Proteine Kohlenhydrate Fette Tabelle 19: Nährwerte von Assugrin Gold (Süssstoff Aspartam) 21 Im zweiten Testdurchlauf hatten die Probanden also insgesamt 4kJ zu sich genommen (5 Assugrin Gold). Die Blutzuckerkurve mit ihren leichten Schwankungen stimmt also mit der Tatsache überein, dass dem Körper kein Zucker hinzugefügt wurde. Die leichten Schwankungen sind normal und können auch beobachtet werden, wenn man den Blutzucker eines Probanden nach 12 Stunden fasten ohne Einnahme irgendwelcher Testsubstanzen beobachtet. Diese leichten Schwankungen gehen auf das Zusammenspiel von Insulin und Glucagon zurück. 22 Was im Vergleich zur Saccharose auffällt, sind die Standardabweichungen. Sie sind um einiges kleiner, was bedeutet, dass die Probanden im 2. Testdurchlauf deutlich ähnlicher auf die Testsubstanz reagiert haben. Die Begründung ist dieselbe wie beim Coca Cola Zero und steht deshalb im Abschnitt Coca Cola Zero. Coca Cola Zero: Wie der Name schon sagt, hat Coca Cola Zero keine Kalorien und der Blutzuckerspiegel verhält sich auch dementsprechend. Brennwert Proteine Kohlenhydrate Fette pro 100 ml pro Portion (250 ml) 0.9 kJ (0.2 kcal) 2.3 kJ (1kcal) 0g 0g 0g 0g 0g 0g Tabelle 20: Nährwerte von Coca Cola Zero Die Kurve ist bis auf die ersten 30 Minuten sogar parallel mit dem Verlauf der Aspartamkurve. Der Nüchternblutzucker ist höher als im 2. Testdurchlauf. Das kann verschiedene Gründe haben. Die Probanden könnten am Vorabend mehr gegessen haben. Sie könnten aufgeregter gewesen sein. Der 3. Testdurchlauf fand am Morgen des ersten Schultages nach den Herbstferien statt. Die Probanden wurden vom Unterricht dispensiert. Die Tatsache, dass die Schüler nicht zur Schule mussten, hat möglicherweise ebenfalls einen erhöhenden Einfluss auf die Nüchternglucose. 21 22 Homepage von Assugrin: http://www.assugrin.ch/daten_d/produkte/assugrin_gold.php http://www.ncbi.nlm.nih.gov/pubmed/19789156 52 Die Standardabweichungen sind allesamt kleiner, als diejenigen des ersten Testdurchlaufes. Denen des zweiten Testdurchlaufes sind sie sehr ähnlich. Die Probanden sprachen auf Coca Cola Zero, wie auch auf Aspartam, ähnlich an. Begründung des ähnlichen Verhaltens auf die Zufuhr von Aspartam und Coca Cola Zero: Es wird dem Körper nichts zugefügt, was Einfluss auf den Blutzuckerspiegel haben könnte. Deshalb verändert sich dieser auch nicht. Der Körper muss auf nichts reagieren und versucht im Sinne der Homöostase den Blutzucker konstant zu halten. Die Folge ist, dass die Streuung der Blutzuckerwerte viel kleiner ist. Faktoren wie Essverhalten, Aktivitätsgrad und biologische Variabilität (Veranlagung, Genetik) spielen erst eine Rolle, wenn der Körper auf eine Erhöhung des Blutzuckers infolge von Nahrungsaufnahme reagieren muss. Die folgenden drei Diagramme veranschaulichen die unterschiedlichen bzw. ähnlichen Reaktionen aller 7 Probanden auf Saccharose bzw. Aspartam und Coca Cola Zero. Saccharose Blutzucker [mmol/l] 10 9 p1 8 p2 7 p3 6 p4 5 p5 4 3 0 30 60 Zeit [min] 90 120 p6 p7 Diagramm 12: Blutzucker der einzelnen Probanden im 1. Durchlauf 53 Aspartam Blutzucker [mmol/l] 10 9 p1 8 p2 7 p3 6 p4 5 p5 4 3 0 30 60 Zeit [min] 90 120 p6 p7 Diagramm 13: Blutzucker der einzelnen Probanden im 2. Durchlauf Coca Cola Zero Blutzucker [mmol/l] 10 9 p1 8 p2 7 p3 6 p4 5 p5 4 3 0 30 60 Zeit [min] 90 120 p6 p7 Diagramm 14: Blutzucker der einzelnen Probanden im 3. Durchlauf 54 4.7 Das Verhalten der Insulinkonzentration Da ich die Ausreisser diskutiert und ersetzt habe, kann ich nun die Insulinkonzentration in meine Diskussion einbinden. 40.00 35.00 30.00 Insulin [mU/l] 25.00 Saccharose 20.00 Aspartam 15.00 Coke Zero 10.00 5.00 0.00 0 Zeit 30 0 min 60 90 Zeit [min] 20 min 120 Diagramm 15: Insulinkonzentration mit Standardabweichungen 30 min 60 min 90 min 120 min Saccharose 4.89 29.29 29.60 11.75 4.93 5.94 Maximum 15.47 57.45 82.26 23.49 15.85 15.09 Aspartam 3.21 3.43 3.65 4.08 3.49 3.76 Maximum 10.57 8.58 8.96 13.11 6.79 11.70 Coke Zero 5.45 7.13 6.97 4.89 6.27 7.27 Maximum 10.78 15.83 15.39 11.30 15.83 15.04 Minimum Standardabweichung Minimum Standardabweichung Minimum Standardabweichung 0.94 4.95 0.66 3.35 2.26 2.84 3.02 19.33 1.89 2.37 1.39 4.41 14.72 23.87 0.75 3.01 0.96 4.68 1.60 8.38 1.42 4.19 2.61 2.96 1.13 5.07 0.66 2.23 3.39 4.32 1.13 5.51 0.85 3.67 4.09 4.11 Tabelle 21: Mittelwerte, Minima, Maxima und Standardabweichung der Insulinkonzentration 55 Saccharose: Der Kurvenverlauf von Insulin stimmt mit dem des Blutzuckers überein. Leicht verzögert zum Blutzucker erreicht die Insulinkonzentration ihr Maximum 30 Minuten nach Einnahme der Saccharose-Wasser Lösung. Im Zeitraum zwischen 20 und 90 Minuten kann Insulin maximal wirken (in diesem Zeitraum wird der Blutzuckerspiegel gesenkt, indem die Glucose in die Zelle aufgenommen wird) und zugleich abgebaut werden. Aber auch das geschieht verzögert zum Blutzucker. Die Verzögerung der Insulinausschüttung-und Wirkung wird im folgenden Diagramm ersichtlich. Verspätete Insulinwirkung Blutzucker Insulin 0 Aspartam: 30 60 Zeit [min] 90 120 Diagramm 16: Die verzögerte Ausschüttung und Wirkung von Insulin Diese Kurve widerspricht der Annahme, dass trotz gleichbleibendem Blutzucker Insulin ausgeschüttet wird. Die Insulinkonzentration nach Einnahme der Aspartam-Wasser Lösung ist konstant und weisst keine Schwankungen auf. Blutzucker und Insulin stimmen also auch in diesem Fall überein. Weder die Blutzucker-noch die Insulinkonzentration verändern sich während diesen 120 Minuten. Somit unterstützt meine Messung die Hypothese, die besagt, dass ausschliesslich der ansteigende Blutzuckerspiegel die β-Zellen zur Insulinausschüttung veranlasst. Steigt der Blutzucker nicht, so wird auch kein Insulin ausgeschüttet. Laut meinen Messungen reicht die blosse Wahrnehmung eines süssen Geschmackes nicht aus, damit Insulin ausgeschüttet wird. Coke Zero: Die Insulinkonzentration im Blut nach Einnahme von Coca Cola Zero unterliegt seltsamen Schwankungen, die nicht mit dem Blutzuckergehalt korrelieren. Zuerst folgt eine Ausschüttung von Insulin ins Blut, obwohl der Blutzucker nicht ansteigt. Bei 60 Minuten knickt die Kurve ein und die niedrigste Insulinkonzentration wird erreicht. Von hier an steigt sie linear an. Obwohl es sich im Versuchsdurchlauf mit Aspartam und Coca Cola Zero um künstliche Süssstoffe handelt, sind die beiden Kurven sehr verschieden. Die Kurve von Aspartam ist strukturiert und nachvollziehbar, 56 während die Coca Cola Zero-Kurve Fragen aufwirft. Sie ist unstrukturiert, schlägt seltsam aus. Worin könnten die Gründe für diese seltsamen Schwankungen liegen? Erklärungsversuch #1 Eine Substanz im Coca Cola verstärkt den Rebound Effekt. Dadurch würde durch eine hormonelle Wirkung dieser Substanz die Glucagon- beziehungsweise Glucosekonzentration erhöht. Die erhöhte Glucosekonzentration würde wiederum die β-Zellen anregen, Insulin ins Blut zu schütten. Das würde den linearen Anstieg von Insulin ab 60 Minuten erklären. Jedoch würde sich in diesem Fall die Blutzuckerkonzentration zuerst erhöhen und danach wieder senken, was jedoch nicht im Ansatz geschieht! Die Blutzuckerkonzentration bleibt über die 120 Minuten konstant. Diese Erklärung ist also falsch. Erklärungsversuch #2 Coca Cola Zero ist ein homogenes Gemisch, bestehend aus drei verschiedenen Süssstoffen (Aspartam, Cyclamat und Acesulfam-K) und vieler anderer Substanzen, welche möglicherweise nicht deklariert sind. Würden wir alle Inhaltsstoffe und deren Anteil kennen, wissen wir noch immer nicht, wie unser Körper auf Zusatzstoffe wie Säuerungsmittel, Natriumcitrate und Aromen inklusive Koffein reagiert. Es wird vermutet, dass Koffein einen steigernden Einfluss auf den Blutzucker hat. Meine Messwerte widersprechen jedoch auch dieser Vermutung. Meine Annahme, dass Coca Cola Zero aufgrund des Süssstoffcocktails den Insulinspiegel stärker ansteigen lässt als isoliertes Aspartam, ist ebenfalls noch nicht geklärt. Trinkt man Coca Cola Zero, meint das Gehirn (Signal der Süss-Rezeptoren auf der Zunge) aufgrund des süssen Geschmackes, dass Kohlenhydrate in Form von Saccharose aufgenommen werden. Die Systemfunktionen im Körper, wie beispielsweise die Verdauung, bereiten sich auf die Verarbeitung der in Aussicht gestellten Stoffe vor. Der Proband weiss aber (kognitiv), dass Coca Cola Zero keinen Zucker enthält. In gewisser Weise stellt man dem Körper mit diesen künstlichen Süssstoffen ein Bein. Dem Körper wird Zucker signalisiert. Er bereitet sich vor, aber tatsächlich kommt kein Zucker. Als würde man am Bahnhof auf einen angekündigten Zug warten, welcher nicht kommt. Erklärungsversuch #3 Die verschiedenen Substanzen, die bekannten und auch die unbekannten, haben unterschiedliche Halbwerts-und Abbauzeiten. Sie verweilen also unterschiedlich lange im Körper und haben zu unterschiedlichen Zeitpunkten Einfluss auf den Körper bzw. auf die Insulinkonzentration. So kommt dieser Verlauf schlussendlich zustande. Die Wahrheit liegt wahrscheinlich in einer Kombination aus Erklärungsversuch #2 und Erklärungsversuch #3. Meine Messwerte unterstützen die Annahme, dass Coca Cola Zero bei übermässigem Verzehr ungesund sein kann. 57 Die Standardabweichungen der Insulinwerte verhalten sich ähnlich wie diejenigen der Blutzuckerkurve. Auch die Begründung ist wieder dieselbe. Die Variabilität zeigt sich erst, wenn der Körper reagieren und handeln muss. Mit Variabilität ist vor allem die Insulinsensitivität, sprich wie gut die Zellen auf Insulin ansprechen, gemeint. Aktivitätsgrad, Essverhalten und Veranlagung können diese beeinflussen. 4.8 Nahrungszufuhr, Appetit und Sättigung Weil die Nahrungsaufnahme, der Appetit und die Sättigung stark voneinander abhängig sind, will ich sie hier in einem Kapitel besprechen und miteinander in Verbindung bringen. 10000 9000 8000 Energie [kJ] 7000 6000 5000 4000 3000 2000 1000 0 Abend Snack Mittag Saccharose Aspartam Coke Zero 1197 2475 2686 3839 3281 3714 3161 2192 2917 Diagramm 17: Nahrungszufuhr 58 10.0 9.0 8.0 Sättigung 7.0 6.0 Saccharose 5.0 Aspartam Coke Zero 4.0 3.0 2.0 Appetit 1.0 0.0 vor nach 30 min 1h 2h 3h Saccharose: 4h Diagramm 18: Appetit und Sättigung Die 8400 Kilojoule (= 200 kcal) entsprechen der Referenzmenge für einen Erwachsenen. Aufgrund ihres gewöhnlichen Appetites vor dem Essen, assen sie weder zu viel noch zu wenig, sodass die Probanden unmittelbar nach dem Essen noch nicht satt waren. Das Sättigungsgefühl kam erst 30 Minuten nach dem Essen. Da zwischendurch ein kleiner Snack gegessen wurde, fühlten sich die Probanden den Tag über immer einigermassen satt und verspürten auch keinen Heisshunger. Wie zu erwarten war, nahm der Appetit im Verlauf des Tages wieder zu. Aspartam: Am Tag des zweiten Testdurchlaufes wurde mit Abstand am meisten gegessen. Vor dem Mittagessen ist der Appetit und das Sättigungsgefühl grösser als im ersten Testdurchlauf. Deshalb essen die Probanden gleichviel zu Mittag, sind danach jedoch satter und haben weniger Appetit. Auch das Abendessen ist beinahe gleich geblieben. Aber: Zwischendurch wurde deutlich mehr gegessen. Das erklärt auch, weshalb die Probanden am zweiten Versuchstag insgesamt satter waren, als im ersten Testdurchlauf. Wenn man ständig etwas isst, dann wird man nicht wirklich hungrig und bleibt satt. Dabei stellt sich die Frage, weshalb die Probanden zu einer erhöhten Nahrungsaufnahme neigten. Coca Cola Zero: Am letzten Versuchstag wurde am wenigsten gegessen. Vor dem Mittagessen war der Appetit am grössten. Das Mittagessen am 3. Versuchstag war das kleinste von allen, machte die Probanden aber am sattesten. Das Sättigungsgefühl war nicht, wie in den beiden ersten Durchläufen, erst nach 30 Minuten am grössten. Aber so schnell wie sie satt waren, wurden sie auch wieder hungrig. Das war auch zu erwarten, denn sie assen sehr wenig zu Mittag. Auch das Abendessen war im Vergleich 59 das kleinste von allen. Das kleine Mittag- und Abendessen wurde mit Snacks versucht zu kompensieren. Die Probanden hatten Heisshunger. Saccharose Aspartam Coca Cola Zero 8400 kJ entsprechen als normal. weniger als normal Nahrungsaufnahme Normales Niveau. der Referenzmenge 9351 kJ. Man isst mehr 7794 kJ.Man isst eines durchschnittlichen Appetit vor dem Essen Erwachsenen Gewöhnlich, dem Körper wurden nur „natürliche“ Stoffe zugeführt Sättigung nach dem Steigend Essen Grösser als bei Am grössten Nahe des grössten Am sattesten. Saccharose Sättigungsgefühls Sättigungsgefühl von allen drei Durchgängen. Sättigung nach 30 Am sattesten Veränderung im Appetit und Sättigung verhalten sich sehr ähnlich, Der Appetit nimmt Probanden länger satt und haben weniger Das Sättigungsgefühl min Tagesverlauf Am sattesten Grösstes abgesehen vom Niveau. Nach Aspartam sind die Appetit. Sinkend schneller wieder zu. lässt sehr schnell wieder nach. Vermutung: Durch die Zufuhr eines Gemisches vieler chemischer und körperfremder Substanzen verwirren wir unseren Körper. Aspartam in isolierter Form scheint in Anbetracht meiner Messwerte weniger schädlich zu sein. 60 5 AUSBLICK Ich konnte mit meiner Feldarbeit vieles in Erfahrung bringen und Aussagen und Vermutungen in Frage stellen. Dennoch basieren meine Resultate auf den Messwerten von 7 Probanden, was nicht gerade viel ist. Um statistisch relevante Aussagen machen zu können, müsste ich auf diesem Gebiet weiterforschen und weitere Versuche durchführen. Ein paar Ideen: Eine grössere Probandengruppe Den Probanden vorschreiben, was sie essen dürfen. So bleibt die Kalorienzahl immer Andere Testflüssigkeiten beziehungsweise die verabreichte Menge Süssstoff variieren konstant. Wie verhalten sich in diesem Fall Appetit und Sättigungsgefühl? 6 DANK An erster Stelle möchte ich mich bei den Probanden bedanken, welche sich freiwillig bereit erklärt haben, bei meinem Versuch mitzumachen. Ich bin sehr dankbar für ihre Kooperation und Mitarbeit. Ein weiterer Dank geht an meine Betreuungsperson, Raphael Riederer. Er konnte mir immer wieder weiterhelfen, brachte mich auf neue Gedanken und stand stets hinter mir. Die Tatsache, dass wir uns nicht immer einig waren und verschiedene Ansichten und Ideen hatten, liess uns interessante und anregende Diskussionen führen. Grossen Dank schulde ich dem endokrinologischen Labor der Universität Zürich. Damit sind vor allem Frau Dr. Maren Dietrich und Herr Dr. Richard Züllig gemeint. Ich durfte in ihrem Labor meine Insulin ELISA durchführen. Erst als ich die Messungen durchgeführt habe, merkte ich, dass es beinahe unmöglich gewesen wäre, den Nachweis von Insulin mittels ELISA an der Schule durchzuführen. Dazu kommt noch, dass Frau Dietrich und Herr Züllig vor lauter guten Ideen sprudelten und mir enorm helfen konnten. Sie haben mir alle Fragen beantworten können, und ich durfte sie immer kontaktieren. Ein besonderer Dank gebührt auch mein Vater, Paul Wieler. Er hatte immer sehr gute Einwände und konnte mir immer wieder aufs Neue helfen. Aber auch denjenigen, die jetzt ungenannt geblieben sind, sei an dieser Stelle ein Dankeschön gesagt. Ich war enorm froh, dass mir so viele Leute zur Seite standen. Ohne euch wäre das Ganze nicht möglich gewesen! 61 7 GLOSSAR23 Aminosäure Carbonsäure, die neben der funktionellen Carboxylgruppe (-COOH) die funktionelle Gruppe den Amine (-NH2) enthält. Diese Aminosäuren liegen in der Zelle in freier Form als Bausteine für Proteine (wie bspw. Insulin) vor. Carrier-Proteine Auch Transportproteine oder Carrier genannt; sind Proteine, die in die Membran eingelagert sind und spezifischen Substanzen den Durchtritt durch die Membran ermöglichen. Sie können die Substanz auch entgegen ihres Konzentrationsgefälles transportieren. Chromosom Ein Chromosom ist ein DNA-Doppelstrang, der die Erbinformation eines Individuums enthält. Ein Chromosomenabschnitt wird als Gen bezeichnet. Jedes Gen hat eine andere Erbinformation codiert. Die Zellen des menschlichen Körpers sind diploid, was bedeutet, dass in jedem Zellkern jedes Chromosom zweimal vorhanden ist. Depolarisation Im Ruhezustand, wenn ein Neuron keine Signale weiterleiten muss, ist dessen Membran nicht neutral geladen. Es herrsch eine Spannung von -70 mV über der Membran (negativer Ladungsüberschuss im Innern des Neurons). Strömen positive Ladungen (K+, Na+ oder Ca2+) durch Kanäle ins Innere, dann wird die Ungleichverteilung der Ladungsträger ausgeglichen. Die Depolarisation der Membran beschreibt den Vorgang, in dem das Membranpotenzial eines Neurons positiver wird. Endoplasmatisches Reticulum (ER) Ein Zellorganell, das aus einem Membransystem besteht und das bei der Synthese, der Umwandlung und beim Transport von Stoffen eine zentrale Rolle spielt. Exocytose Eine Art des Stofftransports aus der Zelle. Dabei verschmelzen Vesikel mit der Zellmembran, wodurch deren Inhalt ins Zelläussere gerät. Genexpression Vorgang der Merkmalsausbildung, indem die Zelle die Information eines Genes nutzt. Um Proteine (wie bspw. Insulin) herzustellen, muss zuerst das Gen in eine mRNA transkribiert werden (Transkription). Diese mRNA codiert nun die Aminosäurensequenz (Abfolge der Aminosäuren) für das zu produzierende Protein. Die mRNA kann an den Ribosomen gelesen und in die Aminosäurensequenz übersetzt werden (Translation). Prof. Dr. Jürgen Markl et. al. (Klett 2010), Klett Markl Biologie 1. Auflage, S. 483-500 & www.wikipedia.com & flexikon. doccheck.com 23 62 Golgi-Apparat Zellorganell, welcher aus einem Stapel Membranvesikel besteht. Spielt vor allem beim Transport von Substanzen eine wichtige Rolle. Die Substanzen werden vom Golgi-Apparat in Vesikel verpackt, wodurch sie mittels Exocytose aus der Zelle transportiert werden können. Kinase Enzyme, die einen Phosphatrest eines ATP-Moleküls auf andere Substrate übertragen kann. So laufen die Phosphorylierungen in den meisten Fällen. Membranpotenzial Damit ist die Ladung gemeint, die über der Membran liegt. Sie entsteht durch eine Ungleichverteilung von Ladungsträgern zwischen dem Innern und Äusseren der Zelle. mRNA „messenger RNA“; Die im Zellkörper in Form von DNA enthaltene Informationen können gelesen und benutzt werden. Dafür wird ein Gen (DNA) abgelesen und in eine andere „Sprache" übersetzt. So entsteht die mRNA, die dann an den Ribosomen gelesen werden kann. Ribosomen Proteinkomplex, an dem die Translation der mRNA stattfindet. Sie befinden sich auf der Oberfläche des ER. Synapse Verbindungsstelle von zwei Neuronen. Hier wird das Signal von der Präsynapse auf die Postsynapse übertragen. Transkription Dieser Vorgang beschreibt die Übersetzung der DNA in eine mRNA im Zellkern. Translation Synthese einer Aminosäurenkette. Die mRNA kann an den Ribosomen in die Aminosäurensequenz übersetzt werden. Translokation Ortsveränderung von Genen innerhalb eines Chromosoms. 63 8 QUELLENVERZEICHNIS 8.1 Literatur Prof. Dr. Jürgen Markl et. al. (Klett 2010), Klett Markl Biologie, 1. Auflage Florian Horn et. al. (Thieme 2012), Biochemie des Menschen: Das Lehrbuch für das Medizinstudium 5. Auflage, Gertrud Rehner et. al. (Spektrum Akademischer Verlag, 2010), Biochemie der Ernährung 3. Auflage, Stephen D. Anton et. al. (Elsevier, 2010), Effects of Stevia, Aspartame and Sucrose on food intake, satiety and postprandial glucose an insulin levels Christine Knopf (Diplomarbeit, 2000), Beziehung zwischen Struktur und Geschmack bei Aspartam und seinen Analogen HC. Pape et. al. (Thieme, 2014), Physiologie, 7. Auflage M. R. Weihrauch (Review, 2004), Artificial sweeteners – do they bear a carcinogenic risk? Mercodia Insulin ELISA Gebrauchsinformationen 8.2 Internet www.roche.com (Biochemical Pathways) www.wikibooks.org/wiki/Statistik:_Tabelle_der_Chi-Quadrat-Verteilung www.ncbi.nlm.nih.gov (National Center for Biotechnology Information) www.wikipedia.com flexikon.doccheck.com 9 ABBILDUNGS-UND TABELLENVERZEICHNIS 9.1 Diagramme Diagramm 1: Veranschaulichung der Ähnlichkeit der einzelnen Kurvenverläufe von Sättigung und Appetit ................................................................................................................................................. 29 Diagramm 2: Die verwertbaren Kurven von Appetit und Sättigung ................................................... 30 Diagramm 3: Kalibratorkurve .............................................................................................................. 37 Diagramm 4: Durchschnittlicher Blutzuckerspiegel aller Probanden .................................................. 38 Diagramm 5: Durchschnittliche Insulinkonzentration aller Probanden .............................................. 40 Diagramm 6: Durchschnittliche Nahrungszufuhr in Kilojoule aller Probanden................................... 41 Diagramm 7: Durchschnittlicher Appetit aller Probanden im Tagesverlauf........................................ 42 Diagramm 8: Durchschnittliches Sättigungsgefühl aller Probanden im Tagesverlauf inkl. Standardabweichungen ....................................................................................................................... 44 64 Diagramm 9: Korrigierte Insulinkurve Diagramm 10: Ursprüngliche Insulinkurve .......................... 50 Diagramm 11:Blutzuckerspiegel mit Standardabweichung ................................................................ 50 Diagramm 12: Blutzucker der einzelnen Probanden im 1. Durchlauf ................................................. 53 Diagramm 13: Blutzucker der einzelnen Probanden im 2. Durchlauf ................................................. 54 Diagramm 14: Blutzucker der einzelnen Probanden im 3. Durchlauf ................................................. 54 Diagramm 15: Insulinkonzentration mit Standardabweichungen ...................................................... 55 Diagramm 16: Die verzögerte Ausschüttung und Wirkung von Insulin .............................................. 56 Diagramm 17: Nahrungszufuhr ........................................................................................................... 58 Diagramm 18: Appetit und Sättigung .................................................................................................. 59 9.2 Tabellen Tabelle 1: Kategorisierung süssender Stoffe ....................................................................................... 25 Tabelle 2: ELISA zusammengefasst ...................................................................................................... 32 Tabelle 3: Inhalte des Mercodia Insulin ELISA Kit ................................................................................ 33 Tabelle 4: Kreuzreaktionen .................................................................................................................. 34 Tabelle 5: Angaben zu den Probanden ................................................................................................ 38 Tabelle 6: Durchschnittlicher Blutzuckerspiegel und Standardabweichungen (STABW) .................... 39 Tabelle 7: Durchschnittliche Insulinkonzentrationen und Standardabweichungen (STABW) ........... 40 Tabelle 8: Durchschnittliche Standardabweichungen beim Appetit ................................................... 42 Tabelle 9: Fläche unter den Appetitkurven ......................................................................................... 43 Tabelle 10: Durchschnittliche Standardabweichungen beim Sättigungsgefühl .................................. 44 Tabelle 11: Flächen unter den Sättigungskurven ................................................................................ 45 Tabelle 12: Homeostatic Model Assessment....................................................................................... 47 Tabelle 13: Korrelationskoeffizienten.................................................................................................. 48 Tabelle 14: Blutzucker und Insulin von Proband 1 im ersten Testdurchlauf ...................................... 48 Tabelle 15: Literaturwerte Insulinkonzentration nach künstlichen Zuckerersatzstoffen ................... 49 Tabelle 16: Chi Quadrat Test Proband 7 .............................................................................................. 49 Tabelle 17: Chi Quadrat Verteilung für den Freiheitsgrad 6................................................................ 49 Tabelle 18: Mittelwerte, Minima, Maxima und Standardabweichung der Blutzuckerkonzentration 51 Tabelle 19: Nährwerte von Assugrin Gold (Süssstoff Aspartam)......................................................... 52 Tabelle 20: Nährwerte von Coca Cola Zero ......................................................................................... 52 Tabelle 21: Mittelwerte, Minima, Maxima und Standardabweichung der Insulinkonzentration ....... 55 65 9.3 Abbildungen Abbildung 1: Die Glykolyse vereinfacht dargestellt. Ein schwarzer Punkt ist stellvertretend für ein Kohlenstoffatom. ................................................................................................................................... 8 Abbildung 2: Mitochindrium .................................................................................................................. 9 Abbildung 3: Glykolyse und Milchsäuregärung ................................................................................... 12 Abbildung 4: Drei verschiedene Einstiegsmöglichkeiten für die Gluconeogenese5 ............................ 13 Abbildung 5: Das Polysaccharid Glykogen ........................................................................................... 14 Abbildung 6: Ein Triacylglycerin aus einem Glycerinkopf und drei Fettsäuren ................................... 15 Abbildung 7: Biosynthese des Insulins................................................................................................. 17 Abbildung 8: Auslösen der Insulinsekretion durch Glucose ................................................................ 18 Abbildung 9: Insulinrezeptor und Signalweiterleitung ........................................................................ 19 Abbildung 10: Der Blutzuckerverlauf früher und heute ...................................................................... 22 Abbildung 11: Die Geschmackspapille ................................................................................................. 26 Abbildung 12: Entstehung eines süssen Geschmackes ....................................................................... 27 Abbildung 13: Sättigungs-und Appetit-Scorecard ............................................................................... 29 Abbildung 14: Blutserum und Blutzellen durch Zentrifugation getrennt ............................................ 34 Abbildung 15: Auswaschen der Vertiefungen ..................................................................................... 35 Abbildung 16: Unterschiedlich starke Verfärbungen je nach Insulinkonzentration ........................... 36 66 10 ANHANG 10.1 Rohdaten und Messwerte 10.1.1 Blutzucker [mmol/l] Saccharose 0 20 30 60 90 120 4.5 4.9 Proband 1 4.8 6.3 4.7 3.9 3.8 Proband 3 5.4 7.7 7.2 5.6 5.6 Proband 2 Proband 4 Proband 5 Proband 6 Proband 7 4.6 5.6 5.5 4.9 5 6.9 8.2 8.2 4.8 7.7 9 7.8 4.5 9.4 8.1 3.6 5.4 6.4 4.1 5.2 4.8 4.3 4.7 5.6 4.4 5.2 5.8 4.7 5.4 5.8 Mean 5.11 7.79 6.57 4.89 4.76 5.17 Min 4.60 6.30 4.50 3.60 3.80 4.40 Standardabw Max Aspartam 0.38 5.6 0 1.00 9.4 20 1.86 9 30 1.03 6.4 60 0.66 5.6 120 4.8 4.7 4.9 4.7 4.6 5.1 4.9 Proband 3 5.6 5.6 5.6 5.3 5.2 Proband 4 Proband 5 Proband 6 Proband 7 4.9 5.9 5.5 5 5.3 4.8 6.2 5.4 5 5.3 4.3 6.2 5.7 5.2 5.8 4.7 5.4 5.6 4.9 5.7 5.8 90 Proband 1 Proband 2 0.54 5.2 4.9 4.8 5.7 5.1 5.3 5.4 5.1 5 5.7 Mean 5.30 5.29 5.34 5.24 5.07 5.19 Min 4.90 4.70 4.30 4.70 4.80 4.70 Standardabw Max 0.39 5.9 0.52 6.2 0.68 6.2 0.36 5.7 0.33 5.7 0.32 5.7 67 Coke Zero 0 20 30 60 90 120 4.5 5.1 Proband 1 5.1 5.2 4.7 5.1 5.4 Proband 3 5.8 5.9 5.7 5.7 5.5 Proband 2 Proband 4 4.8 6 Proband 5 5.5 Proband 7 5.6 Proband 6 5.6 4.9 6.2 5.6 5.6 5.6 4.9 6.2 5.8 5.4 5.8 5.2 5.8 5.6 5.6 5.6 5.9 5.5 5.4 5.3 5.1 5.7 6.5 5.3 5.5 5.6 Mean 5.49 5.57 5.50 5.51 5.36 5.54 Min 4.80 4.90 4.70 5.10 4.50 5.10 Standardabw Max 10.1.2 Insulin [mU/l] Saccharose 0.41 6 0 Proband 1 0.94 Proband 3 15.47 Proband 5 2.83 Proband 2 Proband 4 Proband 6 Proband 7 Mean Standardabw Min Max 0.43 6.2 20 0.94 15.47 90 6.5 120 5.57 1.13 57.45 82.26 23.49 15.85 11.23 17.45 19.06 3.58 3.30 26.60 4.95 60 5.9 0.48 7.64 2.17 4.89 30 5.8 0.42 19.81 50.00 6.32 6.2 0.26 3.02 3.68 2.83 0.54 12.36 23.77 31.79 29.29 19.33 3.02 57.45 17.26 24.43 14.72 2.83 17.17 1.60 31.23 10.47 23.87 8.38 29.60 14.72 82.26 11.75 1.60 23.49 1.79 2.08 1.13 4.53 4.93 5.07 1.13 15.85 1.51 15.09 1.70 7.64 5.94 5.51 1.13 15.09 68 Aspartam 0 20 30 60 90 120 Proband 1 1.23 2.17 1.51 1.89 1.51 1.79 Proband 3 10.57 8.58 8.96 13.11 6.79 11.70 Proband 5 2.26 2.26 2.08 2.55 3.30 Proband 2 Proband 4 Proband 6 Proband 7 Mean Standardabw Min Max CokeZero 0.66 2.08 2.55 3.11 3.21 3.35 0.66 10.57 0 2.36 3.58 1.98 1.89 3.43 3.43 2.37 1.89 8.58 20 2.08 6.60 0.75 3.40 3.65 3.01 0.75 Proband 3 10.78 15.83 10.43 Proband 5 5.74 5.22 6.7 Proband 6 Proband 7 Mean Standardabw Min Max 3.22 5.91 6.61 5.45 2.84 2.26 10.78 8.43 5.74 4.68 6.97 0.96 15.39 2.64 0.66 5.19 3.49 2.23 0.66 1.51 3.58 0.85 3.58 3.76 3.67 0.85 6.79 11.70 90 120 5.39 7.13 11.3 15.83 15.04 4.43 6.09 4.09 4.61 4.7 5.09 3.3 4.35 4.41 15.83 1.42 3.04 15.39 1.39 4.19 0.96 6.43 7.13 4.08 60 6.26 Proband 4 3.40 30 6.87 1.39 1.60 13.11 2.26 3.65 1.42 8.96 Proband 1 Proband 2 5.09 4.96 2.61 4.89 2.96 2.61 11.30 3.39 3.91 4.09 4.26 4.78 5.04 5.22 10.52 4.32 4.11 6.27 3.39 15.83 7.27 4.09 15.04 69 10.1.3 Nahrungszufuhr [kJ] Saccharose Proband 1 Proband 2 Proband 3 Proband 4 Proband 5 Proband 6 Proband 7 Aspartam Proband 1 Proband 2 Proband 3 Proband 4 Proband 5 Proband 6 Proband 7 Coke Zero Proband 1 Proband 2 Proband 3 Proband 4 Proband 5 Proband 6 Proband 7 Mittag 1549 Snack 3182 1465 712 3182 712 4815 0 5715 4187 2638 1302 1884 Mittag 1926 0 Snack 3350 3350 2428 837 12770 2449 4334 4354 4200 Abend 837 14257 8140 Insgesamt 3601 4187 11849 1256 628 2805 1424 2303 419 1424 2307 9689 3819 1097 4702 7955 11640 2219 2805 7244 8374 1306 1675 3350 7034 837 703 Snack 3140 4438 2470 11472 Mittag 1424 Insgesamt 703 3362 6406 Abend 4124 2470 1256 6406 Abend 1047 1507 1507 2931 6523 6523 16091 9932 Insgesamt 3350 5736 5736 5652 2521 14516 2202 7118 3626 12452 70