Kein Folientitel - Münchner Wissenschaftstage
Werbung
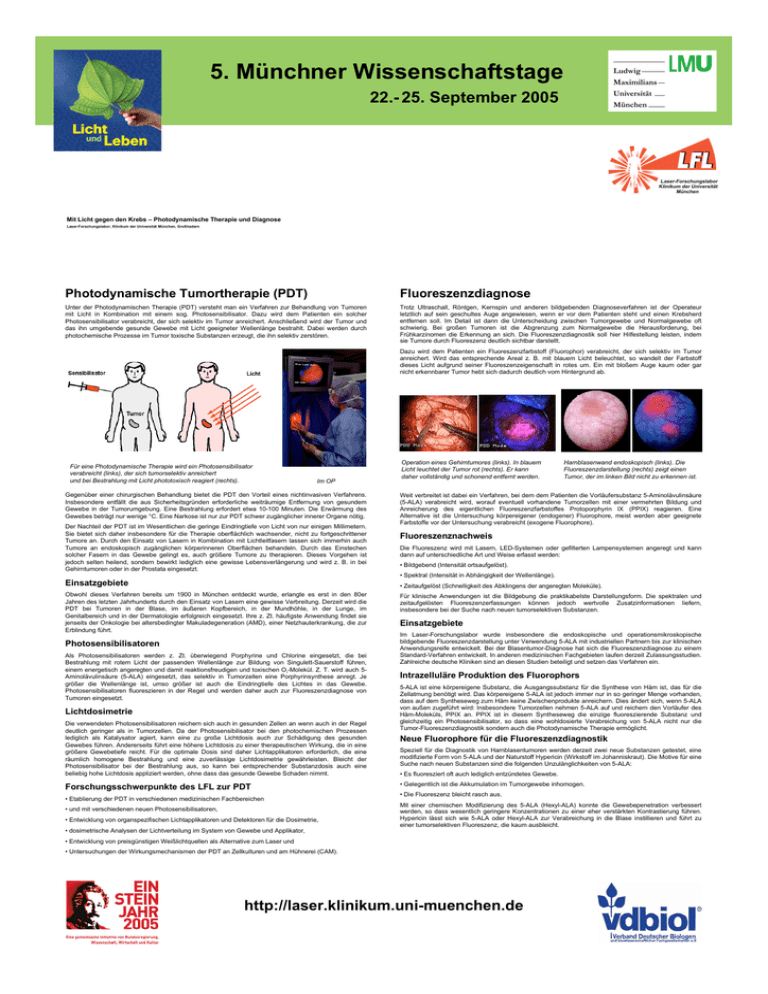
5. Münchner Wissenschaftstage 22.- 25. September 2005 Mit Licht gegen den Krebs – Photodynamische Therapie und Diagnose Laser-Forschungslabor, Klinikum der Universität München, Großhadern Photodynamische Tumortherapie (PDT) Fluoreszenzdiagnose Unter der Photodynamischen Therapie (PDT) versteht man ein Verfahren zur Behandlung von Tumoren mit Licht in Kombination mit einem sog. Photosensibilisator. Dazu wird dem Patienten ein solcher Photosensibilisator verabreicht, der sich selektiv im Tumor anreichert. Anschließend wird der Tumor und das ihn umgebende gesunde Gewebe mit Licht geeigneter Wellenlänge bestrahlt. Dabei werden durch photochemische Prozesse im Tumor toxische Substanzen erzeugt, die ihn selektiv zerstören. Trotz Ultraschall, Röntgen, Kernspin und anderen bildgebenden Diagnoseverfahren ist der Operateur letztlich auf sein geschultes Auge angewiesen, wenn er vor dem Patienten steht und einen Krebsherd entfernen soll. Im Detail ist dann die Unterscheidung zwischen Tumorgewebe und Normalgewebe oft schwierig. Bei großen Tumoren ist die Abgrenzung zum Normalgewebe die Herausforderung, bei Frühkarzinomen die Erkennung an sich. Die Fluoreszenzdiagnostik soll hier Hilfestellung leisten, indem sie Tumore durch Fluoreszenz deutlich sichtbar darstellt. Dazu wird dem Patienten ein Fluoreszenzfarbstoff (Fluorophor) verabreicht, der sich selektiv im Tumor anreichert. Wird das entsprechende Areal z. B. mit blauem Licht beleuchtet, so wandelt der Farbstoff dieses Licht aufgrund seiner Fluoreszenzeigenschaft in rotes um. Ein mit bloßem Auge kaum oder gar nicht erkennbarer Tumor hebt sich dadurch deutlich vom Hintergrund ab. Für eine Photodynamische Therapie wird ein Photosensibilisator verabreicht (links), der sich tumorselektiv anreichert und bei Bestrahlung mit Licht phototoxisch reagiert (rechts). Im OP Gegenüber einer chirurgischen Behandlung bietet die PDT den Vorteil eines nichtinvasiven Verfahrens. Insbesondere entfällt die aus Sicherheitsgründen erforderliche weiträumige Entfernung von gesundem Gewebe in der Tumorumgebung. Eine Bestrahlung erfordert etwa 10-100 Minuten. Die Erwärmung des Gewebes beträgt nur wenige °C. Eine Narkose ist nur zur PDT schwer zugänglicher innerer Organe nötig. Der Nachteil der PDT ist im Wesentlichen die geringe Eindringtiefe von Licht von nur einigen Millimetern. Sie bietet sich daher insbesondere für die Therapie oberflächlich wachsender, nicht zu fortgeschrittener Tumore an. Durch den Einsatz von Lasern in Kombination mit Lichtleitfasern lassen sich immerhin auch Tumore an endoskopisch zugänglichen körperinneren Oberflächen behandeln. Durch das Einstechen solcher Fasern in das Gewebe gelingt es, auch größere Tumore zu therapieren. Dieses Vorgehen ist jedoch selten heilend, sondern bewirkt lediglich eine gewisse Lebensverlängerung und wird z. B. in bei Gehirntumoren oder in der Prostata eingesetzt. Einsatzgebiete Operation eines Gehirntumores (links). In blauem Licht leuchtet der Tumor rot (rechts). Er kann daher vollständig und schonend entfernt werden. Harnblasenwand endoskopisch (links). Die Fluoreszenzdarstellung (rechts) zeigt einen Tumor, der im linken Bild nicht zu erkennen ist. Weit verbreitet ist dabei ein Verfahren, bei dem dem Patienten die Vorläufersubstanz 5-Aminolävulinsäure (5-ALA) verabreicht wird, worauf eventuell vorhandene Tumorzellen mit einer vermehrten Bildung und Anreicherung des eigentlichen Fluoreszenzfarbstoffes Protoporphyrin IX (PPIX) reagieren. Eine Alternative ist die Untersuchung körpereigener (endogener) Fluorophore, meist werden aber geeignete Farbstoffe vor der Untersuchung verabreicht (exogene Fluorophore). Fluoreszenznachweis Die Fluoreszenz wird mit Lasern, LED-Systemen oder gefilterten Lampensystemen angeregt und kann dann auf unterschiedliche Art und Weise erfasst werden: • Bildgebend (Intensität ortsaufgelöst). • Spektral (Intensität in Abhängigkeit der Wellenlänge). • Zeitaufgelöst (Schnelligkeit des Abklingens der angeregten Moleküle). Obwohl dieses Verfahren bereits um 1900 in München entdeckt wurde, erlangte es erst in den 80er Jahren des letzten Jahrhunderts durch den Einsatz von Lasern eine gewisse Verbreitung. Derzeit wird die PDT bei Tumoren in der Blase, im äußeren Kopfbereich, in der Mundhöhle, in der Lunge, im Genitalbereich und in der Dermatologie erfolgreich eingesetzt. Ihre z. Zt. häufigste Anwendung findet sie jenseits der Onkologie bei altersbedingter Makuladegeneration (AMD), einer Netzhauterkrankung, die zur Erblindung führt. Photosensibilisatoren Als Photosensibilisatoren werden z. Zt. überwiegend Porphyrine und Chlorine eingesetzt, die bei Bestrahlung mit rotem Licht der passenden Wellenlänge zur Bildung von Singulett-Sauerstoff führen, einem energetisch angeregten und damit reaktionsfreudigen und toxischen O²-Molekül. Z. T. wird auch 5Aminolävulinsäure (5-ALA) eingesetzt, das selektiv in Tumorzellen eine Porphyrinsynthese anregt. Je größer die Wellenlänge ist, umso größer ist auch die Eindringtiefe des Lichtes in das Gewebe. Photosensibilisatoren fluoreszieren in der Regel und werden daher auch zur Fluoreszenzdiagnose von Tumoren eingesetzt. Lichtdosimetrie Die verwendeten Photosensibilisatoren reichern sich auch in gesunden Zellen an wenn auch in der Regel deutlich geringer als in Tumorzellen. Da der Photosensibilisator bei den photochemischen Prozessen lediglich als Katalysator agiert, kann eine zu große Lichtdosis auch zur Schädigung des gesunden Gewebes führen. Andererseits führt eine höhere Lichtdosis zu einer therapeutischen Wirkung, die in eine größere Gewebetiefe reicht. Für die optimale Dosis sind daher Lichtapplikatoren erforderlich, die eine räumlich homogene Bestrahlung und eine zuverlässige Lichtdosimetrie gewährleisten. Bleicht der Photosensibilisator bei der Bestrahlung aus, so kann bei entsprechender Substanzdosis auch eine beliebig hohe Lichtdosis appliziert werden, ohne dass das gesunde Gewebe Schaden nimmt. Forschungsschwerpunkte des LFL zur PDT • Etablierung der PDT in verschiedenen medizinischen Fachbereichen • und mit verschiedenen neuen Photosensibilisatoren, • Entwicklung von organspezifischen Lichtapplikatoren und Detektoren für die Dosimetrie, • dosimetrische Analysen der Lichtverteilung im System von Gewebe und Applikator, Für klinische Anwendungen ist die Bildgebung die praktikabelste Darstellungsform. Die spektralen und zeitaufgelösten Fluoreszenzerfassungen können jedoch wertvolle Zusatzinformationen liefern, insbesondere bei der Suche nach neuen tumorselektiven Substanzen. Einsatzgebiete Im Laser-Forschungslabor wurde insbesondere die endoskopische und operationsmikroskopische bildgebende Fluoreszenzdarstellung unter Verwendung 5-ALA mit industriellen Partnern bis zur klinischen Anwendungsreife entwickelt. Bei der Blasentumor-Diagnose hat sich die Fluoreszenzdiagnose zu einem Standard-Verfahren entwickelt. In anderen medizinischen Fachgebieten laufen derzeit Zulassungsstudien. Zahlreiche deutsche Kliniken sind an diesen Studien beteiligt und setzen das Verfahren ein. Intrazelluläre Produktion des Fluorophors 5-ALA ist eine körpereigene Substanz, die Ausgangssubstanz für die Synthese von Häm ist, das für die Zellatmung benötigt wird. Das körpereigene 5-ALA ist jedoch immer nur in so geringer Menge vorhanden, dass auf dem Syntheseweg zum Häm keine Zwischenprodukte anreichern. Dies ändert sich, wenn 5-ALA von außen zugeführt wird: Insbesondere Tumorzellen nehmen 5-ALA auf und reichern den Vorläufer des Häm-Moleküls, PPIX an. PPIX ist in diesem Syntheseweg die einzige fluoreszierende Substanz und gleichzeitig ein Photosensibilisator, so dass eine wohldosierte Verabreichung von 5-ALA nicht nur die Tumor-Fluoreszenzdiagnostik sondern auch die Photodynamische Therapie ermöglicht. Neue Fluorophore für die Fluoreszenzdiagnostik Speziell für die Diagnostik von Harnblasentumoren werden derzeit zwei neue Substanzen getestet, eine modifizierte Form von 5-ALA und der Naturstoff Hypericin (Wirkstoff im Johanniskraut). Die Motive für eine Suche nach neuen Substanzen sind die folgenden Unzulänglichkeiten von 5-ALA: • Es fluoresziert oft auch lediglich entzündetes Gewebe. • Gelegentlich ist die Akkumulation im Tumorgewebe inhomogen. • Die Fluoreszenz bleicht rasch aus. Mit einer chemischen Modifizierung des 5-ALA (Hexyl-ALA) konnte die Gewebepenetration verbessert werden, so dass wesentlich geringere Konzentrationen zu einer eher verstärkten Kontrastierung führen. Hypericin lässt sich wie 5-ALA oder Hexyl-ALA zur Verabreichung in die Blase instillieren und führt zu einer tumorselektiven Fluoreszenz, die kaum ausbleicht. • Entwicklung von preisgünstigen Weißlichtquellen als Alternative zum Laser und • Untersuchungen der Wirkungsmechanismen der PDT an Zellkulturen und am Hühnerei (CAM). http://laser.klinikum.uni-muenchen.de











