Thermodynamik 6 (Entropie)
Werbung

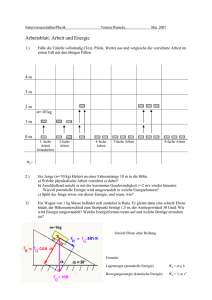
2.7 Entropie Irreversible Vorgänge: Der wohl grundlegendste Satz der Physik ist der Energieerhaltungssatz. Dieser besagt, dass Energie jeglicher Art in einem abgeschlossenen System niemals verbraucht werden kann. Energie wird lediglich in andere Energieformen umgewandelt. Trotzdem ist im Alltag häufig von „Energieverbrauch“ die Rede. Es wird zum Beispiel empfohlen, den „Energieverbrauch“ eines Haushalts zu senken um die Umwelt zu schonen. Was kann man sich nun unter dem Begriff Energieverbrauch vorstellen? Mit dem Begriff Energieverbrauch ist nicht der Verlust an Energie gemeint, sondern eine Entwertung der Energie während der Energieumwandlung. Energieverbrauch ~ Energieentwertung (umgangssprachlich) (physikalisch) Unter der Entwertung der Energie versteht man den Vorgang, bei dem Energie aus einer wertvollen Energieform in eine weniger wertvolle Energieform umgewandelt wird. Eine Energieform bezeichnet man als wertvoll, wenn sie in andere Energieformen umgewandelt werden kann, ohne dass zusätzlich Arbeit verrichtet werden muss. Beispiele: mechanische Energie (z.B. Lageenergie oder Spannenergie) chemische Energie (Energie in fossilen Brennstoffen) Kernenergie (Bindungsenergie der Nukleonen im Atomkern) Energie, die nicht ohne zusätzlich von außen verrichtete Arbeit in andere Energieformen umgewandelt werden kann, nennt man weniger wertvolle Energie. Beispiel: Thermische Energie (Wärme) Zur Verdeutlichung des Begriffs der Energieentwertung soll im Folgenden ein kleines Beispiel aus der Mechanik betrachtet werden. Setzt man einen Holzklotz auf den höchsten Punkt einer schiefen Ebene, so besitzt er dort Lage- bzw. potenzielle Energie. Ist der Neigungswinkel der Ebene groß genug, so kann der Klotz die Ebene © M. Brennscheidt hinuntergleiten. Falls nun die Oberfläche der schiefen Ebene sehr rau ist, rutscht der Klotz langsam mit gleichbleibender Geschwindigkeit die schiefe Ebene herab, bis er am tiefsten Punkt stehen bleibt. Die am Anfang zur Verfügung stehende Lageenergie ist bei diesem Vorgang scheinbar verloren gegangen. Bei genauerer Betrachtung ist jedoch festzustellen, dass sich die Ebene und der Holzklotz beim Herabrutschen leicht erwärmt haben. Die wertvolle potentielle Energie ist in Reibungswärme umgewandelt worden. Nach dem Energieerhaltungssatz wäre es nun kein Problem die thermische Energie der Ebene und des Klotzes zu nutzen, um den Holzklotz wieder die Ebene heraufzubefördern. Ein derartiger Vorgang kann jedoch in der Natur nicht beobachtet werden (Anschaulich gesprochen würde es der thermischen Energie niemals „einfallen“ sich in potentielle Energie zurück zu verwandeln). Vorgänge die selbstständig nur in einer Richtung ablaufen, werden irreversible Vorgänge genannt. Am obigen Beispiel wird nun auch deutlich, dass die Begriffe wertvolle und weniger wertvolle Energieform sinnvoll sind. So ist die weniger wertvolle Energieform „Wärme“ in der Regel das „Endprodukt“ einer Energieumwandlung und die wertvollen Energieformen wie mechanische oder chemische Energie das „Startprodukt“ eines irreversiblen Vorgangs. Irreversible, also nicht reversible Vorgänge findet man überall in der Physik. So wird ein einmal angestoßenes Faden- oder Federpendel niemals unendlich lange pendeln, sondern nach einer gewissen Zeit zur Ruhe kommen. Die mechanische Energie des Pendels wird schließlich in Wärmeenergie der Umgebungsluft oder des Pendels selbst umgewandelt. Dieser Vorgang ist nicht umkehrbar. Auch ein Autofahrer, der sein Auto mit einer gewissen kinetischen Energie vor einen Brückenpfeiler fährt kommt zu dem Schluss, dass soeben ein irreversibler Vorgang stattgefunden hat. Die kinetische Energie des Autos wurde in Verformungsenergie umgewandelt. Ein rückwärts Ablaufen dieses Vorgangs würde den Autofahrer zwar freuen ist aber leider physikalisch unmöglich. Auch in der Thermodynamik finden irreversible Vorgänge statt. Bringt man zum Beispiel zwei Körper mit unterschiedlicher Temperatur in Kontakt miteinander, so findet ein Temperaturausgleich zwischen den Körpern statt. Auch dieser Vorgang ist irreversibel. Die beiden Körper gehen niemals wieder in ihren Ausgangszustand zurück. © M. Brennscheidt Alle Beispiele zeigen: Es gibt nur eine Richtung des Ablaufs natürlicher Vorgänge. Mit zunehmender Zeit wird immer mehr Energie in thermische Energieformen umgewandelt. Erklärung von irreversiblen Vorgängen mit Hilfe der Wahrscheinlichkeitsrechnung: Die meisten Vorgänge in der Natur laufen irreversibel ab, dass heißt der Ablauf eines Vorgangs findet nur in einer Richtung statt. Der Grund hierfür ist nicht offensichtlich. Scheinbar ist es eine Eigenschaft der Natur bzw. des Universums, dass Vorgänge irreversibel ablaufen. Einen Erklärungsansatz für diese Eigenschaften liefert die Mathematik. Mit Hilfe der Wahrscheinlichkeitsrechnung soll nun folgender irreversibler Vorgang beschrieben werden: Ein Gas befindet sich in einem geschlossenen Behälter, der über ein Ventil mit einem zweiten luftleeren Behälter verbunden ist. Wird das Ventil geöffnet, so strömt ein Teil des Gases in den leeren Behälter. Nach kurzer Zweit befindet sich in beiden Behältern die gleiche Menge an Gas. Auch dieses Experiment zeigt einen irreversiblen Vorgang, der nur in einer Richtung abläuft. Das Gas würde sich niemals vollständig in den Anfangsbehälter zurückziehen. Um dies zu erklären betrachten wir nun zunächst einen Fall in dem sich nur ein einziges Gasatom im linken Behälter befinden soll. Wird das Ventil geöffnet, so kann sich das Gasatom in beiden Behältern frei bewegen. Die Wahrscheinlichkeit, das Teilchen im Ausgangsbehälter anzutreffen, liegt bei 50% bzw. ½. Fügt man ein zweites Gasatom hinzu, so beträgt die Wahrscheinlichkeit dafür, beide Atome im Ausgangsbehälter anzutreffen, 25% bzw. ¼. Bei drei Gasatomen beträgt die Wahrscheinlichkeit nur noch 1/8. Es wird also mit jedem hinzukommendem Atom unwahrscheinlicher die Gasteilchen gleichzeitig im Ausgangsbehälter anzutreffen. Anzahl der Teilchen im Gas © M. Brennscheidt Wahrscheinlichkeit, dass sich alle Gasteilchen wieder im Ausgangsvolumen befinden! Bei nur hundert Gasteilchen, also einer noch unvorstellbar geringen Menge an Gas, ist die Wahrscheinlichkeit bereits 1023 mal geringer als einen Sechser im Lotto zu tippen. Anzahl der Teilchen im Gas Wahrscheinlichkeit, dass sich alle Gasteilchen wieder im Ausgangsvolumen befinden! Gasteilchen Bei normalen Gasmengen in der Größenordnung eines Mols nähert sich die Wahrscheinlichkeit der Null. Es ist also im gewissen Sinne nicht physikalisch unmöglich, dass sich das Gas auf sein Ausgangsvolumen zurückzieht, sondern nur derart unwahrscheinlich, dass es in der Lebensdauer dieses Universums nicht eintreten wird. Hieraus kann folgender Satz geschlossen werden: Satz: Bei einem irreversiblen Prozess geht ein Zustand mit einer geringen Wahrscheinlichkeit in einen Zustand höherer Wahrscheinlichkeit über! Die Entropie: Der Begriff Energie ist einer der wichtigsten Begriffe der Physik. Die Betrachtung von irreversiblen Prozessen zeigt jedoch, dass dieser nicht ausreicht, um physikalische Vorgänge vollständig zu beschreiben. Es ist notwendig einen weiteren Begriff einzuführen, der auch den Richtungsaspekt bei physikalischen Vorgängen beinhaltet, die sog. Entropie. Der Begriff Entropie ist nicht so leicht verständlich wie der Energiebegriff und wird in der Regel im Physikstudium nur in Rahmen der theoretischen Physik als nicht besonders anschauliche physikalische Größe eingeführt. Aus diesem Grund wird hier der Entropiebegriff mit Hilfe eines Modells anschaulich erklärt. Auf die theoretische und mathematisch recht anspruchsvolle Herangehensweise möchte ich hier verzichten und weise den erfahrenen Leser auf Bücher zur Theoretische Thermodynamik hin (Torsten Fließbach- Lehrbuch zur theoretischen Physik IV). Zur Motivation zunächst ein Zitat von Ludwig Boltzmann: „Anschaulich ist das, woran man sich gewöhnt hat“ Betrachtet man zwei Körper mit unterschiedlicher Temperatur besteht zwischen ihnen die Temperaturdifferenz . © M. Brennscheidt und aber gleicher Masse, so Der Körper mit der höheren Temperatur hat mehr Wärme, also mehr thermische Energie gespeichert. Bringt man nun die beiden Körper in Kontakt miteinander, so gibt der Körper mit der höheren Temperatur die Wärmemenge an den kälteren Körper ab, bis ein Temperaturausgleich stattgefunden hat. Die Wärme ist gewissermaßen vom heißeren Körper auf den kälteren Körper „geflossen“. Dieser Vorgang funktioniert auch, wenn man die Körper nicht direkt miteinander in Kontakt bringt, sondern einen wärmeleitenden Körper zwischen sie bringt. Dabei gehen wir von einem sehr guten Wärmeleiter mit einer sehr geringen Wärmekapazität aus: Auch hier geht die thermische Energie Temperaturausgleich statt. vom heißen auf den warmen Körper über und es findet ein In einem letzten Schritt verbiegen wir nun noch den Wärmeleiter und ändern ein wenig die Form der Körper, sodass eine Analogie zu einem bereits bekannten physikalischen Sachverhalt auffällt: © M. Brennscheidt Wie man nun sieht, ist ein derartiges System ähnlich aufgebaut wie ein elektrischer Stromkreis. Die beiden Körper mit der Temperatur und entsprechen den Polen einer Stromquelle. Die Temperaturdifferenz entspricht im elektrischen Stromkreis der Spannung . Genau wie die Spannung den elektrischen Strom antreibt, so treibt die Temperaturdifferenz den Wärmestrom an. Dabei ist anzumerken, dass die Spannung auch als Potentialdifferenz angegeben werden kann: mit . Die elektrischen Potenziale und entsprechen hier den Temperaturen T1 und T2. Eine weitere Analogie ergibt sich zwischen thermischer Energie und elektrischer Energie .So wird in der obigen Anordnung die Wärmemenge transportiert und in der unteren Anordnung die elektrische Energie Die Formel für die elektrische Energie wird im Kapitel Elektrizitätslehre eingehend betrachtet Aus diesem Grund wir auf eine Herleitung an dieser Stelle verzichtet. bzw. Die elektrische Energie ergibt sich aus dem Produkt aus Spannung und der elektrischen Ladung . Dabei ist die Spannung gewissermaßen der Antrieb für die elektrischen Ladungsträger , die die elektrische Energie durch den Stromkreis transportieren. Da in der Wärmelehre genau wie in der Elektrizitätslehre Energie transportiert wird, kann eine analoge Formel für die thermische Energie aufgestellt werden. Dabei wird lediglich die Spannung (elektrische Potentialdifferenz) durch die Temperaturdifferenz ersetzt. © M. Brennscheidt Die Träger der elektrischen Energie, also die Ladungsträger werden hier durch die Träger der thermischen Energie ersetzt. Letztere bezeichnet man schließlich als Entropie . Durch Umformen der Gleichung ergibt sich für die Entropie die Formel: Auch wenn die Vorstellung der Entropie als Träger der thermischen Energie vergleichbar ist mit der Vorstellung von elektrischen Ladungen als Träger der elektrischen Energie, so sollte man sich die Entropie trotzdem nicht als Teilchen vorstellen. So fließen beim Transport von Wärmeenergie nicht wirklich mikroskopisch kleine Entropieteilchen. Genauso fließen beim Transport von elektrischer Energie nicht wirklich elektrische Ladungsträger vom Kraftwerk zur Steckdose. (Die Elektronen bewegen sich bei der Stromstärke von 1A nur mit einer verschwindend kleinen Geschwindigkeit von ca. 0,00734mm/s). Trotzdem besitzen beide Modellvorstellungen aus Anschauungsgründen eine gewisse Berechtigung und führen zu einem besseren Verständnis der eher abstrakten physikalischen Größen Ladung und Entropie. © M. Brennscheidt