Modul 8 - pdf.sharing
Werbung

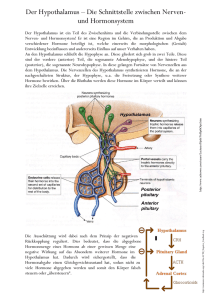
Modul 8 2 Insulintherapie 2 Physiologie 2 Diabetes 3 Therapie Typ I-Diabetes 3 Hypothalamus-und Hypophysenhormone 5 Allgemeiner Regelkreis 6 Schilddrüse und Schilddrüsenerkrankungen 6 Regelkreis 6 Bildung von Schilddrüsenhormonen 7 T3 und T4-Wirkung 7 Hypothyreose 8 Hyperthyreose 9 Sexualhormone 10 Regelkreis 10 GnRH und Gonadotropine 11 Androgene 12 Estradiol und Progesteron 12 Weitere Regelkreise 14 Nebennierenrinde 14 Wachstumshormone 15 Dopamin und Prolaktin 16 Neurohypophyse 16 Quellenangaben: VL-Folien der Vorlesungsreihe „Allgemeine Pharmakologie und Toxikologie“ der Universität Mainz aufgezeichnete Videos der Vorlesungsreihe „Allgemeine Pharmakologie und Toxikologie“ der Universität Mainz, Plattform Ilkum 1 Modul 8 Insulintherapie Physiologie Insulin entsteht in den 𝛽-Zellen des Pankreas. Zunächst als Propräinsulin und wird nach dem Abspalten des Signalpeptids zu Proinsulin. Nachdem auch das C-Peptid abgetrennt wurde, liegt Insulin als Hexamer in Vesikeln gespeichert vor. Da auch das C-Peptid in diesen Vesikel gespeichert wird, ist die Bestimmung im Blut ein wichtiger diagnostischer Marker. Die Freisetzung von Insulin erfolgt abhängig vom Blutzucker: Glucose wird über den GLUT₂-Transporter aufgenommen, die 𝛽-Zelle betreibt Glykolyse und es entsteht letztendlich ATP. ATP-abhängige K⁺-Kanäle öffnen sich, es kommt zu einer Depolarisation der Zelle. Dadurch öffnen sich spannungsabhängige Ca²⁺-Kanäle und Calcium-getriggert kommt es zur Insulin-Freisetzung. Ein weiterer Mechanismus, der schon bei Nahrungsaufnahme einsetzt, ist die Wirkung von GLP₁. Nach Ausschüttung dieses Hormons aus dem Darm, bindet es ebenfalls an die Zellen und setzt über einen weiteren Weg Insulin frei (siehe Schema). Gleichzeitig regt es die Neubildung von Insulin an. Letztendlich ist auch dieser Prozess von Glucose abhängig, da cAMP aus ATP entsteht und dieses ausreichend vorhanden sein muss. Die Wirkung von Insulin in den Zielzellen entfaltet sich entweder schnell, durch den Einbau von GLUT₄, über den dann Glucose in die Zelle aufgenommen werden kann, oder durch genomische Effekte, die die Synthese bestimmter Enzyme steigen oder hemmen. Über Phosphorylierung und Dephosphorylierung kommt es zu Aktivierung oder Hemmung vorhandener Enzyme, um die Glucoseverwertung in den Zielzellen zu steuern. 2 Diabetes Typ I: Es besteht ein absoluter Insulinmangel. Die Ursachen liegen in der Regel in autoimmunologische Vorgängen. Typ II: Es dominiert eine Insulinresistenz. Später kann es auch zu einem Mangel kommen. In fast allen Fällen liegt gleichzeitig eine Adipositas vor. Die Gefahren einer Diabetes-Erkrankung sind zum einen die akute Erhöhung des Blutzuckers, die z.B. bei einem Typ-1-Diabetiker in ein „Coma diabeticum“ münden kann, zum anderen die Langzeitschäden an den Gefäßen (Makro- und Mikroangiopathie). Therapie Typ I-Diabetes Die Behandlung erfolgt immer mit Insulin. Die Zielwerte der Blutglukose liegen etwas höher, als bei gesunden Personen, um einen Kompromiss zwischen Blutzucker-Anpassung und der Vermeidung der Hypoglykämie zu finden. Zur Behandlung stehen unterschiedliche Insuline zur Verfügung, die sich hinsichtlich von Wirkeintritt und Wirkdauer unterscheiden. 1. Human-Insulin Dieses Insulin ist gentechnisch hergestellt und gleicht dem humanen Insulin. Es wird s.c. appliziert, kann aber im Notfall auch i.v. zugeführt werden. Da es auch als Hexamer vorliegt, muss es zunächst zerfallen. Es muss daher 20-30 Minuten vor dem Essen appliziert werden. Die Wirkdauer beträgt 4-6 Stunden, eine Gabe ist mehrfach täglich notwendig. 2. Verzögerungsinsulin Um eine mehrfache Gabe zu reduzieren auf 1-2x täglich, wurde ein Insulin entwickelt, welches als Suspension mit NPH (neutrales Protamin Hagedorn) vorliegt. Der Wirkeintritt ist erst nach 1-2 Stunden, dafür wirkt es 8-12 Stunden. 3. Insulinanaloga Hier hat man sich zu Nutze gemacht, das ein Austausch in der Aminosäuresequenz Auswirkungen auf Wirkeintritt und Wirkdauer haben. Der Austausch ist in der Regel namensgebend. Es sind die kinetischen Eigenschaften verändert. Kurz wirksam (WE: 0,25 h, WD: 2-3 h) • Insulin lispro • Insulin aspart • Insulin glulisin intermediär wirksam (WE: 1-2 h, WD: 20 h) • Insulin detemir lang wirksam (WE: 3-4 h, WD: 20-40 h) • Insulin glargin 3 Bei der Therapie unterscheidet man die konventionelle von der Basis-Bolus-Therapie. Die konventionelle Therapie ist indiziert bei Patienten, mit eingeschränkter Medikations-Compliance. Dabei wird morgens und abends eine definierte Menge Insulin gespritzt und ein genauer Ernährungsplan erstellt. Bei der Basis-Bolus-Therapie kann der Patient individuell auf Anforderungen reagieren (Sport, bestimmte Mahlzeiten). Man kombiniert hier langwirksames Insulin mit einem kurzwirksamen Wirkstoff vor der Nahrungsaufnahme. Der Bedarf kann anhand einer Faustregeln abgeschätzt werden: Basal: 0,7-1,0 IE/h Prandial:1,0-1,5 IE/10g Kohlenhydrate Zu einer Verstärkung des BZ-senkenden Effekts von Insulin kann es kommen bei: 𝛽-Blockern: Die Glykogenolyse ist gehemmt 𝞪-Blocker: Die Glykogenolyse ist ebenfalls gehemmt. ACE-Hemmer: Mechanismus unklar Zu einer Abschwächung des Insulineffektes kommt es bei Einnahme von: Glucokortikoiden: Steigerung der Gluconeogenese Schilddrüsenhomonen: Erhöhung der Insulinresistenz 𝛽-Sympathomimetika: Steigerung der Gykogenolyse 4 Hypothalamus-und Hypophysenhormone Aus dem Hypothalamus werden die sogenannten Releasing- und Inhibitinghormone freigesetzt. Bis auf Dopamin handelt sich bei allen Hormonen um Peptide, was eine orale Einnahme unmöglich macht. Die Hormone werden im Hypothalamus freigesetzt und gelangen über den Blutweg zum Hypophsenvorderlappen (Adenohypophyse). Hier werden dann die entsprechenden Hormone freigesetzt. Dabei handelt es sich um Proteine oder Glykoproteine. Aus dem Hypophysenhinterlappen, der Neurohypophyse, werden die Peptide ADH und Oxytocin freigesetzt. Die Hormone der Adenohypophyse sind sogenannte trope Hormone und wirken auf die jeweiligen peripheren Drüsen ein. Im Folgenden werden die einzelnen Regelkreise, Erkrankungen und Therapieansätze besprochen. 5 Allgemeiner Regelkreis Nach Freisetzung der Hormone aus dem Hypothalamus kommt es zu einer Freisetzung der tropen Hormone aus dem Hypophysenvorderlappen. Diese wirken dann auf das jeweilige Erfolgsorgang, welches wiederum Hormone produziert. Wichtig ist das negative Feedback. Die Hormone aus den Erfolgsorganen „drosseln“ die Hormonproduktion in Hypothalamus und Hypophyse, es werden dort dann weniger Releasinghormone und trope Hormone ausgeschüttet. Bei Funktionsstörungen teilt man den Regelkreis in Etagen ein. Bei einer Erkrankung des Erfolgsorgans spricht man von einer primären Störung, auf Höhe der Hypophyse von einer sekundären Erkrankung und bei Funktionsstörungen des Hypothalamus von einer tertiären Erkrankung. Schilddrüse und Schilddrüsenerkrankungen Regelkreis Aus dem Hypothalamus wird TRH freigesetzt. Dies stimuliert in der Hypophyse die Freisetzung von TSH. TSH wirkt direkt auf die Schilddrüse und stimuliert die Bildung und Freisetzung der Schilddrüsenhormone T3 und T4. TSH hat zudem eine trophische Funktion und bewirkt eine Vergrößerung der einzelnen Schilddrüsenzellen. T3 und T4 hemmen die Freisetzung von TRH und TSH. Zu diagnostischen Zwecken kann man einen sogenannten TRH-Stimulations-Test machen. Nach TRH-Gabe misst man den TSH-Spiegel. Bei einer massiven Freisetzung von TSH liegt dem vermutlich eine primäre Hypothyreose zu Grunde, da das negative Feedback der Schilddrüsenhormone fehlt. Eine seltenere Ursache wäre eine sekundäre Hyperthyreose, z.B. bei einem Tumor. Dabei wird generell zuviel TSH produziert. Wenn nach TRH-Gabe kaum ein Anstieg des TSH gemessen werden kann, handelt es sich entweder um eine sekundäre Hypothyreose (Hypophyseninsuffizienz) oder eine primäre Hyperthyreose, da das negative Feedback durch die erhöhten Schilddrüsenhormone für eine Verminderung der TSH-Ausschüttung sorgt. Diese sogenannte Etagen-Diagnostik ist auf alle Regelkreise anwendbar. Der TRH-Test hat diagnostisch eigentlich keine Bedeutung mehr. Da sich die meisten Erkrankungen auf die primäre Ebene, also die Schilddrüse, beziehen, misst man in der Regel nur noch die TSH-Konzentration und bei Bedarf die freien Schilddrüsenhormone. 6 Bildung von Schilddrüsenhormonen Die Schilddrüse nimmt über den Natrium-Iodid-Transporter das benötigte Iod auf. Über den sogenannten Pendrin-Transporter gelangt das Iod von der Follikelepithelzelle in das Kolliod. Dort wird Thyreoglobulin iodiert und mittels Peroxidase kommt es innerhalb des großen Moleküls zu Kopplung und die Schilddrüsenhormone entstehen. Noch sind sie gebunden an Thyreoglobulin. Mittels Endozytose gelangt dieses zurück in die Zelle und durch Proteolyse entstehen T3 (Liothyronin) und T4 (Levothyroxin). TSH hat auf alle diese Vorgänge einen Einfluss, der wichtigste ist der Einbau des NISTransporters in die Zellen. T3 und T4-Wirkung Nach der Abgabe der Schilddrüsenhormone ins Blut, werden diese an TBG (Thyroxinbindenes-Globulin) gebunden. In der Peripherie muss T4 zunächst dejodiert werden. T4 ist also die „Speicherform“, T3 die aktive Form. T3 bindet an nukleäre Transkriptionsfaktoren und führt zu einer gesteigerten Genexpression. Die Hauptwirkungen betreffen vor allem den Stoffwechsel und sind in folgender Tabelle aufgeführt: 7 Hypothyreose Bei einer Unterfunktion der Schilddrüse herrscht ein Mangel an Hormonen vor. Dies äußert sich in vielfältigen Symptomen, die sich durch die Wirkung der Schilddrüsenhormone erklären lassen. Gewichtszunahme, Kälteempfinden, Bradykardie, trockene Haut, Konzentrationsschwäche, Müdigkeit und Antriebsarmut sind einige der Symptome. Kommt es bereits beim Fetus zu einer Hypothyreose (Kretinismus), kann dies zu einer geistigen Retadierung führen. Die Ursache einer Hypothyreose ist meistens primär, betrifft also die Schilddrüse selbst. Gründe können z.B. ein Jodmangel sein, oder die Autoimmunerkrankung Morbus Hashimoto. Bei einem Jodmangel kommt es meistens zunächst zu einer euthyreoten Struma. Das Wachstum ist bedingt durch die vermehrte TSH-Freisetzung. Hält der Mangel länger an, kann dies letztlich in einer Unterfunktion enden. Bei einem Morbus Hashimoto kommt es durch Antikörper gegen die Schilddrüse zu einer chronischen Entzündung, Gewebe wird zerstört und die Schilddrüse produziert unzureichende Mengen an Hormonen. Medikamentöse Behandlung: Euthyreote Struma: Kaliumiodid Substitution des fehlenden Iods, senkt die Gefahr der Hypothyreose. Dosierung: 100-200ug/ d bei Kindern, 300-500 ug/d bei Erwachsenen. Kontraindiziert ist die Gabe bei Hyperthyreose und funktioneller Autonomie („heiße Knoten“). Hypothyreose: L-Thyroxin (T4) Substitution der fehlenden Schilddrüsenhormone. Man gibt die Speicherform T4, damit es nicht zu einem Peak von T3 kommt und damit zu Symptomen einer Überfunktion. Das eingenommen L-Thyroxin wird im Körper dejodiert und steht dann zur Verfügung. Das Medikament wird in der Regel eingeschlichen (Ausnahme ist das hypothyreote Koma, eine seltene Komplikation der Unterfunktion). Die Dosis wird durch regelmäßige Kontrolle des TSH-Spiegels festgelegt und erfordert nicht selten Fingerspitzengefühl. Je nach Restfunktion der Schilddrüse sind unterschiedliche Dosen erforderlich und reichen von 25 bis 300ug/d. Das Medikament muss morgens nüchtern, 30-60 Minuten vor dem Frühstück eingenommen werden. Relative Kontraindikationen sind kardiale Erkrankungen. 8 Hyperthyreose Zu einer Überfunktion kann es bspw. durch sogenannte heiße Knoten kommen, oder durch die Autoimmunerkrankung Morbus Basedow. Auch hier gibt es Antikörper gegen die Schilddüse. Diese bewirken allerdings keine Entzündung, sondern aktivieren den TSHRezeptor und die Synthese der Hormone wird gesteigert. Da es keine negative Rückkopplung gibt, leiden die Patienten an einer Überfunktion, die sich durch Tachykardie, vermehrtes Schwitzen, Gewichtsabnahme, Nervosität und Schlafstörungen äußern kann. Auch hier kommt es häufig zu einer Struma. Medikamentöse Behandlung: Thiamazol, Carbimazol Die Wirkstoffe drosseln die Bildung der Schilddrüsenhormone, indem sie die Peroxidase hemmen. Unerwünschte Wirkungen sind allergische Reaktionen, Hepatotoxizität und Agranulozytose. Bei einer thyreotoxischen Krise wird neben hochdosiertem Thiamazol auch Betablocker verabreicht und ggf. Glucokortikoide. Perchlorat: Wenn die Überfunktion jodinduziert ist, kann man mit diesem Wirkstoff die Jodaufnahme in die Schilddrüse einschränken und so die Produktion der Hormone hemmen. 9 Sexualhormone Regelkreis Der Hypothalamus schüttet pulsatil GnRH aus (etwa alle 2h), was die Freisetzung von FSH und LH aus dem Hypophysenvorderlappen stimuliert. Diese wirken auf die Gonaden. FSH: Follikelstimulierendes Hormon. Bewirkt bei der Frau die Reifung des Graafschen Follikes und damit die Synthese von Estradiol. Beim Mann wird die Gametogenese geregelt. LH: Luteinisierendes Hormon. Es bewirkt die Ovulation und Gelbkörpersynthse uund damit die Progesteronfreisetzung. Beim Mann wird die Synthese von Testosteron stimuliert. Eine Besonderheit ist das HCG, welches von der Placenta gebildet und als LH der Schwangerschaft bezeichnet wird. Auch in diesem Regelkreis gibt es ein negatives Feedback. Im Rahmen des weiblichen Zyklus kommt es hier allerdings zu einer Besonderheit. In der Mitte des Zyklus findet der Eisprung statt, der durch LH stimuliert wird. Damit dies auch von statten gehen kann, hat in der Mitte des Zyklus Estradiol einen positiven Rückkopplungseffekt. Dadurch wird die Hypophyse sensitiver für GnRH und setzt mehr LH frei. Es kommt zu Ovulation und damit zu Progesteronbildung. Die Sexualhormone, die in den Gonaden entstehen sind Estrogene, Gestagene und Androgene. Es handelt sich um Steroidhormone, die ausgehend von Cholesterin synthetisiert werden. Die Wirkung der Steroidhormone liegt in der Aktivierung von Transkriptionsfaktoren. Im Folgenden werden die unterschiedlichen therapeutischen Ansatzpunkte, die Sexualhormone betreffend, erläutert. 10 GnRH und Gonadotropine GnRH: Das Hormon des Hypothalamus hat verschiedene Einsatzgebiete. Man verabreicht es zum Beispiel bei Fertilitätsstörungen, bei denen zuwenig dieses Hormons gebildet wird, also hypothalamisch bedingt ist. Bei der exogenen Applikation muss die Gabe auch pulsatil erfolgen. Dies gelingt mittels computergesteuerter Infusion. Eine weitere Indikation ist der Hodenhochstand. Der Hodenabgang ist in der zweiten Phase androgenabhängig und deswegen unternimmt man einen Therapieversuch mit GnRH. Die Erfolgsquote liegt etwa bei 20%. Leuprorelin: Bei permanenter Gabe von GnRH kommt es zu einer Rezeptordownregulation. Da das Hormon nur eine kurze HWZ hat, nimmt man ein Analogon, z.B. Leuprorelin, welches 200x potenter ist und eine längere Halbwertszeit aufweist („Superagonist“). Durch die Gabe kommt es zunächst zu einem Anstieg der Sexualhormone, dann wird der Rezeptor für GnRH durch den Körper runter reguliert. Durch diese Downregulation werden keine Sexualhormone mehr gebildet, der Spiegel sinkt gegen Null. Dies kommt einer hormonellen Kastration gleich, die nach Absetzen des Wirkstoffes reversibel ist. Gewünscht ist dies bei der palliativen Therapie des Prostatakarzinoms. Das Karzinom wächst zumindest teilweise unter dem Einfluss von Testosteron. Bei der Frau ist z.B. die Endometriose eine Indikation. Um dem Anstieg der Sexualhormone zu Beginn (Flair-Phänomen) entgegenzuwirken, wird am Anfang der Therapie ein Antiantrogen parallel dazu gegeben. Cetrorelix: Den gleichen Effekt wie Leuprorelin erreicht man mit einem GnRH-Antagonist. Hier kommt es zu Beginn nicht zu einem Flair-Phänomen. Die Konsequenzen sind die Gleichen, der Spiegel der Sexualhormone sinkt. Indikation ist die In-vitro-Fertilisation, um den Eisprung zu kontrollieren. Bei der IVF wird der weibliche Zyklus imitiert. In den ersten beiden Wochen wird FSH gegeben, dann wird mittels LH, bzw HCG die Ovulation ausgelöst. Die Oozyten können dann entnommen und befruchtet werden. Damit dies funktioniert, wird die endogene Hormonproduktion ausgeschaltet. Dies erreicht man mit Cetrorelix. Gonadrotropine: Indikation sind wie oben bereits beschrieben die IVF und bei hypophysärer Sterilität. 11 Androgene Die Wirkung der Androgene umfasst geschlechtsspezifische Wirkungen wie z.B. Ausbildung der Geschlechtsorgane, Funktion der Geschlechtsdrüsen (Prostata und Samenblase) und die Reifung von Samenzellen. Geschlechtsunspezifische Wirkungen sind unter anderem die Stimulation der Hämatopoese und eine anabole Wirkung. Medikamentöse Einsatzgebiete: Androgen-Rezeptor-Agonisten Bei Hypogonadismus und aplastischer Anämie. Cyproteronacetat/Flutamid Androgen-Rezeptor-Antagonisten. Indikation ist das fortgeschrittene Prostata-Ca, um das Wachstum einzuschränken. Finasterid Anti-Androgen, bzw. 5a-Reduktase-Inhibitor. Wird eingesetzt bei der benignen Prostata-Hyperplasie. Diese tritt vermehrt auf, wenn zuviel Dihydrotestosteron vorliegt. Dieses wiederum entsteht aus Testosteron durch die 5a-Reduktase. Estradiol und Progesteron Auch Estrogene und Gestagene haben geschlechtsspezifische und unspezifischen Wirkungen. Zu den wichtigen geschlechtsspezifischen Wirkungen gehören die Regulation des Menstruationszyklus, Proliferation des Endometriums und Änderung des Zervikalsekrets. Durch das Zusammenspiel der Hormone wird der weibliche Zyklus reguliert. So hat Estradiol ein positives Feedback in der Mitte des Zyklus und es kommt zu einer vermehrten LHFreisetzung. Dies bewirkt die Ovulation und Gelbkörperreifung, welcher Progesteron produziert. 12 Medikamentöse Einsatzgebiete: Kontrazeptiva Bei den oralen Kontrazeptiva kommen in der Regel Ethinylestradiol und Levonorgestrel zum Einsatz. Die oral eingenommen Hormone hemmen die Freisetzung von LH und FSH und verhindern damit die Ovulation. Zudem wird der Zervixschleim schlecht penetrierbar für Spermien. In der Regel handelt es sich um Kombinationspräparate. Diese können als Einphasenpräparate eingenommen werden, die Dosis beider Hormone ist immer gleich. Bei den Zwei- und Dreistufenpräparaten ist die Dosis jeweils unterschiedlich und dem Zyklus angepasst. Die Wahl der Kontrazeptiva hängt von den individuellen Bedürfnissen der Patientinnen ab. Bei Wasserretention, Endometriose, Übelkeit und Mastopathie ist ein Gestagen-betontes Präparat zu bevorzugen. Bei Durchbruchsblutungen, Depressivität und mangelnder Lipido ein Estrogen-betontes. Weitere Kontrazeptiva sind der Nuva-Ring oder transdermale Systeme. Auch hier handelt es sich um Kombinationspräparate. Eine unerwünschte Wirkung der Kontrazeptiva ist ein gesteigertes Thromboserisiko. Dieses kommt vor allem zu Stande, weil es unter Östrogenen zu einer gesteigerten Synthese von Gerinnungsfaktoren kommt. Weitere Nebenwirkungen sind eine geringe Zunahme von Brust- und Zervixkarzinomen, eine herabgesetzte Glucosetoleranz, Hypertonie, Amenorrhoe und subjektive Beschwerden wie z.B. ein Lipidoverlust. Kontraindiziert sind sie z.B. bei kardialen Erkrankungen, Raucherinnen >30 Jahren, bei Lebererkrankungen und Gerinnungsstörungen. Niedrig dosierte Gestagen-Präparate („Mini-Pille“) funktionieren nicht über den FeedbackMechanismus, sondern ändern den Zervixschleim so, dass eine Befruchtung verhindert wird. Bei diesen Präparaten ist die Gefahr für Thrombosen sehr gering, allerdings ist ein genaues Einnahmeschema zu befolgen und die Sicherheit liegt unter dem von Kombinationspräparaten. Die „Pille danach“ ist ein hochdosiertes Levonogestrel-Präparat, die Wirkung ist letztendlich unklar. Man geht davon aus, dass die Ovulation und Nidation verhindert wird. Der Wirkstoff sollte innerhalb von 12h nach dem Geschlechtsverkehr eingenommen werden, spätestens jedoch nach 72h. 13 Progesteron-Rezeptor-Antagonisten Mifepriston Es kommt zu einer Kontraktion des Myometriums und einer Dilatation der Zervix. Indikation ist der Schwangerschaftsabbruch in den ersten sieben Wochen. Estrogen-Rezeptor-Antagonisten Fulvestrant Der Wirkstoff ist ein kompetitiver Antagonist am Estrogen-Rezeptor. Es kommt zu einer Hemmung der Estrogen-sensitiven Genexpression. Indikation ist das Östrogen-sensitive Mamma-Ca bei Frauen in der Postmenopause. Selektive Estrogen-Rezeptor-Modulatoren Diese Wirkstoffe wirken teils als Agonist, teils als Antagonist am Rezeptor. Tamoxifen: Ist im Brustgewebe ein Antagonist und im Knochen ein Agonist am Estrogen-Rezeptor. Es wird eingesetzt beim Mamma-Ca und senkt das Risiko für ein Rezidiv und gleichzeitig die Gefahr einer Osteoporose. Clomifen: Ist überwiegend ein Antagonist und wird zur Ovulationsauslösung eingesetzt. Aromatase-Inhibitoren Exemestan und Anastrozol. Blockieren die körpereigene Östrogen-Synthese. Indikation ist das estrogenabhängige Mamma-Ca. Weitere Regelkreise Nebennierenrinde Aus dem Hypothalamus wird CHR ausgeschüttet, dadurch wird die Freisetzung von ACTH stimuliert. Dieses wiederum bewirkt eine Synthese und Sekretionssteigerung von Glucocortikoiden in der Nebennierenrinde. Auch hier kann man mittels eines Tests Funktionsstörungen aufdecken. Der sogenannte CHR-Test ist klinisch zur Diagnostik eines Morbus Cushing durchaus relevant. Er dient dazu, die Ursache des Cushing zu finden. Kommt es nach CHR-Gabe zu einem massiven Anstieg des ACTH, liegt die Ursache zentral und ist z.B. die Folge eines ACTH-produzierenden Adenoms. Liegt die Ursache peripher, also im Bereich der Nebennierenrinde, kommt es durch das negative Feedback zu keiner erhöhten ACTH-Freisetzung. 14 Wachstumshormone Die Freisetzung des Growth Hormon aus dem Hypophysenvorderlappen unterliegt der Kontrolle von GHRH und Somatostatin aus dem Hypothalamus. GH wirkt direkt in der Peripherie und auf die Leber, wo IGF freigesetzt wird. Beide Hormone (GH und IGF) führen zu Wachstum von peripherem Gewebe. Die Sekretion von GH ist in den ersten vier Lebensjahren am größten, sowie während der Pubertät. Unter Hormoneinfluss wird Fett mobilisiert, Glucose bereit gestellt (nicht direkt verwertet) und die Proteinsynthese gesteigert. Es kommt zu Knochenwachstum , Knorpelaufbau und Muskelwachstum. Tiefer Schlaf bei Kindern fördert die Sekretion von GH. Ein Mangel an GH bewirkt einen hypophysären Minderwuchs, ein Überschuss im Kindesalter führt zu Riesenwuchs, bei Erwachsenen zu Akromegalie (z.b. durch ein GHproduzierendes Adenom). Therapiemöglichkeiten: GH (Somatotropin): Wird subkutan bei hypophysärem Minderwuchs verabreicht. Pegvisomant: Ein GH-Rezeptor-Antagonist. Indikation ist die Akromegalie. Der Wirkstoff wird subkutan verabreicht. Octreotid: Ein Somatostatin-Analogon. Indikation ist ebenfalls die Akromegalie. Es kann zudem bei endokrin aktiven Tumoren im GIT eingesetzt werden und das Tumorwachstum hemmen. Es bewirkt außerdem eine Vasokonstriktion von Gefäßen im Splanchnikusgebiet und kann zur Blutungsstillung eingesetzt werden. 15 Dopamin und Prolaktin Der Hypothalamus produziert PRH, welches wiederum die Prolaktinfreisetzung in der Adenohypophyse steigert, Dopamin hemmt die Freisetzung. Prolactin wird auf die Milchdrüsen, die Milchsekretion wird gesteigert. Durch das Saugen des Babys an der Brustwarze wird dieser Effekt verstärkt. Man ist sich nicht sicher, ob PRH eventuell Oxytocin oder TRH entspricht. Prolactin hemmt die pulsative Freisetzung von GnRH, was während der Stillzeit zu einem nicht 100%igem Schutz vor einer erneuten Schwangerschaft führt. Therapeutischer Ansatz: Bromocriptin: Es handelt sich um einen D2-Agonisten (Ergolin), die Prolactin-Freisetzung wird gehemmt. Indikationen ist zum Beispiel das Abstillen. Das Medikament wird allerdings nur in Ausnahmefällen eingesetzt, die Nebenwirkungen sind vielfältig. Neurohypophyse Oxytocin: Bewirkt Wehen und Milchfluss während der Stillzeit.Indikation zum therapeutischen Einsatz ist die Geburtseinleitung, Wehenschwäche und eine postpartale Uterusatonie mit der Gefahr von starken Blutungen. Atosiban: Oxytocin-Rezeptor-Antagonist. Wird eingesetzt zur Wehenhemmung bei drohender Frühgeburt. Vasopressin (ADH): Wird durch die Neurohypophyse bei sinkendem Volumen und steigender Osmolarität freigesetzt. Wirkt über die Rezeptoren V1 (Vasokonstriktion) und V2 (Wasserrückresorption). Desmopressin: Ein V2-Rezeptor-Agonist. Wird bei Diabetes insipidus centralis eingesetzt, bei welchem zu wenig Vasopressin produziert wird. Felypressin: Ein V1-Rezeptor-Agonist. Ist ein Vasokontriktorzusatz in Lokalanästhetika und kann bei Kontraindikation für Katecholamine gegeben werden. Eine fixe Kombination ist z.B. Prilocain mit Felypressin. 16