Synthese und Reaktivität von Phosphor-Kohlenstoff
Werbung

Synthese und Reaktivität von Phosphor-KohlenstoffKäfigverbindungen
Der Naturwissenschaftlichen Fakultät der Friedrich-Alexander-Universität
Erlangen-Nürnberg
zur
Erlangung des Doktorgrades Dr. rer. nat.
vorgelegt von
Lars Rohwer
aus Villingen-Schwenningen
Als Dissertation genehmigt von der Naturwissenschaftlichen Fakultät der
Universität Erlangen-Nürnberg
Tag der mündlichen Prüfung:
13.04.2012
Vorsitzender der Promotionskommission: Prof. Dr. Rainer Fink
Erstberichterstatter:
Prof. Dr. Ulrich Zenneck
Zweitberichterstatter:
Prof. Dr. Lutz Dahlenburg
2
"Ich sage euch: man muss noch Chaos in sich haben, um einen tanzenden Stern gebären zu
können. Ich sage euch: ihr habt noch Chaos in euch." - Zarathustras Vorrede
3
Die vorliegende Arbeit entstand in der Zeit von September 2004 bis Januar 2012 am
Department Chemie und Pharmazie der Friedrich-Alexander-Universität Erlangen-Nürnberg.
4
Meiner Familie
5
6
Danksagung
An dieser Stelle möchte ich mich auch bei all jenen herzlich bedanken, ohne deren Hilfe und
Unterstützung diese Arbeit nicht zustande gekommen wäre.
Besonders bedanken möchte ich mich bei meinem Doktorvater Prof. Dr. Ulrich Zenneck für
seine Unterstützung, sein Vertrauen, für die zahlreichen Konferenzteilnahmen und nicht
zuletzt für die beiden Segeltörns mit der gesamten Arbeitsgruppe. Außerdem möchte ich mich
dafür bedanken, dass er mir die Möglichkeit gegeben hat, mich neben der Promotion am
Institut der Anorganischen Chemie einzubringen und dort Verantwortung zu tragen.
Ein ebenso großer Dank gilt meinen Kolleginnen Christine Höhn und Irene Keller für die
hervorragende Zusammenarbeit und die zahllosen anregenden Diskussionen. Die gute
Zusammenarbeit innerhalb des herausfordernden Themengebiets unseres Projekts war eine
unschätzbare Hilfe für mich. Bei meiner langjährigen Kollegin Ilona Jipa, die einem anderen
Projekt zugeteilt war, möchte ich mich herzlichst bedanken für die stets von ihr ausgehende
gute Laune, die zum guten Klima im Arbeitskreis beigetragen hat und die umfassende
Verpflegung.
Ein herzliches Dankeschön geht auch an Prof. Dr. Dr. h.c. mult. Rudi van Eldik, der einen
Teil der Finanzierung der Arbeit übernommen hat, mir durch die richtigen Worte zur richtigen
Zeit Kraft gegeben und Mut gemacht hat und ein großes Vorbild für mich geworden ist.
Mein Dank gilt auch allen derzeitigen Mitgliedern des Arbeitskreises van Eldik, die mich gut
in ihrem Arbeitskreis aufgenommen haben, insbesondere Dr. Matthias Schmeißer, Dr.
Christoph Fertinger, Sabine Rothbart und Klaus Pokorny.
Ein ganz besonderes Dankeschön geht auch an Dr. Andreas Scheurer und Dr. Ralph Puchta,
die mir beide durch ihr umfassendes und vielfältiges Wissen der Chemie oftmals neue
Denkanstöße gegeben haben.
Besonders bedanken möchte ich mich auch bei Prof. Dr. Walter Bauer, der durch spezielle
NMR-Messungen wesentlich zum Verständnis der P–C-Käfige beigetragen hat.
Mein Dank gilt allen Mitarbeitern der Anorganischen Chemie, die Messungen für diese Arbeit
angefertigt haben: Martin Bachmüller, Christina Wronna, Dr. Frank Heinemann, Panagiotis
Bakatselos, Susanne Hoffmann, Oliver Tröppner und ganz besonders Dr. Achim Zahl und
Jochen Schmidt, die durch eine unüberschaubare Anzahl an
31
P-NMR-Routinemessungen
diese Arbeit erst ermöglicht haben.
Natürlich möchte ich mich auch bei meinen Eltern herzlich für die Unterstützung über viele
Jahre bedanken. Das hier ist zum großen Teil auch Euer Verdienst.
Danke, Steffi! Dein freudiges Wesen hat mir über einige Rückschläge bei dieser Arbeit
hinweggeholfen, deine tatkräftige Unterstützung hat viel zum erfolgreichen Abschluss der
Schreibarbeit beigetragen.
7
Konferenz-Teilnahmen
Poster:
• Chiral-at-Metal P-Tethered Arene Ruthenium(II) Complexes: Catalysts for Enantioselective
Transfer Hydrogenation, 2nd Erlangen Symposium on Redox-Active Metal Complexes –
Control of Reactivity via Molecular Architecture, Deutschland, Erlangen, 4.-7.10.2006.
• Asymmetric P–C Cage Compounds and Their Transition Metal Complex Chemistry,
6th European Workshop on Phosphorus Chemistry, Italien, Florenz, 26.-27.3.2009.
• Asymmetric P–C Cage Compounds and Their Transition Metal Complex Chemistry,
7th European Workshop on Phosphorus Chemistry, Ungarn, Budapest, 25.-26.3.2010.
• Asymmetric P–C Cage Compounds and Their Transition Metal Complex Chemistry,
3rd European Association for Chemical and Molecular Sciences Chemical Congress,
Deutschland, Nürnberg, 29.9.-2.9.2010.
• Cage-Chiral P–C-Compounds: A Novel Class of Self-Healing Chiral Ligands, 3rd Erlangen
Symposium on Redox-Active Metal Complexes: Control of Reactivity via Molecular
Architecture, Deutschland, Erlangen, 5.-8.10.2011.
Vorträge:
• Darstellung asymmetrischer Arenruthenium(II)-Henkelkomplexsalze aus Ruthenium(III)chlorid und ihr katalytisches Potential, Seminar des Graduiertenkollegs, Deutschland,
Veilbronn, 13.-14.11.2004.
• Chiral-at-Metal P-Tethered Arene Ruthenium(II) Complexes: Catalysts for Enantioselective
Transfer Hydrogenation, IXth Regional Seminar of PhD-Students on Organometallic and
Organophosphorous Chemistry, Polen, Szklarska Poręba, 10.-14.4.2005.
• Chiral-at-Metal Donor-Tethered Arene Ruthenium(II) Complexes: Catalysts for Enantioselective Hydrogenation, Xth International Seminar of PhD. Students on Organometallic and
Coordination Chmeistry, Tschechien, Medlov, 17.-22.2006.
8
Abkürzungsverzeichnis
CD
Circulardichroismus
COD
1,5-Cyclooctadien
D
Deuterium
d.e.
diastereomeric excess (Diastereomerenüberschuss)
DFT
Dichtefunktional-Theorie
DME
1,2-Dimethoxyethan
EA
Elementaranalyse
e.e.
enantiomeric excess (Enantiomerenüberschuss)
Et
Ethylrest
η
Haptizität
IR
Infrarot-Spektroskopie
L
Liter
M
molar, [mol L-1]; Zentralmetall
Me
Methylrest
mL
Milliliter
MS
Massenspektrometrie
NMR
nuclear magnetic resonance (Kernspinresonanz-Spektroskopie)
Ph
Phenylrest
RSA
Röntgenstrukturanalyse
RT
Raumtemperatur
T
Temperatur
tBu
tert-Butylrest
THF
Tetrahydrofuran
Bei NMR-, IR-, Massen-Spektren:
brs
breites Singulett
COSY
correlated spectroscopy (Korrelations NMR-Spektroskopie)
d
Dublett
δ
chemische Verschiebung
9
dd
Doppeldublett
DOSY
diffusion ordered spectroscopy (diffusionsaufgelöste NMRSpektroskopie)
dt
Dublett vom Triplett
ESI
Elektrospray Ionisation
EXSY
exchange spectroscopy (Austausch NMR-Spektroskopie)
FD
Felddesorptionsionisation
Hz
Hertz
n
Kopplungskonstante über n Bindungen [Hz]
J
m
Multiplett, mittlere Bandenintensität (im IR)
+
[M ]
Molekülion
m/z
Masse-Ladungs-Quotioent
ν
Valenzschwingung
ν
Wellenzahl [cm-1]
NOESY
nuclear overhauser effect spectroscopy (Kern-Overhauser-Effekt-NMRSpektroskopie)
ppm
parts per million
q
Quartett
s
Singulett, starke Bandenintensität (im IR)
sh
Bandenschulter
t
Triplett
TOF
time of flight
w
wenig intensive Bande
vs
sehr starke Bandenintensität
10
Inhaltsverzeichnis
1. Einleitung
15
1.1 1-Triorganylstannyl-1,3,4-triphosphol - Synthesebaustein des P5-
15
Deltacyclens
1.2 Synthese von P5-Deltacyclenen
19
1.3 Metallkomplexe von P–C-Käfigverbindungen
23
1.4 Ziel dieser Arbeit
30
2. Ergebnisse und Diskussion
2.1 Charakterisierung von P5-Deltacyclen 17a/b
32
32
2.2 Chrom-, Molybdän- und Wolframpentacarbonylkomplexe des P5Deltacyclens
43
2.2.1 Darstellung der Chrom-, Molybdän- und Wolframpentacarbonyl-P5deltacyclenkomplexe 44, 45 und 46
2.2.2 Molekülstruktur von Molybdänpentacarbonyl-P5-deltacyclen 45a
43
44
2.2.3 NMR-Spektroskopische Charakterisierung der Chrom-, Molybdän- und
Wolframpentacarbonyl-P5-deltacyclenkomplexe 44a-d, 45a-d und 46a-d
47
2.2.3.1 NMR-Spektroskopische Charakterisierung der Chrom-, Molybdänund Wolframpentacarbonyl-P5-deltacyclenkomplexe 44a, 45a und
46a
49
2.2.3.2 NMR-Spektroskopische Charakterisierung der Chrom-, Molybdänund Wolframpentacarbonyl-P5-deltacyclenkomplexe 44b, 45b und
46b
53
2.2.3.3 NMR-Spektroskopische Charakterisierung der Chrom-, Molybdänund Wolframpentacarbonyl-P5-deltacyclenkomplexe 44c/d, 45c/d
und 46c/d
56
2.2.4 13C-NMR-Spektroskopische Charakterisierung und IR-Spektren der
Chrom-, Molybdän- und Wolframpentacarbonyl-P5-deltacyclenkomplexe
44a-d, 45a-d und 46a-d
59
2.2.5 Vergleich der Chrom-, Molybdän- und Wolframpentacarbonyl-P5deltacyclenkomplexe 44a-d, 45a-d und 46a-d
61
11
2.2.6 Vergleich der Wolframpentacarbonylkäfigkomplexe 37, 39 und 46a-d
2.3 Ein (η6-Aren)ruthenium(II)-Komplexe des P5-Deltacyclens
2.3.1 Darstellung von [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II) 47
63
64
64
2.3.2 Molekülstruktur von [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II)
65
47
6
2.3.3 Spektroskopische Charakterisierung von [(η -Benzol)dichloro(P5-deltacyclen)ruthenium(II) 47
67
2.3.4 Zwei Enantiomerenreine [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II)-Komplexe 47’ und 47’’
71
2.4 Rhodium(III)-Käfigkomplexe des P5-Deltacyclens
73
2.4.1 Darstellung der Rhodium(III)-P5-deltacyclen-Zweikernkomplexe 48a und
48b
73
2.4.2 Molekülstruktur des Rhodium(III)-P5-deltacyclen-Zweikern-komplexes
48
74
2.4.3 NMR-Spektroskopische Charakterisierung der Rhodium(III)-P5deltacyclen-Zweikernkomplexe 48a und 48b
2.5 iso-P5-Deltacyclen
77
84
2.5.1 Darstellung von iso-P5-Deltacyclen 49a/b
84
2.5.2 NMR-Spektroskopische Charakterisierung von iso-P5-Deltacyclen 49a/b
86
2.6 Chrom-, Molybdän- und Wolframpentacarbonylkomplexe des iso-P5Deltacyclens
91
2.6.1 Darstellung der Chrom-, Molybdän- und Wolframpentacarbonyl-iso-P5deltacyclenkomplexe 42a/b, 50a/b und 43a/b
91
2.6.2 Molekülstruktur von Molybdänpentacarbonyl-iso-P5-deltacyclenkomplex
50a
92
2.6.3 Spektroskopische Charakterisierung der Chrom-, Molybdän- und
Wolframpentacarbonyl-iso-P5-deltacyclenkomplex 42a/b, 50a/b und
43a/b
95
2.7 P5-Homocunean
101
2.7.1 Darstellung von P5-Homocunean 51
101
2.7.2 Spektroskopische Charakterisierung von P5-Homocunean 51
103
2.8 Chrom-, Molybdän- und Wolframpentacarbonylkomplexe des P5-Homocuneans
12
106
2.8.1 Darstellung der Chrom-, Molybdän- und Wolframpentacarbonyl-P5106
homocuneankomplexe 52, 53 und 54
2.8.2 Molekülstruktur von Chrom-, Molybdän- und Wolframpentacarbonyl-P5-
107
homocunean 52, 53 und 54
2.8.3 Spektroskopische Charakterisierung der Chrom-, Molybdän- und
Wolframpentacarbonyl-P5-homocuneankomplexe 52, 53 und 54
111
3. Zusammenfassung
115
4. Experimenteller Teil
121
4.1 Materialien und Methoden
121
4.2 Beschreibung der Versuche
123
4.2.1 Synthese und Charakterisierung von P5-Deltacyclen 17a/b
123
4.2.2 Synthese der Chrom-, Molybdän- und Wolframpentacarbonyl-P5deltacyclenkomplexe 44a-d, 45a-d und 46a-d
124
4.2.2.1 Spektroskopische und analytische Daten der Chrompentacarbonyl-P5125
deltacyclenkomplexe 44a-d
4.2.2.2 Spektroskopische und analytische Daten der Molybdänpentacarbonyl-P5-deltacyclenkomplexe 45a-d
127
4.2.2.3 Spektroskopische und analytische Daten der Wolframpentacarbonyl128
P5-deltacyclenkomplexe 46a-d
6
4.2.3 Synthese und Charakterisierung von [(η -Benzol)dichloro(P5-deltacyclen)ruthenium(II) 47
130
4.2.4 Synthese und Charakterisierung der Rhodium(III)-P5-deltacyclenZweikernkomplexe 48a und 48b
4.2.5 Synthese und Charakterisierung von iso-P5-Deltacyclen 49a/b
131
132
4.2.6 Synthese der Chrom-, Molybdän- und Wolframpentacarbonyl-iso-P5deltacyclenkomplexe 42a/b, 50a/b und 43a/b
134
4.2.6.1 Spektroskopische und analytische Daten der Chrompentacarbonyliso-P5-deltacyclenkomplexe 42a/b
135
4.2.6.2 Spektroskopische und analytische Daten der Molybdänpentacarbonyl-iso-P5-deltacyclenkomplexe 50a/b
135
13
4.2.6.3 Spektroskopische und analytische Daten der Wolframpentacarbonyliso-P5-deltacyclenkomplexe 43a/b
4.2.7 Synthese und Charakterisierung von P5-Homocunean
137
137
4.2.8 Synthese der Chrom-, Molybdän- und Wolframpentacarbonyl-P5homocuneankomplexe 52, 53 und 54
139
4.2.8.1 Spektroskopische und analytische Daten von ChrompentacarbonylP5-homocuneankomplex 52
139
4.2.8.2 Spektroskopische und analytische Daten von Molybdänpentacarbonyl-P5-homocuneankomplex 53
140
4.2.8.3 Spektroskopische und analytische Daten von WolframpentacarbonylP5-homocuneankomplex 54
5. Anhang
5.1 Kristallstrukturanalysen
5.1.1 Kristallstrukturdaten von Molybdänpentacarbonyl-P5-deltacyclen 45a
141
142
142
143
5.1.2 Kristallstrukturdaten von [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II) 47
144
5.1.3 Kristallstrukturdaten von Rhodium(III)-P5-deltacyclen-Zweikernkomplex 48
5.1.4 Kristallstrukturdaten von Molybdänpentacarbonyl-iso-P5-deltacyclen 50a
146
5.1.5 Kristallstrukturdaten von Chrompentacarbonyl-P5-homocunean 52
147
5.1.6 Kristallstrukturdaten von Molybdänpentacarbonyl-P5-homocunean 53
148
5.1.7 Kristallstrukturdaten von Wolframpentacarbonyl-P5-homocunean 54
149
6. Literaturverzeichnis
14
145
150
1. Einleitung
1.1 1-Triorganylstannyl-1,2,4-Triphosphol - Synthesebaustein des P5-Deltacyclens
Schon 1961 entdeckte T. E. Gier das erste Phosphaalkin Methinophosphid (H–C≡P), dem
aber aufgrund schwieriger Synthesebedingungen, Handhabbarkeit und seiner geringen
Stabilität wenig Bedeutung in der Synthese zukam.[1] Zwanzig Jahre später wurde durch die
Entdeckung praktikabler Synthesewege des stabilen Phosphaalkens 1 und des Phosphaalkins
2 der Grundstein für die Synthese einer Vielzahl neuer niedervalenter Phosphorverbindungen
gelegt (Abb. 1.1.1).[2,3,4]
Abb. 1.1.1 Synthese von Phosphaalkin 2 aus Phosphaalken 1 (R = C(CH3)3, CH3, C6H11 oder C6H5).
Phosphaalkine gehen bevorzugt Cycloadditionsreaktionen mit Dienen ein. So setzte M. Regitz
tert-Butylphosphaalkin 2a erfolgreich als Dienophil in einer Hetero-Diels-Alder-Reaktion mit
Cyclopentadien um. Mit einem zweiten Molekül tert-Butylphosphaalkin 2a wurde eine
weitere pericyclische Reaktion beobachtet, die zu dem in Abb. 1.1.2 gezeigten P2-Deltacyclen
3 führt.[5]
Abb. 1.1.2 Darstellung von P2-Deltacyclen 3.
Eine ähnliche Umsetzung von tert-Butylphosphaalkin wurde später von A. Elvers mit einem
Triphospholring als Dien durchgeführt, womit die Grundlage des in dieser Arbeit
verwendeten P–C-Käfigs geschaffen war (Kapitel 1.2).
15
Die beiden Verbindungen 1 und 2 stellen auch ideale Edukte für die Herstellung von
ungesättigten Phosphorheterocyclen dar. Abb. 1.1.3 zeigt, dass durch geeignete Reaktionen
sukzessive alle Kohlenstoffatome des Cyclopentadiens durch Phosphoratome ersetzt werden
können. Inzwischen sind alle grundsätzlich möglichen Phosphacyclopentadienid-Anionen
[CnRnP5-n]- (n = 0 - 4) synthetisiert und charakterisiert worden.
Abb. 1.1.3 Oligophosphacyclopentadienid-Anionen 4[6], 5[7], 6[8,9,10,11], 7[12,13,14], 8[8,9,15], 9[12,13] und 10[12,16].
Aufgrund der guten Zugänglichkeit galt dem Triphosphacyclopentadienid mit R = tert-Butyl
8a besonderes Interesse. Erstmals gelang G. Becker die Synthese des 3,5-Di(tert-butyl)-1,2,4triphosphacyclopentadienid-Anions durch die Umsetzung von Li[P(SiMe3)2] mit tertButylphosphaalkin 2a. Dabei entsteht das Diphosphacyclopentadienid 6a als Nebenprodukt
(Abb. 1.1.4).[15]
Abb. 1.1.4 Darstellung der Lithiumsalze von 6a und 8a.
Unabhängig voneinander fanden J. F. Nixon und A. H. Cowley, dass durch die Reduktion von
tert-Butylphosphaalkin 2a mit Natriumamalgam das Natriumsalz des Triphosphacyclopentadienids 8a dargestellt werden kann. (Abb. 1.1.5).[8,9]
16
Abb. 1.1.5 Darstellung der Natriumsalze von 6a und 8a durch Reduktion von tert-Butylphosphaalkin 2a mit
Natriumamalgam.
Die Herstellung der Alkalimetallsalze von 6a und 8a ist auch durch Reduktion von tertButylphosphaalken 1a mit Alkalimetallen möglich (Abb. 1.1.6).[17] Die Trennung der beiden
Natriumphosphacyclopentadienide erfolgt über fraktionierte Kristallisation bei -78 °C.
Bezogen auf 1a erhält man dadurch das reine Natriumsalz des 3,5-Di(tert-butyl)-1,2,4triphosphacyclopentadienids 8a-Na in Ausbeuten von ca. 5 %. Dieser Syntheseweg vermeidet
das reaktive Li[P(SiMe3)2] als Edukt und das toxische Quecksilber des Natriumamalgams und
wurde darum für die Käfigsynthesen dieser Arbeit verwendet.
Abb. 1.1.6 Darstellung der Natriumsalze von 6a und 8a durch Reduktion von Phosphaalken 1a mit
Natriummetall.
Mit verschiedenen Triorganylzinnchloriden R3SnCl gelang A. Elvers die Umsetzung des
Natriumsalzes von [3,5-Di(tert-butyl)-1,2,4-triphosphacyclopentadienid] 8a-Na zu den 1-Triorganylzinn-3,5-di(tert-butyl)-1,2,4-triphosphacyclopentadienen 11a-c (Abb. 1.1.7).[17,18]
Diese sind aufgrund geringerer Hydrolyse- und Oxidationsempfindlichkeit wesentlich
einfacher zu handhaben.
17
Na+(THF)1-2
SnR3
P
tBu
tBu
P
Toluol / -30°C
+ R3SnCl
P
P
tBu
- NaCl
P
tBu
P
11a-c
8a-Na
Abb. 1.1.7 Darstellung der Stannyltriphosphole 11a (R = C6H5), 11b (R = CH3), 11c (R = C4H9).
Mit Hilfe der Stannyltriphosphole 11 lassen sich Komplexe darstellen, die mit den
Triphosphacyclopentadienidanionen 8 unzugänglich sind (Abb. 1.1.8). Das Triorganylzinnfragment bildet dabei eine gute Abgangsgruppe, da es durch die relativ labile Sn–PBindung leicht wieder abgespalten werden kann.[17,18]
tBu
tBu
P
P
tBu
P
+ [BrMn(CO) 5]
- BrSnPh3
- 2 CO
OC
11a
P
P
Mn
P
tBu
tBu
tBu
P
Sn
+ SnCl2
- 2 ClSnMe3
CO
P
tBu
P
tBu
CO
12
P
SnMe3
2 tBu
P
P
SnPh3
P
P
P
11a
tBu
13
Abb. 1.1.8 Darstellung der Phosphacyclopentadien-Komplexe 12 und 13.
Die Trialkylstannyltriphosphole 11a-c unterliegen bei Raumtemperatur einem raschen
Austausch des Zinnfragments zwischen den beiden benachbarten Phosphoratomen. Dies
konnte mittels Tieftemperatur
31
P-NMR-Spektren und durch
119
Sn-NMR-Messungen gezeigt
werden. Daher liegt Triphenylstannyltriphosphol als Enantiomerenpaar 11a’ und 11a’’ vor
(Abb. 1.1.9).[17] Die Aktivierungsenergie für die [1,5]-sigmatrope Umlagerung in das andere
Enantiomer beträgt ∆G‡ = 31.5 ± 1 kJ mol-1. In Folgereaktionen der Stannyltriphosphole
11a-c entstehen somit in der Regel ebenfalls Enantiomeren- bzw. Diastereomerenpaare.[17]
18
Abb. 1.1.9 Austausch des Triphenylzinnfragments zwischen den beiden benachbarten Phosphoratomen von 11a.
Bildung des Enantiomerenpaars 11a’ und 11a’’.
Aufgrund der stereochemischen Eigenschaften von 11a bildet sich mit [CpCo(C2H4)2] der
chirale 18-Valenzelektronenkomplex 14 als racemisches Gemisch zweier Enantiomere
(Abb. 1.1.10).
SnPh3
SnPh3
Co
+
tBu
P*
tBu
P
P
tBu
P*
- C2H4
P
P
tBu
Co
11a
14
Abb. 1.1.10 Darstellung des racemischen Komplexes 14.
Bedingt durch die η4-Koordination des Liganden kann das Zinnfragment seinen Platz
zwischen den Phosphoratomen des Heterocyclus nicht mehr tauschen. Somit wird das
Phosphoratom, an welches das Zinnatom gebunden ist, im Komplex 14 zum stabilen
stereogenen Zentrum.[17]
1.2 Synthese von P5-Deltacyclenen
Mit dem dynamisch verbundenen Enantiomerenpaar des Stannyltriphosphols 11a’/11a’’
führte A. Elvers erfolgreich die Umsetzung mit zwei Molekülen tert-Butylphosphaalkin 2a
durch. Als Endprodukte wurden von ihm die Triphenylstannyl-P5-Deltacyclene 16a’ und
16a’’ als spiegelsymmetrisches Enantiomerenpaar in einer Ausbeute von 80 % erhalten
(Abb. 1.2.1).
19
SnPh3
P*
tBu
SnPh3
P
P
11a'
P*
P
tBu
tBu
+ tBu
tBu
P
11a''
P
2a
SnPh3
*
P
*
P
P
*
tBu
Ph3Sn
P*
*
P
tBu
tBu
P
*
P
P
tBu
tBu
tBu
15''
15'
+ tBu
P
2a
tBu
*
P
tBu
*
P
SnPh3
* tBu
*
*P
P* P
*
tBu
*
*
P
SnPh 3
tBu
P* tBu *
* P
*
P
*
P
tBu
tBu
16a'
16a''
Abb. 1.2.1 Bildung des stannylierten P5-Deltacyclen-Enantiomerenpaares 16a’ und 16a’’ durch eine [4+2]- und
[2+2+2]-Cylcoadditionsreaktion von zwei Molekülen tert-Butylphosphaalkin 2a mit dem TriphospholEnantiomerenpaar 11a’ und 11a’’.
Der Mechanismus der Reaktion konnte plausibel erklärt werden. Eine [4+2]-Cycloaddition
von 2a und 11a’/11a’’ leitet die Käfigbildung ein, die mit einer [2+2+2]-Cycloaddition
abgeschlossen wird. Das stannylierte P5-Deltacyclen 16a enthält sieben stereogene Zentren
und daher wäre theoretisch eine große Anzahl an Stereoisomeren denkbar. Bemerkenswerterweise wird nur das Enantiomerenpaar 16a’ und 16a’’ gebildet. Die beiden pericyclischen
Reaktionsschritte sind damit hoch diastereoselektiv.[18]
Beim ersten Schritt ist die eine Seite des Triphosphols durch den raumfüllenden
Triphenylzinnrest gegen eine Annäherung des tert-Butylphosphaalkins 2a abgeschirmt. Somit
20
kann die [4+2]-Cycloaddition zwischen 2a und 11a’ und 11a’’ nur von der dem Zinnfragment
abgewandten Ringseite aus erfolgen (Abb. 1.2.2). Die Reaktion verläuft dabei
orbitalkontrolliert, die sterische Behinderung durch die beiden tert-Butylgruppen spielt eine
untergeordnete Rolle.
SnPh3
P
P
tBu
P
P
tBu tBu
tBu
Ph3Sn
P
P
tBu
tBu
P
tBu
Ph3Sn
P
P
P
tBu
P
tBu
P
11a''
11a'
Abb. 1.2.2 Annäherung des HOMO der beiden Enantiomere 11a’ und 11a’’ an das LUMO von tertButylphosphaalkin 2a, sowie eine nicht realisierte Kombination.
Cycloadditionsreaktionen lassen sich einfach mit der Grenzorbitalmethode beschreiben. Die
Orbitalüberlappung trägt einen großen Beitrag zur Bildung der Reaktionsprodukte bei. Die
Überlappung der pz-Orbitale ist bei gleichen Kernen am größten und spielt hier bei der
Steuerung der Regioselektivität des ersten Reaktionsschrittes die entscheidende Rolle. Die
Überlappung von Orbitalen unterschiedlicher Kerne ist energetisch ungünstiger als die
Überlappung ähnlich dimensionierter Orbitale. Somit wird die in Abb. 1.2.2 rechts
dargestellte Kombination der Orbitale nicht realisiert, während die beiden ersten trotz der
beiden benachbarten tert-Butylgruppen bevorzugt eingegangen werden. Die effektive
Orbitalüberlappung
Substituenten.
überwiegt
damit
die
sterische
Abstoßung
der
raumfüllenden
[18]
Im Anschluss an die [4+2]-Cycloadddition addiert ein weiteres Molekül tert-Butylphosphaalkin 2a an die postulierten Tetraphosphanorbornadien-Intermediate 15’ und 15’’. Diese
konnten bislang weder isoliert noch abgefangen werden, da sie sofort zu den
Käfigverbindungen 16’ und 16’’ weiterreagieren.[19] In diesem Reaktionsschritt fungieren die
beiden Zwischenprodukte 15’ und 15’’ jeweils als Dien gegenüber einem weiteren Molekül
tert-Butylphosphaalkin 2a. Die Reaktion kann als [2+2+2]-Cycloaddition gesehen werden. Es
sind
theoretisch
jeweils
vier
verschiedene
Orientierungsmöglichkeiten
des
tert-
Butylphosphaalkins an 15’ bzw. 15’’ denkbar. Von diesen wird nur eine tatsächlich realisiert,
da nach der Reaktion nur ein einziges Enantiomerenpaar 16’ und 16’’ als Endprodukt
vorliegt, wobei 15’ ausschließlich zu 16’ und 15’’ vollständig zu 16’’ führt.
21
SnPh3
SnPh3
P
P
P
tBu
P
P
P
tBu
P
tBu
tBu
P
tBu
P
tBu
tBu
tBu
P
Abb. 1.2.3 Addition von tert-Butylphosphaalkin 2a an 15’ (links) und rechts eine nicht realisierte Orientierung
der Edukte.
Die Annäherung von 2a erfolgt stets auf der Seite des Diens, die die C–C-Bindung enthält.
Würde der Angriff auf der anderen Seite erfolgen, ergäbe sich ein P–C–C-PhosphiranDreiring, der im Gegensatz zum tatsächlich gebildeten P–P–C-Diphosphiran-Dreiring deutlich
mehr Ringspannung aufweisen würde. Die zwei verbleibenden Orientierungsmöglickeiten des
tert-Butylphosphaalkins 2a sind in Abb. 1.2.3 gegenübergestellt. Hier wird klar, dass die erste
Möglichkeit gegenüber der zweiten aufgrund der dort auftretenden repulsiven Wechselwirkungen zwischen drei tert-Butylgruppen deutlich begünstigt ist.
Nach den beiden hoch diastereoselektiven Cycloadditionsschritten wird der resultierende
Käfig als Enantiomerenpaar 16a’ und 16a’’ erhalten. Die schwache Sn–P-Bindung kann
anschließend als Begleitreaktion einer Säulenchromatographie (SiO2/5 % H2O) hydrolisiert
werden, wobei die Ph3Sn-Gruppe durch ein Wasserstoffatom ersetzt wird. Man erhält dabei
ein P–H-funktionalisiertes P5-Deltacyclen 17 als Mischung zweier Enantiomere 17’ und 17’’
(Abb. 1.2.4).
H
tBu
P
* tBu
*
P
*
P* P
P
*
tBu
*
tBu
H
*
P
tBu
P* tBu *
* P
*
P
*
P
tBu
tBu
17'
17''
Abb. 1.2.4 Molekülstrukturen des P5-Deltacyclen-Enantiomerenpaars 17’ und 17’’.
Es konnte hierbei bisher nicht eindeutig geklärt werden, ob das Proton am sekundären
Phosphoratom die gleiche oder eine entgegengesetzte Position wie das jeweilige
Triorganylzinnfragment von 16’ und 16’’ einnimmt.[19]
22
Die beiden Enantiomere des P5-Deltacylens 17 und seiner Metallkomplexe werden in dieser
Arbeit mit 17’ und 17’’ bezeichnet, da eine systematische Bezeichnung aller stereogenen
Zentren nach den CIP-Regeln zu unübersichtlich ausfallen würde. Wird von der Mischung
beider Enantiomere gesprochen wird nur die jeweilige Nummer ohne die Indices ’ und ’’
verwendet.
Ersetzt man die Ph3Sn-Gruppe von 11a durch eine chiral modifizierte Stannylgruppe, ergeben
sich für die stannylierten P5-Deltacyclene zwei chemisch unterscheidbare Diastereomere. M.
Hofmann konnte diesen Ansatz mit einer cis-Myrtanyldiphenylzinn-Einheit erfolgreich
realisieren und die beiden Diastereomere 16b’ und 16b’’ durch fraktionierte Kristallisation
voneinander trennen (Abb. 1.2.5). Nach der Hydrolyse liefern diese die beiden separierten
Enantiomere 17’ und 17’’.[19,20]
SnPh2R*
tBu
P*
* tBu
*
P
*
P* P
P
*
tBu
*
tBu
tBu
16b'
SnPh2R*
*
tBu
P*
P* tBu *
* P
*
P
*
P
tBu
R* =
(-)-cis-Myrtanyl
16b''
Abb. 1.2.5 Molekülstrukturen der zwei diastereomeren Verbindungen 16b’ und 16b’’.
1.3 Metallkomplexe von P–C-Käfigverbindungen
In der Literatur sind eine Reihe von Metallkomplexen von P–C-Käfigverbindungen
beschrieben worden. Im Folgenden sollen einige Beispiele aufgezeigt werden.
Tetraphosphacuban 18 ist ein Tetramer von tert-Butylphosphaalkin 2a. Weil es hochsymmetrisch ist, besitzt es vier äquivalente Phosphoratome, die als Donoren in Frage
kommen. M. Regitz et al. konnten den Eisen(0)-Komplex [Fe(CO)4(P4C4tBu4)] 19 durch
Umsetzung von 18 mit [Fe2(CO)9] unter Rückfluß in THF darstellen (Abb. 1.3.1).[21] Eine
Koordination von einem bzw. zwei Platinkomplexfragmenten bei Raumtemperatur wurde
später durch J. F. Nixon et al. entdeckt.[22] Je nach Stöchiometrie des eingesetzten Komplexes
können so die Mono- bzw. Bis-Platinkomplexe 20 und 21 erhalten werden (Abb. 1.3.1).
23
Abb. 1.3.1 Metallkomplexe 19, 20 und 21 des Pentaphosphacubans 18.
Ein Pentamer von tert-Butylphosphaalkin 2a ist die in Abb. 1.3.2 gezeigte P–CKäfigverbindung 22. Sie tritt bei einigen Cycloadditionsreaktionen von 2a als Nebenprodukt
auf, kann aber am besten durch eine oxidative Kopplungsreaktion zwischen den
Lithiumsalzen der Diphospholyl- und Triphospholyl-Anionen 6a-Li und 8a-Li mit Hilfe von
FeCl3 oder CoBr2 dargestellt werden.[23] Durch Zugabe von 0.5 Äquivalenten [Pt2Cl4(PEt3)2]
erhält man daraus den Platin(II)-Käfigkomplex 23. Die Koordination des Platins erfolgt
ausschließlich am Diphosphiranring des Käfigs. Die Spiegelsymmetrie von 22 bleibt dadurch
auch im Metallkomplex 23 erhalten.[22]
Abb. 1.3.2 Platinkomplex 23 des P–C-Käfigs 22.
Der in Abb. 1.3.3 gezeigte 16 Valenzelektronenkomplex 24 eines Heptamers von 2a entsteht
als eines von vielen Produkten, wenn (η4-1-Methylnaphtalin)(η6-toluol)eisen(0) mit einem
24
großen Überschuss an tert-Butylphosphaalkin 2a umgesetzt wird. Der Komplex kann durch
wiederholtes Aufreinigen durch Säulenchromatographie aus der Reaktionsmischung isoliert
werden. Die Koordination des Eisens erfolgt im paramagnetischen P–C-Käfigkomplex 24
durch
drei
verschiedene
Ligandfunktionen
des
seitlich
offenen
Käfigs,
nämlich
1,3-Diphosphaallyl, 2-Phosphaallyl und durch eine σ-Bindung eines weiteren Phosphoratoms.
Wie 23 ist auch 24 spiegelsymmetrisch und damit achiral.[24]
tBu
tBu
P
P
Fe
+ 7 tBu
P
tBu
tBu Fe
P
P
2a
P
tBu
tBu
P
tBu
P
24
Abb. 1.3.3 Synthese des Eisenkomplexes 24.
Das Tetraphosphaquadricyclan 25 kann durch die Cylclooligomerisation von tertButylphosphaalkin 2a mit Lewis-Base-Addukten von Imidovanadium(V)-Verbindungen
dargestellt
werden.
Die
Umsetzung
von
25
mit
reaktiven
Übergangsmetall-
Carbonylkomplexen ergibt die Komplexe 26 und 27, bei denen [M(CO)n]-Fragmente an beide
Diphosphiranringe des Quadricyclans koordinieren (Abb. 1.3.4).[25]
Abb. 1.3.4 3-Aza-1,2,4,6-tetraphosphaquadricyclan 25 und Synthese der Übergangsmetallkomplexe 26 und 27.
Für die Synthese des P–C-Käfigs 28 wurde die Cyclooligomerisation von tert-Butylphosphaalkin 2a mit der Lewis-Säure Aluminiumtrichlorid induziert. Die Reaktionsprodukte hängen
hierbei stark vom verwendeten Lösungsmittel ab. In Et2O ergibt sich der tetracyclische Käfig
28 (Abb. 1.3.5). Wird er mit [Fe2(CO)9] umgesetzt findet eine Gerüstumlagerung des Käfigs
unter Freisetzung eines Alkylaluminiumfragments zum Metallkomplex 29 statt.[26]
25
tBu
Et
P + AlEt3
4 tBu
Et2O
2a
Et
P
P
Al
P
tBu
tBu
P
tBu
Et
Et (CO)3
Fe
P
P tBu
tBu
P
tBu
H
P
H
tBu Fe(CO)
Et
2 Fe2(CO)9
-2 Fe(CO)5
-CO
-[AlEt]
28
4
29
Abb. 1.3.5 Cylclooligomerisation von 2a zu 28 zur Synthese des Übergangsmetallkomplexes 29.
Der ungesättigte Käfig 30 lässt sich durch die Umsetzung von Trimethylstannyltriphosphol
11b mit HgCl2 darstellen. Durch eine Umsetzung von 30 mit einem Überschuss an
[W(CO)5THF] erhält man 31. Wie in Abb. 1.3.6 zu sehen ist, sind zwei [W(CO)5]-Fragmente
an 31 koordiniert, eines davon am Phosphoratom der P=C-Doppelbindung.[28]
Abb. 1.3.6 Darstellung des [W(CO)5]-Komplexes 31.
Eine weitere mögliche Reaktion von Übergangsmetallen mit P–C-Käfigverbindungen ist die
oxidative Addition an reaktive P–P-Bindungen. Eine solche Bindung ist z.B. im
Hexaphosphapentaprisman 32 zu finden.[27] 32 kann auf mehrere verschiedene Arten
synthetisiert werden. Eine Möglichkeit ist es, 32 mit Hilfe von Tageslicht durch
Valenzisomerisierung von 30 darzustellen.[28] Hexaphosphapentaprisman 32 ist C2symmetrisch. Aufgrund dieser Symmetrie ergibt sich für die Phosphoratome des Käfigs ein
AA´BB´CC´-Spinsystem, so dass sich in den
31
P-NMR-Spektren drei Signale für die sechs
Phosphoratome ergeben. Die P–P-Bindung von 32 ist herausrangend reaktiv und neigt daher
zu Insertionsreaktionen. So insertieren dort z.B. die Chalkogene Schwefel, Selen und
Tellur.[29] Die P–P-Bindung wird auch von Platinkomplexen gespalten, wobei das Metall
zwischen den beiden Phosphoratomen komplexiert wird. Setzt man [PtCl2(η4-COD)]2 in
CHCl3 mit 32 um, so ergibt sich das Komplexdimer 33 (Abb. 1.3.7). Es besitzt ein
Inversionszentrum in der Mitte der Pt–P–Pt–P-Ebene. Da bei der Dimerisierung die C2-Achse
26
des Hexaphosphapentaprismans verloren geht, zeigen sich sechs Signale für die 12
Phosphoratome im 31P-NMR-Spektrum.[27]
Abb. 1.3.7 Herstellung eines Platin-P–C-Käfig-Dimers 33 aus Hexaphosphapentaprisman 32.
Neben Platin(II) und Eisen(0) wurden zur Komplexierung von P–C-Käfigen in der Literatur
häufig Metalle der Chromtriade in der Oxidationsstufe 0 als [M(CO)5]-Fragmente eingesetzt.
In der Arbeitsgruppe von M. Regitz wurde eine an [W(CO)5] koordinierte P–CKäfigverbindung 35 synthetisiert, die ein Derivat eines P5-Deltacyclen-Isomers von 17
darstellt (Abb. 1.3.8). Vier der fünf Phosphoratome von 35 besetzen analoge Positionen des
Käfiggerüstes von 17. Nur ein Phosphoratom im Triphosphacyclohexenring ist mit einem
benachbarten Gerüstkohlenstoffatom vertauscht. Die anderen drei Gerüstkohlenstoffatome
liegen wieder auf analogen Positionen wie in 17.[30]
NH2Ar
tBu
ArHN
P
+ 4 tBu
C
P
Toluol / 90°C
- C2H4
Ar = o-Tolyl
tBu
P
P
W(CO)5
P
W(CO)5
P
P
tBu
tBu
34
35
Abb. 1.3.8 Herstellung der Wolframpentacarbonyl-Käfigverbindung 35.
Der Syntheseweg zu 35 unterscheidet sich dabei deutlich von den Reaktionen, die 16 und 17
liefern. Statt zunächst einen Triphospholylring zu synthetisieren, wird dieser intermediär aus
einem Dreiring 34 gebildet, an dem bereits ein [W(CO)5]-Fragment gebunden ist. Dieses ist
nötig, um den Phosphiranring zu stabilisieren. Es reagiert in vier Cycloadditionsschritten mit
tert-Butylphosphaalkin 2a zum Komplex 35.[30]
27
Ein weiteres Tetramer von tert-Butylphosphaalkin 2a, das Tetraphosphabishomoprisman 36,
entsteht als Pyrolyseprodukt von 2a. Die in Abb. 1.3.9 gezeigte Struktur von 36 konnte von
M. Regitz et al. durch NMR-spektroskopische Untersuchungen bestimmt werden.[31] Nach der
Koordination von zwei [W(CO)5]-Fragmenten an 36 konnten vom Metallkomplex 37
röntgenfähige Kristalle erhalten werden und dadurch die Strukturbestimmung von 36 bestätigt
werden. Die beiden Wolframatome koordinieren bei 37 an beiden Phosphoratomen des
Diphosphiranrings.[32]
tBu
tBu
P
tBu
P
P
P
W(CO)5
[W(CO)5THF]
tBu
THF
P
P
P
W(CO)5
tBu
tBu
P
tBu
tBu
37
36
Abb. 1.3.9 Tetraphosphabishomoprisman 36 und Synthese des Metallkomplexes 37.
Die P5(CR)5-Käfigverbindung 38 ist strukturell verwandt mit dem P5-Deltacyclen 17
(Abb. 1.3.10). Wegen der zusätzlichen C(t-Bu)-Gruppe zwischen Diphosphiranring und P1
weist 38 eine zweite P=C-Doppelbindung an dieser Position auf, in der sich die P–H-Einheit
von 17 befindet. Ansonsten sind die beiden Moleküle strukturanalog. Verbindung 38 wird
durch eine Cycloaddition von zwei Molekülen P≡C–Me an 2,4,6-Tri-tert-butyl-1,3,5triphosphabenzol synthetisiert. Zwei der Gerüstkohlenstoffatome von 38 sind darum im
Gegensatz zu 17 durch Methylreste statt durch tert-Butylgruppen abgesättigt. Wird 38 mit
[W(CO)5THF]
umgesetzt,
koordinieren
wieder
zwei
[W(CO)5]-Fragmente
an
die
Phosphoratome P4 und P5 und befinden sich damit in den Nachbarpositionen zu den beiden
Methylsubstituenten.[33]
Abb. 1.3.10 Synthese der P–C-Käfigverbindung 38 und deren Metallkomplex 39.
28
In einem Parallelprojekt zur vorgelegten Dissertation konnte I. Keller zwei Metallkomplexe
des P5-Deltacyclenkäfigs 17 mit den Münzmetallen Kupfer und Silber in der Oxidationsstufe
+1 darstellen. Aufgrund der schlechten Löslichkeit beider Komplexe gelang bislang noch
keine vollständige Charakterisierung, die Molekülstrukturen der Verbindungen konnten
jedoch strukturanalytisch bestimmt werden. Das für die Synthesen benutzte Edukt ist das
racemische Gemisch 17. Beide Komplexe liegen als Additionsprodukt der beiden
Enantiomere von 17 vor. Für die Darstellung des Silber(I)-Komplexes 40 wurde Silberacetat
eingesetzt (Abb. 1.3.11). Das Acetatanion deprotoniert das sekundäre Phosphan P1 und eines
der Silberatome koordiniert dort. Das zweite Silberatom koordiniert an das Phosphoratom P5.
Die Verbrückung zwischen den beiden Enantiomeren erfolgt über die Bindungen P1A–Ag1–
P5 und P1–Ag1A–P5A. Die resultierende Verbindung 40 ist Punktsymmetrisch und besitzt
ein Inversionszentrum in der Mitte der Ag–Ag-Bindung.[34]
P1
tBu
2
tBu
H
tBu
P5 tBu
P4
tBu
tBu
2 Ag(OOCCH3)
P2
3
P
P
tBu
Toluol, CH3CN
-CH3COOH
3
tBu
2
P
P5
1
P
P4
P1A
Ag
1
P
Ag1A
2A
P3A tBu
P
tBu
tBu
P4A
5A
tBu
40
17
Abb. 1.3.11 Darstellung des Silber(I)-P5-Deltacyclen-Zweikernkomplexes 40.
Die Synthese der Kupferverbindung wurde mit CuCl durchgeführt. Der resultierende
Zweikernkomplex 41 stellt eine Additionsverbindung beider Reaktionskompnenten dar. Die
Chloroliganden des Metalls werden dabei mit in den Komplex übernommen, der wieder beide
Enantiomere 17’ und 17’’ des Käfigs vereinigt (Abb. 1.3.12).
H
tBu
2
tBu
tBu
P1
P5
P4
tBu
tBu
P2
Toluol, CH3CN
4
P
P3
tBu
17
tBu
2 CuCl
P3
P5
tBu
H
tBu
P1
P2
Cu
P9
8
P10 P
Cl
Cu
Cl
tBu
P7
P6
tBu
tBu
H
41
Abb. 1.3.12 Darstellung des Kupfer(I)-P5-Deltacyclen-Zweikernkomplexes 41.
29
Die Koordination erfolgt hier ebenfalls an P5, jedoch nicht an P1, welches weiterhin ein
Proton trägt. Die Verbrückung kommt über die beiden Chloroliganden der Kupferatome
zustande. Im Gegensatz zu 40 ist die Verbindung 41 im Festkörper C1-symmetrisch.
Durch die Umsetzung eines umgelagerten P5-Deltacyclenkäfigs, dem iso-P5-Deltacyclen, mit
[Cr(CO)5THF] und [W(CO)5THF] wurden von S. Huguet-Torrell die beiden Metallpentacarbonyl-iso-P5-deltacylene
42a
und
43b
synthetisiert,
von
denen
jeweils
eine
Röntgenstruktur erhalten werden konnte.[35] Die Konfiguration der stereogenen Zentren der
CHtBu-Einheit beider Käfiggerüste sind invers zueinander wenn man die entsprechenden
Käfigenantiomere miteinander vergleicht, bei denen die Konfiguration aller anderen
stereogenen Zentren für die beiden Komplexe identisch sind. Damit stellen 42a und 43b die
Metallkomplexe zweier epimerer Käfigverbindungen dar. Mittlerweile konnte C. Höhn den
Wolframpentacarbonyl-iso-P5-deltacyclenkomplex auch enantiomerenrein darstellen. Die
Röntgenstruktur der Kristalle von 43a weisen die Substanz als Epimer von 43b aus, in dem
die CHtBu-Einheit invertiert ist.[36]
tBu
H
(OC)5Cr
(OC)5W
P
tBu
P
P
P
tBu
tBu
tBu
H
P
P
tBu
P
P
H
(OC)5W
P
P
tBu
tBu
P
P
P
P
P
tBu
tBu
tBu
tBu
42a
43a
43b
Abb. 1.3.13 Metallpentacarbonyl-iso-P5-Deltacyclene 42a und 43a und dessen Epimer 43b.
Das Auftreten von Epimeren bei den Metallkomplexen 42 und 43 wirft die Frage nach der
Existenz von Epimeren beim P5-Deltacyclen 17 und seinem Umlagerungsprodukt iso-P5Deltacyclen auf.
1.4 Ziel dieser Arbeit
Nach Substitution der Stannylgruppe von 16 durch ein Wasserstoffatom ist immer eine
weitere, bisher nicht näher untersuchte und nicht abtrennbare Verbindung in den NMRSpektren von 17 zu finden. Es sollte versucht werden, diese zu charakterisieren, um eventuell
auftretende Nebenprodukte der Komplexierungsreaktionen der P–C-Käfigverbindungen
besser identifizieren zu können. Das Auftreten der beiden Epimere bei den Metallkomplexen
30
des iso-P5-Detlacyclens wird als erster Anhaltspunkt für die Charakterisierung der
unbekannten Verbindung gewertet. Um das P5-Deltacyclen 17 in diesem Sinn vollständig zu
charakterisieren, sollte die Orientierung des Protons am sekundären Phosphan in Lösung
bestimmt werden. Derartig erweiterte analytische Daten des P5-Deltacyclens 17 und seines
Nebenprodukts sollten dann zur Charakterisierung von neuen Übergangsmetallkomplexen der
Käfigverbindungen geeignet sein.
Die in der Literatur beschriebenen Metallkomplexe von P–C-Käfigverbindungen weisen ein
breites Spektrum an unterschiedlichen Koordinationsmöglichkeiten auf, die auch für das in
dieser Arbeit untersuchte P5-Deltacyclen 17 gelten sollten. Dabei geht es um die grundlegende
Eignung von 17 und seinen beiden Enantiomeren 17’ und 17’’ als chiraler, sterisch
anspruchsvoller Ligand. Das Fernziel hierbei ist den Käfig in enantiomerenreiner Form in der
asymmetrischen Katalyse einzusetzen.
Im überwiegenden Teil der Arbeit wurde mit dem Racemat 17 des Enantiomerenpaars 17’
und 17’’ gearbeitet. Es steht in sehr viel größerer Menge zur Verfügung und eignet sich daher,
Grundlagen für spätere Arbeiten mit enantiomerenreinen Substanzen zu schaffen. Die dabei
gewonnenen Erkenntnisse sollten dann in einer Zusammenarbeit mit C. Höhn genutzt werden,
die sich mit der Synthese enantiomerenreiner Folgeprodukte der beiden Enantiomere 17’ und
17’’ beschäftigt hat.
Für die Komplexierungsexperimente wurden zunächst die [M(CO)5THF]-Komplexe der
Chromtriade als Reaktionspartner für 17 ausgewählt. Damit sollten sich die reaktivsten
Donorzentren des Käfigs bestimmen lassen. Gleichzeitig enthalten die meisten bislang
bekannten P–C-Käfigkomplexe M(CO)n-Einheiten. Das eröffnet Vergleichsmöglichkeiten
und verbindet dieses Projekt mit den Vorarbeiten von S. Huguet-Torrell. Anschließend sollten
die Versuche auf Redoxaktive Metallkomplexe mit einem katalytischen Potential ausgedehnt
werden, um das Fernziel der Synthese neuer Übergangsmetallkomplexkatalysatoren ansteuern
zu können. Dazu gehören insbesondere Komplexe von Ru2+- und Rh1+-Ionen.
Auch die erstmals von S. Huguet-Torrell beobachtete Umlagerung des P5-Deltacyclens 17 in
das iso-P5-Deltacyclen ist noch nicht vollständig verstanden. Es bietet sich an sich auch mit
dieser interessanten Reaktion eingehend zu beschäftigen weil die Möglichkeit von weiteren
Folgereaktionen reizt, die das Tor eventuell zu weiteren neuen P–C-Käfigverbindungen und
ihren Metallkomplexen öffnen könnten.
31
2 Ergebnisse und Diskussion
2.1 Charakterisierung von P5-Deltacyclen 17a/b
Da in den meisten Teilen der vorliegenden Arbeit mit einer racemischen Mischung beider
Enantiomere des P5-Deltacyclens 17 und seiner Folgeverbindungen gearbeitet wurde, ist bei
der Nennung einer Verbindungsnummer das jeweilige Enantiomerengemisch gemeint.
Einzelne Enantiomere werden mit den Indices ’ und ’’, also etwa mit 17’ und 17’’ bezeichnet,
wobei darauf geachtet wurde, die Indices konsequent auf jeweils analoge Stereoisomere der
Käfige anzuwenden.
Bislang
wurde
davon
ausgegangen, dass
alle
sieben
stereogenen
Zentren
der
Enantiomerenmischung des P5-Deltacyclens 17 gleichermaßen als Bild und Spiegelbild
auftreten. Dieser Fall ist gesichert für das Edukt 16a des P–H-Käfigs 17, dessen
Phosphoratom P1 anstelle des Wasserstoffatoms H1 eine Triphenylstannylgruppe trägt.[20]
Wie für das stannylierte P5-Deltacyclenen 16a mit seiner achiralen Stannylgruppe, wurde
bislang davon ausgegangen, dass auch in den NMR-Spektren der Kerne 1H, 13C und 31P von
17 jeweils nur ein Signalsatz für den Käfig auftritt. Nach der Hydrolyse der Phosphor-ZinnBindung von 16 wird jedoch neben der schon beschriebenen Substanz 17a[18,19] eine weitere
bisher nicht charakterisierte Verbindung 17b beobachtet. Die stannylierte Verbindung 16, die
das Edukt in der Käfigsynthese darstellt, ist allerdings analysenrein und eventuelle
Nebenprodukte sind dort nicht erkennbar. Die in den NMR-Spektren des P5-Deltacyclens 17a
beobachtbare Verbindung 17b liegt in Lösungen des vollständig destannylierten P5Deltacyclens stets im Verhältnis von ca. 0.15 : 1 zum Käfig 17a vor. Alle Versuche
scheiterten bislang, die Verbindung durch Kristallisation oder Chromatographie abzutrennen.
Für die Metallkoordination ist aber die Reinheit des Liganden von essentieller Bedeutung. Es
wurde daher 17b weiter untersucht.
Zunächst zeigt sich in den Massenspektren (ESI-ToF) des Gemisches der Substanzen 17a und
17b neben den Peaks des Käfig-Monomers auch Signale einer weiteren Verbindung mit der
doppelten Masse des Monomers. Die Signale zeigen in Abhängigkeit von der
Ionisationsmethode unterschiedliche Intensitäten, blieben aber jedoch immer unterhalb von
5 %. Diese Messergebnisse legten zunächst die Existenz eines Käfig-Dimeres nahe. Da in den
Massenspektren aber Dimere auch bei der Ionisation der Moleküle entstehen können, wurden
31
P-DOSY-NMR-Messungen an dem Gemisch 17a/17b von W. Bauer durchgeführt. Diese
deuten auch darauf hin, dass 17b etwas größer als 17a sein sollte, allerdings beträgt der
32
bestimmte Diffusionsquotient nur ca. 1.14 und ist damit weit kleiner als für ein Dimer zu
erwarten wäre. Das
31
P{1H}-NMR-Spektrum des Gemisches 17a/17b ist in der Abb. 2.1.1
gezeigt. Neben deutlichen Intensitätsunterschieden der Signalgruppen, die den jeweiligen
Substanzen zuzuordnen sind fällt auf, dass 17b wie 17a fünf Signalgruppen jeweils gleicher
integraler Intensität aufweist, die eine gewisse Ähnlichkeit mit den Signalen von 17a
aufweisen. Wenn es sich bei 17b also um ein Dimer von 17a handeln sollte, wäre zu fordern,
dass die Dimerisierung zu jeweils äquivalenten Paaren von P-Kernen für die beiden Bausteine
des Dimers führt, die zudem nur vernachlässigbare P–P-Kopplungen zwischen beiden
Molekülhälften aufweisen dürfen. Literaturbekannt sind Dimerisierungsreaktionen von
Diphosphiranen, bei denen Tetraphacyclohexan-Sechsringe entstehen.[40] Eine DiphosphiranEinheit bilden C1, P2 und P3 im P5-Deltacyclen 17. Ein Bindungsbruch zwischen P2 und P3
wird auch bei der Komplexierung zum Rhodium(III)-Zweikernkomplex 48 beobachtet, der in
Kapitel 2.5 besprochen wird. Damit schien eine Dimerisierung möglich, die im resultierenden
1,2,4,5-Tetraphosphacyclohexan jedoch größere
1
JPP-Kopplungen zwischen den beiden
Molekülhälften aufweisen müsste, die starke Änderungen zwischen den
31
P{1H}-NMR-
Spektren von Monomer und Dimer zur Folge hätten. Um die Existenz der entsprechenden
Dimere weiter zu hinterfragen, wurden von R. Puchta DFT-Rechnungen angefertigt
(B3LYP/6-31G*). Sie ergaben instabile und gegenüber dem Monomer um ca. 80 kcal mol-1
energetisch ungünstigere Dimere.[37,38] Zudem dimerisieren die in der Literatur beschriebenen
Diphosphirane nur bei geringem sterischen Anspruch der Ringperipherie.[39] Damit sprechen
alle bislang zugänglichen Daten von 17b gegen eine dimere Verbindung.
Da eine Elementaranalyse des Gemisches von 17a und 17b mit der Zusammensetzung von
17a vereinbar ist kann sie sich bei 17b nicht wesentlich von 17a unterscheiden. Die Abb.
2.1.1 zeigt das 31P-NMR-Spektrum des Gemisches aus 17a und 17b mit Vergrößerungen der
17b zugeordneten Peaks für die Phosphoratome P1, P2, P3 und P5. Beide Verbindungen
besitzen fünf Phosphoratome, von denen jeweils zwei Signale beider Verbindungen ähnliche
chemische Verschiebungen aufweisen. So liegen beide Signale von P4 in der Region, die
charakteristisch für P=C-Doppelbindungen ist, und P2 und P3 liegen durch die Ringspannung
des Diphosphiranrings relativ weit im Hochfeld.[39,40] Anhand von P–H gekoppelten
31
P-
NMR- und 1H-NMR-Spektren kann gezeigt werden, dass das in beiden Verbindungen
vorhandene P–H-Proton H1 an P1 gebunden ist. Diese Beobachtungen legen eine enge
Strukturverwandschaft von 17a und 17b nahe. Es wird daher angenommen, dass 17a und 17b
Epimere sind, die sich nur in der Konfiguration des Phosphoratoms P1 unterscheiden (Abb.
2.1.2). Diese Hypothese wird im Folgenden durch die Analyse der NMR-Spektren belegt.
33
Abb. 2.1.1 31P-NMR-Spektrum (122 MHz, CDCl3, 25°C) des Gemisches der Substanzen 17a und 17b im
Verhältnis 1 : 0.15.
H1
tBu
P4
P1
tBu
P3
P5
tBu
H1
tBu
P4
P2
P1
tBu
2
P3 P
P5
tBu
tBu
17a
tBu
17b
Abb. 2.1.2 Schematische Molekülstruktur der Epimere 17a und 17b.
Dazu werden die chemischen Verschiebungen und Kopplungskonstanten von 17b diskutiert
und mit 17a verglichen. Eine Auflistung der NMR-Daten von 17a und 17b ist in Tabelle
2.1.1 zu finden. Wie man an den Peaks P1, P2 und P3 von 17b erkennen kann, liegt die
Annahme eines Spinsystem höherer Ordnung nahe. Daher können den Spektren nicht alle
Kopplungsdaten direkt entnommen werden. Um die Kopplungsdaten von 17a und 17b
34
dennoch vergleichen zu können, wurde das
31
P-NMR-Spektrum von 17b simuliert
(Abb. 2.1.3).[41] Die Simulation gelang unter Annahme eines ABCDE-Spinsystems. Die aus
der Simulation bestimmten
31
P,31P-Kopplungskonstanten von 17a und 17b sind in Tabelle
2.1.2 aufgeführt. Generell wurde in dieser Arbeit auf die Ermittlung der relativen Vorzeichen
der Kopplungskonstanten verzichtet. Die genannten Größen stellen daher nur die Beträge der
Kopplungskonstanten dar. Da die Übereinstimmung der simulierten Spektren alle
wesentlichen Signalkonturen liefert, kann davon ausgegangen werden, dass bereits die
entscheidenden Kopplungsphänomene der untersuchten Käfige richtig erfasst wurden.
Das Signal von P4 findet sich bei 17b bei 366.1 ppm um ca. 27 ppm tieffeldverschoben
gegenüber δ(P4) = 339.6 ppm bei 17a. Beide Signale liegen damit in der Region, die für P=CDoppelbindungen charakteristisch ist.[39] Der Peak von P5, das keine direkt benachbarten
Kopplungspartner besitzt, ist für 17b bei δ(P5) = 88.3 ppm zu beobachten. Bei 17a liegt das
entsprechende Signal bei δ(P5) = 105.0 ppm. Im Gegensatz zu 17a spaltet P5 bei 17b deutlich
stärker auf und liegt als Dublett vom Quartett vor.
Tabelle 2.1.1 Chemische Verschiebung in ppm und ausgewählte Kopplungskonstanten in Hz in den 31P{1H}NMR- und 1H-NMR-Spektren von 17a und 17b.
δ(P4)
δ(P5)
δ(P1)
δ(P2)
δ(P3)
17a
339.6
105.0
-51.7
-112.5
17b
366.1
88.3
-18.7
-107.1
2
3
JP1P5
δ(H1)
-120.2
9.1
4.9
0
-107.9
128.4
4.1
36.6
JH1P5
Die große Aufspaltung des Signals kann der Kopplung 2JP5P1 zugeordnet werden. Sie beträgt
bei 17b 128.3 Hz. Diese Kopplung findet sich auch im komplizierten Aufspaltungsmuster von
P1 wieder. Die entsprechende Kopplung bei 17a ist wesentlich kleiner und beträgt nur 9.1 Hz.
Die im Vergleich zu 17a stark vergrößerte Kopplung 2JP1P5 bei 17b erreicht damit einen
Betrag, der auch mit einer 1JPP verträglich wäre. So lassen sich in der Literatur z.B. beim
Diphosphan P2H4 noch ähnlich große 1J-Kopplungskonstanten (1JPP = 108 Hz) finden. Auch
bei tertiären Phosphanen kommen ähnliche direkte Kopplungen vor, wie z.B. bei dem
zweifach
chlorierten
Diphosphiran
Cl2CP2(2,4,6-tBu3C6H2)(2,4,6-t(C5H11)3C6H2)
(1JPP = 138 Hz), jedoch sind diese Kopplungen in der Regel größer.[42,43] Alle anderen 2J- und
3
J-Kopplungskonstanten sind in beiden Verbindungen ähnlich groß. Bei 17b befindet sich das
Signal von P1 bei –18.7 ppm mit einer Kopplung 1JP1P2 von 212.0 Hz. Sie beträgt bei 17a
238.4 Hz und fällt damit etwas größer aus. Das Signal liegt mit δ(P1) = –51.7 ppm bei 17a
tieffeldverschoben gegenüber 17b. Die beiden Signale von P2 und P3 der Verbindung 17b
35
befinden sich bei 25 °C bei –107.1 und –107.9 ppm. Sie werden bei 50 °C isochron und sind
dann als ein Multiplett bei –107.9 ppm zu finden. Die Kopplungskonstante 1JP2P3 von 17b
beträgt 152.2 Hz. Sie entspricht damit fast der bei 17a aus dem Spektrum bestimmten
Kopplungskonstante zwischen P2 und P3. Die Signale der beiden Phosphoratome P2 und P3
liegen bei 17a bei –112.5 ppm und –120.2 ppm und damit deutlich weiter auseinander als die
entsprechenden Signale bei 17b. Dadurch spalten die Signale von P1, P2 und P3 durch deren
1
J-Kopplungen bei 17a zu Dubletts bzw. zum Dublett vom Dublett auf. Die relative Nähe der
Signale von P2 und P3 ruft bei 17b die Aufspaltung der Peaks P1, P2 und P3 zu Multipletts
hervor. Die beiden direkten Kopplungen
1
JP1P2 und 1JP2P3 17a und 17b belegen die
Konnektivität der Kette P1–P2–P3 beider Verbindungen. Es zeigt sich, dass alle Kopplungskonstanten mit Ausnahme von 2JP5P1 bei 17a und 17b ähnlich groß sind, wobei die
Konnektivitäten aller Phosphoratome unangetastet erscheinen. Zudem betreffen alle größeren
Abweichungen der chemischen Verschiebungen zwischen 17a und 17b die Atome H1, P1 und
P5. Diese beobachteten Unterschiede deuten auf einen Zusammenhang zwischen diesen
Atomen hin, der im Folgenden mit den zusätzlichen Daten aus dem 1H-NMR-Spektrum des
Gemisches von 17a/b näher betrachtet wird. Es kann aber schon durch die bisherigen
Gemeinsamkeiten davon ausgegangen werden, dass die Verbindungen 17a und 17b als
Epimere anzusehen sind.
Tabelle 2.1.2 Simulierte 31P,31P -Kopplungskonstanten von 17a und 17b in Hz. Der Simulation liegt ein
ABCDE-Spinsystem zugrunde.
2
JP4P5
3
JP4P1
2
JP5P1
2
JP5P2
2
JP5P3
1
JP1P2
2
JP1P3
1
JP2P3
17a
12.4
6.7
9.1
7.5
7.3
238.4
3.1
158.2
17b
11.2
4.2
128.3
9.0
6.4
212.0
5.9
152.2
Im 1H-NMR-Spektrum des Gemisches 17a/b finden sich jeweils vier Signale der tertButylgruppen zwischen 1.0 ppm und 1.7 ppm im Mengenverhältnis beider Substanzen. Bei
17b spaltet das P–H-Proton zu einem ddd-Signal bei δ(H1) = 4.1 ppm auf. Die direkte
Kopplung 1JH1P1 beträgt 198 Hz, zwei weitere 37 und 4 Hz. Durch ein protonengekoppeltes
31
P-NMR-Spektrum ließ sich die größere der beiden der Kopplungskonstante 3JH1P5 zuordnen,
während
2
JH1P2 nur 4 Hz beträgt. Das Signal von H1 von 17a befindet sich bei
δ(H1) = 4.9 ppm und damit ca. 0.8 ppm tieffeldverschoben gegenüber H1 von 17b.
36
P5
P4
366.4
366.0 365.6
90.0
89.0
88.0
87.0
P3
P2
P1
-15.5
-17.5
-18.5
-21.5
-105.0
-106.0
-107.0
-108.0
-109.0
Abb. 2.1.3 Simulation (oben) und gemessene (unten) 31P{1H}-NMR-Signale von 17b (122 MHz, CDCl3, 25°C).
Die Abweichung (RMS) zwischen gemessenem und berechnetem Spektrum beträgt 0.036. In der Simulation
wurde eine feste Linienbreite von 5.5 Hz verwendet.
Das beobachtete Doppeldublett resultiert aus den 1JH1P1 = 179 Hz und 2JH1P2 = 5 Hz. Der
auffallend große Unterschied des Kopplungsbetrags von 3JH1P5 bei 17a und 17b deutet auf
einen Karplus-artige Beziehnung zwischen den beiden Atomen H1 und P5 hin. Die KarplusBeziehung stellt eine Korrelation zwischen der Größe von 3J-Kopplungskonstanten und den
zugeordneten Diederwinkeln in der NMR-Spektroskopie her (Abb. 2.1.4).[44,45] In der
Literatur findet sich für den speziell vorliegenden Fall einer 3J-Kopplung über H–P–C–PBindungen keine experimentellen Vergleichsbefunde. Eine analoge Konstellation wurde
allerdings für 3JPH-Kopplungen bei Phosphonaten (P–C–C–H) und Hydroxyphosphonaten
gefunden.[46,47] Die dort beschriebene Beziehung ergibt deutlich größere 3J-Kopplungskonstanten für Diederwinkel φ zwischen 150 - 180° als bei Winkeln zwischen 45 - 90°, was
im Einklang mit den hier gemachten Beobachtungen steht, wenn man die Inversion von P1 als
Ursache für die Bildung des Epimerenpaars 17a/b akzeptiert und 17a als die Spezies
identifiziert, bei der H1 auf der gleichen Seite des Käfigs steht wie P5.
37
Abb. 2.1.4 Newman-Projektion mit Blick auf die Achse P1–C4. Gauche- (im laufenden Text als cis bezeichnet)
und trans-Stellung von H1 zu P5 für die Verbindungen 17a und 17b, (X = freies Elektronenpaar).
Analoge Beobachtungen von Epimeren findet sich auch bei den [M(CO)5]-Komplexen 44a-d,
45a-d, 46a-d und des Ruthenium(II)-Komplexes 47 wieder, die in den Kapiteln 2.2 und 2.3
besprochen werden (Abb. 2.1.5). Die chemischen Verschiebungen der Phosphoratome und
des P–H-Protons H1, sowie ausgewählte Kopplungskonstanten von 17a und 17b sind in
Tabelle 2.1.3 den Werten, die für die [Mo(CO)5]-Komplexe 45a-d und den Ruthenium(II)Komplex 47 ermittelt wurden, gegenübergestellt. Es lässt sich erkennen, dass die
Unterschiede, bei den NMR-Parametern von 17a und 17b in ähnlicher Größe auch bei den
Epimeren der [M(CO)5]-Komplexserie a-d beobachtet werden können. Der Ruthenium(II)Komplex 47, der sowohl in Lösung als auch im Kristall als Metallkomplex des einzelnen
Epimers 17b erhalten werden konnte, dient der Absicherung der spektroskopisch ermittelten
Konfiguration. Die Kopplung 3JH1P5 liegt bei 17b in ähnlicher Größenordnung wie bei den
Epimeren der Metallkomplexe mit den Indices b, d und bei 47, in denen das Proton jeweils
trans zu P5 steht. Im Gegensatz hierzu ist eine derartige trans-Kopplung bei 17a nicht
vorhanden. Dies ist vergleichbar mit der Situation, die in den Metallkomplexreihen a und c
gefunden wurde. Ebenso verhält sich die 2J-Kopplung zwischen P1 und P5, die bei 17b und
seinen Metallkomplexen groß und bei 17a und seinen Derivaten klein ist. Eine Tieffeldverschiebung des Signals von H1 im 1H-NMR wie bei 17b im Vergleich mit 17a lässt sich
auch bei den Epimeren b und a bzw. deren Koordinationsisomeren d und c wiederfinden.
Auch die bei 17b zu 17a beobachtete Hochfeldverschiebung des Signals von P5 auf ca. 88
ppm ist bei b und a bzw. d und c vorhanden. Die NMR-Daten der Metallkomplexe bestätigen
die getroffene Zuordnung der Orientierung des Protons im Bezug auf das P5Deltacyclengerüst. Von 47 konnte zudem eine Kristallstruktur erhalten werden, bei der die
Position von H1 aufgrund der Koordination des Ruthenium-Fragments an P1 verifiziert
werden konnte.
38
H1
tBu
P4
P5
P1
tBu
2
P3 P
tBu
H1
tBu
P4
P5
M
P1
tBu
2
P3 P
P4
tBu
P5
P1
tBu
2
P3 P
tBu
tBu
17a
45c, 47
45a
H1
P5
tBu
M
tBu
P1
tBu
2
P3 P
M
tBu
tBu
tBu
P4
H1
tBu
P4
P5
H1
H1
tBu
P1
tBu
2
P3 P
P4
tBu
P5
P1
tBu
2
P3 P
M
tBu
tBu
tBu
tBu
17b
45d
45b
45: M = Mo(CO)5
47: M = RuCl2( 6-C6H6)
Abb. 2.1.5 Aus den Spektren abgeleitete Strukturen von 17a und 17b und ihrer Metallkomplexe 45a-d und 47
Tabelle 2.1.3 Chemische Verschiebung in ppm und ausgewählte Kopplungskonstanten in Hz in den 31P{1H}NMR- und 1H-NMR-Spektren von 17a, 17b, 45a, 45b, 45c, 45d und 47. Fett gedruckte Werte entsprechen
koordinierten Phosphoratomen.
δ(P4)
δ(P5)
δ(P1)
δ(P2)
δ(P3)
17a
339.6
105.0
-51.7
-112.5
17b
366.1
88.3
-18.7
45a
341.6
107.0
45c
349.1
45b
2
3
JP1P5
δ(H1)
-120.2
9.1
4.9
0
-107.1
-107.9
128.4
4.1
36.6
-42.4
-84.6
-140.5
9.1
5.3
5.8
113.4
-34.8
-118.9
-110.2
38.3
6.4
0
366.7
89.8
-11.0
-80.0
-125.1
121.4
4.3
39.5
45d
359.3
85.4
-10.2
-108.9
-119.0
115.5
5.1
27.9
47
351.7
78.5
22.9
-115.4
-126.6
77.2
4.9
26.3
JH1P5
In den vorliegenden Röntgenstrukturanalysen des P5-Deltacyclens 17 konnte die
Positionierung des Protons im Festkörper aufgrund der Restelektronendichte des unmittelbar
benachbarten freien Elektronenpaars am sekundären Phosphanatom nicht eindeutig
zugeordnet werden.[20] Nach der Destannylierung von 16 beträgt das Verhältnis von 17a und
39
17b in den untersuchten Lösungen immer ca. 1 : 0.15. Die Anteile in den Epimerenmischungen der [M(CO)5]-Komplexe des P5-Deltacylcens entsprechen jedoch nicht diesem
Verhältnis. Daher lag die Vermutung nahe, dass die Produktmischung nicht durch die
bevorzugte Protonierung einer Seite des P5-Deltacyclenkäfigs zustande kommt, sondern dass
die beiden Epimere 17a und 17b in einem Gleichgewicht stehen.
Aufgrund dieses Befundes wurden von T. Shubina DFT-Rechnungen zur Epimerisierung von
P5-Deltacyclen 17 angefertigt. Für die Inversion von P1, die der Epimerisierung von 17 zu
den beiden Epimeren 17a und 17b zugrunde liegt, ergibt sich eine Barriere von +31 kcal mol-1
(dE+ZPE, B3LYP/cc-pVDZ)[37]. Damit kann ein schnelles Epimersierungsgleichgewicht von
17a und 17b über diesen Mechanismus bei Raumtemperatur ausgeschlossen werden.
Andererseits beträgt der berechnete Energieunterschied beider Epimere nur 1.25 kcal mol-1.
Es könnte also durchaus möglich sein, dass die recht hohe Inversionsbarriere durch einen
anderen Reaktionsweg umgangen wird. Aus der Literatur ist bekannt, dass chirale sekundäre
Phosphane aufgrund ihrer amphoteren Natur racemisierungsanfällig sind. Eine Racemisierung
kann aufgrund der Basizität des Phosphors über eine Protonierung zum achiralen
Phosphoniumion erfolgen.[48] Alternativ kann man sich auch ein basisch katalysierten
Mechanismus vorstellen, bei dem P1 erst deprotoniert und dann wieder reprotoniert wird. Das
intermediäre sekundäre Phosphid wäre wieder achiral in dieser Position. Mithilfe deuterierter
protischer Lösungsmittel konnten in der Literatur H/D-Austauschreaktionen an sekundären
Phosphanen beobachtet werden.[49,50] Ein solches Experiment wurde auch mit 17a/b
durchgeführt. Gibt man einige Tropfen D2O zu einer Lösung von 17a/b in THF, findet an P1
der erwartete H/D-Austausch statt (Abb. 2.1.6). Er lässt sich am besten bei den Signalen von
17a beobachten. Im 31P{1H}-NMR-Spektrum erscheint das in 17a durch die Kopplung 1JP1P2
zum Dublett aufgespaltene Signal von P1 für P–D um 1.5 ppm hochfeldverschoben als
Dublett von Tripletts im Intensitätsverhältnis 1 : 1 : 1 mit einer Kopplungskonstante 1JP1D1
von 27.6 Hz. Die aus dem 1H-NMR-Spektrum bestimmte Kopplungskonstante 1JP1H1 liegt für
17a bei 179.1 Hz. Das Verhältnis der Kopplungskonstanten 1JP1H1 : 1JP1D1 beträgt 6.5 und
folgt damit dem Quotienten der gyromagnetischen Verhältnisse beider Kerne. Das bedeutet
für den Ersatz von H1 durch D1, dass keine signifikanten Veränderungen der
Molekülgeometrie erfolgt sind. Eine leichte Hochfeldverschiebung um 0.4 ppm ist auch beim
benachbarten Phosphoratom P2, jedoch nicht mehr bei P3 erkennbar. Nach 30 Minuten sind
mehr als die Hälfte, nach 12 h bereits 95 % der Protonen gegen Deuteronen ausgetauscht. Das
stark aufspaltende Phosphoratom P1, an dem auch bei 17b das Proton gebunden ist verschiebt
40
sich beim H/D-Austausch ebenso ins Hochfeld. Der genaue Wert kann aber aufgrund der
Aufspaltung des Signals von P1 bei 17b nicht ermittelt werden.
P3
P2(D)
P1H
P1D
P2(H)
-53.4
-54.2
-55.0
-55.8
-56.6
-57.4
-113.5
-115.5
-117.5
-119.5
-121.5
-123.5
Abb. 2.1.6 Ausgewählte Signale von 17a aus dem 31P{1H}-NMR-Spektren (122 MHz, CDCl3, 25°C) von 17a/b
in D2O/THF nach 30 Minuten (oben) und 12 h (unten) nach Probenpräparation.
Das Konzentrationsverhältnis der Verbindung 17a zu 17b blieb auch nach dem
Isotopenaustauschexperiment mit D2O konstant. Das spricht für ein Gleichgewicht zwischen
den beiden Verbindungen. Um diesen Sachverhalt zu überprüfen, wurden AustauschSpektroskopie-Messungen (EXSY) mit dem Gemisch 17a/b von W. Bauer angefertigt. Die
Messungen wurden bei 50 °C durchgeführt. Bei dieser Temperatur sind die Signale für P2
und P3 im Fall 17b isochron, während sich bei 25 °C noch zwei getrennte Signale für die
beiden Phosphoratome ergeben. Aus den in Abb. 2.1.7 gezeigten
31
P-EXSY-Spektren der
Käfigverbindung ist ersichtlich, dass 17a mit der Struktur 17b tatsächlich in einem
dynamischen Gleichgewicht steht. Jeder der zu 17a und 17b gehörigen Peaks zeigt mit
seinem Austauschpartner Kreuzsignale auf beiden Seiten der Diagonalsignale. Die mit X
gekennzeichneten Signale sind Verunreinigungen, die durch Umkristallisieren entfernt
werden können. Sie zeigen dementsprechend auch keine Kreuzsignale. Das NMR-Zeitfenster
für die durchgeführten EXSY Messungen beträgt 600 ms. Dieses kann zur Einordnung der
Austauschgeschwindigkeit herangezogen werden. Innerhalb dieser Zeit muss der Austausch
bei 50 °C vollständig vollzogen sein. Bei einem rascheren Austausch müsste eine Koaleszenz
der Signale in den NMR-Spektren beobachtet werden.
41
P5 17a
P4 17a
P4
17b
P5
17b
X
X
X
P2 17a
P1 17a
P3 17a
P2/P3
17b
P1
17b
Abb. 2.1.7 31P-EXSY-Spektren (202 MHz, CDCl3, 50°C) des P5-Deltacyclens 17a und 17b. Verunreinigungen
sind mit X gekennzeichnet.
Das P5-Deltacyclen ist also nicht mit einer weiteren Verbindung verunreinigt, sondern es
besteht ein Gleichgewicht zwischen zwei Epimeren 17a und 17b. Diese Epimeren-Mischung
wurde auf ihre Ligandeigenschaften hin untersucht.
42
2.2 Chrom-, Molybdän- und Wolframpentacarbonylkomplexe des P5-Deltacyclens
2.2.1 Darstellung der Chrom-, Molybdän- und Wolframpentacarbonyl-P5deltacyclenkomplexe 44, 45 und 46
Bei der Umsetzung von geeigneten reaktiven Übergangsmetallcarbonylkomplexen mit dem
Epimerengemisch von 17a und 17b sind mehrere Phosphordonoren als Koordinationsstellen
möglich. Alle Phosphoratome der beiden Käfigepimere bilden potentielle Ligandfunktionen
(Kapitel 1.3). Sie unterscheiden sich jedoch hinsichtlich ihrer Hybridisierung sowie ihrer
sterischen
Zugänglichkeit.
Die
vier
tert-Butyl-Substituenten
schirmen
die
freien
Elektronenpaare der Phosphoratome unterschiedlich stark ab. Um die reaktivsten Positionen
für
die
Metallkoordination
herauszufinden,
wurde
das
racemische
Gemisch
der
Käfigverbindungen 17a und 17b mit in situ generierten [M(CO)5THF]-Komplexen (M = Cr,
Mo, W) umgesetzt (Abb. 2.2.1).
H
tBu
P
tBu
P
P
P
H
P
tBu
P
P
P
M(CO)5
P
P
P
P
M(CO)5
tBu
tBu
tBu
44a, 45a und 46a
44b, 45b und 46b
THF
P
+ [M(CO)5THF]
-40°C
H
tBu
tBu
44: M = Cr
45: M = Mo
46: M = W
P
P
P
(OC)5M
tBu
M(CO)5
P
tBu
tBu
17a/b
P
tBu
+
P
tBu
tBu
H
tBu
P
H
P
tBu
+
P
P
P
P
tBu
tBu
tBu
tBu
44c, 45c und 46c
44d, 45d und 46d
Abb. 2.2.1 Koordination der Metallpentacarbonyle von Chrom, Molybdän und Wolfram am P5-Deltacyclen.
Bildung der Isomere a, b, c und d.
Ein Carbonyl-Ligand der Metallhexacarbonyle wurde hierfür jeweils durch Belichtung einer
THF-Lösung mit einer Hg-Dampflampe durch THF ersetzt und dieses Gemisch bei -40 °C zu
einer Lösung des Gemisches aus 17a und 17b in THF gegeben. Unter Substitution des
schwach gebundenen THF-Moleküls können dann [M(CO)5]-Fragmente an ein oder mehrere
Phosphoratome des Käfigs gebunden werden. Die Metallhexacarbonyle wurden hierbei
43
sowohl
äquimolar
als
auch
in
hohem
Überschuss
eingesetzt.
Ungeachtet
der
Reaktionsdurchführung entstehen bei der Reaktion Komplexgemische mit einem einzelnen
koordinierten [M(CO)5]-Fragment pro Molekül P5-Deltacyclen. In den FD-Massenspektren
erscheinen daher die Molekülpeaks mit 100 % Intensität bei m/z = 625 für Chrom, 668 für
Molybdän und 757 für Wolfram. Diese Werte entsprechen den jeweiligen Einkernkomplexen.
Weitere Peaks, die Mehrkernkomplexen oder Dimeren zugeordnet werden könnten, werden
nicht beobachtet. Die Zusammensetzung bestätigt sich durch die Elementaranalysen der
Gemische von 44a-d, 45a-d und 46a-d. Ein Vorliegen als Mehrkernkomplexe kann somit für
alle vier Verbindungen ausgeschlossen werden. Die Gesamtausbeute der Chrom-, Molybdänund Wolframverbindungen betragen 69 %, 78 % und 72 %. Die erhaltenen Verbindungen
werden in den folgenden Kapiteln charakterisiert.
2.2.2 Molekülstruktur von Molybdänpentacarbonyl-P5-deltacyclen 45a
Von der Verbindung 45a konnten aus n-Hexan bei +4 °C gelbe Kristalle gezüchtet werden,
die für eine Röntgenstrukturanalyse geeignet waren. In Abb. 2.2.2 ist die Molekülstruktur von
45a gezeigt. Die Kristallstruktur von 45a weist eine trikline Elementarzelle in der
zentrosymmetrischen Raumgruppe P 1 (Nr. 2) auf. In der Elementarzelle sind zwei Moleküle
von 45a vorhanden, die Bild und Spiegelbild eines Enantiomerenpaars darstellen. Vergleicht
man die in Tabelle 2.2.1 aufgeführten Bindungslängen und Bindungswinkel innerhalb der
Käfigstruktur mit denen des unkoordinierten Käfigs 17,[19,20] so kann man feststellen, dass
Abweichungen innerhalb des Käfiggerüstes minimal ausfallen. Die größten Unterschiede
lassen sich bei den Bindungen rund um P2 finden, an dem die [M(CO)5]-Einheit koordiniert
ist. Sie sind um ca. 2 pm kürzer als vor der Koordination. Die tert-Butylgruppen werden
durch die Koordination ebenfalls nicht wesentlich beeinflusst. Deren C–C-Bindungslängen
bleiben nahezu identisch und ihre Bindungswinkel weichen maximal 2° von denen des
unkoordinierten P–H-Käfigs ab. Die Winkel der Carbonylgruppen zueinander weichen etwas
mehr von der idealen Oktaedergeometrie des Molybdänhexacarbonyls ab. Dort sind Mo–
C≡O-Bindungen linear aufgebaut. Bei 45a weichen die Winkel C–Mo–C und Mo–C≡O um
bis zu 3.7° von dem Wert 180° ab. Die Winkel P2–Mo–C7 und P2–Mo–C8 betragen 95.5 und
92.8°. Diese Abweichung von 90° verdeutlicht die sterische Abstoßung der Carbonylliganden
durch die tert-Butylgruppe an C1. Die Winkel der anderen beiden cis-ständigen Carbonyle
liegen mit 86.5 und 87.7° unterhalb von 90°, da sie im Festkörper in Richtung der sterisch
weniger anspruchsvollen Seite des Käfigs weisen. Der sterische Anspruch des P5-
44
Deltacyclenliganden verändert also vor allem die Struktur des [M(CO)5]-Fragments, während
der Käfig selbst im Wesentlichen unverändert bleibt. Dies kann auf die dreidimensionale
Vernetzung der P–P-, P–C- und C–C-Gerüstbindungen zurückgeführt werden, während die
Carbonylliganden des oktaedrisch koordinierten Molybdänatoms jeweils nur mit einer
einzelnen Bindung am Metallzentrum fixiert sind. Die Bindungsabstände von Molybdän zu
den cis-ständigen Carbonylkohlenstoffen beträgt 205 pm, die Bindung zum trans-ständigen ist
auf 200 pm verkürzt. Dies lässt sich anhand der Metall-CO-π-Rückbindung erklären. Liegen
Phosphordonor und CO-Akzeptor trans zueinander, so kann der π-Akzeptor-Ligand CO von
der σ-Donor-Wirkung des Phosphoratoms profitieren und die Bindung zum Metall verkürzt
sich. Der Bindungsabstand zwischen P2 und Mo beträgt 253 pm. Der Diederwinkel zwischen
H1–P1–C4–P5 beträgt 44.1°. Dieser ist für die Zuordnung der Kristallstruktur zu den in den
Spektren beobachtbaren Epimeren wichtig.
O2
O1
P1
C6
C5
C9
H1
O5
Mo
C4
C7
C2
P5
O3
P2
C8
C1
P4
C3
P3
O4
Abb. 2.2.2 Molekülstruktur eines Enantiomers von 45a im Kristall. Die Wasserstoffatome der tert-Butylgruppen
wurden der Übersicht halber weggelassen.
45
Tabelle 2.2.1 Ausgewählte Bindungslängen und Bindungswinkel von 45a in pm und °
P1–C4
187.68(17)
C4–C2–P4
107.09(10)
P5–C4–P1
103.37(8)
P1–P2
214.88(6)
C4–C2–P3
107.36(10)
C1–P2–Mo
143.60(5)
P2–C1
186.11(16)
P4–C2–P3
98.06(7)
P2–Mo–C5
86.52(5)
P2–P3
219.51(6)
C2–C4–P5
101.28(10)
P2–Mo–C6
87.68(5)
P3–C1
185.80(16)
C1–P3–P2
53.89(5)
P2–Mo–C7
95.46(5)
P3–C2
192.38(17)
P3–C1–P2
72.34(6)
P2–Mo–C8
92.75(5)
P4–C3
168.79(16)
P3–C1–P5
108.86(8)
P2–Mo–C9
172.66(5)
P4–C2
189.26(17)
P5–C1–P2
110.31(8)
C5–Mo–C7
176.32(7)
P5–C3
184.15(17)
C1–P2–P3
53.76(5)
C6–Mo–C8
177.15(6)
P5–C1
189.37(17)
C4–P1–P2
94.86(5)
Mo–C5–O1
177.34(17)
P5–C4
189.74(16)
P2–P1–Mo
135.09(2)
Mo–C6–O2
177.57(16)
C2–C4
159.3(2)
C4–P1–Mo
110.40(2)
Mo–C7–O3
178.12(16)
P2–Mo
252.68(4)
C2–C4–P1
111.00(10)
Mo–C8–O4
178.11(15)
Die Bindungslängen und Bindungswinkel der von S. Huguet-Torrell bestimmten
Kristallstrukturen von 44a und 46a weichen nur minimal von denen bei 45a gefundenen
ab.[35] Die Bindungslängen der Bindungen von P2, an dem die [M(CO)5]-Fragmente bei 44a,
45a und 46a koordiniert sind, sind in Tabelle 2.2.2 aufgeführt und denen des P5-Deltacyclens
17 gegenübergestellt.
Tabelle 2.2.2 Vergleich ausgewählter Bindungslängen von 17[20], 44a[35], 45a und 46a[35] in pm.
46
P2–P1
P2–P3
P2–C1
P2–M
44a
215.65(6)
220.18(15)
186.98(15)
239.72(5)
45a
214.88(6)
219.51(6)
186.11(16)
252.68(4)
46a
215.54(6)
220.01(6)
186.47(16)
252.17(4)
17
216.49(13)
221.64(11)
188.8(3)
-
2.2.3 NMR-Spektroskopische Charakterisierung der Chrom-, Molybdän- und Wolframpentacarbonyl-P5-deltacyclenkomplexe 44a-d, 45a-d und 46a-d
In den
31
P-NMR-Spektren der Reaktionsmischungen zeigen sich stets für alle drei Metalle
vier isomere Käfigkomplexe. Versuche, diese Mischungen säulenchromatographisch oder
durch fraktionierte Kristallisation zu trennen, blieben erfolglos. Auch die NMR-Spektren der
isolierten Kristalle von 44a, 45a und 46a zeigen in Lösung wieder alle vier Isomere. Das
bedeutet, in den Lösungen isomerisieren die rein kristallisierten Isomere zu einer Mischung
aus allen vier Komplexen. Dieser Befund schließt die Isolation von reinen Isomeren aus,
wenn die Substanzen in Lösung gehandhabt werden. Abb. 2.2.3 zeigt beispielhaft ein
31
P{1H}-NMR-Spektrum der Mischung von 45a-d. Es lässt sich erkennen, dass die Mischung
aus vier verschiedenen Verbindungen mit jeweils fünf Phosphoratomen besteht, die in
unterschiedlich großen Anteilen vorliegen. Die einzelnen Anteile variieren je nach Ansatz und
verwendetem [M(CO)5]-Fragment. Generell ist aber der Anteil von 44b, 45b und 46b immer
der kleinste.
Abb. 2.2.3 31P{1H}-NMR-Spektrum (122 MHz, CDCl3, 25°C) der Isomerenmischung von 45a-d.
47
Die jeweils vier Verbindungen können durch die unterschiedlich großen Koordinationsverschiebungen der drei Metallatome jeweils als Paare zweier Koordinationsisomere
identifiziert werden, bei denen die Metallkoordination entweder an P1 oder an P2 erfolgt
(Tabelle 2.2.3). Innerhalb der Komplexreihen a und b unterscheiden sich die chemischen
Verschiebungen von P2 stark während sie bei P1 nur wenig voneinander abweichen. Bei c
und d ist dagegen die Differenz von δ(P2) zwischen den Metallpentacarbonylkomplexen groß
und fällt für δ(P1) gering aus. Die Metallkoordination erfolgt daher bei Metallkomplexen des
Typs a und b an P2 und bei c und d an P1. Die Signale der weiteren Phosphoratome P3 - P5
zeigen bei analogen Verbindungen der Chrom-, Molybdän- und Wolframkomplexe nahezu
identische chemische Verschiebungen. Die genaue Analyse der einzelnen Verbindungen
erfolgt in den folgenden Kapiteln.
Tabelle 2.2.3 δ(P1) und δ(P2) in ppm der 12 untersuchten [M(CO)5]-Komplexe.
P1
P2
P1
P2
44a
-42.0
-56.9
44b
-11.7
-51.9
45a
-42.4
-84.6
45b
-11.0
-80.0
46a
-39.7
-111.7
46b
-9.7
-106.7
P1
P2
P1
P2
44c
-10.3
-118.8
44d
13.1
-109.1
45c
-34.8
-118.9
45d
-10.2
-108.9
46c
-56.4
-116.9
46d
-33.0
-105.8
Für die P1- und P2-Koordination lassen sich jeweils zwei Signalsätze erkennen, so dass in
allen drei Fällen vier verschiedene [M(CO)5]-Komplexe auftreten. Da durch die
Massenspektren und Elementaranalysen Mehrkernkomplexe und Dimere als Produkte
ausgeschlossen werden konnten, deuten die doppelten Spektrensätze beider Koordinationsisomere wie bei 17a/b auf die Existenz von Epimeren hin. Das Konzentrationsverhältnis der
Epimere 17a und 17b in Lösung beträgt immer ca. 1 : 0.15. Bei den [M(CO)5]-Komplexen
findet man dieses Verhältnis nicht. Allerdings stehen 17a und 17b in einem raschen
Gleichgewicht miteinander, während der Isomerisierungsprozess für die Metallkomplexe
nicht unerwartet deutlich langsamer ist, so dass bei Raumtemperatur die Gleichgewichte nicht
vollständig erreicht werden. Höhere Temperaturen zur Förderung der Isomerisierungsgeschwindigkeit verbieten sich aber, weil die Metalle dabei wieder abgespalten und 17a/b
48
regeneriert werden. Das Vorliegen von Koordinationsisomeren und Epimeren zeigt sich auch
in den 1H-NMR-Spektren der Mischungen. Die chemische Verschiebung des Protons H1 und
die Aufspaltungen der Signale durch die 1H,31P-Kopplungen fallen in den einzelnen isomeren
Verbindungen stark unterschiedlich aus. Abb. 2.2.4 zeigt das 1H-NMR-Spektrum von 44a-d.
Die genaue Diskussion der NMR-Spektren der einzelnen Verbindungen erfolgt in den
folgenden Kapiteln.
Da alle vier Isomere der [M(CO)5]-Komplexe 44a-d, 45a-d und 46a-d als Racemate
vorliegen und die stereogenen Zentren somit sowohl R- als auch S-Konfiguration besitzen
können, wird im Folgenden eine Unterscheidung anhand der Stellung des Protons H1 in
Relation zu P5 vorgenommen: Bei den Verbindungen der Komplextypen a und c steht das
Proton am P1 cis (bzw. gauche) zu P5, während es bei den Komplexfamilien b und d trans
dazu steht.
tBu 44a-d
H1 44a
H1 44d
H1 44c
H1 44b
6.50
ppm7.0
6.00
6.0
5.50
5.0
5.00
4.0
4.50
3.0
4.00
2.0
1.0
0.0
Abb. 2.2.4 1H-NMR-Spektrum (300 MHz, CDCl3, 25°C) der Isomerenmischung von 44a-d.
2.2.3.1 NMR-Spektroskopische Charakterisierung der Chrom-, Molybdän- und
Wolframpentacarbonyl-P5-deltacyclenkomplexe 44a, 45a und 46a
Zunächst sollen die oft als Hauptkomponente auftretenden Verbindungen 44a, 45a und 46a
näher
betrachtet
werden.
Die
chemischen
Verschiebungen
und
ausgewählte
49
Kopplungskonstanten der Chrom-, Molybdän- und Wolframpentacarbonylkäfigverbindungen
44a, 45a und 46a sind in Tabelle 2.2.4 zusammengefasst. Abb. 2.2.5 zeigt die Struktur dieser
Verbindungen mit der in dieser Arbeit verwendeten Nummerierung der Phosphoratome.
Erkennbar ist, dass sich die chemische Verschiebung der unkoordinierten Phosphoratome bei
den unterschiedlichen [M(CO)5]-Komplexen 44a, 45a und 46a nur unwesentlich ändert. Beim
Phosphoratom P2 ist jedoch eine Hochfeldverschiebung des Signals von je ca. 28 ppm
zwischen 44a, 45a und 46a zu beobachten. Diese Signalverschiebung kommt durch die
Koordination der verschiedenen Metalle an P2 zustande.
Abb. 2.2.5 Schematische Molekülstruktur eines Enantiomers der Komplexserie a.
Tabelle 2.2.4 Chemische Verschiebung in ppm und ausgewählte Kopplungskonstanten in Hz in den 31P{1H}NMR-Spektren von 44a, 45a und 46a im Vergleich mit den beiden P5-Deltacyclenepimeren 17a und 17b.
1
JP1P2
1
JP2P3
2
P4
P5
P1
P2
P3
JP1P5
44a
343.6
108.2
-42.0
-56.9
-148.0
234.4
186.7
10.0
45a
341.6
107.0
-42.4
-84.6
-140.5
225.7
182.2
9.1
46a
341.9
106.7
-39.7
-111.7
-141.1
224.1
183.6
10.1
17a
339.5
105.0
-51.7
-112.5
-120.2
238.3
158.2
8.9
17b
366.1
88.3
-18.7
-107.1
-107.9
212.0
152.2
128.4
Koordinierte Phosphoratome verlagern einen Teil ihrer Elektronendichte auf die gebundenen
Metallzentren. Das führt zu einer vom koordinierten Metall abhängigen Änderung der
31
P-
NMR-Verschiebung des betreffenden Ligandkerns. Die Koordinationsverschiebung ∆δ ist
daher definiert als Differenz der chemischen Verschiebungen von komplexiertem und freiem
Ligand. Wie in Tabelle 2.2.4 aufgezeigt, tritt die stärkste Koordinationsverschiebung von
+55.6 ppm bei Chrom auf, während bei der Wolframverbindung nur eine geringe
50
Verschiebung von +0.8 ppm beobachtet wird. Aus der Literatur ist bekannt, dass die
31
P-
Koordinationsverschiebung durch [M(CO)5]-Fragmente der Chromtriade bei gleichen
Phosphanliganden bei Chrom im Vergleich zum Wolfram am stärksten ins Tieffeld erfolgt.
Die chemische Verschiebung des Phosphoratoms bei analogen Molybdänkomplexen liegt
stets dazwischen. Der regelmäßige Gang der ∆δ31P-Werte für die hier untersuchten [M(CO)5]P5-Deltacyclenkomplexe steht damit in voller Übereinstimmung.[51] Im
31
P{1H}-NMR-
Spektrum von 46a finden sich für P2 die Satelliten einer 1JP2W-Kopplung von 226 Hz, die die
Bindung P2–W belegen.
Im Folgenden werden die in Tabelle 2.2.4 angegebenen Werte der Metallkomplexe 44a, 45a
und 46a mit denen von 17a/b verglichen. Dabei zeigt sich, dass die Verbindungen des
Komplextyps a dem Epimer 17a zugeordnet werden kann. Die chemische Verschiebung von
P4 liegt in der üblichen Region für P=C-Doppelbindungen bei δ(P4) ca. 342 ppm und ist nur
unwesentlich gegenüber dem P5-Deltacyclenepimer 17a (δ(P4) ca. 340 ppm) verschoben.
Ebenso ist das Signal von P5 bei ca. 107 ppm im Vergleich zum Ausgangsmaterial 17a (δ(P5)
ca. 105 ppm) kaum verschoben. Zwei große Kopplungen sind in den 31P{1H}-NMR-Spektren
der Verbindungen 44a, 45a und 46a direkt erkennbar. Abhängig vom Metallatom liegen
1
JP2P3-Kopplungskonstanten zwischen 182 Hz und 187 Hz vor. Eine weitere große Kopplung
ist zwischen P1 und P2 in den Spektren von 44a, 45a und 46a beobachtbar. Die 1JP1P2Kopplungskonstanten liegen zwischen 224 Hz und 234 Hz. Damit ist P2 als mittleres
Phosphoratom der P–P–P-Einheit des Käfigs bei allen drei Verbindungen eindeutig
identifizierbar. Die starke Hochfeldverschiebung von P2 und P3 wird analog den
Phosphiranen durch die Ringspannung verursacht.[40] Bei P2 wird diese Verschiebung
teilweise durch die Koordinationsverschiebung kompensiert.
Um die Kopplungskonstanten der Phosphoratome zu ermitteln, die aus dem
31
P-NMR-
Spektrum nicht einfach ablesbar sind, wurde das Spektrum exemplarisch für den
Molybdänkomplex 45a simuliert.[41] Die Beträge der ermittelten Kopplungskonstanten sind in
Tabelle 2.2.5 zusammengefasst. Die simulierten Signale von 45a sind im
31 1
{ H}P-NMR-
Spektrum in Abb. 2.2.6 den experimentell beobachtbaren Signalen gegenübergestellt. Sowohl
die Käfigepimere 17a/b als auch alle Isomere der [M(CO)5]-Komplexe 45a-d, 46a-d und
47a-d weisen ABCDE-Spinsysteme auf. Teilweise führen Kopplungen zwischen mehreren
Phosphoratomen zu komplex aufgespaltenen Multipletts. So ergibt sich beispielsweise das in
Abb. 2.2.6 abgebildete Multiplett P5 des einzeln stehenden Kerns durch merkliche
Kopplungen allen anderen Phosphoratomen des Käfigs. Die Kopplungskonstanten mit drei
der vier Phosphoratome betragen ca. 10 Hz. Einzig die Kopplung mit P2 fällt mit 26 Hz mehr
51
als doppelt so groß aus. Alle weiteren Kopplungen über zwei bzw. drei Bindungen sind
kleiner. Die Kopplung 2JP5P1 fällt mit ca. 10 Hz fast identisch mit 17a aus. Damit lässt sich
aufgrund des Karplus-Zusammenhangs die Position von H1 eindeutig cis-ständig zu P5
festlegen.
Tabelle 2.2.5 Simulierte 31P,31P Kopplungskonstanten von Molybdänpentacarbonyl-P5-deltacyclen 45a in Hz.
1
JP1P2
225.8
2
JP4P5
10.3
2
JP5P2
25.8
2
JP4P3
1.3
3
JP4P2
5.7
1
JP2P3
182.3
2
JP5P1
9.1
2
JP5P3
10.3
2
JP1P3
0.2
3
JP4P1
7.8
P1
P4
P5
341.8 341.4
107.6
107.2
106.8
106.2 -41.0
-41.6
-42.2
-42.8
-43.4
P3
P2
-82.7
-83.3
-83.9
-84.5
-85.1
-85.7
-85.3
-139.2
-139.8
-140.4
-141.0
Abb. 2.2.6 Simulierte (oben) und gemessene (unten) Signale der Verbindung 45a aus dem 31P{1H}-NMRSpektrum (122 MHz, CDCl3, 25°C) der Isomerenmischung von 45a-d. Die Abweichung (RMS) zwischen
gemessenem und berechnetem Spektrum beträgt 0.019 Hz. In der Simulation wurde eine feste Linienbreite von 5
Hz verwendet.
In den 1H-NMR-Spektren des Komplextyps a treten die vier tert-Butylgruppen als separierte
Singuletts zwischen 1.2 und 1.7 ppm auf. Des Weiteren lässt sich bei ca. 5.3 ppm das Signal
des Wasserstoffkerns H1 erkennen, welches zum ddd aufspaltet. Die direkte Kopplung 1JH1P1
beträgt 176 Hz und entspricht dem Wert der P–H-Kopplung des unkoordinierten P5Deltacyclens 17a. Neben der großen
52
1
J-Kopplung treten noch zwei weitere kleine
Kopplungen von jeweils etwa 5 Hz auf. Möglich erscheinen eine 2J-Kopplung des Protons mit
P2 und 3J-Kopplungen mit P3 bzw. P5. Um die Kopplungspartner eindeutig zu identifizieren,
wurde ein protonengekoppeltes
der bereits erwarteten
1
31
P-NMR-Spektrum aufgenommen. Dort lassen sich neben
J-Kopplung zwischen P1 und H1 noch P2 und P5 als
Kopplungspartner erkennen. Analog zur Verbindung 17a lässt sich keine Kopplung 3JH1P5 bei
den [M(CO)5]-Komplexen des Typs a finden. Die Kopplung ist bei 17b aufgrund der
Karplus-Beziehung 37 Hz groß. Damit bestätigt sich auch im 1H-NMR-Spektrum die
Zuordnung der Komplexisomere a zum Epimer 17a.
Da die Verbindungen 44a-d, 45a-d und 46a-d jeweils nur als Mischung von vier einkernigen
Komplexen vorliegen und eine eindeutige Zuordnung aller
Verbindung schwer möglich ist, wird die Diskussion der
13
13
C-Signale zu der jeweiligen
C-NMR-Daten am Ende dieses
Kapitels erfolgen.
2.2.3.2 NMR-Spektroskopische Charakterisierung der Chrom-, Molybdän- und
Wolframpentacarbonyl-P5-deltacyclenkomplexe 44b, 45b und 46b
Die beiden Komplexfamilien a und b stellen Epimere dar, die sich nur in der Konfiguration
von P1 unterscheiden. Abb. 2.2.7 zeigt die schematische Struktur der Verbindungen 44b, 45b
und 46b mit der Nummerierung der Phosphoratome. Auch bei diesen zeigen sich große
Übereinstimmungen bei den chemischen Verschiebungen in den 31P-NMR-Spektren zwischen
den verschiedenen [M(CO)5]-Komplexen, die sich als Gruppe dem Epimer 17b zuordnen
lassen. Die spektroskopischen Daten sind in Tabelle 2.2.6 zusammengefasst. Die
31
P-NMR-
Signale von 45b sind in der Abb. 2.2.8 aufgeführt.
Abb. 2.2.7 Schematische Molekülstruktur eines Enantiomers der Komplexserie b.
53
Wie bei 44a tritt auch bei 44b eine starke Koordinationsverschiebung von +55.2 ppm für P2
auf. Analog zur Komplexfamilie a findet man für den Molybdän- und Wolframkomplex 45b
und 46b geringere Koordinationsverschiebungen von +27.1 ppm bzw. +0.4 ppm. Aufgrund
des geringen Anteils von etwa 5 % der Verbindung 46b in der Produktmischung von 46a-c
sind für 46b keine Wolfram-Satelliten erkennbar.
Tabelle 2.2.6 Chemische Verschiebung in ppm und Kopplungskonstanten in Hz in den 31P{1H}-NMR-Spektren
von 44b, 45b und 46b
1
JP1P2
1
2
P4
P5
P1
P2
P3
JP2P3
JP1P5
44b
368.3
90.9
-11.7
-51.9
-131.8
214.1
190.3
121.4
45b
366.7
89.8
-11.0
-80.0
-125.1
205.0
184.5
121.4
46b
366.7
89.4
-9.7
-106.7
-125.6
202.9
186.5
120.8
17a
339.5
105.0
-51.7
-112.5
-120.2
238.3
158.2
8.9
17b
366.1
88.3
-18.7
-107.1
-107.9
212.0
152.2
128.4
Vergleicht man Tabelle 2.2.4 und Tabelle 2.2.6 hinsichtlich der direkten Kopplungen 1JP1P2
und 1JP2P3 der Komplexserien a und b so findet man ähnliche Werte. Die Konnektivität der
direkten Nachbarn P1, P2 und P3 erscheint somit unangetastet. Bei näherer Betrachtung fällt
eine Tendenz innerhalb einer Metall-Reihe auf: Die
31
P,31P-Kopplungen der Chrom-
verbindungen weisen sowohl bei 44a, als auch bei 44b die größten Werte im Vergleich zu den
Molybdän- und Wolframverbindungen 45a/b und 46a/b auf, die sich nur wenig voneinander
unterscheiden.
Die Differenz der chemischen Verschiebungen der einzelnen Signale in den
31
P-NMR-
Spektren, die bei den Epimeren 17a und 17b beobachtbar ist, findet sich auch bei den
Komplexserien a und b wieder. Die Signale von P4 sind bei den Komplexen des Typs b bei
ca. 367 ppm zu beobachten. Im Vergleich zur Komplexserie a sind sie um ca. 25 ppm ins
Tieffeld verschoben, was der Differenz zwischen 17a und 17b nahezu entspricht. Wie auch
für 17a/b beobachtet ist die chemische Verschiebung von P2 der Serie b im Vergleich zu a
nur um ca. 5 ppm tieffeldverschoben. Allerdings sind die Unterschiede bei den angrenzenden
Phosphoratomen P1 und P3 deutlicher ausgeprägt. Verglichen mit a ist P3 der Komplexreihe
b um ca. 16 ppm und P1 sogar um ca. 30 ppm tieffeldverschoben. Diese unterschiedliche
chemische Verschiebung der beiden Signale ist auch bei 17a und 17b zu beobachten. Eine
deutliche Änderung der chemischen Verschiebung ist auch bei P5 beobachtbar. Analog zu
54
17a und 17b erscheinen die Peaks von P5 in b gegenüber a um ca. 17 ppm auf ca. 90 ppm
hochfeldverschoben. Zusätzlich zur deutlichen Verschiebung von P1 und P5 tritt zwischen
den beiden Phosphoratomen bei b eine verhältnismäßig große Kopplung 2JP1P5 von 121 Hz auf
wie sie auch schon bei 17b beobachtet wurde. Im Vergleich dazu fällt die Kopplung 2JP1P5 bei
17a und bei den Komplexen der Serie a mit ca. 9 Hz eindeutig kleiner aus. Da die Kopplung
2
JP1P5 bei 17b einen ähnlichen Betrag aufweist, ist neben den schon diskutierten
Ähnlichkeiten in den chemischen Verschiebungen eine eindeutige Zuordnung der [M(CO)5]Komplexe des Typs b zum Käfigepimer 17b möglich. Diese Zuordnung wird auch in der
folgenden Diskussion des 1H-NMR-Spektrums bestätigt.
P4
91.00
367.50 367.00 366.50 366.00 365.50
367.0
P1 45d
P5
366.0 91.0
90.50
90.00
90.0
89.50
89.00
89.0
88.50
P2
P1 45b
-9.0
-10.0
-11.0
-12.0
-9.0
-10.0
-11.0
-12.0
-78.0
-78.0
-79.0
-80.0
-80.0
P3
-81.0
-82.0
-82.0
-124.0
-125.0
-126.0
-124.0
-125.0
-126.0
Abb. 2.2.8 Ausgewählte Signale von 45b aus dem 31P{1H}-NMR-Spektrum (122 MHz, CDCl3, 25°C) des
Gemisches von 45a-d. Für P1 von 45b überlappen die Peaks mit denen des P1 von 45d, welches in wesentlich
höherer Konzentration in der Mischung vorhanden ist als 45b.
In den 1H-NMR-Spektren von 44b-46b findet sich neben den tert-Butylgruppen zwischen 1.2
ppm und 1.7 ppm jeweils ein Dublett vom Dublett bei ca. 4.4 ppm. Das Signal von H1 ist
damit ca. 1 ppm hochfeldverschoben gegenüber dem Signal von H1 bei den Komplexen des
Typs a. Eine ähnlich starke Hochfeldverschiebung ist auch für H1 von 17b im Vergleich zu
17a zu beobachten. H1 spaltet bei 44b-46b durch die Kopplungen mit P1 und P5 jeweils zu
Doppeldubletts auf. Sowohl die Kopplung 1JH1P1 von 196 Hz als auch die Kopplung 3JH1P5 von
30 bis 39 Hz lässt sich in den protonengekoppelten
31
P-NMR-Spektren wiederfinden. Die
direkte Kopplung 1JP1H1 vergrößert sich bei den [M(CO)5]-Komplexen des Typs b im
Vergleich mit den Konfigurationsisomeren a analog zu 17b und 17a von 176 Hz auf 196 Hz.
Die Karplus-Beziehung der Kopplung 3JH1P5, die bei 17a und 17b beobachtet wurde, tritt auch
bei den Komplexepimeren a und b auf. So sind die Kopplungen 3JH1P5 beim Komplextyp a
und bei 17a kleiner als 8 Hz, während sie bei den Komplexen der Serie b und bei 17b
zwischen 37 Hz und 40 Hz betragen.
Anhand der für beide Komplexserien a und b gefundenen Unterschiede der chemischen
Verschiebungen, sowie der Kopplungskonstanten zwischen den einzelnen Phosphoratomen
55
und den Analogien zu den beiden Epimeren 17a und 17b kann daher gezeigt werden, dass es
sich bei den Verbindungstypen a und b um die beiden an [M(CO)5]-Fragmente koordinierten
Epimere 17a und 17b des P5-Deltacyclens handelt.
2.2.3.3 NMR-Spektroskopische Charakterisierung der Chrom-, Molybdän- und
Wolframpentacarbonyl-P5-deltacyclenkomplexe 44c/d, 45c/d und 46c/d
Die Verbindungen der Komplexreihen c und d stellen Koordinationsisomere von a und b dar,
wobei diesem Fall das Phosphoratom P1 die Koordinationsstelle bildet (Abb. 2.2.9). Die
Verbindungen des Typs c entstammen hierbei dem Epimer 17a, während die Komplexserie d
aus 17b entsteht. Abb. 2.2.10 zeigt Ausschnitte der Verbindungen 45c und 45d aus dem 31PNMR-Spektrum des Gemisches 45a-d. In der Tabelle 2.2.7 werden die ermittelten
chemischen Verschiebungen und Kopplungskonstanten der 31P{1H}-NMR-Spektren von 44c46c und 44d-46d aufgeführt.
Abb. 2.2.9 Schematische Molekülstrukturen der beiden epimeren Komplexserien c und d.
Da die Koordination bei den Metallkomplexen der Typen c und d an P1 erfolgt, zeigt dieses
Signal den zu erwartenden Trend bei den Koordinationsverschiebungen in den
31
P-NMR-
Spektren. Die δ(P1)-Werte variieren zwischen 44c und 46c bzw. 44d und 46d jeweils um ca.
45 ppm. Die Koordinationsverschiebungen betragen bei den Verbindungen 44c, 45c und 46c
+41.4, +16.9 und -4.7 ppm. In der Komplexreihe d liegen die Koordinationsverschiebungen
∆δ(P1) für 44d, 45d und 46d bei +31.8, +8.5 und -14.2 ppm. Bei den [W(CO)5]Verbindungen finden sich für P1 zusätzlich noch die
183
W-Satelliten, mit
1
JWP1-
Kopplungskonstanten von 222.5 Hz bei 46c und 210.4 Hz bei 46d. Das belegt die
Koordination der [M(CO)5]-Fragmente für 44c-46c und 44d-46d an P1 eindeutig. Die
chemischen Verschiebungen der Phosphoratome P2 - P5 für die beiden homologen
56
Substanzserien sind demgegenüber fast unverändert. Die Signale können den benannten
Käfigpositionen anhand ihrer chemischen Verschiebungen und durch die 1JPP-Kopplungen
zugeordnet werden. δ(P4) liegt jeweils in der Region, die für P=C-Doppelbindungen
charakteristisch ist.[39] Die zwei aufgrund der Ringspannung des Diphosphiranrings
hochfeldverschobenen Peaks liegen in der gleichen Region wie beim unkoordinierten P5Deltaccyclen und lassen sich als P2 und P3 identifizieren.[40] Die Kopplungen 1JP2P3 liegen je
nach [M(CO)5]-Fragment bei c und d zwischen 149 und 159 Hz. Die zweite direkte Kopplung
1
JP1P2 beträgt zwischen 209 und 223 Hz. Die 1J-Kopplungen der Komplexepimere c und d
sind daher vom Betrag her ähnlich wie die jeweiligen Kopplungen bei 17a/b. Die Kopplungen
2
JP1P5 sind bei den Komplexserien c und d deutlich größer als bei den Koordinationsisomeren
des Typs a. Die Kopplungen 2JP1P5 sind für die Komplexe c weniger als halb so groß wie für d
aber etwa fünfmal größer als bei 17a, dem zugeordneten freien Liganden. Dieser große
Unterschied wird auf die Metallkoordination von P1 zurückgeführt, die die elektronische
Situation dieses Kerns stark verändert. Der Einfluss der Metalle auf die 2JP1P5 für die
Komplexserie d ist schwächer. Sie bleibt in der gleichen Größenordnung wie beim Liganden
17b.
P5
P4
349.5
349.0
P2 45c
P1
P3 45c
348.5
114.0 113.0 112.0 -33.0 -34.0 -35.0 -36.0 -37.0 -105.0 -110.0 -115.0 -120.0
P3 45d
P5
P4
P2 45d
P1 45d
P1 45b
360.00
360.0
359.50
359.00
359.0
358.50
86.00 85.50 85.00 84.50
86.0
85.0
-8.0 -9.0 -10.0-11.0-12.0-13.0
-8.0
-10.0
-12.0
-105.0 -110.0 -115.0 -120.0
Abb. 2.2.10 Ausschnitte aus dem 31P{1H}-NMR-Spektrum der Komplexmischung 45a-d (122 MHz, CDCl3,
25°C) für 45c (oben) und 45d (unten). Im Bereich von -107 ppm bis -121 ppm überlagern sich die Signale von
P2 und P3 beider Verbindungen.
57
Die chemischen Verschiebungen der jeweils vier Singuletts der tert-Butylgruppen der
einzelnen Komplexe in den 1H-NMR-Spektren liegen zwischen 1.1 und 1.7 ppm. Die
Kopplung
1
JH1P1 und δ(H1) werden durch die Metallkoordination an P1 bei den
Komplexserien c und d stärker beeinflusst als bei a und b. Daher weichen die entsprechenden
Werte bei c und d stärker voneinander ab (Tabelle 2.2.8).
Tabelle 2.2.7 Chemische Verschiebung in ppm und ausgewählte Kopplungskonstanten in Hz in den 31P{1H}NMR-Spektren von 44c-46c und 44d-46d im Vergleich mit 17a und 17b.
1
JP1P2
1
JP2P3
2
P4
P5
P1
P2
P3
JP1P5
44c
351.1
114.9
-10.3
-118.8
-110.4
233.5
158.6
41.9
45c
349.1
113.4
-34.8
-118.9
-110.2
223.6
158.4
38.3
46c
350.9
114.4
-56.4
-116.9
-109.8
223.2
158.2
47.7
44d
357.1
82.6
13.1
-109.1
-120.4
219.4
152.2
106.1
45d
359.3
85.4
-10.2
-108.9
-119.0
209.5
149.4
115.5
46d
357.3
84.9
-33.0
-105.8
-121.2
210.4
149.8
111.8
17a
339.5
105.0
-51.7
-112.5
-120.2
238.3
158.2
8.9
17b
366.1
88.3
-18.7
-107.1
-107.9
212.0
152.2
128.4
Die jeweils zu Dubletts aufgespaltenen Signale des Protons H1 von 44c, 45c und 46c sind
zwischen 6.3 ppm und 6.8 ppm zu finden. Ihre 1JH1P1-Kopplungskonstanten liegen zwischen
288 Hz und 303 Hz. Bei 44d, 45d und 46d sind die chemischen Verschiebungen von H1
zwischen 5.0 ppm und 5.4 ppm im Vergleich zu 44c-46c hochfeldverschoben und das Signal
ist jeweils zum ddd aufgespalten. Die direkte Kopplung 1JH1P1 beträgt je nach [M(CO)5]Fragment zwischen 316 Hz und 331 Hz und die beiden beobachtbaren H–P-Fernkopplungen
liegen bei ca. 27 und 10 Hz. Die größere der beiden Konstanten kann anhand von
protonengekoppelten
31
P-NMR-Spektren jeweils der Kopplung 3JH1P5 und die kleinere der
Kopplung 2JH1P2 zugeordnet werden. Alle Kopplungsbeträge von H1 zu den benannten
Phosphoratomen lassen sich bei deren Signalen in den Multipletts identifizieren.
58
Tabelle 2.2.8 Chemische Verschiebung in ppm und ausgewählte Kopplungskonstanten in Hz in den 1H-NMRSpektren von 44c-46c und 44d-46d im Vergleich mit 17a und 17b.
δ(H1)
2.2.4
13
1
JH1P1
2
JH1P2
3
JH1P5
44c
6.2
292.9
-
-
45c
6.4
288.2
6.0
3.6
46c
6.8
303.0
-
-
44d
5.0
319.4
10.2
26.7
45d
5.1
318.2
9.0
27.9
46d
5.4
331.0
10.9
26.5
17a
4.9
179.1
4.7
-
17b
4.1
197.7
4.4
36.6
C-NMR-Spektroskopische Charakterisierung und IR-Spektren der Chrom-,
Molybdän- und Wolframpentacarbonyl-P5-Deltacyclenkomplexe 44a-d, 45a-d und 46a46d
Die chemischen Verschiebungen der tert-Butylgruppen und der Gerüstkohlenstoffatome der
Komplexfamilien 44, 45 und 46 unterscheiden sich in ihren
13
C{1H}-NMR-Spektren nur
minimal. Daher wird im Folgenden die Charakterisierung der Verbindungen von
Wolframpentacarbonyl-P5-Deltacyclen 46a, 46b, 46c und 46d beispielhaft für alle [M(CO)5]Komplexe diskutiert. Weil die [M(CO)5]-Komplexe als untrennbare Isomerenmischung
44a-d, 45a-d und 46a-d vorliegen, werden für die
13
C{1H}-NMR-Spektren der jeweiligen
Komplexgemische in allen Fällen vier Signalsätze erwartet. Für die tert-Butylgruppen von
46a-d sind jedoch nur sieben Multipletts für die C(CH3)3-Kohlenstoffatome und für die
quartären C(CH3)3-Kohlenstoffatome beobachtbar. Theoretisch sollten 2 x 16 Multipletts
auftreten. Eine genaue Zuordnung der Signale zu den einzelnen Verbindungen ist für die tertButylgruppen daher nicht möglich. Da sich aber die chemischen Verschiebungen der Signale
nur wenig unterscheiden, überlagern sie sich zu komplexen Multipletts. Die Multipletts bei δ
= 32.7, 33.2, 34.7, 34.5, 35.4, 36.2, und 36.4 ppm sind aufgrund ihrer chemischen
Verschiebung und ihrer Intensität den C(CH3)3-Kohlenstoffatomen zuzuordnen. Diese
grundsätzliche Zuordnung konnte durch ein J-moduliertes APT
13
C{1H}-NMR-Spektrum
bestätigt werden. Die Signale bei δ = 37.8, 38.1, 38.6, 39.4, 40.1, 41.5 und 41.8 ppm sind den
quartären C(CH3)3-Kohlenstoffatomen der tert-Butylgruppen zuzuordnen. Für die Käfig59
gerüstkohlenstoffatome sind insgesamt acht Signale der 16 erwarteten beobachtbar. Die
genaue Zuordnung dieser Signalsätze zu den vier Verbindungen kann aus den vorliegenden
Daten nicht erfolgen. Die Zuordnung der Signale zu einzelnen Gerüstkohlenstoffpositionen ist
aber möglich (Abb. 2.2.11). Zwei Peaks bei δ(C1) = 64.1 und 66.8 ppm werden dem
Kohlenstoffatom C1 im Diphosphiranring zugeordnet. Sie sind gegenüber dem Signal von C1
des unkoordinierten Käfigs 17 (δ(C1) = 69.4 ppm) leicht hochfeldverschoben. Vier
Multipletts bei 81.4, 85.5, 93.4 und 95.4 ppm können den beiden benachbarten
Gerüstkohlenstoffatomen C2 und C4 zugeordnet werden. Sie liegen nahe C2 und C4 von 17
(δ = 83.6 und 90.4 ppm). Zwei Signale von sp2-hybridisierten Kohlenstoffatome liegen bei δ
= 217.2 und 222.5 ppm und damit in einem Bereich, der für P=C-Doppelbindungen
charakteristisch ist.[39] Gegenüber dem Signal von C3 von 17, welches bei δ(C3) = 225.7 ppm
liegt, sind beide leicht hochfeldverschoben. Da die Carbonylkohlenstoffatome direkt an das
jeweilige Metall gebunden sind, sind diese Signale im Gegensatz zu den restlichen
Kohlenstoffatomen in den 13C-NMR-Spektren stärker gegeneinander verschoben.
Abb. 2.2.11 Schematische Molekülstrukturen von Metallpentacarbonyl-P5-deltacyclen 44a-d, 45a-d und 46a-d.
Weil die Epimere 44b-46b in allen Gemischen den geringsten prozentualen Anteil aufweisen,
konnten die wenig intensiven Signale der Carbonylkohlenstoffatome dieser Verbindungen in
keinem
13
C-NMR-Spektrum
beobachtet
werden.
Alle
Signale
der
cis-ständigen
Kohlenstoffatome sind zu Doppeldubletts aufgespalten, während die trans-ständigen nur
Dubletts
bilden.
Bei
den
[Cr(CO)5]-Komplexen
befinden
sich
die
cis-ständigen
Carbonylkohlenstoffatome von 44a, 44c und 44d zwischen 215.1 und 215.7 ppm. Die
zugehörigen trans-ständigen Kohlenstoffatome sind zwischen 220.6 und 221.7 ppm
beobachtbar. Bei den [Mo(CO)5]-Komplexen wurden nur die Signale der cis-ständigen
Carbonyle von 45a und 45d identifiziert, die bei 204.2 und 204.8 ppm liegen. Die Peaks der
60
cis-ständigen Carbonyle von 46a, 46c und 46d liegen zwischen 196.0 und 197.2 ppm, die der
trans-ständigen zwischen 197.6 und 199.1 ppm.
Die IR-Banden der jeweiligen [M(CO)5]-Komplexgemische 44, 45 und 46 liegen alle in
ähnlichen Bereichen. Exemplarisch sollen hier deshalb die bei 45a-d gefundenen
charakteristischen Banden diskutiert werden. Die Banden der verschiedenen Komponenten
einer Mischung überlagern sich und können daher nicht getrennt betrachtet werden. Die drei
für [M(CO)5]-Komplexe zu erwartende Banden sind bei 2069, 1944 und 1913 cm-1 zu
beobachten. Diese sind gegenüber [M(CO)6] zu niedrigeren Frequenzen verschoben, was auf
verstärkte π-Rückbindungsanteile zu den verbliebenen fünf Carbonylliganden zurückzuführen
ist. Die 13C-NMR- und IR-Spektren sind damit mit den Ergebnissen, der 1H- und
31
P-NMR-
Spektren, Elementar- und Strukturanalysen vereinbar, bieten aber selbst keine signifikanten
Informationen über die komplexen Substanzgemische.
2.2.5
Vergleich
der
Chrom-,
Molybdän-
und
Wolframpentacarbonyl-P5-
deltacyclenkomplexe 44a-d, 45a-d und 46a-d
Nachdem die Charakterisierung der einzelnen Verbindungen der Komplexserien a, b, c und d
abgeschlossen ist, werden sie im Folgenden miteinander verglichen. Wie 17a und 17b haben
sich die beiden Verbindungsserien a und b als Epimere erwiesen, die sich in der
Konfiguration von P1 unterscheiden. Bei a und b ist jeweils an P2 ein [M(CO)5]-Fragment
koordiniert. Analoge Verhältnisse finden sich bei den beiden Substanzfamilien c und d. Sie
unterscheiden sich wieder in der Konfiguration von P1, doch ist in diesem Fall P1 auch das
Bindeglied zum Metall der [M(CO)5]-Fragmente. Bei den Verbindungen der Serien a und c
steht das Proton H1 am Phosphoratom P1 cis (bzw. gauche) zu P5, während es bei b und d
trans dazu steht. Wie schon beschrieben, zeigen die beiden Epimerenpaare a/b und c/d
untereinander
teilweise
deutlich
Kopplungskonstanten in den
31
unterschiedliche
chemische
Verschiebungen
und
P{1H}-NMR-Spektren. Die Kopplungskonstanten 1JP1H1 sind
beim Komplextyp a um 20 Hz kleiner als bei seinen epimeren Verbindungen b. Bei den
beiden epimeren Verbindungsserien c und d, an denen das [M(CO)5]-Fragment zusätzlich
zum Proton an P1 gebunden ist, fällt der Unterschied der Kopplung 1JP1H1 mit 30 Hz etwas
größer aus, beide übertreffen hier aber die 1JP1H1 des jeweils zugeordneten Liganden 17a bzw.
17b um gut 100 Hz. Dieser Effekt ist auf die veränderten elektronischen Verhältnisse
zurückzuführen. Außerdem bestehen sowohl zwischen den Komplexserien a und c als auch
zwischen b und d einige Gemeinsamkeiten, vor allem bei den δ(P1)- und δ(P5)-Werten und
61
deren
Kopplungskonstanten.
Die
2
Kopplungskonstante
JP1P5 ist
bei
den
beiden
Verbindungstypen b und d deutlich größer als bei ihren Epimeren a und c, deren 2JP1P5-Werte
um ca. 110 Hz bzw. 64 - 77 Hz übertroffen werden. Auch die Kopplung 3JH1P3 für die
Käfigkomplextypen b und d übersteigt die ihrer Epimere a und c um ein Mehrfaches.
Während die 3JH1P5 für die Komplexfamilien a und c sowie für ihren Liganden 17a meist
unbeobachtbar sind und höchstens 5 Hz beträgt, werden für b und d und 17b Beträge
zwischen 27 Hz und 39 Hz gefunden. Diese Unterschiede weisen, wie auch schon bei 17a und
17b, auf eine Karplus-artige Beziehung zwischen H1 und P5 hin. Die chemischen
Verschiebungen von P5 betragen für die Komplextypen b und d zwischen 80 und 90 ppm,
während sie für a und c zwischen 110 und 115 ppm in den 31P-NMR-Spektren zu finden sind.
Der gleiche Trend gilt wieder für 17b und 17a. Die Peaks des Phosphoratoms P1 für b und d
sind um 15 - 30 ppm tieffeldverschoben im Vergleich zu ihren Epimeren. Auch das gilt
wieder für die jeweiligen Liganden.
Zu den vier Isomeren 44a-d wurden von T. Shubina DFT-Rechnungen (B3PW91/cc-pVDZ)
angefertigt, um ihre relativen Energien miteinander vergleichen zu können (Abb. 2.2.12). Die
Energien der berechneten Komplexe weichen vom energetisch günstigsten Komplex 44a nur
um 0.6 kcal mol-1 (44d), 0.7 kcal mol-1 (44c) und 1.1 kcal mol-1 (44b) ab. Das erklärt die bei
allen drei Metallen beobachtete Bildung von vier isomeren Einkernkomplexen.
44a
mol-1
0.0 kcal
45.9°
44b
44c
mol-1
mol-1
1.1 kcal
155.0°
0.7 kcal
41.1°
44d
0.6 kcal mol-1
160.0°
Abb. 2.2.12 Berechnete Molekülstrukturen von 44a-d mit ihren relativen Energien und den Diederwinkeln H1–
P1–C4–P5.
Das in den Rechnungen stabilste Komplexisomer 44a ist stereochemisch mit den drei
kristallisierbaren und strukturell untersuchten Komplexen 44a, 45a und 46a identisch,
qualitativ spiegeln sich die berechneten Unterschiede auch in den Verhältnissen der
62
Produktmischung von 44, 45 und 46 wieder. So werden z.B. von den Verbindungen des Typs
b immer die mit Abstand kleinsten Anteile in den Produktmischungen beobachtet. Damit
ergibt sich eine grundsätzliche Übereinstimmung von Theorie und den in dieser Arbeit
präsentierten Experimenten.
2.2.6 Vergleich der Wolframpentacarbonylkäfigkomplexe 37, 39 und 46a-d
In der Literatur finden sich zwei P–C-Käfigverbindungen, deren [W(CO)5]-Komplexe 37 und
39 eine gewisse Strukturanalogie zu 46a-d aufweisen (Abb. 2.2.13).[32,33] Bei dem P–CKäfigkomplex 39, der mit 17a/b durch das Norbornengerüst und den Diphosphiranring
strukturell verwandt ist erfolgt die Koordination zweier [W(CO)5]-Fragmente an P4 und P5,
deren analoge Positionen bei 17a/b keine Metallatome tragen.[33] Gleichzeitig sind die den
Kernen P1 und P2 von 17a/b entsprechenden Positionen von 39 durch die zwischen ihnen
zusätzlich eingebaute C(tert-Butyl)-Einheit deutlich stärker abgeschirmt. Die sterische
Entlastung von P4 und P5 durch die beiden Methylgruppen von 39 bei gleichzeitiger
sterischer Belastung von P1 und P2 durch eine zusätzliche tert-Butylgruppe verschiebt darum
die Ligandeigenschaften der Phosphoratome von 39 zu Kernen, die im Fall von 17a/b
komplexchemisch inaktiv sind.
Im Vergleich hierzu ergibt sich bei 37 die Koordination zweier [W(CO)5]-Fragmente an
beiden Phosphoratomen P2 und P3 des Diphosphiranrings.[32] Auch hier ist ein
Norbornenfragment mit einem Diphosphiranring direkt verknüpft. Die Koordination von P2
teilen 37 und 45a/b, P3 wurde jedoch bei den P5-Deltacyclenen 17 in keinem Fall von einem
Metall besetzt. Im Gegensatz zu 17 bzw. 45 bildet der Triphosphacyclohexenring von 37 ein
1,2,4-Triphosphacycolhexanisomer aus, bei dem P3 durch den Nachbarn P4 im Ring sterisch
gegenüber der Situation bei 17 entlastet ist, in dem sich an dieser Stelle die Einheit C2(tertButyl) befindet.
Abb. 2.2.13 [W(CO)5]-Verbindungen der P–C-Käfigverbindungen 45a/b, 37[32] und 39[33].
63
Diese Beispiele sind als Hinweis darauf zu werten, dass die Ligandeigenschaften der bislang
untersuchten P–C-Käfigverbindungen in erster Linie von der sterischen Zugänglichkeit der
freien Elektronenpaare der Phosphoratome bestimmt werden. Andere Strukturmerkmale wie
etwa die Positionierung der betrachteten Phosphoratome in kleinen Ringen oder in
P=C-Doppelbindungssystemen, die beide deutlichen Einfluss auf die Basizität der beteiligten
freien Elektronenpaare ausüben, scheinen demgegenüber deutlich nachrangig.
Es fällt auf, dass 37 und 39 als zweikernige Komplexe auftreten. Eine derartige Koordination
von zwei [M(CO)5]-Fragmenten ist bei 17a/b auch mit hohen Überschüssen an
[M(CO)5THF]-Komplexen nicht zu erhalten. Das deutet auf eine insgesamt stärkere
Abschirmung der Käfigliganden 17a und 17b durch die vier tert-Butylgruppen des
Käfiggerüsts als bei 37 und 39. Gerade gegenüber 37 kann der Unterschied aber nicht groß
sein. Er reicht aber aus um die Ligandeigenschaften von 17a und 17b auf ein einzelnes
[M(CO)5]-Fragment zu beschränken. Der P5-Deltacyclenkäfig ist hinsichtlich seiner
Bindungen innerhalb des Käfigs relativ starr. Eine Koordination der [M(CO)5]-Fragmente
erfolgt vor allem aufgrund sterischer Gründe ausschließlich an P1 oder an P2, wobei von
beiden Koordinationsisomeren jeweils beide Epimere von 17a/b in den Reaktionsmischungen
gefunden wurden.
2.3 Ein (η6-Aren)ruthenium(II)-Komplex des P5-Deltacyclens
2.3.1 Darstellung von [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II)] 47
Nachdem die Koordination von [M(CO)5]-Fragmenten an 17a und 17b zu einem
untrennbaren Substanzgemisch aus stabilen Komplexen geführt hat, wurde untersucht ob dies
auch für andere Übergangsmetallkomplexe des P5-Deltacyclenkäfigs gilt. Ruthenium stellt in
zahlreichen Katalysatoren das aktive Metallzentrum dar. In früheren Arbeiten im Arbeitskreis
Zenneck
wurden
(η6-Aren)Ruthenium(II)-Komplexe
mit
chiralen
Phosphanliganden
erfolgreich in der katalytischen Transferhydrogenierung eingesetzt.[52,53] Demzufolge war es
von Interesse die Epimerenmischung des P5-Deltacyclens 17a/b an Ruthenium(II) zu
koordinieren. Als Ruthenium-Precursor wurde das Benzoldichlororuthenium(II)-Dimer
verwendet.
Die
Umsetzung
von
P5-Deltacyclen
17a/b
mit
[(η6-C6H6)RuCl2]2
in
Methylenchlorid liefert den einkernigen Komplex 47 in 93 % Ausbeute (Abb. 2.3.1). Wie aus
den NMR-Spektren und der Molekülstruktur im Kristall ersichtlich, wird aus dem
Epimerengemisch 17a/b selektiv nur ein Epimer mit [(η6-C6H6)RuCl2]-Fragmenten zum
Komplex 47 umgesetzt. Da die Epimerenmischung zu ca. 87 % aus 17a und 13 % aus 17b
64
besteht, die Gesamtausbeute aber über 90 % beträgt, ist dies ein klarer Beweis für das
dynamische Gleichgewicht, zwischen den beiden Epimeren. Die Ursache für diese
erstaunliche Selektivität soll im Folgenden diskutiert werden.
Cl
H
H
tBu
P
tBu
P
P
P
P
+ 0.5
tBu
Ru
P
tBu
Cl
Cl
Ru
Ru
Cl
Cl
P
CH2Cl2
P
P
Cl
P
tBu
tBu
tBu
tBu
17a/b
47
Abb. 2.3.1 Synthese von [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II)] 47.
2.3.2 Molekülstruktur von [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II)] 47
Aus einer THF-Lösung von 47 bei Raumtemperatur konnten Kristalle erhalten werden, die für
eine Röntgenstrukturanalyse geeignet waren. Wie 45a kristallisiert der Rutheniumkomplex in
der zentrosymmetrischen Raumgruppe P 1 (Nr. 2) mit einer triklinen Elementarzelle. In der
Elementarzelle sind vier Moleküle des Komplexes enthalten, wobei jeweils zwei Moleküle
unabhängig voneinander sind. Die anderen beiden bilden das jeweilige Enantiomer dazu. Die
beiden symmetrieunabhängigen Moleküle besitzen die gleiche Konfiguration und
unterscheiden sich nur geringfügig in ihren Bindungslängen und -winkeln voneinander. Es
handelt sich bei den beiden also nicht um Epimere. Zusätzlich sind in der Elementarzelle noch
zwei unabhängige, fehlgeordnete THF-Moleküle vorhanden. Die Molekülstruktur von einem
der beiden unabhängigen Moleküle von 47 ist in der Abb. 2.3.2 dargestellt. Wie man dort
erkennen kann, ist das Epimer 17b an das [(η6-C6H6)RuCl2]-Fragment gebunden. Dieses
Epimer entspricht der thermodynamisch instabileren Komponente der Mischung des P5Deltacyclens 17a/b die nur zu ca. 13 % vorhanden ist. Bindungslängen und Bindungswinkel
von 47 sind in Tabelle 2.3.1 aufgeführt. Wie bei der Struktur von 45a unterscheiden sich die
Bindungslängen und -winkel des Käfiggerüstes kaum von denen, die in der Röntgenstruktur
des unkoordinierten P5-Deltacyclens 17 bestimmt wurden.[19,20] Der sterische Anspruch des
Benzolrings und der beiden Chloroliganden ist größer als der fünf Carbonylliganden der
[M(CO)5]-Komplexe. Die Bindungslänge P1–Ru beträgt 238.9 pm und ist damit ca. 7 pm
länger als bei anderen [(η6-Aren)Ru(II)Cl2(PHR2)]-Komplexen.[54,55]
65
C10
C30
C25
C26
C1
P5
C3
P4
C24
P2
P3
C21
Ru
C4
P1
C23
C22
Cl1
C2
C40
H1
C20
Cl2
Abb. 2.3.2 Molekülstruktur eines Enantiomers von 47 im Kristall. Die Wasserstoffatome der tert-Butylgruppen
und des Benzolrings wurden der Übersicht halber weggelassen.
Tabelle 2.3.1 Ausgewählte Bindungslängen und Bindungswinkel von 47 in pm und °.
66
P1–C4
189.14(19)
P1–Ru
238.91(5)
C2–C4–P5
100.89(11)
P1–P2
217.09(7)
Ru–Cl1
241.01(5)
C1–P3–P2
54.71(6)
P2–C1
188.76(19)
Ru–Cl2
239.91(6)
P3–C1–P2
72.87(7)
P2–P3
221.00(7)
Ru–C21
221.1(2)
P3–C1–P5
109.80(10)
P3–C1
183.3(2)
Ru–C22
221.0(2)
P5–C1–P2
113.54(10)
P3–C2
191.73(19)
Ru–C23
217.9(2)
C1–P2–P3
52.42(6)
P4–C3
168.1(2)
Ru–C24
218.2(2)
C4–P1–P2
98.27(6)
P4–C2
189.82(18)
Ru–C25
218.4(2)
C2–C4–P1
111.76(12)
P5–C3
184.6(2)
Ru–C26
217.6(2)
P5–C4–P1
99.24(9)
P5–C1
188.71(19)
C4–C2–P4
106.82(12)
P2–P1–Ru
105.35(2)
P5–C4
190.60(19)
C4–C2–P3
107.49(12)
C4–P1–Ru
134.47(6)
C2–C4
159.9(3)
P4–C2–P3
97.45(8)
Cl1–Ru–Cl2
86.76(2)
Die Abstände zwischen dem Rutheniumion und den η6-Kohlenstoffatomen des Benzolrings
betragen zwischen 217.6 pm und 221.1 pm, die Ru–Cl-Distanzen 239.9 pm und 241.0 pm und
der Winkel Cl1–Ru–Cl2 beträgt 86.8°. Dieser Winkel und die Bindungslängen Ru–C6H6 und
Ru–Cl entsprechen in etwa den in der Literatur gefundenen Werten.[54,55] Der für die NMREigenschaften bedeutsame Diederwinkel H1–P1–C4–P5 beträgt 164.7°. Dieser Winkel weicht
nur um gut 15° von den 180° für eine ideale trans-ständigen Anordnung von H1 und P5 ab
und erklärt damit die vergleichsweise große Kopplung zwischen beiden Atomen in den NMRSpektren von 47. Der Grund für die selektive Umsetzung von Epimer 17b ist wahrscheinlich
die sterische Abstoßung durch die tert-Butylgruppen an C2 und C4, die eine Koordination des
raumfüllenden [(η6-C6H6)RuCl2]-Fragments bei der Reaktion mit dem anderen Epimer 17a
erfährt (Abb. 2.3.3).
C6H6
Cl1
P2
Ru
Cl2
P3
H1
tBu an C4
tBu an C2
Abb. 2.3.3 Kalottenmodell der Molekülstruktur von 47.
2.3.3 Spektroskopische Charakterisierung von [(η6-Benzol)dichloro(P5deltacyclen)ruthenium(II)] 47
Im FD-Massenspektrum von 47 findet sich der Basispeak mit 100 % Intensität bei m/z = 432,
der dem freien Käfig entspricht. Der Molekülpeak des einkernigen Komplexes 47 mit nur 3 %
Intensität bei m/z = 683 gibt einen ersten Hinweis auf die im Vergleich zu den [M(CO)5]67
Komplexen deutlich schwächere Bindung zwischen dem Ruthenium(II)-Ion und dem P5Deltacyclen. Im Einklang damit ist bei 47 eine säulenchromatographische Aufreinigung nicht
möglich, da das Metall hierdurch vollständig vom P5-Deltacyclenliganden dekomplexiert
wird, wobei die Epimerenmischung 17a und 17b wieder zurückgewonnen werden kann. Da
das [(η6-C6H6)RuCl2]2-Dimer im verwendeten Lösungsmittel wenig, der resultierende
Komplex 47 aber gut löslich ist, können beide Komplexe leicht voneinander getrennt werden.
Im 31P{1H}-NMR-Spektrum von 47 finden sich im Gegensatz zu den Isomerengemischen der
Komplexe 44a-d, 45a-d und 46a-d nur fünf Signalgruppen einer einzigen Komplexspezies
(Abb. 2.3.4). Die starke Koordinationsverschiebung des Signals von P1 von +74.6 ppm weist
P1 als in diesem Fall ausschließlich aktive Ligandfunktion des Käfigs aus (Tabelle 2.3.2). Die
Kristallstruktur von 47 bestätigt diesen Befund. Damit sind die Strukturen der Verbindung 47
im Festkörper und in Lösung analog. Eine Verwandtschaft zu den ebenfalls an P1
koordinierten [M(CO)5]-Komplexfamilien c und d liegt nahe. Da von diesen beiden
Komplextypen bislang keine Kristallstruktur erhalten werden und daher die Aussagen über
deren Stereochemie nur anhand der NMR-Daten gemacht werden konnten, ist mit den Daten
von 47 eine Überprüfung der im Kapitel 2.2.3.3 vorgenommenen Strukturinterpretation
möglich. Die Kopplung 1JP1P2 ist für 47 mit 260.7 Hz etwa 49 Hz größer als bei 17b und um
37 Hz und 51 Hz größer als bei den vergleichbaren [M(CO)5]-Komplexen c und d. Eine
geringe Tieffeldverschiebung auf δ(P5) = 78.5 ppm lässt sich bei 47 im Vergleich mit 17b
(δ(P5) = 88.3 ppm) feststellen, während der Unterschied zu 17a (δ(P5) = 115.0 ppm) deutlich
stärker ausfällt. Ebenso stimmt die chemische Verschiebung von P5 bei 47 auch eher mit den
δ(P5)-Werten überein, die bei den [M(CO)5]-Komplexen des Typs d (ca. 84 ppm) beobachtet
werden. Im Gegensatz dazu weichen sie bei den Komplexen der Serie c (ca. 114 ppm)
deutlich davon ab. Die Ähnlichkeit der chemischen Verschiebungen von P5 bei 17b und den
Komplexserien b, d und 47 ist ein Hinweis darauf, dass die Molekülstruktur von 47 den
Grundzügen der Strukturen von 17b und den Komplexreihen b und d entspricht. Die
Kopplung 2JP1P5 liegt mit 77.2 Hz für 47 in etwa zwischen den Werten, die bei den Epimeren
der [M(CO)5]-Komplexe c und d auftreten, bei denen das [M(CO)5]-Fragment an P1
koordiniert. Die Signale der Phosphoratome P2, P3 und P4 sind bei 47, verglichen mit c und
d, in ähnlichen Bereichen anzutreffen. Der Peak von P4 findet sich bei 351.7 ppm in der
typischen P=C-Doppelbindungsregion.[39] Sowohl δ(P2) mit -115.4 ppm und δ(P3) mit -126.6
ppm als auch deren direkte Kopplung 1JP2P3 von 149.1 Hz entsprechen den Werten des
Diphosphiranrings von 17a/b, 44c-46c und 44d-46d.
68
Tabelle 2.3.2 Chemische Verschiebungen in ppm und ausgewählte Kopplungskonstanten in Hz aus den 31P{1H}NMR- und 1H-NMR-Spektren von 47, 17a und 17b.
δ(P4)
δ(P5)
δ(P1)
δ(P2)
δ(P3)
47
351.7
78.5
22.9
-115.4
17a
339.6
105.0
-51.7
17b
366.1
88.3
-18.7
P5
2
3
JP1P5
δ(H1)
-126.6
77.2
4.9
26.3
-112.5
-120.2
9.1
4.9
0
-107.1
-107.9
128.4
4.1
36.6
JH1P5
P3
P2
P4
-115.0
-120.0
-125.0
79.00 78.50 78.00 77.50
P1
24.0
ppm
300
300
ppm (t1)31 1
23.0
P3
P1
P5
22.0
P2
21.0
200
200
100
100
00
-100
-100
-200
-200
Abb. 2.3.4 P{ H}-NMR-Spektrum (122 MHz, CDCl3, 25°C) von 47. Die Peaks von P5, P1, P2 und P3 sind
gespreizt dargestellt.
Im 1H-NMR-Spektrum von 47 sind drei Signale für die vier tert-Butylgruppen bei 1.2, 1.4
und 1.6 ppm zu finden, deren Integrationsverhältnis 1 : 1 : 2 beträgt. Das Signal bei 1.6 ppm
entspricht damit zwei zufällig isochronen tert-Butylgruppen. Die Protonen des η6-gebundenen
Benzolrings am Ruthenium bilden bei Raumtemperatur ein Singulett bei 5.9 ppm, der Ring
rotiert also schnell in der NMR-Zeitskala. Das Proton H1 spaltet bei 4.9 ppm zum ddd auf.
Dieser Wert ist ähnlich denen von Komplextyp d (5.0 - 5.4 ppm), was für eine
Strukturanalogie von 47 und der Komplexserie d spricht. Die bei deren Epimeren c (6.3 - 6.8
ppm) gefundenen chemischen Verschiebungen von H1 weichen im Vergleich dazu deutlich
ab. Da die direkte Kopplung 1JP1H1 stark vom koordinierten Metall beeinflusst wird, ist der
69
Wert von 399 Hz für 47 deutlich größer als die Beträge, die bei den [M(CO)5]-Komplexen des
Typs c und d beobachtet wurden. Des Weiteren koppelt H1 mit P5 und P2 mit 3JP5H1 = 26 Hz
und 2JP2H1 = 10 Hz. Kopplungen ähnlicher Größe zu P5 und P2 lassen sich auch für H1 bei
den Komplexen des Typs d finden. Im Gegensatz dazu kann man bei deren Epimeren c keine
Kopplung 3JP5H1 beobachten. Aufgrund der vielen diskutierten Ähnlichkeiten zwischen der
[M(CO)5]-Serie d und 47 kann man von analogen Strukturen ausgehen. Damit wird die in
Kapitel 2.2.2 getroffene Zuordnung der Isomere bei den [M(CO)5]-Komplexen 44a-d, 45a-d
und 46a-d bestätigt.
Das
13
C-NMR-Spektrum ergibt wie das
31
P-NMR-Spektrum von 47 einen einfachen Satz an
Signalen. Die chemische Verschiebung der acht Multipletts der tert-Butylgruppen liegen bei
33.3, 34.2, 35.3 und 37.3 ppm für die C(CH3)3-Kohlenstoffatome und bei 35.9, 38.3, 41.5 und
41.6 ppm für die quartären C(CH3)3-Kohlenstoffatome. Die sechs Kohlenstoffatome des
Benzolrings ergeben ein Singulett bei 87.7 ppm, wie schon aus dem 1H-NMR-Spektren
geschlossen rotiert der Ring rasch in der NMR-Zeitskala. Das Signal des Kohlenstoffatoms
C1 im Diphosphiranring liegt bei 67.6 ppm nahe dem analogen Signal von 17 (δ(C1) = 69.1
ppm). Die Peaks der beiden benachbarten Gerüstkohlenstoffatome C2 und C4 sind bei δ =
88.1 und 95.2 ppm ebenfalls im gleichen Bereich zu finden wie die entsprechenden Signalen
von 17 (δ = 83.6 und 90.4 ppm). Eine eindeutige Zuordnung der beiden Kohlenstoffatome zu
den beiden Signalen kann aus den vorliegenden Daten ebenso wenig wie bei 17 erfolgen. Das
Signal des sp2-hybridisierten Kohlenstoffatoms der P=C-Doppelbindung C3 liegt mit 216.4
ppm leicht hochfeldverschoben zum Signal von C3 bei 17 (δ(C3) = 225.6 ppm) vor.
Im Gegensatz zu den [M(CO)5]-Komplexen ergibt sich für 47 ausweislich der NMR-Spektren
nur eine einzige Verbindung. Die Reaktion verläuft also sowohl regio- als auch stereoselektiv.
Da eine Epimerisierung von P1 im Fall der Koordination eines Metalls an diesem
Phosphoratom durch Erhöhung der Inversionsbarriere deutlich behindert wird,[56] ist zu
fordern, dass das dominierende Ligandmolekül 17a vor der Komplexierung in 17b überführt
wird. Aus dem raschen Gleichgewicht zwischen 17a und 17b wird die ursprüngliche
Nebenkomponente 17b selektiv durch die Komplexierung an das Rutheniumion
herausgenommen. Die eindeutige Selektion eines einzelnen Stereoisomers und eines Epimers
belegt den größeren Raumbedarf des [(η6-C6H6)RuCl2]-Fragments gegenüber den im
vorhergehenden Abschnitt bearbeiteten [M(CO)5]-Komplexen.
70
2.3.4 Zwei Enantiomerenreine [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II)]Komplexe 47’ und 47’’
Da die Reaktion von [(η6-C6H6)RuCl2]2 mit dem P5-Deltacyclen 17a/b erfreulicherweise nur
eine Verbindung hervor brachte, in der das redoxaktive Metall Ruthenium an P1 koordiniert
ist lag es auf der Hand, diesen Befund auf enantiomerenreine Käfige anzuwenden, die als
optische Antipoden 17’a/b und 17’’a/b im Projekt von C. Höhn bearbeitet werden. Das
Problem der Epimerisierung gilt für die separierten Enantiomere natürlich genauso wie für
das Racemat 17a/b. Die Konfiguration des labilen stereogenen Zentrums P1 im Käfig ist
durch die Metallkoordination ebenfalls stabilisiert. Da die Rutheniumverbindung 47 die
grundsätzlichen Voraussetzungen für einen definierten chiralen Katalysatorkomplex erfüllt,
wurde versucht, den Metallkomplex auch enantiomerenrein darzustellen. In Zusammenarbeit
mit C. Höhn wurden hierfür zur Komplexbildung die vorher voneinander getrennten
Käfigenantiomere 17’ und 17’’ verwendet. Die für die beiden Eduktverbindungen, den chiral
substituierten P–C-Käfigverbindungen 16’ und 16’’, bestimmten d.e. Werte betragen 98 %
und 92 %.[20] Es kann davon ausgegangen werden, dass die entsprechenden e.e. Werte von 17’
und 17’’ nur unwesentlich davon abweichen.[36] Beide Enantiomere wurden separat mit
[(η6-C6H6)RuCl2]2 umgesetzt, wobei analog zur in Kapitel 2.3.1 beschriebenen Synthese
verfahren wurde. Die in zwei Enantiomere getrennten Folgeprodukte werden als 47’ und 47’’
bezeichnet. Ausbeuten, Massen- und NMR-Spektren der Produkte 47’ und 47’’ entsprechen
denen des racemischen Komplexes 47. Wie zu erwarten, konnten die beiden Epimere des
Komplexes 47 separat dargestellt werden. Leider konnten von keinem der beiden
enantiomerenreinen
Komplexen
Kristalle
ausreichender
Qualität
für
eine
Röntgenstrukturanalyse gewonnen werden, da die Kristallisationstendenz aufgrund der
fehlenden Zentrosymmetrie der zu erwartenden Kristalle erheblich verringert wird. Wie für
separierte Enantiomere einer chiralen Verbindung erwartet, drehen 47’ und 47’’ die Ebene des
polarisierten Lichtes gegenläufig. Zudem wurden von beiden Substanzen CD-Kurven im
Wellenlängenbereich zwischen 250 und 900 nm aufgenommen.[57] In Abb. 2.3.5 sind diese
CD-Kurven gezeigt und denen der beiden Enantiomere des P5-Deltacyclens 17’ und 17’’
gegenübergestellt. Bei den dargestellten CD-Spektren repräsentiert die schwarze Kurve das
Enantiomer 47’ und die rote Kurve das Enantiomer 47’’. Wie für Enantiomere zu erwarten,
bilden die beiden CD-Kurvenpaare jeweils Bild und Spiegelbild. Die Abweichungen von
einer idealen Spiegelsymmetrie beider Kurven werden als Folge der unterschiedlichen
Enantiomerenüberschüsse beider Substanzen interpretiert.
71
PH(S)
200
150
100
CD [mdeg]
17’’
50
17’’
0
-50
17’
-100
17’
-150
200
300
400
500
600
λ [nm]
PH(R)Ru
PH(S)Ru
100
80
47’
60
CD [mdeg]
40
20
47’
0
-20
Cl
Cl
Ru
-40
-60
H
tBu
P
tBu
47’’
P
-80
P
P
tBu
-100
tBu
-120
47’’
47-R
200
300
400
500
600
700
λ [nm]
Abb. 2.3.5 CD-Kurven von 17’, 17’’,[20] 47’ und 47’’.[36]
72
P
800
900
Die deutlich ausgeprägten Kurvenverläufe belegen aber die hohen Enantiomerenüberschüsse
der optischen Antipoden, liefern aber keine konkreten Messwerte. Die Ähnlichkeiten der
Kurvenverläufe für beide Substanzpaare im Bereich 250 – 450 nm wird auf dominante
Einflüsse der chiroptischen Eigenschaften der P–C-Käfige für diesen Spektralbereich
gedeutet.[36] Erst oberhalb von 550 nm liefern die [(η6-C6H6)RuCl2]-Fragmente merkliche
Beiträge, die auf dd- und CT-Übergänge deuten.[58] Weitere Übergänge wären im UV-Bereich
unterhalb von 250 nm zu erwarten, die spektroskopisch aber nicht mehr erfassbar sind. In
diesem Bereich verhindert die Eigenabsorption des Lösungsmittels die Messung der CDBanden.
Mit
der
erfolgreichen
Synthese
hoch
enantiomerenangereicherter
Rutheniumkäfig-
verbindungen wurde ein wichtiger Schritt in Richtung der asymmetrische Katalyse gemacht,
bei der sterisch anspruchsvolle chirale Liganden wie der P5-Deltacyclenkäfig von großem
Interesse sind. Sowohl in protischen Lösungsmitteln, als auch in Gegenwart primärer Amine
wird 47 jedoch rasch dekomplexiert und ist daher für die katalytische Transferhydrogenierung
ungeeignet. Um die in diesem Fall zu labile Metallkoordination zu stabilisieren, könnten
funktionalisierte P5-Deltacyclen- oder andere P–C-Käfigliganden mit mehreren aktiven
Liganfunktionen als Chelatligand eingesetzt werden. Untersuchungen zur Funktionalisierung
von 17 laufen im Rahmen des Projekts von I. Keller.[34]
2.4 Rhodium(III)-Käfigkomplexe des P5-Deltacyclens
2.4.1 Darstellung der Rhodium(III)-P5-deltacyclen-Zweikernkomplexe 48a und 48b
Wie das Edelmetall Ruthenium in den Oxidationsstufen (0) und (II) wird auch das im
Periodensystem benachbarte Rhodium bevorzugt in zwei verschiedenen Oxidationsstufen als
reaktives Zentralmetall in der homogenen Katalyse eingesetzt. Hier handelt es sich jedoch um
die Oxidationsstufen (I) und (III). Dabei enthalten die interessanteren Katalysatoren das
Rhodium als Rh(I) wie etwa im Wilkinson-Katalysator [Rh(Cl)(PPh3)3][59], der zudem
monofunktionale Phosphane als Liganden enthält, die in Teilen möglicherweise auch von
chiralen P–C-Käfigliganden ersetzt werden können. Es wurde daher versucht, eine geeignete
Rhodium(I)-Ausgangsverbindung mit dem P5-Deltacyclenkäfig 17a/b zu verbinden, indem
zwei Äquivalente des Käfigs mit einem Äquivalent Cyclooctadienchlororhodium(I)-Dimer in
THF bei Raumtemperatur umgesetzt wurden (Abb. 2.4.1). Die Reaktion verläuft erfolgreich,
jedoch zeigen sowohl der Molekülpeak im Massenspektrum der Verbindung bei m/z = 1040,
73
als auch eine Kristallstrukturanalyse der bereitwillig kristallisierenden Substanz unerwartete
Ergebnisse.
Abb. 2.4.1 Bildung des Rhodium(III)-P5-deltacyclen-Zweikernkomplexes 48.
Das Produkt stellt eine dimere Rh(III)-Spezies dar und nicht einen ursprünglich erwarteten
monomeren Rh(I)-Käfigkomplex. Das Metall hat sich oxidativ unter Öffnung der P2–P3Bindung des Dreirings an den Käfig 17 angelagert. Der dimere Rhodium(III)-Käfigkomplex
48 wird in 37 % Ausbeute erhalten. Eine Röntgenstrukturanalyse des aus THF kristallisierten
Rhodium(III)- P5-deltacyclen-Zweikernkomplexes 48 konnte gelöst werden (Abb. 2.4.2). In
den NMR-Spektren, die in Kapitel 2.4.3 genauer diskutiert werden, zeigen sich jedoch zwei
Verbindungen 48a und 48b, die einander sehr ähnlich sind und miteinander im Gleichgewicht
stehen. Aus den Kopplungsdaten lässt sich entnehmen, dass es sich bei beiden Spezies um
Zweikernkomplexe handelt. Neben der in der Röntgenstrukturanalyse gefundenen mesoVerbindung 48 lassen sich noch zwei enantiomere chirale Strukturen 48’ und 48’’ postulieren,
die als Enantiomere identische NMR-Signale aufweisen. Allerdings lässt sich keine
Zuordnung der beiden Signalsätze zu den Strukturen 48 oder 48’/48’’ ableiten. Im Folgenden
wird daher 48 als Modell für die weitere Diskussion von 48a und 48b herangezogen.
2.4.2 Molekülstruktur des Rhodium(III)-P5-deltacyclen-Zweikernkomplexes 48
Die zweikernige Verbindung 48 konnte aus THF monokristallin gewonnen werden. Die aus
der Kristallstrukturanalyse von 48 bestimmte Molekülstruktur ist in der Abb. 2.4.2 gezeigt.
Wie 45a und 47 kristallisiert der Rhodium-Zweikernkomplex in einer triklinen Elementarzelle
in der zentrosymmetrischen Raumgruppe P 1 (Nr.2). In der Elementarzelle ist aber nur ein
Molekül enthalten. Die Struktur weist ein Inversionszentrum in der Mitte der von den vier
Kernen Rh1, Rh1A, P1 und P1A aufgespannten Ebene auf. Die beiden P–C-Käfigteile des
dimeren Komplexes stellen damit Bild und Spiegelbild, also ein racemisches Gemisch eines
Enantiomerenpaars im Festkörper dar. Die P–P-Bindung des Dreirings zwischen P2 und P3
74
wird im Dimer gelöst, wobei zwei Bindungen zu einem Rhodiumatom ausgebildet werden.
Das Käfig-Proton H1, welches im Edukt 17 noch an P1 gebunden war, ist bei 48 zum
Phosphoratom P3 gewechselt. P1 koordiniert an beide Rhodiumatome des Moleküls und
verbrückt somit beide Teile des Dimers. Die Rhodiumatome sind fünffach koordiniert. Neben
der im Edukt vorhandenen Bindung zu einem Chloratom bildet Rh1 eine Bindung zu P1, P2
und P3 innerhalb einer Molekülhälfte aus. Die fünfte Bindung wird zu P1A der anderen
Molekülhälfte ausgebildet. Rh1A ist entsprechend mit P1 des ersten Käfigs verbunden, sowie
mit P1A, P2A, P3A und Cl1A der zweiten Molekülhälfte. Ausgewählte Bindungslängen und
-winkel von 48 sind in Tabelle 2.4.1 zusammengefasst. Die Rhodiumatome sind verzerrt
quadratisch pyramidal koordiniert. Die Grundfläche wird von P3, Cl1, P1A und P1 gebildet.
Rh1 steht geringfügig über dieser Fläche. Die Winkelsumme um das Rhodiumatom in Bezug
auf die vier Liganden der Pyramidengrundfläche beträgt 358.5°, nur 1.5° vom Idealwert 360°
entfernt. Abweichend von der idealen Struktur befinden sich P1 und Rh1-Atom 15 bzw. 16
pm außerhalb der von P3, Cl1 und P1A aufgespannten Ebene. Wegen der Bindungen P1–P2
und P2–C1 weicht die Pyramidenspitze P2 stark von der idealen Geometrie ab. Entsprechend
sind die Winkel P2–Rh1–P1 und P2–Rh–P3 auf 54.0° und 74.4° verkleinert und die Winkel
P2–Rh1–P1A und P2–Rh1–Cl1 auf 96.5° und 136.2° vergrößert.
Cl1
P2
C4A
C1
P3
Rh1
C2A
P1A
C3
P5
C2
P1
P4A
P5A
Rh1A
C3A
P3A
P4
C1A
C4
P2A
Cl1A
Abb. 2.4.2 Molekülstruktur von 48 im Kristall. Die Wasserstoffatome der tert-Butylgruppen wurden der
Übersicht halber weggelassen.
75
Durch den Bindungsbruch zwischen P2 und P3 vergrößert sich der Bindungswinkel P2–C1–
P3 um 21° gegenüber dem intakten Diphosphiranring. Weitere Folgen der Öffnung des Käfigs
sind Winkeländerungen der koordinierten Phosphoratome P1, P2 und P3. So ist der Winkel
P5–C1–P2 um 8° kleiner und C4–P1–P2 um 7° größer als die jeweiligen Winkel im freien P5Deltacyclen. Dazu kommen die Wechselwirkungen mit den beiden Rhodiumatomen im
Bereich der Phosphoratome P1, P2 und P3 die den Käfig 17 weiter deformieren. Das betrifft
gleichermaßen
die
Bindungswinkel
und
die
innerhalb
des
Käfigs
liegenden
Bindungsabstände, an denen diese Atome beteiligt sind. Am stärksten betroffen ist die
Bindung P1–C4, die um etwa 7 pm auf ca. 194 pm gestreckt ist. Die Bindung P1–P2 ist mit
213 pm die kürzeste P–P-Bindung eines Käfigs bei den in dieser Arbeit diskutierten
Komplexen.
Tabelle 2.4.1 Ausgewählte Bindungslängen und Bindungswinkel der Rhodiumverbindung 48a in pm und °.
P1–C4
193.8(3)
P1–Rh1A
240.53(9)
C1–P2–Rh1
92.79(10)
P1–P2
212.84(11)
Rh1–Cl1
237.03(9)
C4–P1–Rh1A
142.07(10)
P2–C1
191.0(3)
C4–C2–P4
108.9(2)
Rh1–P1–Rh1A
101.93(3)
P3–C1
184.6(3)
C4–C2–P3
99.37(18)
P3–Rh1–P1A
157.29(3)
P3–C2
188.3(3)
P4–C2–P3
103.57(14)
C1–P3–Rh1
98.11(10)
P4–C3
168.3(3)
C2–C4–P5
101.32(19)
P1–P2–Rh1
63.65(3)
P4–C2
189.3(3)
P3–C1–P2
94.36(14)
P2–Rh1–P1
54.00(3)
P5–C3
184.2(3)
P3–C1–P5
106.45(15)
P2–Rh1–Cl1
136.24(3)
P5–C1
189.3(3)
P5–C1–P2
103.64(15)
P2–Rh1–P1A
96.53(3)
P5–C4
191.2(3)
C4–P1–P2
103.57(10)
P2–Rh1–P3
74.40(3)
C2–C4
160.8(4)
C2–C4–P1
110.02(19)
P1–Rh1–P1A
78.07(3)
P1–Rh1
235.75(9)
P5–C3–P4
114.36(17)
P1–Rh1–P3
79.84(3)
P2–Rh1
233.06(9)
P5–C4–P1
102.16(14)
P3–Rh1–Cl1
96.75(3)
P3–Rh1
222.43(8)
P2–P1–Rh1
62.35(3)
Cl1–Rh1–P1A
103.82(3)
Bis auf die Bindungen mit den koordinierenden Phosphoratomen sind die Bindungslängen
und -winkel der nicht an der Koordination beteiligten Atome P4, P5, C1, C2, C3 und C4 im
Vergleich zu 17 kaum verändert. Die Bindungslänge Rh1–Cl1 beträgt 237 pm und ist damit
ca. 4 pm kürzer als die Rh–Cl-Abstände in Tetra(phosphino)chlororhodium(I)-[60,61,62] und
Tris(phosphino)trichloro-rhodium(III)-Komplexen[63,64,65] und ca. 2 pm länger als in dem
vierfach koordinierten Rhodium(III)-Komplex [RhCl(PPh3)(PtBu)3].[66] In 48 betragen die
76
Abstände zwischen Rh1 und den beiden formal anionischen Phosphoratomen P1 und P2 236
pm und 233 pm. Die verbrückende Bindung zu P1A mit 241 pm ist sogar noch etwas länger.
Die drei Bindungen liegen damit im Bereich zwischen 220 pm und 243 pm der für Phosphid–
Rhodium-Bindungen in der Literatur gefunden wird.[66,67,68] Wesentlich kürzer fällt die
Bindung zwischen Rh1 und dem sekundären Phosphanatom P3 aus. Die Bindungslänge P3–
Rh1 beträgt hier 222 pm. In der Literatur gefundene Bindungslängen Rh(III)–PR3 liegen
zwischen 221 pm und 242 pm.[69,70,71] Bekannt sind sowohl Rhodium-Komplexe bei denen die
Phosphid–Rhodium-Bindungen kürzer[66,67] als auch länger[68,72,73] ausfallen als die Phosphan–
Rhodium-Bindungen im gleichen Komplex. Der Unterschied der Phosphid– und Phosphan–
Rhodium-Bindungslängen fällt bei 48 allerdings mit 10.7 pm - 18.1 pm ein wenig größer aus.
2.4.3 NMR-Spektroskopische Charakterisierung der Rhodium(III)-P5-deltacyclenZweikernkomplexe 48a und 48b
In Lösungen des Reaktionsproduktes sind in den 31P-NMR-Spektren zwei einander sowohl in
den chemischen Verschiebungen als weitestgehend auch in den Multiplizitäten der Peaks
ähnelnde Sätze mit jeweils fünf Signalen sichtbar. Untereinander weisen beide Sätze deutlich
unterschiedliche Intensitäten auf. Sie gehören somit zu zwei unterschiedlichen Verbindungen
48a und 48b. Wird die schlecht lösliche Mischung beider Verbindungen im NMR-Röhrchen
für 10 Minuten im Ultraschallbad behandelt, zeigt sich im Spektrum nur noch die Verbindung
48a. Nach einem Tag lagern bei Raumtemperatur tritt in der gleichen Probe die zweite
Verbindung 48b erneut mit ca. 35 % auf. Diese Beobachtungen deuten darauf hin, dass die
beiden Verbindungen im Gleichgewicht stehen. Eine mögliche Interpretation wäre die
Annahme
eines
Monomer-Dimer-Gleichgewichts.
Es
wird
jedoch
weder
in
den
Massenspektren ein Peak für ein hypothetisches Monomer beobachtet, noch deuten die NMRDaten auf eine solche Struktur hin. Beide in den NMR-Spektren beobachteten Verbindungen
48a und 48b sind mit der Molekülstruktur von 48 vereinbar (Abb. 2.4.3). Die 31P{1H}-NMRSpektren der beiden Verbindungen sind in der Abb. 2.4.4 zu sehen. Die chemischen
Verschiebungen der Signale sind in Tabelle 2.4.2 zusammengefasst. Die Beträge der
Kopplungskonstanten lassen sich aufgrund der überlagernden Kopplungen nicht bei allen
Peaks direkt ermitteln. Die Kopplungen mit dem Rhodium könnten aufgrund der schlechten
Löslichkeit beider Verbindungen auch nicht direkt aus
103
Rh-NMR-Spektren bestimmt
werden. Sie lassen sich aber teilweise aus 31P-NMR-Spektren entnehmen.
77
P1 48a
P1 48b
P2 48a
P2 48b
P4 48a/b
75.0
ppm (t1)
70.0
65.0
60.0
15.0
ppm (t1)
10.0
5.0
P3 48a/b
P3 48a
P5 48a/b
P2 48a
P3 48b
P1 48a/b
P2 48b
-15.0 -16.0 -17.0 -18.0 -19.0 -20.0 -21.0
ppm (t1)
ppm
300
250
200
150
50
100
0
P1
P2
P4
74.0
ppm (t1)
73.0
72.0
71.0
70.0
69.0
10.0
ppm (t1)
68.0
5.0
0.0
P3
P5
P3
P2
P1
X
ppm
-15.0
ppm (t1)
300
-20.0
250
-25.0
200
X
150
100
50
0
Abb. 2.4.4 31P{1H}-NMR Spektren (122 MHz, CDCl3, 25°C) der Mischung 48a und 48b (oben) und der reinen
Verbindung 48a (unten). X = Restsignale von 48b.
78
Abb. 2.4.3 Zweikern-Komplex 48 mit Benennung der Phosphoratome.
Da für beide Verbindungen nur fünf Signale im
31
P-NMR-Spektrum erkennbar sind, müssen
die als Zweikernkomplexe vorliegenden Verbindungen 48a und 48b jeweils zwei äquivalente
Käfigliganden aufweisen. Auf die Nennung der jeweiligen zweiten Molekülhälfte wird darum
im Folgenden aufgrund der besseren Lesbarkeit des Textes verzichtet
Tabelle 2.4.2 Chemische Verschiebungen in ppm und ausgewählte Kopplungskonstanten in Hz in den 31P{1H}und 1H-NMR-Spektren von 48a und 48b.
JP3P1A
1
4.3
466.9
103.7
4.4
445.5
103.6
P4
P5
P2
P1
P3
H1
48a
323.3
94.3
71.4
4.6
-19.7
48b
327.3
91.4
61.4
10.4
-18.6
2
JP3Rh1
Die Signale der P=C-Doppelbindungen der Komplexe 48a und 48b entsprechen den beiden
am weitesten ins Tieffeld verschobenen Signale bei δ(P4) = 323.3 ppm und 327.3 ppm. Der
als Triplett aufgespaltene Peak bei δ(P5) = 94.3 ppm kann dem Phosphoratom P5 von 48a
zugeordnet werden. Unweit davon, bei δ(P5) = 91.4 ppm, findet sich der entsprechende Peak
von 48b, der im Spektrum als breites Singulett erscheint. Die Signale von P2 von 48a und
48b unterscheiden sich hinsichtlich ihrer chemischen Verschiebung und Multiplizität am
stärksten voneinander. Bei 48a findet sich P2 bei δ(P2) = 71.4 ppm als Dublett vom Triplett.
Die entsprechenden Signale von 48b sind demgegenüber 10 ppm hochfeldverschoben und
liegen dort als Dublett von zwei Multipletts vor. Wie im P,P-COSY-Spektrum in Abb. 2.4.5
zu sehen ist, koppeln die Phosphoratome P5 und P2 in beiden Verbindungen miteinander. Die
Beträge dieser Kopplung 2JP5P2 sind in beiden Verbindungen nicht bzw. nicht exakt
bestimmbar. Bei 48a kann deshalb für die 2JP5P2-Kopplung nur ein Bereich zwischen 35 und
45 Hz angegeben werden. Bei 48b ist die entsprechende Kopplung aufgrund des weiter
79
aufgespaltenen Signals von P2 nicht bestimmbar. Des Weiteren kann im P,P-COSY-Spektrum
eine Kopplung zwischen P5 und P1 beobachtet werden. Kopplungskonstanten sind auch hier
nicht bestimmbar. Über 9 ppm breite Tripletts von Multipletts bei 4.6 ppm bzw. 10.4 ppm
können P1 von 48a und 48b zugeordnet werden. Wie Abb. 2.4.5 zu entnehmen ist, koppelt P1
bei 48a mit P5, P2 und P3. Die entsprechenden Kreuzsignale von 48b sind jedoch so
schwach, dass sie bei entsprechend eingestelltem Schwellenwert fast im Grundrauschen
verschwinden. Sie können daher in Abb. 2.4.5 nicht dargestellt werden. Aufgrund der Breite
des Signals von P1 bei beiden Verbindungen können die Kopplungskonstanten nur indirekt
aus den Signalaufspaltungen der Kopplungspartner bestimmt werden. Literaturbekannte 1JRhPKopplungen sind normalerweise kleiner als 200 Hz und liegen bei Rhodium(III)Verbindungen größenordnungsmäßig eher bei 100 Hz.[74] Daher sollte die Identifikation der
1
JRhP-Konstanten möglich sein. Die 1JP1P2 für 48a kann demnach als die große Aufspaltung
von 389 Hz im Signal von P2 identifiziert werden. Bei einem mit beiden Kernen an Rh(III)
koordiniertem Diphosphid fand man eine größenmäßig vergleichbare Kopplung 1JPP von 363
Hz.[68]
H1A
P3A
Cl
tBu
P1
tBu
H1
P3
P4
P5
tBu
Rh
P4A
2A
P
P2
Rh
Cl
tBu
5A
tBu P
P1A
tBu
tBu
tBu
Abb. 2.4.5 P,P-COSY-Spektrum (122 MHz, CDCl3, 25°C) der Mischung aus Verbindung 48a und 48b.
80
Die deutlich vergrößerte Kopplung 1JP1P2 steht auch im Einklang mit den in der Literatur
beschriebenen größeren Kopplungskonstanten für an Rhodium gebundene Phosphoratome. So
findet sich bei Hey-Hawkins et al. eine um ca. 70 Hz gegenüber dem unkoordinierten Edukt
vergrößerte Kopplung 1JPP in einem P–P–Rh-Dreiring.[75,76] Die analoge Kopplung kann für
48b aufgrund des stärker aufspaltenden Signals von P2 nicht genau angegeben werden, liegt
aber in ähnlicher Größenordnung wie bei 48a. Die beiden Doppeldubletts bei δ = -19.7 und
-18.6 ppm sind dem Phosphoratom P3 in den beiden Verbindungen 48a und 48b zugeordnet.
Die Abstände der einzelnen Peaks betragen bei 48a 467 Hz und 104 Hz, und bei 48b 446 Hz
und 104 Hz. Die beiden kleineren Kopplungskonstanten entsprechen dem Erwartungswert für
1
JRhP-Kopplungen. Da im P,P-COSY-Spektrum für beide Verbindungen nur jeweils ein
Phosphoratom als Kopplungspartner für P3 auftritt, können die beiden kleineren
Aufspaltungen den jeweiligen 1JP3Rh1-Kopplungen zugeordnet werden. Die große Kopplung
2
JP1P3A von 467 Hz bzw. 446 Hz ist nicht ungewöhnlich für die Kopplung zweier trans-
ständiger Phosphanliganden bei Rhodium(III)-Komplexen. Die zu erwartende 2JPP-Kopplung
zweier Phosphoratome, die cis-ständig an Rhodium(III) koordinieren, ist hingegen wesentlich
kleiner. Größenordnungsmäßig liegen diese Kopplungskonstanten bei 10 - 30 Hz.[68,77] Der
Bindungswinkel P3–Rh1–P1A in der Kristallstruktur beträgt 157° und für P3–Rh1–P1 80°.
Damit sind die Kopplungskonstanten 2JP1P3A für 48a und 48b der Kopplung zwischen den
beiden Molekülhälften des Dimers zuzuordnen. Monomere Strukturen können damit für beide
Verbindungen ausgeschlossen werden. Das Käfigproton H1 kann für beide Substanzen 48a
und 48b eindeutig an P3 lokalisiert werden. Die aus protonengekoppelten 31P-NMR-Spektren
ermittelten 1JP3H1-Kopplungskonstanten betragen bei 48a 360 Hz bzw. bei 48b 372 Hz.
Im 1H-NMR-Spektrum der Mischung von 48a und 48b ergeben die jeweils acht tertButylgruppen aufgrund der Molekülsymmetrie und der Ähnlichkeit beider Verbindungen
insgesamt vier Singuletts. Diese liegen bei 1.3, 1.4, 1.6 und 1.7 ppm und weisen ein
Integrationsverhältnis von 1 : 1 : 1 : 1 auf. Bei 48a bildet H1, das an P3 gebunden ist, ein
Dublett vom Dublett bei 4.3 ppm. Die direkte Kopplungskonstante 1JH1P3 beträgt 360 Hz. Die
Zuordnung zum entsprechenden Käfigphosphoratom P3 ist durch ein protonengekoppeltes
31
P-NMR-Spektrum möglich. Die zweite Kopplung von H1 beträgt 39 Hz. Da diese kleinere
Kopplung im protonengekoppelten
31
P-NMR nicht identifizierbar war, bestand die
Möglichkeit, dass es sich bei ihr um eine 2JH1Rh1-Kopplung handeln könnte, also eine
agostische Wechselwirkung des Protons mit dem Rhodiumzentrum.[78] Weil die stark
aufspaltenden breiten Peaks im
31
P-NMR-Spektrum die Identifikation einer eventuell
vorhandenen kleinen P–H-Kopplung erschweren, wurde ein P,H-COSY-Spektrum der
81
relevanten Peaks aufgenommen (Abb. 2.4.6). Hier zeigt sich die schon beobachtete direkte
Kopplung 1JH1P3 und dass die zweite kleinere Kopplung 3JH1P1 zugeordnet werden kann. Es
liegt also keine Kopplung zwischen H1 und Rh1 vor. In der Verbindung 48b ist das Signal
von H1 bei 4.4 ppm in direkter Nachbarschaft zum entsprechenden Signal von 48a zu finden.
Die Kopplungskonstanten 1JH1P3 bzw. 3JH1P1 betragen hier 372 und 34 Hz. Die Kopplung
3
JH1P1 von 48a und 48b ist demnach ähnlich groß wie die Kopplung 3JH1P5, die in den
[M(CO)5]-Komplexserien b und d aufgrund der Karplus-Relation mit großen Diederwinkeln
H1–P1–C4–P5 beobachtet wurden. In der Molekülstruktur 48 beträgt der Diederwinkel H1–
P3–Rh1–P1 176.8°. Die räumliche Anordnung dieser Atome bei 48a und 48b sollte daher
nicht stark von der Struktur 48 abweichen. Neben den schon beschriebenen Peaks sind im
Hochfeldbereich bis -60 ppm keine hydridischen Protonen erkennbar. Somit können
unmittelbar an Rhodium gebundene Protonen ausgeschlossen werden.
Abb. 2.4.6 P,H-COSY-Spektrum (CDCl3, 25°C) der Verbindung 48a.
Im 13C-NMR-Spektrum ergeben die zwei Verbindungen 48a und 48b wie auch schon im 1HNMR-Spektrum aufgrund der Ähnlichkeit beider Moleküle nur einen Satz an Signalen für
ihre tert-Butylgruppen. So sind zwischen 36 und 41 ppm vier Multipletts der quartären
C(CH3)3-Kohlenstoffe der tert-Butylgruppen sichtbar. Die primären C(CH3)3-Kohlenstoffatome der tert-Butylgruppen ergeben ebenfalls vier Signale, die zwischen 30 und 35 ppm
82
liegen und zu Multipletts aufgespalten sind. Die Zuordnung der Signale anhand der
chemischen Verschiebung konnte auch durch ein J-moduliertes
13
C-NMR-Spektrum (APT)
verifiziert werden. Die Gerüstkohlenstoffatome sind aufgrund der zu erwartenden linienreichen Multipletts nicht beobachtbar.
Aus den diskutierten NMR-Spektren zeigt sich, dass beide Verbindungen 48a und 48b
strukturell sehr ähnlich beschaffen sein müssen. Sie stehen zudem im Gleichgewicht, wobei
dieses vollständig zu 48a verschiebbar ist. Sowohl die chemischen Verschiebungen als auch
die beobachtbaren Kopplungskonstanten in den
31
P-NMR-Spektren sind untereinander
ähnlich. In den 1H- und 13C-NMR-Spektren findet sich für die tert-Butylgruppen nur ein Satz
an Signalen. Ein Vorliegen als Zweikernkomplex kann bei 48a und 48b aufgrund der großen
Kopplung zwischen P3 und P1A und der Massenspektren als sicher erachtet werden. Bei
beiden Substanzen ist das Proton H1 an P3 gebunden. Auch die chemischen Verschiebungen
für von H1 von 48a und 48b unterscheiden sich kaum. Die Kopplung 3JH1P1 ist bei beiden
Verbindungen relativ groß. Diese Kopplung lässt sich über einen Karplus-artiger
Zusammenhang mit dem in der Molekülstruktur 48 beobachteten Diederwinkel H1–P3–Rh–
P1 von nahe 180° in Einklang bringen. Die Phosphoratome P3 beider Spezies 48a und 48b
können an Hand der signifikanten Kopplungskonstante 1JP3Rh1 als Bindungspartner des
Rhodiums identifiziert werden. Daher kann eine Bildung von Epimeren aus der Inversion des
stereogenen Zentrums P3 ausgeschlossen werden. Alle anderen Phosphoratome besitzen kein
direkt gebundenes Proton und hydridische Protonen am Rhodium konnten auch
ausgeschlossen werden. Die enge spektroskopische Verwandtschaft von 48a und 48b und ihre
gleichzeitige Vereinbarkeit mit der im Festkörper bestimmten Molekülstruktur 48 fordert eine
Lösung des Strukturproblems, bei der die beiden Käfigliganden der Zweikernkomplexe
jeweils nur einen einzelnen Signalsatz liefern. Bei 48 ist das durch das Inversionszentrum
garantiert, das die beiden modifizierten Käfigenantiomere 17’ und 17’’ als Liganden
miteinander verbindet. Neben dem aus dem Enantiomerenpaar 17’ und 17’’ gebildeten
Zweikernkomplex muss aber noch ein weiteres Zweikernkomplexpaar existieren, welches
jeweils zwei gleiche Enantiomere der geöffneten Käfigliganden miteinander verbindet. Das
betrifft die Kombination (17’)2Rh2Cl2 48’ und (17’’)2Rh2Cl2 48’’, die ihrerseits wieder ein
Enantiomerenpaar bilden. Beide können C2-symmetrisch sein und sie hätten identische NMRSpektren, die sich aber von denen der meso-Verbindung (17’)(17’’)Rh2Cl2 48 unterscheiden
(Abb. 2.4.7). Diese Interpretation der Befunde steht im Einklang mit allen experimentellen
Beobachtungen. Demnach gibt es ein bei Raumtemperatur langsames Gleichgewicht
83
zwischen den Stereoisomeren 48a und 48b, bei denen die epimeren Fragmente (17’)RhCl und
(17’’)RhCl ausgetauscht werden.
Abb. 2.4.7 Schematische Molekülstruktur der beiden Enantiomere 48’ und 48’’
Die zentrosymmetrische Version 48 ist in ihren Kristallisationseigenschaften bevorzugt. Sie
wird darum im Festkörper beobachtet. Das Enantiomerenpaar der chiralen Version des
Zweikernkomplexes müsste hingegen beide Enantiomere zentrosymmetrisch in einer
Elementarzelle unterbringen um vergleichbare Kristallisationsbedingungen zu ermöglichen.
Das ist entropisch benachteiligt. Eine Zuordnung von 48a und 48b zu diesen beiden Fällen ist
zurzeit noch nicht möglich.
2.5 iso-P5-Deltacyclen
2.5.1 Darstellung von iso-P5-Deltacyclen 49a/b
S. Huguet-Torrell hatte in seinen Arbeiten versucht, das Käfigproton H1 von 17 durch eine
chirale Alkylgruppe aus Alkylhalogeniden zu substituieren. Beim Versuch zur Deprotonierung von 17 mit Lithiumorganylen beobachtete er jedoch anstelle der geplanten
Substitutionsreaktion eine unerwartete Umlagerung des Käfigs zum iso-P5-Deltacyclen 49,
bei der P1 und C4 einschließlich des tert-Butylsubstituenten den Platz tauschen. Das
Wasserstoffatom H1 behält seine Position in Bezug auf den Käfig bei diesem Prozess. Aus
einer R2PH-Einheit wird damit eine R2CHt-Bu-Gruppe (Abb. 2.5.1). Diese Reaktion erwies
sich als reproduzierbar und stellt einen effizienten Weg zur Synthese von Isomeren des P5Deltacyclens in Ausbeuten von bis zu 88 % dar. Um 17 zu iso-P5-Deltacyclen 49 umzulagern,
wird ein Equivalent n-Butyllithium langsam zu einer Lösung von 17 in THF bei -78 °C
gegeben. Die Kontrolle der Zugabegeschwindigkeit ist wichtig, da sonst weitere Isomere des
Käfigs entstehen, die bislang nur teilweise charakterisiert werden konnten.
84
Abb. 2.5.1 Umlagerungsreaktion von 17a/b zu den beiden Epimeren 49a und 49b des iso-P5-Deltacyclens.
Die anfangs hellgelbe Lösung von 17 färbt sich bei Zugabe des ersten Tropfens nButyllithium schlagartig dunkelblau. Die Reaktionsmischung verändert anschließend ihre
Farbe von blau über grün nach rot und ist nach Beendigung der Reaktion nach ca. 1 h wieder
gelb. Bei der Reaktion entstehen zwei Epimere 49a und 49b, wobei deren Verhältnis in den
Reaktionsmischungen ca. 1 : 0.12 beträgt.
Ein möglicher Reaktionsweg der Umlagerung ist in Abb. 2.5.2 gezeigt. Dieser ionische
Mechanismus konnte in DFT-Rechnungen von T. Shubina nachvollzogen werden. Zunächst
wird die P–H-Gruppe am P5-Deltacyclenkäfig 17 mit Hilfe der starken Base n-Butyllithium
deprotoniert und in ein Phosphid-Anion überführt. Im folgenden Schritt wechseln P1 und C4
unter Bildung eines Carbanions die Plätze. Der berechnete Übergangszustand dieses Schrittes
liegt energetisch 4.9 kcal mol-1 über dem Phosphid-Anion, das Carbanion ist um 17.7 kcal
mol-1 stabiler als das Phosphid-Anion (RB3LYP\CC-pVDZ).[37] Die Stabilisierung des
Carbanions erfolgt möglicherweise ylidartig über eine partielle Delokalisierung der negativen
Ladung auf die zwei angrenzenden Phosphoratome. Die Reprotonierung des prochiralen
Carbanions erfolgt spätestens bei der säulenchromatographischen Aufarbeitung des
Rohprodukts (SiO2/5 %H2O). Durch die Regenerierung des stereogenen Zentrums C4 ergibt
sich das beobachtete Epimerengemisch 49a und 49b.[36] Alternativ könnte der Mechanismus
der Umlagerung auch radikalisch ablaufen. Als Hinweis auf diese Hypothese sind die,
während der Reaktion Beobachtbaren Farben zu werten. In ESR-Spektren, die unter den
Reaktionsbedingungen der Umlagerungsreaktion von U. Zenneck aufgenommen wurden,
konnten auch tatsächlich verschiedene Radikale beobachtet werden. Die Spektren ließen sich
jedoch nicht weiter interpretieren. Auch zu diesem Reaktionsweg wurden DFT-Rechnungen
von T. Shubina angefertigt (RB3LYP\CC-pVDZ).[37] Der Mechanismus erfolgt analog dem
ionischen Reaktionsweg über ein Phosphorradikal das zu einem Kohlenstoffradikal umlagert.
Der berechnete energetische Unterschied zwischen Phosphorradikal und Kohlenstoffradikal
85
liegt bei 18.1 kcal mol-1. Das unterscheidet sich kaum vom ionischen Mechanismus. Ein
radikalischer Übergangszustand konnte in den DFT-Rechnungen allerdings nicht gefunden
werden. Aufgrund der Ladungsseparation konnten bislang für die beiden Mechanismen keine
diskutierbaren Energiedifferenzen zwischen Edukt und den Intermediaten der alternativen
Reaktionswege in Lösung berechnet werden. Daher kann noch keine endgültige Aussage über
den Reaktionsverlauf gemacht werden.
Abb. 2.5.2 Ionischer Mechanismus der Umlagerung.
2.5.2 NMR-Spektroskopische Charakterisierung von iso-P5-Deltacyclen 49a/b
In den
31
P-NMR-Spektren des Reaktionsgemisches der Umlagerung sind zwei Produkte
erkennbar. Bislang wurde nur das Hauptprodukt 49a als iso-P5-Deltacyclen beschrieben. Die
zweite, stets in geringerem Maße auftretende Verbindung wurde als weitere Käfigverbindung
unbekannter Zusammensetzung bezeichnet und nicht näher charakterisiert.[79] Da der letzte
Reaktionsteilschritt der Umlagerung aus einer Protonierung eines Carbanions bzw. der
Hydrogenierung eines Kohlenstoffradikals besteht, sollten sich zweier Epimere 49a und 49b
bilden, bei denen das stereogene Zentrum von C4 regeneriert wird und die tert-Butylgruppe
entweder cis- oder trans-ständig zu P5 steht. Die zwei im NMR-Spektrum beobachtbaren
Verbindungen sollten also den beiden Epimeren 49a und 49b zugeordnet werden können,
zumal keine weiteren Signalsätze in den NMR-Spektren gefunden werden (Abb. 2.5.3). Eine
zufällige Isochronie des kompletten Signalsatzes beider Epimere ist zwar möglich, aber in
86
Anbetracht der Anzahl der Phosphoratome sehr unwahrscheinlich. Wie im Kapitel 2.6.2
gezeigt wird, konnten in den Röntgenstrukturen der Metallkomplexe des iso-P5-Deltacyclens
zwei Epimere gefunden werden. Daher sollten diese auch im freien iso-P5-Deltacyclenliganden auftreten. In Tabelle 2.5.1 sind die bislang dem iso-P5-Deltacyclen 49a
zugeordneten Signale und Kopplungskonstanten der
31
P- und 1H-NMR-Spektren denen des
Epimers 49b gegenübergestellt.
Tabelle 2.5.1 Chemische Verschiebung in ppm und Kopplungskonstanten in Hz in den 31P{1H}- und 1H-NMRSpektren von 49a und 49b.
δ(P4)
δ(P5/P1) δ(P1/P5)
δ(P2)
δ(P3)
1
JP1P5
1
JP2P3
δ(H1)
49a
347.8
114.8
60.1
-22.0
-137.8
174.9
185.8
3.0
49b
320.7
80.2
46.5
-31.5
-156.0
192.8
193.5
2.0
Abb. 2.5.3 31P{1H}-NMR-Spektrum (122 MHz, CDCl3, 25°C) des Gemisches 49a und 49b.
In den
31
P-NMR-Spektren liegen die Signale von P4 bei δ(P4) = 348 ppm für 49a und
δ(P4) = 321 ppm für 49b. Diese Signale liegen etwa 27 ppm voneinander entfernt im
87
charakteristischen Bereich für P=C-Doppelbindungen. Die Signale von P1 und P5 erscheinen
bei 49a bei 115 und 60 ppm mit einer Kopplung 1JP1P5 von 175 Hz. Die Zuordnung eines der
beiden Peaks zu den Molekülpositionen P1 oder P5 ist aus den bisher diskutierten NMRDaten nicht möglich. Bei 49b erscheinen P1 und P5 jeweils etwas hochfeldverschoben
gegenüber 49a bei 80 und 47 ppm mit einer etwas größeren Kopplung 1JP1P5 von 193 Hz. Sie
können ebenfalls nicht eindeutig P1 oder P5 zugeordnet werden. Auch die Kopplungen zu den
anderen Phosphoratomen im Käfig, die alle sowohl mit P1 als auch P5 über zwei Bindungen
verknüpft sind und daher
2
J-Kopplungen aufweisen, ermöglichen keine eindeutige
Zuordnung. Die Kopplungskonstanten wurden teilweise mithilfe einer Simulation ermittelt,
deren Ergebnisse in der Abb. 2.5.4 den Signalen des gemessenen
49a und 49b gegenübergestellt sind. Tabelle 2.5.2 fasst die
31
31
P-NMR-Spektrums von
31
P, P-Kopplungskonstanten
zusammen. Man kann deutlich erkennen, dass die Kopplungskonstanten von 49a und 49b mit
Ausnahme der Kopplung 2JP3P5 sehr ähnlich ausfallen. Das Signal von P2 findet sich sowohl
bei 49a mit δ(P2) = -22 ppm, als auch bei 49b mit δ(P2) = -32 ppm deutlich tieffeldverschoben zu den entsprechenden Peaks im Eduktgemisch 17a/b (δ(P2) = -112 und -107
ppm). Dies ist dem veränderten chemischen Umfeld zuzuschreiben. Der Diphosphiranring ist
beim iso-P5-Deltacyclen über P2 an eine CHtBu-Gruppe gebunden und nicht mehr wie bei
17a/b an das Phosphoratom P1.
P5/P1
P4
P1/P5
P2
P3
49a
Simulation
gemessen
348.0
347.4
115.8
114.8
113.8
60.8 60.2 59.6 59.0 -21.3
81.0
80.0
79.0
47.4
-22.5
-137.0
-138.0
49b
Simulation
gemessen
321.0 320.4
46.4
45.4 -30.6
-31.6
-32.8 -155.3 -156.3
Abb. 2.5.4 Peaks der simulierten und gemessenen 31P{1H}-NMR-Spektren (122 MHz, CDCl3, 25°C) von 49a
und 49b. Die Abweichung (RMS) zwischen den gemessenen und berechneten Spektren beträgt 0.006 Hz für 49a
und 0.035 Hz für 49b. In der Simulation wurde eine feste Linienbreite von 4 Hz verwendet.
88
Tabelle 2.5.2 Simulierte 31P,31P-Kopplungskonstanten der iso-P5-Deltacyclene 49a und 49b in Hz.
2
JP1P4
2
JP4P5
3
JP2P4
2
JP3P4
1
JP1P5
2
JP1P2
2
JP1P3
2
JP2P5
2
JP3P5
1
JP2P3
49a
21.2
22.5
0.1
4.4
174.9
0.1
9.8
14.9
14.9
185.8
49b
20.3
18.9
0.6
9.9
192.8
0.1
11.4
12.1
0.2
193.5
Die direkte 1JP2P3-Kopplung beträgt bei 49a 186 Hz und bei 49b 194 Hz. Die Signale von P3
kommen in 49a und 49b nach wie vor relativ weit im Hochfeldbereich bei -138 ppm und -156
ppm in der typischen Region für Diphosphirane.
Im 1H-NMR-Spektrum von 49a und 49b befinden sich jeweils vier große Peaks im
Integrationsverhältnis 1 : 1 : 1 : 1 zwischen 1.2 und 1.5 ppm, die den tert-Butylgruppen
zugeordnet werden können. Bei 49a befindet sich das Signal des C–H-Protons H1 bei 3.0
ppm zum Dublett mit einer Kopplungskonstante von 6 Hz aufgespalten. Ebenfalls zum
Dublett aufgespalten ist H1 bei 49b, dessen chemische Verschiebung 2.0 ppm beträgt. Die
Kopplungskonstante fällt mit 15 Hz etwas größer aus als bei 49a. Die um 1 ppm
unterschiedliche chemische Verschiebung von H1 bei 49a und 49b kann in gleichem Ausmaß
auch bei 17a/b und den Epimeren der [M(CO)5]-Komplexe des P5-Deltacyclens beobachtet
werden. Dort ist in den Fällen, in denen das Proton trans-ständig zu P5 steht, das Signal von
H1 immer um ca. 1 ppm hochfeldverschoben gegenüber dem Signal des jeweiligen Epimers.
Außerdem koppelt H1 bei 17a/b, 44a-d, 45a-d und 46a-d mit unterschiedlichen Kopplungsbeträgen zum jeweiligen geminalen oder vicinalen Kopplungspartner, je nachdem ob es cisoder trans-ständig zu P5 steht. Die beobachteten 2J-Kopplungen sind dabei stets kleiner als 9
Hz. Die Kopplung 3JH1P5 der Verbindungen 17b, 44d-46d und 44b-46b, bei denen das P–HProton H1 trans-ständig zu P5 steht, ist jedoch mit 28 bis 40 Hz signifikant größer. Dieser
Karplus-artige Zusammenhang sollte auch beim iso-P5-Deltacyclen gelten. Da der
Unterschied der Kopplungskonstanten bei 49a und 49b geringer ausfällt, kann durch die
Größe der Kopplung alleine keine Zuordnung zum Kopplungspartner erfolgen. Die
Korrelation von Kopplungsgröße und chemischer Verschiebung bei 49a und 49b lässt sich
jedoch als starker Hinweis deuten, dass H1 bei 49b trans-ständig zu P5 steht.
Dementsprechend wäre 49a dasjenige Epimer, bei dem H1 cis-ständig zu P5 steht. Durch ein
P,H-COSY-Spektrum kann daher eine Zuordnung der Signale im 31P-NMR-Spektrum zu den
Phosphoratomen P1 und P5 erfolgen. Die Kopplung JPH1 ist bei 49a zwischen H1 und dem
Peak bei 60 ppm und bei 49b zwischen H1 und dem Peak bei 47 ppm zu beobachten. Somit
deutet alles darauf hin, dass das Signal von 49a bei 60 ppm P1 und entsprechend das Signal
von 49b bei 47 ppm P5 zugeordnet werden kann. Damit wäre eine Signalzuordnung von
89
δ(P1) = 60 ppm und δ(P5) = 115 ppm bei 49a und von δ(P1) = 80 ppm und δ(P5) = 47 ppm
bei 49b zu treffen. Ein Unterschied der chemischen Verschiebung in den
31
P-NMR-Spektren
von bis zu 68 ppm zwischen einem Phosphoratom der beiden Epimere erscheint relativ groß,
zumal eine intuitive Zuordnung der Peaks anhand der chemischen Verschiebung anders
ausfallen würde. Der größere Unterschied bei den chemischen Verschiebungen von P5 der
Epimere des iso-P5-Deltacyclens 49a/b im Vergleich zu den Epimeren des P5-Deltacyclens
17a/b wird möglicherweise durch die stärker voneinander abweichende Geometrie der beiden
Epimere 49a und 49b hervorgerufen. Dort verändert sich neben der Position von H1 auch die
Position der tert-Butylgruppe an C4. Diese erfährt bei 49a eine sterische Abstoßung durch die
tert-Butylgruppe an C2 und bei 49b durch die tert-Butylgruppe an C1. Zudem findet man bei
den [M(CO)5]-Komplexen der iso-P5-Deltacyclen-Epimere ebenfalls größenordnungsmäßig
ähnliche Unterschiede in den chemischen Verschiebungen bei P1 und P5 von ca. 50 ppm,
wobei die Zuordnung der Signale dort über die Metallkoordination am P1 eindeutig ist. Die
NMR-Daten sprechen für die hier getroffene Zuordnung von P1 und P5 bei 49a/b, dennoch ist
sie mit entsprechender Vorsicht zu betrachten.
Da das Epimer 49b in viel geringerem Anteil in der Produktmischung enthalten ist, ließen
sich in den 13C{1H}-NMR-Spektren bislang nur die Signale von 49a beobachten. Vier große
Multipletts zwischen 33.0 ppm und 33.8 ppm können den primären C(CH3)3Kohlenstoffatomen der tert-Butylgruppen zugeordnet werden. Die zugehörigen quartären
C(CH3)3-Kohlenstoffatome finden sich bei 34.1, 35.6, 37.3 und 42.9 ppm und spalten zu ddd
mit 2JCP- Kopplungskonstanten zwischen 6 und 17 Hz auf. Das Signal bei 65.4 ppm kann dem
Gerüstkohlenstoffatom C4 zugeordnet werden und ist damit gegenüber dem Edukt 17 um ca.
20 ppm hochfeldverschoben. Das ddd setzt sich zusammen aus zwei 43 und 53 Hz großen
direkten
1
JCP-Kopplungen und einer 2JCP-Kopplung, die 16 Hz beträgt. Zwei weitere
Gerüstkohlenstoffatome treten als linienreich aufgespalten Multipletts bei δ(C1) = 66.7 ppm
und δ(C2) = 99.4 ppm in ähnlichen Regionen wie im Edukt 17 auf. Das Signal des
Kohlenstoffatoms der P=C-Doppelbindung kommt in der dafür typischen Region bei δ(C3) =
220.3 ppm. Es spaltet zum ddd mit Kopplungskonstanten von 6, 11 und 52 Hz auf.
90
2.6 Chrom-, Molybdän- und Wolframpentacarbonylkomplexe des iso-P5-Deltacyclens
2.6.1 Darstellung der Chrom-, Molybdän- und Wolframpentacarbonyl-iso-P5deltacyclenkomplexe 42a/b, 50a/b und 43a/b
Analog zu den Umsetzungen von 17a/b wurde das Epimerengemisch des iso-P5-Deltacyclens
49a/b mit [M(CO)5THF] (M = Cr, Mo, W) umgesetzt, um die komplexchemisch reaktivsten
Phosphordonoren des umgelagerten Käfigs zu bestimmen (Abb. 2.6.1).
H
tBu
H
(OC)5M
tBu
tBu
(OC)5M
P
P
tBu
P
P P
P
P
tBu
+ [M(CO)5THF]
P
THF
P P
P
tBu
tBu
tBu
49a/b
42: M = Cr
50: M = Mo
43: M = W
H
tBu
+
P
P P
P
tBu
tBu
tBu
42a, 43a und 50a
42b, 43b und 50b
Abb. 2.6.1 Bildung der beiden [M(CO)5]-Epimere 42a/b, 43a/b und 50a/b.
Wie schon von S. Huguet-Torrell beobachtet bindet das Epimerengemisch 49a/b jeweils nur
ein [M(CO)5]-Fragment, auch wenn die Metallkomponente in zehnfachem Überschuss
eingesetzt wird. In FD-Massenspektren erscheinen dementsprechend die Molekülpeaks als
Basispeaks bei m/z = 625 für den Chrom-, 668 für den Molybdän- und 757 für den
Wolframkomplex. Die Ausbeute der Chrom-, Molybdän und Wolframverbindungen betragen
74 %, 71 % und 77 %. Es entstehen zwei epimere 1 : 1 Komplexe, bei denen das [M(CO)5]Fragment stets an P1 koordiniert. Nach der Umsetzung sind beide Signalsätze von 49a und
49b restlos verschwunden. Die Anteile der gebildeten Verbindungen der [M(CO)5]-Komplexe
42a/b, 43a/b und 50a/b entsprechen jedoch nicht denen des eingesetzten Epimerengemisches
von 49a/b, wobei die genauen Anteile je nach Ansatz variieren. Qualitativ kann jedoch
bemerkt werden, dass der Anteil der [M(CO)5]-Komplexen 42b, 43b und 50b deutlich
gegenüber dem entsprechenden Epimer des iso-P5-Deltacyclens 49b ansteigt. Wird die
Produktmischung längere Zeit in Lösung stehen gelassen, zerfällt ein Teil der Komplexe und
es wird sowohl 49a als auch 49b wieder regeneriert. Der beobachtbare Anteil von 49b
gegenüber 49a steigt dann entsprechend dem Verhältnis, das bei der Metallkoordination
beobachtet worden war. Anscheinend wird bei der Metallkoordination das Epimerenverhältnis
des iso-P5-Deltacylens deutlich verschoben.
91
2.6.2 Molekülstruktur von Molybdänpentacarbonyl-iso-P5-deltacyclen 50a
Aus n-Hexan konnten bei +4 °C Einkristalle von 50a erhalten werden, die für eine
Röntgenstrukturanalyse geeignet waren. Die Verbindung 50a kristallisiert in der triklinen
Raumgruppe P 1 (Nr. 2). In der Elementarzelle sind zwei Moleküle des Komplexes enthalten,
die den beiden Enantiomeren des Komplexes entsprechen. Die Molekülstruktur ist in Abb.
2.6.2 gezeigt. Wie dort zu sehen ist, entspricht sie dem Epimer 50a, in dem H1 cis-ständig zu
P5 liegt. Der Diederwinkel H1–C4–P4–P5 beträgt 55.2°. Ausgewählte Bindungslängen und
-winkel der Verbindung sind in Tabelle 2.6.1 aufgeführt. Im Vergleich mit der
Molekülstruktur des Isomers 45a unterscheiden sich die Bindungslängen der Atome von
Diphosphiran- und Tricyclohexenring kaum. Abweichungen zwischen den beiden Strukturen
um ca. 2 pm sind lediglich bei den Bindungen P2–P3, P4–C2 und P5–C1 zu finden. Die
Länge der neu gebildeten P–C-Bindungen beträgt 185.5 pm für C4–P2 und 188.8 pm für P1–
C2. Die Bindungslänge P1–P5 liegt mit 219.3 pm in der Größenordnung, die für P–PBindungen charakteristisch ist.
O1
O5
O2
C9
C5
C6
Mo
C8
O4
C4
C7
H1
P1
O3
C2
P2
P5
C1
P4
C3
P3
Abb. 2.6.2 Molekülstruktur eines Enantiomers von 50a im Kristall. Die Wasserstoffatome der tert-Butylgruppen
wurden der Übersicht halber weggelassen.
Die Bindungswinkel innerhalb der Diphosphiranringe sind in 45a und 50a nahezu identisch.
Im Cyclohexenring von 50a vergrößern sich alle Winkel um bis zu 5.6° gegenüber 45a. Die
92
größten Unterschiede der Bindungswinkel des Käfiggerüsts lassen sich jedoch bei den
Winkeln beobachten, deren Scheitelpunkte durch C4 bzw. P1 gebildet werden. Aufgrund der
gegenüber 45a vergrößerten Bindungslängen C2–P1 und P1–P5, verkleinert sich der Winkel
C2–P1–P5 in 50a um 10.6° gegenüber dem analogen Winkel in 45a. Ebenso verringern sich
die Winkelweiten von C2–P1–C4 und P5–P1–C4 um 4.5° und 10.3° gegenüber den
vergleichbaren Winkeln von 45a. Im Gegensatz dazu vergrößert sich der Winkel P1–C4–P2
um 13.4° in 50a gegenüber C4–P1–P2 in 45a.
Tabelle 2.6.1 Ausgewählte Bindungslängen und Bindungswinkel von 50a in pm und °.
P1–C4
186.12(19)
P4–C2–P1
105.30(9)
Mo–P1–C2
129.15(6)
C4–P2
185.47(18)
P3–C2–P1
105.97(9)
Mo–P1–P5
105.13(2)
P2–C1
186.35(19)
P4–C2–P3
103.65(10)
P1–Mo–C5
95.95(5)
P2–P3
222.00(14)
C2–P1–P5
90.71(6)
P1–Mo–C6
89.70(5)
P3–C1
185.34(19)
C1–P3–P2
53.54(6)
P1–Mo–C7
92.58(5)
P3–C2
191.05(18)
P3–C1–P2
73.35(8)
P1–Mo–C8
93.19(5)
P4–C3
168.73(19)
P3–C1–P5
113.80(10)
P2–Mo–C9
175.69(6)
P4–C2
187.64(19)
P5–C1–P2
112.24(9)
C5–Mo–C7
171.34(7)
P5–C3
184.6(2)
C1–P2–P3
53.12(6)
C6–Mo–C8
176.61(7)
P5–C1
187.16(18)
C2–P1–C4
106.51(8)
Mo–C5–O1
174.49(16)
P1–P5
219.93(7)
P5–P1–C4
93.12(6)
Mo–C6–O2
176.92(17)
P1–C2
188.75(18)
P1–C4–P2
108.40(9)
Mo–C7–O3
172.60(16)
P1–Mo
260.03(5)
Mo–P1–C4
120.07(6)
Mo–C8–O4
176.56(16)
Der deutlichste Strukturunterschied zwischen den Valenzisomeren 50a und 45a in Bezug auf
die jeweilige Metallkoordination besteht darin, dass das Metallatom bei 50a von zwei tertButyl-Einheiten benachbart ist, während bei 45a nur eine tert-Butyl-Gruppe direkt neben dem
Metall steht. Das deutet auf einen vermehrten sterischen Druck zwischen dem [Mo(CO)5]Fragment und den beiden flankierenden tert-Butyl-Substituenten von 50a, der als Ursache für
die Verlängerung der Bindung P1–Mo (260.0 pm) von 50a um ca. 7 pm gegenüber der P–MoBindung von 45a (252.7 pm) infrage kommt. In beiden Fällen werden auch die
Carbonylliganden aus der idealen Oktaederposition gedrängt. Nur der Winkel P1–Mo–C6,
93
beträgt bei 50a ca. 90°, da die Carbonylgruppe C6≡O2 im Festkörper auf das sterisch weniger
anspruchsvolle Proton H1 ausgerichtet ist. Die entsprechenden Winkel der anderen drei cisständigen Carbonylliganden, die in Richtung der tert-Butylgruppen von C3 und C4 orientiert
sind, betragen zwischen 92.6 und 96.0°. Die Bindungswinkel Mo–C≡O sind auf bis zu 172.6°
gegenüber der linearen Bindung verkleinert. Entsprechend weichen die Winkel C–Mo–C um
bis zu 8.7° von 180° ab. Die Abweichungen von der idealen Oktaedergeometrie des
Molybdänhexacarbonyls fallen damit ebenso wie die Bindungslänge P1–Mo bei 50a
insgesamt etwas größer aus als bei 45a. Das belegt den gegenüber 45a gewachsenen
sterischen Anspruch des Käfigliganden von 50a.
Von C. Höhn und S. Huguet-Torrell konnten Kristallstrukturen der [Cr(CO)5]- und [W(CO)5]Komplexe von 49a und 49b beobachtet werden,[35,36] deren Daten im Folgenden mit 50a
verglichen werden. Die Bindungslängen und -winkel in der Molekülstruktur des iso-P5Deltacyclengerüsts von [Cr(CO)5]-Komplex 42a[35] sind nahezu identisch mit 50a (Tabelle
2.6.2). Die Bindungslängen beider Strukturen weichen um maximal 1.4 pm, die Winkel nur
um bis zu 0.3° voneinander ab. Die Bindungslänge P1–Cr (247.2 pm) ist ebenfalls um ca. 7
pm länger als in 44a. Einzige Ausnahme ist der Winkel P1–P5–C1, der bei 50a um 1.4°
kleiner ausfällt. Es ist daher davon auszugehen, dass die Struktur des [W(CO)5]-Komplexes
43a ebenfalls im Wesentlichen der von 42a und 50a entsprechen sollte. Von 43a ist nur eine
Molekülstruktur in enantiomerenreiner Form 43a’’[36] verfügbar. Auch hier finden sich im
Vergleich mit 50a nur geringfügige Änderungen in Bindungslängen und -winkeln. Auffällig
ist bei 43a’’ jedoch eine Verlängerung der Bindung P2–P3 auf 228.4 pm und die dadurch
verursachten Veränderungen der angrenzenden Bindungswinkel. Dies kann aber möglicherweise durch die unterschiedliche Raumgruppe und die dadurch veränderten Packungseffekte
verursacht werden.
Die Molekülstruktur 43b[35], in der das [W(CO)5]-Fragment an P1 des iso-P5-DeltacyclenEpimers 49b gebunden ist, weist hingegen deutliche Unterschiede zu den Strukturen der
Komplexepimere des Typs a auf. Am stärksten fällt der Unterschied der Komplexisomere bei
der Bindungslänge von P2–P3 aus, die bei 43b nur 215.1 pm beträgt und damit um ca. 7 pm
kürzer ist, als bei 50a bzw. um ca. 13 pm kürzer als bei 43a’’. Entsprechend unterschiedlich
sind auch die bei 43b beobachteten Bindungswinkel im Vergleich mit den Winkeln der
Komplexepimere a. Am stärksten unterscheiden sich die Winkel P5–P1–C4 (100.5°) und C2–
P1–C4 (97.8°), die um ca. 7.4 bzw. 8.7° von den Winkeln bei 50a abweichen. Ebenso ändern
sich die drei anderen Bindungswinkel mit P1 als Winkelscheitel. Die Winkel W–P1–P5
(109.9°) und M–P1–C4 (126.7°) vergrößern sich um ca. 5 bzw. 7° und der Winkel W–P1–C2
94
(123.6°) verringert sich um ca. 6° gegenüber den entsprechenden Winkeln von 50a. Damit
orientiert sich das an P1 koordinierte [W(CO)5]-Fragment von der tert-Butylgruppe an C4
weg, die bei 43b cis-ständig zu P5 steht. Zudem weichen die Metallcarbonylbindungswinkel
bei 43b teilweise etwas stärker von der idealen Oktaedergeometrie ab als bei 50a. Bei 43b
betragen die Winkel W–C–O zwischen 172.9 und 178.5° und die beiden Winkel C–W–C
168.7 und 176.9°. Die Winkel P1–W–C betragen zwischen 90.5 und 97.4°.
Tabelle 2.6.2 Ausgewählte Bindungslängen und -winkel von 42a[35], 43a’’[36], 43b[35] und 50a in pm und °.
P1–M
P1–C4
P2–P3
P2–C1
C2–P1–C4
P5–P1–C4
42a
247.15(5)
186.83(15)
222.16(7)
186.85(15)
106.40(6)
92.94(5)
50a
260.03(5)
186.12(19) 222.00(14) 186.35(19)
106.51(8)
93.12(6)
43a’’
258.51(9)
186.1(4)
228.42(19)
185.9(5)
107.01(19)
92.81(14)
43b
261.21(8)
188.4(4)
215.1(3)
190.5(3)
97.84(17)
100.59(15)
2.6.3 Spektroskopische Charakterisierung der Chrom-, Molybdän- und
Wolframpentacarbonyl-iso-P5-deltacyclenkomplexe 42a/b, 50a/b und 43a/b
In den Kristallstrukturen der [W(CO)5]-Komplexe konnte sowohl 43a’’ als auch 43b
beobachtet werden.[35,36] Damit ist die Existenz beider Epimere des iso-P5-Deltacyclens 49a/b
in Form ihrer [W(CO)5]-Komplexe nachgewiesen. In den NMR-Spektren der [M(CO)5]Komplexe lassen sich daher, wie auch schon beim freien Ligand 49a/b, zwei Signalsätze
finden, die den beiden Epimerenserien der iso-P5-Deltacyclenkomplexe a und b zugeordnet
werden können (Abb. 2.6.3). Der Fall, dass die NMR-Spektren beider Epimere zufällig
identisch wären, kann verworfen werden, da sich die beiden Substanzen zumindest in den
Kopplungen des Käfigprotons H1 deutlich unterscheiden müssten. Die Käfigstruktur von 49a
kann den [M(CO)5]-Komplexen 42a, 43a und 50a und entsprechend 49b den Komplexen
42b, 43b und 50b zugeordnet werden. Die Tabelle 2.6.3 zeigt die chemische Verschiebung
der Chrom-, Molybdän und Wolframpentacarbonyl-iso-P5-Deltacyclene des Typs a und b in
den 31P{1H}-NMR-Spektren. Es zeigt sich, dass wie im Fall der [M(CO)5]-Komplexe des P5Deltacyclens
jeweils
vier
der
fünf
Käfigphosphoratome
untereinander
ähnliche
Verschiebungen aufweisen. Das Phosphoratom P1 weist im Gegensatz dazu stark
95
unterschiedliche chemische Verschiebungen für die verschiedenen Metalle auf und kann
damit als koordinierendes Phosphoratom identifiziert werden.
Abb. 2.6.3 31P{1H}-NMR-Spektrum (122 MHz, CDCl3, 25°C) des Gemisches 50a und 50b. Nummerierung von
H1 und den Käfigatomen bei 42a/b (M = Cr) und 43a/b (M = W) wie bei 50a/b.
In Abb. 2.6.4 sind die gespreizten
31
P-NMR-Peaks der [Mo(CO)5]-Verbindungen 50a und
50b und deren Simulation abgebildet. Die daraus resultierenden 31P,31P-Kopplungskonstanten
sind in der Tabelle 2.6.4 zusammengestellt. Die weit ins Tieffeld verschobenen Signale bei
ca. 361 und 372 ppm der Komplexe können dem jeweiligen sp2-hybridisierten Phosphoratom
P4 zugeordnet werden. Beide Signale liegen damit deutlich verschoben gegenüber δ(P4) der
Edukte 49a und 49b. Die sehr viel stärkere Tieffeldverschiebung der [M(CO)5]-Komplexe b
gegenüber dem freien Epimer 49b wird möglicherweise durch die Abstoßung des [M(CO)5]Fragments von der tert-Butylgruppe an C4 verursacht. Dies könnte auch ein Grund für den
unterschiedlichen Betrag der Kopplungskonstanten 2JP1P4 sein. Bei beiden Epimeren des
freien Liganden 49a und 49b beträgt sie ca. 20 Hz. Während 2JP1P4 bei 50a auf 30.6 Hz steigt,
96
sinkt der Wert der Konstante bei seinem Epimer 50b auf 4.6 Hz. Die Kopplungskonstante
2
JP4P5 beträgt hingegen in beiden Metallkomplexepimeren ca. 15 Hz.
Tabelle 2.6.3 Chemische Verschiebung in ppm und ausgewählte Kopplungen in den 31P{1H}-NMR-Spektren der
Komplexe 42a/b, 43a/b und 50a/b und ihrer Liganden 49a/b.
1
JP1P5
1
P4
P5
P1
P2
P3
JP2P3
42a
360.8
135.7
102.4
4.8
-129.4
161.1
190.7
50a
357.6
136.3
79.1
0.5
-132.9
153.5
190.5
43a
356.8
140.1
57.6
1.9
-129.8
149.9
191.2
42b
371.4
86.9
148.3
-16.7
-139.6
155.1
175.5
50b
371.5
87.0
124.7
-16.7
-143.5
146.8
176.6
43b
371.5
92.4
103.7
-19.8
-141.9
142.4
175.2
49a
347.8
114.8
60.1
-22.0
-137.8
174.9
185.8
49b
320.7
46.5
80.2
-31.5
-156.0
192.8
193.5
Im Gegensatz zu den Edukten 49a/b lassen sich die Signale von P1 und P5 durch die
Koordinationsverschiebung bei den [M(CO)5]-Komplexen eindeutig ihren Molekülpositionen
zuordnen. Bei allen in dieser Arbeit analysierten P–C-Käfigverbindungen fällt die
Koordinationsverschiebung für die koordinierten Phosphoratome der [W(CO)5]-Komplexe
minimal aus. Das ist die Grundlage der in der Tabelle 2.6.3 getroffenen Zuordnung von P1
und P5. So ergibt sich für P1 eine Koordinationsverschiebung ∆δ(31P) von +42.3, +19.0 und
-2.5 ppm bei 42a, 43a und 50a und von +68.1, +44.5 und +23.5 ppm bei 42b, 43b und 50b.
Entsprechend dem Unterschied der Koordinationsverschiebungen beider Epimere fällt auch
∆δ(P5) des benachbarten Phosphoratoms aus. Bei 50a beträgt δ(P5) = 136.3 ppm und ist
damit um ca. +22 ppm zum Signal von P5 bei 49a tieffeldverschoben. Die entsprechende
Verschiebung beträgt bei 50b (δ(P5) = 87.0 ppm) im Vergleich mit 49b ca. +41 ppm. Die
Kopplung 1JP1P5 fällt bei 50a (153.5 Hz) und 50b (146.8 Hz) aufgrund der Metallkoordination
an P1 deutlich geringer aus als in 49a und 49b. Die Signale von P2 sind sowohl bei 50a
(δ(P2) = 0.5 ppm), als auch bei 50b (δ(P2) = -16.7 ppm) stärker tieffeldverschoben als P2 in
49a und 49b. Eine Tieffeldverschiebung gegenüber den Edukten ist auch bei P3 bei 50a
(δ(P3) = -132.9 ppm) und 50b (δ(P3) = -143.5 ppm) beobachtbar. Die Kopplung 1JP2P3 der
beiden Phosphoratome beträgt 190.5 Hz bei 50a und 176.6 Hz bei 50b.
97
P4
P1
P5
P2
P3
50a
Simulation
gemessen
358.0 356.8 137.2 136.0
80.2 79.4 78.6
P1
P4
1.6
0.8
P5
0.0
-131.8
-132.8
P2
-133.8
P3
50b
Simulation
gemessen
371.8 371.0
125.6 124.0
88.0
86.8
-15.8
-16.8
-17.8 -142.5
-143.5
-144.5
Abb. 2.6.4 Simulierte und gemessene 31P{1H}-NMR-Spektren (122 MHz, CDCl3, 25°C) von 50a und 50b. Die
Abweichung (RMS) zwischen den gemessenen und berechneten Spektren beträgt 0.013 Hz für 50a und 0.036 Hz
für 50b. In der Simulation wurde eine Linienbreite von 4 Hz verwendet.
Tabelle 2.6.4 Simulierte 31P-31P Kopplungskonstanten der Epimere 49a und 49b des iso-P5-Deltacyclens und der
iso-P5-Deltacyclenkomplexe 50a und 50b in Hz.
2
JP1P4
2
JP4P5
3
JP2P4
2
JP3P4
1
JP1P5
2
JP1P2
2
JP1P3
2
JP2P5
2
JP3P5
1
JP2P3
50a
30.6
14.9
0.1
10.1
153.5
10.5
18.6
14.2
14.0
190.5
50b
4.6
15.8
0.1
0.1
146.8
16.1
15.2
0.1
9.4
176.6
49a
21.2
22.5
0.1
4.4
174.9
0.1
9.8
14.9
14.9
185.8
49b
20.3
18.9
0.6
9.9
192.8
0.1
11.4
12.1
0.2
193.5
In den 1H-NMR-Spektren der [M(CO)5]-Komplexe 42a/b, 43a/b und 50a/b liegen die Signale
der tert-Butylgruppen jeweils als vier Singuletts im Integrationsverhältnis 1 : 1 : 1 : 1
zwischen 1.1 ppm und 1.6 ppm. Wie schon bei den Epimeren 49a und 49b beobachtet, beträgt
auch bei den [M(CO)5]-Verbindungen des Typs a und b der Unterschied der chemischen
Verschiebung des C–H-Protons H1 ca. 1 ppm. Gegenüber 49b ist das Signal von H1 der
[M(CO)5]-Komplexe 42b, 43b und 50b um ca. 0.9 ppm tieffeldverschoben und erscheint bei
2.9 ppm. Eine Tieffeldverschiebung der gleichen Größenordnung findet sich bei 49a und den
[M(CO)5]-Komplexen 42a, 43a und 50a, deren Signale von H1 bei ca. 3.9 ppm beobachtbar
sind. Das Signal von H1 von 49a, 49b, 50a und 50b ist jeweils zum Dublett aufgespalten mit
Kopplungskonstanten JH1P zwischen ca. 4 und 15 Hz. Die Zuordnung dieser Kopplung kann
98
aus dem in Abb. 2.6.5 gezeigten P,H-COSY-Spektrum erfolgen. Dort ist ersichtlich, dass H1
von 50b mit P5 und von 50a mit P1 koppelt. Damit überwiegt bei den [M(CO)5]-Komplexen
42b, 43b und 50b wie auch beim Liganden 49b die Kopplung 3JH1P5 des trans zu P5
stehenden Protons H1. Bei der Komplexen 42a, 43a und 50a und deren Liganden 49a ist
hingegen die geminale Kopplung 2JH1P1 dominant. Die Kopplungsbeträge 3JH1P5 sind bei den
[M(CO)5]-Komplexen des Typs b mit ca. 4 Hz deutlich geringer als bei 49b (15 Hz), während
sich die 2JH1P1 bei den Komplexen a gegenüber 49a von ca. 6 Hz auf 9 Hz vergrößert. Dies
kann durch die Metallkoordination am Phosphoratom P1 erklärt werden. Sie verstärkt
geminale- und 3J(cis)-Kopplungen gegenüber 3J(trans)-Kopplungen.[51] Aus den chemischen
Verschiebungen von H1 und seinen Kopplungen erscheint somit eine Zuordnung des iso-P5Deltacyclenepimers 49a zu den [M(CO)5]-Komplexen 42a, 43a und 50a und entsprechend
von 49b zu 42b, 43b und 50b am wahrscheinlichsten.
Abb. 2.6.5 Ausschnitt aus dem P,H-COSY-Spektrum (CDCl3, 25°C) der Mischung aus 49a, 49b, 50a und 50b.
In den 13C{1H}-NMR-Spektren der [M(CO)5]-Komplexe 42a/b, 43a/b und 50a/b finden sich
die Signale der primären C(CH3)3-Kohlenstoffatome der tert-Butylgruppen als vier
Multipletts im Bereich zwischen 32 und 36 ppm und die der quartären C(CH3)399
Kohlenstoffatome als vier Multipletts zwischen 34 und 42 ppm. Aufgrund der zu erwartenden
linienreichen Aufspaltung sind die Gerüstkohlenstoffatome nicht in den Spektren der
[M(CO)5]-Komplexe zu beobachten. Für die tert-Butylgruppen des Epimers sollte ein zweiter
Satz Signale beobachtbar sein. Die Signale überlagern aber wahrscheinlich mit den schon
beschriebenen kompliziert aufgespaltenen Multipletts und können daher nicht separat
identifiziert werden.
Die CO-Valenzschwingungen in den IR-Spektren der [M(CO)5]-Komplexe 42a/b, 43a/b und
50a/b liegen in ähnlichen Bereichen. Exemplarisch sollen die νCO-Banden von 50a und 50b
kurz diskutiert werden. Die Banden der beiden Komplexe überlagern sich und können daher
nicht getrennt betrachtet werden. Die drei für [M(CO)5]-Komplexe erwarteten Banden sind
bei 2069, 1993 und 1941 cm-1 zu beobachten. Sie liegen im gleichen Bereich, wie bei 45a-d
und sind damit gegenüber [M(CO)6] ähnlich stark zu niedrigeren Frequenzen verschoben. Das
deutet auf vergleichbar ausgeprägte σ-Bindungen der koordinierenden Phosphoratome und
entsprechend verstärkte π-Rückbindungsanteile zu den verbliebenen fünf Carbonylliganden.
Die
13
C-NMR- und IR-Spektren bestätigen damit die Ergebnisse, die durch die bisherigen
Spektren und Analysen vorlagen.
Aus der Anzahl der P1 - P5 jeweils direkt benachbarten tert-Butylgruppen lässt sich für 49a/b
eine ungünstigere sterische Situation als in 17a/b erwarten. Im Unterschied zu den [M(CO)5]Verbindungen des P5-Deltacyclens (44a-d, 45a-d und 46a-d) koordinieren dementsprechend
beide Epimere des iso-P5-Deltacyclens 49a/b nur an das Phosphoratom P1. Eine Koordination
von [M(CO)5]-Fragmenten der Chromtriade an P2, die bei 17a/b beobachtet wurde, konnte
bei 49a/b nicht gefunden werden. Möglicherweise schirmt die tert-Butylgruppe an C4, die
sich im iso-P5-Deltacyclen in unmittelbarer Nachbarschaft zu P2 befindet, dieses
Phosphoratom sterisch so weit ab, das dort keine Koordination von [M(CO)5] mehr erfolgen
kann. Durch die Umlagerungsreaktion ist P5 im iso-P5-Deltacyclen 49a/b nun nicht mehr in
gleichem Umfang von der tert-Butylgruppe an C4 blockiert wie 17a/b. Der sterische
Anspruch durch die tert-Butylgruppen an C1 und C3 scheint auszureichen, um eine
Koordination von [M(CO)5]-Fragmenten der Chromtriade an P5 zu verhindern. Das sterisch
weniger anspruchsvolle Eisentetracarbonyl lässt sich im Gegensatz zu den hier berichteten
Resultaten auch an P5 koordinieren. Einkristalle eines disubstituierten iso-P5-Deltacyclens
konnten von M. Hofmann erhalten werden. Die beiden [Fe(CO)4]-Fragmente koordinieren
hierbei an P1 und P5.[80] Versuche, iso-P5-Deltacyclen mit [(η6-C6H6)RuCl2]2 umzusetzen,
ergaben keinen beobachtbaren stabilen Komplex. Bei P5-Deltacyclen wurde aufgrund der
höheren Raumfüllung des [(η6-C6H6)RuCl2]-Fragments nur Komplex 47 beobachtet.
100
Insgesamt lässt sich aus diesen Resultaten ein höherer sterische Anspruch ableiten, den die
Koordinationsstellen des iso-P5-Deltacyclens im Vergleich mit P5-Deltacyclen aufweisen.
2.7 P5-Homocunean
2.7.1 Darstellung von P5-Homocunean 51
Durch die Zugabe von einem Äquivalent Benzophenon zur Reaktionsmischung aus P5Deltacyclen 17a/b und n-Butyllithium ergibt sich statt iso-P5-Deltacyclen 49a/b ein anderes
Umlagerungsprodukt, das als P5-Homocunean 51 identifiziert werden konnte. Die Ausbeute
von 51 beträgt bis zu 90 %. Die Bezeichnung P5-Homocunean wurde von der Nomenklatur
des Kohlenwasserstoffverbindung abgeleitet. Cunean ist ein Isomer des Cubans und lässt sich
aus diesem katalytisch mit Hilfe von Silber(I)- oder Palladium(II)-Ionen synthetisieren.[81] Im
P5-Homocunean ist eine der ursprünglichen C–C-Bindungen des Gerüsts um eine CHREinheit erweitert worden, die in diesem Fall zwei Phosphorkäfigatome miteinander verbindet
(Abb. 2.7.1). Im Gegensatz zu den bisher diskutierten Käfigen ist das P5-Homocunean
vollständig gesättigt. Die P=C-Doppelbindung des P5-Deltacyclens ist nicht mehr vorhanden.
Da diese Bindung als schwaches Chromophor der Käfigverbindungen wirkt, ist P5Homocunean 51 im Gegensatz zu den bisher diskutierten gelben Käfigverbindungen ein
farbloses Pulver.
tBu
P
P
Ag+ oder Pd2+
tBu
Cuban
Cunean
P
H
P
P
tBu
tBu
P5-Homocunean 51
Abb. 2.7.1 Bildungsreaktion von Cunean. Nomenklatur des P5-Homocuneans 51.
Eine alternative Darstellungsmöglichkeit für das P5-Homocunean wurde zeitgleich von I.
Keller entdeckt. Sie konnte das P5-Deltacyclen 17 mit einem Äquivalent Cs2CO3 in THF bei
Raumtemperatur ebenfalls zu 51 umsetzen, wobei das iso-P5-Deltacyclen 49a/b und ein
weiteres bisher nicht charakterisiertes Nebenprodukt höherer Masse im Reaktionsgemisch
beobachtet wurden.[34]
101
H
tBu
n-BuLi
P
P
P
P
PhCOPh
tBu
P
P
tBu
P
THF
tBu
H
tBu
P
P
P
tBu
tBu
tBu
49a
51
Abb. 2.7.2 Postulierter Reaktionsmechanismus der Bildung von P5-Homocunean 51 aus dem Epimer 49a des
iso-P5-Deltacyclens.
Die Beobachtung von 49a/b als Nebenprodukt der Umlagerung bei milderen Bedingungen
führt zur Überlegung, dass 49a/b ein denkbares Zwischenprodukt der Umlagerung von 17 in
51 sein könnte. Folgt man dieser Hypothese, lässt sich eine einfache Valenzisomerisierung
von 49a zum isolierten P5-Homocunean 51 formulieren, wobei das von der Epimerisierung
betroffene stereogene Zentrum C4 von diesem Prozess unberührt bleibt (Abb. 2.7.2). Die
Umlagerung sollte darum wieder zu zwei Epimeren von 51 führen. Um die Mechanismushypothese zu verifizieren, wurde versucht, die Umlagerung zu 51 auch mit dem Gemisch der
Epimere des iso-P5-Deltacyclens 49a/b durchzuführen. Die Reaktion von 49a/b mit jeweils
einem Äquivalent Benzophenon und n-Butyllithium zum P5-Homocunean 51, erweist sich
tatsächlich als möglich, jedoch entstehen hierbei eine Vielzahl an Nebenprodukten. Es ergibt
sich auch eine wesentlich geringere Ausbeute von nur ca. 15 %. Ebenso lässt sich eine Lösung
beider Epimere von iso-P5-Deltacyclen 49a/b in THF durch Zugabe von 0.1 molarer
wässriger NaOH innerhalb von 45 Minuten zu 51 umlagern. Auch hier entstehen einige nicht
vollständig aufgeklärte Nebenprodukte, die aber alle wie P5-Homocunean 51 keine P=CDoppelbindung mehr aufweisen. Es erscheint möglich, dass eines der beobachteten
Nebenprodukte
aus
der
Umlagerung
des
iso-P5-Deltacyclens
dem
bislang
nicht
nachgewiesenen CH(tert-Butyl)-Epimer des P5-Homocuneans 51 entspricht. Bislang konnte
dies jedoch noch nicht zweifelsfrei verifiziert werden. Bei der oben beschriebenen Reaktion
von P5-Deltacyclen 17a/b mit n-Buthyllithium und Benzophenon entsteht jedoch
ausschließlich 51.
102
2.7.2 Spektroskopische Charakterisierung von P5-Homocunean 51
Das FD-Massenspektrum weist mit 100 % Intensität einen Molekülpeak bei m/z = 432 auf.
Das bestätigt die Bewertung von 51 als Isomer von 17. Da vom freien Liganden 51 keine
Kristalle ausreichender Qualität für eine Röntgenstrukturanalyse erhalten werden konnten,
stützt sich die folgende Diskussion der NMR-Daten auf die Molekülstrukturen, die von den
[M(CO)5]-Komplexen der Chromtriade erhalten werden konnten (Kapitel 2.8.2). Das
31
P{1H}-NMR Spektrum von P5-Homocunean 51 zeigt wieder fünf Signale, im Gegensatz zu
P5-Deltacyclen 17a/b und iso-P5-Deltacyclen 49a/b wird aber nur ein Signalsatz für 51
gefunden (Abb. 2.7.3).
H1
tBu
P1
C3
C2
P4
5
P
tBu
P5
P1
C4
tBu
2
P3 P
P3
P2
P4
C1
tBu
51
300
200
100
0
-100
-200
Abb. 2.7.3 31P{1H}-NMR-Spektrum (122 MHz, CDCl3, 25°C) von P5-Homocunean 51.
Die gespreizten Signale aus dem
31
P{1H}-NMR-Spektrum des P5-Homocuneans 51 sind in
der Abb. 2.7.4 der Simulation des Spektrums gegenübergestellt. Die chemischen
Verschiebungen und Kopplungskonstanten sind in Tabelle 2.7.1 zusammengefasst. Das im
Edukt 17a/b in der charakteristischen P=C-Doppelbindungsregion angesiedelte Signal von P4
ist im Produkt 51 nicht mehr beobachtbar. P4 bildet stattdessen zusammen mit P5 und C3 in
51 einen zweiten Dreiring. Infolgedessen verschieben sich beide Signale nach δ(P4) = -41.4
103
und δ(P5) = -102.6 ppm stark ins Hochfeld. Die Kopplungskonstante 1JP4P5 beträgt 182 Hz.
Der aus dem Edukt 17 übernommene Dreiring beinhaltet die zwei Phosphoratome P2 und P3,
deren Signale bei δ(P2) = 5.2 und δ(P3) = 42.1 ppm zu finden sind. Beide koppeln direkt mit
einer Kopplungskonstante von 1JP2P3 = 167 Hz. Das aufgrund der Umlagerung nicht mehr
direkt an P5 gebundene P1 wird zu einem nach 83.7 ppm tieffeldverschobenen Multiplett.
Tabelle 2.7.1 Chemische Verschiebung in ppm und 31P,31P-Kopplungskonstanten in Hz im 31P-NMR-Spektrum
von P5-Homocunean 51.
51
P1
P3
P2
P4
P5
83.7
42.1
5.2
-41.4
-102.6
1
JP3P2
167.8
2
JP3P4
24.2
3
JP2P4
14.8
2
JP1P3
16.2
2
JP1P4
24.6
1
JP4P5
182.5
2
JP3P5
7.3
2
JP2P5
8.3
2
JP1P2
15.7
2
JP1P5
0.0
P1
84.0
83.6
P3
83.2
43.0
42.6
42.2
P2
41.8
41.4
41.0
6.0
P4
-40.3
-40.7
-41.1
-41.5
5.6
5.2
4.8
4.4
P5
-41.9
-42.3
-101.8
-102.2
-102.6
-103.0
-103.4
Abb. 2.7.4 Simuliertes (oben) und gemessenes (unten) 31P{1H}-NMR-Spektrum (122 MHz, CDCl3, 25°C) von
P5-Homocunean 51. Die Abweichung (RMS) zwischen gemessenem und berechnetem Spektrum beträgt 0.013.
In der Simulation wurde eine feste Linienbreite von 2 Hz verwendet.
Im 1H-NMR-Spektrum des P5-Homocuneans 51 ergeben die tert-Butylgruppen vier Singuletts
zwischen 1.0 und 1.3 ppm im Integrationsverhältnis 1 : 1 : 1: 1. Das C–H-Käfigproton H1 ist
bei 2.7 ppm als breites Singulett zu finden. Die chemische Verschiebung des entsprechenden
Käfigprotons H1 bei 49a liegt mit 2.9 ppm im ähnlichen Bereich, während δ(H1) = 2.0 ppm
104
des iso-P5-Deltacyclen-Epimers 49b sich deutlich davon unterscheidet. Die Übereinstimmung von 49a und 51 kann als Hinweis auf analoge Konfigurationen für C4 bei 49a und
51 gewertet werden. Das Singulett von H1 wird von zwei 13C-Satelliten mit einer 1JCH1 = 125
Hz begleitet. Das entspricht dem Erwartungswert für ein sp3-hybridisiertes Kohlenstoffatom.
Daher sollten die von C4 ausgehenden Bindungen nicht stark von der idealen
Tetraedergeometrie abweichen und der sterische Druck auf dieses Atom eher gering sein.
Im
13
C{1H}-NMR-Spektrum sind bei 29.5, 30.0 und 31.3 ppm drei voneinander getrennte
Multipletts für die C(CH3)3-Kohlenstoffatome der tert-Butylgruppen sichtbar. Das Signal bei
31.3 ppm ist deutlich intensiver als die beiden anderen und entsteht daher aus einer
Überlagerung der C(CH3)3-Gruppen zweier tert-Butylgruppen. Die Peaks der quartären
C(CH3)3-Kohlenstoffatome der tert-Butylgruppen sind bei 34.9, 35.6, 36.7 und 37.6 ppm zu
finden und spalten als dd oder ddd auf. Die Multipletts der Gerüstkohlenstoffatome liegen im
13
C{1H}-NMR-Spektrum bei 38.4 56.2, 66.5 und 72.5 ppm. Das Signal bei 66.5 ppm kann C4
zugeordnet werden, da es als einziges der vier Gerüstkohlenstoffatome nur zwei
Phosphoratome als direkte Nachbarn hat und daher zu einem dd aufspaltet. Alle anderen
Gerüstkohlenstoffatome bilden Dubletts vom Doppeldublett aus. Das Signal von C1 liegt bei
δ = 56.6 ppm. Die Zuordnung ist durch den Vergleich der chemischen Verschiebungen der
Signale der Gerüstkohlenstoffe der [M(CO)5]-Komplexe des P5-Homocuneans möglich. Die
chemische Verschiebung von C1 ändert sich ebenso wenig durch die Metallkoordination wie
die des Signals von C4. Die beiden anderen Gerüstkohlenstoffatome C2 und C3 sind direkt an
P4 gebunden, an dem die Koordination erfolgt. Dementsprechend werden für beide Kerne
Koordinationsverschiebungen bei den Metallkomplexen beobachtet. Das Signal von C3
erscheint bei 72.5 ppm in der gleichen Region wie C4 des anderen Diphosphiranrings und das
Signal von C2 lässt sich bei 38.4 ppm beobachten. Die Daten aus dem
13
C-NMR-Spektrum
bestätigen die Zusammensetzung von 51 ohne neue Erkenntnisse zu liefern. Das
13
C-NMR-
Spektrum von 51 ist damit mit den Ergebnissen aus den 1H- und 31P-NMR-Spektren und der
Elementaranalyse vereinbar, bietet aber selbst keine signifikanten Informationen über die P–
C-Käfigverbindung.
In den NMR-Spektren von 51 lässt sich im Gegensatz zu 17a/b und 49a/b jeweils immer nur
ein Signalsatz finden. Es entsteht folglich nur eine Verbindung. Möglicherweise blockieren
die beiden tert-Butylgruppen an C1 und C3 die Position, die die tert-Butylgruppe an C4
einnehmen müsste, um ein CH(tert-Butyl)-Epimer von 51 zu erzeugen. Da von 51 keine
Kristallstruktur erhalten werden konnte, wird der sterische Anspruch der tert-ButylSubstituenten von 51 anhand der Molekülstruktur des Molybdänpentacarbonyl-P5105
homocunean-Komplexes in Kapitel 2.8.2 untersucht. Die Epimere 17a und 17b stehen in
einem dynamischen Gleichgewicht und Verschiebungen des Epimerenverhältnisses von 49a
und 49b sind durch die Koordination von [M(CO)5]-Fragmenten ebenfalls bereits beobachtet
worden. Zudem wurde auch bei der Synthese von [(η6-C6H6)RuCl2(P5C20H37)] 47 das
Gleichgewicht der Epimere von 17 vollständig zu einem einzigen Produkt verschoben. Eine
derartige Verschiebung des Gleichgewichts zu einem Epimer erscheint daher möglich, sofern
die Energien beider hypothetischen Epimere aufgrund der sterischen Wechselwirkungen ihrer
tert-Butylgruppen stark unterschiedlich ausfallen. Zumindest durch die Umlagerungsreaktion
von 17a/b mit n-Buthyllithium und Benzophenon wird ausschließlich 51 gebildet und somit
das Epimerengleichgewicht von 17a/b auf ein einziges Käfigenantiomer 51 refokussiert.
2.8 Chrom-, Molybdän- und Wolframpentacarbonylkomplexe des P5-Homocuneans
2.8.1 Darstellung der Chrom-, Molybdän- und Wolframpentacarbonyl-P5homocuneankomplexe 52, 53 und 54
Die Synthese der [M(CO)5]-Komplexe von 51 erfolgt analog zu der Umsetzung von iso-P5Deltacyclen 49a/b mit [M(CO)5THF] bei Raumtemperatur. Ungeachtet der Konzentrationsverhältnisse zwischen der [M(CO)5]-Komponente und dem Liganden 51 entsteht jeweils nur
eine spektroskopisch beobachtbare und isolierbare Verbindung mit einem koordinierten
[M(CO)5]-Fragment (Abb. 2.8.1). Die Ausbeuten betragen für Chrompentacarbonyl-P5homocunean 52 74 %, für Molybdänpentacarbonyl-P5-homocunean 53 68 %, und für
Wolframpentacarbonyl-P5-homocunean 54 79 %.
H
tBu
H1
tBu
tBu
P
tBu
P
P
P
tBu
51
C3
[M(CO)5THF]
4
P
THF
52: M = Cr
53: M = Mo
54: M = W
P
(CO)5M
P1
C2
P5
C
tBu
4
tBu
2
P3 P
C1
tBu
52, 53 und 54
Abb. 2.8.1 Synthese der Chrom-, Molybdän- und Wolframpentacarbonyl-P5-homocunean-Komplexe 52 - 54.
106
2.8.2 Molekülstruktur von Chrom-, Molybdän- und Wolframpentacarbonyl-P5homocunean 52, 53 und 54
Alle drei [M(CO)5]-Verbindungen 52 - 54 ließen sich bei +4 °C aus n-Hexan
auskristallisieren. Sie kristallisieren in der orthorhombischen Raumgruppe Pnma (Nr. 62),
ausgewählte Bindungslängen und -abstände sind in Tabelle 2.8.1 zusammengefasst. Da alle
drei Strukturen isotyp sind und sich hinsichtlich der Bindungslängen und -winkel der
molekularen Bausteine untereinander keine starken Unterschiede ergeben, wird im Folgenden
nur die Struktur von 53 im Detail beschrieben. Das in der Röntgenstrukturanalyse gefundene
Molekül liegt auf einer kristallographischen Spiegelebene. Die daraus resultierende
Fehlordnung hat zur Folge, dass theoretisch zwei unterschiedliche Moleküle im Kristall
enthalten sein könnten oder nur eines der beiden Moleküle vorhanden ist. Die beiden
kristallographisch möglichen Strukturen weisen eine Bindung zwischen P2 und C4 auf die
kristallographisch nicht eindeutig als Einfach- oder Doppelbindung klassifizierbar ist. Es lässt
sich Restelektronendichte an C4 finden, was auf ein H-Atom an C4 und damit auf eine
Einfachbindung zwischen P2 und C4 hindeutet. Auch die beiden Bindungen P2–P3 und
P2–C1 sind mit einer Doppelbindung P2=C4 nicht vereinbar. Bestätigt wird dieser Befund
durch das
31
P{1H}-NMR-Spektrum. Dort fehlt im Gegensatz zum Edukt 17 ein Signal im
charakteristischen Spektralbereich für sp2-hybridisierte Phosphoratome. Somit ergibt sich die
in Abb. 2.8.2 dargestellte Molekülstruktur für 53 im Kristall. Die Bindungslängen P3–P2,
C1–P2, P2–C4 und C4–P1 von 53 sind den entsprechenden Bindungsabständen von 50a
ähnlich. Die Molekülhälfte dieser Käfiggerüstatome ist durch die Umlagerungsreaktion nur
wenig verändert. Die Bindungswinkel zwischen den Atomen P3, P2, C1, C4 und P1 weichen
dementsprechend bei 53 auch nur um bis zu 4° von den entsprechenden Winkeln von 50a ab.
Durch die Valenzisomerisierung werden die Bindungen P1–C3 und P4–P5 geknüpft und
dadurch ein weiterer Diphosphiranring P4–P5–C3 und ein Diphosphacyclobutanring
P1–C2–P4–C3 gebildet. Die P=C-Doppelbindung von 50a wird durch die Isomerisierung in
eine P–C-Einfachbindung umgewandelt. Entsprechend wird die im iso-P5-Deltacyclen
vorhandene Bindung P1–P5 gelöst. Der Abstand zwischen den beiden Phosphoratomen P1
und P5 beträgt in 53 ca. 319 pm. Die Längen der Bindungen zwischen den Atomen C2, P1,
C3, P4 und P5 und deren Winkel weichen bei 53 im Vergleich zu den [Mo(CO)5]-Komplexen
45a und 50a stärker voneinander ab als bei 45a im Vergleich mit 50a. Die Bindung P5–C3 ist
um ca. 9 pm kürzer als die anderen drei P–C-Bindungen in den beiden Diphosphiranringen.
107
C30
H1
C40
C4
C3
P1
O1
P5
C5
P2
P4
C1
O2
C2
C6
P3
Mo
C10
C20
C9
O5
C8
O4
C7
O3
Abb. 2.8.2 Molekülstruktur von 53 im Kristall. Die Wasserstoffatome der tert-Butylgruppen wurden der
Übersicht halber weggelassen.
Die Winkel des neu gebildeten Diphosphiranrings entsprechen bis auf C3–P4–P5 (51.8°)
denen im Diphosphiranring, der von P2, P3 und C1 gebildet wird. In 53 beträgt die Bindung
P4–C3 189.5 pm. Sie ist damit um ca. 21 pm länger als die entsprechende P4=C3Doppelbindung in 45a bzw. 50a und bildet in 53 die Verbindung zwischen dem
Diphosphiran- und dem Diphosphacyclobutanring. Im Diphosphacyclobutanring betragen die
Bindungslängen von C2–P4 und P4–C3 189.5 pm, während die beiden anderen Bindungen
C3–P1 und P1–C2 mit 186.5 pm etwas kürzer ausfallen. Ebenso unterscheiden sich
insbesondere durch die bei der Käfigumlagerung neu gebildeten Ringe die Bindungswinkel
von 53 teilweise stark im Vergleich zu 45a und 50a.
Der Bindungsabstand Mo–P4 beträgt 253 pm. Die Bindungslängen M–P4 betragen 242 pm
bei Chrompentacarbonyl-P5-Homocunean 52 und 253 pm bei Wolframpentacarbonyl-P5Homocunean 54. Damit sind die Bindungslängen M–P4 nur um ca. 2 pm länger als die
jeweiligen Bindungen M–P2 der entsprechenden P5-Deltacyclen-[M(CO)5]-Komplexe 44a,
45a und 46a, aber um ca. 5 pm kürzer als die jeweiligen Bindungen M–P1 der entsprechenden
iso-P5-Deltacyclen-[M(CO)5]-Komplexe 42a, 43a’’, 43b und 50a.
108
Tabelle 2.8.1 Ausgewählte Bindungslängen und Bindungswinkel von 52, 53 und 54 in pm und °.
52
53
54
P1–C4
188.1(3)
188.0(2)
188.2(2)
P2–C4
185.9(3)
185.5(2)
185.6(2)
P2–C1
187.1(2)
186.85(17)
186.77(18)
P2–P3
221.05(11)
220.57(9)
220.35(9)
P3–C1
189.43(11)
189.53(9)
189.48(10)
P3–C2
196.18(17)
195.24(14)
195.52(14)
P4–C3
190.15(15)
189.49(12)
189.07(13)
P4–C2
190.15(15)
189.49(12)
189.07(13)
P5–C3
180.31(17)
180.51(14)
180.63(14)
P5–C1
183.58(16)
182.75(14)
182.84(14)
P1–C3
186.84(15)
186.55(13)
186.54(13)
P1–C2
186.84(15)
186.54(13)
186.55(13)
P4–M
242.01(7)
254.59(4)
253.06(5)
P4–P5
219.88(8)
219.08(7)
219.13(7)
P1–C2–P4
92.589(4)
92.54(5)
92.629(1)
P1–C2–P3
108.905(2)
108.757(62)
108.691(63)
P4–C2–P3
105.503(3)
105.785(63)
105.65(7)
C2–P1–C3
85.96(9)
85.92(8)
85.77(8)
C1–P3–P2
53.57(7)
53.56(6)
53.58(6)
P3–C1–P2
71.89(6)
71.75(5)
71.69(5)
P3–C1–P5
114.99(10)
114.90(9)
114.89(9)
P5–C1–P2
125.71(10)
125.95(9)
125.95(8)
C1–P2–P3
54.54(4)
54.69(3)
54.72(3)
C2–P1–C4
111.37(10)
111.52(8)
111.58(8)
P1–C4–P2
112.56(14)
112.35(12)
112.26(12)
P4–C3–P5
72.76(6)
72.57(5)
72.66(5)
P4–P5–C3
55.68(5)
55.61(4)
55.45(4)
C3–P4–P5
51.55(5)
51.82(4)
51.89(4)
109
Die Bindungsabstände von Molybdän zu den cis-ständigen Carbonylkohlenstoffatomen
betragen bei 53 ca. 205 pm. Die Bindung zum trans-ständigen ist auf 199 pm verkürzt.
Aufgrund des sterischen Anspruchs des P5-Homocuneans weichen sowohl die Mo–C≡OBindungen als auch die C–Mo–C-Bindungen um bis zu 4.8° von der Linearität ab. Die
maximale Abweichung ist hierbei um ca. 2° größer als bei 45a, jedoch um ca. 6° geringer als
bei 50a.
Die Trends bei den Bindungslängen M–P der [M(CO)5]-Komplexe bei P5-Deltacyclen, iso-P5Deltacyclen und P5-Homocunean stehen damit im Einklang mit den dort beobachteten
Abweichungen der idealen Oktaedergeometrie der Carbonylliganden. Diese beiden Effekte
sind auf die sterischen Anspruch der Koordinationsstellen zurückzuführen. Im P5-Deltacyclen
17 weisen die zwei Koordinationsstellen des Käfigs jeweils nur eine benachbarte tertButylgruppe auf. Im Gegensatz dazu sind beim iso-P5-Deltacyclen 49 zwei tert-Butylgruppen
direkt dem koordinativ aktiven Phosphoratom P1 benachbart, das als Brückenkopfform drei
Fünfringen angehört. Die Winkelsumme um P1 beträgt bei 50a 277.0°. Beim P5-Homocunean
51 sind ebenfalls zwei tert-Butylgruppen direkt dem Koordinationszentrum P4 benachbart. P4
ist ebenfalls ein Brückenkopfatom, gehört aber einem Drei- einem Vier- und einem Fünfring
an. Die dadurch stark verkleinerten Bindungswinkel um P4 verursachen eine ausgeprägt
konvexe Käfigoberfläche in diesem Bereich des Käfigs, die zu größeren Winkeln zwischen
der P–M- und den beiden flankierenden C–C(CH3)3-Bindungen führt. Das entlastet die
Wechselwirkung zwischen dem [M(CO)5]-Fragment und den beiden benachbarten tertButylgruppen. Die Winkelsumme um P4 beträgt bei 53 234.2°. Daraus lässt sich der sterische
Anspruch um die koordinierenden Phosphoratome in der Reihenfolge P5-Deltacyclen < P5Homocunean < iso-P5-Deltacyclen ableiten. Wie schon bei iso-P5-Deltacyclen 49a/b ergaben
Versuche 51 mit [(η6-C6H6)RuCl2]2 umzusetzen keinen beobachtbaren stabilen Komplex.
Bei den [M(CO)5]-Komplexen des iso-P5-Deltacyclens wurden zwei Epimere aufgrund der
unterschiedlichen Konfiguration des stereogenen Zentrums C4 gefunden. Im Gegensatz dazu
wird bei P5-Homocunean 51 und seinen [M(CO)5]-Komplexen stets nur eine Spezies
gefunden. Im Folgenden wird daher der unterschiedliche Raumbedarf rund um das stereogene
Zentrum C4 der beiden Strukturen 50a und 53 miteinander verglichen (Abb. 2.8.3). Bei 50a
und 53 stimmt die Orientierung von H1 und der tert-Butylgruppe an C4 in Bezug auf den
Diphosphiranring C2–P2–P3 überein. Die Abstände zwischen den quartären Kohlenstoffatomen der tert-Butylgruppen an C4 und C2 betragen bei 53 501 ppm und bei 50a 456 pm.
Bei 53 nähert sich zusätzlich die tert-Butylgruppe an C3 durch den Ringschluss zum
Diphosphiranring P4–P5–C3 an C4 an. Der Abstand zwischen den beiden quartären
110
Kohlenstoffatomen der tert-Butylgruppen an C3 und C4 beträgt bei 53 ebenfalls 501 pm. Die
Seite, auf der sich das Proton H1 befindet, ist davon noch stärker betroffen.
tBu an C4
tBu an C4
tBu an C3
H1
P5
P2
Mo(CO)5
an P1
P1 H1
P5
P2
Mo(CO)5
an P4
tBu an C1
tBu an C3
53
tBu an C1
50a
Abb. 2.8.3 Kalottenmodelle der Molekülstrukturen von 53 und 50a.
Der Abstand zwischen H1 und dem quartären Kohlenstoffatom der tert-Butylgruppe an C1
fällt zwar bei 53 mit 436 pm etwas größer aus als bei 50a (425 pm), der Abstand zwischen H1
und dem quartären Kohlenstoffatom der tert-Butylgruppe an C3 ist jedoch bei 53 bedeutend
kleiner. Er beträgt bei 50a 577 pm und bei 53 nur 338 pm. Die sterische Abstoßung, die eine
tert-Butylgruppe an der Stelle des Protons H1 durch die tert-Butylgruppe an C3 erfahren
würde, ist möglicherweise dafür verantwortlich, dass bei der Umlagerung zum P5Homocunean 51 nur ein Epimer gebildet wird. Im Gegensatz dazu ist die entsprechende tertButylgruppe an C3 beim iso-P5-Deltacyclen 49a so weit entfernt, dass ausreichend Platz für
die Inversion der Konfiguration von C4 vorhanden ist und sich somit das Epimer 49b bilden
kann.
2.8.3 Spektroskopische Charakterisierung der Chrom-, Molybdän- und Wolframpentacarbonyl-P5-homocuneankomplexe 52, 53 und 54
Die
31
P{1H}-NMR-Spektren der Chrom-, Molybdän- und Wolframpentacarbonyl-P5-
homocuneankomplexe 52, 53 und 54 unterscheiden sich erwartungsgemäß nur wenig, wenn
man von der chemischen Verschiebung des koordinierenden Phosphoratoms P4 absieht.
Tabelle 2.8.2 zeigt ausgewählte NMR-Daten von P5-Homocunean und seinen Chrom-,
111
Molybdän- und Wolframpentacarbonylkomplexen. Die Abb. 2.8.4 zeigt das
31
P{1H}-NMR-
Spektrum von 54.
Tabelle 2.8.2 Chemische Verschiebungen in ppm und ausgewählte Kopplungskonstanten in Hz in den 31P{1H}NMR-Spektren von 51, 52, 53 und 54.
1
P3
P2
P4
P5
52
89.6
28.4
6.9
18.8
-101.5
181.0
169.6
53
88.0
30.5
6.1
-10.3
-97.4
175.0
169.8
54
88.3
28.2
6.5
-35.6
-94.6
174.1
169.8
51
83.7
42.1
5.2
-41.4
-102.6
182.5
167.8
H1
tBu
P1
P1
C3
C2
P4
P5
(CO)5W
P2
JP4P5
1
P1
JP3P2
tBu
4
C
tBu
2
P3 P
P5
C1
tBu
54
P3
P4
X
ppm
100
50
0
X
-50
-100
Abb. 2.8.4 31P{1H}-NMR-Spektrum (122 MHz, CDCl3, 25°C) von Wolframpentacarbonyl-P5-homocunean 54.
Die Wolfram-Satelliten sind mit X gekennzeichnet.
P3 ist bei 52 – 54 bei ca. 28 ppm zu finden und damit um ca. 14 ppm hochfeldverschoben
gegenüber dem Käfig 51. Die durch die Bindung eines [M(CO)5]-Fragments an P4
112
hervorgerufene Koordinationsverschiebung beträgt für den Chromkomplex 52 +60.2 ppm. Sie
fällt bei Molybdän- und Wolframkomplex 53 und 54 mit +31.1 ppm bzw. -5.8 ppm wie zu
erwarten geringer aus. Bei 54 lassen sich auch Wolfram-Satelliten an P4 mit einer
Kopplungskonstante 1JWP4 von 225 Hz beobachten. Die chemische Verschiebung des P4
benachbarten P5 wird durch die Koordination ebenfalls leicht beeinflusst. So lässt sich eine
mit der Ordnungszahl zunehmende leichte Tieffeldverschiebung gegenüber dem freien
Liganden erkennen.
Das
31
P{1H}-NMR-Spektrum
von
Wolframpentacarbonyl-P5-homocunean
54
wurde
simuliert, um die aus den Spektren nicht unmittelbar ablesbaren Spin-Spin Kopplungsdaten zu
bestimmen.[41] Die Simulationsergebnisse werden in der Abb. 2.8.4 gezeigt und den
experimentellen Spektren gegenübergestellt. Die ermittelten Kopplungskonstanten sind in der
Tabelle 2.8.3 zusammengefasst.
P1
88.6
88.4
88.2
88.0
P3
29.2
29.8
28.4
28.0
P2
27.6
27.2
7.4
7.0
P4
-34.0
-34.8
-35.6
6.2
5.8
5.4
P5
XX
X
6.6
X
-36.4
-37.2
-93.8
-94.2
-94.6
-95.0
-95.4
Abb. 2.8.4 Simulierte (oben) und gemessene (unten) 31P{1H}-NMR-Signale (122 MHz, CDCl3, 25°C) von
Wolframpentacarbonyl-P5-homocunean 54. Die Wolfram-Satelliten sind mit X gekennzeichnet. Die Abweichung
(RMS) zwischen gemessenem und berechnetem Spektrum beträgt 0.010. In der Simulation wurde eine feste
Linienbreite von 2 Hz verwendet.
113
Tabelle 2.8.3 Simulierte 31P,31P-Kopplungskonstanten von Wolframpentacarbonyl-P5-homocunean 54 in Hz.
1
JP3P2
169.8
2
JP3P4
26.3
3
JP2P4
14.2
2
JP1P3
16.6
2
JP1P4
22.0
1
JP4P5
174.1
2
JP3P5
5.1
2
JP2P5
9.4
2
JP1P2
12.6
2
JP1P5
5.2
Auch die 1H-NMR-Spektren der Komplexe des 52 - 54 sind nahezu identisch. Vier Singuletts
für die Wasserstoffatome der tert-Butylgruppen sind bei δ = 1.1, 1.2, 1.3 und 1.4 ppm mit den
Integrationsverhältnissen 1 : 1 : 1 : 1 im Spektrum von 52 beobachtbar. Das C–H-Proton H1
findet sich bei 52 als Singulett bei 2.8 ppm. Ebenso sind die chemischen Verschiebungen der
Peaks bei den Komplexen 52 - 54 in den
13
C{1H}-NMR-Spektren erwartungsgemäß ähnlich
und unterscheiden sich nur um etwa 2 ppm. Bei 52 sind die C(CH3)3-Kohlenstoffatome der
tert-Butylgruppen als Multipletts bei 29.8, 30.0, 31.1 und 31.4 ppm zu sehen. Die quartären
C(CH3)3-Kohlenstoffatome der tert-Butylgruppen sind etwas weiter im Tieffeld bei 35.1,
36.4, 37.3 und 40.0 ppm zu finden. Die Zuordnung der Gerüstkohlenstoffatome von 52 erfolgt
analog 51. Bei 52 finden sich die Signale der Gerüstkohlenstoffatome bei δ(C1) = 46.3 ppm,
δ(C2) = 55.6 ppm, δ(C4) = 64.37 ppm und δ(C3) = 82.2 ppm. Die Kopplungskonstanten der
Gerüstkohlenstoffatome entsprechen etwa denen, die beim P5-Homocunean 51 gefunden
wurden. Leichte Abweichungen finden sich nur bei den beiden direkten Nachbarn von P4, an
dem die [M(CO)5]-Fragmente koordiniert sind.
Die Frequenzen der in den IR-Spektren identifizierten CO-Banden von 52 - 54 unterscheiden
sich kaum voneinander. Bei 53 sind die drei für [M(CO)5]-Komplexe erwarteten
Carbonylbanden bei 2073, 1950 und 1928 cm-1 zu beobachten. Die Beträge liegen nahe bei
denen, die für 45a-d und 50a/b gefunden wurden.
114
3. Zusammenfassung
Hauptziel dieser Arbeit war es, die Komplexchemie des asymmetrischen P5-Deltacyclenkäfigs
17 und seiner Umlagerungsprodukte zu untersuchen. P5-Deltacyclen 17 stand dabei als
Racemat zur Verfügung, dessen Synthese und einige wesentliche Eigenschaften in
Vorläuferprojekten aufgeklärt worden waren. Es fehlte jedoch noch die Aufklärung eines
Nebenprodukts der Synthese, welches sich aus dem Reaktionsgemisch nicht entfernen ließ.
Da es sich bislang der Isolierung in Substanz entzog, sollte seine Aufklärung mit den
Methoden der Molekülspektroskopie versucht werden. 17 und sein Nebenprodukt wurden
darum einer intensiven NMR-Studie unterzogen. Diese erbrachte eine Reihe von Belegen
dafür, dass es sich bei den beiden Verbindungen um die Epimere 17a und 17b handelt, bei
denen das stereogene Zentrum P1, welches das einzige Käfigproton H1 trägt, in einem
Inversionsgleichgewicht steht. 17a ist dabei die deutlich dominierende Komponente (Abb.
3.1). Belege für die Dynamik des Vorgangs konnten erbracht werden. Drei grundsätzliche
Wege für die wechselseitige Umwandlung zwischen 17a und 17b wurden diskutiert. Der
Austausch kann sauer oder basisch katalysiert oder durch direkte Inversion von P1 erfolgen.
Ein erfolgreicher H/D-Austausch von H1 mit D2O belegt die Bedeutung der beiden ionischen
Reaktionspfade. Eine DFT-Rechnung ergab eine Inversionsbarriere von +31 kcal mol-1 für
P1.
H1
tBu
P4
P1
tBu
P3
P5
H1
tBu
P4
P2
tBu
P1
tBu
2
P3 P
P5
tBu
tBu
17a
tBu
87 : 13
17b
Abb. 3.1 Inversionsgleichgewicht von 17a und 17b.
Im Gegensatz zu den freien Käfigverbindungen kristallisieren die entsprechenden
Übergangsmetallkomplexe der Käfige oft bereitwillig, wenn die Größe des MLn-Fragments
gut zur Größe des Käfigs passt. In früheren Arbeiten konnten dazu bereits einige [M(CO)5]Komplexe von 17 präpariert und strukturell charakterisiert werden. Die komplexen NMRSpektren blieben bei diesen Untersuchungen bislang jedoch unaufgeklärt. Das dynamische
115
Epimerengemisch 17a/b wurde mit den in situ generierten [M(CO)5THF]-Komplexen der
Metalle Chrom, Molybdän und Wolfram umgesetzt (Abb. 3.2).
Abb. 3.2 Koordination der Metallpentacarbonyle von Chrom, Molybdän und Wolfram am P5-Deltacyclen 17a/b.
Bildung der Koordinationsisomere a und c und deren Epimere b und d.
Wie für ein Epimerengemisch zu erwarten, wurden stabile [M(CO)5]-Komplexe von 17a und
17b gefunden, es treten jedoch die zwei Käfigpositionen P1 und P2 als Ligandfunktionen auf,
so dass in allen Fällen vier Komplexisomere beobachtet wurden. Auch die NMR-Spektren der
reinen Kristalle von 44a, 45a und 46a zeigen jeweils alle vier Komplexe, nachdem sie wieder
in Lösung gebracht wurden. Das belegt die Existenz von Gleichgewichten zwischen den
Epimeren und den Koordinationsisomeren der Komplexe.
Neben der Koordination von [M(CO)5]-Fragmenten an 17a/b wurde versucht auch Komplexe
mit redoxaktiven Metallen darzustellen. Eine Umsetzung des Epimerengemischs 17a/b mit
dem Benzoldichlororuthenium(II)-Dimer erwies sich als erfolgreich (Abb. 3.3). Das Produkt
47 konnte in bis zu 93 % Ausbeute isoliert werden. Es wurde hierbei im Gegensatz zu den
[M(CO)5]-Komplexen nur eine einzige Verbindung gebildet, bei der das Ruthenium an P1
koordiniert ist. Eine Metallkoordination an P2 findet hier aufgrund des höheren sterischen
Anspruchs
des
[(η6-C6H6)RuCl2]-Fragments
nicht
statt.
Außerdem
wird
bei
der
Metallkoordination ebenfalls aus sterischen Gründen selektiv nur der Komplex 47 gebildet,
bei dem das Käfigproton H1 wie in 17b trans-ständig zu P5 steht. Damit selektiert die
Komplexierungsreaktion das für den freien Liganden benachteiligte Epimer 17b aus dem
vorgelagerten Gleichgewicht.
116
Cl
H
H
tBu
P
tBu
P
P
P
P
tBu
+ 0.5
Ru
P
tBu
Cl
Cl
Ru
Ru
Cl
Cl
P
CH2Cl2
P
P
Cl
P
tBu
tBu
tBu
tBu
47 93%
17a/b
6
Abb. 3.3 Darstellung von [(η -Benzol)dichloro(P5-Deltacyclen)ruthenium(II)] 47.
In
Zusammenarbeit
mit
C.
Höhn
wurde
der
Rutheniumkomplex
47
auch
in
enantiomerenreiner Form synthetisiert. Der Erhalt der optischen Aktivität der beiden
Enantiomere 17’ und 17’’ bei der Komplexierung konnte anhand von CD-Kurven der
Verbindungen 47’ und 47’’ gezeigt werden, die ebenfalls ein separiertes Enantiomerenpaar
bilden. Mit 47 ist die prinzipielle Darstellbarkeit enantiomerenreiner Metallkomplexe mit dem
chiralen, sterisch anspruchsvollen P5-Deltacyclenliganden aufgezeigt worden.
Neben Ruthenium wurde auch Rhodium als redoxaktives Metall mit dem Epimerengemisch
des P5-Deltacyclens 17a/b umgesetzt. Dafür wurde das Cyclooctadienrhodium(I)chloridDimer verwendet. Statt eines erwarteten monomeren Rh(I)-Käfigkomplexes entsteht ein
Rh(III)-Zweikernkomplex 48. Das Metall hat sich oxidativ unter Öffnung der P–P-Bindung
des Dreirings von 17 und der Ausbildung eines Rh(III)-Komplexes an den Käfig angelagert.
Die beiden Phosphoratome P2 und P3, die den Diphosphiranring des freien Käfigs 17 bilden,
koordinieren im Komplex 48 jeweils ein Rhodium(III)-Ion. Das Phosphoratom P1 koordiniert
an beide Rhodiumzentren und verbrückt damit den Zweikernkomplex. Um dies zu
ermöglichen, ist das ursprünglich an P1 gebundene Käfigproton H1 an das Phosphoratom P3
des Komplexes gewandert. Einschließlich der Bindung jeweils eines Chloratoms ergibt sich
für beide Rhodiumatome eine fünffache Koordination. Die Molekülstruktur des
Komplexdimers 48 im Kristall ist in der Abb. 3.4 gezeigt. Es enthält die geöffnete Version
beider Enantiomere des P5-Deltacyclens 17 als Liganden. 48 weist ein kristallographisches
Inversionszentrum in der Mitte der Ebene Rh1–P1–Rh1A–P1A auf. Es bildet damit eine
meso-Verbindung in den NMR-Spektren von 48. Es zeigen sich allerdings zwei Sätze
unterschiedlicher Intensität mit jeweils fünf Signalen, die beide mit der im Kristall
beobachteten Spezies vereinbar wären. Die beiden in Lösung vorliegenden Versionen 48a und
48b von 48 stehen in einem chemischen Gleichgewicht, das vollständig zu 48a verschiebbar
ist. Eine der beiden Komponenten, 48a oder 48b, wird als meso-Verbindung 48 aufgefasst.
Eine klare Zuordnung gelang jedoch noch nicht, weil die als zweite Komponente des
117
Gemisches
betrachtete
racemische
Form
zweier
Komplexdimere
der
jeweiligen
Ligandenenantiomere 17’ und 17’’ phänotypisch gleiche NMR-Spektren generieren würden.
Die beiden Dimere hätten demnach die Form (17’)2Rh2Cl2 und (17’’)2Rh2Cl2 Diese sollten
C2-symmetrisch sein und wären NMR-spektroskopisch identisch. Zwischen Zentro- und C2Symmetrie kann NMR-spektroskopisch bei der gegebenen Auflösung der Spektren nicht
unterschieden werden.
Cl1
P2
C4A
C1
P3
Rh1
C2A
P1A
C3
P5
C2
P1
P4A
P5A
Rh1A
C3A
P3A
P4
C1A
C4
P2A
Cl1A
Abb. 3.4 Molekülstruktur des Rhodiumkäfig-Zweikernkomplexes 48 im Kristall.
Neben der Metallkoordination von 17a/b wurden zwei Käfigumlagerungen des P5Deltacyclens und die Koordinationseigenschaften der auf diesem Weg neu zugänglichen P–CKäfigverbindungen untersucht. Die erste Umlagerung des P5-Deltacyclens 17a/b durch nButhyllitium zum iso-P5-Deltacyclen 49 wurde bereits von S. Huguet-Torrell gefunden. Im
iso-P5-Deltacyclen 49 hat das sekundäre Phosphanatom P1 mit seiner benachbarten Gruppe
C4-tert-Butyl den Platz getauscht. Dabei wandert H1 von P1 nach C4 (Abb. 3.5). Anhand von
DFT-Rechnungen zur Umlagerung wurden zwei Reaktionsmechanismen ergebnisoffen
diskutiert. In dieser Arbeit konnte gezeigt werden, dass auch das iso-P5-Deltacyclen aus
einem Epimerengemisch 49a/b besteht. Die Epimere ergeben sich aus der Konfiguration von
C4 bei dem H1 und die tert-Butylgruppe ihre Plätze tauschen können. In den NMR-Spektren
liegen daher wieder zwei Signalsätze im Verhältnis von ca. 0.15 : 1 vor. Mit der
Epimerenmischung wurden [M(CO)5]-Komplexe dargestellt (M = Cr, Mo, W). Die
Koordination erfolgt für beide Epimere ausschließlich an P1. Es ergeben sich daher jeweils
118
zwei Komplexe pro Metall, deren relatives Verhältnis zueinander jedoch nicht dem des
Edukts 49a/b entspricht. Das belegt wieder die Existenz eines Gleichgewichts zwischen den
Epimeren. Eine Koordination an andere Phosphoratome durch [M(CO)5]-Fragmente ist
vermutlich aufgrund des sterischen Anspruchs der tert-Butylgruppen nicht möglich. Im
Gegensatz zu 17a/b weisen die beiden potentiellen Ligandfunktionen P1 und P2 von 49a/b
jeweils zwei direkt benachbarte tert-Butylgruppen auf. Für P1 reicht die Lücke zwischen den
beiden benachbarten tert-Butylgruppen von 49a/b gerade noch zur Bindung von [M(CO)5]Fragmenten, [(η6-C6H6)RuCl2] kann nicht koordiniert werden. Für P2 stehen die beiden tertButylgruppen offensichtlich auch zu eng beieinander, um koordinationschemisch überhaupt
aktiv zu werden.
C4
P4
P
H
H
tBu
P
tBu
1
2
P3 P
5
P1
n-BuLi / THF
tBu
P4
-78°C - RT
SiO2 / 5% H2O
P
5
C
tBu
2
P3 P
P1
+
P4
tBu
P5
tBu
tBu
tBu
17a/b
49a
49b
H
tBu
H
P
tBu
P
THF
P P
P
tBu
42: M = Cr
50: M = Mo
43: M = W
tBu
(OC)5M
P
[M(CO)5THF]
4
C
tBu
2
P3 P
tBu
(OC)5M
H
tBu
tBu
4
tBu
+
P
P P
P
tBu
tBu
tBu
42a, 43a und 50a
42b, 43b und 50b
Abb. 3.5 Umlagerung zu den beiden Epimeren des iso-P5-Deltacyclens 49a und 49b und Umsetzung zu den
[M(CO)5]-Komplexen 42a/b, 43a/b und 50a/b.
Neben der Umlagerung zum iso-P5-Deltacyclen 49a/b wurde eine weitere Umlagerung des
P5-Deltacyclens 17a/b entdeckt. Wird der Lösung von 17a/b in THF ein Äquivalent
Benzophenon beigemischt, ergibt sich nach der Zugabe von n-Buthyllithium das P5Homocunean 51. Zusätzlich zu dem schon bei iso-P5-Deltacyclen beobachteten Platzwechsel
von P1 und der Gruppe C4-tert-Butyl ergibt sich 51 durch eine Valenzisomerisierung bei der
die P=C-Doppelbindung von 17a/b bzw. 49a/b aufgehoben und der Fünfring, der diese
Doppelbindung enthält, in eine Kombination eines Vierrings mit einem ankondensierten
Dreiring umgewandelt wird (Abb. 3.6). Es konnte gezeigt werden, dass die Synthese von 51
119
auch aus 49a/b möglich ist. Fasst man 49 als Intermediat der Bildung von 51 auf, lässt sich
ein Reaktionsmechanismus postulieren, der in Abb. 3.6 formuliert ist. P5-Homocunean 51
entsteht im Gegensatz zu 49a/b nur als einheitliche Verbindung. Epimere oder andere Isomere
konnten nicht beobachtet werden, was auf die Raumfüllung der tert-Butylgruppen
zurückgeführt wird. Von 51 wurden ebenfalls [M(CO)5]-Komplexe der Chromtriade
dargestellt. Die [M(CO)5]-Fragmente koordinieren hier ausschließlich an P4, einem
Phosphoratom des neu gebildeten Diphosphiranrings. Auch hier wurde jeweils nur ein
Komplex erhalten. Eine Epimerisierung wurde nicht beobachtet.
Abb. 3.6 Darstellung von P5-Homocunean 51 und den [M(CO)5]-Komplexen 52, 53 und 54.
Anhand der Molekülstruktur der [Mo(CO)5]-Komplexe mit den Käfigen 17, 49 und 51 ließ
sich der sterische Anspruch der Käfigliganden im Bereich der jeweiligen koordinierenden
Phosphoratome ableiten. Der Raumbedarf der Liganden steigt in der Reihenfolge P5Deltacyclen < P5-Homocunean < iso-P5-Deltacyclen. Dabei weisen die Ligandfunktionen von
49a/b und 51 jeweils zwei tert-Butylgruppen in der direkten Nachbarschaft des bindenden
Phosphoratoms auf, während es bei 17a/b nur eine tert-Butylgruppe als Nachbar der beiden
koordinationschemisch aktiven Phosphoratome gibt. Bei 51 ist der sterische Druck der
Substituenten geringer als bei 49a/b, weil das bindende P4 zwei kleinen Ringen mit
entsprechend kleinen Bindungswinkeln angehört. Zusammengefasst ermöglichen diese
Effekte die Käfigliganden bei Kombination mit geeigneten [MLn]-Fragmenten als selektive
Liganden mit definierter Stereochemie zu wirken. Das gilt insbesondere für den
[(η6-C6H6)Ru(II)]-Komplex 47, der als einheitliche Substanz aus einem Epimerengemisch
erhalten werden kann und der im Rahmen dieser Arbeit enantiomerenrein in beiden optischen
Varianten präpariert wurde. Gleiches gilt für die [M(CO)5]-Komplexe von 51, die als
stereochemisch einheitliche Liganden in dieser Studie racemisch dargestellt wurden. Auf
Basis dieser Ergebnisse konnte C. Höhn den [W(CO)5]-Komplex 54 wieder in optisch aktiver
Form synthetisieren und strukturanalytisch charakterisieren.
120
4. Experimenteller Teil
4.1 Materialien und Methoden
Alle Reaktionen wurden unter Stickstoff- bzw. Argonatmosphäre in ausgeheizten, evakuierten
und mit dem Inertgas gefluteten Glasapparaturen mit der Schlenk-Technik durchgeführt. Die
verwendeten Lösungsmittel wurden nach Literaturvorschrift[82] unter Stickstoffatmosphäre
absolutiert, getrocknet und unmittelbar vor Gebrauch frisch destilliert. Alle deuterierten
Lösungsmittel bis auf D2O wurden nach gängigen Methoden getrocknet, entgast und über
Molekularsieb (4 Å) aufbewahrt. Kommerziell verfügbare Edukte wurden vor der Synthese
durch Destillation oder Kristallisation gereinigt. Flüssige Edukte wurden vor der Verwendung
entgast und mit Stickstoff gesättigt.
Folgende Substanzen wurden nach Literaturvorschriften synthetisiert:
Piperidindichlorophosphan,[83]
Tris(trimethylsilyl)phosphan[84]
(der
dafür
notwendige
Lithium-Sand wurde aus Lithium Granulat gewonnen. Hierzu wurde das Granulat in einer
Stahlapparatur unter Argonatmosphäre in entgastem Parafinöl auf 220 °C erhitzt, mittels eines
Ultra-Turrax-Rührers ca. 30 Sekunden zerkleinert, im Eisbad abgeschreckt, abfiltriert und mit
n-Hexan
gewaschen),
(2,2-Dimethyl-1-trimethylsiloxy-1-propyliden)trimethylsilyl-
phosphan,[85] tert-Butylphosphaalkin,[85] Natrium-[3,5-di(tert-butyl)-1,2,4-triphosphacyclopentadienid],[18]
1-Triphenylstannyl-3,5-di(tert-butyl)-1,2,4-triphosphacyclopentadien,[18]
Triphenylstannyl-P5-deltacyclen.[18]
Standard-1H-,
13
C- und
31
P-NMR-Spektren, einschließlich P,H- und P,P-COSY-Spektren:
Bruker AVANCE DPX300 NB, Bruker AVANCE DRX400 WB und JEOL JNM-LA400.
Die chemischen Verschiebungen werden in den 1H- und
13
C-NMR-Spektren in ppm relativ
zum verwendeten Lösungsmittel angegeben und auf δ(TMS) = 0 ppm umgerechnet. In den
31
P-NMR-Spektren beziehen sich die chemische Verschiebungen auf 85 % H3PO4 (δ = 0) als
externen Standart. Die 13C-NMR-Spektren wurden 1H-breitbandentkoppelt aufgenommen. Es
wurden nur Beträge von Kopplungskonstanten bestimmt und angegeben.
P,P-EXSY- und
31
P-DOSY-Messungen wurden an einem JEOL Alpha500 Spektrometer von
Prof. Dr. Walter Bauer aufgenommen (1H: 500 MHz; 31P: 202 MHz).
121
Für die eindimensionalen-, COSY- und EXSY-Spektren wurde ein 5 mm BreitbandProbenkopf verwendet. Für die DOSY-Spektren wurde ein 5 mm Invers-Probenkopf mit aktiv
abgeschirmten Gradientenspulen benutzt. Die Parameter für die einzelnen Spektren: P,PEXSY: Standard phasensensitive NOESY Sequenz. Um off-resonance Effekte zu vermeiden,
wurden mehrere Spektren mit begrenzten spektralen Breiten zwischen 9 und 20 kHz
aufgenommen. Typische Parameter: 512 Datenpunkte bei f2, zero filled bis 1024, 128
Datenpunkte bei f1, zero filled bis 256, 16 bis 64 scans pro t1-Inkrement, RelaxationszeitIntervall 2.0 s, Mischzeit 600 ms. 31P-DOSY Diffusionsmessungen: Um off-resonance Effekte
zu vermeiden, wurden mehrere Spektrenscharen mit begrenztem spektralen Aufnahmebereich
unterschiedlicher Spektrenbreite aufgenommen. Es wurde die BPPLED-Pulssequenz
verwendet (Äquivalent bei Bruker: ledbpgs2s). Eine Spektrenschar von 16 Spektren mit
Gradientenstärken bis zu 35 G/cm, Diffusions delay 80 ms, 2048 scans pro GradientenInkrement, Relaxationszeit-Intervall 1.5 s wurde aufgenommen. Die Auswertung der Spektren
erfolgte mit der JEOL T1/T2 Routine.
Massenspektrometrie: Jeol The MStation, JMS 700, UHR-TOF Bruker Daltonik maXis.
Zur Ionenerzeugung wurde am Jeol The MStation, JMS 700-Gerät die FD-Methode
verwendet. Die Werte in % beziehen sich auf den höchsten auftretenden Massenpeak (relative
Intensität). Zur Ionenerzeugung wurde an dem UHR-TOF Bruker Daltonik maXisMassenspektrometer die ESI-Methode verwendet. Die Massenspektren an diesem Gerät
wurden in der Gruppe Prof. Dr. Ivana Ivanović-Burmazović aufgenommen. Die Detektion
fand im positiven Ionenmodus statt. Die Quellenspannung beträgt 3.4 kV. Das Trocknungsgas
(N2)
zum
Entfernen
des
Lösungsmittels
wurde
auf
180
°C
geheizt.
Die
Durchflußgeschwindigkeit wurde auf 500 µ L h-1 eingestellt. Das Gerät wurde vor jedem
Experiment durch die direkte Einspritzung der Agilent ESI-TOF Tuning Mischung (niedrige
Konzentration) kalibriert. Dadurch kann ein m/z Bereich von einfach geladenen Peaks bis zu
2700 Da in beiden Ionenmodi erreicht werden.
Elementaranalysen: Euro Vector Euro EA 3000.
IR-Spektren: ATI Mattson 60 AR Infinity FT-IR.
CD-Spektren: JASCO J-815 Spektropolarimeter.
122
4.2 Beschreibung der Versuche
4.2.1 Synthese und Charakterisierung von P5-Deltacyclen 17a/b
Die Synthese von P5-Deltacyclen 17 als Racemat erfolgte nach Literaturvorschrift.[20]
Triphenylstannyl-P5-deltacyclen 16 (0.568 g, 0.727 mmol) wurde durch Hydrolyse auf einer
Chromatographiesäule (SiO2/5 % H2O) mit n-Hexan in eine Mischung aus den Epimeren 17a
und 17b (0.305 g, 0.705 mmol, 97.0 %) überführt, die sich nicht trennen ließen.
Spektroskopisch ergibt sich ein Gleichgewicht mit einem konstanten Mengenverhältnis von
87 : 13 für 17a und 17b.
tBu
P4
3
tBu
C
H1
C4
C2
P5
tBu
P1
tBu
2
P3 P
P4
3
C1
tBu
tBu
C
H1
C4
C2
P5
P1
tBu
2
P3 P
C1
tBu
17b
17a
17a: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.02 (s, 9 H, C(CH3)3), 1.33 (s, 9 H, C(CH3)3),
1.45 (s, 9 H, C(CH3)3), 1.53 (s, 9 H, C(CH3)3), 4.91 (dd, 1 H, 1JH1P1 = 179.1 Hz, 2JH1P2 = 4.7
Hz, 1 H, H1) ppm. 31P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -120.20 (dd,1JP3P2 = 158.2
Hz, 2JP3P5 = 7.3 Hz, P3), -112.50 (ddd, 1JP2P1 = 238.4 Hz, 1JP2P3 = 158.2 Hz, 2JP2P5 = 7.5 Hz,
P2), -51.77 (ddd, 1JP1P2 = 238.4 Hz, 2JP1P5 = 9.1 Hz, 2JP1P4 = 6.7 Hz, P1), 105.03 (m, 2JP5P4 =
12.4 Hz, 2JP5P1 = 9.1 Hz, 2JP5P2 = 7.5 Hz, 2JP5P3 = 7.3 Hz, P5), 339.60 (dd, 2JP4P5 = 12.4 Hz,
3
JP4P1 = 6.7 Hz, P4) ppm.
17b: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.11 (s, 9 H, C(CH3)3), 1.24 (s, 9 H, C(CH3)3),
1.50 (s, 9 H, C(CH3)3), 1.68 (s, 9 H, C(CH3)3), 4.14 (ddd, 1 H, 1JH1P1 = 197.7 Hz, 3JH1P5 = 36.6
Hz, 2JH1P2 = 4.4 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -107.93
(m, 1JP3P2 = 152.2 Hz, 2JP3P1 = 5.9 Hz, 2JP3P5 = 6.4 Hz, P3), -107.11 (m, 1JP2P1 = 212.0 Hz,
1
JP2P3 = 152.2 Hz, 2JP2P5 = 9.0 Hz, P2), -18.72 (m, 1JP1P2 = 212.0 Hz, 2JP1P5 = 128.3 Hz, 2JP1P3
= 5.9 Hz, 3JP1P4 = 4.2 Hz, P1), 88.31 (dq, 2JP5P1 = 128.3 Hz, 2JP5P4 = 11.2 Hz, 2JP5P2 = 9.0 Hz,
2
JP5P3 = 6.4 Hz, P5), 366.05 (d, 2JP4P5 = 11.2 Hz, 3JP4P1 = 4.2 Hz, P4) ppm.
123
17a/b:
13
C{1H}-NMR (67.8 MHz, CDCl3, 25°C): δ = 33.15 (m, C(CH3)3), 33.49 (m,
C(CH3)3), 35.09 (m, C(CH3)3), 35.64 (m, C(CH3)3), 36.42 (m, C(CH3)3), 38.55 (dd, 2JCP =
15.9 Hz, 2JCP = 12.6 Hz, C(CH3)3), 40.02 (dd, 2JCP = 16.0 Hz, 2JCP = 12.2 Hz, C(CH3)3), 41.50
(ddd, 2JCP = 16.7 Hz, 2JCP = 14.5 Hz, 2JCP = 3.3 Hz, C(CH3)3), 69.06 (m, C1), 83.56 (m, C2
oder C4), 90.41 (m, C2 oder C4), 225.64 (m, C=P) ppm.
MS (ESI-ToF, CHCl3/MeOH): m/z (%) 433.17 (100) [MH]+, (FD, n-Hexan): m/z (%) 432
(100) [M]+, 864 (0.5) [M2]+.
EA: C20H37P5 (432.38): ber. C 55.56, H 8.62; gef. C 55.99, H 8.62.[86]
4.2.2 Synthese der Chrom- Molybdän- und Wolframpentacarbonyl-P5-deltacyclenkomplexe 44a-d, 45a-d und 46a-d
Exemplarisch für die Molybdänkomplexe 43a-d
Eine Suspension aus [Mo(CO)6] (0.095 g, 0.360 mmol) in 50 mL frisch destilliertem THF
wurde mit einer Quecksilberdampflampe 1 h belichtet. Die resultierende gelbe Lösung von
[Mo(CO)5THF] in THF wurde in eine -40 °C kalte Lösung aus dem Epimerengemisch 17a/b
des P5-Deltacyclens (0.078 g, 0.180 mmol) in 50 mL THF gegeben und 1 h bei dieser
Temperatur gerührt. Danach wurde das Kältebad entfernt und die Reaktionsmischung weitere
6 h bei Raumtemperatur gerührt. Das Rohprodukt wurde durch Säulenchromatographie (SiO2,
n-Hexan) gereinigt und die flüchtigen Bestandteile im Vakuum abgezogen. Es entstanden
jeweils Mischungen aus vier isomeren [Mo(CO)5(P5C20H37)]-Komplexen (0.094 g, 0.140
mmol, 78.4 %) 45a-d als gelbes Öl. Nimmt man diese in n-Hexan auf, kann ein Teil der
Produkte kristallin erhalten werden, die sich als Einkristalle der Komponente 45a erwiesen.
Lösungen der Einkristalle des Komplexes 45a liefern wieder die Spektren des Gemisches der
vier Verbindungen 45a-d.
Die Komplexe 44a-d und 46a-d wurden wie oben beschrieben synthetisiert mit folgenden
Ansatzgrößen und Ausbeuten:
[Cr(CO)6] (0.097 g, 0.441 mmol) und 17a/b (0.095 g, 0.220 mmol) ergaben die
[Cr(CO)5(P5C20H37)]-Komplexe 44a-d (0.095 g, 0.152 mmol, 69.3 %).
[W(CO)6] (0.154 g, 0.437 mmol) und 17a/b (0.126 g, 0.291 mmol) ergaben die
[W(CO)5(P5C20H37)]-Komplexe 46a-d (0.158 g, 0.209 mmol, 71.7 %).
124
4.2.2.1 Spektroskopische und analytische Daten der Chrompentacarbonyl-P5deltacyclenkomplexe 44a-d
44a: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.19 (s, 9 H, C(CH3)3), 1.39 (s, 9 H, C(CH3)3),
1.54 (s, 9 H, C(CH3)3), 1.65 (s, 9 H, C(CH3)3), 5.29 (ddd, 1JH1P1 = 175.8 Hz, 2JH1P2 = 5.3 Hz,
3
JH1P5 = 5.2 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -148.04 (dd,
1
JP3P2 = 186.7 Hz, P3), -56.87 (dddd, 1JP2P1 = 234.4 Hz, 1JP2P3 = 186.7 Hz, 2JP2P5 = 26.9 Hz,
P2), -41.95 (dt, 1JP1P2 = 234.4 Hz, P1), 108.19 (m, 2JP5P2 = 26.9 Hz, P5), 343.63 (s, P4) ppm.
31
P-NMR (121.5 MHz, CDCl3, 25°C): δ = -149.45 (dd, 1JP3P2 = 186.7 Hz, P3), -58.07 (ddddd,
1
JP2P1 = 234.4 Hz, 1JP2P3 = 186.7 Hz, 2JP2P5 = 26.9 Hz, 2JP2H = 5.3 Hz, P2), -43.26 (dddd, 1JP1P2
= 234.4 Hz, 1JP1H = 175.8 Hz, P1), 106.84 (m, 2JP5P2 = 26.9 Hz, 3JP5H = 5.2 Hz, P5) ppm.
44b: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.21 (s, 9 H, C(CH3)3), 1.25 (s, 9 H, C(CH3)3),
1.54 (s, 9 H, C(CH3)3), 1.66 (s, 9 H, C(CH3)3), 4.41 (dd, 1JH1P1 = 195.8 Hz, 3JH1P5 = 39.0 Hz, 1
H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -131.80 (dd, 1JP3P2 = 190.3 Hz,
P3), -51.88 (ddt, 1JP2P1 = 214.1 Hz, 1JP2P3 = 190.3 Hz, P2), -11.72 (dt, 1JP1P2 = 214.1 Hz, 2JP1P5
= 121.4 Hz, P1), 90.92 (dm, 2JP5P1 = 121.4 Hz, P5), 368.3 (s, P4) ppm. 31P-NMR (121.5 MHz,
125
CDCl3, 25°C): δ = -133.21 (dd, 1JP3P1 = 190.3 Hz, P3), -53.09 (ddt, 1JP2P1 = 214.1 Hz, 1JP2P3 =
190.3 Hz, P2), -13.05 (dddd, 1JP1P2 = 214.1 Hz, 2JP1P5 = 121.4 Hz, 1JP1H = 195.7 Hz, P1),
89.58 (m, 2JP5P1 = 121.4 Hz, 3JP5H = 39.0 Hz ,P5) ppm.
44c: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.11 (s, 9 H, C(CH3)3), 1.36 (s, 9 H, C(CH3)3),
1.52 (s, 9 H, C(CH3)3), 1.66 (s, 9 H, C(CH3)3), 6.28 (d, 1JH1P1 = 292.9 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -118.77 (dd, 1JP2P1 = 233.5 Hz, 1JP2P3 = 158.6
Hz, P2), -110.36 (dd, 1JP3P2 = 158.6 Hz, P3), -10.25 (ddd, 1JP1P2 = 233.5 Hz, 2JP1P5 = 41.9 Hz,
P1), 114.92 (dt, 2JP5P1 = 41.9 Hz, P5), 351.93 (t, P4) ppm.
31
P-NMR (121.5 MHz, CDCl3,
25°C): δ = -120.04 (dd, 1JP2P1 = 233.5 Hz, 1JP2P3 = 158.6 Hz, P2), -111.69 (d, 1JP3P2 = 158.6
Hz, P3), -11.52 (dddd, 1JP1P2 = 233.5 Hz, 2JP1P5 = 41.9 Hz, 1JP1H = 293.5 Hz, P1), 113.58 (t
2
JP5P1 = 41.9 Hz, P5) ppm.
44d: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.15 (s, 9 H, C(CH3)3), 1.48 (s, 9 H, C(CH3)3),
1.52 (s, 9 H, C(CH3)3), 1.63 (s, 9 H, C(CH3)3), 4.98 (ddd, 1JH1P1 = 319.4 Hz, 2JH1P2 = 10.1 Hz,
3
JH1P5 = 26.7 Hz, 1 H, H1) ppm. 31P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -120.40 (dt,
1
JP3P2 = 152.2 Hz, P3), -109.16 (ddd, 1JP2P1 = 219.4 Hz, 1JP2P3 = 152.2 Hz, P2), 13.09 (dd,
1
JP1P2 = 219.4 Hz, 2JP1P5 = 106.1 Hz, P1), 82.95 (dq, 2JP5P1 = 106.1 Hz, P5), 357.06 (d, P4)
ppm.
31
P-NMR (121.5 MHz, CDCl3, 25°C): δ = -121.75 (d, 1JP3P1 = 152.2 Hz, P3), -110.37
(dddd, 1JP2P1 = 219.4 Hz, 1JP2P3 = 152.2 Hz, 2JP2H1 = 10.1 Hz, P2), 11.78 (ddd, 1JP1P2 = 219.4
Hz, 2JP1P5 = 106.1 Hz, 1JP1H1 = 319.1 Hz, P1), 81.58 (dm, 2JP5P1 = 106.1 Hz, 3JP5H1 = 26.7 Hz,
P5) ppm.
44a-d:
13
C{1H}-NMR (67.8 MHz, CDCl3, 25°C): δ = 32.86 (m, C(CH3)3), 33.12 (m,
C(CH3)3), 33.69 (m, C(CH3)3), 34.52 (m, C(CH3)3), 35.43 (m, C(CH3)3), 36.11 (m, C(CH3)3),
36.46 (m, C(CH3)3), 37.82 (m, C(CH3)3), 38.11 (m, C(CH3)3), 38.65 (m, C(CH3)3), 39.29 (m,
C(CH3)3), 40.12 (m, C(CH3)3), 41.47 (m, C(CH3)3), 41.83 (m, C(CH3)3), 215.11 (dd, 2JCP2 =
11.3 Hz, 3JCP = 4.9 Hz, cis-CO 44a), 215.47 (dd, 2JCP1 = 9.3 Hz, 3JCP = 6.2 Hz, cis-CO 44c),
215.65 (dd, 2JCP1 = 9.7 Hz, 3JCP = 6.7 Hz, cis-CO 44d), 220.59 (d, 2JCP2 = 3.8 Hz, trans-CO
44a), 221.6 (d, 2JCP1 = 7.1 Hz, trans-CO 44c), 221.69 (d, 2JCP1 = 5.7 Hz, trans-CO 44d) ppm.
IR ν/cm-1 (KBr): 2955m (νC–H), 2900sh (νC–H), 2864w (νC–H), 2742w (νC–H), 2064s
(CO), 1941vs (CO), 1924vs (CO), 1392m (tBu), 1361m (tBu).
MS (FD, n-Hexan): m/z (%) = 625 (100) [M]+.[87]
EA: C25H37O5P5Cr (624.43): ber. C 48.09, H 5.97; gef. C 48.39, H 5.79.
126
4.2.2.2 Spektroskopische und analytische Daten der Molybdänpentacarbonyl-P5deltacyclenkomplexe 45a-d
45a: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.21 (s, 9 H, C(CH3)3), 1.39 (s, 9H, C(CH3)3),
1.54 (s, 9 H, C(CH3)3), 1.65 (s, 9 H, C(CH3)3), 5.26 (ddd 1JH1P1 = 175.8 Hz, 2JH1P2 = 5.5 Hz,
3
JH1P5 = 5.8 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -140.45 (dd,
1
JP3P2 = 182.2 Hz, P3), -84.57 (dddd, 1JP2P1 = 225.7 Hz, 1JP2P3 = 182.2 Hz, 2JP2P5 = 25.6 Hz,
P2), -42.40 (dt, 1JP1P2 = 225.7 Hz, P1), 106.96 (m, 2JP5P2 = 25.6 Hz, P5), 341.56 (m, P4) ppm.
31
P-NMR (121.5 MHz, CDCl3, 25°C): δ = -141.85 (dd, 1JP3P2 = 182.2 Hz, P3), -85.78 (ddddd,
1
JP2P1 = 225.7 Hz, 1JP2P3 = 182.2 Hz, 2JP2P5 = 25.6 Hz, 2JP2H1 = 5.5 Hz, P2), -43.72 (dddd,
1
JP1P2 = 225.7 Hz, 1JP1H1 = 175.8 Hz, P1), 105.60 (m, P5) ppm.
RSA im Anhang.
45b: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.17 (d, 9 H, C(CH3)3), 1.36 (s, 9H, C(CH3)3),
1.53 (s, 9 H, C(CH3)3), 1.68 (d, 9 H, C(CH3)3), 4.31 (dd, 1JH1P1 = 196.4 Hz, 3JH1P5 = 39.5 Hz,
1 H, H1) ppm. 31P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -125.10 (dd, 1JP3P2 = 184.5 Hz,
P3), -79.96 (ddt, 1JP2P1 = 205.0 Hz, 1JP2P3 = 184.5 Hz, P2), -11.04 (dd, 1JP1P2 = 205.0 Hz,
2
JP1P5 = 121.4 Hz, P1), 89.81 (d, 2JP5P1 = 121.4 Hz, P5), 366.65 (m, P4) ppm. 31P-NMR (121.5
MHz, CDCl3, 25°C): δ = -126.51 (dd, 1JP3P2 = 184.5 Hz, P3), -81.12 (ddt, 1JP2P1 = 205.0 Hz,
1
JP2P3 = 184.5 Hz, P2), -12.34 (ddd, 1JP1P2 = 205.0 Hz, 2JP1P5 = 121.4 Hz, 1JP1H1 = 196.4 Hz,
P1), 88.47 (dddd, 2JP5P1 = 121.4 Hz, 3JP5H1 = 39.5 Hz, P5) ppm.
45c: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.12 (d, 9 H, C(CH3)3), 1.41 (s, 9H, C(CH3)3),
1.53 (s, 9 H, C(CH3)3), 1.68 (d, 9 H, C(CH3)3), 6.38 (ddd 1JH1P1 = 288.2 Hz, 2JH1P2 = 6.0 Hz,
3
JH1P3 = 3.6 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -118.94 (dd,
1
JP2P1 = 223.6 Hz, 1JP2P3 = 158.4 Hz, P2), -110.20 (dd, 1JP3P2 = 158.4 Hz, 2JP3P5 = 9.7 Hz, P3),
-34.77 (ddd, 1JP1P2 = 223.6 Hz, 2JP1P5 = 38.3 Hz, 2JP1P4 = 10.2 Hz, P1), 113.39 (ddd, 2JP5P1 =
38.3 Hz, 2JP5P4 = 10.3 Hz, 2JP5P3 = 9.7 Hz, P5), 349.09 (dd, 2JP4P5 = 10.3 Hz, 2JP4P1 = 10.2 Hz,
P4) ppm. 31P-NMR (121.5 MHz, CDCl3, 25°C): δ = -118.94 (dd, 1JP2P1 = 223.6 Hz, 1JP2P3 =
158.4 Hz, P2), -111.51 (dd, 1JP3P2 = 158.4 Hz, 2JP3P5 = 9.7 Hz, 3JP3H1 = 3.6 Hz, P3), -36.04
(dddd, 1JP1P2 = 223.6 Hz, 2JP1P5 = 38.3 Hz, 2JP1P4 = 10.2 Hz, 1JP1H1 = 288.2 Hz, P1), 112.42
(ddd, 2JP5P1 = 38.3 Hz, 2JP5P4 = 10.3 Hz, 2JP5P3 = 9.7 Hz, P5) ppm.
127
45d: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.15 (d, 9 H, C(CH3)3), 1.50 (s, 9H, C(CH3)3),
1.52 (s, 9 H, C(CH3)3), 1.63 (d, 9 H, C(CH3)3), 5.05 (ddd 1JH1P1 = 318.2 Hz, 2JH1P2 = 9.0 Hz,
3
JH1P5 = 27.9 Hz, 1 H,H1) ppm. 31P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -119.04 (ddd,
1
JP3P2 = 149.4 Hz, P3), -108.90 (ddd, 1JP2P1 = 209.5 Hz, 1JP2P3 = 149.4 Hz, P2), -10.19 (dddd,
1
JP1P2 = 209.5 Hz, 2JP1P5 = 115.5 Hz, P1), 85.43 (dddd, 2JP5P1 = 115.5 Hz, P5), 359.33 (d, P4)
ppm. 31P-NMR (121.5 MHz, CDCl3, 25°C): δ = -120.38 (ddd, 1JP3P2 = 149.4 Hz, P3), -110.11
(dddd, 1JP2P1 = 209.5 Hz, 1JP2P3 = 149.4 Hz, 2JP2H = 9.0 Hz, P2), -11.68 (ddddd, 1JP1P2 = 209.5
Hz, 2JP1P5 = 115.5 Hz, 1JP1H1 = 318.2 Hz, P1), 84.07 (dm, 2JP5P1 = 115.5 Hz, 3JP5H1 = 27.9 Hz,
P5) ppm.
45a-d:
13
C{1H}-NMR (75.5 MHz, CDCl3, 25°C): δ = 32.82 (m, C(CH3)3), 33.12 (m,
C(CH3)3), 33.72 (m, C(CH3)3), 34.44 (m, C(CH3)3), 35.50 (m, C(CH3)3), 36.11 (m, C(CH3)3),
36.46 (m, C(CH3)3), 38.01 (m, C(CH3)3), 38.67 (m, C(CH3)3), 40.09 (m, C(CH3)3), 41.79 (m,
C(CH3)3), 204.16 (d, 2JCP2 = 6.8 Hz, cis-CO 45d), 204.78 (dd, 2JCP2 = 8.3 Hz, 3JCP = 4.3 Hz,
cis-CO 45a) ppm.
IR ν/cm-1 (KBr): 2960s (νC–H), 2926sh (νC–H), 2859m (νC–H), 2069s (CO), 1944s (CO),
1913sh (CO), 1393w (tBu), 1363m (tBu).
MS (FD, n-Hexan): m/z (%) = 668 (100) [M]+.
EA: C25H37O5P5Mo (668.37): ber. C 44.93, H 5.58; gef. C 45.25, H 5.86.
4.2.2.3 Spektroskopische und analytische Daten der Wolframpentacarbonyl-P5deltacyclenkomplexe 46a-d
46a: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.21 (s, 9 H, C(CH3)3), 1.39 (s, 9H, C(CH3)3),
1.54 (s, 9 H, C(CH3)3), 1.66 (s, 9 H, C(CH3)3), 5.26 (ddd 1JH1P1 = 175.9 Hz, 2JH1P2 = 5.1 Hz,
3
JH1P5 = 7.2 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -141.05 (dd,
1
JP3P2 = 183.6 Hz, P3), -111.71 (dddd, 1JP2P1 = 224.1 Hz, 1JP2P3 = 183.6 Hz, 2JP2P5 = 28.6 Hz,
1
JP2W = 226.4 Hz, P2), -39.68 (dt, 1JP1P2 = 224.1 Hz, P1), 106.65 (m, 2JP5P2 = 28.6 Hz, P5),
341.87 (d, P4) ppm. 31P-NMR (121.5 MHz, CDCl3, 25°C): δ = -142.31 (dd, 1JP3P2 = 183.6 Hz,
P3), -112.96 (ddddd, 1JP2P1 = 224.1 Hz, 1JP2P3 = 183.6 Hz, 2JP2P5 = 28.6 Hz, 1JP2W = 226.4 Hz,
2
JP2H1 = 5.1 Hz, P2), -40.93 (dddd, 1JP1P2 = 224.1 Hz, 1JP1H1 = 175.9 Hz, P1), 105.41 (m,
3
JP5H1 = 7.2 Hz, P5) ppm.
128
46b: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.18 (s, 9 H, C(CH3)3), 1.24 (s, 9 H, C(CH3)3),
1.53 (s, 9 H, C(CH3)3), 1.69 (d, 9 H, C(CH3)3), 4.39 (dd, 1JH1P1 = 195.9 Hz, 3JH1P5 = 36.9 Hz,
1 H, H1) ppm. 31P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -125.62 (dd, 1JP3P1 = 186.5 Hz,
P3), -106.72 (dd, 1JP2P1 = 202.9 Hz, 1JP2P3 = 186.5 Hz, P2), -9.72 (dd, 1JP1P2 = 202.9 Hz, 2JP1P5
= 120.8 Hz, P1), 89.38 (dm, 2JP5P1 = 120.8 Hz, P5), 366.72 (brs, P4) ppm. 31P-NMR (121.5
MHz, CDCl3, 25°C): δ = -126.91 (dd, 1JP3P2 = 186.5 Hz, P3), -107.96 (dd, 1JP2P1 = 202.9 Hz,
1
JP2P3 = 186.5 Hz, P2), -10.97 (dddd, 1JP1P2 = 202.9 Hz, 2JP1P5 = 120.8 Hz, 1JP1H1 = 195.9 Hz,
P1), 88.12 (dd, 1JP5P1 = 120.8 Hz, 3JP5H1 = 36.9 Hz, P5) ppm.
46c: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.12 (d, 9 H, C(CH3)3), 1.32 (s, 9H, C(CH3)3),
1.53 (s, 9 H, C(CH3)3), 1.69 (d, 9 H, C(CH3)3), 6.82 (d 1JH1P1 = 303.0 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -116.90 (dd, 1JP2P1 = 223.2 Hz, 1JP2P3 = 158.2
Hz, P2), -109.76 (dd, 1JP3P2 = 158.2 Hz, P3), -56.44 (ddd, 1JP1P2 = 223.2 Hz, 2JP1P5 = 47.7 Hz,
1
JP1W = 222.5 Hz, P1), 114.40 (ddd, 2JP5P1 = 47.4 Hz, P5), 350.86 (ddd, P4) ppm.
31
P-NMR
(121.5 MHz, CDCl3, 25°C): δ = -118.16 (dd, 1JP2P1 = 223.2 Hz, 1JP2P3 = 158.2 Hz, P2), 109.76 (dd, 1JP3P2 = 158.2 Hz, P3), -57.68 (dddd, 1JP1P2 = 223.2 Hz, 2JP1P5 = 47.7 Hz, 1JP1W =
222.5 Hz, 1JP1H1 = 303.0 Hz, P1), 113.15 (ddd, 2JP5P1 = 47.4 Hz, P5) ppm.
46d: 1H-NMR (269.7 MHz, CDCl3, 25°C): δ = 1.14 (d, 9 H, C(CH3)3), 1.35 (m, 9H,
C(CH3)3), 1.53 (s, 9 H, C(CH3)3), 1.64 (d, 9 H, C(CH3)3), 5.38 (ddd 1JH1P1 = 331.0 Hz, 2JH1P2
= 10.9 Hz, 3JH1P5 = 26.5 Hz, 1 H, H1) ppm. 31P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = 121.21 (dt, 1JP3P2 = 149.8 Hz, P3), -105.82 (ddd, 1JP2P1 = 210.4 Hz, 2JP2P3 = 149.8 Hz, P2), 32.98 (dd, 1JP1P2 = 210.4 Hz, 2JP1P5 = 111.8 Hz, 1JP1W = 210.4 Hz, P1), 84.88 (dddd, 1JP5P1 =
111.8 Hz, P5), 357.28 (d, P4) ppm. 31P-NMR (121.5 MHz, CDCl3, 25°C): δ = -122.46 (ddd,
1
JP3P2 = 149.8 Hz, P3), -107.06 (dddd, 1JP2P1 = 210.4 Hz, 1JP2P3 = 149.8 Hz, 2JP2H1 = 10.9 Hz,
P2), -34.22 (ddd, 1JP1P2 = 210.4 Hz, 2JP1P5 = 111.8 Hz, 1JP1W = 210.4 Hz, 1JP1H1 = 331.0 Hz,
P1), 83.62 (d, 1JP5P1 = 111.8 Hz, 3JP5H1 = 26.5 Hz, P5) ppm.
46a-d:
13
C{1H}-NMR (67.8 MHz, CDCl3, 25°C): δ = 32.74 (m, C(CH3)3), 33.15 (m,
C(CH3)3), 34.65 (m, C(CH3)3), 34.52 (m, C(CH3)3), 35.42 (m, C(CH3)3), 36.17 (m, C(CH3)3),
36.42 (m, C(CH3)3), 37.79 (m, C(CH3)3), 38.12 (m, C(CH3)3), 38.56 (m, C(CH3)3), 39.40 (m,
C(CH3)3), 40.11 (m, C(CH3)3), 41.48, (m, C(CH3)3), 41.76 (m, C(CH3)3), 64.08 (m, CtBu),
66.76 (m, CtBu) 81.44 (m, CtBu), 85.53 (m, CtBu), 93.42 (m, CtBu), 95.35 (m, CtBu), 196.01
(dd, 2JCP2 = 6.2 Hz, 3JCP = 4.6 Hz, cis-CO 46a), 196.99 (dd, 2JCP1 = 5.8 Hz, 3JCP = 5.8 Hz, cis129
CO 46d), 197.19 (dd, 2JCP1 = 5.8 Hz, 3JCP = 5.7 Hz, cis-CO 46c), 197.63 (dd, 2JCP1 = 32.2 Hz,
trans-CO 46d), 199.00 (d, 2JCP1 = 25.8 Hz, trans-CO 46c), 199.13 (d, 2JCP2 = 24.5 Hz, transCO 46a), 217.18 (m, C=P), 222.54 (m, C=P) ppm.
IR ν/cm-1 (KBr): 2960m (νC–H), 2929m (νC–H), 2861w (νC–H), 2072w (CO), 1939s (CO),
1392w (tBu), 1363m (tBu).
MS (FD, n-Hexan): m/z (%) = 757 (100) [M]+.
EA: C25H37O5P5W (756.28): ber. C 39.70, H 4.93; gef. C 39.60, H 4.72.[88]
4.2.3 Synthese und Charakterisierung von [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II)] 47
Eine Suspension von [(η6-C6H6)RuCl2]2 (0.083 g, 0.166 mmol) wurde mit dem
Epimerengemisch 17a/b des P5-Deltacyclens (0.131 g, 0.303 mmol) in 20 mL CH2Cl2 versetzt
und einen Tag bei Raumtemperatur gerührt. Die dunkelrote Lösung wurde vom ungelösten
überschüssigen Dichlorobenzolruthenium(II)-Dimeredukt abfiltriert und das Lösungsmittel im
Vakuum entfernt. Dabei bildet sich ein rotes Pulver, welches mit Et2O (2 mL x 3) und nHexan (5 mL x 3) gewaschen wird. [Ru(η6-C6H6)Cl2(P5C20H37)] 47 konnte in 93.3 % (0.193
g, 0.283 mmol) Ausbeute analysenrein erhalten werden. Für die Röntgenstrukturanalyse
geeignete Einkristalle von 47 wurden bei Raumtemperatur aus THF kristallisiert.
H1
Cl
tBu
C
P4
C3
tBu
4
C2
P5
P1
Cl
Ru
tBu
2
P3 P
C1
tBu
47
47: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.20 (s, 9 H, C(CH3)3), 1.40 (m, 9 H, C(CH3)3),
1.58 (s, 9 H, C(CH3)3), 1.59 (s, 9 H, C(CH3)3), 4.90 (ddd, 1JH1P1 = 399.2 Hz, 2JH1P2 = 10.3 Hz,
3
JH1P5 = 26.3 Hz, 1 H, H1), 5.90 (s, 6 H, C6H6) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3,
25°C): δ = -126.60 (m, 1JP3P2 = 149.1 Hz, P3), -115.42 (ddd, 1JP2P1 = 260.7 Hz, 1JP2P3 = 149.1
Hz, 2JP2P5 = 8.9 Hz, P2), 22.93 (dd, 1JP1P2 = 260.7 Hz, 2JP1P5 = 77.2 Hz, P1), 78.49 (dd, 2JP5P1
= 77.2 Hz, 2JP5P2 = 8.9 Hz, P5), 351.70 (m, P4) ppm. 31P-NMR (121.5 MHz, CDCl3, 25°C): δ
130
= -127.91 (d, 1JP3P2 = 149.1 Hz, P3), -116.66 (dddd, 1JP2P1 = 260.7 Hz, 1JP2P3 = 149.1 Hz,
2
JP2P5 = 8.9 Hz, 2JP2H1 = 10.3 Hz, P2), 21.74 (ddd, 1JP1P2 = 260.7 Hz, 2JP1P5 = 77.2 Hz, 1JP1H1 =
399.2 Hz, P1), 77.22 (m, 2JP5P1 = 77.2 Hz, 2JP5P2 = 8.9 Hz, 3JP5H = 26.3 Hz, P5) ppm.
13
C-
NMR (75.5 MHz, CDCl3, 25°C): δ = 33.32 (m, C(CH3)3), 34.20 (m, C(CH3)3), 35.26 (m,
C(CH3)3), 35.88 (m, C(CH3)3), 37.27 (m, C(CH3)3), 38.31 (m, C(CH3)3), 41.45 (m, C(CH3)3),
41.55 (m, C(CH3)3), 67.61 (m, CtBu), 87.70 (s, η6-C6H6), 88.12 (m, CtBu), 95.15 (m, CtBu),
216.44 (m, C=P) ppm.
MS (FD, THF): m/z (%) = 432 (100) [M-RuCl2Ph]+, 683 (3) [M]+.
EA: C26H43Cl2P5Ru (682.47): ber. C 45.76, H 6.35; gef. C 46.10, H 6.20.
RSA im Anhang.
4.2.4 Synthese und Charakterisierung der Rhodium(III)-P5-deltacyclen-Zweikernkomplexe 48a und 48b
Eine Lösung des P5-Deltacyclen-Epimerengemischs 17a/b (0.121 g, 0.280 mmol) in 20 mL
Et2O wurde mit [(1,5-COD)RhCl]2 (0.070 g, 0.140 mmol) versetzt und die dunkelrote Lösung
eine Woche bei Raumtemperatur gerührt. Die flüchtigen Bestandteile des Reaktionsgemisches
wurden im Vakuum entfernt und mit n-Hexan (5 mL x 3) gewaschen. Das erhaltene rote
Pulver wurde dann in CH2Cl2 aufgenommen und das Produkt daraus umkristallisiert.
[RhCl(P5C20H37)]2 48 konnte in 36.6 % (0.059 g, 0.051 mmol) Ausbeute erhalten werden. Für
eine Röntgenstrukturanalyse geeignete Einkristalle von 48 wurden bei Raumtemperatur aus
THF kristallisiert. Lösungen des Komplexes 48 liefern die Spektren zweier Komponenten 48a
und 48b, die in einem chemischen Gleichgewicht stehen, das vollständig zu 48a verschiebbar
ist. Einer der beiden Signalsätze, 48a oder 48b ist der meso-Verbindung 48, der andere dem
C2-symmetrischen Enantiomerenpaar 48’/48’’ zuzuordnen. Eine klare Zuordnung der
Signalsätze zu den Molekülstrukturen ist aus den NMR-Daten nicht möglich.
131
48a: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.25 (s, 18 H, C(CH3)3), 1.38 (s, 18 H,
C(CH3)3), 1.57 (brs, 18 H, C(CH3)3), 1.72 (brs, 18 H, C(CH3)3), 4.32 (dd, 1JH1P3 = 359.8 Hz,
3
JH1P1 = 39.1 Hz, 2H, H1) ppm. 31P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -19.70 (dd,
2
JP3P1A = 466.9 Hz, 1JP3Rh1 = 103.7 Hz, P3), 4.56 (m, 1JP1P2 = 389.1 Hz, 2JP1P3 = 466.9 Hz, P1),
71.39 (dt, 1JP2P1 = 389.1 Hz, P2), 94.34 (t, P5), 323.27 (d, P4) ppm.
31
P-NMR (121.5 MHz,
CDCl3, 25°C): δ = -19.70 (dd, 2JP3P1 = 466.9 Hz, 1JP3Rh1 = 103.7 Hz, 1JP3H1 = 359.8 Hz, P3),
4.56 (m, 1JP1P2 = 389.1 Hz, 2JP1P3 = 466.9 Hz, P1), 71.39 (dt, 1JP2P1 = 389.1 Hz, P2), 94.34 (t,
P5), 323.27 (d, P4) ppm.
48b: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.25 (s, 18 H, C(CH3)3), 1.38 (s, 18 H,
C(CH3)3), 1.57 (brs, 18 H, C(CH3)3), 1.72 (brs, 18 H, C(CH3)3), 4.36 (dd, 1JH1P3 = 372.2 Hz,
3
JH1P1 = 34.2 Hz, 2H, H1) ppm. 31P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -18.62 (dd,
2
JP3P1A = 445.5 Hz, 1JP3Rh1 = 103.6 Hz, P3), 10.42 (m, 2JP1P3A = 445.5 Hz, P1), 61.43 (m, P2),
91.41 (brs, P5), 327.27 (d, P4) ppm.
2
31
P-NMR (121.5 MHz, CDCl3, 25°C): δ = -18.62 (dd,
JP3P1 = 445.5 Hz, 1JP3Rh1 = 103.6 Hz, 1JP3H1 = 359.8 Hz, P3), 10.42 (m, 2JP1P3 = 445.5 Hz,
P1), 61.43 (m, P2), 91.41 (brs, P5), 327.27 (d, P4) ppm.
48a/b:
13
C{1H}-NMR (67.8 MHz, CDCl3, 25°C): δ = 29.76 (m, C(CH3)3), 30.16 (m,
C(CH3)3), 32.41 (m, C(CH3)3), 34.80 (m, C(CH3)3), 35.87 (m, C(CH3)3), 37.25 (m, C(CH3)3),
39.27 (m, C(CH3)3), 41.46 (m, C(CH3)3) ppm.
MS (FD, THF): m/z (%) = 1140 (50) [M]+.
EA: C40H74Cl2P10Rh2 x 0.7 CH2Cl2 (1141.49): ber. C 40.71 %, H 6.33 %; gef. C 40.81, H
6.22.
RSA im Anhang.
4.2.5 Synthese und Charakterisierung von iso-P5Deltacyclen 49a/b
iso-P5-Deltacylcen wurde nach Literaturvorschrift synthetisiert.[79] Zu einer Lösung des P5Deltacyclen-Epimerengemischs 17a/b (0.068 g, 0.157 mmol) in 40 mL THF wurde bei -78 °C
langsam tropfenweise 0.1 mL n-Butyllithium (0.010 g, 0.160 mmol, 1.6 M, n-Hexan)
gegeben. Die hellgelbe Lösung färbt sich mit der Zugabe des ersten Tropfens schlagartig
dunkelblau. Nach einer Stunde Rühren bei –78 °C wurde die Reaktionsmischung auf
Raumtemperatur erwärmt und weitere 6 Stunden gerührt. Während der Reaktionszeit färbt
132
sich die Lösung von dunkelblau nach grün, rot und schließlich gelb. Die flüchtigen
Bestandteile der Reaktionsmischung wurden im Vakuum abgezogen und das Rohprodukt
durch Säulenchromatographie (SiO2, n-Hexan) gereinigt. Nach dem Trocknen erhält man eine
untrennbare Mischung der beiden Epimeren 49a und 49b (0.060 g, 0.139 mmol, 88.2 %)
analysenrein als gelbes Pulver.
49a: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.14 (s, 9 H, C(CH3)3), 1.17 (s, 9 H, C(CH3)3),
1.34 (s, 9 H, C(CH3)3), 1.47 (s, 9 H, C(CH3)3), 3.03 (d, 1JH1P1 = 6.3 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -137.81 (m, 1JP3P2 = 185.8 Hz, 2JP3P5 = 14.9
Hz, 2JP3P1 = 9.8 Hz, P3), -22.03 (dd, 1JP2P3 = 185.8 Hz, 2JP2P5 = 14.9 Hz, P2), 60.13 (ddd,
1
JP1P5 = 174.9 Hz, 2JP1P4 = 21.2 Hz, 2JP1P3 = 9.8 Hz, P1), 114.82 (ddt, 1JP5P1 = 174.9 Hz, 2JP5P4
= 22.5 Hz, 2JP5P2 = 14.9 Hz, 2JP5P3 = 14.9 Hz, P5), 347.77 (t, 2JP4P5 = 22.5 Hz, 2JP4P1 = 21.2
Hz, P4) ppm.
49b: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.13 (s, 9 H, C(CH3)3), 1.14 (s, 9 H, C(CH3)3),
1.37 (s, 9 H, C(CH3)3), 1.48 (s, 9 H, C(CH3)3), 1.96 (d, 1JH1P5 = 15.0 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -156.05 (dt, 1JP3P2 = 193.5 Hz, 2JP3P1 = 11.4
Hz, 2JP3P4 = 9.9 Hz, P3), -31.53 (dd, 1JP2P3 = 193.5 Hz, 2JP2P5 = 12.1 Hz, P2), 46.52 (ddd,
1
JP5P1 = 192.8 Hz, 2JP5P4 = 18.9 Hz, 2JP5P2 = 12.1 Hz, P5), 80.15 (ddd, 1JP1P5 = 192.8 Hz, 2JP1P4
= 20.3 Hz, 2JP1P3 = 11.4 Hz, P1), 320.73 (ddd, 2JP4P5 = 18.9 Hz, 2JP4P1 = 20.3 Hz, 2JP4P3 = 9.9
Hz, P4) ppm.
49a/b:
13
C{1H}-NMR (67.8 MHz, CDCl3, 25°C): δ = 32.99 (m, C(CH3)3), 33.25 (m,
C(CH3)3), 33.38 (m, C(CH3)3), 33.76 (m, C(CH3)3), 34.11 (ddd, 3JCP = 12.7 Hz, 3JCP = 7.2 Hz,
3
JCP = 5.5 Hz, C(CH3)3), 35.56 (ddd, 3JCP = 12.1 Hz, 3JCP = 10.4 Hz, 3JCP = 10.3 Hz,
C(CH3)3), 37.33 (ddd, 3JCP = 16.2 Hz, 3JCP = 13.2 Hz, 3JCP = 6.5 Hz, C(CH3)3), 42.85 (t, 3JCP =
133
17.3 Hz, C(CH3)3), 65.44 (ddd, JCP = 53.4 Hz, JCP = 42.9 Hz, JCP = 15.8 Hz, CC(CH3)3),
66.72 (m, CC(CH3)3), 99.39 (m, CC(CH3)3), 220.25 (ddd, JCP = 51.9 Hz, JCP = 10.0 Hz, JCP =
5.2 Hz, CC(CH3)3) ppm.
MS (ESI-ToF, CH2Cl2/MeOH): m/z (%) = 433.17 (100) [MH]+.
EA: C20H37P5 (432.38): ber. C 55.56 %, H 8.62 %; gef. C 55.17, H 8.52.
4.2.6 Synthese der Chrom-, Molybdän- und Wolframpentacarbonyl-iso-P5-deltacyclenkomplexe 42a/b, 50a/b und 43a/b
Exemplarisch für die Molybdänkomplexe 50a/b
Eine Lösung der Epimerenmischung von iso-P5-Deltacyclen 49a/b (0.050 g, 0.116 mmol) in
20 mL THF werden bei Raumtemperatur mit einem Überschuss einer frisch hergestellten
gelbe Lösung von [Mo(CO)5THF] versetzt. Diese wurde zuvor durch Belichtung von
[Mo(CO)6] (0.153 g, 0.580 mmol) in 60 mL THF mit einer Quecksilberdampflampe
hergestellt. Nach 3 Tagen Rühren bei Raumtemperatur wird das Lösungsmittel im Vakuum
abgezogen und das gelbe Rohprodukt durch Säulenchromatographie (SiO2, n-Hexan)
gereinigt. Die beiden Komplexepimere von [Mo(CO)5(iso-P5C20H37)] 50a und 50b (0.055 g,
0.083 mmol, 71.4 %) werden analysenrein als gelbes Pulver erhalten. Für eine
Röntgenstrukturanalyse geeignete Einkristalle von 50a wurden bei +4 °C aus n-Hexan
kristallisiert.
Die Komplexe 42a/b und 43a/b wurden wie oben beschrieben synthetisiert mit folgenden
Ansatzgrößen und Ausbeuten:
[Cr(CO)6] (0.050 g, 0.227 mmol) und 49a/b (0.041 g, 0.095 mmol) ergaben die [Cr(CO)5(isoP5C20H37)]-Komplexe 42a/b (0.046 g, 0.074 mmol, 77.9 %).
[W(CO)6] (0.068 g, 0.194 mmol) und 49a/b (0.035 g, 0.081 mmol) ergaben die [W(CO)5(isoP5C20H37)]-Komplexe 43a/b (0.047 g, 0.062 mmol, 76.7 %).
134
4.2.6.1 Spektroskopische und analytische Daten der Chrompentacarbonyl-iso-P5deltacyclenkomplexe 42a/b
42a: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.26 (s, 9 H, C(CH3)3), 1.32 (s, 9 H, C(CH3)3),
1.45 (s, 9 H, C(CH3)3), 1.57 (s, 9 H, C(CH3)3), 3.82 (d, 1JH1P1 = 8.8 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -129.44 (dddd, 1JP3P2 = 190.7 Hz, 2JP3P1 = 17.8
Hz, 2JP3P5 = 14.5 Hz, 2JP3P4 = 11.1 Hz, P3), 4.79 (ddd, 1JP2P3 = 190.7 Hz, 2JP2P5 = 14.5 Hz,
2
JP2P1 = 10.0 Hz, P2), 102.39 (dddd, 1JP1P5 = 161.1 Hz, 2JP1P4 = 31.2 Hz, 2JP1P3 = 17.8 Hz,
2
JP1P2 = 10.0 Hz, P1), 135.71 (dddd, 1JP5P1 = 161.1 Hz, 2JP5P2 = 14.5 Hz, 2JP5P3 = 14.5 Hz,
2
JP5P4 = 14.4 Hz, P5), 360.75 (ddd, 2JP4P1 = 31.2 Hz, 2JP4P5 = 14.4 Hz, 2JP4P3 = 11.1 Hz, P4)
ppm.
42b: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.14 (s, 9 H, C(CH3)3), 1.44 (s, 9 H, C(CH3)3),
1.53 (s, 9 H, C(CH3)3), 1.56 (s, 9 H, C(CH3)3), 2.87 (d, 1JH1P5 = 3.4 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -139.61 (ddd, 1JP3P2 = 175.5 Hz, 2JP3P1 = 15.6
Hz, 2JP3P5 = 10.0 Hz, P3), -16.69 (dd, 1JP2P3 = 175.5 Hz, 2JP2P1 = 15.6 Hz, P2), 86.91 (ddd,
1
JP1P5 = 155.1 Hz, 2JP5P4 = 15.8 Hz, 2JP5P3 = 10.0 Hz, P5), 148.30 (dt, 1JP5P1 = 155.1 Hz, 2JP1P2
= 15.6 Hz, 2JP1P3 = 15.6 Hz, P1), 371.35 (d, 2JP4P5 = 15.8 Hz, P4) ppm.
42a/b:
13
C{1H}-NMR (67.8 MHz, CDCl3, 25°C): δ = 32.20 (m, C(CH3)3), 33.28 (m,
C(CH3)3), 33.65 (m, C(CH3)3), 34.29 (m, C(CH3)3), 35.01 (m, C(CH3)3), 35.63 (m, C(CH3)3),
38.39 (m, C(CH3)3), 41.85 (m, C(CH3)3), 216.54 (dd, 2JCP5 = 9.4 Hz, 3JCP1 = 5.5 Hz, cis-CO
42b), 220.43 (d, 2JCP5 = 3.4 Hz, trans-CO 42b) ppm.
IR ν/cm-1 (KBr): 2956m (νC–H), 2862w (νC–H), 2060m (CO), 1985sh (CO), 1934vs (CO),
1392w (tBu), 1363m (tBu).
MS (FD, n-Hexan): m/z 625 (100) [M]+.
EA: C25H37O5P5Cr (624.43): ber. C 48.09, H 5.97; gef. C 47.83, H 5.84.[88]
4.2.6.2 Spektroskopische und analytische Daten der Molydänpentacarbonyl-iso-P5deltacyclenkomplexe 50a/b
50a: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.27 (s, 9 H, C(CH3)3), 1.30 (s, 9 H, C(CH3)3),
1.48 (s, 9 H, C(CH3)3), 1.55 (s, 9 H, C(CH3)3), 3.87 (d, 1JH1P1 = 8.6 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -132.86 (dddd, 1JP3P2 = 190.5 Hz, 2JP3P1 = 18.6
Hz, 2JP3P5 = 14.0 Hz, 2JP3P4 = 10.1 Hz, P3), 0.51 (ddd, 1JP2P3 = 190.4 Hz, 2JP2P5 = 14.2 Hz,
135
2
JP2P1 = 10.5 Hz, P2), 79.12 (dddd, 1JP1P5 = 153.6 Hz, 2JP1P4 = 30.6 Hz, 2JP1P3 = 18.6 Hz, 2JP1P2
= 10.5 Hz, P1), 136.30 (dddd, 1JP5P1 = 153.6 Hz, 2JP5P4 = 14.9 Hz, 2JP5P2 = 14.2 Hz, 2JP5P3 =
14.0 Hz, P5), 357.63 (ddd, 2JP4P1 = 30.6 Hz, 2JP4P5 = 14.9 Hz, 2JP4P3 = 10.1 Hz, P4) ppm. 31PNMR (121.5 MHz, CDCl3, 25°C): δ = -132.86 (dddd, 1JP3P2 = 190.5 Hz, 2JP3P1 = 18.6 Hz,
2
JP3P5 = 14.0 Hz, 2JP3P4 = 10.1 Hz, P3), 0.51 (ddd, 1JP2P3 = 190.4 Hz, 2JP2P5 = 14.2 Hz, 2JP2P1 =
10.5 Hz, P2), 79.12 (ddddd, 1JP1P5 = 153.6 Hz, 2JP1P4 = 30.6 Hz, 2JP1P3 = 18.6 Hz, 2JP1P2 = 10.5
Hz, 2JP1H1 = 8.6 Hz, P1), 136.30 (dddd, 1JP5P1 = 153.6 Hz, 2JP5P4 = 14.9 Hz, 2JP5P2 = 14.2 Hz,
2
JP5P3 = 14.0 Hz, P5) ppm.
RSA im Anhang.
50b: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.17 (s, 9 H, C(CH3)3), 1.43 (s, 9 H, C(CH3)3),
1.52 (s, 9 H, C(CH3)3), 1.57 (s, 9 H, C(CH3)3), 2.88 (d, 1JH1P5 = 3.4 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -143.45 (ddd, 1JP3P2 = 176.6 Hz, 2JP3P1 = 15.2
Hz, 2JP3P5 = 9.4 Hz, P3), -16.68 (dd, 1JP2P3 = 176.6 Hz, 2JP2P1 = 16.1 Hz, P2), 87.03 (ddd,
1
JP1P5 = 146.7 Hz, 2JP5P4 = 15.8 Hz, 2JP5P3 = 9.4 Hz, P5), 124.72 (ddt, 1JP1P5 = 146.7 Hz, 2JP1P2
= 16.1 Hz, 2JP1P3 = 15.2 Hz, 2JP1P4 = 4.6 Hz, P1), 371.45 (dd, 2JP4P5 = 15.8 Hz, 2JP4P1 = 4.6 Hz,
P4) ppm. 31P-NMR (121.5 MHz, CDCl3, 25°C): δ = -143.45 (ddd, 1JP3P2 = 176.6 Hz, 2JP3P1 =
15.2 Hz, 2JP3P5 = 9.4 Hz, P3), -16.68 (dd, 1JP2P3 = 176.6 Hz, 2JP2P1 = 16.1 Hz, P2), 87.03
(dddd, 1JP1P5 = 146.7 Hz, 2JP5P4 = 15.8 Hz, 2JP5P3 = 9.4 Hz, 2JP1H1 = 3.4 Hz, P5), 124.72 (ddt,
1
JP1P5 = 146.7 Hz, 2JP1P2 = 16.1 Hz, 2JP1P3 = 15.2 Hz, 2JP1P4 = 4.6 Hz, P1) ppm.
50a/b:
13
C{1H}-NMR (67.8 MHz, CDCl3, 25°C): δ = 32.88 (m, C(CH3)3), 33.57 (m,
C(CH3)3), 33.65 (m, C(CH3)3), 34.48 (m, C(CH3)3), 35.09 (m, C(CH3)3), 35.66 (m, C(CH3)3),
38.33 (m, C(CH3)3), 42.05 (m, C(CH3)3), 205.10 (dd, 2JCP1 = 7.0 Hz, 3JCP5 = 4.1 Hz, cis-CO
50a), 205.67 (t, 2JCP5 = 6.4 Hz, 3JCP1 = 6.4 Hz, cis-CO 50b), 209.30 (d, 2JCP5 = 25.8 Hz, transCO 50b), 209.94 (d, 2JCP = 25.8 Hz, trans-CO 50a) ppm.
IR ν/cm-1 (KBr): 2960s (νC–H), 2926sh (νC–H), 2859m (νC–H), 2069s (CO), 1993vs (CO),
1941sh (CO), 1393w (tBu), 1362m (tBu).
MS (ESI-ToF, CHCl3/MeOH): m/z 671.05 (100) [MH3]+.
EA: C25H37O5P5Mo (668.38): ber. C 44.93, H 5.58; gef. C 45.24, H 5.85.
136
4.2.6.3 Spektroskopische und analytische Daten der Wolframpentacarbonyl-iso-P5deltacyclenkomplexe 43a/b
43a: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.14 (s, 9 H, C(CH3)3), 1.34 (s, 9 H, C(CH3)3),
1.49 (s, 9 H, C(CH3)3), 1.56 (s, 9 H, C(CH3)3), 3.83 (d, 1JH1P1 = 9.1 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -129.81 (dddd, 1JP3P2 = 191.2 Hz, 2JP3P1 = 19.4
Hz, 2JP3P5 = 14.5 Hz, 2JP3P4 = 12.3 Hz, P3), 1.86 (ddd, 1JP2P3 = 191.2 Hz, 2JP2P5 = 14.5 Hz,
2
JP2P1 = 11.1 Hz, P2), 57.58 (dddd, 1JP1P5 = 149.9 Hz, 2JP1P4 = 32.3 Hz, 2JP1P3 = 19.4 Hz, 2JP1P2
= 11.1 Hz, P1), 140.12 (dddd, 1JP5P1 = 149.9 Hz, 2JP5P4 = 14.5 Hz, 2JP5P2 = 14.5 Hz, 2JP5P3 =
14.5 Hz, P5), 356.80 (ddd, 2JP4P1 = 32.3 Hz, 2JP4P5 = 14.5 Hz, 2JP4P3 = 12.3 Hz, P4) ppm.
43b: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.17 (s, 9 H, C(CH3)3), 1.45 (s, 9 H, C(CH3)3),
1.52 (s, 9 H, C(CH3)3), 1.58 (s, 9 H, C(CH3)3), 2.93 (d, 1JH1P5 = 3.6 Hz, 1 H, H1) ppm.
31
P{1H}-NMR (121.5 MHz, CDCl3, 25°C): δ = -141.90 (ddd, 1JP3P2 = 175.2 Hz, 2JP3P1 = 15.0
Hz, 2JP3P5 = 10.0 Hz, P3), -19.81 (dd, 1JP2P3 = 175.2 Hz, 2JP2P1 = 16.7 Hz, P2), 92.43 (ddd,
1
JP5P1 = 142.4 Hz, 2JP5P4 = 15.6 Hz, 2JP5P3 = 10.0 Hz, P5), 103.69 (dt, 1JP1P5 = 142.4 Hz, 2JP1P2
= 16.7 Hz, 2JP1P3 = 15.0 Hz, 1JP1W = 105.9 Hz, P1), 371.45 (d, 2JP4P5 = 15.6 Hz, P4) ppm.
43a/b:
13
C{1H}-NMR (67.8 MHz, CDCl3, 25°C): δ = 32.84 (m, C(CH3)3), 33.30 (m,
C(CH3)3), 33.41 (m, C(CH3)3), 34.45 (m, C(CH3)3), 35.19 (m, C(CH3)3), 35.61 (m, C(CH3)3),
38.39 (m, C(CH3)3), 41.85 (m, C(CH3)3), 197.00 (d, 2JCP1 = 25.8 Hz, cis-CO 43a), 197.74 (m,
cis-CO 43b), 198.36 (d, 2JCP5 = 5.1 Hz, trans-CO 43a), 198.56 (d, 2JCP5 = 3.9 Hz, trans-CO
43b) ppm.
IR ν/cm-1 (KBr): 2956s (νC–H), 2925s (νC–H), 2856s (νC–H), 2068s (CO), 1936vs (CO),
1931sh (CO), 1392w (tBu), 1363m (tBu).
MS (FD, n-Hexan): m/z 668 (100) [M]+.
EA: C25H37O5P5W (756.28): ber. C 39.70, H 4.93; gef. C 39.60, H 4.72.[89]
4.2.7 Synthese und Charakterisierung von P5-Homocunean 51
Eine hellgelbe Lösung der Epimerenmischung von P5-Deltacyclen 17a/b (0.068 g, 0.157
mmol) und Benzophenon (0.034 g, 0.189 mmol) in 40 mL THF wurde auf -78 °C gekühlt.
Unter starkem Rühren wurde 0.11 mL n-Butyllithium (0.011 g, 0.176 mmol, 1.6 M, n-Hexan)
dazugetropft. Die Lösung verfärbt sich mit dem ersten Tropfen schlagartig dunkelblau, nach
ca. 30 min rot, dann gelb und entfärbt sich schließlich. Nach einer Stunde Rühren bei -78 °C
137
wurde die Reaktionsmischung auf Raumtemperatur erwärmt und weitere 6 Stunden gerührt.
Die flüchtigen Bestandteile wurden im Vakuum abgezogen und das Rohprodukt durch
Säulenchromatographie (SiO2, n-Hexan) gereinigt. Nach dem Trocknen erhält man P5Homocunean 51 als farbloses Pulver in einer Ausbeute von 89.7 % (0.061 g, 0.141 mmol).
51: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 0.95 (s, 9 H, C(CH3)3), 1.18 (s, 9 H, C(CH3)3),
1.24 (s, 9 H, C(CH3)3), 1.34 (s, 9 H, C(CH3)3), 2.68 (s, 1 H, H1) ppm. 31P{1H}-NMR (121.5
MHz, CDCl3, 25°C): δ= -102.62 (ddd, 1JP5P4 = 182.4 Hz, 2JP5P3 = 7.5 Hz, P5), -41.36 (dddd,
1
JP4P5 = 182.4 Hz, 2JP4P1 = 24.6 Hz, 2JP4P3 = 24.5 Hz, 2JP4P2 = 14.5 Hz, P4), 5.24 (dddd, 1JP2P3
= 167.7 Hz, 2JP2P4 = 14.5 Hz, 2JP2P1 = 15.7 Hz, P2), 42.14 (dddd, 1JP3P2 = 167.7 Hz, 2JP3P4 =
24.5 Hz, 2JP3P1 = 16.0 Hz, 2JP3P5 = 7.5 Hz, P3), 83.69 (m, 2JP1P4 = 24.6 Hz, 2JP1P3 = 16.0 Hz,
2
JP1P2 = 15.7 Hz, P1) ppm. 13C{1H}-NMR (75.5 MHz, CDCl3, 25°C): δ = 29.54 (m, C(CH3)3),
29.96 (ddd, 3JCP = 10.7 Hz, 3JCP = 7.8 Hz, 3JCP = 5.4 Hz, C(CH3)3), 31.29 (dd, 3JCP = 10.7 Hz,
3
JCP = 9.4 Hz, C(CH3)3), 34.90 (dd, 2JCP = 17.0 Hz, 2JCP = 15.2 Hz, C(CH3)3), 35.59 (ddd, 2JCP
= 14.3 Hz, 2JCP = 14.3 Hz, 2JCP = 4.4 Hz, C(CH3)3), 36.65 (ddd, 2JCP = 20.2 Hz, 2JCP = 16.2
Hz, 2JCP = 13.0 Hz, C(CH3)3), 37.59 (ddd, 2JCP = 20.2 Hz, 2JCP = 12.0 Hz, 2JCP = 11.2 Hz,
C(CH3)3), 38.38 (ddd, 1JCP = 68.6 Hz, 1JCP = 23.2 Hz, 1JCP = 10.5 Hz, C2), 56.23 (ddd, 1JCP =
81.3 Hz, 1JCP = 54.8 Hz, 1JCP = 43.5 Hz, C1), 66.49 (dd, 1JCP = 55.1 Hz, 1JCP = 42.4 Hz, C4),
72.45 (ddd, 1JCP = 65.1 Hz, 1JCP = 36.6 Hz, 1JCP = 20.0 Hz, C3) ppm.
MS (FD, CDCl3): m/z (%) = 432 (100) [M]+.
EA: C20H37P5 (432.38): ber. C 55.56, H 8.62; gef. C 55.53, H 8.63.[90]
138
4.2.8 Synthese der Chrom- Molybdän- und Wolframpentacarbonyl-P5-homocuneankomplexe 52, 53 und 54
Exemplarisch für die Molybdänkomplexe 53
Eine Lösung von P5-Homocunean 51 (0.032 g, 0.074 mmol) in 20 mL THF werden bei
Raumtemperatur mit einem Überschuss einer frisch hergestellten Lösung von [Mo(CO)5THF]
versetzt. Diese wurde vorher durch einstündige Belichtung von [Mo(CO)6] (0.185 g, 0.7
mmol) in 60 mL THF mit einer Quecksilberdampflampe hergestellt. Nach 3 Tagen Rühren
bei Raumtemperatur wird das Lösungsmittel im Vakuum abgezogen und das Rohprodukt
durch Säulenchromatographie (SiO2, n-Hexan) gereinigt. Man erhält [Mo(CO)5-P5Homocunean] 53 (0.034 g, 0.051 mmol, 68.4 %) als gelbes Pulver. Röntgenfähige Kristalle
von 53 konnten aus n-Hexan bei +4°C auskristallisiert werden.
Die Komplexe 52 und 54 wurden wie oben beschrieben synthetisiert mit folgenden
Ansatzgrößen und Ausbeuten:
[Cr(CO)6] (0.040 g, 0.182 mmol) und 51 (0.032 g, 0.074 mmol) ergaben den [Cr(CO)5-P5Homocunean]-Komplex 52 (0.034 g, 0.054 mmol, 73.6 %). Röntgenfähige Kristalle von 52
konnten aus n-Hexan bei +4°C auskristallisiert werden.
[W(CO)6] (0.350 g, 0.995 mmol) und 51 (0.135 g, 0.312 mmol) ergaben den [W(CO)5-P5Homocunean]-Komplex 54 (0.187 g, 0.247 mmol, 79.1 %). Röntgenfähige Kristalle von 54
konnten aus n-Hexan bei +4°C auskristallisiert werden.
4.2.8.1
Spektroskopische
und
analytische
Daten
von
Chrompentacarbonyl-P5-
homocuneankomplex 52
52: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.15 (s, 9 H, C(CH3)3), 1.22 (s, 9 H, C(CH3)3),
1.25 (s, 9 H, C(CH3)3), 1.43 (s, 9 H, C(CH3)3), 2.78 (s, 1 H, H1) ppm. 31P{1H}-NMR (121.5
MHz, CDCl3, 25°C): δ = -101.53 (dm, 1JP5P4 = 181.0 Hz, P5), 6.89 (dm, 1JP2P3 = 169.6 Hz,
139
P2), 18.83 (dm, 1JP4P5 = 181.0 Hz, P4), 28.44 (dm, 1JP3P2 = 169.6 Hz, P3), 89.57 (P1) ppm.
13
C{1H}-NMR (75.5 MHz, CDCl3, 25°C): δ = 29.80 (m, C(CH3)3), 30.01 (m, C(CH3)3), 31.12
(m, C(CH3)3), 31.38 (dd, 3JCP = 9.1 Hz, 3JCP = 8.8 Hz, C(CH3)3), 35.11 (dd, 2JCP = 16.7 Hz,
2
JCP = 16.4 Hz, C(CH3)3), 36.37 (dd, 2JCP = 14.2 Hz, 2JCP = 14.1 Hz, C(CH3)3), 37.31 (ddd,
2
JCP = 19.6 Hz, 2JCP = 16.4 Hz, 2JCP = 5.5 Hz, C(CH3)3), 37.96 (ddd, 2JCP = 20.6 Hz, 2JCP =
11.5 Hz, 2JCP = 11.5 Hz, C(CH3)3), 46.30 (ddd, 1JCP = 65.0 Hz, 1JCP = 16.1 Hz, 1JCP = 16.0 Hz,
CC(CH3)3), 55.61 (ddd, 1JCP = 81.1 Hz, 1JCP = 54.8 Hz, 1JCP = 45.1 Hz, CC(CH3)3), 64.70 (dd,
1
JCP = 55.1 Hz, 1JCP = 45.4 Hz, CC(CH3)3), 82.22 (ddd, 1JCP = 69.3 Hz, 1JCP = 21.8 Hz, 1JCP =
19.9 Hz, CC(CH3)3), 215.19 (dd, 2JCP4 = 11.0 Hz, 3JCP5 = 3.3 Hz, cis-CO), 221.10 (d, 2JCP4 =
2.8 Hz, trans-CO) ppm.
IR ν/cm-1 (KBr): 2958m (νC–H), 2929sh (νC–H), 2862w (νC–H), 2063m (CO), 1944vs (CO),
1930sh (CO), 1391w (tBu), 1363w (tBu).
MS (ESI-ToF, CHCl3/MeOH): m/z 625.08 (100) [M]+.
EA: C25H37O5P5Cr (624.43): ber. C 48.09, H 5.97; gef. C 48.07, H 6.16.
RSA im Anhang.
4.2.8.2 Spektroskopische und analytische Daten von Molybdänpentacarbonyl-P5homocuneankomplex 53
53: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.14 (s, 9 H, C(CH3)3), 1.22 (s, 9 H, C(CH3)3),
1.25 (s, 9 H, C(CH3)3), 1.45 (s, 9 H, C(CH3)3), 2.77 (s, 1 H, H1) ppm. 31P{1H}-NMR (121.5
MHz, CDCl3, 25°C): δ = -97.35 (dm, 1JP5P4 = 175.0 Hz, P5), -10.31 (dm, 1JP4P5 = 175.0 Hz,
P4), 6.09 (dm, 1JP2P3 = 169.8 Hz, P2), 30.52 (dm, 1JP3P2 = 169.8 Hz, P3), 88.03 (P1) ppm.
13
C{1H}-NMR (75.5 MHz, CDCl3, 25°C): δ = 29.57 (ddd, 3JCP = 7.4 Hz, 3JCP = 7.4 Hz, 3JCP =
3.0 Hz, C(CH3)3), 29.99 (ddd, 3JCP = 11.5 Hz, 3JCP = 7.1 Hz, 3JCP = 5.7 Hz, C(CH3)3), 31.11
(m, C(CH3)3), 31.37 (dd, 3JCP = 10.7 Hz, 3JCP = 9.0 Hz, C(CH3)3), 35.15 (dd, 2JCP = 17.0 Hz,
2
JCP = 15.9 Hz, C(CH3)3), 36.28 (dd, 2JCP = 14.4 Hz, 2JCP = 14.3 Hz, C(CH3)3), 37.42 (m,
C(CH3)3), 37.97 (ddd, 2JCP = 21.0 Hz, 2JCP = 11.4 Hz, 2JCP = 11.4 Hz, C(CH3)3), 44.60 (ddd,
1
JCP = 66.7 Hz, 1JCP = 15.1 Hz, 1JCP = 14.7 Hz, CC(CH3)3), 55.44 (m, CC(CH3)3), 65.15 (dd,
1
JCP = 55.3 Hz, 1JCP = 44.8 Hz, CC(CH3)3), 79.79 (m, CC(CH3)3), 204.30 (dd, 2JCP = 8.1 Hz,
2
JCP = 3.1 Hz, cis-CO), 210.18 (d, 2JCP = 32.7 Hz, trans-CO) ppm.
IR ν/cm-1 (KBr): 2956s (νC–H), 2928sh (νC–H), 2860m (νC–H), 2073s (CO), 1950vs (CO),
1928vs (CO), 1389m (tBu), 1361s (tBu).
MS (ESI-ToF, CHCl3/MeOH): m/z 671.05 (100) [MH2]+.
140
EA: C25H37O5P5Mo (668.37): ber. C 44.93, H 5.58; gef. C 45.19, H 5.77.
RSA im Anhang.
4.2.8.3 Spektroskopische und analytische Daten von Wolframpentacarbonyl-P5homocuneankomplex 54
54: 1H-NMR (300.1 MHz, CDCl3, 25°C): δ = 1.15 (s, 9 H, C(CH3)3), 1.22 (s, 9 H, C(CH3)3),
1.26 (s, 9 H, C(CH3)3), 1.46 (s, 9 H, C(CH3)3), 2.75 (s, 1 H, H1) ppm. 31P{1H}-NMR (121.5
MHz, CDCl3, 25°C): δ = -94.57 (dm, 1JP5P4 = 174.1 Hz, P5), -35.63 (dm, 1JP4P5 = 174.1 Hz,
1
JWP = 225.0 Hz, P4), 6.49 (m, 1JP2P3 = 169.8 Hz, P2), 28.16 (m, 1JP3P2 = 169.8 Hz, P3), 88.27
(P1) ppm.
13
C{1H}-NMR (100.5 MHz, CDCl3, 25°C): δ = 29.69 (ddd, 3JCP = 7.5 Hz, 3JCP =
7.5 Hz, 3JCP = 3.0 Hz, C(CH3)3), 29.99 (ddd, 3JCP = 11.4 Hz, 3JCP = 6.5 Hz, 3JCP = 5.2 Hz,
C(CH3)3), 31.38 (dd, 3JCP = 10.8 Hz, 3JCP = 8.8 Hz, C(CH3)3), 31.59 (m, C(CH3)3), 35.17 (dd,
2
JCP = 16.8 Hz, 2JCP = 16.3 Hz, C(CH3)3), 36.45 (dd, 2JCP = 14.5 Hz, 2JCP = 13.5 Hz,
C(CH3)3), 37.37 (ddd, 2JCP = 19.0 Hz, 2JCP = 17.6 Hz, 2JCP = 5.1 Hz, C(CH3)3), 38.01 (ddd,
2
JCP = 19.7 Hz, 2JCP = 12.2 Hz, 2JCP = 11.7 Hz, C(CH3)3), 45.79 (ddd, 1JCP = 66.5 Hz, 1JCP =
15.2 Hz, 1JCP = 14.7 Hz, CC(CH3)3), 56.29 (m, CC(CH3)3), 65.14 (dd, 1JCP = 54.9 Hz, 1JCP =
44.9 Hz, CC(CH3)3), 79.98 (m, CC(CH3)3), 196.23 (dd, 2JCP = 6.0 Hz, 2JCP = 2.9 Hz, cis-CO),
198.37 (d, 2JCP = 32.8 Hz, trans-CO) ppm.
IR ν/cm-1 (KBr): 2958s (νC–H), 2930sh (νC–H), 2900m (νC–H), 2863m (νC–H), 2072s (CO),
1982sh (CO), 1940vs (CO), 1391m (tBu), 1363m (tBu).
MS-FD: m/z (%) = 757 (100) [M]+.
EA: C25H37O5P5W (756.28): ber. C 39.70, H 4.93; gef. C 39.95, H 4.93.
RSA im Anhang.
141
5. Anhang
5.1 Kristallstrukturanalysen
Die röntgenstrukturanalytischen Untersuchungen der Substanzen wurden von Dr. F. W.
Heinemann und P. Bakatselos mit einem Bruker SMART APEX 2 Röntgendiffraktometer
(MoKα-Strahlung (λ = 0.71073 Å) mit Graphitmonochromator) (Verbindungen 45a, 50a, 53),
einem Bruker-Nonius Kappa Röntgendiffraktometer mit CCD-Flächenzähler (MoKαStrahlung (λ = 0.71073 Å) mit Graphitmonochromator) (Verbindungen 47, 48a, 52), sowie
mit einem Bruker Kappa APEX 2 IµS Duo Röntgendiffraktometer (MoKα-Strahlung (λ =
0.71073 Å) mit einer QUAZAR fokussierenden Montel-Optik) (Verbindung 54) durchgeführt.
Hilfsmittel und Programme:
Ed. A. J. C. Wilson, International Tables for Crystallography, Vol. C, Kluwer Academic
Publishers, Dordrecht 1992.
Messungen:
APEX 2 (Bruker AXS, 2009)
COLLECT (Bruker AXS, 2002)
Datenreduktion:
SAINT (Bruker AXS, 2009)
EvalCCD (Duisenberg et al., 2003)
Absorptionskorrektur:
SADABS (Bruker AXS, 2009)
Strukturlösung und Verfeinerung:
SHELXTL NT 6.12 (Bruker AXS, 2002)
142
5.1.1 Kristallstrukturdaten von Molybdänpentacarbonyl-P5-deltacyclen 45a
O2
O1
P1
C6
C5
C9
H1
O5
Mo
C4
C7
C2
P5
O3
P2
C8
C1
P4
C3
P3
O4
Summenformel:
C25H37MoO5P5
Molmasse [g mol-1]:
668.34
Kristallfarbe, -form:
gelb, Block
Kristallgröße [mm]:
0.40×0.18×0.14
Meßtemperatur [K]:
100
Kristallsystem:
triklin
Raumgruppe:
P 1 (Nr. 2)
Kristalldaten:
a [Å] = 10.5432(2)
α [°]
= 86.442(1)
b [Å] = 11.4738(2)
β [°]
= 85.596(1)
c [Å] = 13.0010(3)
γ [°]
= 74.186(1)
V [Å3] = 1507.36(5)
Z
=2
Berechnete Dichte [g cm-3]: 1.473
µ [mm-1]:
0.733
F(000):
688
Absorptionskorrektur:
SADABS
Tmin; Tmax:
0.653; 0.746
2Θ-Bereich [°]:
5.2≤2Θ≤57.4
gemessene Reflexe:
27487
unabhängige Reflexe:
7544
R1; wR2:
0.0265; 0.0660
GooF F2:
1.042
143
5.1.2 Kristallstrukturdaten von [(η6-Benzol)dichloro(P5-deltacyclen)ruthenium(II)] 47
C10
C30
C25
C26
C1
P5
C3
C24
P2
P3
P4
C21
Ru
C4
C23
P1
C22
Cl1
C2
C40
H1
C20
Cl2
Summenformel:
C30H43Cl2P5Ru
Molmasse [g mol-1]:
754.53
Kristallfarbe, -form:
orangebraun, Block
Kristallgröße [mm]:
0.25×0.20×0.15
Meßtemperatur [K]:
150
Kristallsystem:
triklin
Raumgruppe:
P 1 (Nr. 2)
Kristalldaten:
a [Å] = 12.6517(7)
α [°]
= 105.755(5)
b [Å] = 15.5829(7)
β [°]
= 90.427(5)
c [Å] = 19.228(2)
γ [°]
= 105.758(5)
V [Å3] = 3497.7(4)
Z
=4
-3
Berechnete Dichte [g cm ]: 1.433
µ [mm-1]:
0.853
F(000):
1568
Absorptionskorrektur:
SADABS
Tmin; Tmax:
0.790; 0.880
2Θ-Bereich [°]:
6.7≤2Θ≤55.8
gemessene Reflexe:
100992
unabhängige Reflexe:
16658
R1; wR2:
0.0275; 0.0622
GooF F2:
1.033
144
5.1.3 Kristallstrukturdaten von Rhodium(III)-P5-deltacylcen-Zweikernkomplex 48
Cl1
P2
C4A
C1
P3
Rh1
C2A
P1A
C3
P5
C2
P1
P4A
P5A
Rh1A
C3A
P3A
P4
C1A
C4
P2A
Cl1A
Summenformel:
C52H74Cl2O3P10Rh2
Molmasse [g mol-1]:
1357.72
Kristallfarbe, -form:
rot, Block
Kristallgröße [mm]:
0.20×0.18×0.16
Meßtemperatur [K]:
150
Kristallsystem:
triklin
Raumgruppe:
P 1 (Nr. 2)
Kristalldaten:
a [Å] = 11.308(2)
α [°]
= 72.477(8)
b [Å] = 11.382(1)
β [°]
= 82.090(11)
c [Å] = 14.271(2)
γ [°]
= 61.136(8)
V [Å3] = 1533.9(3)
Z
=1
-3
Berechnete Dichte [g cm ]: 1.470
µ [mm-1]:
0.925
F(000):
708
Absorptionskorrektur:
SADABS
Tmin; Tmax:
0.623; 0.865
2Θ-Bereich [°]:
7.1≤2Θ≤54.2
gemessene Reflexe:
42602
unabhängige Reflexe:
6768
R1; wR2:
0.0380; 0.1034
GooF F2:
1.048
145
5.1.4 Kristallstrukturdaten von Molybdänpentacarbonyl-iso-P5-deltacyclen 50a
O1
O5
O2
C5
C9
C6
Mo
C8
C4
C7
O4
H1
P1
O3
C2
P2
P5
C1
P4
C3
P3
Summenformel:
C25H37MoO5P5
Molmasse [g mol-1]:
668.34
Kristallfarbe, -form:
gelb, Prisma
Kristallgröße [mm]:
0.24×0.23×0.16
Meßtemperatur [K]:
100
Kristallsystem:
triklin
Raumgruppe:
P 1 (Nr. 2)
Kristalldaten:
a [Å] = 10.4516(4)
α [°]
= 70.846(1)
b [Å] = 10.4791(4)
β [°]
= 83.241(1)
c [Å] = 15.8048(6)
γ [°]
= 65.658(1)
Z
=2
3
V [Å ] = 1489.5(1)
Berechnete Dichte [g cm-3]: 1.490
µ [mm-1]:
0.742
F(000):
688
Absorptionskorrektur:
SADABS
Tmin; Tmax:
0.690; 0.746
2Θ-Bereich [°]:
5.1≤2Θ≤55.8
gemessene Reflexe:
24699
unabhängige Reflexe:
6942
R1; wR2:
0.0270; 0.0621
GooF F2:
1.046
146
5.1.5 Kristallstrukturdaten von Chrompentacarbonyl-P5-homocunean 52
C30
C40
H1
C3
O1
C4
P1
P5
C5
P2
P4
C6
O4
O2
C1
C2
Cr
C20
C10
P3
C8
C9
C7
O5
O3
Summenformel:
C25H37CrO5P5
Molmasse [g mol-1]:
624.40
Kristallfarbe, -form:
blassgelb, Bruchstück
Kristallgröße [mm]:
0.32×0.16×0.14
Meßtemperatur [K]:
150
Kristallsystem:
orthorhombisch
Raumgruppe:
Pnma (Nr. 62)
Kristalldaten:
a [Å] = 17.184(2)
α [°]
= 90
b [Å] = 14.1150(8)
β [°]
= 90
c [Å] = 12.698(2)
γ [°]
= 90
Z
=4
3
V [Å ] = 3080.1(6)
Berechnete Dichte [g cm-3]: 1.347
µ [mm-1]:
0.663
F(000):
1304
Absorptionskorrektur:
SADABS
Tmin; Tmax:
0.786; 0.991
2Θ-Bereich [°]:
5.5≤2Θ≤56.0
gemessene Reflexe:
49485
unabhängige Reflexe:
3868
R1; wR2:
0.0287; 0.0822
GooF F2:
1.213
147
5.1.6 Kristallstrukturdaten von Molybdänpentacarbonyl-P5-homocunean 53
C30
H1
C40
C4
C3
P1
O1
P5
C5
P2
P4
C1
O2
C2
C6
P3
Mo
C10
C20
C9
C8
O5
O4
C7
O3
Summenformel:
C25H37MoO5P5
Molmasse [g mol-1]:
668.34
Kristallfarbe, -form:
blassgelb, Block
Kristallgröße [mm]:
0.52×0.30×0.22
Meßtemperatur [K]:
100
Kristallsystem:
orthorhombisch
Raumgruppe:
Pnma (Nr. 62)
Kristalldaten:
a [Å] = 17.139(8)
α [°]
= 90
b [Å] = 14.1193(2)
β [°]
= 90
c [Å] = 12.76650(10)
γ [°]
= 90
V [Å3] = 3089.52(6)
Z
=4
-3
Berechnete Dichte [g cm ]: 1.437
µ [mm-1]:
0.715
F(000):
1376
Absorptionskorrektur:
SADABS
Tmin; Tmax:
0.674; 0.746
2Θ-Bereich [°]:
4.3≤2Θ≤55.8
gemessene Reflexe:
57966
unabhängige Reflexe:
3834
R1; wR2:
0.0198; 0.0486
GooF F2:
1.086
148
5.1.7 Kristallstrukturdaten von Wolframpentacarbonyl-P5-homocunean 54
C30
H1
C40
C4
C3
P1
O1
P5
C5
P2
P4
C1
O2
C2
C6
P3
W
C8
C9
O5
C10
C20
O4
C7
O3
Summenformel:
C25H37O5P5W
-1
Molmasse [g mol ]:
756.25
Kristallfarbe, -form:
gelb, Block
Kristallgröße [mm]:
0.24×0.22×0.14
Meßtemperatur [K]:
100
Kristallsystem:
orthorhombisch
Raumgruppe:
Pnma (Nr. 62)
Kristalldaten:
a [Å] = 17.114(2)
α [°]
= 90
b [Å] = 14.098(2)
β [°]
= 90
c [Å] = 12.737(2)
γ [°]
= 90
V [Å3] = 3073.1(6)
Z
=4
Berechnete Dichte [g cm-3]: 1.635
µ [mm-1]:
4.051
F(000):
1504
Absorptionskorrektur:
SADABS
Tmin; Tmax:
0.579; 0.746
2Θ-Bereich [°]:
4.0≤2Θ≤59.3
gemessene Reflexe:
61206
unabhängige Reflexe:
4502
R1; wR2:
0.0128; 0.0316
GooF F2:
1.084
149
6. Literaturverzeichnis
[1]
[2]
[3]
[4]
[5]
[6]
[7]
[8]
[9]
[10]
[11]
[12]
[13]
[14]
[15]
[16]
[17]
[18]
[19]
[20]
[21]
[22]
[23]
[24]
[25]
[26]
[27]
[28]
[29]
[30]
[31]
[32]
[33]
[34]
[35]
[36]
[37]
[38]
[39]
150
T. E. Gier, J. Am. Chem. Soc. 1961, 83, 1769–1770.
G. Becker, Z. anorg allg Chem. 1976, 423, 242-254.
G. Becker, G. Gresser, W. Uhl, Z. Naturforsch.B 1981, 36b, 16-19.
W. Rösch, U. Hees, M. Regitz, Chem. Ber. 1987, 120, 1645-1652.
U. Annen, M. Regitz, Tetrahedron Lett. 1988, 29, 1681-1684.
E. H. Braye, I. Caplier, R. Saussez, Tetrahedron 1971, 27, 5523-5537.
N. Maigrot, N. Avarvari, C. Charrier, F. Mathay, Angew. Chem. Int. Ed. Engl. 1995, 34, 590-592.
A. H. Cowley, S. W. Hall, Polyhedron 1989, 8, 849-850.
R. Bartsch, J. F. Nixon, Polyhedron 1989, 8, 2407.
N. Maigrot, L. Ricard, C. Charrier, F. Mathay, Angew. Chem. Int Ed. Engl. 1990, 29, 534-535.
M. L. Sierra, N. Maigrot, C. Charrier, L. Ricard, F. Mathay, Organometallics 1992, 11, 459-462.
M. Baudler, D. Düster, D. Ouzounis, Z. Anorg. Allg. Chem. 1987, 544, 87-94.
M. Baudler, J. Hahn, Z. Naturforsch. B 1990, 45b, 1139-1142.
N. Maigrot, M. L. Sierra, C. Charrier, L. Ricard, F. Mathay, Bull. Soc. Chim. Fr. 1994, 131, 397.
G. Becker, W. Becker, R. Knebl, H. Schmidt, U. Weber, M. Westerhausen, Nova Acta Leopold 1985,
59, 55-67.
M. Baudler, T. Etzbach, Chem. Ber. 1991, 124, 1159-1160.
A. Elvers, Dissertation, FAU Erlangen-Nürnberg 1998.
A. Elvers, F. W. Heinemann, B. Wrackmeyer, U. Zenneck, Chem. Eur. J. 1999, 5, 3143-3153.
M. Hofmann, Dissertation, FAU Erlangen-Nürnberg 2002.
M. Hofmann, C. Höhn, F. W. Heinemann, U. Zenneck, Chem. Eur. J. 2009, 15, 5998-6007.
M. Birkel, J. Schulz, U. Bergsträßer, M. Regitz, Angew. Chem., Int. Ed. Engl. 1992, 31, 879-882.
V. Caliman, P. B. Hitchcock, C. Jones. J. F. Nixon, Phosphorus, Sulfur Silicon Relat. El. 1996, 113, 1537.
R. Bartsch, P. B. Hitchcock, J. F. Nixon, J. Organomet. Chem. 1989, 375, C31-C34.
D. Hu, H. Schäufele, H. Pritzkow, U. Zenneck, Angew. Chem. Int. Ed. Eng.. 1989, 28, 900-902.
C. Peters, F. Tabellion, A. Nachbauer, U. Fischbeck, F. Preuss, M. Regitz, Z. Naturforsch. 2001, 56b,
951-962.
A. Hoffmann, S. Leininger, M. Regitz, J. Organomet. Chem. 1997, 539, 61-66.
M. M. Al-Ktaifani, P. B. Hitchcock, J. F. Nixon, Dalton Trans. 2008, 9, 1132–1135.
M. M. Al-Ktaifani, W. Bauer, U. Bergsträßer, B. Breit, M. D. Francis, F. W. Heinemann, P. B.
Hitchcock, A. Mack, J. F. Nixon, H. Pritzkow, M. Regitz, M. Zeller, U. Zenneck, Chem. Eur. J. 2002,
8, 2622-2633.
M. M. Al-Ktaifani, P.B. Hitchcock, M.F. Lappert, J.F. Nixon, P. Uiterweerd, Dalton Trans. 2008, 21,
2825.
M. Julino, M. Slany, U. Bergsträßer, F. Merqier, F. Mathey, M. Regitz, Chem. Ber. 1995, 128, 991-997.
T. Wettling, J. Schneider, O. Wagner, C. G. Kreiter, M. Regitz, Angew. Chem. Int. Ed. Engl. 1989, 28,
1013-1014.
P. B. Hitchcock, C. Jones, J. F. Nixon, J. Chem. Soc., Chem. Commun. 1995, 2167-2168.
C. Jones, C. Schulten, A. Stasch, Dalton Trans. 2007, 19, 1929-1933.
I. Keller, einzureichende Dissertation.
S. Huguet-Torell, einzureichende Dissertation.
C. Höhn, einzureichende Dissertation.
A. D Becke, J. Phys. Chem. 1993, 97, 5648-5652; C. Lee, W. Yang, R.G. Parr, Phys. Rev. B 1988, 37,
785-789; P.J. Stephens, F.J. Devlin, C.F. Chabalowski, M.J. Frisch, J.Phys.Chem. 1994, 98, 1162311627.
M. J. Frisch, G. W. Trucks, H. B. Schlegel, G. E. Scuseria, M. A. Rob, J. R. Cheeseman, J. A.
Montgomery Jr., T. Vreven, K. N. Kudin, J. C. Burant, J. M. Millam, S. S. Iyengar, J. Tomasi, V.
Barone, B. Mennucci, M. Cossi, G. Scalmani, N. Rega, G. A. Petersson, H. Nakatsuji, M. Hada, M.
Ehara, K. Toyota, R. Fukuda, J. Hasegawa, M. Ishida, T. Nakajima, Y. Honda, O. Kitao, H. Nakai, M.
Klene, X. Li, J. E. Knox, H. P. Hratchian, J. B. Cross, V. Bakken, C. Adamo, J. Jaramillo, R. Gomperts,
R. E. Stratmann, O. Yazyev, A. J. Austin, R. Cammi, C. Pomelli, J. W. Ochterski, P. Y. Ayala, K.
Morokuma, G. A. Voth, P. Salvador, J. J. Dannenberg, V. G. Zakrzewski, S. Dapprich, A. D. Daniels,
M. C. Strain, O. Farkas, D. K. Malick, A. D. Rabuck, K. Raghavachari, J. B. Foresman, J. V. Ortiz, Q.
Cui, A. G. Baboul, S. Clifford, J. Cioslowski, B. B. Stefanov, G. Liu, A. Liashenko, P. Piskorz, I.
Komaromi, R. L. Martin, D. J. Fox, T. Keith, M. A. Al-Laham, C. Y. Peng, A. Nanayakkara, M.
Challacombe, P. M. W. Gill, B. Johnson, W. Chen, M. W. Wong, C. Gonzalez, and J. A. Pople,
Gaussian 03; Revision C.02, Gaussian, Inc., Wallingford, CT, 2004.
M. Baudler, F. Saykowski, Z. anorg. allg. Chem. 1982, 486, 39-44.
[40]
[41]
[42]
[43]
[44]
[45]
[46]
[47]
[48]
[49]
[50]
[51]
[52]
[53]
[54]
[55]
[56]
[57]
[58]
[59]
[60]
[61]
[62]
[63]
[64]
[65]
[66]
[67]
[68]
[69]
[70]
M. Baudler, E. Saykowski, Z. Naturforsch. B 1978, 33b, 1208-1213.
K. Marat, Spinworks 3.1.7, University of Manitoba, 2010.
E.G. Finer, R.K Harris, Chem. Commun. (London) 1968, 110-112.
M. Yoshifuji, S. Sasaki, N. Inamoto, J. Chem. Soc,. Chem. Commun. 1989, 1732-1733.
M. Karplus, J. Chem. Phys. 1959, 30, 11-15.
M. Karplus, J. Am. Chem. Soc. 1963, 85, 2870-2871.
L. Evelyn, L. D. Hall, P. R. Steinert, D. H. Stokes, Org. Magn. Resonance 1973, 5, 141-145.
C. Benezra, J. Am. Chem. Soc. 1973, 21, 6890-6894.
A. Bader, M. Pabel, A. C. Willis, S. B. Wild, Inorg. Chem. 1996, 35, 3874-3877.
J. Albert, J. M. Cadena, J. Granell, G. Muller, D. Panyella, C. Sañudo, Eur. J. Inorg. Chem. 2000, 6,
1283-1286.
N. V. Dubrovina, H. Jiao., V. I. Tararov, A. Spannenberg, R. Kadyrov, A. Monsees, A. Christiansen, A.
Börner, Eur. J. Org. Chem. 2006, 15, 3412–3420.
O. Kühl, Phosphorous-31 NMR Spectroscopy, Springer-Verlag, Berlin Heidelberg 2008.
L. Rohwer, Diplomarbeit, FAU Erlangen-Nürnberg 2004.
P. Pinto, G. Marconi, F. W. Heinemann, U. Zenneck, Organometallics 2004, 23, 374-380.
S. I. M. Paris, F. R. Lemke, R. Sommer, P. Lönnecke, E. Hey-Hawkins, J. Organomet. Chem. 2005,
690, 1807-1813.
I. Moldes, E. de la Encarnación, J. Ros, A. Alvarez-Larena, J. F. Piniella, J. Organomet. Chem.1998,
566, 165-174.
R. de Vaumas, A. Marinetti, L. Ricard, F. Mathey, J. Am. Chem. Soc. 1992, 114, 261-266.
N. Berova, L. Di Bari, G. Pescitelli, Chem. Soc. Rev. 2007, 36, 914-931.
B. Le Guennic, W. Hieringer, A. Görling, J. Autschbach, J. Phys. Chem. A 2005, 109, 4836-4846.
J. A. Osborn, F. H. Jardine, J. F. Young, G. Wilkinson, J. Am. Chem. Soc. A 1966, 1711-1732.
J. Wassenaar, B. de Bruin, M. A. Siegler, A. L. Spek, J. N. H. Reek, J. I. van der Vlugt, Chem.
Commun. 2010, 46, 1232–1234.
D. J. Darensbourg, N. W. Stafford, F. Joó, J. H. Reibenspies, J. Organomet. Chem. 1995, 488, 99-108.
D. Penno, I. O. Koshevoy, F. Estevan, M. Sanaú, M. A. Ubeda, J. Pérez-Prieto, Organometallics 2010,
29, 703–706.
K. Raghuraman, N. Pillarsetty, W. A. Volkert, C. Barnes, S. Jurisson, K. V. Katti, J. Am. Chem. Soc.
2002, 124, 7276–7277.
T. Suzuki, K. Isobe, K. Kashiwabara, J. Fujita, S. Kaizaki, J. Chem. Soc., Dalton Trans. 1996, 37793786.
P. G. Edwards, J. S. Fleming, S. J. Coles, M. B. Hursthouse, J. Chem. Soc., Dalton Trans. 1997, 32013206.
D. Fenske, H. Schottmüller, Z. anorg. allg. Chem. 1998, 624, 443-451.
F. A. Ajulu, D. Carmichael, P. B. Hitchcock, F. Mathey, M. F. Meidine, J. F. Nixon, L. Ricard, M. L.
Riley, J. Chem. Soc., Chem. Commun. 1992, 750-752.
D. Yakhvarov, P. Barbaro, L. Gonsalvi, S. M. Carpio, S. Midollini, A. Orlandini, M. Peruzzini, O.
Sinyashin, F. Zanobini , Angew. Chem. Int. Ed. 2006, 45, 4182 –4185.
J. Duran, D .Oliver, A. Polo, J. Real, J. Benet-Buchholz, X. Fontrodona, Tetrahedron: Asymmetry 2003,
14, 2529–2538.
M. Green, C. L. McMullin, G. J. P. Morton, A. G. Orpen, D. F. Wass, R. L. Wingad, Organometallics
2009, 28, 1476-1479.
[71]
[72]
[73]
[74]
[75]
[76]
[77]
[78]
[79]
[80]
[81]
[82]
[83]
[84]
A. C. Skapski, F. A. Stephens, J. Chem. Soc., Dalton Trans. 1973, 1789-1793.
S. J. Geier, D. W. Stephan, Chem. Commun. 2008, 2779–2781.
S.Gomez-Ruiz, R.Wolf, E.Hey-Hawkins, Dalton Trans. 2008, 1982–1988.
S. D. Timpa, C. M. Fafard, D. E. Herbert, O. V. Ozerov, Dalton Trans. 2011, 40, 5426–5429.
A. Schisler, P. Lönnecke, E. Hey-Hawkins, Inorg. Chem. 2005, 44, 461-464.
A. Schisler, P. Lönnecke, U. Huniar, R. Ahlrichs, E. Hey-Hawkins, Angew. Chem. Int. Ed. Engl. 2001,
40, 4217-4219.
J. Wassenaar, M. A. Siegler, A. L. Spek, B. de Bruin, J. N. H. Reek, J. I. van der Vlugt, Inorg. Chem.
2010, 49, 6495–6508.
A. Vigalok, O. Uzan, L. J. W. Shimon, Y. Ben-David, J. M. L. Martin, D. Milstein, J. Am. Chem. Soc.
1998, 120, 12539-12544.
C. Höhn, Diplomarbeit, FAU Erlangen-Nürnberg 2008.
M. Hofmann, unveröffentliche Ergebnisse.
P. E. Eaton, L. Cassar, J. Halpern, J. Am. Chem. Soc. 1970, 92, 6366–6368.
D. D. Perrin W. L. F. Armarego, Purification of Laboratory Chemicals, 3rd Edition, ButterworthHeinemann-Ltd., Oxford, 1994.
R. B King, N. D. Sadanani, Syn. React. Inorg. Met. 1984, 15, 149-153.
E. Nieke, H. Westermann, Synthesis 1988, 4, 330.
151
[85]
[86]
[87]
[88]
[89]
[90]
152
W. A. Herrmann, G. Brauer, H. H. Karsch, Synthetic Methods of organometallic and Inorganic
Chemistry, Vol.3, Thieme Verlag, Stuttgart New York 1996, 11.
Der Wert der Elementaranalyse wurden entnommen aus: M. Hofmann, C. Höhn, F. W. Heinemann, U.
Zenneck, Chem. Eur. J. 2009, 15, 5998-6007.
Der Wert der FD-Masse wurde entnommen aus: S. Huguet-Torell einzureichende Dissertation.
Die Werte der FD-Masse und Elementaranalyse wurden entnommen aus: S. Huguet-Torell
einzureichende Dissertation.
Die Werte der FD-Masse und Elementaranalyse wurden entnommen aus: S. Huguet-Torell
einzureichende Dissertation.
Der Wert der Elementaranalyse wurden entnommen aus: I. Keller einzureichende Dissertation.



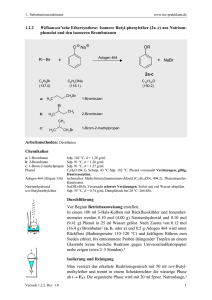
![6.3.1 1-Oxa-spiro[2.5]octan - Institut für Organische Chemie](http://s1.studylibde.com/store/data/001356875_1-96e669e5c88ad586db9f9f199d424d05-300x300.png)






