Die Molekül - Department Chemie und Biologie
Werbung

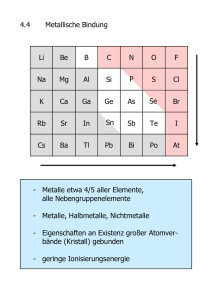
Vorlesung Anorganische Chemie I im WS 2006/7 (Teil 3) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien einer Grundvorlesung zur Anorganischen Chemie aus dem Institut für Anorganische Chemie der Universität Bonn sowie des Buches „Allgemeine und Anorganische Chemie“, Binnewies u.a., Spektrum Verlag) Grundlegende Aspekte von Molekül- und Kristallstrukturen -Das VSEPR Modell - Kristallographische und kristallchemische Grundbegriffe -Dichte Kugelpackungen - Lücken in dichten Kugelpackungen -Wichtige Strukturtypen von kristallinen Feststoffen Das VSEPR Modell (Valence Shell Elektron Pair Repulsion) - Verteilung der Bindungselektronenpaare und einsamen Elektronenpaare (vollständige Lewis-Formel !) um ein Zentralatom herum auf einer Kugeloberfläche in maximalem Abstand voneinander Das VSEPR Modell Die Molekül- und Kristallstrukturen der Elemente Kugelpackungen von Einzelatomen, Besonderheiten z.B. bei Ga, Fe, Mn ... alle anderen: 1-, 2- oder 3-dimensionale Molekülstrukturen (manchmal bilden die Moleküle selbst wieder Kugelpackungen) Das Prinzip der dichten Kugelpackungen Prinzip: möglichst dichte räumliche Packung der Atome oder Moleküle Primitive Packung Dichte Packung Raumerfüllung: 74% ! Das Prinzip der dichten Kugelpackungen Hexagonal dichte Kugelpackung: Stapelfolge ABABAB... Elementarzelle (verschiedene Möglichkeiten!) Das Prinzip der dichten Kugelpackungen Kubisch dichte Kugelpackung: Stapelfolge ABCABCABC ... A C B A Das Prinzip der dichten Kugelpackungen Elementarzelle und Stapelrichtung der Schichten bei der kubisch dichten Kugelpackung Das Prinzip der dichten Kugelpackungen Koordinationszahl für alle dichten Kugelpackungen CN = 12 Das Prinzip der dichten Kugelpackungen Elementarzelle und Raumerfüllung am 2-dim. Modell Das Prinzip der dichten Kugelpackungen Anteil des Kugelvolumens im Inneren der Elementarzelle ? → Raumerfüllung = (n VKugel) / VElementarzelle → Bedingung: Kugeln berühren sich und sind gleich groß → Raumerfüllung ist ~74% bei allen dichten Kugelpackungen Das Prinzip der dichten Kugelpackungen HCP (Be, Mg, Zn, Cd, Ti, Zr, Ru ...) Raumerfüllung = 74% CCP (Cu, Ag, Au, Al, Ni, Pd, Pt ...) Kubisch raumzentrierte Kugelpackung (keine dichte Kugelpackung) bcc Raumerfüllung ~ 68% Koordinationszahl (CN) = 8 + 6 z.B. Fe, Cr, Mo, W, Ta, Ba ... Kristallsysteme Elementarzelle - Basisvektoren – Gitterkonstanten - Rechtshändigkeit Wichtige Molekül- und Kristallstrukturen von Elementen Symmetrieelemente, Punktgruppen, Kristallklassen !! Die Strukturchemie des Elementes Bor wird von B12Molekülen mit Ikosaederstruktur dominiert Das Ikosaeder ist eines der fünf platonischen Polyeder: - Tetraeder - Oktaeder - Würfel - Ikosaeder - Pentagondodekaeder Das Ikosaeder ist durch eine große Zahl von Symmetrieelementen gekennzeichnet und eine ideale Struktur für Moleküle, die aus Atomen mit einer geringen Zahl von Valenzelektronen bestehen. Anordnung von B12-Ikosaedern mit der Topologie einer dichtesten Kugelpackung im tetragonalen Bor-T50 (Z=50) Es gibt zahlreiche (> 20) Modifikationen des Elementes Bor, die teilweise durch geringe Verunreinigungen stabilisiert sind Graphit, Diamant, Fulleren (C60) : 3 Modifikationen des Elementes Kohlenstoff Graphit Diamant Fulleren (C60) „Buckminsterfulleren“ R. Buckminster-Fuller (Architekt) H.W. Kroto, R.E. Smalley N.P. Chemie (1996) B12-Ikosaeder im Inneren eines B60-Käfigs mit der Topologie des Fullerenmoleküls (Bor-R105) Symmetrieverwandtschaft zwischen Ikosaeder und Fulleren Die Elemente Si und Ge kristallisieren in der Diamantstruktur Weißer Phosphor besteht aus tetraederischen P4 - Molekülen metastabil, reaktiv, gespannte Bindungen 2,3 Å Andere Phosphormodifikationen (schwarzer P, roter P, violetter P) besitzen einen komplizierten Aufbau ohne P4 – Moleküle; die P-Atome sind aber in allen Modifikationen dreibindig ! Die Struktur des schwarzen Phosphors P (schwarz): a=3.314 Å, b=10.478 Å, c=4.376 Å Z = 8, Cmca - gewellte Schichten von dreibindigen P-Atomen thermodynamisch stabil !! van der WaalsBindung Molekül- und Kristallstruktuktur von α-Schwefel Das kronenförmige S8 - Molekül Räumliche Anordnung der S8 Moleküle im orthorhombischen α-Schwefel Selen und Tellur bilden vorzugsweise eindimensionale ketten(schrauben)förmige Moleküle N2, O2 und die Halogene bilden im festen Zustand Molekülgitter bei denen die Anordnung der Molekülschwerpunkte häufig verzerrten Kugelpackungen entspricht Kristallstruktur von Iod Wichtige (groß-)technische Verfahren zur Gewinnung von Elementen 1. Alkali- und Erdalkalimetalle: - Wegen der ausgeprägten Reaktivität gegenüber Sauerstoff und Wasser spezielle Verfahren meist unter Schutzgas z.B. Schmelzflußelektrolyse (Mg, Na), Hochtemperaturdestillation (Ba, Rb, Cs) 2. Aluminium: - Ausgangsstoffe sind die natürlichen Mineralien Korund (α-Al2O3) und Bauxit (AlO(OH) + Fe-Oxide, Ti-Oxid ...) Bayer-Verfahren: a) Bauxit/Korund + heiße NaOH AlO(OH) + OH- + H2O → [Al(OH)4]- (in Lösung) b) Abkühlen der Lösung 2[Al(OH)4]- + 2H+ → Al2O3↓ + 5H2O Schmelzflußelektrolyse von Al2O3/Kryolith (Graphitanode) Al2O3 + 3C → 2Al + 3CO↑ (ca. 930 0C, Eutektikum mit Kryolith,20% Al2O3) Verhalten von Al(OH)3 in wässriger Lösung 4. Kohlenstoff: a) Graphit: natürliche Lagerstätten (China ...), auch künstlich durch „Pyrolyse“ von C-Verbindungen bei sehr hoher Temperatur b) Fulleren: Graphitoberfläche mit Hochenergielaser bestrahlen (T > 10.000 K) c) Ruß: technisches Produkt durch unvollständige Verbrennung von Kohlenwasserstoffen (keine eigenständige C-Modifikation) d) Diamant: → Graphit auf T ~ 1500 0C und 50 kbar → CH4 in Plasmaentladung thermisch zersetzen (Diamantschichten) Hochdruck/-temperatursynthese von Diamant Diamantschichten durch Abscheidung aus der Gasphase 5. Technische Darstellung von Roh-Silicium SiO2 + 2C → Si + 2CO (Lichtbogen) Anschließend Verarbeitung zu Reinst-Silicium Das flüssige SiHCl3 wird destilliert und thermisch zersetzt: Si + 3HCl → SiHCl3 + H2 2SiHCl3 → Si + H2 + 3Cl2 5a. Reinst-Silicium → Große Einkristalle → Scheiben („wafer“) werden aus einer Si-Schmelze „gezogen“ Tiegelziehen Für Anwendungen in der Solar- und Halbleitertechnik wird das Silicium anschließend mit „Dotierstoffen“ (meist Elemente aus der 3. und 5. Hauptgruppe) wieder gezielt verunreinigt („Dotierung“) 6. Großtechnische Phosphorgewinnung Die technische Herstellung von weißem Phosphor erfolgt aus natürlich vorkommenden Phosphaten (z.B. Apatit) durch Reduktion mit Koks unter Beimengung von Quarzsand im elektrischen Lichtbogen bei ca. 1400°C 1542 kJ + Ca 3(PO4)2 + 3 SiO2 + 5 C -----> P2↑ + 3 CaSiO3 + 5 CO 7. Linde Verfahren zur Verflüssigung von Luft 1. Mehrstufige Kompression mit anschließender adiabatischer*) Expansion nach dem Gegenstromprinzip (Joule-Thomson-Effekt**)) 2. Tieftemperaturdestillation *) adiabatisch: ohne Wärmeaustausch mit der Umgebung **) J-T-Effekt: Reale Gase kühlen sich bei Expansion ab (Voraussetzung: T < TInversion) 8. Schwefel-Gewinnung nach dem Frasch-Verfahren: Elementarer Schwefel wird durch überhitztes Wasser aus dem Gestein heraus zur Oberfläche gepresst. 9. Chloralkalielektrolyse zur Gewinnung von H2, Cl2 und NaOH s. Diagramme: Chlor und NaOH 10. - Rohgold wird direkt aus goldhaltigem Erdreich durch Auflösen in NaCN-Lösung in Gegenwart von Luft (!) angereichert (Au geht dabei als komplexes Cyanid [Au(CN)2]1- in Lösung) - Reingold: Rohgold wird anodisch aufgelöst und kathodisch wieder als reines Gold abgeschieden (Spannungsreihe !); Silber ähnlich ! 11a. Elektroschmelze zur Gewinnung von Stahl aus Schrott z.B. Deutsche Edelstahlwerke Siegen-Geisweid 11b. Hochofenprozeß zur Gewinnung von Roheisen → Stahl Stahlerzeugung: - Reduktion des C-Gehaltes auf < 1%, - Reduktion des Gehaltes an störenden Begleitelementen (P, Si usw.) durch Frischen, Desoxidation, Entschwefelung. → Eisenoxidhaltige Schlacke - Entfernung des im flüssigen Fe gelösten Sauerstoffs