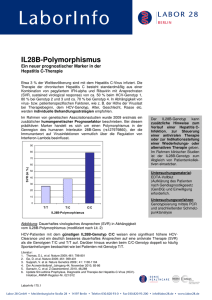
Beurteilung des antiviralen Therapieverlaufs der Hepatitis C
Werbung

Universitätsklinikum Ulm Zentrum für Innere Medizin Klinik für Innere Medizin I Kommissarischer Ärztlicher Direktor: Prof. Dr. Götz von Wichert Beurteilung des antiviralen Therapieverlaufs der Hepatitis C-Infektion anhand seriell erhobener Laborparameter Dissertation zur Erlangung des Doktorgrades der Medizin der Medizinischen Fakultät der Universität Ulm vorgelegt von Anna Katrin Merz, geb. Schultheiß aus Blaubeuren Amtierender Dekan: Prof. Dr. Thomas Wirth 1. Berichterstatter: PD Dr. Michael Fuchs 2. Berichterstatter: PD Dr. Martin Bommer Tag der Promotion: 15.06.2012 Diese Arbeit ist meinem Ehemann Andreas und meinen Eltern in Liebe und Dankbarkeit gewidmet Inhaltsverzeichnis Inhaltsverzeichnis 1 Abkürzungsverzeichnis ......................................................................................... III 2 Einleitung ............................................................................................................. 1 3 2.1 Epidemiologie, Prävention und Übertragungswege .................................................. 1 2.2 Diagnostik der HCV Infektion ................................................................................... 3 2.3 HCV-Genotypen ....................................................................................................... 6 2.4 Krankheitsverlauf und Folgekomplikationen der Hepatitis C ..................................... 7 2.5 Therapie der chronischen Hepatitis C ....................................................................... 9 2.6 Fragestellung der Doktorarbeit .............................................................................. 11 Material und Methoden ...................................................................................... 13 3.1 Patientenkollektiv ................................................................................................. 13 3.2 Therapiedauer, Medikamente und deren Dosierung mit ggf. Dosisanpassung ......... 14 3.3 Therapiedurchführung und Beurteilung des Therapieerfolges, d.h. Erfassung des Ansprechens...................................................................................................................... 16 4 3.4 Ein- und Ausschlusskriterien .................................................................................. 17 3.5 Laborparameter, Ratios, Histologie, Genotypisierung ............................................. 19 3.5.1 Laborparameter und Ratios/Scores ........................................................................... 19 3.5.2 Histologie .................................................................................................................... 20 3.5.3 Genotypisierung ......................................................................................................... 21 3.6 Datenerhebung ..................................................................................................... 22 3.7 Statistik ................................................................................................................. 22 Ergebnisse .......................................................................................................... 24 4.1 Verlauf der laborchemischen Parameter unter Therapie und Aufgliederung in Genotypen ........................................................................................................................ 25 4.1.1 Verlauf der Leukozytentiter unter Therapie............................................................... 25 4.1.2 Verlauf der Erythrozytentiter unter Therapie ............................................................ 26 4.1.3 Verlauf der Hämoglobinkonzentration unter Therapie.............................................. 27 4.1.4 Verlauf der Thrombozytentiter unter Therapie ......................................................... 28 4.1.5 Verlauf der Bilirubinkonzentration unter Therapie.................................................... 29 4.1.6 Verlauf der AST-Konzentration unter Therapie.......................................................... 30 4.1.7 Verlauf der ALT-Konzentration unter Therapie .......................................................... 31 4.1.8 Verlauf der GGT-Konzentration unter Therapie ......................................................... 32 4.1.9 Verlauf des APRI Score unter Therapie ...................................................................... 34 I Inhaltsverzeichnis 4.1.10 4.2 Verlauf der HCV-RNA unter Therapie .................................................................... 34 Verlauf der laborchemischen Parameter unter Therapie und Aufgliederung in Interferon-alphacon 1 und Peginterferon-α2b .................................................................... 36 4.2.1 Verlauf der Erythrozyten und Leukozyten unter Therapie......................................... 36 4.2.2 Verlauf des Hämoglobins unter Therapie................................................................... 37 4.2.3 Verlauf der Thrombozyten unter Therapie ................................................................ 38 4.2.4 Verlauf des Bilirubins gesamt unter Therapie ............................................................ 39 4.2.5 Verlauf der AST und ALT unter Therapie .................................................................... 40 4.2.6 Verlauf der GGT unter Therapie ................................................................................. 41 4.2.7 Verlauf des AST:ALT Verhältnisses unter Therapie .................................................... 42 4.2.8 Verlauf des APRI Score unter Therapie ...................................................................... 43 4.2.9 Verlauf der HCV-RNA unter Therapie ......................................................................... 44 4.3 Verlauf anderer wichtiger klinischer Parameter unter Therapie und Aufgliederung in Genotypen ........................................................................................................................ 45 4.3.1 Grad der Fibrose (Staging) .......................................................................................... 45 4.3.2 Auftreten einer Steatose ............................................................................................ 46 4.3.3 Grad der Entzündung (Grading) ................................................................................. 46 4.3.4 Anteil der Non-Responder .......................................................................................... 47 4.3.5 Häufigkeit des Relapse ............................................................................................... 48 4.3.6 Ausheilungsraten nach Genotyp ................................................................................ 49 4.4 Verlauf anderer wichtiger klinischer Parameter unter Therapie und Aufgliederung in Interferon-alphacon 1 und Peginterferon-α2b .................................................................... 50 4.4.1 Anteil der Non-Responder .......................................................................................... 50 4.4.2 Relapsehäufigkeit ....................................................................................................... 51 4.4.3 Ausheilungsraten nach Therapie ................................................................................ 52 4.4.4 Ausheilungsrate unter Berücksichtigung der einzelnen Nadirwerte ......................... 53 4.5 Verlauf ausgewählter laborchemischer Parameter unter Aufgliederung nach Therapieansprechen und Zusammenfassung von GT1/4 und GT2/3 .................................... 56 4.5.1 Verlauf der Leukozytentiter........................................................................................ 56 4.5.2 Verlauf der Hämoglobinkonzentration....................................................................... 58 4.5.3 Verlauf der Thrombozytentiter .................................................................................. 60 5 Diskussion........................................................................................................... 62 6 Zusammenfassung .............................................................................................. 78 7 Literaturverzeichnis ............................................................................................ 80 II Abkürzungsverzeichnis 1 Abkürzungsverzeichnis AFP Alpha-1-Fetoprotein ALT Alaninaminotransferase APRI AST- to- Platelet- Ratio Index AST Aspartataminotransferase EIA Enzymimmunoassay Ery Erythrozyten GGT Gamma- Glutamyl-Transferase Hb Hämoglobin HBV Hepatitis B Virus HCV Hepatitis C Virus HIV Humanes Immundefizienzvirus INR International Normalized Ratio I.E. Internationale Einheiten i.v. Intravenös l Liter Leuko Leukozyten ng, µg, etc. Nanogramm, Mikrogramm, etc. PCR Polymerase chain reaction (Polymerasekettenreaktion) PEG Polyethylenglykol RIBA Rekombinanter Immunoblot Assay RNA Ribonucleic acid (Ribonukleinsäure) s.c. Subkutan SVR Sustained Virological Response (Ausheilungsrate) tgl. Täglich Thrombo Thrombozyten TSH Thyroideastimulierendes Hormon WHO Weltgesundheitsorganisation III Einleitung 2 Einleitung 2.1 Epidemiologie, Prävention und Übertragungswege Heute sind weltweit etwa 170 Millionen Menschen chronisch mit dem Hepatitis C Virus infiziert. Nach Angaben des Robert Koch-Institutes traten im Jahr 2009 5.412 Neuinfektionen in Deutschland auf, wobei seit 2005 eine tendentielle Senkung der jährlichen Inzidenz zu erkennen ist [40]. Geographisch gibt es starke Unterschiede hinsichtlich der Prävalenzdaten wie Abbildung 1 zeigt. So weisen einige afrikanische, sowie südamerikanische Staaten und Gebiete aus dem Fernen Osten erhöhte Hepatitis C Virus Prävalenzen auf, wohingegen Europa, Nordamerika, die westlichen Teile Asiens und Australien eine geringfügige Verbreitung des Hepatitis C Virus zeigen. Abbildung 1. Weltweite Prävalenz von Hepatitis C Virus-Infektionen im Jahre 2007 [52]. Nach dessen Entdeckung im Jahre 1989 konnten die vormals als Non-A, Non-B bezeichneten Hepatitiden endgültig genauer definiert werden. Da das Hepatitis C Virus häufigste Ursache der Posttransfusionshepatitis darstellte, konnte diese nach Testung aller Blutkonserven stark reduziert werden. So wird laut WHO aktuell eine 1 Einleitung Übertragungswahrscheinlichkeit einer Hepatitis C Infektion durch ein infiziertes Blutpräparat mit 1: 4,2 Millionen angegeben [40]. Das Hepatitis C Virus wird auf parenteralem Wege übertragen- hauptsächlich durch das Eindringen von HCV-infizierten Blutbestandteilen in die Blutbahn. Obwohl geringe Mengen HCV-RNA in Körperflüssigkeiten wie Tränen, Speichel, Schweiß, Muttermilch und Samenflüssigkeit gefunden werden konnten, geht man nicht davon aus, dass diese einen weiteren potentiellen Übertragungsweg darstellen. Als mögliche und nicht auszuschließende Übertragungswege gelten heutzutage jedoch unter anderem Tätowierungen, Piercings und Akupunktur. Abbildung 2 zeigt die Aufgliederung der möglichen Übertragungswege des Hepatitis C Virus nach deren prozentualem Vorkommen. Von den bekannten Risikogruppen nehmen die i.v. Drogenkonsumenten den Hauptteil bei der Inzidenz einer Hepatitis C Infektion ein. Hauptrisiko hierbei ist das sog. “needlesharing“, der Austausch von Nadeln oder Spritzen unter Drogenabhängigen. Weitere Übertragungswege sind kontaminierte Blutprodukte, Transplantate, nosokomiale Infektionen (z.B. Operationen oder Hämodialyse), sowie die vertikale Mutter-Kind Transmission. Unklar bleibt der hohe Anteil von 30% an sog. sporadischen Infektionen mit Hepatitis C, bei denen zum Zeitpunkt der Diagnosestellung nicht mehr sicher nachvollziehbar ist, über welchen Übertragungsweg die Infektion entstand [44]. 2 Einleitung Abbildung 2. Übertragungswege des Hepatitis C Virus. HCV wird ausschließlich parenteral übertragen (Centers for Disease Control and Prevention-CDC 2010). 2.2 Diagnostik der HCV Infektion Bei auffälliger Anamnese, sowie klinischen Zeichen einer Hepatitis oder chronischen Lebererkrankung und pathologischen laborchemischen Parametern (v.a. Erhöhung der Transaminasen) sollte eine Diagnostik auf eine HCV Infektion durchgeführt werden [1]. Die serologische Diagnostik erfolgt hierbei durch den Nachweis von HCV Antikörpern (Anti-HCV) mittels eines Enzymimmunoassays der 3. Generation (EIA3). Dieser Assay ist hochspezifisch und -sensitiv (89-99%) [9]. Bei begründetem Zweifel an einem positiv ausgefallenen Anti-HCV Test – wenn beispielsweise die Leberwerte eines Patienten im Normbereich liegen und dieser keine Riskofaktoren aufweist, bedarf es eines Bestätigungstestes (z.B. Rekombinanter Immunoblot Assay (RIBA) II). Ansonsten erfolgt als nächstes die molekulargenetische Diagnostik, die auf dem qualitativen Nachweis von HCV-RNA durch Polymerase chain reaction (PCR) beruht. Die Sensitivität des Viruslastnachweises per RT-PCR liegt standardmäßig bei 30-50 IU/ml. Liegt die Viruslast eines Patienten unterhalb dieser Nachweisgrenze, so ist er HCV-RNA negativ, liegt er oberhalb so ist er HCV-RNA positiv [43]. Fällt bei einem Patienten der qualitative HCVRNA Nachweis mittels PCR positiv aus, so ist von einer replikativen Hepatitis C Virusinfektion auszugehen und es erfolgt dann eine Genotypisierung sowie eine quantitative HCV-RNA Bestimmung [36]. 3 Einleitung Im frühen Stadium einer akuten Hepatitis C Infektion können noch keine virusspezifischen Antikörper detektiert werden; sie sind erst 7-8 Wochen nach der Infektion nachweisbar. Man spricht hierbei auch von einem “serodiagnostischen Fenster“. Da die HCV-RNA jedoch bereits 1-2 Wochen nach der Infektion nachgewiesen werden kann, sollte stets eine HCV-RNA Bestimmung erfolgen, um die durch fehlende Detektierbarkeit von HCV Antikörpern zu Beginn einer Infektion entstehende diagnostische Lücke, zu umgehen. Eine zusätzliche quantitative Bestimmung der HCV-RNA dient der Beurteilung des Therapieerfolges. Jedoch zeigt auch der HCV-RNA Nachweis mittels PCR Nachteile. Diese bestehen v.a. in der generell mangelnden Vergleichbarkeit der einzelnen Tests und einer fehlenden Standardisierung. Auch nach Festlegung zweier WHO-HCV-RNA Standards bleibt dies schwierig [1]. Ebenso ist das Durchführen einer quantitativen PCR recht kostspielig und bringt einen relativ hohen laboratorischen Aufwand mit sich [50]. Abbildung 3. Algorithmus der virologisch-serologischen Diagnostik bei HCV-Infektion [36]. Abbildung 3 zeigt nochmals das Vorgehen zur Diagnosesicherung einer Hepatitis C Infektion. 4 Einleitung Vor Therapiebeginn gehört zur Standarddiagnostik ein Differentialblutbild, die Bestimmung der Transaminasen (AST, ALT), des Bilirubins, der Lebersyntheseparameter (Albumin), der Glucose, der Nierenfunktionsparameter (Kreatinin), des Gerinnungsstatus (Quick, INR), sowie die Abklärung einer Schilddrüsenfunktionsstörung (Bestimmung des basalen TSH). Zusätzlich zur Oberbauchsonografie kann bei Verdacht auf eine Leberzirrhose noch zusätzlich AFP bestimmt werden. Die Leberbiopsie ist aktuell Goldstandard, wenn es darum geht, bei einer chronischen Hepatitis C Infektion die begleitende Fibrosierung und Entzündungsaktivität des Lebergewebes zu berurteilen. Sie dient somit auch der Absicherung der Diagnose sowie der Bestätigung ihrer Chronizität. Ferner gibt sie Aufschluss über den Schweregrad der Hepatitis C Infektion und ist für die weitere Therapieentscheidung und den Therapieverlauf von Bedeutung. Sie birgt jedoch auch gewisse Risikofaktoren durch ihre Invasivität [1]. Neben diesem direkten Fibrosetest gewinnen zunehmend indirekte Fibrosetests wie die AST/ALT Ratio und der APRI Score bei der Beurteilung des Lebergeschehens an Bedeutung. Sie sind weniger invasiv und kostengünstiger und zeigen bei chronischer HCV Infektion in mehreren Studien bereits eine hohe Aussagekraft zur Erkennung der Schwere einer Leberschädigung. Bei einer fortgeschrittenen, signifikanten Fibrose oder Zirrhose ist die AST/ALT Ratio > 1, ansonsten < 1. Der APRI Score ist definiert als AST- to- Platelet- Ratio Index und wird folgendermaßen berechnet: APRI = ((AST (U/l)/ASTReferenz) x 100)/Thrombozytenkonzentration (109/l). Eine signifikante Fibrose zeigt sich bei Werten > 1,5. Diese ist jedoch bei Werten < 0,5 praktisch ausgeschlossen. Ebenso wurden für den APRI Score Schwellenwerte für eine Leberzirrhose festgelegt. Bei Werten < 1,0 gilt diese als ausgeschlossen, wohingegen bei Werten > 2,0 von einer signifikanten Zirrhose ausgegangen werden muss [48]. Die Bestimmung des Genotyps vor Beginn einer Therapie ist deswegen sinnvoll, weil dadurch die jeweils für den einzelnen Genotyp spezifische Dauer einer Therapie, sowie die Dosierung der Medikamente ermittelt worden ist und somit berücksichtigt werden kann. So fand man in Studien heraus, dass Patienten mit einer HCV Infektion und den 5 Einleitung Genotypen 1 und 4 ein besseres virologisches Ansprechen zeigen, wenn sie 48 Wochen lang mit einer hohen Ribavirindosis von 1000-1200 mg/Tag behandelt werden, im Gegensatz zu Patienten mit Genotyp 2 oder 3, bei denen bessere Therapieerfolge erzielt werden konnten, wenn sie nur 24 Wochen mit einer Ribavirindosis von nur 800 mg/Tag behandelt wurden [20]. Als Überwachungsintervalle und Therapiekontrolle sollte eine klinische Untersuchung, Bestimmung des Blutbildes, der Transaminasen, der Glukose und ggf. des Kreatinins alle 4 Wochen, eine TSH-Bestimmung alle 12 Wochen erfolgen. Eine Blutbildkontrolle alle 14 Tage in den ersten 1-2 Monaten ist wünschenswert. Bisher galt eine HCV-RNA Nachweiskontrolle quantitativ 12 Wochen und qualitativ 24 Wochen nach Therapiebeginn als sinnvoll [16]. Seit Abschluss der Studie hat sich das Therapiemonitoring jedoch verändert. Aktuell wird bereits nach 4 Wochen Therapie der HCV-RNA Status kontrolliert [17]. Der Therapieerfolg sollte nach einer 24-wöchigen Nachbeobachtung mittels einer PCR bestätigt werden. Sollte nach 12 Wochen Therapie keine Viruslastminderung um mindestens den Faktor 100 aufgetreten sein, ist ein Fortführen wenig sinnvoll, gleichsam nach einer 24-wöchigen Therapie mit einer nachweisbaren HCV-RNA im Serum [16]. 2.3 HCV-Genotypen RNA-Viren weisen aufgrund der relativen Ungenauigkeit (ca. 1 Mutation pro 104 Nukleotide [28]) des für die Replikation benötigten Enzyms RNA-abhängige RNAPolymerase (RdRP) eine sehr hohe genetische Variabilität auf. Diese Tatsache hat zu einer Entstehung verschiedener Genotypen (1-6; 31-34% Sequenzabweichung) und Subtypen (a-c; 20-23% Sequenzabweichung) geführt [3, 37, 41]. Wie in Abbildung 4 ersichtlich treten in Westeuropa und den USA die Genotypen 1a (u.a. der amerikanische Prototyp der 1989 als erstes kloniert wurde [8]) und 1b gefolgt von den Genotypen 2 und 3 am häufigsten auf. 6 Einleitung Abbildung 4. Genotypenverteilung weltweit nach Forns & Bukh (1999) [14]. Die Erfolgswahrscheinlichkeit der aktuellen Kombinationstherapie mit pegyliertem Interferon-α und Ribavirin (s.u.) ist ebenfalls maßgeblich abhängig vom Genotyp mit dem ein Patient infiziert ist. So kann bei den Genotypen 2 und 3 zu 80-90% mit einem Erfolg der Therapie gerechnet werden, während die Erfolgsquote bei Genotyp 1 nur bei ca. 50% liegt [2]. Des weiteren besitzt das HCV Genom eine hohe Mutationsrate. Daraus resultieren ständig neue, sog. Quasispezies, die es der heutigen Medizin schwer machen, die Viruspersistenz im menschlichen Organismus zu verhindern. So beschreibt Cao, dass diese Quasispezies bei einem Patienten innerhalb seiner HCV Infektion auftreten können und somit eine Heterogenität nach sich ziehen und einen wichtigen Faktor für die Ausheilungsrate darstellen. In dieser Studie zeigten Patienten mit einer höheren Heterogenität des HCV Virusgenoms eine geringere Ausheilungsrate als Patienten mit einer niedrigeren Virusheterogenität [7]. 2.4 Krankheitsverlauf und Folgekomplikationen der Hepatitis C Die Inkubationszeit bei einer Infektion mit dem Hepatitis C Virus beträgt durchschnittlich 15-160 Tage. Die akute Hepatitis C verläuft in 75% der Fälle asymptomatisch, nur 25% zeigen eine klinische Symptomatik. Diese kann sich in grippeähnlichen Symptomen wie Abgeschlagenheit, subfebrilen Temperaturen, oder gastrointestinalen Beschwerden 7 Einleitung (Appetitlosigkeit, Übelkeit) äußern, und deshalb auch häufig nicht richtig diagnostiziert werden, oder (in 10-20% der Fälle) einen ikterischen Verlauf nehmen mit Gelbfärbung der Skleren und der Haut, Juckreiz, Dunkelfärbung des Urins und Entfärbung des Stuhls. Symptomatische, ikterische HCV Infektionen können in ca. 25% der Fälle spontan ausheilen [18, 33]. Die spontane Ausheilungsrate aller akuten Verlaufsformen beträgt 1545% [22]. Asymptomatische HCV Infektionen verlaufen meist chronisch. Eine akute Hepatitis C kann, in den seltensten Fällen, auch fulminant verlaufen und zu akutem Leberversagen führen [13]. Die Mehrheit aller akuten HCV Infektionen gehen in einen chronischen Verlauf über [15]. Die chronische Hepatitis C ist definiert als Virushepatitis, die nach 6 Monaten nicht ausgeheilt ist und eine persistierende Virusreplikation und eine fehlende Viruselimination zeigt. Bis zu 20% der Patienten mit chronischer Hepatitis C entwickeln innerhalb von 20 Jahren eine Leberzirrhose [15], von den Zirrhosepatienten wiederum entwickeln 1-7% pro Jahr ein primäres Leberzellkarzinom [27]. Bei HIV- und HCV Doppelinfektionen (Drogenabhängige, Empfänger von Blutprodukten) sind die Verläufe oft rasch progredient [25, 39]. Hauptfolgekomplikation der chronischen Hepatitis C stellt die irreversible Leberzellschädigung dar. Extrahepatische Komplikationen können unter anderem renale Komplikationen, Neuropathien, Lymphome, autoimmune Thyreoiditis oder das SjögrenSyndrom mit oder ohne Kryoglobulinämie, Porphyria cutanea oder Diabetes umfassen [2, 19]. Der Verlauf der Erkrankung kann vom Alter zum Zeitpunkt der Infektion abhängen. So erkannte man, dass eine Infektion mit dem Hepatitis C Virus nach dem 40. Lebensjahr eine ungünstigere Prognose der Lebererkrankung mit sich bringt [39]. Auch die Dauer der Infektion, das gleichzeitige Auftreten anderer Lebererkrankungen (z.B. Coinfektionen mit HBV), chronischer Alkoholkonsum, deutlich erhöhte Transaminasen (3-5 fache des oberen Normwertes) oder ein männliches Geschlecht können den Krankheitsverlauf negativ beeinflussen [1]. Zusätzliche Prädispositionen sind eine höhere Ausgangsviruslast, eine bereits fortgeschrittene Fibrose, eine afro-amerikanische Herkunft und eine vorzeitige Beendigung der Ribaviringabe oder Reduktion der PEG-Interferondosis [1]. 8 Einleitung Zudem zeigte sich, dass Patienten mit einer geringen Entzündungsaktivität und einem niedrigen Fibrosegrad mit nur 20 bis 25% in 25-30 Jahren eine Leberzirrhose entwickeln [31, 35]. 2.5 Therapie der chronischen Hepatitis C Folgende Medikamente finden derzeit zur Therapie der chronischen Hepatitis C in Deutschland Anwendung: Interferon-α2a (Roferon), Interferon-α2b (Intron A), Peginterferon-α2a (Pegasys), Peginterferon-α2b (PegIntron), Ribavirin (Rebetol, Copegus). Interferon alfacon-1 (Inferax) kam früher ebenfalls als Hepatitis C Therapeutikum zum Einsatz und wurde auch in der PACT Studie u.a. angewandt, ist aktuell in Europa jedoch nicht mehr zugelassen. Interferone sind artspezifische Glykoproteine und gehören zur Gruppe der interzellulären Botenstoffe. IFN-α wird von Monozyten gebildet. Interferone wirken virustatisch, antiproliferativ und modulierend bei Immun- und Entzündungsvorgängen. Interferon-α2a und-α2b werden gentechnisch synthetisiert und unterscheiden sich von natürlich vorkommendem Interferon-α2 nur in einer Aminosäure (Position 23). Interferon alfacon-1 (Consensus Interferon) ist ein nicht natürlich vorkommendes Interferon, dessen Aminosäure-Consensussequenz von den natürlichen Interferonen abgeleitet wurde. Verglichen mit einzeln rekombinantem Interferon-α2 weist Consensus Interferon eine 10-fach erhöhte Wirksamkeit in der Hepatitis C Therapie auf [5]. Wird nun Polyethylenglykol (PEG) an Proteine, und in diesem Fall an Interferon konjungiert, verlängert sich die Halbwertszeit und somit die Pharmakokinetik. Die Halbwertszeit des Standardinterferons beträgt 8 Stunden, wohingegen das Peginterferonα2a eine Halbwertszeit von 60-80 Stunden, das Peginterferon-α2b 30-40 Stunden aufweisen. Pegylierte Interferone zeigen zudem einen deutlich gleichmäßigeren Wirkspiegel als Standardinterferone und werden deshalb nicht jeden oder jeden zweiten Tag appliziert, wie es bei Consensus Interferon der Fall ist, sondern nur einmal pro Woche. Wegen der unterschiedlichen PEG-Molekülgrösse wird das Peginterferon-α2a in einer festen Dosierung gegeben, während das Peginterferon-α2b körpergewichtsbezogen verabreicht werden muss [54]. Ribavirin ist ein Guanosinanalogon, das nach oraler Applikation von eukaryotischen Zellen aufgenommen wird und nach intrazellulärer Phosphorylierung virostatisch wirksam wird. Es ist jedoch nur in der Kombinationstherapie mit Interferon-α wirksam [12]. 9 Einleitung Die neuesten Forschungsergebnisse zeigen zudem einen potentiellen Wandel in der zukünftigen Behandlung der chronischen Hepatitis C. Sogenannte Proteaseinhibitoren wie Telaprevir und Boceprevir befinden sich aktuell erfolgreich in Phase III Studien und könnten noch dieses Jahr genehmigt werden. Diese Proteaseinhibitoren haben einen entscheidenen Vorteil. Während Interferone und Ribavirin eine breitbasige antivirale Wirkung haben, greifen sie direkt in den Replikationszyklus des Hepatitis C Virus ein, indem sie ein wichtiges Enzym des Virus, die NS3/NS4a Protease hemmen und somit die Translation und den Bau neuer Viruspartikel verhindern. Durch eine Tripeltherapie von Interferon, Ribavirin und eines Proteaseinhibitors war es beispielsweise möglich, beim schwer zu therapierbaren Genotyp 1 eine bessere Ausheilungsrate zu erzielen. Zusätzlich könnte aus den bisherigen Forschungsergebnissen eine Verkürzung der langen Therapiedauer von Genotyp 1 und 4 resultieren [38]. Die Standardtherapie einer chronischen Hepatitis C ist die Applikation von pegyliertem Interferon in Kombination mit Ribavirin. Durch die Kombinationstherapie konnten die Ansprechraten im Vergleich zur Interferonmonotherapie verbessert werden. Ebenso zeigte sich ein positiver Effekt auf einen möglichen Relapse. Eine Ribavirinmonotherapie wird nicht praktiziert, da sie kein virologisches Ansprechen zeigt. Bei Ribavirinunverträglichkeit oder Kontraindikationen für Ribavirin wird eine Monotherapie mit pegyliertem Interferon-α durchgeführt [1]. Patienten mit einem Rückfall nach Interferon-α-Monotherapie können mit der o.g. Kombinationstherapie für 24-48 Wochen (je nach Genotyp) behandelt werden. Bei Patienten mit einem Relapse unter einer Kombinationstherapie (Interferon/Ribavirin oder PEG-Interferon/Ribavirin) sollte zunächst eine genaue Überprüfung der Vortherapie durchgeführt werden, um eventuell aufgetretene Fehlerquellen und Mängel auszuschliessen (z.B. mangelnde Compliance, hohes Nebenwirkungsprofil der Medikamente, fehlende Dosierunganpassungen etc). Anschließend kann erneut bei suboptimaler Vortherapie eine Re-Therapie mit PEGInterferon und Ribavirin für 12- 24 Wochen - je nach Genotyp und viralem Ansprechen unter Therapie- versucht werden. Sollte sich auf eine Interferonmonotherapie oder eine Kombinationstherapie (Interferon/Ribavirin) kein virologisches Ansprechen zeigen (sog. Non-Response), wird empfohlen eine Kombinationstherapie mit PEG-Interferon und Ribavirin für 24-48 Wochen (je nach Genotyp) durchzuführen [17]. 10 Einleitung Von einer niedrigdosierten Langzeitmonotherapie mit einem pegylierten Interferon sozusagen “palliativ“ zur Verhinderung des Fortschreitens der Leberfibrosierung und der durch die Hepatitis C Infektion resultierenden klinischen Folgekomplikationen wird abgeraten [1]. 2.6 Fragestellung der Doktorarbeit Nach derzeitig aktuellem Stand in der Diagnostik einer Hepatitis C Infektion ist der Goldstandard die qualitative und quantitative Bestimmung der HCV-RNA im Serum mittels RT-PCR. Sie dient aber nicht nur der Sicherung einer Erstinfektion, sowie einer ReInfektion, sondern ist auch wichtigster Parameter, wenn es darum geht, ein Therapieansprechen und den Therapieverlauf zu beurteilen. Sie definiert somit ein dauerhaft virologisches Ansprechen (sog. SVR), ebenso wie einen Rückfall (Relapse) und ein konstantes Nichtansprechen auf eine antivirale Kombinationstherapie (sog. NonResponder). Zudem wird sie bei einer potentiellen Therapieänderung bzw. Dosisanpassung als wichtigster Verlaufsmarker herangezogen. In der folgenden Arbeit werden andere Parameter in Ihrem Verlauf unter einer antiviralen Kombinationstherapie mit Interferon alfacon-1 bzw. Peginterferon-α2b und Ribavirin bei einer nachgewiesenen Hepatitis C Infektion beobachtet. Es wird untersucht, ob diese einen signifikanten Aussagewert liefern über den Therapieverlauf und das Therapieansprechen, um in Zukunft den aktuell gängigen Marker- die HCV-RNA durch PCR ermittelt- ersetzen zu können. Diese einzelnen Parameter sind: Leukozyten/nl, Erythrozyten x 106/µl, Hämoglobinkonzentration g/dl, Thrombozyten/nl, Bilirubinkonzentration µM, AST, ALT, GGT U/l, die AST/ALT Ratio und der APRI Score. Diese Parameter werden sowohl in Gesamtheit als auch getrennt nach den zwei Kriterien ausgewertet, welcher Genotyp vorherrscht und welche Interferontherpie die Patienten verabreicht bekamen. Zusätzlich wurde vor Therapiebeginn durch eine Leberbiopsie und histologische Aufarbeitung der Fibrose-, Steatose- und Entzündungsgrad beurteilt. Diese werden ebenfalls im Hinblick auf den Therapieverlauf und das Therapieansprechen untersucht. 11 Einleitung Anschließend werden die Non-Responder und der Relapseanteil des Studienkollektivs ausgewertet, graphisch dargestellt und mit den anderen Ergebnissen in Zusammenhang gebracht. Definitionen der beiden Begriffe folgen im Teil “Material und Methoden“. Als Referenzgraphik dient jeweils die HCV-RNA Konzentration und die Ausheilungsrate (SVR). Diese wird zusätzlich in Gesamtheit, als auch unter Betrachtung der einzelnen Genotypen, der verabreichten Therapie und unter Berücksichtigung der jeweiligen Nadirwerte der einzelnen laborchemischen Parameter in Bezug gesetzt. Dabei beschreibt der Nadirwert den tiefsten Wert der einzelnen Laborparameter oder der Viruslast (hier der HCV-RNA) während einer antiretroviralen Therapie [6]. Zuletzt erfolgt eine Aufgliederung der Patienten, die sich in der SVR als Responder oder Non-Responder herausstellten und solchen, die einen Relapse erlitten. Dabei wird bei den einzelnen Parametern Leukozyten, Hämoglobin und Thrombozyten der unterschiedliche Verlauf der drei Patientengruppen bis Woche 12 untersucht, um dadurch eventuell Rückschlüsse auf ein vorläufiges Therapieansprechen oder – versagen zu erhalten. Dasselbe erfolgt nochmals bei den jeweiligen Nadirwerten der o.g. Parameter (Leukozyten, Hämoglobin, Thrombozyten). 12 Material und Methoden 3 Material und Methoden 3.1 Patientenkollektiv Für diese Arbeit wurden Daten von insgesamt 103 Patienten ausgewertet, die aufgrund ihrer diagnostizierten Hepatitis C Infektion im Zeitraum von Januar 2000 bis April 2003 am Universitätsklinikum Ulm behandelt wurden. Die Behandlung bestand aus einer Kombinationstherapie eines Interferonpräparates und des Nukleosidanalogons Ribavirin. Dabei bekamen 39 Patienten das Consensus Interferon (Interferon alfacon-1) plus Ribavirin verabreicht, während 64 Patienten mit PEG-Interferon (pegyliertem Interferonα2b) plus Ribavirin behandelt wurden. Von diesen 64 Patienten bekamen jedoch 8 für die ersten 12 Wochen zunächst eine Monotherapie mit Hochdosisinterferon--2b (Intron A) und ab Woche 13 eine Anschlusstherapie als Erhaltungstherapie mit PEG-Interferon plus Ribavirin. Diese 8 Patienten wurden in der PEG-Interferongruppe ausgewertet. Hierbei fielen alle Patienten in die Datenauswertung mitein, die wenigstens einmal eine Studienmedikation erhalten hatten. Das Gesamtkollektiv der behandelten Patienten zeigt folgende Geschlechterverteilung: 59,2% Männer (61 Patienten) und 40,8% Frauen (42 Patientinnen). Von den insgesamt 39 Patienten, die mit Interferon alfacon-1 plus Ribavirin behandelt wurden, betrug der Anteil der Frauen 46,1% (18 Patientinnen), der Anteil der Männer 53,9% (21 Patienten). Die Geschlechterverteilung der Patienten, die PEG-Interferon plus Ribavirin verabreicht bekamen, sah folgendermaßen aus: 62,5% Männer (40 Patienten) und 37,5% Frauen (24 Patientinnen). Somit herrschte eine insgesamt recht ausgeglichene Verteilung auf die beiden unterschiedlichen Therapieformen, was das Geschlecht angeht. Ein Ungleichgewicht kommt lediglich bei der unterschiedlichen Gesamtanzahl der Patienten zustande, weil deutlich mehr Patienten in die Auswertung eingingen, die die Pegylierte Interferonform als Therapie hatten (25 Patienten mehr als bei Consensus Interferon). 13 Material und Methoden Ein weit größerer Unterschied lässt sich in der Aufgliederung der Genotypen erkennen. Während Genotyp 1 und Genotyp 3 recht große und somit für die Auswertung signifikante Patientenzahlen besitzen, beschränken sich diese bei Genotyp 2 auf insgesamt 8, bei Genotyp 4 auf 4 Patienten. Dies macht eine signifikante Auswertung im Verlauf deutlich schwieriger. Die genaue Patientenaufteilung bezüglich der Genotypen ist in Tabelle 1 nochmals dargestellt. Tabelle 1. Patientenkollektiv der vorliegenden Arbeit nach Genotyp (Universitätsklinikum Ulm, 20002003. Genotyp Anzahl Patienten 1 35 2 8 3 56 4 4 Das Durchschnittsalter betrug bei der Gruppe des Consensus Interferons 37,6 Jahre, bei der Gruppe der pegylierten Interferonform 38,6 Jahre. 3.2 3.3 Therapiedauer, Dosisanpassung Medikamente und deren Dosierung mit ggf. Die Dauer der Teilnahme an der Studie betrug 72 Wochen (48 Wochen Behandlung und 24 Wochen Nachbeobachtung), wobei die Genotypen 2 und 3 nur 24 Wochen therapiert wurden. Eine Fortführung der Behandlung fand dann statt, wenn die Patienten mittels PCR in der 12. Therapiewoche einen negativen HCV-RNA Wert im Serum aufwiesen. Sollte dieser postitiv gewesen sein und sich im Wesentlichen nicht quantitativ vom Ausgangswert unterscheiden, erfolgte ein Therapieabbruch. Zeigten Patienten jedoch nach 12-wöchiger Therapie einen deutlichen quantitativen Abfall der Viruslast auf mind. > 2 log Stufen, wurde die Behandlung für weitere 4 Wochen fortgesetzt. Dann musste der qualitative HCV-RNA Nachweis negativ sein, sonst folgte der Therapieabbruch. Folgende Medikamente wurden verwendet (Tabelle 2): 14 Material und Methoden Tabelle 2. Medikamente mit Dosierung, Therapiedauer, Applikationsart und – häufigkeit. I.E. Internationale Einheiten, mind. Mindestens, s.c. subcutan (Universitätsklinikum Ulm, 2000-2003). Wirkstoff/Name Dosierung/Dosis- Therapieart anpassung Interferon-alphacon 1, Consensus- 9 µg Inferax 24 bis Konventionelle Therapie: Interferon, Inferax 48 Wochen 1x täglich s.c. plus Ribavirin täglich Interferon-alphacon 1, Consensus- 27 µg Inferax in den Intensivierte Therapie: 1x Interferon, Inferax ersten 2 Wochen, täglich s.c. Monotherapie, 18 µg Inferax für 10 ab Woche 12 Wochen, dann 9 µg Kombinationstherapie von Inferax als 9 µg Inferax und Ribavirin Erhaltungstherapie für mind. 12 weitere Wochen PEG-Interferon-2b, PEGIntron 80-150 µg, mind. Konventionelle Therapie: 1,5 mg/kg KG 1x pro Woche s.c., plus Ribavirin täglich Interferon-2b, Intron A 107 I.E. in den Intensivierte Therapie: 1x ersten 2 Wochen, täglich s.c. Monotherapie, 5x107 I.E. für 10 anschließend für mind. 12 Wochen, dann Wochen 1x pro Woche Erhaltungstherapie PEG-Intron s.c. kombiniert mit PEG-Intron 1,5 mit Ribavirin µg/kg KG Ribavirin, Rebetol, Copegus individuelle von max. 1400 mg täglich Dosierung und oral, Dosisanpassung auf Dosisanpassung, mind. 800 mg täglich oral Tagesdosis mind. 10,6 mg/kg KG 15 Material und Methoden 3.4 Therapiedurchführung und Beurteilung des Therapieerfolges, d.h. Erfassung des Ansprechens Die Therapieeinleitung erfolgte nach ausführlicher Aufklärung des Patienten über das Studiendesign, den Versuchsablauf, die Therapie sowie deren Nebenwirkungen durch einen zur Studie zugelassenen Prüfarzt, sowie nach schriftlicher Einverständniserklärung des Patienten zunächst unter stationärem Aufenthalt, da in den ersten 48 Stunden nach erstmaliger Interferonapplikation die schwerwiegendsten unerwünschten Ereignisse auftreten und somit eine adäquate Reaktion und Behandlung erfolgen konnte. Diese schwerwiegenden unerwünschten Ereignisse wie beispielsweise eine anaphylaktische Reaktion treten seltener auf als initiale Arzneimittelreaktionen von leichtem bis mässigem Schweregrad wie grippeähnliche Symptome, Fieber, Schüttelfrost, Müdigkeit, Übelkeit. Als Nebenwirkung des Ribavirins ist die hämolytische Anämie, sowie eine Erhöhung des Bilirubins und der Harnsäure im Serum zu nennen. Diese Nebenwirkungen bilden sich in der Regel nach Absetzen des Medikaments wieder zurück. Bei sich entwickelnder oder bestehender Anämie wurde den Patienten kein Erythropoetin zur Therapie verabreicht. Zur selbständigen Therapie wurden die Patienten oder deren Familienmitglieder suffizient in die Verabreichung der subkutanen Injektionen unterwiesen, so dass die Therapie ambulant fortgeführt werden konnte. Die Patienten wurden des weiteren im Laufe der gesamtem Studie in regelmäßigen und vom Studiendesign zeitlich festgelegten Abschnitten zur Kontrolle und Erhebung der Studiendaten in die Leberambulanz des Universitätsklinikums Ulm wiedereinbestellt. Die SVR (Sustained Virologic Response) und somit die Erfassung des Ansprechens auf die Therapie und die Beurteilung des Therapieerfolges erfolgte über die Ermittlung des HCVRNA Ergebnisses. Hierbei wurde ein sog. Langzeitansprechen erfasst. Dieses ist definiert durch die fehlende Nachweisbarkeit der HCV-RNA im Serum mittels sensitivem Assay (hier mittels PCR) mind. 24 Wochen nach Therapieende [1]. 16 Material und Methoden 3.5 Ein- und Ausschlusskriterien Die nachfolgenden Ein- und Ausschlusskriterien für die untersuchten Patienten wurden vom Studienprotokoll (PegIntron against Consensus Trial (PACT)) übernommen. Die Studie lag vor Beginn einer Ethikkomission zur Beratung vor und erhielt ihr positives Votum am 26.06.2002, sowie das Aktenzeichen 105/2002. Folgende Einschlusskriterien mußten erfüllt werden: Patienten mit histologisch gesicherter chronischer Hepatitis C. Die Biopsie sollte zum Zeitpunkt der Aufnahme in die Studie nicht länger als 18 Monate zurückliegen. Alter: 18-65 Jahre bzw. nach Ermessen des behandelnden Prüfarztes Gewicht: ≥ 45 kg Kompensierte Lebererkrankung mit den folgenden hämatologischen und biochemischen Mindestkriterien: Hämoglobin ≥ 13 g/dl für Männer und ≥ 12 g/dl für Frauen Leukozyten ≥ 3.000/mm3 Thrombozyten ≥ 80.000/mm3 Gesamtbilirubin ≤ 1,5 fache des Normalwertes (Ausnahme Morbus Meulengracht/ Gilbert Syndrom) Albumin stabil und ≥ 3,5 g/dl Serumkreatinin ≤ 1,4 mg/dl Hämoglobin A1c < 8% bei Patienten mit Diabetes mellitus TSH im Normbereich des Testlabors Antinukleäre Antikörper (ANA) ≤ 1:160 HIV negativ (mittels ELISA ermittelte positive Testergebnisse müssen per Western Blotting Verfahren bestätigt werden) HCV-Antikörper positiv HCV-RNA im Serum nachweisbar HCV-Genotypisierung oder Serotypisiering Erhöhte ALT- Werte Augenärztliche Untersuchung bei Patienten mit den Begleiterkrankungen Diabetes mellitus und arterielle Hypertonie 17 Material und Methoden Alpha-Fetoprotein (AFP) im Normbereich (falls außerhalb des Normbereiches und ≥ 50 ng/ml muss das Vorliegen eines hepatozellulären Karzinoms mittels Sonographie ausgeschlossen worden sein) Schriftliche Einverständniserklärung nach Aufklärung durch den Prüfarzt Folgende Ausschlusskriterien mußten erfüllt werden: Lebererkrankungen mit einer anderen Ursache als chronische Hepatitis C, bestimmt anhand der anamnestischen Daten des Patienten und der Leberbiopsie Mögliche andere Ursachen der Lebererkrankung: HIV- Koinfektion unbehandelte Hämochromatose Alpha-1-Antitrypsinmangel Morbus Wilson Autoimmunhepatitis Patienten nach Nieren- und Lebertransplantation Schwere Leberfunktionsstörung (Quickabfall) bedingt durch Alkohol-, Medikamenten- oder Drogenkonsum Medikamenten- oder drogenbedingte Lebererkrankung Bestehender aktiver Alkohol- oder Drogenabusus (Methadon- substituierte Patienten können nach Ermessen des Prüfarztes in die Studie eingeschlossen werden) Nachweis einer dekompensierten Lebererkrankung (z.B. bei Vorliegen von Aszites, Varizenblutung, spontaner Enzephalopathie) Adipositas induzierte Lebererkrankung Jeder vorbestehende Krankheitszustand, der die Teilnahme des Patienten an der Studie und deren Abschluss aufgrund mangelnder Compliance beeinträchtigen könnte (z.B. vorbestehende psychiatrische Erkrankungen wie eine ungenügend behandelte aktive Depression oder bekannte Suizidalneigung etc.) Therapiebedürftiges ZNS-Trauma oder therapiebedürftige Epilespie Jede bekannte Funktionsstörung des kardiovaskulären Systems, einschließlich Myokardinfarkt, Linksherzinsuffizienz, 18 Angina pectoris, klinisch relevante Material und Methoden Herzrhythmusstörungen oder Herzklappenerkrankungen/-anomalien, Koronaroperationen, Koronarangioplastie Ungenügend eingestellte chronische, obstruktive Lungenerkrankung (COPD) Immunologisch vermittelte Erkrankungen (wie z.B. Lupus erythematodes, entzündliche Darmerkrankungen, Sklerodermie, Autoimmunthyreoiditis, rheumatoide Arthritis, etc.) Klinisch manifeste Gicht Schwangere oder stillende Frauen, Frauen mit aktuellem Kinderwunsch Vorsichtsmaßnahmen: Sexuell aktive Frauen im gebärfähigen Alter müssen für die Dauer der Behandlung und für 6 Monate nach Therapieende eine medizinisch sichere Empfängnisverhütung anwenden (z. B. orale Kontrazeptiva, Intrauterinpessar) Sexuell aktive Männer müssen für die Dauer der Behandlung und für 7 Monate nach Therapieende eine akzeptable Empfängnisverhütungsmethode anwenden (Vasektomie, Kondom, etc.) 3.6 Laborparameter, Ratios, Histologie, Genotypisierung 3.6.1 Laborparameter und Ratios/Scores Vor Therapiebeginn und nach Beendigung der Behandlung, sowie nach dem Ende der 6monatigen Nachbeobachtungszeit erfolgte bei allen Patienten eine körperliche Untersuchung. Des weiteren wurden während des gesamten Behandlungszeitraums regelmässige Laborkontrollen durchgeführt. Hierbei wurden Leukozyten, Erythrozyten, Hämoglobin, Thrombozyten, Transaminasen und das basale TSH sowie Trijodthyronin (T3) und Thyroxin (T4) zum Ausschluss einer Interferon-induzierten Thyreopathie erfasst. Zusätzlich erfolgte eine regelmässige Kontrolle des Bilirubin gesamt. Bilirubin ist ein Abbauprodukt des Hämoglobins, genauer des Häm-Anteils. Dieses liegt zunächst als indirektes, unkonjugiertes Bilirubin vor. Nach Konjugation mit Glukuronsäure in der Leber kann es dann als direktes, konjugiertes Bilirubin mit der Galle in den Darm ausgeschieden werden. Als Bilirubin gesamt bezeichnet man folglich die Summe der direkten und 19 Material und Methoden indirekten Bilirubinkonzentration [4, 42]. Aus methodischen Gründen wurde zur Vereinfachung jeweils der Wert des Bilirubins gesamt in den Ergebnisteil miteinbezogen. Die Transaminasen (AST, ALT, GGT) wurden in U/l gemessen und beschreiben damit die jeweilige Aktivität des Enzyms, da die eigentliche Enzymkonzentration im Plasma meist sehr gering ist (z.B. Normwert der AST 100 µg/l) [21]. Als wichtigster Parameter zur Beurteilung des Therapieverlaufes und Therapierfolges und der Notwendigkeit einer potentiellen Dosisanpassung wurde die quantitative HCV-RNA Messung mittels PCR herangezogen und regelmäßig erhoben. Die HCV-RNA Konzentration im Serum diente als Vergleichs- und Referenzwert aller übrigen beobachteten chemischen Laborparameter. Sie wird in Internationalen Units (IU/ml Serum) angegeben, wobei 50 IU/ml 100 Kopien /ml entsprechen [26]. Die Viruslastbestimmung mittels PCR wurde mithilfe des COBAS AMPLICOR HCV TM MONITOR Tests der Firma Roche durchgeführt. Dieser Test ist ein In-vitro-Nukleinsäure- Amplifikationstest zur quantitativen Bestimmung der HCV-RNA in Humanserum. Nach manueller Aufreinigung der HCV-RNA aus 200 µl Serum oder Plasma erfolgte die Reverse Transkription, Amplifikation und Detektion auf dem COBAS® AMPLICOR®. Während der gesamten Reaktion wurden drei Kontrollen mitgeführt (Negativkontrolle, niedrigkonzentrierte HCV-RNA, hochkonzentrierte HCV-RNA), die in jeder Probe die Qualität der Ergebnisse sicherstellen sollten. Zusätzlich erfolgte die Erhebung und Beobachtung zweier nichtinvasiver diagnostischer Parameter unter Therapie, die bei chronischen Hepatopathien aufgestellt werden können: die AST/ALT Ratio und der APRI Score. 3.6.2 Histologie Vor Therapiebeginn wurde bei 97 von 103 Patienten eine Lebergrobnadelpunktion nach Menghini durchgeführt und das gewonnene Präparat in der Abteilung für Pathologie des Universitätsklinikums Ulm histologisch aufgearbeitet und untersucht. Hierbei wurde v.a. die Entzündungsaktivität des Lebergewebes, der Grad der Fibrose und Steatose beurteilt. Die Leberbiopsie gilt hierbei zur Zeit trotz der zahlreich verfügbaren direkten und indirekten Fibrosetests (wie z. B. die AST/ALT Ratio und der APRI Score) als Goldstandard zur Beurteilung des Schweregrades einer Fibrose und Leberzirrhose [48]. Zur 20 Material und Methoden Stadieneinteilung des Fibrosegrades (Staging) wurde das Metavir Scoring System herangezogen. Hierbei steht Grad 0 für keine vorhandene Fibrose, Grad I für leichte Fibrose (portale Fibrose ohne Septen), die Grade II-IV für mäßige bis schwere Fibrose (II: wenige Septen, III: zahlreiche Septen ohne Zirrhose), wobei Grad IV dem Endstadium der Zirrhose entspricht. Ab Stadium ≥ II wird die Fibrose als klinisch signifikant erachtet [11, 39, 48]. Die Entzündungsaktivität wurde nach dem Scoresystem von Desmet und Scheuer eingeteilt [11, 39, 48]: Grad I: minimale Entzündungsaktivität Grad II: milde Entzündungsaktivität Grad III: mäßige Entzündungsaktivität Grad IV: schwere Entzündungsaktivität Bei der Steatose wurde lediglich das Vorhandensein oder nicht Vorhandensein im Leberbiopsat des jeweiligen Patienten berücksichtigt. 3.6.3 Genotypisierung Die Genotypisierung der untersuchten HCV Patienten erfolgte am Universitätsklinikum Ulm durch den reversen Hybridisierungsassay INNO-LiPA HCV II Streifentest der Firma Bayer. Dadurch konnten die 6 Haupttypen des Hepatitis C Virus, sowie die wichtigsten Subtypen bestimmt werden. Der Test beruht auf folgendem Prinzip: der untersuchte DNA Abschnitt wird zunächst mittels PCR amplifiziert. Anschließend erfolgt eine Hybridisierung dieser Amplikate an sequenzspezifischen Gensonden, die auf einem Nitrocellulosestreifen aufgebracht sind. Dabei bleiben nur die Bindungen erhalten, bei denen die Sequenz des Amplifikates zu 100% mit der Sequenz der Gensonde übereinstimmt. An diesen Hybridkomplex bindet nun ein Konjugat. Nun wird durch Zugabe des Substrates BCIP/NBT ein Farbkomplex gebildet, der auf der Nitrocellulosemembran sichtbar wird. Mit einer Farbschablone kann dann der Genotyp und der Subtyp abgelesen werden [29]. 21 Material und Methoden 3.7 Datenerhebung Die Datenerhebung wurde prospektiv mittels Krankenakten und Studienprotokollen der Leberambulanz, des Archivs und den Datenbanken der Abteilung Innere Medizin I des Universitätsklinikums Ulm unter Leitung des ärztlichen Direktors Prof. Dr. Guido Adler durchgeführt. Es wurden v.a. Anamnesebögen, Arztbriefe, Verlaufsprotokolle der laborchemischen Parameter, Histologieberichte und Medikationsbögen zur Auswertung herangezogen. Die Datenerhebung selbst und die daraus resultierende Datenauswertung mit graphischer Darstellung erfolgte mithilfe des Kalkulationsprogrammes Microsoft Excel 2010. Bei 67 Patienten konnte eine regelrechte Therapiedauer erreicht werden. 16 Patienten zeigten aufgrund starker unerwünschter Nebenwirkungen oder mangelnder Compliance einen vorzeitigen, selbständigen Therapieabbruch. Ebenso wurden bei der Auswertung der einzelnen Ergebnisse die Patienten berücksichtigt, die während der Therapie bzw. nach Therapieende nicht auf die Behandlung ansprachen (sog. Non-Responder) oder einen Rückfall erlitten (sog. Relapse). Bei einem Non-Responder besteht definitionsgemäß nachweisbar ein Abfall der HCV-RNA bis Woche 12, der kleiner als 100-fach ist, oder bei denen HCV-RNA unter Therapie im Blut bis zu Woche 24 nachweisbar ist [1]. In dieser Studie gab es 7 Non-Responder und somit einen Anteil von 8%. Bei einem Relapse hat der Patient bei Therapieende keine nachweisbare HCV-RNA im Blut, jedoch ein positives HCV-RNA Ergebnis nach Therapieende [1]. Insgesamt entwickelten 13 Patienten einen Relapse und stellen damit einen Anteil von 14,9%. 3.8 Statistik Zur Auswertung der quantitativen Laborparameter im zeitlichen Verlauf wurden die arithmetischen Mittel der Werte aller Patienten nach Genotyp oder Behandlungsart jeweils errechnet und graphisch dargestellt. Aufgrund der niedrigen Patientenzahlen – insbesondere bei den Genotypen 2 und 4 – wurde auf eine weitergehende Statistik zur Signifikanzprüfung verzichtet. 22 Material und Methoden Für die qualitativen Parameter wie Fibrose, Steatose, Entzündung, SVR-Rate, Relapse oder Non-Responder wurden jeweils die Anzahl der Patienten pro Genotyp oder Behandlungsart in dem jeweiligen Stadium oder mit dem jeweiligen Phänotyp bestimmt, in Relation zur Gesamtpatientenzahl gesetzt und ebenso graphisch aufgetragen. Der APRI-Score wurde aus den Mittelwerten der jeweiligen Patientengruppen (nach Genotyp oder Therapieart) nach der folgenden Formel berechnet: APRI = ((AST (U/l)/ASTReferenz) x 100)/Thrombozytenkonzentration (109/l). Als ASTReferenz-Wert wurden auf 40 (U/l) verwendet [5, 32]. Der Nadirwert ist definiert als der jeweils niedrigste Wert eines Parameters und wurde aus den nach dem oben aufgeführten Verfahren berechneten Mittelwerten für die jeweiligen Patientengruppen (nach Genotyp oder Therapieart) bestimmt. 23 Ergebnisse 4 Ergebnisse Im Folgenden wird zunächst der Verlauf der einzelnen laborchemischen Parameter (Leukozyten, Erythrozyten, Hämoglobin, Thrombozyten, Bilirubin, AST, ALT, GGT), das Verhältnis von AST und ALT (AST/ALT-Ratio), das Verhältnis des AST zur Thrombozytenzahl (APRI Score), sowie die Viruslast (mittels positiver HCV-RNA) des Patientenkollektivs unter Aufgliederung in die einzelnen Genotypen erläutert. Anschließend erfolgt die Untersuchung der o.g. Parameter unter Berücksichtigung der beiden Therapieformen Interferon-alphacon 1 plus Ribavirin bzw. Peginterferon-α2b plus Ribavirin. Des Weiteren sind Diagramme anderer wichtiger Parameter (Fibrose- und Entzündungsgrad, das Vorhandensein einer Steatose) zur näheren Beschreibung des ursprünglichen Schweregrades einer Hepatitis C und anschließendem Therapieansprechen - je nach Genotyp - aufgeführt. Sie wurden histologisch mittels Leberbiopsie erfasst. Ferner wird die Anzahl der Non-Responder und Patienten mit erkennbarem Relapse im Therapieverlauf bzw. nach Therapieende aufgezeigt. Zusätzlich wird die Ausheilungsrate (SVR) je nach Genotyp, Therapieform und im Hinblick auf die Nadirwerte der einzelnen laborchemischen Parameter betrachtet. Zuletzt erfolgt eine Aufgliederung der Patienten in Responder, Non-Responder und solche, die einen Relapse erlitten bis Woche 12 bei den folgenden Parametern: Leukozyten, Hämoglobin und Thrombozyten. Dasselbe wurde nochmals bei den jeweiligen Nadirwerten der o.g. Parameter (Leukozyten, Hämoglobin, Thrombozyten) durchgeführt. Bei der Analyse und Interpretation der Abbildungen ist die jeweils geringe Anzahl der Patientenzahlen von Genotyp 2 und Genotyp 4 unseres Studienkollektives zu berücksichtigen. Daher wurden bei der Auswertung der Therapieverläufe bei den Leukozyten-, Hämoglobin- und Thrombozytenkonzentrationen und deren Nadirwerten 24 Ergebnisse die Genotypen 1 und 4, sowie 2 und 3 zur besseren Veranschaulichung gemeinsam ausgewertet. 4.1 Verlauf der laborchemischen Parameter unter Therapie und Aufgliederung in Genotypen Woche 0 stellt hierbei die sogenannte Baseline dar. Diese ist definiert als erste Woche der Interferontherapie, jedoch noch vor der ersten Interferoninjektion und oralen Ribaviringabe. Die folgend aufgeführten laborchemischen Normwerte wurden jeweils der Literatur entnommen [21]. 4.1.1 Verlauf der Leukozytentiter unter Therapie Abbildung 5 zeigt den Verlauf der Leukozytenwerte der vier untersuchten Genotypen (GT1-4) von Therapiebeginn (Woche 0) bis Therapieende (Woche 48). 9 GT1 GT2 GT3 GT4 Leukozyten/nl 8 7 6 5 4 3 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 5. Verlauf der Leukozytentiter nach Genotyp. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Die Normwerte eines gesunden, nicht an Hepatitis C erkrankten Menschen liegen bei 410/nl. Bei Therapiebeginn (Woche 0) liegen zunächst noch bei allen vier Genotypen normwertige Leukozytenzahlen vor (Baseline von 6,9 bis 8,3/nl). 25 Ergebnisse Unabhängig vom untersuchten Genotyp kommt es in den Wochen 2 bis 12 zu einem Abfall der Leukozyten auf etwa 50% der Baseline. Hierbei verhalten sich die Genotypen 2 und 3 fast deckungsgleich im Verlauf (jeweils 3,3/nl in Woche 12). Bei Genotyp 1 bleibt der Leukozytentiter im Laufe der gesamten Therapie auf niedrigem Niveau (< 4,0/nl ab Woche 4), während Patienten mit den Genotypen 2-4 insbesondere ab Woche 24 eine deutliche Erholung zeigen (Abbildung 5). 4.1.2 Verlauf der Erythrozytentiter unter Therapie Die Normwerte eines gesunden Menschen liegen bei einer Erythrozytenkonzentration von 4,0 bis 5,2 x 106/µl bei Frauen und 4,5 - 5,9 x 106/µl bei Männern. Erythrozyten (x106/µl) 5,5 5 4,5 4 3,5 GT1 GT2 GT3 GT4 3 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 6. Verlauf der Erythrozytentiter nach Genotyp. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Dieser Normbereich wird - wie aus Abbildung 6 ersichtlich - im Patientenkollektiv lediglich kurzzeitig und geringfügig von Genotyp 2 in den Wochen 12 und 24 und Genotyp 1 in Woche 48 mit Werten kleiner als 4,0 x 106/µl unterschritten. Zwar zeigen Probanden aller Genotypen bei den Erythrozytenwerten einen Abfall im Verlauf- bezogen auf die Baselinedieser beschränkt sich aber auf eine Differenz von ungefähr 0,5 bis 1 x 106/µl (10 bis 20%). Ganz ähnlich auch hier das Verhalten der Genotypen 2 und 3 bis Woche 24. In Woche 48 erreichen diese Patienten in etwa das Niveau der Baseline, oder einen noch leichtgradig höheren Wert, während Patienten mit Genotyp 1 ebenso wie bei den Leukozytentitern 26 Ergebnisse weiterhin leicht gesenkte Erythrozytenkonzentrationen (Abfall zur Baseline um ca. 20%) aufweisen. Der steilste Anstieg in der Erythrozytenkonzentration ist bei Genotyp 2 ab Woche 24 zu finden (ca. 25% Zuwachs) 4.1.3 Verlauf der Hämoglobinkonzentration unter Therapie Der normale Hämoglobingehalt des Blutes beträgt bei der Frau 12-16 g/dl, beim Mann 1418 g/dl. Hämoglobinkonzentration (g/dl) 18 16 14 12 GT1 GT2 GT3 GT4 10 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 7. Verlauf der Hämoglobinkonzentration nach Genotyp. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 20002003). Die Hämoglobinwerte der Genotypen 1 und 4 ähneln sich im Verlauf mit einer Erniedrigung bis zu den Wochen 12 und 24 und einer anschliessenden Erholung in Woche 48. Die Genotypen 2 und 3 hingegen zeigen einen deutlich anderen Kurvenverlauf und gleichen sich diesmal auch nicht. Genotyp 2 erreicht den niedrigsten Wert von 11,7 g/dl in Woche 12. Der darauffolgende plötzliche Hämoglobinanstieg von Genotyp 2 von 11,8 g/dl auf 16,6 g/dl in Woche 48 liegt möglicherweise darin begründet, dass der Hb-Wert in der Patientengruppe mit Genotyp 2 in Woche 48 bei nur einem Patienten erhoben wurde und somit zu diesem Zeitpunkt als nur wenig aussagekräftig anzusehen ist. Nach einer Erniedrigung der Hämoglobinkonzentration bis Woche 4 zeigt Genotyp 3 dann in Woche 12 einen steilen Anstieg und erreicht einen höheren Wert (15,5 g/dl) als bei der Baseline (15,2 g/dl), dann erkennt man einen erneuten Einbruch in Woche 24, gefolgt von 27 Ergebnisse einem neuen, fast ebenso steilen Anstieg in Woche 48. Der Baseline-Wert wird hier fast wieder erreicht (14,9 g/dl). Der Normbereich der Hämoglobinkonzentration wird bei allen Genotypen während des gesamten Therapieverlaufes jedoch nicht signifikant unterschritten (Abbildung 7). 4.1.4 Verlauf der Thrombozytentiter unter Therapie Der normwertige Gehalt an Thrombozyten eines Gesunden liegt bei 150- 350/nl. 300 GT1 GT2 GT3 GT4 Thrombozyten/nl 250 200 150 100 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 8. Verlauf der Thrombozytentiter nach Genotyp. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Die Baseline aller Genotypen startet im Normberich zwischen 214/nl und 271/nl. Die Genotypen 1, 3 und 4 zeigen hier einen ähnlichen Verlauf unter Therapie mit einer Erniedrigung der Thrombozytenzahl bis zu Woche 4 und 12 und einer anschließenden Erholung in den Wochen 24 und 48. Sie erreichen dort ungefähr wieder das Niveau der Baseline. Allein Genotyp 2 zeigt einen anderen, alternierenden Verlauf. In Woche 2 kommt es zunächst zu einem Abfall auf bis zu 128/nl mit einer anschließend kurzzeitigen Erholung in Woche 4 auf 151/nl. Dann kommt es zu einem erneuten Rückgang der Thrombozytenzahl in Woche 12 auf den insgesamt niedrigsten Wert von 122/nl gefolgt von einem erneuten Anstieg in Woche 24 auf einen Wert von 180/nl und einem letzten Abfall auf 161/nl in Woche 48. Allein Genotyp 2 unterschreitet den Normbereich der Thrombozytenkonzentration in den Wochen 2 und 12 (Abbildung 8). 28 Ergebnisse 4.1.5 Verlauf der Bilirubinkonzentration unter Therapie Der Normbereich des gesamten (direkten und indirekten) Bilirubins liegt bei 3,4-18,8 µM. 30 Bilirubin (Gesamt, µM) GT1 GT2 GT3 GT4 25 20 15 10 5 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 9. Verlauf der Bilirubin-Konzentration nach Genotyp. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 20002003). Patienten der Genotypen 1, 3 und 4 bleiben während der gesamten Behandlungszeit im Normbereich und zeigen in Ihrem Kurvenverlauf keine gravierenden Abweichungen. Auffallend ist, dass Patienten, die mit HCV des Genotyps 2 infiziert sind, in Woche 2 mit einem Wert von 26 µM deutlich oberhalb des Normbereiches liegen. Dieser fällt bis Woche 24 deutlich (11,4 µM) und steigt zum Ende in Woche 48 wieder an und erreicht dort einen Endwert von 15 µM (Abbildung 9). 29 Ergebnisse 4.1.6 Verlauf der AST-Konzentration unter Therapie Der Normbereich der AST-Konzentration liegt bei < 15 U/l für Frauen, < 18 U/l für Männer. 70 GT1 GT2 GT3 GT4 AST-Konzentration (U/l) 60 50 40 30 20 10 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 10. Verlauf der Aspartataminotransferase (AST)-Konzentration nach Genotyp. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Abbildung 10 lässt im untersuchten Patientenkollektiv eine signifikante Erhöhung der Baseline bei den Genotypen 1-3 erkennen. Patienten der Genotypen 2 und 3 weisen hierbei die höchsten Konzentrationen in Woche 0 mit durchschnittlich 56 bis 60 U/l auf, erzielen jedoch im Verlauf ebenso den stärksten Abfall des AST auf 18 und 22 U/l in Woche 48. Ferner kommt es bei Patienten aller Genotypen, mit Ausnahme von Genotyp 4, zu einem konstant abfallenden AST-Titer während des Therapieverlaufs. Dessen ASTTiter bewegt sich insgesamt auf konstant niedrigem Niveau. 30 Ergebnisse 4.1.7 Verlauf der ALT-Konzentration unter Therapie Der Normbereich der ALT-Konzentration beträgt für Frauen < 17 U/l und für Männer < 22 U/l . 140 GT1 GT2 GT3 GT4 ALT-Konzentration (U/l) 120 100 80 60 40 20 0 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 11. Verlauf der Alaninaminotransferase (ALT)-Konzentration nach Genotyp. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Abbildung 11 zeigt – ähnlich wie Abbildung 10 - eine stark erhöhte ALT-Baseline für alle untersuchten Genotypen. Auch hier zeigen die Genotypen 2 mit 85 U/l und 3 mit 120 U/l die höchsten ALT- Ausgangskonzentrationen, sowie den stärksten Abfall bis Woche 48 um 66 U/l ( Genotyp 2) und 90 U/l ( Genotyp 3). Ebenso zeigen die Genotypen 1 und 4 einen Abfall der ALT-Konzentration im Verlauf, jedoch lange nicht so gravierend als bei den Genotypen 2 und 3. Zusätzlich weisen Patienten des Genotyps 4 in Woche 48 mit > 60 U/l wieder stark erhöhte Werte auf. 31 Ergebnisse 4.1.8 Verlauf der GGT-Konzentration unter Therapie Bei Frauen beträgt der Normwert der GGT-Konzentration 4-18 U/l, bei Männern 6-28 U/l. 80 GGT-Konzentration (U/l) 70 60 50 40 30 20 10 GT1 GT2 GT3 GT4 0 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 12. Verlauf der Gamma-Glutamyltransferase (GGT)-Konzentration nach Genotyp. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Abbildung 12 zeigt, dass Patienten aller Genotypen auch eine insgesamt stark erhöhte GGT-Konzentration (höchster Wert bei Genotyp 1 mit 69 U/l) in Woche 0 aufweisen. Diese verringert sich bei Genotyp 1 und 3 - ähnlich der AST- und ALT-Konzentrationen - im Therapieverlauf deutlich auf ca. 30 U/l. Der Konzentrationsverlauf von GGT für die Genotypen 2 und 4 ist sehr pleomorph. So fällt die GGT-Konzentration von Genotyp 2 erst nach Woche 4, dann aber sehr rapide als insgesamt stärkster Abfall bis Woche 48 auf 13 U/l ab, während Patienten des Genotyps 4 von Anfang an niedrige GGT-Titer aufweisen und auch keinen so großen Schwankungen unterliegen. 3.1.8 Verlauf des AST:ALT Verhältnisses unter Therapie 32 Ergebnisse 1 GT1 GT2 GT3 GT4 AST/ALT-Ratio 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 13. Verlauf des Verhältnisses von Aspartataminotransferase (AST) zu Alaninaminotransferase (ALT) (AST/ALT-Ratio) nach Genotyp. Das AST/ALT-Ratio wurde aus den jeweiligen Mittelwerten von AST und ALT der Patienten mit Hepatitis C Infektion der entsprechenden Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) berechnet und ist über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Auffällig in Abbildung 13 ist, dass Patienten aller Genotypen ein AST:ALT Verhältnis < 1 aufweisen. Daraus ist ersichtlich, dass im gesamten Patientenkollektiv mit einer konstanten AST/ALT Ratio < 1 definitionsgemäß noch keine schwere Leberfibrose oder Zirrhose aufgetreten ist. Die Kurven der einzelnen Genotypen unterscheiden sich in ihrem Verlauf sehr. Ausgangswerte reichen von 0,37 (Genotyp 4) bis 0,66 (Genotyp 2). Die Genotypen 2 und 3 zeigen bei näherer Betrachtung dennoch einen ähnlichen Verlauf mit einer leichten Steigung in Woche 2 auf 0,76 bzw. 0,68 und halten dieses Niveau bis Woche 24. Genotyp 3 behält dieses Niveau bis Woche 48 bei, Genotyp 2 erfährt hier erneut einen Anstieg auf einen Wert von 0,95 und ist somit deutlich oberhalb des Ausgangswertes von 0,66. Genotyp 1 verhält sich etwas anders. Ein erster Höchstwert mit 0,88 wird in Woche 4 erreicht der zweite in Woche 48 mit einem Wert von 0,89 nach einem vorhergehenden Abfall in den Wochen 12 und 24. Bei Genotyp 4 steigen die Werte bis Woche 12 um mehr als das doppelte an (von 0,37 Baseline bis 0,76) und fallen dann rapide bis Woche 48 annähernd auf den Ausgangswert (0,33) ab. 33 Ergebnisse 4.1.9 Verlauf des APRI Score unter Therapie 1 GT1 GT2 GT3 GT4 APRI-Score 0,8 0,6 0,4 0,2 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 14. Verlauf des Aspartataminotransferase/Thrombozyten-Ratio Index (APRI Score) nach Genotyp. Der APRI Score wurde wie in Material und Methoden beschrieben für die Mittelwerte der Patienten mit Hepatitis C Infektion der jeweiligen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) berechnet und ist über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Abbildung 14 zeigt, dass Genotyp 4 insgesamt die niedrigsten Werte bezüglich des APRI Score besitzt und im gesamten Therapieverlauf konstant unter 0,5 bleibt und somit keine signifikante Fibrose vorliegt. Ebenso erreicht kein Genotyp den Schwellenwert einer eindeutigen Leberzirrhose von 1,0. Anders als der AST/ALT Ratio erfolgt beim APRI Score eine genauere Unterteilung des Schweregrades der Leberfibrosierung. Alle Genotypen außer Genotyp 4 lassen hier deutlich eine leicht- bis mittelgradige Fibrose erkennen, die jedoch laut Definition des APRI Score mit Werten unterhalb von 1,5 ebenfalls nicht signifikant sind. Den höchsten APRI Score erreicht Genotyp 2 in Woche 2 mit einem Wert von 0,87. 4.1.10 Verlauf der HCV-RNA unter Therapie Der Viruslastnachweis bezüglich HCV-RNA mittels PCR ist zur Zeit immer noch der wichtigste Vorhersagewert zur Ausheilungsrate und dem Ansprechen einer Therapie bei chronischer Hepatitis C. Hiermit erkennt man auch einen Rückfall (Relapse) des Patienen, sowie die sogenannten Non-Responder. In der folgenden Abbildung sind die Patienten in 34 Ergebnisse % aufgezeigt, die zum jeweiligen Zeitpunkt alle noch ein positives HCV-RNA Ergebnis besaßen. % HCV-RNA positive Patienten 100 GT1 GT2 GT3 GT4 total 75 50 25 0 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 15. Verlauf der Nachweisbarkeit von Hepatitis C Virus Ribonukleinsäure (HCV-RNA) nach Genotyp. Die relativen Anteile der Patienten mit nachweisbarer HCV-RNA der einzelnen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). In Abbildung 15 wird deutlich, dass die Anzahl der HCV-RNA positiven Patienten aller Genotypen bereits ab Woche 2 abnimmt und bis Woche 12 deutlich niedrigere Werte erreicht werden. Auch hier zeigen die Genotypen 2 und 3 in Woche 12 den stärksten Abfall auf 2,3% (Genotyp 3) bzw. 12,5% (Genotyp 2). Genotyp 2 lässt in den Wochen 24 bis 48 einen weiteren Abfall auf letztlich 0% erkennen, wohingegen Genotyp 3, ebenso wie Genotyp 4 ab Woche 12 eine steigende Anzahl an Patienten mit erneut pos. HVC-RNA aufweisen (erhöhte Relapserate). Schließlich scheint Genotyp 1 therapieresistenter als die anderen Genotypen zu sein. Die Werte bleiben im Verlauf bis Woche 12 deutlich über denen der anderen Genotypen und zeigen auch in Woche 24 (16,7%) und 48 (23,1%) einen höheren persistierenden Anteil an Patienten mit positiver HCV-RNA. Bei der Auswertung der Ergebnisse muss erneut auf die geringe Patientenanzahl von Genotyp 2 hingewiesen werden, da nur Werte eines Patienten dieses Genotyps für Woche 48 zu Verfügung standen und die SVR für die anderen Patienten zu einem früheren Zeitpunkt (anhand der vorhandenen Daten in Woche 24) bestimmt werden musste, bei der 7 von 8 Patienten einen negativen HCV-RNA Wert aufwiesen und somit 35 Ergebnisse die 0% in Woche 48 höchstens ein Richtwert sein kann und eine Tendenz widerspiegelt, jedoch nicht als Absolutwert für den Stand in Woche 48 angesehen werden darf. 4.2 Verlauf der laborchemischen Parameter unter Therapie und Aufgliederung in Interferon-alphacon 1 und Peginterferon-α2b 4.2.1 Verlauf der Erythrozyten und Leukozyten unter Therapie Erythrozyten (x106/µl) 6 5 4 Inferax PEG 3 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 16. Verlauf der Erythrozytentiter nach Therapieart. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). 8 Leukozyten/nl 6 4 2 Inferax PEG 0 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 17. Verlauf der Leukozytentiter nach Therapieart. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). 36 Ergebnisse Sowohl der Kurvenverlauf von Inferax (Interferon-alphacon 1) als auch von Peginterferonα2b in Bezug auf die Erythrozyten- und Leukozytenkonzentrationen ähneln dem der Genotypenaufteilung. Des weiteren verhält sich der Kurvenverlauf der beiden Therapieformen sowohl bei den Leukozyten- als auch bei den Erythrozytentitern fast deckungsgleich. Es kommt bei beiden zunächst zu einem leichten Abfall der Werte von Woche 0 bis Woche 12 und anschließend zu einem Anstieg bis Woche 48. Der Abfall bis Woche 12 beträgt bei den Erythrozyten etwa 1,0 x 106/µl für beide Therapieformen, bei den Leukozyten ist dieser im Verhältnis deutlich höher mit 4,3/nl (Interferon-alphacon 1) und 3,2/nl (Peginterferon-α2b). Der Anstieg bis Woche 48 erreicht Werte bis 4,6 x 106/µl der Erythrozytenkonzentration und Werte bis 5,4/nl der Leukozytenkonzentration. Die Erythrozytenkonzentrationen scheinen somit insgesamt konstanter zu sein und geringereren Schwankungen zu unterliegen (Abbildungen 16 und 17). 4.2.2 Verlauf des Hämoglobins unter Therapie Hämoglobinkonzentration (g/dl) 16 14 12 Inferax PEG 10 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 18. Verlauf der Hämoglobin (Hb)-Konzentration nach Therapieart. Die Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycolkonjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Der Kurvenverlauf des Hämoglobins bei Interferon-alphacon 1 und Peginterferon-α2b ist annähernd deckungsgleich, zeigt normale Hb-Werte und unterliegt ebenfalls keinen großen Schwankungen. Die Baseline liegt bei 15,0 g/dl (Peginterferon-α2b) bzw. 15,4 g/dl (Interferon-alphacon 1). Anschließend kommt es zu einem leichten Abfall auf 12,6 g/dl (Peginterferon-α2b) und 12,1 g/dl (Interferon-alphacon 1) bis Woche 12. Der Unterschied der beiden Therapieformen zeigt sich vor allem im Zeitpunkt des höchsten Abfalles. Bei 37 Ergebnisse Inferax passiert dieser erst ab Woche 2 und reicht bis Woche 12, Peginterferon-α2b hat seinen stärksten Hämoglobinabfall ganz zu Anfang von Woche 0 bis Woche 4. Dieser ist auch auf den Gesamtwert betrachtet nicht so groß wie bei der Inferaxgruppe. Bei beiden Therapieformen erholen sich die Werte wieder bis Woche 48 und liegen dort bei 13,8 g/dl (Abbildung 18). 4.2.3 Verlauf der Thrombozyten unter Therapie Thrombozyten/nl 250 200 150 Inferax PEG 100 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 19. Verlauf der Thrombozytentiter nach Therapieart. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Vergleicht man die beiden Therapieformen miteinander, zeigen sie auch bei der Thrombozytenkonzentration einen ähnlichen Kurvenverlauf (Abbildung 19). Der höchste Thrombozytenabfall (78,6/nl) ist - wie bei den Genotypen auch - in Woche 2 und zwar bei Interferon-alphacon 1 zu verzeichnen und zeigt dann bis Woche 12 konstant niedrige Werte von ca. 150/nl. Dieser liegt bei Peginterferon-α2b etwas höher mit 176/nl. Danach kommt es zu einer Erholung bis Woche 48, die bei Interferon-alphacon 1 einen steileren Verlauf nimmt und einen Wert von 221/nl erreicht (Peginterferon-α2b 207/nl). 38 Ergebnisse 4.2.4 Verlauf des Bilirubins gesamt unter Therapie Bilirubinkonzentration (µM) 18 16 14 12 10 Inferax PEG 8 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 20. Verlauf der Bilirubinkonzentration nach Therapieart. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Betrachtet man den oben angeführten Graphen des Bilirubins gesamt (Abbildung 20), so erkennt man unter beiden Therapieformen wieder einen ähnlichen Kurvenverlauf. Dieser zeigt zunächst einen Anstieg bis Woche 2 auf einen Höchstwert von 16,7 µM (bei Peginterferon-α2b) gefolgt von einem steten Abfall zunächst steiler in den Wochen 2-4 und langsamer in den darauffolgenden Wochen 12 bis 48. Das Peginterferon-α2b liegt dabei immer, wenn auch nur leicht über dem Interferon-alphacon 1 (Differenz von ca. 2-4 µM). 39 Ergebnisse 4.2.5 Verlauf der AST und ALT unter Therapie AST-Konzentration (U/l) 60 50 40 30 Inferax PEG 20 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 21. Verlauf der Aspartataminotransferase (AST)-Konzentration nach Therapieart. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). 120 ALT-Konzentration (U/l) Inferax PEG 100 80 60 40 20 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 22. Verlauf der Alaninaminotransferase (ALT)-Konzentration nach Therapieart. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycolkonjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Ähnlich wie bei den Graphen der einzelnen Genotypen zeigt sich hier ein konstanter Rückgang der AST- und ALT-Konzentrationen im Blut unabhängig von der Therapieform (Abbildung 21 und 22). Auch hier liegen die Messwerte des Peginterferon-α2b - wenn auch nur minimal - über denen des Interferon-alphacon 1 (Differenz von ca. 1-11 U/l) mit 40 Ergebnisse Ausnahme der AST-Konzentration in Woche 2 und 4, in denen das Peginterferon-α2b die Therapie mit Inferax geringfügig um ca. 4-5 U/l. unterschreitet. 4.2.6 Verlauf der GGT unter Therapie GGT-Konzentration (U/l) 80 60 40 Inferax PEG 20 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 23. Verlauf der Gamma-Glutamyltransferase (GGT)-Konzentration nach Therapieart. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Die GGT-Konzentrationen zeigen bei beiden Interferontherapien den fast gleichen Verlauf (Abbildung 23). Nach anfänglichem Anstieg der Werte in Woche 2 auf bis zu 77 U/l (bei Interferon-alphacon 1) kommt es auch hier ähnlich wie beim Verlauf des gesamten Bilirubins, sowie der AST- und ALT Konzentration zu einem steten Abfall bis Woche 48 auf Werte bis 28 U/l (Interferon-alphacon 1). 41 Ergebnisse 4.2.7 Verlauf des AST:ALT Verhältnisses unter Therapie AST/ALT-Ratio 1 0,8 0,6 Inferax PEG 24 48 0,4 0 2 4 12 Wochen nach Therapiebeginn Abbildung 24. Verlauf des Verhältnisses von Aspartataminotransferase (AST) und Alaninaminotransferase (ALT) (AST/ALT-Ratio) nach Therapieart. Das AST/ALT-Ratio wurde aus den jeweiligen Mittelwerten von AST und ALT der Patienten mit Hepatitis C Infektion der entsprechenden Therapieart (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) berechnet und ist über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Bezüglich des AST : ALT-Verhältnisses zeigen die Patienten bei beiden Behandlungsformen stets Werte kleiner 1 (Höchstwerte von 0,69 bei Peginterferon-α2b und 0,96 bei Inferax) und somit keine Zeichen einer schweren Fibrose oder Leberzirrhose, was mit den Ergebnissen der Genotypen übereinstimmt. Hierbei schneidet Inferax mit höheren Werten ebenso insgesamt schlechter ab und erreicht seinen niedrigsten Wert in Woche 24 mit 0,73 und kommt hier dem pegylierten Interferon mit 0,69 am nächsten (Abbildung 24). 42 Ergebnisse 4.2.8 Verlauf des APRI Score unter Therapie 1 APRI-Score 0,8 0,6 0,4 Inferax PEG 0,2 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 25. Verlauf des APRI Score nach Therapieart. Der APRI Score wurde wie in Material und Methoden beschrieben für die Mittelwerte der Patienten mit Hepatitis C Infektion der jeweiligen Therapieart (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) berechnet und ist über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Der APRI Score zeigt bei Inferax eine stärkere Erhöhung, besonders in Woche 2 mit einem Höchstwert von 0,81, sinkt dann aber ebenso wie bei Peginterferon-α2b und erreicht mit 0,29 etwa den gleichen Wert in Woche 48 wie Peginterferon-α2b mit entsprechend 0,30. Auch hier zeigt sich bei beiden Therapieformen keine signifikante, jedoch sicherlich eine leichte Fibrose bis Woche 4, unter der Inferaxtherapie dauert diese noch etwas länger an (bis Woche 12) (Abbildung 25). 43 Ergebnisse 4.2.9 Verlauf der HCV-RNA unter Therapie 100 % HCV-RNA pos. Patienten Inferax PEG 80 60 40 20 0 0 2 4 12 24 48 Wochen nach Therapiebeginn Abbildung 26. Verlauf der Nachweisbarkeit von Hepatitis C Virus Ribonukleinsäure (HCV-RNA) nach Therapieart. Die relativen Anteile aller Patienten mit nachweisbarer HCV-RNA in Abhängigkeit der jeweiligen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64) sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) dargestellt (Universitätsklinikum Ulm, 2000-2003). Abbildung 26 zeigt bei beiden Therapieformen einen ähnlichen Verlauf mit einem steilen Abfall der HCV-RNA Konzentration und einem Nadirwert von 13,6% HCV-RNA positiver Patienten (Peginterferon-α2b) in Woche 12 bzw. 3,6% (Inferax) in Woche 24. In Woche 48 zeigt die Gruppe mit Consensus Interferontherapie einen Anteil HCV-RNA positiver Patienten von 16%, die Gruppe mit pegylierter Interferontherapie hingegen 21,6%. 44 Ergebnisse 4.3 Verlauf anderer wichtiger klinischer Parameter unter Therapie und Aufgliederung in Genotypen 4.3.1 Grad der Fibrose (Staging) % aller Patienten 60 40 GT1 GT2 20 GT3 GT4 0 Grad 0 Grad I Grad II Grad III Grad IV Fibrose Abbildung 27. Grad der Hepatitis C Virus-induzierten Fibrose nach Genotyp. Die relativen Anteile aller Patienten der einzelnen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) in den einzelnen Fibrosestadien (Grad 0 bis Grad IV) zu Therapiebeginn sind dargestellt (Universitätsklinikum Ulm, 20002003). In Abbildung 27 werden die einzelnen Fibrosegrade in Aufgliederung in die Genotypen deutlich. Man sieht auch hier in Korrelation zur AST/ALT Ratio und dem APRI Score, dass die Gesamtheit des Patientenkollektivs keine schwergradige Fibrose aufweist. Allein die Genotypen 1 und 3 erreichen einen Fibrosegrad IV mit weniger als 10% der Patienten. Der Hauptteil weist einen Grad I oder II auf. Hier sind alle Genotypen vertreten. Bei Grad I wird der Höchstwert von 54,8% von Genotyp 1 erreicht, gefolgt von Genotyp 4 mit 50%. Bei Grad II ähnliche Werte von Genotyp 4 und Genotyp 2 mit jeweils 50%. Den Fibrosegrad 0 erreichen nur die Genotypen 1 (6,5%), 2 (16,7%) und 3 (17,3%). 45 Ergebnisse 4.3.2 Auftreten einer Steatose 80 % aller Patienten 60 40 20 0 GT1 GT2 GT3 GT4 Gesamt Abbildung 28. Grad der Hepatitis C Virus-induzierten Steatose nach Genotyp. Die relativen Anteile aller Patienten der einzelnen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4 und Gesamt n=103) mit Steatose zu Therapiebeginn sind dargestellt (Universitätsklinikum Ulm, 2000-2003). Fast 60% aller Patienten haben eine Steatose. Hierbei sind alle Genotypen betroffen, von Genotyp 1 mit 54,8% über Genotyp 2 mit 57,1% und Genotyp 3 mit 62,7% bis hin zu Genotyp 4 mit 66,7% (Abbildung 28). 4.3.3 Grad der Entzündung (Grading) % aller Patienten 80 60 GT1 40 GT2 GT3 20 GT4 0 Grad 0 Grad I Grad II Grad III Grad IV Entzündung Abbildung 29. Grad der Hepatitis C Virus-induzierten Entzündung nach Genotyp. Die relativen Anteile aller Patienten der einzelnen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4) in den einzelnen Entzündungsstadien (Grad 0 bis Grad IV) zu Therapiebeginn sind dargestellt (Universitätsklinikum Ulm, 2000-2003). 46 Ergebnisse Den höchsten Entzündungsgrad (Grad IV) erreicht Genotyp 2 mit einem Patientenanteil von 16,7% -gefolgt von Genotyp 1- jedoch nur mit 3,2%. Ein ähnliches Bild zeigt der Entzündungsgrad III, mit einem Anteil von 16,7% bei Genotyp 2 und 6,5% bei Genotyp 1. Genotyp 3 ist hier ebenso vertreten mit 9,4%. Am häufigsten bei allen Genotypen findet sich jedoch der leicht- bis mittelgradige Entzündungbereich. Grad I zeigen die Genotypen 1, 3 und 4 mit ähnlichen Prozentanteilen- Genotyp 3 mit 32,1%, Genotyp 4 mit 50% und Genotyp 1 den Höchstwert mit 51,6%. Genotyp 2 fehlt hier. Anführer bei Grad II einer nachweisbaren Entzündung ist eindeutig Genotyp 2 mit 66,7% gefolgt von Genotyp 4 mit 50% und den Genotypen 3 mit 49,1% und 1 mit 35,5%. Lediglich Patienten mit den Genotypen 1 und 3 weisen kein Entzündungsgeschehen (Grad 0) auf. Dieses Ergebnis ähnelt dem der indirekten Fibrosetests (Abbildung 29). 4.3.4 Anteil der Non-Responder 20 % aller Patienten 15 10 5 0 GT1 GT2 GT3 GT4 Gesamt Abbildung 30. Anteil der Non-Responder nach Genotyp der Hepatitis C Virus Infektion. Die relativen Anteile aller Patienten der einzelnen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4 und Gesamt n=103), die nicht auf die Therapie ansprachen (Non-Responder), sind dargestellt (Universitätsklinikum Ulm, 2000-2003). Im Folgenden wird nun der Anteil an Non-Respondern unter den einzelnen Genotypen betrachtet (Abbildung 30). Genotyp 1 zeigt mit 16,1% aller Patienten hier den höchsten Anteil. An zweiter Stelle folgt Genotyp 2 mit 12,5%. Bei Genotyp 3 sind nur 2,2% der Patienten Therapieversager, bei Genotyp 4 findet sich kein Non-Responder. In der Gesamtheit haben wir in dem Patientenkollektiv mit 8% eine Minderheit an NonRespondern. 47 Ergebnisse 4.3.5 Häufigkeit des Relapse 40 % aller Patienten 30 20 10 0 GT1 GT2 GT3 GT4 Gesamt Abbildung 31. Relapsehäufigkeit nach Therapieende nach Genotyp. Die relativen Anteile aller Patienten der einzelnen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4 und Gesamt) die nach anfänglichem Therapieerfolg zum Therapieende (48 Wochen nach Therapiebeginn) wieder nachweisbare HCV-RNA aufweisen (Relapse), sind dargestellt (Universitätsklinikum Ulm, 2000-2003). In Abbildung 31 wird nun der Relapseanteil des Patientenkollektivs im Hinblick auf die einzelnen Genotypen ersichtlich. Kein Relapse zeigen Genotyp 2-Patienten, den höchsten Relapseanteil mit 33,3% zeigen Patienten mit Genotyp 4 gefolgt von Genotyp 1 mit 16,1% und schließlich Genotyp 3 mit 15,6%. Das Patientenkollektiv hat insgesamt einen Relapseanteil von 14,9%. 48 Ergebnisse 4.3.6 Ausheilungsraten nach Genotyp 100 Ausheilungsrate (SVR) % aller Patienten eines Genotyps 80 60 40 20 0 GT1 GT2 GT3 GT4 Gesamt Abbildung 32. Ausheilungsrate nach Therapieende nach Genotyp. Die prozentuale Ausheilungsrate (Sustained Virological Response Rate, SVR) der Patienten der einzelnen Genotypen (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4 und Gesamt n=103) zum Therapieende (48 Wochen nach Therapiebeginn), ist dargestellt (Universitätsklinikum Ulm, 2000-2003). Die Gesamtausheilungsrate ist mit 77% sehr hoch, wie Abbildung 32 zeigt. Patienten des Genotyps 2 zeigen mit 87,5% die höchste Ausheilungsrate, gefolgt von Genotyp 3 mit 82,2%, Genotyp 1 mit 67,7% und schließlich Genotyp 4 mit 66,7% (Abbildung 34). 49 Ergebnisse 4.4 Verlauf anderer wichtiger klinischer Parameter unter Therapie und Aufgliederung in Interferon-alphacon 1 und Peginterferon-α2b 4.4.1 Anteil der Non-Responder 20 % aller Patienten 15 10 5 0 Inferax PEG Gesamt Abbildung 33. Anteil der Non-Responder nach Therapieart. Die relativen Anteile aller Patienten der einzelnen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64, Gesamt n=103) die nicht auf die Therapie ansprachen (Non-Responder) sind dargestellt (Universitätsklinikum Ulm, 2000-2003). Mit ca. 10,3% finden sich in der mit Peginterferon-α2b behandelten Gruppe deutlich mehr Non-Responder als in der Consensus-Interferongruppe mit 3,4% (Abbildung 33). 50 Ergebnisse 4.4.2 Relapsehäufigkeit % aller Patienten einer Therapieart 20 15 10 5 0 Inferax PEG Gesamt Abbildung 34. Relapsehäufigkeit nach Therapieende nach Therapieart. Die relativen Anteile aller Patienten der einzelnen Therapiearten (Inferax n=39 vs. Polyethylenglycol-konjugiertes Interferon-α (PEG) n=64, Gesamt n=103) die nach anfänglichem Therapieerfolg zum Therapieende (48 Wochen nach Therapiebeginn) wieder nachweisbare HCV-RNA aufweisen (Relapse), sind dargestellt (Universitätsklinikum Ulm, 2000-2003). Bezüglich des Auftretens eines Relapse schneidet die PEG-Interferongruppe geringfügig besser ab. Der Anteil der Patienten, die einen solchen Rückfall aufweisen, beträgt hier 13,8%, die Consensus Interferongruppe erreicht einen Wert von 17,2% (Abbildung 34). 51 Ergebnisse 4.4.3 Ausheilungsraten nach Therapie 100 Ausheilungsrate (SVR) % aller Patienten einer Behandlungsart 80 60 40 20 0 Inferax PEG Gesamt Abbildung 35. Ausheilungsrate nach Therapieart. Die prozentuale Ausheilungsrate (Sustained Virological Response Rate, SVR) der Patienten der einzelnen Therapiearten (Inferax n=39 vs. Polyethylenglycolkonjugiertes Interferon-α (PEG) n=64, Gesamt n=103) zum Therapieende (48 Wochen nach Therapiebeginn), ist dargestellt (Universitätsklinikum Ulm, 2000-2003). Abbildung 35 zeigt, dass sich innerhalb des ausgewerteten Patientenkollektivs nur geringfügige Unterschiede bezüglich der beiden Kombinationstherapien auf die Ausheilungsraten ergeben. Die SVR beträgt bei der Behandlung mit Peginterferon-α2b 75,9%, bei der Consensus Interferongruppe 79,3%. 52 Ergebnisse 4.4.4 Ausheilungsrate unter Berücksichtigung der einzelnen Nadirwerte Tabelle 3. Erreichzeitpunkte der Nadirwerte (Wochen nach Therapiebeginn) nach Hepatitis C Virus Genotyp (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4 und Gesamt n=103). Die Nadirwerte wurden als die jeweils niedrigsten Werte der arithmetischen Mittel der jeweiligen Laborparameter nach Genotyp über alle Messzeitpunkte bestimmt (s. Material und Methoden). Die Erreichzeitpunkte der jeweiligen Nadirwerte sind in der Tabelle aufgetragen. Leuko Leukozyten, Ery Erythrozyten, Hb Hämoglobin, Thrombo Thrombozyten, Bili Bilirubin (Universitätsklinikum Ulm, 2000-2003). Genotyp GT1 Leuko 48 Ery 48 Hb 24 Thrombo 2 Biliges. 48 AST 24 ALT 48 GGT 48 GT2 12 24 12 12 24 48 48 48 GT3 12 12 24 12 24 48 48 48 GT4 4 12 12 4 12 24 12 24 Gesamt 12 12 24 12 48 48 48 48 Aus Tabelle 3 wird ersichtlich, dass die Nadirwerte (Gesamt - ohne Aufgliederung in die einzelnen Genotypen) der Leukozyten- , Erythrozyten- und Thrombozytentiter in Woche 12 erreicht werden. Der tiefste Wert des Hämoglobins wird in Woche 24 erreicht. Die erhöhten leberspezifischen Parameter AST, ALT, GGT und Bilirubin gesamt erholen sich am langsamsten mit Erreichen des Nadirwertes in Woche 48. Des weiteren lässt eine Unterteilung in die Genotypen erkennen, dass Genotyp 1 im Hinblick auf den Nadirwert der Leukozyten, Erythrozyten und des Bilirubins gesamt, deutlich höher ist im Vergleich zu den Genotypen 2 und 3. Tabelle 4. Höhe der einzelnen Nadirwerte nach Genotyp (GT1 n=35, GT2 n=8, GT3 n=56, GT4 n=4 und Gesamt n=103). Die Nadirwerte wurden als die jeweils niedrigsten Werte der arithmetischen Mittel der jeweiligen Laborparameter nach Genotyp über alle Messzeitpunkte bestimmt (s. Material und Methoden). Leuko Leukozyten, Ery Erythrozyten, Hb Hämoglobin, Thrombo Thrombozyten, Bili Bilirubin (Universitätsklinikum Ulm, 2000-2003). GT1 Leuko (1/nl) 3,4 Ery Hb Thrombo (106/µl) (g/dl) (1/nl) 4,0 12,2 161,5 GT2 3,3 3,9 11,7 121,6 11,4 18,0 19,0 13,0 GT3 3,3 4,1 12,7 163,0 9,2 22,4 29,9 27,7 GT4 4,2 4,7 14,4 176,0 9,0 21,0 34,8 21,7 Gesamt 3,5 4,1 12,5 162,4 9,6 25,2 32,2 29,9 53 Biliges. (µM) 9,6 AST (U/l) 24,8 ALT (U/l) 32,4 GGT (U/l) 33,3 Ergebnisse Die einzelnen Werte des jeweiligen Nadir sind – nach Genotyp unterteilt – in Tabelle 4 aufgeführt. Es zeigt sich, dass Genotyp 2 bei allen laborchemischen Parametern -außer beim Bilirubingehalt- den niedrigsten Nadirwert besitzt. Des Weiteren erreichen die Nadirwerte der Leukozyten-, Erythrozyten-, Thrombozyten- und Hämoglobinkonzentrationen vereinzelt den pathologischen Bereich und zeigen im Vergleich zur Baseline deutlich einen Abfall im Verlauf an. Im Gegensatz dazu sind die Leberwerte AST, ALT und GGT unter Therapie anfangs stark erhöht und liegen im pathologischen Bereich, nähern sich beim Nadir jedoch wieder ihrem physiologischen Bereich an. Der Nadirwert der Bilirubinkonzentration hingegen liegt bei allen Genotypen im physiologischen Bereich. Tabelle 5. Höhe und Erreichzeitpunkte der einzelnen Genotypen der Nadirwerte (Woche 0-12) für Leukozyten, Thrombozyten und Hämoglobin. Die Nadirwerte wurden als die jeweils niedrigsten Werte der arithmetischen Mittel der jeweiligen Laborparameter über alle Messzeitpunkte bestimmt (s. Material und Methoden). Genotypen 1 und 4 sowie 2 und 3 wurden für diese Auswertung zusammengefasst und die Werte sind aufgegliedert nach Respondern (Genotyp 1+4 n=23, Genotyp 2+3 n=44), Non-Respondern (Genotyp 1+4 n=5, Genotyp 2+3 n=2) und Relapse-Patienten (Genotyp 1+4 n=6, Genotyp 2+3 n=7). Leuko Leukozyten, Hb Hämoglobin, Thrombo Thrombozyten (Universitätsklinikum Ulm, 2000-2003). Nadirwerte Leuko/nl % Abfall von Woche 0 Woche Thrombo/nl % Abfall von Woche 0 Woche Hb (g/dl) % Abfall von Woche 0 Woche Genotyp 1+4 (n=34) Genotyp 2+3 (n=53) Responder Non-Responder Relapse Responder Non-Responder Relapse 4,0 3,1 3,3 3,1 3,1 3,4 46 12 174 45 12 129 51 12 136 55 12 159 55 4 79 45 4 155 29 2 12,3 28 12 12,4 42 4 13,4 32 12 13,3 46 12 12,4 18 2 12,4 18 12 22 12 12 12 11 4 21 12 14 12 Tabelle 5 zeigt die Nadirwerte der Leukozyten-, Hämoglobin- und Thrombozytentiter aufgegliedert in das jeweilige Therapieansprechen der Patienten mit den Genotypen 1+4 bzw. 2+3. Außerdem ist der Erreichzeitpunkt des jeweiligen Nadir sowie dessen %-Abfall bezogen auf den Ausgangswert in Woche 0 dargestellt. Bei den Genotypen 1+4 zeigen die Responder bei den Leukozytentitern den höchsten Nadirwert von 4,0/nl und damit einen Abfall um 46% bezogen auf den durchschnittlichen 54 Ergebnisse Ausgangswert aller Responderpatienten in Woche 0. Den niedrigsten Nadir erreichen die Nonresponder mit 3,1/nl (jedoch geringste%-Abfall um 45%). Den grössten %-Abfall mit 51% haben hier die Relapsepatienten. Sie erreichen jedoch mit 3,3/nl nicht den niedrigsten absoluten Nadirwert. Die Nadirwerte aller Therapieansprecharten der Genotypen 1+4 werden zum gleichen Zeitpunkt in Woche 12 erreicht. Die Responder und Non-Responder der Genotypen 2+3 haben den gleichen Leukozyten-Nadirwert von 3,1/nl und den gleichen %-Abfall um 55%, jedoch einen anderen Erreichzeitpunkt. Dieser liegt bei den Respondern später, bei Woche 12. Die Non-Responder erreichen den Nadir in Woche 4. Der Nadirwert der Relapsepatienten liegt etwas höher bei 3,4/nl und wird ebenfalls früh erreicht in Woche 4. Der %-Abfall ist niedriger mit 45%. Die Responder der Genotypen 1 + 4 zeigen bei der Hämoglobinkonzentration den niedrigsten Nadirwert von 12,3 g/dl, der %-Abfall ist jedoch mit 18% nur der zweithöchste nach den Non-Respondern mit einem Abfall von 22%. Alle Therapieansprechraten erreichen ihren Nadir in Woche 12. Bei den Genotypen 2+3 hingegen haben die Responder den höchsten Nadirwert von 13,3 g/dl, mit 11% den niedrigsten Abfall, aber den frühesten Erreichzeitpunkt in Woche 4. Die Thrombozytenkonzentration der Responder der Genotypen 1+4 ist auf den Nadirwert bezogen der höchste mit 174/nl, gefolgt von den Relapsepatienten mit 136/nl und den Non-Respondern mit 129/nl. Der %-Abfall folgt dieser Reihenfolge nicht. Die Responder zeigen jedoch den frühesten Erreichzeitpunkt des Nadir in Woche 2, gefolgt von den Relapsepatienten in Woche 4 und den Non-Respondern in Woche 12. Bei den Genotypen 2+3 zeigen die Responder ebenfalls den höchsten Nadirwert von 159/nl, gefolgt von Patienten mit einem Relapse (155/nl) und den Non-Respondern (79/nl). Der %-Abfall und auch die Erreichzeitpunkte lassen diese Reihenfolge nicht erkennen. 55 Ergebnisse 4.5 Verlauf ausgewählter laborchemischer Parameter unter Aufgliederung nach Therapieansprechen und Zusammenfassung von GT1/4 und GT2/3 4.5.1 Verlauf der Leukozytentiter 8 Leukozyten/nl Responder Non-Responder Relapse 6 4 2 0 2 4 12 Wochen nach Therapiebeginn Abbildung 36. Verlauf der Leukozyten von Patienten der Genotypen 1 und 4 aufgegliedert nach Respondern, Non-Respondern und Relapse-Patienten bis Woche 12. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen 1 und 4 sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) und aufgegliedert nach Respondern (n=23), Non-Respondern (n=5) und RelapsePatienten (n=6) dargestellt (Universitätsklinikum Ulm, 2000-2003). Abbildung 36 zeigt den jeweiligen Leukozytenverlauf bis Woche 12 der Genotypen 1+4 der Responder, Non-Responder und den Patienten, die im Laufe der Therapie einen Relapse erlitten. Man erkennt, dass sich die Responder und Relapsepatienten im Verlauf sehr ähneln. Beide Therapieantworten zeigen insgesamt bis Woche 12 einen Abfall um die Hälfte des Ausgangswertes. Die Leukozytenwerte sinken bei den Respondern um 45,9%, bei den Relapsepatienten geringfügig mehr um 50,7% im Vergleich zum Ausgangswert in Woche 0. Der stärkste Abfall ist bei beiden bis Woche 2 zu verzeichnen: der Wert der Responder sinkt um 43,2%, der Wert der Relapsepatienten um 46,3%. Ein Unterschied lässt sich ab Woche 2 erkennen. Während die Responder bis Woche 12 sehr konstant bleiben, erfahren die Relapsepatienten ab Woche 4 einen erneuten Abfall um 10,8%. Die Non-Responder lassen einen ähnlich starken Abfall der Leukozytenkonzentration um 45,6% des Ausgangswertes bis Woche 12 erkennen. Der steilste Abfall erfolgt jedoch später von Woche 2 bis 4 um 32,7%. Dieser ist bei weitem niedriger als bei den anderen Therapieverläufen. 56 Ergebnisse 8 Leukozyten/nl Responder Non-Responder Relapse 6 4 2 0 2 4 Wochen nach Therapiebeginn 12 Abbildung 37. Verlauf der Leukozyten von Patienten der Genotypen 2 und 3 aufgegliedert nach Respondern, Non-Respondern und Relapse-Patienten bis Woche 12. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der jeweiligen Genotypen 2 und 3 sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) und aufgegliedert nach Respondern (n=44), Non-Respondern (n=2) und RelapsePatienten (n=7) dargestellt (Universitätsklinikum Ulm, 2000-2003). In Abbildung 37 ist der Leukozytenverlauf der Genotypen 2+3 nach dem jeweiligen Therapieansprechen dargestellt. Der stärkste Abfall ist bei allen bis Woche 2 erkennbar (Responder und Non-Responder um 39,1%, Relapsepatienten um 35,5% zum Ausgangswert der Baseline). Anders als bei den Genotypen 1+4 zeigen die Responderpatienten der Genotypen 2+3 ab Woche 2 einen erneuten Abfall der Leukozytenkonzentration bis Woche 12, wohingegen die Non-Responder und Patienten mit einem Relapse nach Woche 4 geringfügig wieder ansteigen, die Non-Responder hier stärker um 9,7% (Relapse um 2,9%). 57 Ergebnisse 4.5.2 Verlauf der Hämoglobinkonzentration Hämoglobinkonzentration (g/dl) 16 Responder Non-Responder Relapse 14 12 0 2 4 12 Wochen nach Therapiebeginn Abbildung 38. Verlauf der Hämoglobinkonzentration von Patienten der Genotypen 1 und 4 aufgegliedert nach Respondern, Non-Respondern und Relapse-Patienten bis Woche 12. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der Genotypen 1 und 4 sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) und aufgegliedert nach Respondern (n=23), Non-Respondern (n=5) und Relapse-Patienten (n=6) dargestellt (Universitätsklinikum Ulm, 2000-2003). Beim Verlauf der Hämoglobinkonzentration zeigen Responder der Genotypen 1+4 einen konstanten Abfall (Differenz von 6,7% bis Woche 2, weiterer Abfall um 6,4% bis Woche 4 und 6,1% bis Woche 12). Die Non-Responder und Relapsepatienten hingegen haben den höchsten Abfall von Woche 2 bis 4 (um 14,9% bzw. 6,8%). Der weitere Abfall von Woche 4 bis Woche 12 ist deutlich geringer als bei den Respondern (1,6% bei den NonRespondern, 2,9% bei den Relapsepatienten) (Abbildung 38). 58 Ergebnisse Hämoglobinkonzentration (g/dl) 16 14 12 Responder Relapse 0 Non-Responder 2 4 Wochen nach Therapiebeginn 12 Abbildung 39. Verlauf der Hämoglobinkonzentration von Patienten der Genotypen 2 und 3 aufgegliedert nach Respondern, Non-Respondern und Relapse-Patienten bis Woche 12. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der Genotypen 2 und 3 sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) und aufgegliedert nach Respondern (n=44), Non-Respondern (n=2) und Relapse-Patienten (n=7) dargestellt (Universitätsklinikum Ulm, 2000-2003). Abbildung 39 zeigt den Verlauf der Hämoglobinkonzentration der Genotypen 2+3 des jeweiligen Therapieansprechens. Die Responder zeigen einen Abfall bis Woche 4 mit dem steilsten %-Abfall zwischen Woche 2 und 4 um 9,5% und um insgesamt 11,4% bis Woche 4 zum Ausgangswert in Woche 0. Dann folgt ein erheblicher Wiederanstieg von Woche 4 bis Woche 12 um 19,5%. Relapsepatienten haben ebenfalls von Woche 2 bis Woche 4 ihren stärksten %-Abfall um 8%. Non-Responder zeigen ihren größten %-Abfall früher von Woche 0 bis 2 um 13,3%. Im Gegensatz zu den Respondern zeigen die Non-Responder und Relapsepatienten keinen erneuten Wiederanstieg bis Woche 12. 59 Ergebnisse 4.5.3 Verlauf der Thrombozytentiter 250 Thrombozyten/nl Responder Non-Responder Relapse 200 150 100 0 2 4 Wochen nach Therapiebeginn 12 Abbildung 40. Verlauf der Thrombozyten von Patienten der Genotypen 1 und 4 aufgegliedert nach Respondern, Non-Respondern und Relapse-Patienten bis Woche 12. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der Genotypen 1 und 4 sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) und aufgegliedert nach Respondern (n=23), Non-Respondern (n=5) und Relapse-Patienten (n=6) dargestellt (Universitätsklinikum Ulm, 2000-2003). Die Responder der Genotypen 1+4 haben beim Verlauf der Thrombozytenkonzentration den stärksten Abfall sehr früh, von Woche 0 bis Woche 2 um 28,4%. Ebenso zeigen sie mit diesem Wert den höchsten Abfall überhaupt. Die Patienten mit einem Relapse sinken um max. 24,4% zur selben Zeit, wohingegen die Non-Responder erst sehr viel später -von Woche 4 bis Woche 12- ihren größten Abfall um 19,9% haben. Des weiteren wird ersichtlich, dass sich die Responder auch wieder am frühesten und längsten erholen bezogen auf die Thrombozytenkonzentration (ab Woche 2 bis Woche 12 um insgesamt 9,2%). Diese Erholung findet bei den Non-Respondern ebenfalls zum gleichen Zeitpunkt statt (ab Woche 2), jedoch nur bis Woche 4 und einem deutlich geringeren Anteil von 3,8%. Dann erfolgt bei den Non-Respondern bis Woche 12 ein erneuter Abfall von 19,9% bezogen auf den Wert zu Woche 4. Die Relapsepatienten hingegen zeigen eine Erholung erst später ab Woche 4 bis Woche 12 und auch einen geringeren %-Anteil von 5,1% im Gegensatz zu den Respondern (Abbildung 40). 60 Ergebnisse 250 Responder Non-Responder Relapse Thrombozyten/nl 200 150 100 50 0 2 4 Wochen nach Therapiebeginn 12 Abbildung 41. Verlauf der Thrombozyten von Patienten der Genotypen 2 und 3 aufgegliedert nach Respondern, Non-Respondern und Relapse-Patienten bis Woche 12. Die Mittelwerte aller Patienten mit Hepatitis C Infektion der Genotypen 2 und 3 sind über den zeitlichen Therapieverlauf (Wochen nach Therapiebeginn) und aufgegliedert nach Respondern (n=44), Non-Respondern (n=2) und Relapse-Patienten (n=7) dargestellt (Universitätsklinikum Ulm, 2000-2003). In der Abbildung 41 ist der Verlauf der Thrombozytenkonzentration der Genotypen 2+3 im Hinblick auf das Therapieansprechen dargestellt. Die Responder zeigen hier ebenso ihren stärksten Abfall sehr früh von Woche 0 bis Woche 2 um 24,7%. Dies ist jedoch nicht der insgesamt grösste Abfall. Diesen zeigen die Non-Responder mit 34,7% erst sehr viel später von Woche 4 bis Woche 12. Die Relapsepatienten erreichen ihren max. Abfall wieder früher von Woche 0 bis Woche 2 um 18,4%. Sie sind ebenso die einzigen unter den Genotypen 2+3, die eine Erholung von Woche 2 bis Woche 4 um 8,4% haben. 61 Diskussion 5 Diskussion In dieser Arbeit wurden Daten eines Studienkollektivs herangezogen, dessen Patienten nachweislich an einer chronischer Hepatitis C erkrankt waren und sich von Januar 2000 bis April 2003 am Universitätsklinikum Ulm einer Kombinationstherapie mit Interferon und dem Nukleosidanalogon Ribavirin unterzogen haben. Hierbei wurden zwei chemisch verschiedene Interferonarten gewählt: Interferon-alphacon 1, das sogenannte Consensus Interferon und Peginterferon-α-2b, eine pegylierte Interferonform. Zum Zeitpunkt der PACT-Studie gehörten diese Therapieformen laut Leitlinie der Deutschen Gesellschaft für Verdauungs- und Stoffwechselkrankheiten beide zur Standardtherapie bei Behandlung einer chronischen Hepatitis C Infektion [1]. Die Therapie mit pegyliertem Interferon (in Kombination mit Ribavirin) ist jedoch durch eine Steigerung der dauerhaften Ansprechraten und eine vereinfachte Handhabung durch eine Reduktion der Applikationshäufigkeit von ursprünglich mehrmals wöchentlich auf einmal pro Woche gekennzeichnet [1]. Diese Tatsache führte unter anderem zu einer größeren Compliance der Patienten. Daher etablierte sich bei der Behandlung einer chronischen Hepatitis C die Kombinationstherapie aus Peginterferon-α-2a bzw. -2b und Ribavirin als Goldstandard [32]. In unserem Studienkollektiv wurde den Patienten Peginterferon-α-2b (80-150 µg) einmal wöchentlich bzw. Interferon-alphacon 1 (9-27 µg) täglich als Injektion verabreicht. 8 Patienten erhielten für die ersten 12 Wochen zunächst eine Monotherapie mit Hochdosisinterferon--2b (Intron A, zunächst 107 I.E. in den ersten 2 Wochen, dann 5x107 I.E. für 10 Wochen), und ab Woche 13 eine Anschlusstherapie als Erhaltungstherapie mit PEG-Interferon plus Ribavirin. Bei Ribavirin erfolgte ebenso jeweils eine tägliche Einnahme von 800 bis 1200 mg oral als Kapsel oder Filmtablette. In der Gesamtheit wurden Daten von 103 Patienten ausgewertet, wobei 39 Patienten der Studie Consensus Interferon und 64 Patienten Peginterferon-α2b verabreicht bekamen. In die endgültige Analyse konnten jedoch nur 87 Patienten eingeschlossen werden. Gründe hierfür waren v.a. die mangelnde Compliance der Patienten bei hohem Nebenwirkungsprofil und langer Studienzeit. Es kam zu einem vorzeitigen, selbständigen 62 Diskussion Therapieabbruch oder zur Nichtwahrnehmung der Kontrolltermine v.a. gegen Ende der Studie. Bei 35 Patienten wurde der Genotyp 1, bei 8 Patienten Genotyp 2, bei 56 Genotyp 3 und bei 4 Patienten Genotyp 4 diagnostiziert. Der wichtigste Parameter zur Kontrolle des Therapieansprechens und des Therapieverlaufes war die quantitative und qualitative Messung der Viruslast (HCV-RNA) mittels RT-PCR. Die Hauptfragestellung dieser Arbeit liegt nun in der Auswertung, inwiefern eine Aussage hinsichtlich des Therapieansprechens, des Therapieverlaufes und der Ausheilungsrate getroffen werden kann, wenn man den Verlauf einzelner laborchemischer Parameter je nach Genotyp und je nach Interferon unter Therapie verfolgt und ob diese Parameter die HCV-RNA potentiell als wegweisenden Kontrollmarker in der Zukunft zuverlässig ersetzen könnten. Dies würde v.a. eine Einsparung von Kosten und Aufwand bedeuten, da das Erheben von einzelnen laborchemischen Parametern deutlich kostengünstiger ist und weniger Aufwand bedeutet als die mehrfache Durchführung einer RT-PCR. Des Weiteren werden Aspekte wie die Ausgangshistologie, der Relapse- und NonResponderanteil sowie die einzelnen Nadirwerte berücksichtigt, ob diese Aufschluss über die Ausheilungsrate liefern. Bezüglich der HCV-RNA-Viruslast sprechen die Genotypen 2 und 3 verglichen mit den Genotypen 1 und 4 deutlich schneller auf die Therapie an, weisen die niedrigsten Prozentsätze HCV-RNA positiver Patienten und somit den besten Therapieerfolg nach Therapieende auf. Dies deckt sich mit den Ergebnissen der Ausheilungsrate (SVR) und den Ergebnissen vergleichbarer Studien. So zeigen Maieron et al. 2010, dass Patienten mit den Genotypen 2 und 3 eine bessere SVR mit insgesamt 67,8% erzielten als Patienten mit den Genotypen 1 und 4, die lediglich eine Ausheilungsrate von 35,4% besaßen [30]. Ebenso schreiben Cuenca et al. 2010, dass in Ihrer Studie mehr als 50% der Patienten mit Genotyp 1 keine Ausheilung unter antiviraler Therapie erfuhren [10]. Vergleicht man den Anteil HCV-RNA positiver Patienten der beiden Therapieformen, so zeigen sich weniger ausgeprägte Unterschiede als bei der Aufgliederung nach Genotypen und auch eine geringere Übereinstimmung mit der Ausheilungsrate (SVR). Die Consensus 63 Diskussion Interferongruppe mit Interferon-alphacon 1 schneidet hinsichtlich der SVR überraschenderweise besser ab als die PEG-Interferongruppe und zeigt einen steileren Abfall und insgesamt niedrigeren Verlauf des prozentualen Anteils an HCV-RNA positiven Patienten. Diese Beobachtung könnte möglicherweise in der im Vergleich zum pegylierten Interferon höheren Interferonrezeptoraffinität des Consensus Interferons begründet liegen [5]. Die Ausheilungsraten sind jedoch mit einer Differenz von nur 3,4% annähernd gleich. Mögliche Ursachen für diese Differenz können u.a. die höhere Anzahl der NonResponder (10,3% der PEG-Gruppe gegenüber 3,4% der mit Consensus Interferon behandelten Gruppe), eine insgesamt höhere Anzahl an untersuchten Patienten in der PEG-Gruppe, und eine geringere Anzahl an auszuwertenden Daten bei dieser Gruppe im Langzeitverlauf sein (HCV-RNA in Woche 48 wurde bei 27 PEG-Interferonpatienten nicht erhoben). Eine genauere Betrachtung dieser möglichen Störfaktoren, die ebenfalls bei den Genotypen eine Rolle spielen und zu einer Verzerrung und Verschiebung der ausgewerteten Daten führen können, folgt. Erstaunlicherweise erzielt im analysierten Studienkollektiv die Gruppe, die mit ConsensusInterferon therapiert wurde ein besseres Ergebnis mit einer konstant niedrigeren Anzahl an HCV-RNA positiven Patienten und widerspricht hier der gängigen Literatur. Laut Zeuzem et al. 2004 weist zwar eine niedrig dosierte Peginterferon-α2b Therapie keine besseren dauerhaften virologischen Ansprechraten auf im Vergleich zu Standardinterferon (47% SVR), dies ändert sich jedoch bei höherer Dosierung des Peginterferon-α2b. Bei einer Applikation von 1,5 µg/kg KG/Woche Peginterferon-α2b plus Ribavirin konnte die SVR von 47 auf 54% gesteigert werden [53]. Mögliche Ursachen der unterschiedlichen Ergebnisse unseres Studienkollektivs zur Literatur sind ebenfalls die oben angeführten Störfaktoren. Setzt man die Leukozytenkonzentrationen in Bezug zur Ausheilungsrate und zur Anzahl HCV-RNA positiver Patienten, so erkennt man sowohl bei Auswertung nach Genotypen, als auch nach Therapieform, dass ein insgesamt steilerer Abfall der Leukozytenwerte unter die Normgrenze von 4-10/nl, sowie eine schnellere Erholung der Werte nach Therapieende auf eine insgesamt höhere SVR und eine niedrigere Anzahl HCV RNApositiver Patienten schließen lassen. Dies trifft insbesondere – wie oben bereits beschrieben – für Patienten mit den Genotypen 2 und 3, sowie für die Consensus 64 Diskussion Interferongruppe zu. Der eigentliche Leukozytenverlauf mit beginnendem Abfall zu Therapiebeginn und anschließender Erholung nach Therapieende ist sicherlich eine typische Nebenwirkung der Therapie mit Interferon durch Supression des Knochenmarks [49]. Interferon kann daher ebenso einen Einfluss bei der Steile des Abfalls und des erneuten Wiederanstiegs der Leukozyten spielen und somit eine Korrelation zur Ausheilungsrate und der Anzahl HCV-RNA- positiver Patienten begründen. Folglich kann anhand der Leukozytentiter und deren Verlauf keine klare Aussage getroffen werden bezüglich Virustiter und Ausheilungsverlauf. Hierzu bedarf es weiterer Studien, die dies untersuchen. Ebenso bleibt unklar, inwiefern das Leukozytenprofil von bereits negativ gewordenen Patienten bezüglich der HCV-RNA unter Interferontherapie mit dem HCVRNA positiver Patienten übereinstimmt und somit eine Schlussfolgerung und Korrelation bezüglich der Viruslast gezogen werden kann. Da die Erythrozytenkonzentration während des gesamten Therapieverlaufes weitgehend im Normbereich bleibt, keinen großen Schwankungen unterliegt und nur kurzfristig von Patienten des Genotyps 2 in den Wochen 12 und 24 geringfügig unterschritten wird, scheint diese somit keinen signifikanten Aufschluss sowohl über die aktuelle HCV Infektion, noch über den Therapieerfolg im Verlauf zu geben. Dieselbe Tendenz wie bei den Leukozyten scheint jedoch auch hier vorhanden zu sein. Tendenziell lassen niedrigere Erythrozytenwerte während der Therapie – wie diese v.a. bei den Genotypen 2 und 3 in den Wochen 4 und 12 vorkommen – und eine schnelle Erholung nach Therapieende eine bessere Ausheilungsrate vermuten. Eine signifikante Korrelation fehlt auch hier. Zudem müssen die typischen Nebenwirkungen des Ribavirins mitberücksichtigt werden. So beschreiben Vcev et al. 2009, dass eine Therapie mit Ribavirin zu einer dosisabhängigen reversiblen intravaskulären Anämie bei 10% der Patienten führen kann [51]. Dies ist sicherlich ein Grund für die leichten Abfälle der Erythrozytenkonzentration und des Hämoglobins unter Therapie. 65 Diskussion Der Hämoglobingehalt bei der Genotypenunterteilung unterliegt zwar zeitweise starken Schwankungen, liegt aber während des gesamten Therapieverlaufes und nach Therapieende im Normbereich und kann somit die Viruslast bzw. die HCV-RNA nicht als Kontrollparameter in Zukunft ersetzen. Des Weiteren zeigen die Therapieformen hinsichtlich der Erythrozytenkonzentration annähernd kongruente Kurvenverläufe und somit keine signifikanten Unterschiede, was auf eine spezifische Korrelation zur SVR hinweisen könnte. Beim Verlauf der Hämoglobinkonzentration zeigt sich jedoch bei den Therapieformen folgender Unterschied. Während bei PEG-Interferon der steilste Hämoglobinabfall bereits sehr früh von Woche 0 bis 4 stattfindet, ist dieser bei der – im Hinblick auf die SVR – besser abschneidenden Inferaxgruppe später in den Wochen 2 bis 12 zu beobachten und fällt auch größer aus. Somit resultiert die Tendenz eines besseren Therapieansprechens (SVR) aus einem größeren und zeitlich später auftretenden Abfall der Hämoglobinkonzentration während der Therapie. Dieses Ergebnis bestätigt sich später in der Diskussion bei Auswertung nach Therapieansprechen. Insofern als die Thrombozytenkonzentrationen bei allen Patienten mit Ausnahme von Patienten des Genotyps 2 ebenso im Normbereich bleiben, zeigen sie (außer Genotyp 2) einen ähnlichen Verlauf wie die bisher betrachteten Parameter. Der zu beobachtende initiale Abfall der Thrombozytenkonzentration mit anschließender langsamer Erholung ist wie bei den Leukozyten wahrscheinlich auf die typische Nebenwirkung der Interferontherapie zurückzuführen. Daher sind regelmäßige laborchemische Kontrollen jedes Patienten unter Interferontherapie von großer Bedeutung. Laut der Literatur kommt es bei 30% bis 40% der Patienten unter Kombinationstherapie von Interferon und Ribavirin zu einer Blutbildveränderung (u.a. einer Thrombopenie), die zu einer Dosisreduktion der Medikamente führen kann [1]. Eine klare Aussage bezüglich Ausheilungsrate lässt sich jedoch nicht treffen. Der andersartige, alternierende Verlauf von Genotyp 2 wird sicherlich von der geringen Patientenanzahl beeinflusst (in Woche 48 konnten insgesamt nur die Daten eines Patienten erhoben werden). Dennoch zeigt Genotyp 4 mit einer ebenso geringen Patientenanzahl eine weitaus größere Ähnlichkeit des Kurvenveralufs mit den Genotypen 1 und 3. Die Genotypen mit der höchsten SVR (Genotyp 2 und 3) hingegen zeigen hier keinerlei Übereinstimmung in ihrem Verhalten 66 Diskussion und somit kann auch keine klare Korrelation bezüglich des Verlaufs der Thrombozytenkonzentration und der SVR aufgezeigt werden. Was die Therapieformen bei der Thrombozytenkonzentration angeht, so ist ebenfalls ein steilerer Abfall und Wiederanstieg, sowie insgesamt niedrigere Werte wie sie die InferaxGruppe zeigt, einer besseren SVR gegenüberzusetzen. In unserem Patientenkollektiv wurde bei regelmässiger Blutentnahme zur Kontrolle der laborchemischen Parameter jeweils das gesamte Bilirubin, bestehend aus direktem und indirektem Bilirubin gemessen. Der Bilrubingehalt (gesamt) der einzelnen Genotypen zeigt zunächst zu Therapiebeginn eine leichte Erhöhung mit anschließendem Abfall. Der Gesamtverlauf bleibt jedoch konstant im Normbereich (außer bei Genotyp 2) und zeigt kaum Differenzen zwischen Werten der Baseline und Werten in Woche 48. Die kurzzeitig starke Erhöhung von Genotyp 2 in Woche 2 auf 26 µM bleibt- wie bereits bei der Thrombozytenkonzentrationhinsichtlich der Aussagekraft auf die SVR aufgrund der geringen Patientenzahl und der geringen Übereinstimmung mit Genotyp 3 fraglich. Einen ähnlichen Verlauf weisen die beiden Interferonformen auf, wobei das PEGInterferon insgesamt höhere Bilirubinkonzentrationen erreicht. Vergleicht man nun die Anzahl HCV-RNA positiver Patienten und die SVR mit den einzelnen Bilirubingraphen, so lässt sich kein eindeutiger Bezug herstellen. Der anfänglich starke Rückgang der HCV-RNA positiven Patientenzahl in Woche 2 steht zwar einer konstanten Bilirubinerhöhung gegenüber, diese ist jedoch nicht signifikant, ebenso zeigen sich keine genotyp- oder interferonspezifischen Eigenschaften, die mit der SVR in Zusammenhang gebracht werden könnten. Somit zeigt sich, dass der Bilirubingehalt zwar nach wie vor ein guter Marker zur aktuellen Leberfunktion ist, jedoch keine Aussagekraft bezüglich der Viruslast und der Ausheilungsrate hat. Weitere Parameter, die eine Leberzellschädigung anzeigen und somit potentiell gut geeignet sind, der Erkennung und Verlaufsbeobachtung von Lebererkrankungen zu dienen, sind die Enzyme Aspartat-Aminotransferase (AST), die Alanin-Aminotransferase (ALT) sowie die Gamma-Glutamyltransferase (GGT). Diese Enzyme werden in der Leber synthetisiert und ermöglichen als Biokatalysatoren leberspezifische Stoffwechselvorgänge 67 Diskussion der Zellen. Bei Leberzellschädigung oder Zellverlust steigt die Konzentration dieser Enzyme im Blut an. ALT ist hierbei leberspezifischer, AST findet sich auch in der Muskulatur, GGT dagegen spricht eher für alkoholische Leberschäden oder Galleabflusstörungen. Dabei sagt die Höhe der Aktivität der einzelnen Enzyme nicht unbedingt etwas über die Schwere der Hepatitis aus, kann jedoch zur Beobachtung des Krankheitsverlaufs herangezogen werden. So kann z.B. der Abfall eines zu Therapiebeginn erhöhten ALT ein Therapieansprechen andeuten, eine erneute Erhöhung nach Therapieende spricht für einen Relapse [24, 45]. Diese Verlaufsparameter dienen somit der Einschätzung der aktuellen entzündlichen Aktivität und Leberfunktion. Betrachtet man die AST- und ALT-Konzentrationen im Verlauf in unserem Studienkollektiv, erkennt man, dass die Genotypen 2 und 3 mit den höchsten Konzentrationen zur Baseline starten, den steilsten Abfall während der Therapie durchlaufen und nach Therapieende die niedrigsten Werte aufweisen. Diese beiden Genotypen erreichten die höchsten Ausheilungsraten. Genotyp 1 zeigte weder einen starken Abfall im Therapieverlauf, noch vergleichbar hohe Ausgangstiter. Bei Genotyp 4 fällt auf, dass nur die ALT-Konzentration nach Therapieende wieder stark ansteigt, während dies im Schaubild der AST-Konzentration nicht der Fall ist. Diese Erhöhung deckt sich mit dem höchsten Relapseanteil, den ebenfalls Patienten des Genotyps 4 zu verzeichnen haben. Ob hier jedoch eine Schlussfolgerung des Wiederanstiegs der ALT nach Therapie auf die Relapsewahrscheinlichkeit gezogen werden kann, bleibt unklar, da bei Genotyp 4 in Woche 48 lediglich 2 Patienten ausgewertet wurden. Die geringe Patientenzahl von Genotyp 4 ist auch bei der folgenden Beobachtung zu berücksichtigen, im Zuge derer sich zeigt, dass der ALT Verlauf bei Genotyp 4 die bisher größten Übereinstimungen zur Anzahl HCV-RNA positiver Patienten aufweist. Beide erreichen den Nadirwert in Woche 4 und zeigen nach Therapieende einen deutlichen Wiederanstieg und somit den höchsten Relapseanteil. Ob die ALT eine sichere und aussagekräftige Vorhersage auf die Ausheilungsrate und den Relapseanteil bei Genotyp 4 ist, lässt sich hier nicht klar aufzeigen. So beschreiben auch Tedeschi und Seeff, dass die ALTKonzentration zwar ein wichtiger Parameter für die Abschätzung der aktuellen Leberentzündung ist, jedoch nicht suffizient mit der Aktivität einer HCV begründeten 68 Diskussion Krankheit korreliert [50]. Des Weiteren schreiben Tedeschi und Seeff, dass ALT in der Bewertung des Ausmaßes der Leberbeteiligung bei chronischer Hepatitis C aufgrund der unbeständigen Korrelation mit den histologischen Ergebnissen diese in Zukunft als wegweisenden Parameter bezüglich der Therapieindikation und Therapiedauer nicht ablösen wird. So fanden sie bei Patienten mit normalen Transaminasewerten deutlich histologische Veränderungen [50]. Bezüglich der beiden Therapieformen hinsichtlich der Beurteilung der Ausheilungsrate schneidet ALT als Marker insgesamt besser ab als AST. So zeigt ALT bei der Consensus Interferongruppe in Übereinstimmung mit dem Verlauf HCV-RNA positiver Patienten einen steileren Konzentrationsabfall und insgesamt konstant niedrigere Werte als bei der PEG Interferongruppe. Diese Konstanz liegt bei AST nicht vor. Sonst ähneln sich AST und ALT in ihrem Verlauf bei den beiden Therapieformen sehr und kongruieren nicht signifikant mit der HCV-RNA, die ja zu Therapieende wiederansteigt. GGT zeigt bei den Genotypen 1 und 3 bei Therapiebeginn zunächst eine Erhöhung und im Therapieverlauf einen deutlichen Abfall auf niedrigere Werte mit ca. 30 U/l. Somit steht ein anfänglich leichter Anstieg der GGT und ein steter Abfall auf deutlich niedrigere Werte als zu Therapiebeginn einem zunächst weniger steilen, und im Laufe der Therapie immer steiler werdenden Rückgang HCV-RNA positiver Patienten gegenüber. Die Genotypen 2 und 4 zeigen dieses Bild evtl. aufgrund der geringen Patientenzahl unseres Studienkollektivs nicht. Ferner erkennt man, dass Genotyp 1 mit deutlich höheren Ausgangswerten von durchschnittlich 69,2 U/l eine geringere SVR besitzt als Genotyp 3 mit einem Ausgangswert von 56 U/l. Somit zeigt sich, dass GGT als möglicher Parameter zur Aussagekraft bezüglich der SVR und vor allem des Therapieverlaufes durch die Inkongruenz der Kurven – verglichen mit der HCV-RNA – in Zukunft nicht in Betracht kommt. Hwang et al. fanden jedoch im Jahr 2000, dass GGT bei chronischer Hepatitis C zwar nicht mit dem HCV-RNA Titer oder den einzelnen Genotypen korreliert, jedoch Patienten mit erhöhten GGT Werten unter Interferontherapie eine geringere SVR Rate erzielten als Patienten mit normwertiger GGT (8% vs 30%) [23]. Letzteres konnte in unserer Studie durch höhere SVR der Patienten mit Genotyp 3 und niedrigerer GGT Konzentration zur Baseline im Gegensatz zu Genotyp 1 mit höheren GGT Ausgangswerten und insgesamt durchschnittlich kleinerem SVR Anteil bestätigt werden. 69 Diskussion Die indirekten Fibrosetests - wie die AST/ALT Ratio und der APRI Score - zählen zur nichtinvasiven Diagnostik bei chronischen Hepatopathien und stehen in Konkurrenz zum aktuellen Goldstandard- der Gewinnung einer Leberhistologie mittels Leberbiopsie (direkter Fibrosetest) [48]. Vergleicht man die Abbildungen 13 und 14 der indirekten Fibrosetests mit dem Staging der Leberbiopsie (Abbildung 27), so erkennt man den größten Unterschied in der Beurteilung des bestehenden Fibrosegrades im leicht bis mittelgradigen Bereich (Grad I und II). Während bei den indirekten Tests Patienten der Genotypen 1 und 2 tendenziell die höchsten und Patienten des Genotyps 4 die niedrigsten Werte aufweisen, zeigen letztere beim direkten Fibrosetest in diesem Bereich mitunter die höchsten Werte. Einzig Genotyp 3 liegt bei den direkten und den indirekten Tests jeweils im Mittelfeld. Dies spricht bei leicht- bis mittelgradiger Fibrose für eine geringe Sensitivität der indirekten Fibrosetests und geht mit der aktuellen Literatur konform [1]. Im Folgenden soll untersucht werden, ob sowohl die direkten (Histologie) als auch die indirekten Fibrosetests (AST/ALT Ratio, APRI Score) Aussagekraft bezüglich der Ausheilungsrate besitzen. Alle Fibrosetests (direkt und indirekt) zeigen, dass das gesamte Patientenkollektiv durchschnittlich keine schwergradige Leberfibrose oder Leberzirrhose aufweist. Vergleicht man nun die den AST/ALT Ratio (Abbildung 24) und den APRI Score (Abbildung 25) mit der Anzahl HCV-RNA positiver Patienten beider Therapieformen, so lässt sich keine signifikante Übereinstimmung oder ein möglicher Vorhersagewert erkennen. Man erkennt lediglich, dass das Consensus Interferon mit einer insgesamt niedrigeren Viruslast im Verlauf und einer etwas höheren Ausheilungsrate einen höheren Fibrosegrad in den indirekten Fibrosetets besitzt. Der deutliche Anstieg der AST/ALT Ratio des Consensus Interferons um 0,23 in Woche 48 fehlt beim APRI Score und auch der HCV-RNA positive Anteil zeigt hier lediglich eine leichte Erhöhung mit ca. 12%. Ebenso zeigen die Graphen der AST/ALT Ratio und des APRI Score nach Genotyp keine Übereinstimmung mit der Anzahl HCV RNA-positiver Patienten oder der Ausheilungsrate. Somit kann hier keine korrelative Aussage getroffen werden. Was jedoch auffällt ist, dass auch hier – wie bereits bei Aufgliederung nach den Therapieformen – die Genotypen mit 70 Diskussion den mitunter höchsten Fibrosegraden (Genotyp 2 und 3) eine bessere Ausheilung durch die niedrigsten Prozentsätze an HCV-RNA positiven Patienten im Verlauf aufweisen. Genotyp 4, der die schlechteste SVR zeigt, weist die niedrigsten Werte bei den indirekten Fibrosetests auf. Dies steht im Widerspruch zur Literatur: Nachnani et al. fanden 2007, dass bei Patienten, die an chronischer Hepatitis C leiden, ein AST/ALT Ratio ≥ 1 als Vorhersagewert für das Ausbleiben der SVR unter Therapie mit PEG Interferon und Ribavirin herangezogen werden kann [34]. Hierbei ist zu berücksichtigen, dass Patienten der PACT Studie diese hohen Werte > 1 nicht erreichen und daher nur von einer anderen Tendenz der oben angeführten Studienergebnisse im Vergleich zu den Ergebnissen von Nachnani et al. gesprochen werden kann. Bei den direkt durchgeführten Fibrosetests ist zu beachten, dass diese keine Verlaufsparameter darstellen und bei jedem Patienten dieser Studie nur einmalig vor Therapiebeginn durchgeführt wurden. Dies gilt auch für das Grading und den Grad der Steatose. Daher ist es sinnvoll, eine Aussage lediglich bezüglich der einzelnen Genotypen zu treffen. Die erreichten Fibrosegrade sind bei den Genotypen sehr unterschiedlich verteilt, jedoch sind alle Grade – von leichtgradig (Grad 0-I) bis mittelgradig (Grad II-III) und schwergradig (Grad IV) – vertreten. Bei Genotyp 4 kann im Staging nur eine leicht bis mittelgradige Fibrose beobachtet werden (Grad I und II). Auch hier muss die geringe Patientenzahl bei Genotyp 4 berücksichtigt werden. Ebenso zeigt Genotyp 1 vornehmlich einen leichten Grad der Fibrose (Grad I). Diese beiden Genotypen schneiden aber bezüglich Ausheilungsrate und HCV-RNA im Verlauf schlechter ab als die beiden anderen Genotypen (Genotyp 2 und 3). Diese zeigen eine stärkere Bandbreite in der Fibrosierung. Der Haupteil liegt jedoch auch hier im leicht- bis mittelgradigen Bereich (Grad I und II). Folglich lässt sich aus dem Grad der Fibrose, die vor Therapiebeginn bei den einzelnen Genotypen untersucht wurde, keine klare Aussage machen, welches Therapieansprechen und welche Ausheilungsrate folgen werden. So beschreibt auch die Leitlinie der Deutschen Gesellschaft für Verdauungs- und Stoffwechselkrankheiten, dass ohne Therapie bei einer Hepatitis C und natürlichem Verlauf die Patienten mit einem initial geringen Fibrosestadium (Stadium 0-I) einen ähnlichen Prozentsatz an einer signifikanten 71 Diskussion Fibroseprogression besitzen, wie Patienten mit einem höheren Fibrosestadium (II-IV). Auch lässt sich kein Rückschluss ziehen vom Verlauf der Transaminasen zur Fibrosierung oder deren Fortschreiten. Bei einer Fibroseprogression können normale Transaminasen im Blut vorhanden sein [1]. Auch beim Grading erkennt man keinen klaren Zusammenhang zwischen der Verteilung der Häufigkeit eines bestimmen Entzündungsgrades und der Ausheilungsrate. Während Genotyp 2 vor allem mittlere bis höhere Grade zu verzeichen hat, gleicht das Bild von Genotyp 3 eher der Aufteilung der Fibrosegrade mit den höchsten Anteilen im Bereich der Entzündungsgrade I und II. Diese beiden Genotypen schneiden bezüglich der SVR am besten ab, zeigen bei den Entzündungsgraden jedoch eine absolut unterschiedliches Bild wie oben beschrieben. Ebenso zeigen die hinsichtlich der Ausheilung schlechter abschneidenden Genotypen 1 und 4 eine ähnliche Verteilung wie Genotyp 3 mit den meisten Fällen im leicht- bis mittelgradigen Bereich. Somit ist auch hier keine signifikante Schlussfolgerung von initialem Entzündungsgrad zur Ausheilungsrate möglich. Um dies näher zu untersuchen, und auch einen Bezug zur Progression der Fibrose und Entzündung herstellen zu können, hätten mehrere Leberbiopsien – zumindest eine Weitere nach Therapieende – stattfinden müssen um einen Vergleich zu erhalten. Dies wurde aufgrund der Invasivität des Eingriffs jedoch nicht durchgeführt. Die Häufigkeit des Auftretens einer Steatose ist mit insgesamt fast 60% der Gesamtheit des Patientenkollektivs hoch. Die Auftrennung in Genotypen zeigt eine regelmässige Steatoseverteilung. Mit einer Differenz von insgesamt 11,9% von Genotyp 4 zu Genotyp 1 zeigen sich zwar klar Unterschiede, lassen aber keine Voraussage zur HCV-RNA oder SVR zu, da die Rangliste, bei der Genotyp 1 am besten abschneidet, gefolgt von den Genotypen 2, 3 und 4 nicht mit der Rangliste der SVR nach Genotyp übereinstimmt. Bei der Auswertung der Störfaktoren, die potentiell zu einer Verzerrung der Ergebnisse führen können, muss man die Verteilung der Nonresponder bei den Genotypen betrachten. Den höchsten Anteil hat Genotyp 1, gefolgt von den Genotypen 2 und 3. Am besten schneidet hier Genotyp 4 ab. Diese Non-Responderverteilung geht mit der Literatur konform. So beschrieben Smith und Pontisso [47], dass die Genotypen 2 und 3 eine höhere Responserate als Genotyp 1 aufweisen. Dennoch stehen in unserer klinischen Studie zu wenige Patienten mit Genotyp 4 und Genotyp 2 zur Verfügung, deren Daten 72 Diskussion ausgewertet werden konnten und in die Analyse miteinflossen. Daher ist diese Auswertung bezüglich der Häufigkeitsverteilung der Non-Responder nicht repräsentativ und hat wahrscheinlich auch Auswirkungen auf die Auswertung der SVR und die Anzahl HCV-RNA positiver Patienten nach Therapieende. Um eine signifikante Aussage treffen zu können, ist ein größeres Patientenkollektiv mit den Genotypen 4 und 2 erforderlich, um die genannten Störfaktoren weitestgehend eliminieren zu können. Ebenso wird der HCV-RNA Verlauf und die SVR – wie oben bereits erwähnt – durch die unterschiedliche Verteilung der Patienten auf die Therapieform und deren NonResponderanteil beeinflusst. Dieser ist bei der PEG-Interferongruppe deutlich höher. Der Relapseanteil scheint das Ergebnis weniger zu verzerren, da dieser bei beiden Therapiearten in etwa gleich hoch ist. Der deutlich höhere Relapseanteil von Genotyp 4 im Gegensatz zu den anderen Genotypen liegt sicherlich wieder in der geringen Patientenanzahl begründet und darf nicht als signifikant angesehen werden, zeigt jedoch die Tendenz einer sehr unterschiedlichen Verteilung, die ebenfalls Einfluss auf die Ausheilungsrate nimmt. Bei den Nadirwerten zeigt sich unabhängig von den einzelnen Genotypen zunächst die Tendenz, dass diese bei den Leukozyten-, Erythrozyten- und Thrombozytenkonzentrationen bereits sehr früh erreicht werden- gefolgt vom Hämoglobingehalt, dessen Zeitpunkt etwas später liegt. Die leberspezifischen Parameter AST, ALT, GGT und das Bilirubin gesamt brauchen am längsten, um sich zu erholen. Eine Auftrennung in die Genotypen lässt lediglich erkennen, dass Genotyp 1 – mit Ausnahme der Thrombozytenkonzentration – bei allen anderen untersuchten laborchemischen Parametern durchschnittlich einen späteren Erreichzeitpunkt aufweist als die anderen Genotypen. Bei den jeweiligen Nadirwerten schneidet Genotyp 2 mit Erreichen des niedrigsten Nadirs der einzelnen laborchemischen Parametern am besten ab (Ausnahme ist hier die Bilirubinkonzentration). Eine klare Aussage oder eine Tendenz im Hinblick auf ein zukünftiges Therapieansprechen lässt sich anhand dieser Daten nicht erheben. Im Vergleich zur Baseline zeigen die Nadirwerte der Leukozyten-, Erythrozyten-, Thrombozyten- und Hämoglobinkonzentrationen einen deutlichen Abfall im Verlauf unter Therapie und erreichen vereinzelt den pathologischen Bereich. Die leberspezifischen Laborwerte von AST, ALT und GGT hingegen sind zu Beginn stark erhöht und nähern sich 73 Diskussion beim Nadir dem physiologischen Bereich an bzw. erreichen diesen, womit von einer Normalisierung im Verlauf gesprochen werden kann. Der Nadirwert der Bilirubinkonzentration bildet auch hier wieder eine Ausnahme – er liegt bei allen Genotypen im physiologischen Bereich. Diese Ergebnisse decken sich mit den Kurvenverläufen der einzelnen Parametern unter Therapie. Bei Betrachtung der Nadirwerte, dem Erreichzeitpunkt und dem prozentualen Abfall von Woche 0 bis Woche 12 aufgegliedert in das jeweilige Therapieansprechen der Patienten mit den Genotypen 1+4 bzw. 2+3 für die Leukozyten-, Thrombozyten- und die Hämoglobinkonzentrationen verhält es sich folgendermaßen: Betrachtet man zunächst die einzelnen Werte für die Leukozyten so zeigt der Nadirwert bei beiden Genotypgruppen (Genotyp 1 + 4 und 2+3) ebensowenig signifikante Eigenschaften, die auf eine potentielle Vorhersage bezüglich eines erfolgreichen Therapieansprechens schließen lassen. Dasselbe gilt für den %-Abfall. Bei den Genotypen 2+3 wird der Nadirwert der Responderpatienten jedoch erst später erreicht (Woche 12 anstatt Woche 4 wie bei den Relapsepatienten und Non-Respondern). Daraus könnte man schlussfolgern, dass bei diesen Genotypen für die Leukozytenkonzentration die Tendenz besteht, bei einem späteren Erreichzeitpunkt des Nadirwertes ein besseres Therapieansprechen resultiert. Bei der Hämoglobinkonzentration und den Genotypen 1+4 scheint der tatsächliche Nadirwert (je niedriger, desto besser) ausschlaggebend für den Therapieerfolg zu sein, unabhängig von der Höhe des %-Abfalls oder dem jeweiligen Erreichzeitpunkt. Die Genotypen 2+3 zeigen jedoch nur ein besseres Therapieansprechen, je früher der Nadir erreicht wird (Woche 4), unabhängig vom %-Abfall oder dem eigentlichen Wert. Höhere Nadirwerte und Thrombozytenkonzentrationen eine der früheres Genotypen Erreichen 1+4 der scheinen niedrigsten ein besseres Therapieanprechen nach sich zu ziehen. Der %-Abfall lässt keine Rückschlüsse auf einen zukünftigen Therapieerfolg zu. Auch bei den Genotypen 2+3 sind höhere ThrombozytenNadirwerte anscheinend besser bezogen auf ein Therapieansprechen, auf den Erreichzeitpunkt und den %-Abfall trifft dies nicht zu. 74 Diskussion Beim Verlauf der Leukozytenkonzentration und unter Auftrennung nach dem jeweiligen Therapieansprechen lässt sich aus der Auswertung der Genotypen 1+4 und 2+3 schließen, dass je früher – in diesem Fall bereits bis Woche 2 – ein Abfall stattfindet und je steiler dieser ist, desto besser scheinen die Patienten auf die Behandlung anzusprechen und werden langfristig zu Respondern. Ebenso sollte nach Woche 2 dieses niedrige Niveau der Leukozytenkonzentration erhalten bleiben (wie bei den Respondern der Genotypen 1+4 erkennbar) oder es kann eine erneute Senkung (wie bei den Respondern der Genotypen 2+3) eintreten. Diese Verläufe wirken sich offensichtlich ebenso positiv auf das spätere Therapieansprechen aus. Bei einem weniger steilen Abfall zu einem späteren Zeitpunkt (nach Woche 2) und einem darauffolgenden Wiederanstieg, erhöht sich die Gefahr, einen Relapse zu entwickeln oder ein Non-Responder zu werden. Beim Hämoglobingehalt der Genotypen 1+4 weisen die Responder einen konstanten Abfall bis Woche 12 auf. Die Non-Responder und Relapsepatienten haben den steilsten Abfall früher von Woche 2 bis Woche 4. Ab Woche 4 ist dieser bei beiden deutlich geringer als bei den Respondern. Somit ist ein stärkerer Abfall zu einem späteren Zeitpunkt (ab Woche 4) für die Heilungschanchen wohl begünstigend. In der Literatur konnten Sievert et al. 2011 nachweisen, dass die SVR bei der Therapie einer Hepatitis C Infektion des Genotyps 1 mit pegyliertem Interferon und Ribavirin mit dem Abfall der Hämoglobinkonzentration assoziiert ist. Sie erkannten, dass Patienten mit Genotyp 1 die entweder Zeichen einer Anämie (Serumhämoglobin < 100 g/l zu jedem Zeitpunkt der Behandlung) entwickeln, oder deren Hämoglobinabfall > 30 g/l ist, eine höhere virologische Ansprechrate (SVR) haben als Patienten, bei denen dies nicht auftritt [46]. Bei den Genotypen 2+3 zeigt sich ebenfalls, dass sich ein späterer Hämoglobinabfall günstiger auf die SVR auswirkt (Auftreten nach Woche 2- bei den Respondern und Relapsepatienten, bis Woche 2 bei den Non-Respondern). Bei diesen Genotypen scheint sich laut Patientenkollektiv ein Wiederanstieg ab Woche 4 ebenfalls positiv auszuwirken, denn nur Responder zeigen dieses Bild. Die Thrombozytenkonzentrationen der Responder der Genotypen 1+4 haben einen früheren Abfall und ebenso früheren, aber auch längeren und stärkeren Wiederanstieg im Gegensatz zu den Relapsepatienten. Die Non-Responder dieser Genotypen zeigen 75 Diskussion keinen Wiederanstieg. Folglich deutet ein früher Abfall der Thrombozytenkonzentration, sowie ein früher, starker und langer Wiederanstieg auf gute Ausheilungschancen hin. Bei den Genotypen 2+3 zeigt sich ein etwas anderes Bild der Thrombozytenkonzentrationsverläufe. Zwar ist ein früher Abfall ebenso besser, wie die Responder dieser Genotypen zeigen, einen Wiederanstieg erfahren jedoch nur die Patienten mit einem Relapse. Bei den Respondern fehlt dieser im Gegensatz zu den Genotyppatienten 1+4. Ein Wiederanstieg der Thrombozytenkonzentration scheint somit bei den Genotypen 2+3 keine bessere SVR nach sich zu ziehen. Insgesamt lässt sich durch die Analyse der einzelnen Parameter unter Therapie in unserem Patientenkollektiv keiner finden, der ausreichend mit der HCV-RNA oder der Ausheilungsrate korreliert, um die HCV-RNA ermittelt durch RT-PCR als Vorhersagewert hinsichtlich des Therapieansprechens und des Therapieverlaufs in Zukunft komplett ablösen zu können. Die Leukozytenwerte, die jedoch zu stark durch die Interferontherapie beeinflusst werden und keine suffiziente Korrelation zur HCV-RNA und der SVR aufweisen, zeigen dennoch Potenzial. Ferner kann der insgesamt höchste Relapseanteil, der bei Genotyp 4 zu verzeichnen ist, einem eindeutigen Wiederanstieg der ALT-Konzentration nach Therapieende zugeordnet werden. Die restlichen Genotypen zeigen diese Korrelation in weniger drastischem Ausmaße. Dennoch ist auch hier v.a. aufgrund der geringen Patientendaten von Genotyp 4 in Woche 48 kein klarer Aussagewert zu treffen, der die AST Konzentration mit dem Relapseanteil in Zusammenhang setzt Zum Hämoglobingehalt lässt sich sagen, je später (ab/nach Woche 2) und größer der Hämoglobinabfall, desto bessere Ausheilungschanchen sind zu verzeichnen. Dies ist sowohl bei den Therapiearten, als auch bei allen Genotypen nach Therapieausgang ersichtlich. Bei den Genotypen 2+3 fällt ein zusätzlicher Wiederanstieg des Hämoglobingehaltes ab Woche 4 positiv im Hinblick auf ein Therapieansprechen auf. Dies gilt auch für einen niedrigeren Nadirwert des Hämoglobins bei den Genotypen 1+4 sowie ein früherer Erreichzeitpunkt bei den Genotypen 2+3 (Woche 4). Eine Signifikanz auf den tatsächlichen Ersatz der HCV-RNA durch die Hämoglobinkonzentration oder den Nadirwert des Hämoglobins sowie dessen Erreichzeitpunkt bei der Bestimmung der SVR bleibt bei der unterschiedlichen Genotypenverteilung aus. 76 Diskussion Beim Verlauf der Thrombozytenkonzentration zeigt sich, dass je früher und größer der Abfall ist und je früher der Erreichzeitpunkt des Nadirwertes liegt, desto besser sind die Ausheilungschanchen und das Therapieansprechen. Diese Beobachtung scheint genotypenunspezifisch zu sein. Lediglich die Genotypen 1+4 zeigen zudem einen Wiederanstieg der, je größer und länger im Verlauf ist, einen positiven Effekt auf die SVR zu haben scheint. Ein HCV-RNA Ersatz für die Vorhersage des Therapieansprechens bei einer chronischen Hepatitis C ist der Verlauf der Thrombozytenkonzentration und der Nadirwert jedoch ebensowenig. Ein idealer Parameter für die Beurteilung des antiviralen Therapieverlaufs sollte sich nur bei nachweisbarer HCV-RNA im Blut verändern, durch die Therapie nicht zu sehr beeinflusst werden und am Ende mit der SVR deutlicher und unabhängig vom HCV Genotyp korrelieren. 77 Zusammenfassung 6 Zusammenfassung Mit fast 170 Millionen infizierter Menschen weltweit gehört die Hepatitis C heutzutage zu den häufigsten Ursachen einer chronischen Lebererkrankung, die schwerwiegende Komplikationen wie z.B. Leberzirrhose oder Leberzellkarzinom nach sich ziehen kann. Für diese Arbeit wurden Daten von 103 Patienten eines Studienkollektivs der Universitätsklinik Ulm ausgewertet, die aufgrund ihrer diagnostizierten Hepatitis C Infektion im Zeitraum von Januar 2000 bis April 2003 mit einer Kombinationstherapie eines Interferonpräparates und des Nukleosidanalogons Ribavirin behandelt wurden („PegIntron against Consensus Trial (PACT)“-Studie). Dabei wurde untersucht, ob die Hepatitis C Virus (HCV)-Ribonukleinsäure (RNA) – ermittelt durch Reverse TranskriptasePolymerase-Kettenreaktion (RT-PCR) – als aktueller Goldstandardmarker bezüglich des Therapieansprechens und des Therapieverlaufes durch andere, laborchemische Parameter in Zukunft abgelöst werden kann. Des Weiteren fließen in die Auswertung der Fibrose-, Steatose- und Entzündungsgrad, sowie der Non-Responder- und Relapseanteil des Studienkollektives mitein. Als Referenz dient jeweils die HCV-RNA sowie die Ausheilungsrate (sustained virological response rate, SVR) und es wird eine weitere Unterteilung hinsichtlich des vorherrschenden Genotyps (1-4) vorgenommen, mit welcher Kombinationstherapie die Patienten behandelt wurden und wie das Therapieansprechen auf die jeweilige medikamentöse Behandlung ist. Die Auswertung der Ergebnisse zeigt, dass aktuell kein idealer laborchemischer Parameter vorhanden ist, um in Zukunft in der leitliniengerechten Durchführung der serologischen HCV Diagnostik auf die HCV-RNA als Marker des Viruslastnachweises verzichten zu können. Dies gilt auch im Hinblick darauf, signifikante Vorhersagen für das Therapieansprechen (angezeigt durch die SVR) zu treffen. Jedoch besitzt der zeitliche Verlauf der Leukozytenkonzentration in dieser Hinsicht Potenzial. Je steiler der Abfall zu Therapiebeginn und Wiederanstieg bei Therapieende, sowie konstant niedrige Werte während der Therapie lassen auf eine bessere Ausheilungsrate schließen. Ebenso kann ein möglicher Zusammenhang zwischen der Alaninaminotransferase (ALT)-Konzentration und dem Relapseanteil ausgemacht werden. Je höher und schneller der Wiederanstieg der ALT Konzentration nach Therapieende, 78 Zusammenfassung desto höher die Relapserate. Dennoch sind diese beiden Parameter zu ungenau und werden im betrachteten Studienkollektiv von zu vielen Störfaktoren beeinflusst oder unterliegen einer unterschiedlich starken Verteilung auf die einzelnen Genotypen, um eine Signifikanz zu erreichen. Zusätzlich zeigt die Auswertung, dass der Abfall der Hämoglobinkonzentration mit der SVR korreliert. Je später (ab/nach Woche 2) und je größer der Hämoglobinabfall, desto besser sind die zu verzeichnenden Ausheilungschanchen. Dies ist sowohl bei den Therapiearten, als auch bei allen Genotypen nach Therapieausgang ersichtlich. Bei den Genotypen 2+3 fällt ein zusätzlicher Wiederanstieg des Hämoglobingehaltes ab Woche 4 positiv im Hinblick auf ein Therapieansprechen aus. Dies gilt auch für einen insgesamt niedrigeren Nadirwert des Hämoglobins bei den Genotypen 1+4 und ein etwas früheres Erreichen des Nadirwertes bei den Genotypen 2+3. Die Möglichkeit einer tatsächlichen Substitution der HCV-RNA-Bestimmung durch die Hämoglobinkonzentration oder den Nadirwert des Hämoglobins als Indikator für das Therapieansprechen ist hier nicht gegeben. Die Thrombozytenkonzentrationen lassen einen weiteren Zusammenhang mit der SVR vermuten. Je früher und größer der Abfall ist und je früher der Erreichzeitpunkt des Nadirwertes liegt, desto besser sind die Ausheilungschanchen und das Therapieansprechen. Dies scheint genotypenunspezifisch zu sein. Ein Wiederanstieg und zwar je größer und länger im Verlauf, desto besser trifft nur auf die Genotypen 1+4 zu. Ein Ersatz für HCV-RNA-Messungen für die Vorhersage des Therapieansprechens bei einer chronischen Hepatitis C ist der Verlauf der Thrombozytenkonzentration und der Nadirwert jedoch ebensowenig. Aufgrund dieser Ergebnisse der ausgewerteten PACT-Studie wird die HCV-RNA wohl auch in Zukunft der dominante Marker für das antivirale Therapieansprechen bleiben. 79 Literaturverzeichnis 7 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. Literaturverzeichnis Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften: Prophylaxe, Diagnostik und Therapie der Hepatitis-C-Virus (HCV)-Infektion. S3Leitlinie der Deutschen Gesellschaft für Verdauungs- und Stoffwechselkrankheiten 021/012:10-49 (2009) Bartenschlager R, Frese M und Pietschmann T: Novel insights into hepatitis C virus replication and persistence. Adv Virus Res 63:71-180 (2004) Bartenschlager R und Sparacio S: Hepatitis C virus molecular clones and their replication capacity in vivo and in cell culture. Virus Res 127:195-207 (2007) Berk PD und Javitt NB: Hyperbilirubinemia and cholestasis. Am J Med 64:311-326 (1978) Borsoi Viana MS, Takei K, Collarile Yamaguti DC, Guz B und Strauss E: Use of AST platelet ratio index (APRI Score) as an alternative to liver biopsy for treatment indication in chronic hepatitis C. Ann Hepatol 8:26-31 (2009) Brockmeyer N: HIV-Infektion: Rationale für die antiretrovirale Therapie. Dtsch Ärztebl 95(8):A400-A403 (1998) Cao H: Heterogeneity of hepatitis C-virus in genotype 1 patients treated with the combination therapy of pegylated interferon and ribavirin. Dissertation (2004) Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW und Houghton M: Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science 244:359-362 (1989) Colin C, Lanoir D, Touzet S, Meyaud-Kraemer L, Bailly F und Trepo C: Sensitivity and specificity of third-generation hepatitis C virus antibody detection assays: an analysis of the literature. J Viral Hepat 8:87-95 (2001) Cuenca F, Fernandez C, Devesa MJ, Lopez-Alonso G, Mayol J, Suarez A, Ortega L, Diaz-Rubio M und Ladero JM: Predictive baseline criteria of primary therapeutic failure in chronic hepatitis C genotype 1. Rev Esp Enferm Dig 102:234-238 (2010) Desmet VJ, Gerber M, Hoofnagle JH, Manns M und Scheuer PJ: Classification of chronic hepatitis: diagnosis, grading and staging. Hepatology 19:1513-1520 (1994) Di Bisceglie AM, Conjeevaram HS, Fried MW, Sallie R, Park Y, Yurdaydin C, Swain M, Kleiner DE, Mahaney K und Hoofnagle JH: Ribavirin as therapy for chronic hepatitis C. A randomized, double-blind, placebo-controlled trial. Ann Intern Med 123:897-903 (1995) Farci P, Alter HJ, Shimoda A, Govindarajan S, Cheung LC, Melpolder JC, Sacher RA, Shih JW und Purcell RH: Hepatitis C virus-associated fulminant hepatic failure. N Engl J Med 335:631-634 (1996) Forns X und Bukh J: The molecular biology of hepatitis C virus. Genotypes and quasispecies. Clin Liver Dis 3:693-716, vii (1999) Freeman AJ, Dore GJ, Law MG, Thorpe M, Von Overbeck J, Lloyd AR, Marinos G und Kaldor JM: Estimating progression to cirrhosis in chronic hepatitis C virus infection. Hepatology 34:809-816 (2001) Fried MW, Shiffman ML, Reddy KR, Smith C, Marinos G, Goncales FL, Jr., Haussinger D, Diago M, Carosi G, Dhumeaux D, Craxi A, Lin A, Hoffman J und Yu J: Peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection. N Engl J Med 347:975-982 (2002) 80 Literaturverzeichnis 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. 31. 32. 33. Fuchs M: (2011 Persönliche Mitteilung) Grebely J, Matthews GV und Dore GJ: Treatment of acute HCV infection. Nat Rev Gastroenterol Hepatol 8:265-274 (2011) Gumber SC und Chopra S: Hepatitis C: a multifaceted disease. Review of extrahepatic manifestations. Ann Intern Med 123:615-620 (1995) Hadziyannis SJ, Sette H, Jr., Morgan TR, Balan V, Diago M, Marcellin P, Ramadori G, Bodenheimer H, Jr., Bernstein D, Rizzetto M, Zeuzem S, Pockros PJ, Lin A und Ackrill AM: Peginterferon-alpha2a and ribavirin combination therapy in chronic hepatitis C: a randomized study of treatment duration and ribavirin dose. Ann Intern Med 140:346-355 (2004) Hahn JM: Checkliste Innere Medizin. 3, Georg Thieme Verlag, Stuttgart New York, Anhang (Einband hinten) (2000) Hoofnagle JH: Course and outcome of hepatitis C. Hepatology 36:S21-29 (2002) Hwang SJ, Luo JC, Lai CR, Chu CW, Tsay SH, Lu CL, Wu JC, Chang FY und Lee SD: Clinical, virologic and pathologic significance of elevated serum gamma-glutamyl transpeptidase in patients with chronic hepatitis C. Zhonghua Yi Xue Za Zhi (Taipei) 63:527-535 (2000) Kau A, Vermehren J und Sarrazin C: Treatment predictors of a sustained virologic response in hepatitis B and C. J Hepatol 49:634-651 (2008) Lauer GM und Walker BD: Hepatitis C virus infection. N Engl J Med 345:41-52 (2001) Lee SC, Antony A, Lee N, Leibow J, Yang JQ, Soviero S, Gutekunst K und Rosenstraus M: Improved version 2.0 qualitative and quantitative AMPLICOR reverse transcription-PCR tests for hepatitis C virus RNA: calibration to international units, enhanced genotype reactivity, and performance characteristics. J Clin Microbiol 38:4171-4179 (2000) Llovet JM: Updated treatment approach to hepatocellular carcinoma. J Gastroenterol 40:225-235 (2005) Lohmann V, Roos A, Korner F, Koch JO und Bartenschlager R: Biochemical and structural analysis of the NS5B RNA-dependent RNA polymerase of the hepatitis C virus. J Viral Hepat 7:167-174 (2000) Maertens G und Stuyver L: HCV Genotyping by the Line Probe Assay INNO-LiPA HCV II. Methods Mol Med 19:183-198 (1999) Maieron A, Metz-Gercek S, Hackl F, Ziachehabi A, Fuchsteiner H, Luger C, Mittermayer H und Schofl R: Antiviral treatment of chronic hepatitis C in clinical routine. Wien Klin Wochenschr 122:237-242 (2010) Mathurin P, Moussalli J, Cadranel JF, Thibault V, Charlotte F, Dumouchel P, Cazier A, Huraux JM, Devergie B, Vidaud M, Opolon P und Poynard T: Slow progression rate of fibrosis in hepatitis C virus patients with persistently normal alanine transaminase activity. Hepatology 27:868-872 (1998) Mendeni M, Foca E, Gotti D, Ladisa N, Angarano G, Albini L, Castelnuovo F, Carosi G, Quiros-Roldan E und Torti C: Evaluation of liver fibrosis: concordance analysis between noninvasive scores (APRI and FIB-4) evolution and predictors in a cohort of HIV-infected patients without hepatitis C and B infection. Clin Infect Dis 52:1164-1173 (2011) Micallef JM, Kaldor JM und Dore GJ: Spontaneous viral clearance following acute hepatitis C infection: a systematic review of longitudinal studies. J Viral Hepat 13:34-41 (2006) 81 Literaturverzeichnis 34. 35. 36. 37. 38. 39. 40. 41. 42. 43. 44. 45. 46. 47. 48. 49. 50. Nachnani JS, Gidwani R, Sadeddin E, Clarkston WK, Fiorella R und Alba LM: Clinicopathological predictors to predict sustained viral response rates in patients with chronic hepatitis C infection. Indian J Gastroenterol 26:279-282 (2007) Niederau C, Lange S, Heintges T, Erhardt A, Buschkamp M, Hurter D, Nawrocki M, Kruska L, Hensel F, Petry W und Haussinger D: Prognosis of chronic hepatitis C: results of a large, prospective cohort study. Hepatology 28:1687-1695 (1998) Parthé-Peterhans S und Gohl P: Diagnostik der Hepatitis C-Virus Infektion. Bioscientia 4:2 (2005) Pawlotsky JM: Hepatitis C virus genetic variability: pathogenic and clinical implications. Clin Liver Dis 7:45-66 (2003) Pockros PJ: New direct-acting antivirals in the development for hepatitis C virus infection. Therap Adv Gastroenterol 3:191-202 (2010) Poynard T, Bedossa P und Opolon P: Natural history of liver fibrosis progression in patients with chronic hepatitis C. The OBSVIRC, METAVIR, CLINIVIR, and DOSVIRC groups. Lancet 349:825-832 (1997) Robert-Koch-Institut: Aktuelle Daten und Informationen zu Infektionskrankheiten und Public Health, Zur Situation bei wichtigen Infektionskrankheiten in Deutschland; Virushepatitis B, C und D im Jahr 2009. Epidemiologisches Bulletin 20:177, 183 (2010) Robertson B, Myers G, Howard C, Brettin T, Bukh J, Gaschen B, Gojobori T, Maertens G, Mizokami M, Nainan O, Netesov S, Nishioka K, Shin i T, Simmonds P, Smith D, Stuyver L und Weiner A: Classification, nomenclature, and database development for hepatitis C virus (HCV) and related viruses: proposals for standardization. International Committee on Virus Taxonomy. Arch Virol 143:2493-2503 (1998) Roche SP und Kobos R: Jaundice in the adult patient. Am Fam Physician 69:299304 (2004) Sarrazin C: Highly sensitive hepatitis C virus RNA detection methods: molecular backgrounds and clinical significance. J Clin Virol 25 Suppl 3:S23-29 (2002) Schreier E, Radun D, Neuhauser H und Stark K: Gesundheitsberichterstattung des Bundes - Hepatitis C. Robert-Koch-Institut8-10 (2003) Shiffman ML, Suter F, Bacon BR, Nelson D, Harley H, Sola R, Shafran SD, Barange K, Lin A, Soman A, Zeuzem S und Investigators A: Peginterferon alfa-2a and ribavirin for 16 or 24 weeks in HCV genotype 2 or 3. N Engl J Med 357:124-134 (2007) Sievert W, Dore GJ, McCaughan GW, Yoshihara M, Crawford DH, Cheng W, Weltman M, Rawlinson W, Rizkalla B, Depamphilis JK, Roberts SK und Group CS: Virological response is associated with decline in hemoglobin concentration during pegylated interferon and ribavirin therapy in hepatitis C virus genotype 1. Hepatology 53:1109-1117 (2011) Smith DB und Pontisso P: Heterogeneity of hepatitis C virus. Baillieres Clin Gastroenterol 10:243-255 (1996) Stauber R: Nichtinvasive Diagnose der Leberfibrose bei chronischen Hepatopathien. J Gastroenterol Hepatol Erkr 7:12-17 (2009) Steffen M: Neue antivirale Therapeutika: Nukleosidanaloga bei chronischer Hepatitis B und C. Dtsch Ärztebl 93:A-3117-3120 (1996) Tedeschi V und Seeff LB: Diagnostic tests for hepatitis C: where are we now? Ann Intern Med 123:383-385 (1995) 82 Literaturverzeichnis 51. 52. 53. 54. Vcev A: [Management of side effects during antiviral therapy]. Acta Med Croatica 63:463-467 (2009) World Health Organization W: Prevalence of Hepatitis C virus infection. (2007) Zeuzem S: [Standard treatment of acute and chronic hepatitis C]. Z Gastroenterol 42:714-719 (2004) Zeuzem S, Heathcote JE, Martin N, Nieforth K und Modi M: Peginterferon alfa-2a (40 kDa) monotherapy: a novel agent for chronic hepatitis C therapy. Expert Opin Investig Drugs 10:2201-2213 (2001) 83 Danksagung Danksagung Ganz herzlich möchte ich mich bei Herrn Prof. Dr. Michael Fuchs für die Bereitstellung des Themas der vorliegenden Promotionsarbeit, seine Betreuung und die vielen guten Ratschläge bedanken, die diese Arbeit zur Fertigstellung gebracht haben. Ebenso möchte ich mich bei Herrn Prof. Dr. G. Adler und Prof. Dr. G. v. Wichert bedanken, die mir die Möglichkeit gaben, eine Dissertation in der Abteilung für Innere Medizin I des Universitätsklinikums Ulm abzulegen. Nicht zuletzt gilt mein Dank den Mitarbeitern der Abteilung der Leberambulanz, des Archivs und des Promotionssekreteriates der Universität Ulm; insbesondere Frau Simone Bader für Ihre hilfreiche Unterstützung. Meinem lieben Bruder Stefan, der mich im Studium wie auch heute noch stets als Vetrauensperson begleitet, möchte ich für seine immerwährende Unterstützung, Zuneigung und Liebe danken. 84 Der Lebenslauf wurde aus Gründen des Datenschutzes in der Elektronischen Version entfernt. 85