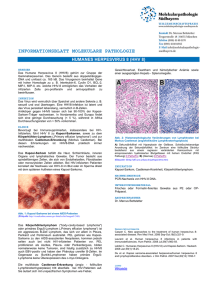
Entdeckung eines neuen Herpesvirus: HHV-8
Werbung

M E D I Z I N AKTUELL Entdeckung eines neuen Herpesvirus: HHV-8 Reinhold Munker1, 2 Walter Verbeek2 Taizo Tasaka2 Jonathan Said3 Jürgen Haas4 HHV-8 in Kaposi-Sarkomen und seltenen H. Phillip Koeffler2 lymphoproliferativen Erkrankungen Das Humane Herpesvirus 8 (HHV-8) wurde kürzlich bei Patienten mit AIDS-assoziiertem Kaposi-Sarkom entdeckt. Es gehört wie das Epstein-Barr-Virus (EBV) zur Familie der Gammaherpesviren, hat jedoch im Gegensatz zu EBV eine wesentlich geringere Durchseuchung in Westeuropa und Nordamerika. Neben dem AIDS-assoziierten Kaposi-Sar- K aposi-Sarkome sind zusammen mit malignen Lymphomen die häufigste Neoplasie bei Patienten mit AIDS, wurden jedoch schon lange vor der Ära der HIV-Infektion beobachtet. AIDS-Patienten mit Kaposi-Sarkom kommen zum weit überwiegenden Teil aus der Risikogruppe der Homosexuellen und sind männlich. Die Kaposi-Sarkome, die nicht AIDSassoziiert sind, kommen endemisch gehäuft in mediterranen Ländern sowie in Zentralafrika vor. Darüber hinaus treten Kaposi-Sarkome vereinzelt auch nach Organtransplantationen bei Immunsupprimierten auf. Aufgrund dieser epidemiologischen Verteilung wurde bereits vor Jahren der Verdacht auf eine infektiöse Ätiologie des Kaposi-Sarkoms geäußert und nach einem auslösenden Agens gesucht. Nachdem zunächst eine ganze Reihe verschiedener Erreger, wie Zytomegalievirus, Humanes Herpesvirus 6, Papillomviren, Mykoplasmen und schließlich HIV-1 selbst, als Auslöser diskutiert wurden, konnten Chang und Mitarbeiter im Jahr 1994 mittels „Representational Display Analysis“, einer neuentwickelten Methode, die auf der Polymerase-Kettenreaktion (PCR) basiert, bisher unbekannte DNA-Sequenzen im Tumorgewebe eines Kaposi-Patienten identifizieren (7). Diese DNA-Sequenzen waren verwandt mit dem Epstein-Barr-Virus des Menschen sowie einem weiteren Vertreter der Gammaherpesvi- kom wurde das Humane Herpesvirus 8 inzwischen in allen anderen Formen des Kaposi-Sarkoms sowie in einer Reihe von seltenen lymphoproliferativen Erkrankungen identifiziert, aber auch vereinzelt bei gesunden Individuen. Die Rolle, die HHV-8 in der Pathogenese der genannten Erkrankungen spielt, ist derzeit Gegenstand heftiger Diskussionen. ren, Herpesvirus saimiri, welches in einigen Affenarten fulminante Lymphome auslöst (23). In den beiden letzten Jahren wurden erstaunliche Fortschritte bei der Erforschung des Aufbaus und der Verbreitung dieses neuen Herpesvirus gemacht. Biologie von HHV-8 HHV-8, welches initial auch als Kaposi-Sarkom-assoziiertes Herpesvirus (KSHV) bezeichnet wurde, gehört taxonomisch aufgrund der Sequenzhomologie zur Unterfamilie der Gammaherpesviren, ähnlich wie EBV und Herpesvirus saimiri. Das Genom von HHV-8 besitzt eine Größe von etwa 140 000 Basenpaaren und wird von mehreren repetitiven Sequenzen mit einer Länge von ungefähr 800 Basenpaaren flankiert (30). HHV-8 hat mehrere Gemeinsamkeiten mit EBV: Der Aufbau des Genoms ist sehr ähnlich, es infiziert auch 1Medizinische Klinik III (Direktor: Prof. Dr. med. Dr. h. c. Wolfgang Wilmanns), Klinikum Großhadern der Ludwig-Maximilians-Universität, München 2Department of Hematology (Direktor: Prof. Dr. med. H. Phillip Koeffler), UCLA Cedars Sinai Medical Center, Los Angeles, CA, USA 3Division of Surgical Pathology (Direktor: Prof. Dr. med. Jonathan Said), UCLA Medical Center, Los Angeles, CA, USA 4 Max-von-Pettenkofer-Institut, Lehrstuhl Virologie (Direktor: Prof. Dr. med. Ulrich Koszinowski), Ludwig-Maximilians-Universität, München A-2642 (50) Deutsches Ärzteblatt 94, Heft 41, 10. Oktober 1997 B-Lymphozyten und wird ebenfalls als Tumorvirus verdächtigt. EBV kann bei der Primärinfektion, die in der Regel im Kindes- und Jugendlichenalter stattfindet, die infektiöse Mononukleose verursachen und persistiert im weiteren Verlauf in niedriger Frequenz in B-Lymphozyten (latente Infektion). Darüber hinaus jedoch besteht eine Assoziation von EBV mit dem in Afrika endemisch vorkommenden Burkitt-Lymphom sowie dem in Südostasien endemischen Nasopharynx-Karzinom. Durch die enge Verwandschaft mit EBV und die Assoziation mit mindestens zwei menschlichen Tumoren ist anzunehmen, daß auch HHV-8 transformierende Potenz besitzt. Bei der Sequenzierung wurden gleich mehrere Gene entdeckt, die eine potentielle Rolle bei der malignen Transformation besitzen könnten. HHV-8 kodiert ein Zyklin-D-ähnliches Protein, welches durch Aktivierung der Proteinkinase cdk6 in den Zellzyklus eingreift (3, 17), ein Homolog zu dem Anti-Apoptose-Protein bcl-2 (34) sowie zwei homologe Proteine zu den Chemokinen MIP-I und MIP-II (27). Besonders interessant jedoch erscheint ein Interleukin-6-homologes Protein, da Interleukin 6 sowohl bei Kaposi-Sarkomen als auch bei einer weiteren Erkrankung, bei der HHV-8 gefunden wurde, der Castlemanschen Erkrankung, offensichtlich eine wichtige Rolle spielt (26, 27). Außerdem kodiert HHV-8 ein Protein, das mit der CD95-(Fas-)Apoptose inter- M E D I Z I N AKTUELL feriert (virales FLIP) (38). Als weiterer Hinweis auf einen infektiösen Prozeß konnten bei Patienten mit Kaposi-Sarkom spezifische Antikörper gegen HHV-8 im Serum nachgewiesen werden (11). Zellinie einzuordnen. In Abbildung 1 ist KS-1 in einer elektronenmikroskopischen Aufnahme zu sehen. Deutlich sind mehrfach umhüllte Viruspartikel zu erkennen. Eine Übertragung von HHV-8 aus Zellinien Elemente gemischt sind. Mittels Insitu-Techniken wurde HHV-8 sowohl in den vaskulären Endothelzellen als auch in Spindelzellen lokalisiert (5, 16). Klinisch fallen KaposiSarkome als erhabene pigmentierte Abbildung 1: Elektronenmikroskopische Darstellung von viralen Einschlußkörpern in der HHV-8-infizierten Zellinie KS-1 (perinukleäre Zisterne, siehe Pfeil, Vergrößerung 1: 56 000) Abbildung 2: Multiple Läsionen eines bioptisch gesicherten Kaposi-Sarkoms bei einem Patienten mit AIDS (generalisierter Befall, teilweise mit Verplattung)* Die Erforschung der Biologie von HHV-8 wurde durch die Etablierung von Zellinien entscheidend erleichtert. Wenn Biopsate von Kaposi-Sarkomen in Kultur genommen werden, so läßt sich HHV-8 meist nur in frühen, jedoch nicht mehr in späteren Passagen nachweisen. Aus HHV-8-assoziierten B-Zell-Lymphomen konnten inzwischen mehrere konstant infizierte Zellinien etabliert werden, die das Virus während der Kultur nicht verlieren (23, 31). Diese B-Zellinien tragen darüber hinaus im Vergleich zu den Primärläsionen der Kaposi-Sarkome ein Vielfaches an Virus. In einigen dieser latent infizierten Zellinien, in denen HHV-8 episomal vorliegt, kann mittels stimulierender Substanzen, wie zum Beispiel Butyrat, eine lytische Infektion induziert werden (13, 16). Eine von uns aus einem malignen Pleuraerguß eines HIV-negativen Patienten gezüchtete HHV-8positive Zellinie, KS-1, ist negativ für die meisten B- und T-Zellantigene. Aufgrund umgelagerter Immunglobulingene ist sie als unreife B- oder Biopsaten auf andere Zellen erwies sich als schwierig, wurde jedoch kürzlich zumindest für einige Passagen auf die embryonale Nierenzellinie 293 beschrieben (10). HHV-8-assoziierte Krankheitsbilder HHV-8 wurde zuerst in AIDSassoziierten Kaposi-Sarkomen entdeckt. Mittels PCR konnten HHV-8Sequenzen von verschiedenen Arbeitsgruppen in 65 bis 100 Prozent der Läsionen von Kaposi-Sarkomen nachgewiesen werden. Es zeigte sich jedoch sehr schnell, daß HHV-8 nicht auf Kaposi-Sarkome bei HIV-Patienten beschränkt ist, sondern auch in Kaposi-Sarkomen nach Organtransplantation und bei spontanen Kaposi-Sarkomen vorkommt. Inzwischen gilt es als sicher, daß HHV-8 in allen Kaposi-Sarkomen nachweisbar ist (1, 7, 9). Histologisch sind KaposiSarkome gekennzeichnet durch eine Proliferation von Endothel- und Spindelzellen, in die entzündliche A-2644 (52) Deutsches Ärzteblatt 94, Heft 41, 10. Oktober 1997 Hautläsionen auf, die bei HIV-infizierten Patienten häufig multizentrisch auftreten (Abbildung 2). Mit Klonalitätsmarkern konnte gezeigt werden, daß Kaposi-Sarkome keine reaktive Proliferation, sondern eine aus einer einzigen Zelle hervorgegangene Neoplasie sind (28). Der klinische Verlauf des Kaposi-Sarkoms variiert von langsam progredient bis fulminant. Ein Hinweis für die ätiopathogenetische Rolle von HHV-8 ist auch, daß diese Virussequenzen in ganz verschiedenen Regionen (Nordamerika, Europa, Asien, Afrika) in Kaposi-Sarkomen nachgewiesen wurden. Der Nachweis von HHV-8 ist mittels PCR an Paraffinfixiertem Material möglich (6). In HIV-infizierten Patienten korreliert der Nachweis von HHV-8 im Blut oder im Sperma direkt mit dem späteren Auftreten eines Kaposi-Sarkoms (39). Wegen der Verwandtschaft mit EBV wurde zunächst in Lymphomen * Wir möchten uns bei Herrn Dr. Jäger, Kuratorium für Immunschwäche, München, für die Überlassung des Fotos bedanken. M E D I Z I N AKTUELL nach HHV-8 gesucht. Die meisten malignen Lymphome sind jedoch negativ für HHV-8, und nur in einer relativ seltenen Gruppe undifferenzierter Lymphome, den „body-cavity-based lymphomas“ oder primären Er- ten vor. PEL proliferieren als Aszites, Pleura- oder Perikarderguß, bilden normalerweise keine Tumoren, sind meist positiv für EBV und haben den Phänotyp unreifer B-Zellen. Im Gegensatz zu Burkitt-Lymphomen ha- Tabelle Seroprävalenz von HHV-8 Nachweis von Antikörpern gegen HHV-8 Probandengruppe IF latente Antigene (12,14,15,35) IF lytische Antigene (15) Immunoblot (p40, p224/236) (11,12,20) ELISA (ORF65) (35) 1) Patienten mit Karposi-Sarkom (KS) a) KS bei AIDS 52–82% 96% 67–80% 81% b) klass. KS 94–100% 100% 100% 94% 2) Risikogruppen Neben Kaposi-Sarkomen und Erguß-Lymphomen konnte HHV-8 noch bei einigen atypischen lymphoproliferativen Syndromen nachgewiesen werden. Hierzu gehören die Multizentrische Castleman-Erkrankung, insbesondere bei HIV-infizierten Patienten (36), und angioimmunoblastische Lymphadenopathien (19). Diese atypischen lymphoproliferativen Erkrankungen haben mit Kaposi-Sarkomen gemeinsam, daß eine Vermehrung proliferativer Zytokine wie Interleukin 6 im Serum beobachtet wird. Auch bei einigen anderen, meist seltenen Erkrankungen wird noch eine Rolle von HHV-8 diskutiert. In der Tabelle sind die mit HHV-8 assoziierten Krankheitsbilder stichpunktartig zusammengefaßt. Diagnostik und Epidemiologie a) Homosexuelle (HIV+) 22–35% b) Homosexuelle (HIV-) 12% c) i.v.-Drogenabhängige (HIV-) 0% d) Hämophile (HIV+) 0–3% e) Hämophile (HIV-) 0% 15% 0% 1% a) Blutspender (USA) 0–1% 10–20% 0% 5% b) Blutspender (D, GB) 3% d) Kinder (USA) 0% 6% e) Erwachsene (Afrika) [12,14] 6–25% 32–82% 90% 13% 23% 31% 5% 0% 3) Normalbevölkerung 2–3% [2] guß-Lymphomen (PEL), ist HHV-8 reproduzierbar nachzuweisen (13, 25). PEL gehören wie Kaposi-Sarkome zu den AIDS-assoziierten Neoplasien, kommen jedoch selten ebenfalls bei nicht HIV-infizierten Patien- ben primäre Erguß-Lymphome keine Überexpression des c-myc-Onkogens. In Abbildung 3 ist der Nachweis von HHV-8 in den Tumorzellen von Patienten mit PEL mittels PCR dargestellt. Die initialen Untersuchungen zeigten eine Spezifität der Expression von HHV-8 für die Läsionen der Kaposi-Sarkome und einige Lymphome beziehungsweise lymphoproliferative Erkrankungen. Bei Patienten mit Kaposi-Sarkom konnte HHV-8 auch in CD19-positiven Zellen nachgewiesen werden, was auf B-Lymphozyten als mögliches Reservoir des Virus hinweist (14). Später wurde HHV-8 mittels PCR im Blut, im Ejakulat und der Prostata von HIV-negativen immunsupprimierten Patienten und vereinzelt bei gesunden Individuen nachgewiesen (4, 8, 22). Diese Daten konnten jedoch zum Teil in anderen Studien nicht reproduziert werden und sind deshalb umstritten (18, 37). Als mögliche Ursache werden PCR-Artefakte oder geographische Unterschiede in der Verbreitung von HHV-8 diskutiert. Doch auch die serologischen Befunde, die im Verlauf des letzten Jahres publiziert wurden, lieferten kein ganz eindeutiges Bild über die Prävalenz des Virus. Der Nachweis von Antikörpern gegen HHV-8-Antigene im Serum ist als Indiz für eine floride oder abgelaufene Infektion zu werten und läßt daher eher Schlüsse über den Verbreitungsgrad Deutsches Ärzteblatt 94, Heft 41, 10. Oktober 1997 (53) A-2645 M E D I Z I N AKTUELL eines Virus zu als die Polymerase-Kettereaktion. Die in mehreren Studien verwendeten Immunfluoreszenztests basierten auf infizierten BZellinien, die entweder unstimuliert zum Nachweis latenter oder stimuliert zur Detektion lytischer Antigene eingesetzt wurden. Zum Nachweis im Immunoblot wurden Zellysate von infizierten Zellen entspreM 1 2 3 4 5 6 7 klassischem oder AIDS-assoziiertem Kaposi-Sarkom seropositiv für HHV-8-Antikörper sind. Bei Risikopatienten, bei denen vor Auftreten eines Kaposi-Sarkoms Serumproben gesammelt wurden, wurde eine Serokonversion sechs bis 75 Monate vor dem klinischen Auftreten des Kaposi-Sarkoms beobachtet (11). Die mittels Immunfluoreszenz er8 9 10 Abbildung 3: Nachweis von HHV-8-DNA-Sequenzen im Tumorgewebe von Patienten mit Kaposi-Sarkom beziehungsweise primären Erguß-Lymphomen (PEL); HHV-8-spezifische Primer, M: Marker für Basenpaare, Agarose-Gel von PCR-Produkten, gefärbt mit Ethidium-Bromid, 1: Kontrolle ohne DNA, 2: positive Kontrolle mit KS-1-DNA; 3: DNA der HHV-8-negativen Zellinie K562, 4: DNA einer Hautläsion eines Kaposi-Sarkoms, 5–10: DNA-Proben von in Los Angeles untersuchten Fällen von PEL chend ihrem Molekulargewicht aufgetrennt und anschließend Antikörper gegen einzelne Virusproteine nachgewiesen. Als stark immunogene Antigene erwiesen sich die latenten HHV-8-Proteinkomplexe p226 und p234, die nukleär lokalisiert sind (12, 20), sowie das in der lytischen Phase exprimierte Protein p40 (11). Einzelne rekombinante Antigene wie p18 (orf 65) (35) oder das von uns verwendete Kapsidprotein orf25 sind in der Regel weniger immunogen und besitzen daher eine geringere Sensitivität (2). Andererseits wird bei Verwendung von rekombinanten Virusproteinen die Spezifität zum Beispiel von kreuzreaktiven Antikörpern gegen verwandte Herpesviren besser kontrolliert. In der Tabelle sind die bisher publizierten Daten zur Seroprävalenz von HHV-8 bei Patienten mit Kaposi-Sarkom, bei HIV-Infizierten und in der Gesamtbevölkerung zusammengefaßt. Aus diesen Daten geht hervor, daß je nach Test bis zu hundert Prozent aller Patienten mit null und 20 Prozent (15). In diesen Untersuchungen haben Personen mit einem höheren Risiko für Geschlechtskrankheiten wie HIV-negative Homosexuelle und HIV-positive Drogenabhängige auch eine höhere Seroprävalenz von HHV-8, was auf eine primäre Übertragung durch Sexualkontakte hinweist. Deutliche Unterschiede scheinen auch zwi- Abbildung 4: Spezifische Antikörper im Serum eines Patienten mit Kaposi-Sarkom, die mit Immunfluoreszenz auf der KS-1-Zellinie nachgewiesen wurden (überwiegende zytoplasmatische Fluoreszenz nach Behandlung der Zellen mit Butyrat, Verdünnung des Serums 1:80, Detektion mit einem FITC-markierten Kaninchen-anti-menschlichen Immunglobulin-Serum) faßten Infektionsraten liegen meist höher im Vergleich zu Immunoblot und ELISA. Die Sensitivität der Immunfluoreszenztests ist höher, da eine polyvalente Immunantwort gegen mehrere Antigene erfaßt wird. Die Sensitivität der Immunfluoreszenztests ist besonders hoch, wenn lytische Antigene untersucht werden, was jedoch möglicherweise auf Kosten der Spezifität geht. Die Seroprävalenz bei HIV-positiven Homosexuellen variiert zwischen 30 und 90 Prozent. Bei Hämophilen, die kein wesentlich erhöhtes Risiko haben, an Kaposi-Sarkom zu erkranken, und bei i.v.-Drogenabhängigen wurde eine Seroprävalenz von 15 beziehungsweise 23 Prozent ermittelt, was sich nicht wesentlich von der Allgemeinbevölkerung im gleichen Testsystem unterschied. Die Prävalenz von HHV-8 in der Allgemeinbevölkerung konnte bisher jedoch auch mit serologischen Methoden nicht eindeutig geklärt werden. Sie variiert zum Beispiel in den USA je nach Studie zwischen A-2646 (54) Deutsches Ärzteblatt 94, Heft 41, 10. Oktober 1997 schen afrikanischen Ländern und Europa beziehungsweise den USA zu bestehen. In Ländern, in denen das Kaposi-Sarkom endemisch vorkommt, liegt die Durchseuchung der Bevölkerung wesentlich höher. Trotz der schlüssigen Hinweise auf eine sexuelle Übertragung sind jedoch auch andere Infektionswege nicht absolut ausgeschlossen. Zusammenfassend läßt sich feststellen, daß sowohl die serologischen wie auch die PCRTests noch einer Verbesserung und Standardisierung bedürfen, um eindeutige Aussagen, zum Beispiel über die Prävalenz in der Normalbevölkerung, machen zu können. Solche Tests würden es auch vereinfachen, die derzeit nicht bekannten klinischen Zeichen einer akuten HHV-8Infektion zu untersuchen. Therapie Vor der Entdeckung von HHV-8 wurden Kaposi-Sarkome mit wechselndem Erfolg abhängig vom klini- M E D I Z I N AKTUELL/FÜR SIE REFERIERT schen Stadium entweder mit lokalen quitär verbreitet. HHV-8 wird in al- koms erhöht. Aufgrund der EpideMaßnahmen wie Exzision und Be- len Formen des Kaposi-Sarkoms so- miologie kann davon ausgegangen strahlung oder mittels systemischer wie bei primären Ergußlymphomen, werden, daß HHV-8 hauptsächlich, Therapie mit Vinblastin, Doxorubicin mit geringerer Häufigkeit bei der jedoch nicht ausschließlich, durch Seund Interferon-a behandelt. Nach sei- Castlemanschen Erkrankung sowie xualkontakte übertragen wird. Rener Entdeckung wurde zunächst in re- in angioimmunoblastischen Lymph- trospektive Studien lassen eine Wirktrospektiven Studien bei HIV-Infi- adenopathien gefunden. HHV-8-po- samkeit der Virostatika Foscarnet zierten die Wirkung von Virostatika sitive Malignome entstehen wahr- und Ganzyklovir vermuten, die jeuntersucht. Tatsächlich wurde in we- scheinlich aufgrund multifaktorieller doch noch nicht als gesichert gelten nigstens einer Studie eine verminder- Genese: Die Infektion mit HHV-8 ist darf. Derzeit sind noch zahlreiche te Inzidenz von KaposiFragen zu HHV-8, zum Sarkomen bei Patienten Beispiel die MechanisKrankheitsbilder assoziiert mit HHV-8 gefunden, die wegen anmen der Transformation derer Herpesvirusinfek- AIDS-assoziiertes Kaposi-Sarkom Chang et al. 1994(7) durch HHV-8, die InfekDupin et al. 1995 (9) tionen mit Ganzyklovir Klassisches Kaposi-Sarkom tionswege und die PrävaNador et al. 1996 (25) oder Foscarnet behandelt Primäre Ergußlymphome lenz in gesunden IndiviSoulier et al. 1996 (36) wurden (21). Prospektive Castlemansche Krankheit duen, nicht vollständig Studien über die Wirkung Angioimmunoblastische beantwortet. Bereits zum Luppi et al. 1996 (19) dieser Virostatika bei Pa- Lymphadenopathie jetzigen Zeitpunkt ist zu Sander et al. 1996 (33) tienten mit Kaposi-Sar- Mycosis fungoides erkennen, daß die ErSaid et al. 1997 (32) kom sind im Moment Enzephalitis forschung von HHV-8 nicht publiziert, jedoch neue therapeutische und wurde über eine positive präventive Strategien für Wirkung von Foscarnet in Einzelbe- zwar notwendig, aber nicht hinrei- die mit HHV-8 assoziierten Erkranobachtungen berichtet (24). Über den chend für eine Transformation der in- kungen bringen dürfte. Erfolg von Virostatika bei HHV-8-as- fizierten Zellen. Weitere, derzeit soziierten lymphoproliferativen Er- nicht eindeutig identifizierte Fakto- Zitierweise dieses Beitrags: krankungen ist derzeit nichts be- ren, wie zum Beispiel Immunsup- Dt Ärztebl 1997; 94: A-2642–2647 pression und Zytokine spielen offen- [Heft 41] kannt. sichtlich ebenfalls eine wichtige Rolle in der Pathogenese HHV-8-assoziier- Die Zahlen in Klammern beziehen sich auf ter Erkrankungen. Die klinischen das Literaturverzeichnis, das über den SonSchlußfolgerungen Zeichen einer akuten HHV-8-Infek- derdruck und über die Internetseiten (unter HHV-8 ist ein neuentdecktes hu- tion sind derzeit nicht bekannt. Ein http://www.aerzteblatt.de) erhältlich ist. manes Herpesvirus, das mit dem Ep- Nachweis von HHV-8 ist im Moment stein-Barr-Virus eng verwandt ist und nur möglich mittels PCR. Serologi- Anschrift für die Verfasser ähnlich wie EBV B-Lymphozyten in- sche Tests sind in Entwicklung, kom- Priv.-Doz. Dr. med. R. Munker fiziert und als tumorinduzierendesVi- merziell jedoch noch nicht erhältlich. Medizinische Klinik III der rus verdächtigt wird. Im Gegensatz Durch den molekularen Nachweis Ludwig-Maximilians-Universität zu EBV ist HHV-8 in der Gesamtbe- von HHV-8 hat sich die diagnostische Klinikum Großhadern völkerung in Nordamerika und Mit- Sicherheit für unklare Hautläsionen Marchioninistraße 15 teleuropa wahrscheinlich nicht ubi- und Frühformen des Kaposi-Sar- 81377 München Knochendichte bei Frauen mit Depression Depressionen sind komplexe Krankheiten, die genetische, entwicklungs- oder umweltbedingte Ursachen haben können. Bei Frauen mit einer depressiven Störung wurde eine verminderte Knochendichte festgestellt. Beim Vergleich der Knochendichte an Hüfte/Femur und Wirbelsäule zwischen 24 Frauen mit aktuellen oder vorausgegangenen Episoden von Depression und ebensovielen psychisch gesunden gleichaltrigen Frauen mit ähnlichem Gewicht und gleichem Me- nopausenstatus zeigte sich bei den depressiven Patientinnen eine um 6,5 Prozent verminderte Mineralisierung der Wirbelsäule, im Bereich des Oberschenkelhalses lag der Unterschied bei 13,6 Prozent. Bei der Untersuchung des Knochenstoffwechsels zeigt sich bei den Frauen mit Depression unter anderem eine höhere Kortisolausscheidung im Urin und eine niedrigere Kalzitoninkonzentration im Serum. Daher kamen die Autoren zu dem Schluß, daß veränderte Verhaltensweisen und neuroendokrinologische Regulationsmechanismen bei Depression die Knochendichte nachweislich in einem Maß verringern, daß besonders bei jüngeren Frauen ein erhöhtes Risiko für spätere pathologische Frakturen entsteht. silk Michelson D, Stratakis C, Hill L et al.: Bone mineral density in women with depression, N Engl J Med 1996; 335: 1176–1181. Dr. Michelson, Warren G. Magnuson Clinical Center, Room 2D 46, MSC 1284, National Institutes of Health, Bethesda, MD 20892–1284, USA. Deutsches Ärzteblatt 94, Heft 41, 10. Oktober 1997 (55) A-2647