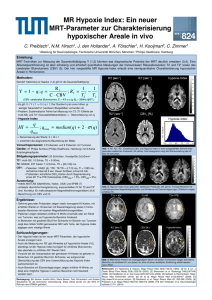
Eigenschaften und Potential der Sliding-Multi-Slice
Werbung

Aus der Radiologischen Universitätsklinik Abteilung Röntgendiagnostik - Medizin Physik der Albert-Ludwigs-Universität Freiburg i. Br. Eigenschaften und Potential der Sliding-Multi-Slice-MRT als abdominale Staging-Untersuchung beim Rektumkarzinom und anderen malignen Tumoren des Beckens INAUGURAL-DISSERTATION zur Erlangung des Medizinischen Doktorgrades der Medizinischen Fakultät der Albert-Ludwigs-Universität Freiburg i. Br. Vorgelegt 2008 von Gregor Sommer geboren in Rottweil 2 Dekan: Prof. Dr. med. Christoph Peters 1. Gutachter: Prof. Dr. rer. nat. Jürgen Hennig 2. Gutachter: PD Dr. med. N. N. Jahr der Promotion: 2008 Inhaltsverzeichnis Einleitung 1 1 Grundlagen 3 1.1 Das Rektumkarzinom . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3 1.1.1 Epidemiologie und Krankheitsbild . . . . . . . . . . . . . . . . . . . . . . . . 3 1.1.2 Klassikation . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5 1.1.3 Diagnostik . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 10 1.1.4 Prognose und Therapie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 15 Spezielle MRT-Verfahren zur Untersuchung groÿer Körperregionen . . . . . . . . . . 19 1.2.1 Move During Scan (MDS): MRT bei bewegtem Patiententisch . . . . . . . . 20 1.2.2 Sliding Multi Slice (SMS) . . . . . . . . . . . . . . . . . . . . . . . . . . . . 21 1.2 2 3 Methoden 25 2.1 Abdomenbildgebung mit SMS . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 25 2.2 Untersuchungsprotokoll . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 27 2.3 Patienten . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 28 2.4 Datenauswertung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 28 Ergebnisse 31 3.1 Bildqualität . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 31 3.2 Detektierbarkeit der Läsionen und CNR . . . . . . . . . . . . . . . . . . . . . . . . . 33 I II 4 INHALTSVERZEICHNIS Diskussion 37 Zusammenfassung 41 Literaturverzeichnis 43 Publikationsliste 55 Danksagung 57 Einleitung Maligne Tumorerkrankungen des Beckens, insbesondere das Rektumkarzinom, gehören zu den häugsten Ursachen krebsbedingter Todesfälle weltweit. Um die Prognose der betroenen Patienten zu ermitteln und zu einer adäquaten Therapieentscheidung zu gelangen, ist die Beantwortung der Frage, ob zum Zeitpunkt der Diagnose bereits eine metastatische Tumorausbreitung stattgefunden hat oder nicht, von entscheidender Bedeutung. Eine suziente Diagnostik erfordert aus diesem Grund über die Beurteilung der lokalen Verhältnisse hinaus die Einbeziehung multipler Organsysteme und Körperregionen. Die heutzutage in Primärdiagnostik und Nachsorge von Tumoren verwendeten Bildgebungsprotokolle entsprechen einer Kombination aus sich zum Teil ergänzenden und teils überlappenden Verfahren [Her 99, Bip 04, Bip 05, Sau 02, Kin 02, Sch 06]. Solche multimodalen Konzepte besitzen einerseits ein hohes diagnostisches Potential, andererseits sind sie aber auch kosteninezient und zeitaufwendig und erfordern ein beträchtliches Ausmaÿ an materieller Ausstattung und Personal. Die Verwendung einer einzigen, sogenannten 'stand alone' Modalität könnte hier signikant zu einem vereinfachten Patientenmanagement beitragen, dadurch Aufwand und Kosten senken und in der Folge nicht zuletzt auch den Patientenkomfort erhöhen [Sch 06]. Die Magnetresonanztomographie (MRT) ist als zuverlässiges Verfahren für das Staging von Tumorerkrankungen bekannt. Insbesondere bei Patienten mit malignen Neoplasien des Beckens, wie dem Rektumkarzinom, gilt sie als führende Methode zur Beurteilung der lokalen Tumorausbreitung [Sto 00, Mar 97, Tor 03] und der Detektion und Dierenzierung von Lebermetastasen [Bip 05, Kin 02]. Ein MRT-Untersuchungsprotokoll, das fähig sein soll, mit multimodalen Verfahren Schritt zu halten, muÿ jedoch nicht nur höchste diagnostische Genauigkeit in der Beantwortung der einzelnen Fragestellungen besitzen, sondern auch in der Lage sein, groÿe Bereiche des menschlichen Körpers in einer vertretbaren Zeitspanne abzubilden [Sch 06]. In den vergangenen Jahren wurden dazu eine Zahl an maÿgeschneiderten Hardwarelösungen [Fen 06, Kra 05, Sch 05] und Aufnahmemethoden [Kru 02, Joh 97, Bar 01, Lud 06, Lau 04] vorgestellt, deren gemeinsames Charakteristikum die Verwendung eines kontinuierlich bewegten Patiententisches 1 2 EINLEITUNG ist. 2006 präsentierten Fautz und Kannengiesser das Sliding-Multi-Slice-Verfahren (SMS), eine axiale 2D-Aufnahmemethode bei kontinuierlich bewegtem Patiententisch, die eine schnelle und nahtlose Abdeckung erweiterter Untersuchungsregionen unter Minimierung von Feldverzerrungen und Bewegungsartefakten ermöglicht [Fau 06]. Die vorliegende Arbeit untersucht erstmals die Anwendbarkeit des SMS-Verfahrens in der bildgebenden Diagnostik solider Tumoren. Zu diesem Zweck wurde eine maÿgeschneiderte SMS-Sequenz zur Darstellung des gesamten Abdomens und Beckens bei kontinuierlich bewegtem Patiententisch in ein Standard-Untersuchungsprotokoll zur hochaufgelösten MRT des Beckens integriert und an einem Kollektiv von 22 Patienten mit malignen Neoplasien des Beckens, hauptsächlich Rektumkarzinomen, evaluiert. Ziele der verwendeten Methode waren: 1. Die Aufnahme hochaufgelöster T1 -gewichteter MRT-Daten des gesamten Abdomens und Beckens bei kontinuierlichem Tischvorschub. 2. Eine schnelle Datenakquisition, die lediglich eine einzige Atemanhaltephase erfordert. 3. Hohe Robustheit gegenüber Bewegungsartefakten insbesondere in den diagnostisch besonders relevanten Bereichen des Oberbauchs und des Retroperitonealraums. Der Inhalt dieser Arbeit wurde 2008 im Journal of Magnetic Resonance Imaging publiziert und beim Jahreskongress 2006 der International Society for Magnetic Resonance in Medicine in Seattle in Form mehrer Beiträge vorgestellt. Kapitel 1 Grundlagen 1.1 Das Rektumkarzinom 1.1.1 Epidemiologie und Krankheitsbild Sechs der fünfzehn in Deutschland häugsten Tumorerkrankungen haben ihren Ursprung in Organen des Beckens. Gemeinsam entfallen auf sie ca. 40 % der jährlichen Krebsneuerkrankungen in Deutschland. Geordnet nach der Häugkeit der Neuerkrankungen pro Jahr (Inzidenz) sind dies [GEK 06]: 1. Darmkarzinome (Männer 16,3 %, Frauen 17,4 %) 2. Prostatakarzinome (22,3 % der Männer) 3. Harnblasenkarzinome (Männer 8,6 %, Frauen 3,5 %) 4. Karzinome des Corpus und der Cervix uteri (5,5 % und 3,2 % der Frauen) 5. Ovarialkarzinome (4,8 % der Frauen) Darmkarzinome stellen damit für beide Geschlechter nach dem Bronchialkarzinom (Männer) beziehungsweise dem Mammakarzinom (Frauen) die zweithäugsten Krebserkrankungen und auch die zweithäugste Krebstodesursache dar. Die Zahl der Neuerkrankungen in Deutschland beträgt etwa 70.000 (= 25 / 100 000 Einwohner) pro Jahr. Damit entwickelt etwa jeder 50. Deutsche im Laufe seines Lebens ein kolorektales Karzinom. Die Tendenz der Erkrankungsraten ist dabei in Deutschland wie auch in anderen westlichen Industrienationen deutlich im Anstieg begrien. Männer erkranken im Mittel mit 69, Frauen mit 75 Jahren. Erkrankungen vor dem 40. Lebensjahr sind eher selten. Als Risikofaktoren für kolorektale Karzinome gelten vorrangig Bewegungsmangel und ernährungsbe3 4 KAPITEL 1. GRUNDLAGEN dingte Faktoren, wie hohe alimentäre Fettzufuhr und schlackenarme Kost. Verwandte ersten Grades von Patienten mit kolorektalen Karzinomen sind überdurchschnittlich häug ebenfalls von Darmkrebs betroen. Einen weitereren Risikofaktor stellt das Auftreten kolorektaler Adenome dar (sogenannte Adenom-Karzinom-Sequenz), wobei vor allem bei Gröÿen über 1 cm oder multiplen Adenomen ein deutlich erhöhtes Entartungsrisiko gegeben ist. Bei der sehr seltenen erblichen familiären adenomatösen Polyposis (FAP) sowie dem erblichen nicht-polypösen kolorektalen Krebssyndrom (HNPCC) treten mit hoher Wahrscheinlichkeit bereits in jüngeren Jahren Darmkrebsfälle in den betroenen Familien auf. In geringerem Maÿe erhöhen chronisch-entzündliche Darmerkrankungen, wie beispielsweise die Colitis ulcerosa, das Darmkrebsrisiko [GEK 06]. Das kolorektale Karzinom tritt in der Regel als soli- Abbildung 1.1: Prozentuale Häugkeit kolorektaler Karzinome nach anatomischer Lage [Ren 04]. tärer Tumor auf. Lediglich in 2-5 % der Fälle wurden multiple primäre Manifestationen beschrieben. Mit etwa 60 % entfällt der weitaus gröÿte Teil aller Manifestationen auf das Rektum. Danach folgen das Sigma mit ca. 20 %, Coecum und Colon ascendens mit ca. 10 % sowie das übrige Colon mit ebenfalls ca. 10 % (Abb. 1.1). Die meisten kolorektalen Karzinome bleiben lange Zeit symptomlos. Bei ca. 25 % der Patienten liegt zum Zeitpunkt der Diagnosestellung bereits eine metastatische Ausbreitung vor. Häuges Symptom ist sichtbares oder okkultes Blut im Stuhl, das bis zum denitiven endoskopischen oder bioptischen Ausschluÿ als Hinweis auf ein Kolorektalkarzinom gelten muÿ. Damit verbunden sind oftmals Allgemeinsysmptome oder Symptome einer Tumoranämie, wie Müdigkeit, Leistungsknick, Schwäche oder Gewichtsverlust. Ein weiteres Symptom kann eine Änderung der Stuhlgewohnheiten sein. Dazu gehören paradoxe Diarrhöen (Durchfall bei eigentlich stenosierendem 1.1. 5 DAS REKTUMKARZINOM Prozeÿ) oder das sogenannte Symptom des falschen Freundes (Stuhlabgang statt vermeintlichem Gasabgang). Bei distal gelegenen Karzinomen besteht vermehrt ein Gefühl der inkompletten Entleerung oder es werden Bleistiftstühle abgesetzt. Schmerzen sind eher selten wegweisend für die Diagnose eines Kolorektalkarzinoms, sondern treten meist erst in fortgeschrittenen Erkrankungsstadien auf [Sie 01, Ren 04]. 1.1.2 Klassikation Einteilung nach anatomischer Lage und Ausbreitung: Staging Wachstum und Ausbreitung solider maligner Tumoren erfolgen auf drei Wegen: 1. Kontinuierliche Ausbreitung 2. Lymphogene Metastasierung 3. Hämatogene Metastasierung Diese dreigliedrige Unterteilung bildet die Grundlage der TNM-Klassikation [UICC 02], die die heute am besten evaluierte Standardeinteilung solider maligner Tumoren darstellt. Das kontinuierliche Wachstum des Primärtumors wird duch das T-Staging erfasst. Die Ausbreitung vollzieht sich bei Rektumkarzinomen vor allem in transversaler Richtung. Die Inltration der nacheinander angeordneten zirkulären Wandschichten von Rektumwand und perirektalen Geweben dient als Klassikationskriterium des T-Staging (Tab. 1.1 und Abb. 1.2). Beschreibung des Befalls Bezeichnung Primärtumor kann nicht beurteilt werden Tx Kein Anhalt für einen Primärtumor T0 Inltration der Submucosa T1 Inltration der Muscularis propria T2 Inltration der Subserosa bzw. des perirektalen Gewebes T3 Inltration von Nachbarorganen oder Perforation des viszeralen Peritoneums T4 Tabelle 1.1: TNM-Klassikation des Rektumkarzinoms, T-Staging. Man unterscheidet die präoperativ klinisch oder bildgebend bestimmten Stadien, die mit dem Index c versehen werden (z.B. cT2 cN0 cM0) von der postoperativ erhobenen, pathologischen Klassikation, die mit dem Index p bezeichnet wird (nach [UICC 02]). 6 KAPITEL 1. GRUNDLAGEN Von der Mucosa ausgehend durchdringt der Tumor dabei die Schichten von Submucosa, Muscularis propria, Subserosa und Serosa, bis es in späten Stadien (T4) zur Inltration benachbarter Organstrukturen des kleinen Beckens, wie der Harnblase, des Uterus, der Prostata, der Ureteren oder der Ovarien, beziehungsweise bei hoch sitzenden Tumoren zur Perforation des viszeralen Peritoneums kommt. In longitudinaler Richtung ist die Ausbreitungstendenz geringer und ndet dann eher in oraler Richtung statt, während die aborale intramurale Metastasierung selten über 2 cm beträgt. Von einem fortgeschrittenen Karzinom spricht man nach Durchbruch der Lamina muscularis (T3-4). Abbildung 1.2: Anatomische Veranschaulichung der T-Klassikation. Modiziert nach [Bee 04]. Bereits mit dem Erreichen der Submucosa (T1) steigt das Risiko für lymphatische Metastasierung sprunghaft auf 10-20 %, da der Tumor hier erstmals Anschluÿ an drainierende Lymphbahnen erhält. Die lymphogene Metastasierung wird durch das N-Staging erfaÿt und erfolgt über Lymphgefäÿe, die entlang der versorgenden Blutgefäÿe verlaufen. Dabei ergibt sich eine entscheidende Abhängigkeit von der Lokalisation des Primärtumors. Rektumkarzinome werden deshalb nach der UICC (Union Internationale Contre le Cancer) [UICC 02] nach Ihrem Abstand von der Anocutanlinie in drei Gruppen unterteilt: 1. Karzinome des oberen Rektumdrittels (12-16 cm ab Anocutanlinie) 2. Karzinome des mittleren Rektumdrittels (6-12 cm ab Anocutanlinie) 3. Karzinome des unteren Rektumdrittels (< 6 cm ab Anocutanlinie) Hoch sitzende Karzinome metastasieren entlang der Rectalis-superior Gefäÿe nach kranial in Richtung der paraaortalen Lymphknoten. Karzinome der mittleren Etage metastasieren zusätzlich entlang der Rectalis media Gefäÿe nach lateral in die Beckenlymphknoten. Tiefsitzende Karzinome metastasieren zusätzlich nach kaudal zu den iliakalen und inguinalen Lymphknoten. Karzinome des unteren Rek- 1.1. 7 DAS REKTUMKARZINOM tumdrittels weisen dabei eine höhere Rate von Lymphknotenmetastasen (34%) auf, als Karzinome des mittleren (11%) und oberen Rektumdrittels (8%) [Nas 02]. 90% der mesorektalen Lymphknotenmetastasen werden unmittelbar um das Karzinom und innerhalb eines Abstandes von 2 cm proximal des Tumors gefunden [Koh 05]. Kriterium des N-Staging ist die Gesamtanzahl befallener mesorektaler Lymphknoten (Tab. 1.2). Beschreibung des Befalls Bezeichnung Status der lymphatischen Metastasierung nicht bekannt Nx Keine regionären Lymphknotenmetastasen N0 Befall von 1-3 mesorektalen Lymphknoten N1 Befall von > 3 mesorektalen Lymphknoten N2 Befall von Lymphknoten entlang zuführender Arterien N3 Tabelle 1.2: TNM-Klassikation des Rektumkarzinoms, N-Staging (nach [UICC 02]) Die Absiedlung von Tumoranteilen via Blutbahn mit Manifestation als Fernmetastasen in anderen Organen wird durch das M-Staging erfaÿt (Tab. 1.3). Sie erfolgt im Falle kolorektaler Tumoren primär über das Pfortadersystem in die Leber (mit 75% bevorzugte Lokalisation). Von dort ist eine sekundäre hämatogene Metastasierung über die Vena cava inferior und die Pulmonalarterien in die Lunge möglich (ca. 15%). Seltener und vor allem in fortgeschrittenen Stadien sind auch das Skelettsystem und das zentrale Nervensystem betroen (jeweils ca. 5%) [Que 97]. Beschreibung des Befalls Bezeichnung Status der Fernmetastasierung nicht bekannt Mx Keine Fernmetastasen M0 Fernmetastasen vorhanden M1 Tabelle 1.3: TNM-Klassikation des Rektumkarzinoms, M-Staging (nach [UICC 02]) Das Gesamtstadium der TNM-Klassikation ergibt sich aus den separat ermittelten T-, N-, und MStadien nach Tab. 1.4. Daneben exisistiert als ebenfalls häug verwendetes Schema die nach AstlerColler modizierte Klassikation nach Dukes [Ast 54], deren Stadien nach Tab. 1.5 mit der TNMKlassikation korreliert werden können. 8 KAPITEL 1. Stadium TNM-Bezeichnung Stadium TNM-Bezeichnung 0 Tis, N0, M0 III A T1-2, N1, M0 I T1-2, N0, M0 III B T3-4, N1, M0 II A T3, N0, M0 III C jedes T, N2, M0 II B T4, N0, M0 IV jedes T, jedes N, M1 GRUNDLAGEN Tabelle 1.4: Stadieneinteilung des Rektumkarzinoms (nach [UICC 02]) Stadium nach Astler-Coller TNM Tumorausbreitung Stadium A T1 N0 M0 Tumor ist auf die Mukosa und Submukosa begrenzt. Keine Lymphknotenmetastasen Keine Fernmetastasen Stadium B1 T2 N0 M0 Tumor erreicht die Muscularis propria ohne sie zu überschreiten. Keine Lymphknotenmetastasen Keine Fernmetastasen Stadium B2 T3 N0 M0 Inltration des perirektalen Fettgewebes. Keine Lymphknotenmetastasen Keine Fernmetastasen Stadium C1 T2 N1 M0 Tumor ist auf die Rektumwand begrenzt. Lymphknotenmetastasen vorhanden Keine Fernmetastasen Stadium C2 T3 N1 M0 Inltration des perirektalen Fettgewebes. Lymphknotenmetastasen vorhanden Keine Fernmetastasen Stadium D M1 Fernmetastasen Tabelle 1.5: Staging des Rektumkarzinoms (Dukes 1932; Astler-Coller 1954 [Ast 54]) 1.1. 9 DAS REKTUMKARZINOM Histopathologische Einteilung Histologisch werden, geordnet nach Häugkeit, folgende Typen kolorektaler Karzinome unterschieden [Que 97]: 1. Dierenzierte Adenokarzinome: Tubulär, azinär oder papillär (80 % aller kolorektalen Karzinome) 2. Muzinöse Adenokarzinome: Adenokarzinome mit mehr als 50 % extrazellulärer muzinöser Tumormasse (10 %) 3. Siegelringzellkarzinom: Prominenter Anteil an Siegelringzellen (häuger assoziiert mit colitis ulcerosa) 4. Plattenepithelkarzinome: Sehr selten (häug beim Karzinom des Analkanals) 5. Adenosquamöses Karzinom: Adenokarzinom mit Anteilen eines Plattenepithelkarzinoms (sehr selten) 6. Kleinzelliges Karzinom: Neuroendokrines Karzinom (hochmaligne) 7. Undierenzierte/anaplastische Karzinome: Maligne epitheliale Tumoren ohne jegliche Dierenzierungszeichen (10 %) Zur Beurteilung der Malignität des Tumors innerhalb des TNM-Schemas dient das sogenannte Grading. Es bezeichnet in drei Stufen den Dierenzierungsgrad des Tumors und wird nach histo- und zytomorphologischen Kriterien anhand bioptisch oder operativ resezierten Tumorgewebes bestimmt (Tab. 1.6). Das histopathologische Staging, das postoperativ am intraoperativ resezierten Material Beschreibung Bezeichnung Hoher Grad der Dierenzierung G1 Mittlerer Grad der Dierenzierung G2 Geringer Grad der Dierenzierung G3 Tabelle 1.6: Histopathologisches Grading von Adenokarzinomen 10 KAPITEL 1. GRUNDLAGEN durchgeführt wird, dient zur Bestätigung bzw. Korrektur und Verfeinerung der präoperativ gewonnenen cTNM-Klassikation. Eine Verfeinerung erfährt hier insbesondere das Stadium T3, das nach dem Grad der perimuskulären Inltration weiter unterteilt wird in pT3a: < 1mm pT3b: 1-5 mm pT3c: 5-15 mm pT3d: > 15 mm. Diese Einteilung spiegelt signikante Unterschiede in der Behandlungsprognose wider, da das Ausmaÿ der lateralen Ausbreitung und damit der Abstand vom Resektionsrand mit dem Metastasierungsund Rezidivrisiko korelliert [DKG 04]. Auch das Stadium T1 erfährt eine weitere histopathologische Spezizierung, die in Kombination mit dem Grading mit der Einteilung in Low-risk-Karzinome (G1, G2; keine Lymphgefäÿinvasion) und High-Risk-Karzinome (G3; Lymphgefäÿinvasion) eine Aussage über das Risiko einer lymphatischen Metastasierung gestattet. 1.1.3 Diagnostik Vorsorge Kolorektale Karzinome sind wie wenige andere maligne Tumore durch Maÿnahmen der sekundären Prävention bereits in Frühstadien erfassbar. Erste Hinweise gibt die Anamnese mit Fragen nach Gewichtsverlust, Stuhlgewohnheiten und Allgemeinsymptomen. Hauptinstrument der Vorsorge ist der fäkale Okkultblut-Test (Hämoccult), dessen Durchführung bei Patienten ab dem 40. Lebensjahr gemeinsam mit der Inspektion des Anus und der digitalen rektalen Untersuchung im Rahmen einer regelmäÿigen Screeninguntersuchung empfohlen wird. Ein positiver Hämoccult-Test, obgleich in 2/3 der Fälle falsch positiv, gilt als Hinweis auf ein colorektales Karzinom und erfordert stets dessen Ausschluÿ durch eine Kolonoskopie. Mittels Hämoccult-Test werden etwa 50 % der Kolorektalkarzinome erfaÿt. Deshalb wird in Abständen von 3-5 Jahren unabhängig vom Hämoccult-Test die Durchführung einer Rektosigmoidoskopie empfohlen. Hochrisikogruppen werden entsprechend früher und engmaschiger überwacht. Insgesamt wird die Sensitivität des derzeitigen Screenings für das Rektumkarzinom mit etwa 75 % angegeben. [Ren 04]. Erstdiagnose und Staging Verfahren der Wahl zur Bestätigung oder zum Ausschluÿ eines kolorektalen Karzinoms bei bestehendem Verdacht ist die Rektosigmoidoskopie beziehungsweise Kolonoskopie mit Biopsie suspekter Strukturen. Dabei erfolgt mit der Messung des Abstands von der Linea anocutanea bereits eine erste 1.1. DAS REKTUMKARZINOM 11 anatomische Klassizierung. Bei positivem rektosigmoidoskopischem Befund wird eine Kolonoskopie des gesamten Colons zum Ausschluÿ von Zweittumoren durchgeführt. Der Nachweis multipler Polypen, Familienanamnese und molekulargenetische Untersuchungen geben Hinweise auf hereditäre Formen (HNPCC oder FAP). In Ausnahmefällen, etwa dann, wenn der betroene Darmabschnitt einer Kolonoskopie nicht zugänglich ist, ist eine Einsatz radiologischer bildgebender Verfahren, wie beispielsweise der Doppelkontrast-Untersuchung oder sogenannten virtuellen Kolonoskopie auch im Rahmen der Erstdiagnose möglich. Ein histologischer Tumornachweis ist jedoch auch hier zwingend erforderlich und muÿ dann gegebenenfalls auf operativem Wege erfolgen. Das Staging nach gesicherter Diagnose ist die Domäne der bildgebenden Diagnostik. Zur lokalen Beurteilung kolorektaler Karzinome (T-Staging) stehen im Wesentlichen drei Verfahren zur Verfügung. Dies sind die endoluminale Sonographie (ES), die Computertomographie (CT) und die Magnetresonanztomographie (MRT). Bei fortgeschrittenen Tumoren mit Verdacht auf lokale Inltration benachbarter Organe des kleinen Beckens kann zusätzlich der Einsatz spezieller Verfahren der urologischen oder gynäkologischen Diagnostik indiziert sein. Die Stärken der Endosonographie liegen nachgewiesenermaÿen in der exakten Evaluation oberächlicher Karzinome bezüglich ihrer Inltrationstiefe. Insbesondere hinsichtlich der Unterscheidung zwischen den Tumorstadien T1 und T2 ist die ES unverzichtbarer Baustein der Stagingdiagnostik (Abb. 1.3). So liegt etwa die Spezität der ES für die Erkennung einer Muscularis-propria-Inltration, die Kriterium für das Stadium T2 ist, mit 80 bis 90 % signikant höher als die der MRT (52 bis 82%) [Bee 04,Bip 04]. Bei fortgeschrittenen Tumorstadien reduzieren sich die Vorteile der ES allerdings zunehmend aufgrund der limitierten akustischen Eindringtiefe [Aka 05, Gar 02]. Die hochaufgelöste MRT des Beckens stellt das Verfahren der Wahl zur lokalen Beurteilung von Rektumkarzinomen der Stadien T2-T4 dar. Hierfür existiert eine Vielzahl von Untersuchungsprotokollen [Aka 05, Bro 04, Chu 06, Kim 06a, Pes 05, Vli 05]. Allen gemeinsam ist die Verwendung nicht fettgesättigter schneller T2 -gewichteter Spinechosequenzen (Turbo-Spinechosequenzen/TSE) mit Schichtdicken von ca 2-3 mm, die senkrecht zum tumortragenden Darmabschnitt ausgerichtet werden. Zur Kontrastoptimierung und zur Ruhigstellung des Darms werden die Aufnahmen nach rektaler Flüssigkeitsinstillation (150 ml) und intravenöser Gabe eines Spasmolytikums (Butylscopolamin oder Glukagon) durchgeführt. Dadurch gelingt in der Regel eine gute Dierenzierung von Submukosa und Muscularis propria, in Einzelfällen sogar eine Darstellung der Mukosa. Karzinome stellen sich in der T2 -TSE hyperintens relativ zur Darmwandmuskultur und hypointens relativ zur Submukosa dar (Abb. 1.3). Die intravenöse Gabe Gadolinium-haltiger Kontrastmittel (KM) in Kombination 12 KAPITEL 1. GRUNDLAGEN mit T1 -gewichteten Gradientenechosequenzen mit Fettsättigung ist Gegenstand kontroverser Diskussion [Mai 00, Oki 96, Vli 05, Vog 97]. Karzinome stellen sich in diesen Aufnahmen hypointens relativ zur Mukosa und Muscularis propria dar, die in der Regel aufgrund ihrer straken Durchblutung eine intensive KM-Aufnahme zeigen. Als Vorteil der KM-unterstützten Bildgebung wird insbesondere eine bessere Beurteilbarkeit der Analsphinkteren bezüglich einer Inltration bei tiefsitzenden Karzinomen genannt [Sch 04]. Nachteile der i.v.-Kontrastmittelapplikation sind der erhöhte zeitliche und nanzielle Aufwand sowie das Risiko möglicher Kontrastmittelnebenwirkungen. Auch mit der Computertomographie ist eine Lokaldiagnostik rektaler Karzinome im Rahmen von Staging und Nachsorge möglich, jedoch ist die Aussagekraft CT gegenüber der MRT in einigen wesentlichen Punkten limitiert. Zu nennen sind in diesem Zusammenhang die fehlende Dierenzierbarkeit der Wandschichten des Rektums, die schlechte Darstellbarkeit der mesorektalen Faszie sowie die mangelnde Genauigkeit bei der Detektion von Tumorinltration in umgebende Organe. Neuere Verfahrensentwicklungen der Multislice-CT (MSCT) erreichen durch hochauösende Akquisition und eine multiplanare Darstellung in sekrechter Angulierung zum tumortragenden Darmabschnitt deutlich verbesserte Ergebnisse [Sin 06, Stü 05, Tay 07]. Ob letzlich eine Vergleichbarkeit der MSCT mit der MRT erreichbar ist, erscheint aber trotz dieser Fortschritte fraglich. Abbildung 1.3: Lokales Staging des Rektumkarzinoms. Links: Endosonographie. Mit Pfeilen gekennzeichnet die vier Wandschichten von Mukosa (1), Muscularis mucosae (2), Submukosa (3) und Muskularis propria (4). Der Tumor (Tu) überschreitet die Muskularis propria nicht und entspricht damit einem Stadium T2. Rechts: T2 w MRT. Die mit dem schwarzen Pfeil gekennzeichtete Muskularis propria ist nicht durchgehend abgrenzbar, der Tumor (weiÿe Pfeile) entspricht damit einem Stadium T3 [Bee 07]. 1.1. DAS REKTUMKARZINOM 13 Zweites wesentliches Ziel der Stagingdiagnostik ist die Detektion von Lymphknotenmetastasen. Eine besondere Eigenschaft des Rektumkarzinoms ist die hohe Frequenz von Mikrometastasen in normal groÿen Lymphknoten [Koh 06]. Eine Studie, die 424 Operationspräparate mit insgesamt 12.759 mesorektalen Lymphknoten auswertete, ermittelte als durchschnittlichen Durchmesser der Lymphknotenmetastasen 3,84 mm, während der durchschnittliche Durchmesser aller gefundenen Lymphknoten bei nur unswesentlich geringeren 3,34 mm lag. Es gestaltet sich daher schwierig, Lymphknoten allein aufgrund ihrer Gröÿe als metastasensuspekt einzuordnen. So hat sich gezeigt, daÿ sich durch die Wahl eines festen Cut-o-Wertes von beispielsweise 5 mm als Dierenzierungskriterium zwischen benigne und maligne nur eine mäÿige Sensitivität und Spezität in der Vorhersage eines Lymphknotenbefalls erreichen läÿt [Mon 99]. Diese Limitation betrit sämtliche Verfahren der morphologischen Bildgebung oenbar in gleichem Maÿe. Eine vergleichende Meta-Analyse ergab hinsichtlich der Lymphknoten-Metastasendetektion keine signikanten Unterschiede zwischen ES (Sensitivität 67%/ Spezität 78%), CT (55%/74%) und MRT (66%/76%) [Bip 04]. Als generell untere Nachweisgrenze für eine verlässliche Detektion von Lymphknotenmetastasen beim Rektumkarznom gilt zurzeit eine Gröÿe von >2 mm [Sch 07]. Honungen, diese Ergebnisse durch das funktionelle Bildgebungsverfahren der FDG-PET wesentlich zu verbessern, konnten sich bisher nicht bestätigen. Als Gründe hierfür wird zum einen die hohe Auösungsgrenze der FDG-PET von ca 5 mm genannt sowie zum anderen der Glukosehypermetabolismus des Primärtumors, durch den umgebende Lymphknotenmetastasen im Bild maskiert werden können [vSc 06]. Dritte Disziplin der präoperativen Staginguntersuchung ist die Beurteilung von Fernmetastasen (MStaging). Das mit einem Anteil von 75% mit Abstand am häugsten von einer Fernmetastierung kolorektaler Karzinome betroene Organ ist die Leber. Die metastatische Ausbreitung ist zum Zeitpunkt der Diagnose in 30%-40% der Fälle auf die Leber beschränkt, eine Resektion in kurativer Absicht ist allerdings in Abhängigkeit von Gröÿe, Lage und Verteilung der Metastasen nur bei einem kleinen Teil der Patienten Erfolg versprechend. Ziel des M-Staging ist es, eine optimale Selektion derjenigen Patienten zu erreichen, die wahrscheinlich von einer chirurgischen Resektion protieren. Die Ultrasonographie (US) stellt aufgrund ihres nicht invasiven Charakters, der geringen Kosten und der breiten Verfügbarkeit ein wertvolles Instrument zum bildgebenden Staging bei Verdacht auf Lebermetastasen kolorektaler Karziniome dar. Die US ist insbesondere hervorragend geeignet, eine erste Unterscheidung zwischen Patienten mit diuser Metastasierung und Patienten mit nur einzelnen oder wenigen Metastasen zu treen. Wesentliche Schwachpunkte der US liegen in der gröÿeren Benutzerabhängigkeit im Vergleich zu CT, MRT und FDG-PET und der zum Teil eingeschränkten Aussagekraft bei der Beurtei- 14 KAPITEL 1. GRUNDLAGEN lung tiefer gelegener Anteile des Leberparenchyms. Patienten mit dem Befund einzelner oder weniger Metastasen in der US sollten deshalb zur denitiven Beurteilung der Resektabiltät einer weiteren Untersuchung mit einem dieser drei genannten Verfahren zugeführt werden. Im Vergleich mit CT und MRT erwies sich die FDG-PET in Meta-Analysen [Kin 02, Bip 05] als das Verfahren mit der höchsten Sensitivität, ihr Einsatz ist jedoch limitiert und bleibt spezialisierten Zentren als ergänzende Untersuchung vorbehalten. Der Vergleich zwischen Spiral-CT und MRT lieferte insgesamt gleichwertige Ergebnisse, allerdings deuten sich Vorteile der kontrastmittelunterstützten MRT mit leberspezischen Gadolinium- und SPIO-Kontrastmitteln gegenüber der KM-unterstützten Spiral-CT an. Die letzliche Entscheidung zwischen der KM-unterstützten CT und der KM-unterstützen MRT ist bei derzeitiger Studienlage in Abhängigkeit von der Geräteverfügbarkeit und der vorhandenen Expertise am jeweiligen Institut individuell zu treen. Insgesamt läÿt sich feststellen, daÿ die KM-unterstützte MRT aufgrund jüngster Verfahrensfortschritte sowohl in Bezug auf das T-Staging als auch für das N- und M-Staging aktuell erwiesenermaÿen eine Führungsrolle unter den bildgebenden diagnostischen Verfahren einnimmt. Eine integrierte Beurteilung von T-, N- und M-Stadium innerhalb eines einzigen, kombinierten MRT-Untersuchungsprotokolls erscheint vor diesem Hintergrund nicht nur diagnostisch sinnvoll, sondern verspricht ausserdem auch aus logistischer Sicht eine Verbesserung des Aufwand-Nutzen-Verhältnisses. Nachsorge Das Hauptaugenmerk der Tumornachsorge kolorektaler Karzinome gilt der Erkennung von solitären Fernmetastasen und Rezidivtumoren, da diese in einem relativ hohen Prozentsatz einer kurativen Therapie zugänglich sind. Einen weiteren Schwerpunkt bildet die Erkennung und Behandlung postoperativer Folgezustände, wie etwa bei der Betreuung von Stomapatienten. Übliche Zeitintervalle für die Nachsorge sind vierteljährliche Untersuchungen in den ersten beiden Jahren gefolgt von halbjährlichen Untersuchungsabständen im 3. bis 5. Jahr. Der Umfang der einzelnen Untersuchungen variiert, sollte jedoch immer Anamnese (Stuhlgewohnheiten, Schmerzen, Blutauagerungen), körperliche Untersuchung (einschlieÿlich digital-rektaler Untersuchung, Stoma und Narben) und eine Laborkontrolle (kleines Blutbild, GPT, AP, Gamma-GT, LDH) beinhalten. Wertvoll ist insbesondere die Bestimmung der Tumormarker CEA und CA 19-9 im Verlauf, da diese bei Rezidiven sehr häug erhöhte Werte aufweisen beziehungsweise einen Wiederanstieg verzeichnen. Weiterhin sollten in regelmäÿigen Abständen durchgeführt werden: Eine Rektosigmoidoskopie zur Beurteilung der Anastomosenregion, 1.1. DAS REKTUMKARZINOM 15 eine Kolonoskopie zur Kontrolle des verbliebenen Dickdarms sowie Untersuchungen der Lunge/des Thorax mittels Röntgen/CT und des Abdomens und Beckens mittels Sonographie/CT/MRT, bei Bedarf ergänzt durch urologische und gynäkologische Untersuchungen. Unter den genannten Verfahren besitzt die MRT aus den in Bezug auf die Staginguntersuchung bereits aufgeführten Gründen auch für die Nachsorge einen hohen und steigenden Stellenwert. 1.1.4 Prognose und Therapie Abbildung 1.4: Vereinfachte schematische Übersicht zur Therapieentscheidung beim Rektumkarzinom (nach [DKG 04]) Die Prognose des Rektumkarzinoms ist trotz immenser Fortschritte in Diagnostik und Therapie während der vergangenen Jahrzehnte auch heute noch relativ schlecht. Als stadienspezische 5-JahresÜberlebensraten werden für Dukes A 90 %, für Dukes B 60 % und für Dukes C 30 % angegeben [Ren 04]. Entsprechend der unterschiedlichen Prognose steht auch die Therapie des Rektumkarzinoms in klarer Abhängigkeit vom Tumorstadium. Ein vereinfachtes Schema zur Therapieentscheidung nach den Empfehlungen der Deutschen Krebsgesellschaft aus dem Jahr 2004 ist in Abb 1.4 zusammengefaÿt. Die sicherlich wesentlichste Entscheidung betrit an oberster Stelle die Unterscheidung zwischen 16 KAPITEL 1. GRUNDLAGEN kurativer und palliativer Therapieintention. Dahinter steht innerhalb der kurativen wie auch innerhalb der palliativen Thrapieansätze (im Schema nicht aufgeführt) die Wahl aus verschiedenen, einzeln oder kombiniert angewandten Verfahren. Die kurative Therapie des Rektumkarzinoms steht immer in Verbindung mit der radikalen operativen Resektion. Daneben nden die Chemotherapie und die Radiotherapie Verwendung innerhalb kurativer Therapieansätze im Sinne adjuvanter (unterstützende Radio- und/oder Chemotherapie postoperativ) oder neoadjuvanter Verfahren (unterstützende Radiound/oder Chemotherapie prä- und postoperativ). Analoge Verfahren stehen, in weniger systematisierter Form und mit insgesamt weiter gefaÿtem Spektrum, für die palliative Therapie zur Verfügung. Operative Therapie Ziel der operativen Therapie in kurativer Intention ist die vollständige Entfernung des Tumors im Gesunden (R0-Resektion) mit partieller oder totaler En-bloc-Entfernung des Mesorektums und des regionären Lymphabussgebietes. Das Ergebnis der chirurgischen Therapie hängt stark vom Operateur und der verwendeten Operationstechnik ab [Her 00]. Je nach Lokalisation und Stadium stehen unterschiedliche Verfahren zur Verfügung. Häugstes Verfahren ist die anteriore Rektumresektion (Abb. 1.5). Abbildung 1.5: Anteriore Rektumresektion [Sie 01] 1.1. DAS REKTUMKARZINOM 17 Das Vorgehen beinhaltet zunächst die vaskuläre Isolation des Tumors durch Absetzung der A. mesenterica inferior unmittelbar distal des Abgangs der A. colica sinistra und Durchtrennung der V. mesenterica inferior am Duodenalknie. Begleitend erfolgt die Lympadenektomie bis an den Abgang der A. mesenterica inferior aus der Aorta. Es folgt bei Karzinomen der unteren zwei Rektumdrittel die komplette Entfernung des Mesorektums zwischen Waldeyerscher Faszie (präsacral) und der ventral gelegenen Denonvillier-Faszie (Total mesorectal excision, TME) [Hea 82]. Bei Karzinomen des oberen Rektumdrittels erfolgt eine partielle Mesorektumexzision. Die einzuhaltenden Sicherheitsabstände betragen oral und aboral mindestens 2 cm in situ. Bei tief inltrierenden Karzinomen oder niedrigem Dierenzierungsgrad sollte deutlich groÿzügiger reseziert werden (3-4 cm in situ). Die Darmkontinuität wird in der Regel mittels End-zu-End-Descendorektostomie wiederhergestellt. Fortgeschrittene Tumoren im Stadium T4 erfordern eine En-bloc-Resektion von tumoradhärenten Organen im Sinne einer multiviszeralen Resektion. Einzelne Fernmetastasen in der Leber stellen nicht notwendigerweise eine Kontraindikation für eine kurative Rektumresektion dar, sondern sind bei geeigneter Lokalisation nach R0-Resektion des Primärtumors ihrerseits mit kurativer Zielsetzung resektabel, sofern keine weiteren extrahepatischen Metastasen nachweisbar sind. Im Sinne der Radikalität kann nur dann kontinenzerhaltend operiert werden, wenn ein Abstand zum Anus von mindestens 2 cm verbleiben kann. Ist ein aboraler Sicherheitsabstand von 2 cm nicht unter Sphinktererhalt möglich, ist eine radikale abdomino-perineale Rektumextirpation nach Miles [Mil 26] mit Anlage eines Anus praeter vorzunehmen. In Grenzfällen kann eine intersphinktäre Resektion (Mitentfernung von Anteilen des Sphincter ani internus mit Anlage eines Colonpouches) den Erhalt der Kontinenz ermöglichen. Die denitive Entscheidung für oder gegen den Kontinenzerhalt kann oft erst intraoperativ getroen werden. Die Sphinkterfunktion muÿ in jedem Falle präoperativ überprüft werden. Die Ausräumung der iliakalen und pelvinen Lymphnoten (Extended pelvic lymphadenectomy, EPL) [Hoj 82] hat sich aufgrund ihrer hohen Morbiditätsrate, die einer nur geringfügig erniedrigten Rate an lokoregionären Lymphknotenrezidiven gegenübersteht, nicht als Routineeingri etablieren können. Ihr Einsatz ist auf Fälle erhöhten Risikos oder erfolgten Nachweises einer lymphatischen Metastasierung entlang der betreenden Lymphbahnen beschränkt. Bei T1- und Low-risk-Karzinomen, die mit einem geringen Risiko für eine lymphogene Metastasierung behaftet sind, ist als Alternative zur TME eine lokale chirurgische Tumorresektion unter kurativer Zielsetzung möglich. Aufgrund ihrer Lokalisation ausgenommen sind Tumoren der anterioren Wand des oberen Rektumdrittels, da hier die Gefahr einer Perforation in die Bauchhöhle besteht. Geeignete Operationsverfahren sind die transanale endoskopische Mikrochirurgie (TEM, [Bue 92]) oder die direkte transanale Exzision. 18 KAPITEL 1. GRUNDLAGEN Adjuvante Therapie Adjuvante Therapie bezeichnet die ergänzende postoperative Tumorbehandlung durch Bestrahlung und/oder Chemotherapeutika. Voraussetzung für eine adjuvante Therapie ist die R0-Resektion des Primärtumors und seines Lymphabussgebietes. Zur Anwendung kommt meist eine systemische Chemotherapie auf der Basis von 5-Fluorouracil [Gro 01,Cha 02], auch in Kombination mit weiteren Substanzen, wie z.B. Levamisol [Lau 89,Moe 95]. Die adjuvante Radiochemotherapie kombiniert die lokale Therapie der Bestrahlung mit der systemisch wirkenden Chemotherapie. Dabei kommt es zusätzlich zum additiven Eekt der beiden Therapien zu einer Verstärkung der lokalen Wirkung der Radiotherapie durch die Chemotherapie. Tab. 1.7 zeigt exemplarisch zwei häug verwendete Therapieschemata. Studien zufolge erhöhen adjuvante Radiochemotherapieverfahren gegenüber der alleinigen operativen Tharapie signikant das rezidivfreie Überleben [Gas 85]. Zudem konnte in mehreren Studien eine signikante Verbesserung der Gesamtüberlebensdauer nachgewiesen werden [Kro 91, OCo 94]; Voraussetzung hierfür ist jedoch eine sorgfältige Indikationsstellung. Maÿgeblich für die Entscheidung für oder gegen die adjuvante Therapie sind die Tumorlokalisation, das postoperative pathologische Tumorstadium und die Qualität der Resektion insbesondere in Bezug auf das Ausmaÿ des zirkumferenziellen Sicherheitsabstandes und den Lymphknotenstatus (vgl. [DKG 04] und Abb. 1.4). Die Nachteile der adjuvanten Therapie bestehen im wesentlichen in der hohen Nebenwirkungsrate: Untersuchungen zur Toxizität und langfristigen Darmfunktion innnerhalb von Langzeitstudien zeigten klare negative Eekte der adjuvanten Therapie bezüglich Kontinenz, Darmaktivität, Stuhlbeschaenheit und perianaler Hautirritation [Kol 94]. NIH-Schema: In der 1. und 5. Bestrahlungswoche 500 mg/m2/Tag 5-FU an 3 Tagen. Radiotherapie mit 50,4 Gy Gesamtdosis bei täglicher Einzeldosis von 1,8 Gy. CAO/ARO/AIO-Studie 94: Radiochemotherapiebeginn 4 Wochen nach Operation, 1000 mg/m2 5-FU als 120-StundenDauerinfusion in der 1. und 5. Bestrahlungswoche; 4 Kurse adjuvante Chemotherapie 5-FU-Bolus in einer Dosierung von 500 mg/m2/Tag über 5 Tage, 3 Wochen Pause. Radiotherapie mit 50,4 Gy Gesamtdosis bei täglicher Einzeldosis von 1,8 Gy. Tabelle 1.7: Mögliche Therapieschemata zur adjuvanten Radiochemotherapie des Rektumkarzinoms (nach [DKG 04]) 1.2. SPEZIELLE MRT-VERFAHREN ZUR UNTERSUCHUNG GROßER KÖRPERREGIONEN 19 Neoadjuvante Therapie Als neoadjuvante Therapie bezeichnet man die präoperative radio- und/oder chemotherapeutische Vorbehandlung von Tumorpatienten mit dem Ziel, die Erfolgschancen einer operativen Resektion in kurativer Absicht zu erhöhen. Sinnvoll und indiziert ist dies bei Patienten mit hohem Lokalrezidivrisiko. Als Kriterien gelten der Durchbruch des Tumors durch die mesorektale Faszie (Stadium T4), das Heranreichen des Tumors bis an den Levatoransatz und Ausbreitung jenseits der Muscularis propria sowie ein Abstand des Tumors von der mesorektalen Faszie von 1 mm oder weniger [DKG 04]. Insbesondere bezüglich des letztgenannten Punktes wurde die Einschätzbarkeit des lokalen Rezidivrisikos durch die Einführung dedizierter hochauösender Dünnschicht-MRT-Verfahren maÿgeblich verbessert, denn diese gestatten eine genaue Beurteilung des verbleibenden Abstands des Tumors vom zirkumferentiellen Resektionsrand (circumferential resection margin, CRM), der der mesorektalen Faszie entspricht [Bro 99]. Bevorzugtes Mittel der neoadjuvanten Therapie ist die kombinierte Radiochemotherapie, die es ermöglicht, eine Verkleinerung des Tumors herbeizuführen (Downstaging) und dadurch im Einzellfall auch eine Resezierbarkeit zuvor irresektabler Tumoren zu erreichen. Vorteile der kombinierten Radiochemotherapie gegenüber einer alleinigen neoadjuvanten Kurzzeitbestrahlung sind die fehlende zeitliche Verzögerung bezüglich des Beginns der systemischen Therapie sowie verbesserte Chancen bezüglich eines möglichen Sphinktererhalts [Min 94]. Der Anteil kompletter Remissisonen nach neoadjuvanter Therapie liegt, abhängig vom initialen Tumorstadium und dem Therapieregime, bei 8-29% [Kim 06b]. 1.2 Spezielle MRT-Verfahren zur Untersuchung groÿer Körperregionen Die Erzeugung eines gleichermaÿen starken und homogenen Magnetfelds ist eine der gröÿten Herausforderungen bei der Entwicklung von Magnetresonanztomographen. Der nutzbare homogene Bereich ist technisch limitiert und umfaÿt ein Volumen von ca. 50 x 50 x 50 cm3 . Die MRT ist deshalb traditionell ein Verfahren zur gezielten Untersuchung lokal begrenzter Strukturen. Für die meisten diagnostischen Anforderungen ist dies ausreichend. Bei Anwendungen wie Angiographien oder der Metastasensuche bei Tumorpatienten ist jedoch die Lokalisation der Pathologie dem Untersucher vor der Untersuchung nicht bekannt, so daÿ das Zielvolumen im Allgemeinen das homogene Magnetfeldvolumen des Scanners deutlich überschreitet. Zur Umgehung dieser Limitierung wurden in den 20 KAPITEL 1. GRUNDLAGEN vergangenen Jahren spezielle Verfahren entwickelt, die eine Datenaufnahme bei kontinuierlich bewegtem Patiententisch ermöglichen (Move-During-Scan (MDS)-Verfahren) und dabei das benötigte homogene Magnetfeldvolumen auf ein Minimum beschränken (Sliding Multi Slice (SMS)-Technik). 1.2.1 Move During Scan (MDS): MRT bei bewegtem Patiententisch Die Entwicklung der MDS-Verfahren begann auf dem Gebiet der MR-Angiographie. Hier brachten die herkömmlichen stationären Aufnahmeverfahren in Kombination mit schrittweisem Tischvorschub [Ear 98,Liu 98,Rue 00] beim Verfolgen des Kontrastmittelbolus (engl. 'bolus chasing') deutliche Nachteile mit sich. Zur Lösung dieses Problems wurden spezielle Aufnahmeverfahren entwickelt, deren gemeinsames Merkmal die Verwendung eines kontinuierlich bewegten Patiententisches ist, dessen Geschwindigkeit auf die Passage des Kontrastmittels abgestimmt wird [Fai 03, Kru 02, Kru 05, Liu 98, Mad 04, Sab 03]. In den vergangenen Jahren wurden diese in der MR-Angiographie entwickelten MDS-Methoden zunehmend auf die Ganzkörperbildgebung übertragen und dabei zusätzlich zum ursprünglich in der Angiographie üblichen dreidimensionalen Ansatz [Bri 00,Kru 02] auf zweidimensionale Verfahren ausgeweitet [Bar 01, Bri 02, Die 99, Gha 03, Sha 03, Wei 03]. Die heute existierenden Verfahren werden nach der Orientierung der aufgenommenen Volumina in coronale Aufnahmeverfahren mit Frequenzkodierung [Bri 02,Kru 02,Kru 05,Mad 04] oder Phasenkodierung [Die 99] entlang der kraniokaudalen Achse (im Folgenden als z-Achse bezeichnet) und die axiale Aufnahmeweise mit Schichtselektionsrichtung entlang der z-Achse [Bar 01, Gha 03, Sha 03, Wei 03] unterschieden. Die axiale Bildgebung liefert im Vergleich eine optimale Homogenität der Bildqualität über das gesamte Gesichtsfeld, da die Daten hier immer im Bereich maximaler Homogenität von Magnetfeld und Spulensensitivität in der Mitte des Magneten akquiriert werden. Die räumliche Auösung in longitudinaler Richtung ist dabei jedoch durch die Scheibendicke limitiert, wodurch coronale Reformatierungen axial aufgenommener Daten eine schlechtere räumliche Auösung besitzen als coronal aufgenommene Daten. Durch den Tischvorschub während der Aufnahme bedingte Bildqualitätsverluste können mittels spezieller Korrekturverfahren minimiert werden. Je nach Verfahren wird dafür die Empfängerfrequenz [Zhu 03] oder die Frequenz der Anregungspulse [Lud 06] dynamisch an die Tischbewegung angepaÿt und so eine exakte Aneinanderreihung von Volumenabschnitten im bewegten Koordinatensystem des Patienten erreicht. Während die kontinuierliche Bewegung des Patiententisches in den ersten publizierten Methoden zur Ganzkörper-MDS-Bildgebung noch mittels eines von Hand bewegten Tischaufsatzes bewerkstelligt wurde [Bar 01,Gha 03,Kru 02], ist die MDS-Funktion heute in einigen käuich erhältli- 1.2. SPEZIELLE MRT-VERFAHREN ZUR UNTERSUCHUNG GROßER KÖRPERREGIONEN 21 chen MRT-Geräten, wie dem Magnetom Avanto der Firma Siemens, bereits mit integriert. Damit ist in vergleichbarer Weise zum Spiral-CT eine koordinierte Steuerung von Datenaufnahme und Tischbewegung vollständig automatisiert über die Bedienkonsole des Gerätes möglich. 1.2.2 Sliding Multi Slice (SMS) SMS ist eine Methode zur verschachtelten Aufnahme eines Mehrschichtpaketes während kontinuierlicher Tischbewegung unter Verwendung langer Wiederholzeiten (= Repetition Times, T R) [Fau 06]. Wie bereits in Abschnitt 1.2.1 erwähnt, besteht der Hauptvorteil der axialen MDS-Verfahren gegenüber der coronalen Aufnahmeweise darin, daÿ sie die Datenaufnahme entlang der kraniokaudalen Achse auf einen engeren Bereich um das Isozentrum des Magneten begrenzen. Bei der Aufnahme von Mehrschichtpaketen reduziert sich dieser Vorteil jedoch mit zunehmender Dicke des Schichtpakets, da das benötigte Volumen im Scanner bei üblicher Mehrschicht-Aufnahmetechnik dem doppelten Volumen des Schichtpakets entspricht (Abb. 1.6 a). Dies reduziert für verschachtelte Mehrschichtaufnahmen, wie sie bei der Verwendung langer T R zur Zeitersparnis üblich sind, die Bildqualität erheblich. Mit dem SMS-Verfahren gelingt es, das zur Datenakqusition benötigte Volumen im Scanner auf das Volumen eines einzigen Schichtpakets, also um 50% zu reduzieren Abb. 1.6 b). Dabei wird, ebenso wie bei der konventionellen Aufnahme von Mehrschichtpaketen, ein aus N parallelen Schichten mit Schichtabständen d bestehendes Paket aufgenommen, indem insgesamt n · N Aufnahmeschritte mit einer Einzeldauer von ∆T nacheinander durchgeführt werden. Der Parameter n bezeichnet dabei die Gesamtzahl der Aufnahmeschritte, die zur Rekonstruktion eines einzelnen Bildes notwendig ist. Es ergibt sich damit T R = N · ∆T . Die Geschwindigkeit der kontinuierlichen Tischbewegung vT isch = d N ·d = n · 4T n · TR (1.1) wird solchermaÿen angepaÿt, daÿ der fahrende Patiententisch während des Zeitraums n·T R exakt die Strecke zurücklegt, die der Ausdehnung eines Schichtpakets entspricht. Zur Datenaufnahme unterteilt SMS den k-Raum in N Segmente, wobei jedem Segment jeweils eine von N Schichtpositionen im Koordinatensystem des Scanners zugeordnet wird (Abb. 1.6 b). Zu jedem k-Raum-Segment gehören n/N Aufnahmeschritte. Wenn eine bestimmte Schicht des Patienten die einem k-Raum-Segment zugehörige Schichtposition passiert, werden die zugehörigen Daten des entsprechenden k-Raum-Segments aufgenommen. Während jedes T R-Intervalls werden so N parallele Schichten des Patienten nachein- 22 KAPITEL 1. GRUNDLAGEN ander angeregt und dabei Daten aus jeweils unterschiedlichen k-Raum-Segmenten sequentiell ausgelesen. Wenn eine Schicht des Patienten letzendlich nach dem Passieren sämtlicher N Positionen das Aufnahmefenster verläÿt, sind alle ihr zugehörigen Daten akquiriert. Wie von Fautz und Kannengieÿer gezeigt, besitzt Sliding Multi Slice einige sehr positive Eigenschaften, die eine Verwendung des Verfahrens in der abdominellen Bildgebung nahe legen: Im Gegensatz zu Multislice Aufnahmeverfahren nimmt SMS die einander entsprechenden k-Raum Daten für jede Schicht entlang derselben räumlichen Trajektorie in Bezug auf das Scannerkoordinatensystem auf. Dies bedeutet insbesondere, daÿ das k-Raum-Zentrum für alle Schichten im Isozentrum des Magneten aufgenommen werden kann. Bildartefakte, denen Eekte zugrunde liegen, die von der z-Koordiante abhängig sind, wie beispielsweise Verzerrungen aufgrund nicht linearer Gradientenfelder, werden dadurch reduziert. Weiterhin geschieht die räumliche Trennung benachbarter Schichten beim SMS-Verfahren anhand ihrer Aufnahmezeit und nicht anhand ihrer Position im Scanner. SMS beendet damit die Aufnahme benachbarter Schichten kontinuierlich in Zeitabständen von n · ∆T und nicht, wie bei konventionellen Verfahren der Fall, in Paketen zu N Schichten. SMS vermeidet so bewegungsbedingte Sprünge zwischen benachbarten Schichten und ermöglicht zudem eine kontinuierliche Darstellung der aufgenommenen Daten in Echtzeit auf der Bedienkonsole des Scanners. 1.2. SPEZIELLE MRT-VERFAHREN ZUR UNTERSUCHUNG GROßER KÖRPERREGIONEN 23 Abbildung 1.6: Schematische Darstellung der räumlichen Aufnahmetrajektorien bei bewegtem Patiententisch für konventionelle Mehrschichtaufnahmen (a) und SMS-Aufnahmen (b). In Richtung der positiven z-Achse sind die räumlichen Aufnahmetrajektorien der verschiedenen Schichten im Koordinatensystem des Scanners, entlang der negativen z-Achse im Koordinatensystem des Patienten dargestellt. Die Reihenfolge der Aufnahmeschritte während eines T R verläuft von links nach rechts, während die Abfolge der Repetitionen (Rep) von oben nach unten dargestellt ist. Die schwarzen Punkte entsprechen ausgewählten Phasenkodierschritten. Entlang einer jeden Schicht sind die verschiedenen Phasenkodierschritte in unterschiedlichen Grauwerten dargestellt. Die schwarzen Pfeile geben die Zuordnung der einzelnen Phasenkodierschritte zu der jeweiligen Scannerposition an, an der ihre Aufnahme erfolgt. Man beachte, daÿ beim SMS-Verfahren die Aufnahme des k-Raum-Zentrums aller Schichten im Isozentrum des Magneten erfolgt (nach [Fau 06]). 24 KAPITEL 1. GRUNDLAGEN Kapitel 2 Methoden 2.1 Abdomenbildgebung mit SMS Ziel des hier vorgestellten Verfahrens war die Aufnahme hochaufgelöster T1 -gewichteter MRT-Daten des gesamten Abdomens und Beckens bei kontinuierlichem Tischvorschub innerhalb einer einzigen Atemanhaltephase. Die verwendete Sliding-Multi-Slice-MRT-Sequenz wurde speziell für diesen Zweck konzipiert. Als Kontrast wurde eine übliche T1 -Gewichtung mit Fettsättigung gewählt, die durch eine Gradientenechosequenz generiert wurde. Zu Beginn der Untersuchung wurden die Patienten gebeten, ihren Atem in Inspirationstellung für 20 Sekunden anzuhalten, während die Daten des Oberbauchs unter kontinuierlichem Tischvorschub akquiriert wurden. Anschlieÿend durften die Patienten wieder normal weiteratmen, während Datenakquisition und Tischbewegung ohne Unterbrechung bis ins Becken fortgesetzt wurden (Abb. 1). Die kraniokaudale Ausdehnung der (pathologisch vergröÿerten) Leber beträgt etwa 10 bis 20 cm. Um diese Distanz während einer Atemanhaltephase von 20 Sekunden abzudecken, sollte die Tischgeschwindigkeit mindestens vT isch = 1cm/s betragen. Entsprechend Gl. (1.1) hängt die Tischgeschwindigkeit vT isch von n, N , d und T R ab. Da T R (= 102 ms) und d (= 6.25 mm) durch den gewünschten Kontrast und die gewünsche Auösung vorgegeben sind, wird vT isch durch die Wahl der Parameter n und N bestimmt. In der verwendeten Sequenz wurde die Anzahl der Phasenkodierschritte unter Verwendung von parallelen Aufnahmemethoden (GRAPPA [Gri 02]) in anterior-posteriorer Richtung mit 24 Referenzzeilen und einem Nettobeschleunigungsfaktor von 1.75) in Kombination mit 7/8 partial Fourier Rekonstruktionsmethoden auf n = 104 reduziert. Damit ergibt sich für die oben angegebenen Parameter eine Schichtanzahl von N = 17. Die Studie wurde auf einem 1.5 T Ganzkörpersystem (Magnetom Avanto, Siemens Medical Solutions, Erlangen, 25 26 KAPITEL 2. METHODEN Deutschland) durchgeführt, das mit einem 18-Kanal-System von externen Phased-Array-Spulen ausgestattet war (Total imaging matrix (Tim), Siemens Medical Solutions, Erlangen, Deutschland). Die einzelnen Spulenelemente wurden zu insgesamt 14 verschiedenen Spulenkongurationen kombiniert, zwischen denen während der Untersuchung in Abhängigkeit von der aktuellen Schichtposition automatisch umgeschaltet wurde. So wurde stets die geeignetste Konguration gewählt, um eine optimale Spulensensitivität zu gewährleisten. Alle erforderlichen Bewegungen des Patiententisches waren automatisiert. Ein Umlagern des Patienten oder ein Auswechseln von Spulen während der Untersuchung war nicht erforderlich. Abbildung 2.1: Darstellung des untersuchten Körperabschnitts mittels reformatierter Übersichtsbilder in coronaler (links) und sagittaler Ebene (rechts). Die unterbrochene Linie veranschaulicht die Grenze zwischen der während des Atemanhaltens aufgenommenen Oberbauchregion (A) und den kaudal gelegenen Arealen von unterem Abdomen und Becken (B), die während freier Atmung aufgenommen wurden. Während sich Region A vollständig artefaktfrei darstellt, unterteilt sich Region B in einen kranial und ventral gelegenen, vorwiegend intestinal dominierten Bereich, der von Bewegungsartefakten beeinträchtigt ist sowie einen dorsal und kaudal gelegenen Bereich, der Retroperitonealraum und Becken beinhaltet und deutlich weniger Beeinträchtigung durch Bewegungsartefakte erfährt. 2.2. 2.2 UNTERSUCHUNGSPROTOKOLL 27 Untersuchungsprotokoll Abb. 2 gibt einen Überblick über das Untersuchungsprotokoll und die verwendeten Scanparameter. Das bisher zur Detektion lokaler Tumorrezidive im Rahmen der Nachsorge von Patienten mit kolorektalem Karzinom am Universitätsklinikum Freiburg verwendete Standard-Untersuchungsprotokoll entspricht den weiÿen Kästen in Abb. 2.2. Es beginnt mit einer sagittalen T2 -gewichteten TurboSpin-Echo-Sequenz (TSE, Seq. 1), gefolgt von einer senkrecht zum tumortragenden Darmabschnitt ausgerichteten, para-axialen, T2 -gewichteten TSE-Sequenz (Seq. 2). Beide Sequenzen werden nach Reinigung des Enddarms, rektaler Wasserfüllung (200 ml) und intravenöser Injektion von Butylsco- R , Boehringer Ingelheim GmbH, Deutschland) durchgeführt. Der abschlieÿende polamin (Buscopan Teil des Beckenuntersuchungsprotokolls besteht aus einer axialen, kontrastmittelverstärkten, fettgesättigten, T1 -gewichteten VIBE-Sequenz (Volume-Interpolated-Breath-hold-Examination, Seq. 4) nach R , Bracco Altana Pharma GmbH, Konstanz, intravenöser Gabe von 20 ml Gd-BOPTA (MultiHance Deutschland). Im modizierten SMS-Untersuchungsprotokoll (linke Spalte in Abb. 2) wurden die oben genannten Standardsequenzen durch die T1 -gewichtete Aufnahme des gesamten Abdomens und Beckens bei kontinuierlich bewegtem Patiententich unter Verwendung von SMS ergänzt. Die zusätzliche Sequenz (Seq. 3a) wurde, abgestimmt auf die portalvenöse Phase der Kontrastmitteldynamik, eine Minute nach Kontrastmittelgabe vor Durchführung der stationären T1 -gewichteten VIBE-Bildgebung des Beckens gestartet. Abbildung 2.2: Untersuchungsprotokoll und Scanparameter. Weiÿe Boxen (Sequenzen 1, 2 und 4): Standardprotokoll zur hochaufgelösten Becken-MRT. Graue Boxen: Verglichene Sequenzen zur T1 gewichteten Abdomen-MRT: 3a) SMS, 3b) konventionelle MRT in Atemanhaltetechnik. 28 KAPITEL 2. 2.3 METHODEN Patienten Die SMS-MRT-Methode wurde an einem Kollektiv von 22 Patienten mit bekannten malignen Tumoren des Beckens untersucht, die der Abteilung Röntgendiagnostik des Universitätsklinikum Freiburg im Rahmen der Routinenachsorge zur MRT des Beckens zugewiesen worden waren. Untersucht wurden 13 Männer und 9 Frauen mit einem Medianalter von 65 Jahren und einer Altersspanne von 25 bis 81 Jahren. Die vertretenen Tumorentitäten waren Rektumkarzinom (16 Fälle), Analkarzinom (2 Fälle), Sigmakarzinom (2 Fälle), Endometriales Stromasarkom (1 Fall) und Ovarialkarzinom (1 Fall). Die aus diesen Untersuchungen erhaltenen Ergebnisse wurden mit einem Referenzstandard verglichen, der durch eine konventionell durchgeführte Abdomen-MRT-Untersuchung in Atemanhaltetechnik gegeben war. Hierfür wurde retrospektiv eine vergleichbar strukturierte Kontrollgruppe deniert, die aus 22 konsekutiv untersuchten Patienten bestand. Die Patienten der Kontrollgruppe hatten keine Untersuchungen aus dem Standardprogramm zur Becken-MRT erhalten, sondern wurden lediglich mit kontrastmittelverstärkten, fettgesättigten, T1 -gewichteten 2D-Gradientenechosequenzen für Ober- und Mittelbauch untersucht (Seq. 3b in Fig 2). Die Kontrollgruppe umfasste ebenfalls 13 Männer und 9 Frauen mit bekannten malignen Tumorerkrankungen des Beckens. Das Medianalter betrug 64 Jahre bei einer Alterspanne von 26 bis 75 Jahren. Die in der Kontrollgruppe vertretenen Tumorentitäten waren Rektumkarzinom (18 Fälle), Sigmakarzinom (2 Fälle) und Analkarzinom (2 Fälle). 2.4 Datenauswertung Die aus den SMS-MRT-Untersuchungen einerseits und den konventionellen MRT-Untersuchungen andererseits erhaltenen Bilddaten wurden bezüglich zweierlei Kriterien ausgewertet. Diese waren: 1. Die Bildqualität in Form einer subjektiven Beurteilung der diagnostischen Aussagekraft der Daten sowie der Präsenz von Bewegungsartefakten. 2. Die objektive Detektierbarkeit der Läsionen in Leber und Knochenmark gegeben durch das Kontrast-zu-Rauschen-Verhältnis (Contrast to Noise Ratio - CNR) der Läsionen verglichen mit dem umliegenden Gewebe. Für die Bewertung der Bildqualität wurde das untersuchte Körpervolumen in drei Regionen unterteilt, die separat ausgewertet wurden: 2.4. DATENAUSWERTUNG 29 1. Oberbauch (Region, die während der Atemanhaltephase aufgenommen wurde) 2. Intestinum 3. Retroperitoneum und Wirbelsäule Die diagnostische Aussagekraft der Bilddaten wurde durch zwei Radiologen unabhängig voneinander auf einer fünfstugen Skala mit den Stufen 5 - exzellent 4 - gut 3 - durchschnittlich 2 - mangelhaft 1 - ungenügend bewertet, denen entsprechende Punktescores entsprachen. Analog wurde das Auftreten von atembedingten Artefakten auf einer dreistugen Skala mit den Stufen 3 - keine sichtbaren Artefakte 2 - geringe Artefakte ohne Beeinträchtigung der diagnostischen Aussagekraft 1 - starke, die diagnostische Aussagekraft vermindernde Artefakte beurteilt. Aus den vergebenen Punktescores für diagnostische Aussagekraft und Artefaktbeeinträchtigung wurden Mittelwerte und deren Standardabweichungen berechnet, um eine methoden- und regionsweise Auswertung der Daten zu ermöglichen. Schluÿendlich wurde für die detektierten Läsionen in Leber und spinalem Knochenmark das CN R = 3 Signal(Laesion)i − Signal(U mgebung)i 1X 3 i=1 Rauschen (2.1) als Mittelwert aus drei aufeinanderfolgenden Messungen je Läsion bestimmt. Zur Beurteilung der Bilddaten wurde eine kommerziell erhältliche PC Netzwerkstation mit JVision DiagnostTM Software (heute IMPAX DiagnostTM, GWI AG, Bonn, Deutschland) verwendet. 30 KAPITEL 2. METHODEN Kapitel 3 Ergebnisse 3.1 Bildqualität Das SMS-Untersuchungsverfahren mit fahrendem Patiententisch wurde von allen 22 Patienten beschwerdelos toleriert. Abb. 3.1 zeigt die Ergebnisse der subjektiven Beurteilung zweier unabhängiger Radiologen in Bezug auf die diagnostische Aussagekraft der Daten und den Grad der Beeinträchtigung durch atmungsbedingte Artefakte. Die diagnostische Aussagekraft der im Oberbauch akquirierten Bilddaten der Patienten der SMS-Untersuchungsgruppe wurde von beiden Auswertern in 19 von 22 Fällen (86 %) mit exzellent beurteilt und in weiteren zwei Fällen (9 %) mit gut. Dies entspricht einer Durschnittsbewertung für die diagnostische Aussagekraft (DA) im Oberbauch von 4.8 ± 0.6. In einem Fall (5 %) zeigten sich aufgrund eines Fehlers bei der Schichtpositionierung, der dazu führte, daÿ die Aufnahme 15 cm kranial der eigentlich dafür vorgesehenen Position startete, stärkere Artefakte im Oberbauch. Der Durchschnittsscore für die Beeinträchtigung durch Artefakte (AB) berechnete sich so zu 2.7 ± 0.5. Für die Kontrollgruppe wurde die diagnostische Aussagekraft der im Oberbauch aufgenommenen Bilddaten in etwa einem Drittel der Fälle als exzellent (Radiologe 1: 13/22, 59 %; Radiologe 2: 15/22, 68 %), in (5/22, 23 %; 4/22, 18 %) Fällen als gut und in (4/22, 18 %; 3/22, 14 %) Fällen als durchschnittlich beurteilt (DA = 4.5 ± 0.8). Insgesamt (2/22, 9 %; 3/22, 14 %) der Datensätze der Kontrollgruppe waren durch stärkere Atemartefakte beeinträchtigt, (5/22, 23 %; 4/22, 18 %) zeigten leichte Artefakte. In (15/22, 68 %; 15/22, 68 %) der Fälle traten keine sichtbaren Artefakte auf (AB = 2.6 ± 0.7). In der Intestinalregion wurden (11/22, 50 %; 1/22, 5 %) als gering durch Atmungsartefakte beeinträchtigt beurteilt. (11/22, 50 %; 21/22, 95 %) zeigten hier starke Artefakte. Die Beurteilung der diagnostischen Aussagekraft ergab dementsprechend vorwiegend die 31 32 KAPITEL 3. ERGEBNISSE Abbildung 3.1: Ergebnisse der subjektiven Beurteilung der Bilddaten durch zwei unabhängige Radiologen 3.2. DETEKTIERBARKEIT DER LÄSIONEN UND CNR 33 Bewertungen 'durchschnittlich' und 'mangelhaft' (DA = 2.6 ± 0.7). Die in den SMS-Daten im Intestinum festgestellten Artefakte traten am stärksten im Bereich unterhalb der Leber auf, der während des ersten Atemzugs der Patienten nach der Atemanhaltephase aufgenommen wurde. In Richtung auf Unterbauch und Becken schwächten sich die Artefakte deutlich ab (Abb. 2.1 und Abb. 3.2). Das stationäre Untersuchungsprotokoll zeigte in (7/22, 32 %; 5/22, 23 %) der Fälle der Kontrollgruppe keine Beeinträchtigung durch Bewegungsartefakte im intestinalen Bereich. In (8/22, 36 %; 9/22, 41 %) Fällen wurden geringe, in (7/22, 32 %; 8/22, 36 %) Fällen schwere Artefakte festgestellt (AB = 1.9 ± 0.8). Die diagnostische Aussagekraft der Daten im Intestinum ergab sich für die Kontrollgruppe entsprechend zu DA = 3.5 ± 0.9 mit einem Schwerpunkt zwischen 'gut' und 'durchschnittlich'. In Bezug auf den Retroperitonealeraum wurden (16/22, 73 %; 7/22, 32 %) der SMS-Datensätze als artefaktfrei beurteilt. (6/22, 27 %; 13/22, 59 %) Datensätze zeigten geringe Artefakte und (0/22, 0 %; 2/22, 9 %) Fälle waren mit starken Artefakten belastet (AB = 2.5 ± 0.5). Die Beurteilungen der diagnostischen Aussagekraft verteilten sich um einen Schwerpunkt zwischen 'exzellent' und 'gut' (DA = 4.6 ± 0.7). In der Kontrollgruppe zeigten sich (17/22, 77 %; 17/22, 77 %) Datensätze ohne Artefakte und (5/22, 23 %; 5/22, 23 %) mit geringen Artefakten. Hier war keiner der Datensätze (0/22, 0 %; 0/22, 0 %) mit starken Artefakten belastet (AB = 2.8 ± 0.4). Die diagnostische Aussagekraft wurde überwiegend als exzellent bewertet (DA = 4.8 ± 0.4). 3.2 Detektierbarkeit der Läsionen und CNR Metastatische Läsionen wurden bei jeweils 14 Patienten (64 %) der SMS-Gruppe und 14 Patienten (64 %) der Kontrollgruppe festgestellt. Lebermetastasen mit Durchmessern zwischen 4 mm und 11 cm wurden bei acht Patienten (36 %) der SMS-Gruppe detektiert (Abb. 3.3 a) mit einem mittleren CNR von 7.0 (Maximum 11.1/Minimum 4.7). In der Kontrollgruppe (Abb. 3.3 b) zeigten sich Lebermetastasen in 13 Fällen (59 %). Hier betrug das mittlere CNR 6.9 (15.9/2.5). Metastasensuspekte Knochenläsionen in der Wirbelsäule (Abb. 3.4 a) mit Gröÿen zwischen 6 mm und 3.3 cm elen bei fünf Patienten (23 %) der SMS-Gruppe auf bei einem mitteleren CNR von 6.4 (7.0/4.8). Die konventionelle MR-Untersuchung ergab bei vier Patienten (18 %) der Kontrollgruppe metastasensuspekte Wirbelläsionen mit einem mittleren CNR von 3.2 (5.1/2.0). Lymphknotenmetastasen von 0.9 bis 1.5 cm Gröÿe wurden bei fünf Patienten (23 %) der SMS-Gruppe diagnostiziert (Abb. 3.4 b und c). 34 KAPITEL 3. ERGEBNISSE Abbildung 3.2: Transversale Schnittbilder, die aus SMS-MRT-Daten an fünf äquidistanten Positionen entlag der kraniokaudalen Achse des Patienten rekonstruiert wurden. Die Bilder a) und b) wurden während der Atemanhaltephase aufgenommen und zeigen eine scharfe Abgrenzbarkeit aller Organund Gewebestrukturen ohne bewegungsbedingte Artefakte. Die Bilder c) bis e) wurden während freier Atmung aufgenommen und zeigen Bewegungsartefakte in den bauchdeckennahen Anteilen des Mittelbauchs, wohingegen Wirbelsäule, Retroperitoneum und Becken artefaktfrei dargestellt sind. 3.2. DETEKTIERBARKEIT DER LÄSIONEN UND CNR 35 In der Kontrollgruppe wurden bei 6 Patienten (27 %) verdächtige Lymphknoten gefunden. Eine CNRBestimmung der Lymphknoten wurde nicht durchgeführt, da sich das die Lymphknoten umgebende Gewebe als zu inhomogen erwies, um verläÿliche Signalwerte erheben zu können. Obgleich die Detektion von Lungenläsionen nicht Ziel der Untersuchung war, wurden bei zwei Patienten (9 %) der SMS-Gruppe Lungenmetastasen der basalen Lungenabschnitten mit erfaÿt (Abb. 3.4 d). Die Gröÿen dieser Herde betrugen 4 mm und 8 mm. Das mittlere CNR der Läsionen ergab sich zu 7.4 (8.4/6.4). In der Kontrollgruppe wurden keine Lungenläsionen diagnostiziert. Abbildung 3.3: Darstellung beispielhafter axialer Oberbauchschichten aus beiden Patientengruppen bei Patienten mit Lebermetastasen (Pfeile): a) Aus SMS-Daten rekonstruiertes Bild, b) aus konventionellen Daten rekonstruiertes Bild. 36 KAPITEL 3. ERGEBNISSE Abbildung 3.4: Aus SMS-Daten rekonstruierte Schichten axialer Orientierung mit beispielhaften pathologischen Befunden (Pfeile): a) Knochenmetastase der Lendenwirbelsäule, b) Lymphknotenmetastase im Fettgewebe des ventralen Abdomens, c) Lympknotenmetastase am Lig. hepatoduodenale, d) Lungenmetastase im rechten Unterlappen. Kapitel 4 Diskussion Bei zahlreichen Tumorerkrankungen stellt die MRT verglichen mit anderen bildgebenden Verfahren eine konkurrenzfähige Methode zur Detektion einer metastatischen Beteiligung von Leber und Knochen sowie des lymphatischen Systems dar [Bip 05,Kin 02,Sch 06]. Nichtsdestoweniger ist die Spiral-CT die derzeitige Methode der Wahl zur Darstellung der Tumorausbreitung in Thorax, Abdomen und Becken, da sie die Möglichkeit der schnellen multiregionalen Untersuchung mit einer hohen Sensitivität und Spezität in der Detektion von Metastasen vereint [Lau 06, Val 01]. Stationäre MRT-Protokolle, wie sie derzeit üblicherweise für Untersuchungen des Abdomens und Beckens verwendet werden, erfordern meist mehrere Atemanhaltephasen sowie mindestens eine Veränderung der Tischposition. Die dafür benötigte Gesamtaufnahmezeit beträgt etwa zwei Minuten [Sch 06]. Die in der vorliegenden Studie zur Untersuchung der Kontrollgruppe angewandte Sequenz ist eine typische Vertreterin dieser Art von Untersuchungsverfahren, wie sie bisher am Universitätsklinikum Freiburg routinemäÿig verwendet wurde. In der vorliegenden Arbeit wurde eine Methode zur axialen Datenakquisition bei kontinuierlich bewegtem Patiententisch erstmals in die gezielte bildgebende Diagnostik von Abdomen und Becken eingeführt. Ziel dabei war es, die wohlbekannte diagnostische Qualität der MRT mit der Zeitezienz einer Spiral-CT-Untersuchung zu verbinden. Die Sliding-Multi-Slice-MRT ist in der in dieser Studie vorgestellten Form in der Lage, das gesamte Abdomen und Becken innerhalb einer einminütigen MRT-Untersuchung abzubilden und bedarf dazu lediglich einer einzigen Atemanhaltephase von 20 Sekunden Dauer. Dies sind Zeitspannen, die mit denen einer Standard-CT-Untersuchung des Abdomens vergleichbar sind. Die vorliegende Studie konnte mittels indirekten Vergleichs zeigen, daÿ die Sliding-Multi-Slice-MRT eine konkurenzfähige Alternative zur konventionellen stationären MRT bei Staging und Nachsorge von Patienten mit malignen Tumorerkrankungen des Beckens darstellt. In Be37 38 KAPITEL 4. DISKUSSION zug auf die Bildqualität ermöglicht SMS die Darstellung des Oberbauchs, des Retroperitonealraums, des Beckens sowie der lumbalen Wirbelsäulenabschnitte unter äuÿerst geringer Beeinträchtigung durch Bewegungsartefakte. Ebenso liefert sie hohen Bildkontrast zur Detektion von Metastasen in Leber, Lunge und Knochen mit stabilem und reproduzierbarem CNR. Verglichen mit der konventionellen stationären MRT zeigte SMS insbesondere in der Region des Oberbauchs bessere Resultate und empehlt sich damit als möglicherweise überlegenes Verfahren zur Beurteilung des metastatischen Befalls von Leber und Oberbauch. In Hinblick auf die Beurteilbarkeit des Retroperitonealraums, der die Hauptlokalisation betroener Lymphknoten bei kolorektalen Karzinomen darstellt, zeigten sich geringe Vorteile zu Gunsten des konventionellen Protokolls. Der wesentliche Nachteil des SMS-Verfahrens lag in der reduzierten Bildqualität in denjenigen Bereichen des Intestinaltrakts, deren zugehörige Daten während der ersten ausgedehnten Atemzüge der Patienten nach der 20 sekündigen Atemanhaltephase aufgenommen wurden. Diese zeigten sich deutlich häuger als konventionelle Aufnahmen derselben Region durch stärkere Bewegungsartefakte belastet. Bei der Beurteilung der Ergebnisse dieser Studie müssen zweierlei konzeptionelle Einschränkungen berücksichtigt werden: Zum ersten war die Anzahl der in dieser Studie eingeschlossenen Patienten oensichtlich zu gering, um den gewonnenen Ergebnissen statistische Signikanz zu verleihen. Zum zweiten war es aufgrund operativer Gründe nicht möglich, ein und dasselbe Patientenkollektiv mit beiden MRT-Verfahren zu untersuchen, so daÿ die Daten der mit der SMS-Methode untersuchten Patienten retrospektiv mit einem vergleichbar strukturierten zweiten Patientenkollektiv verglichen wurden. Beide genannten Gründe erfordern eine weitergehende Evaluierung von SMS im Rahmen prospektiver Studien. Vergleicht man die beiden untersuchten Sequenzen 3a und 3b (Abb. 2.2) mit Blick auf deren technische Eigenschaften, so ist zu erwähnen, daÿ die räumliche Auösung der SMS-Sequenz geringfügig niedriger ist, als die der konventionellen Sequenz zur Aufnahme bei stationärer Patientenliege. Unter Einbeziehung der methodischen Untersuchungen aus [Fau 06] dürfte dies jedoch keinen ernst zu nehmenden Vorteil für die SMS-Methode in Hinblick auf die Bildqualität beteutet haben. SMS kann prinzipiell mit einer Vielzahl unterschiedlichster Pulssequenzen und Kontrastmechanismen verwendet werden [Fau 06]. Methode der Wahl zur Durchführung der vorliegenden Studie war die kontrastmittelverstärkte T1 -gewichtete Bildgebung mit Fettsättigung, da diese einen nachgewiesenenen Stellenwert in der abdominellen Bildgebung beim CRC hat [Bip 05]. CT-Studien haben ergeben, daÿ zur Detektion hypovaskularisierter Metastasen, wie sie für das CRC charakteristisch sind, die Datenakquisition während der portalvenösen Kontrastmittelphase entscheidend ist [Soy 04]. Aus diesem Grund wurde auf eine Akqusition zusätzlicher Daten in der arteriellen und hepatobiliären Phase 39 verzichtet. Dennoch ist davon auszugehen, daÿ die Sliding-Multi-Slice-MRT ebenso auch für die dynamische Drei-Phasen-Kontrastmitteldarstellung des Oberbauchs geeignet ist: Sie gestattet zum einen die Abdeckung der gesamten Leber innerhalb einer Atemanhaltephase von 20 Sekunden, zum anderen ist eine Repositionierung der Patientenliege zwischen den einzelnen Aufnahmen automatisiert binnen Sekunden möglich. Im Allgemeinen ist die räumliche Ausdehnung der Region, die innerhalb einer Atemanhaltephase aufgenommen werden kann, durch die Dauer der Atemanhaltephase und die Tischgeschwindigkeit begrenzt. Beim abdominellen Staging rektaler Tumoren mögen die im Bereich des ventralen Intestinaltrakts aufgetretenen Atmungsartefakte akzeptabel erscheinen, da die Anzahl und die Häugkeit der dort zu erwartenden Pathologien sehr begrenzt ist. Eine generalisierte Anwendbarkeit der Sliding-Multi-Slice-MRT impliziert jedoch, daÿ die Gröÿe des während des Atemanhaltens aufgenommenen Körpervolumens auf jedes beliebige zu untersuchende Gebiet ausgedehnt und angepaÿt werden kann. Die technische Weiterentwicklung der SMS-Verfahren wird sich deshalb mit der Anwendung höherer Tischgeschwindigkeiten zu befassen haben. Dies könnte beispielsweise durch schnellere Pulssequenzen, höhergradige Partial-Fourier Akquisition oder höhere Beschleungungsfaktoren bei der parallelen Datenaufnahme realisierbar sein. Eine weitere Lösungsmöglichkeit könnte die Verwendung dedizierter Aufnahmeschemata mit mehreren Atemanhaltephasen darstellen, deren Ablauf vom Untersucher mit Hilfe einer Echtzeit-Anzeige der aufgenommenen Daten interaktiv über die Gerätekonsole gesteuert werden kann. Schluÿendlich könnte die Entwicklung von Aufnahmeverfahren, die eine Akquisition sämtlicher Daten bei freier Atmung gestatten, eine denitive Lösung des Problems der Atmungsbeeinträchtigung beinhalten. Natürlich werden die SMS-Technik und die konventionelle stationäre MRT in Bezug auf die Anzahl der benötigten Atemanhaltephasen gleichermaÿen von den Errungenschaften dieser genannten Entwicklungen protieren. Deshalb werden beide Verfahren letztlich nach entsprechender Optimierung vergleichbare Ergebnisse in Bezug auf die Anzahl und Dauer der benötigten Atemanhaltephasen bieten können. Die Stärken der SMS-Technik sind in diesem Zusammenhang eher in der Flexibilität und Ezienz bei der Kombination von Atemanhaltenphasen und Phasen freien Atmens innerhalb einer MRT-Untersuchung zu sehen. In der vorgestellten Studie wurde erstmals die Methode der Sliding-Multi-Slice-MRT im klinischen Kontext untersucht. Die erhaltenen Ergebnisse geben trotz der geringen Fallzahl Grund zu der Annahme, daÿ die Aufnahme von MRT-Daten bei kontinuierlich bewegtem Patiententisch mittels SMS groÿes Potential besitzt, sich zu einer Standardmethode der abdominellen Diagnostik bei Erstdiagnose, Staging und Nachsorge von Patienten mit malignen Tumorerkrankungen des Beckens zu entwickeln. Aus technischem Blickwinkel ist die Methode zeitezient, einfach in etablierte Becken-MRT-Protokolle in- 40 KAPITEL 4. DISKUSSION tegrierbar und im Vergleich zu dedizierten konventionellen Abdomen-MRT-Untersuchungen sehr komfortabel durchführbar. Vom klinischen Standpunkt aus gesehen zeigt die Methode vielversprechende Eigenschaften in Bezug auf die Detektion von Lebermetastasen, retroperitonealem Lymphknotenbefall und spinaler Knochenmarksinltration. Zusammenfassung Zielsetzung Ziel der vorliegenden Arbeit war es, die von Fautz und Kannengiesser entwickelte, so genannte SMS-Technik (Sliding Multi Slice-Verfahren zur Aufnahme axialer 2D Bilddaten bei kontinuierlichem Tischvorschub) in ein MRT-Untersuchungsprotokoll des Beckens zu integrieren, um bei Patienten mit malignen Tumorerkrankungen des Beckens eine zusätzliche Beurteilung des gesamten Abdomens innerhalb eines Untersuchungsvorganges zu ermöglichen. Methoden Axiale 2D-Daten wurden bei kontinuierlichem Tischvorschub mit einer T1 -gewichteten Gradientenechosequenz mit Fettsättigung aufgenommen. Die Patienten hielten ihren Atem während der ersten 20 s der Untersuchung an und atmeten anschlieÿend normal weiter, wobei Datenaufnahme und Tischbewegung nicht unterbrochen wurden. Die Sequenzparameter wurden daran angepaÿt, optimale Bildqualität über das gesamte Gesichtsfeld zu erreichen. Die Methode wurde an 22 Patienten mit malignen Tumorerkrankungen des Beckens evaluiert. Hauptsächlich vertretene Tumorentität war das Rektumkarzinom. Zwei Radiologen verglichen die Bildqualität der SMS-Sequenz unabhängig voneinander mit der eines konventionellen MRT-Verfahrens mit stationärem Patiententisch. Ergebnisse Die Auswertung der Daten ergab eine hohe diagnostische Aussagekraft der SMS-Daten in Körperregionen, die wenig oder keinen Atembewegungen unterworfen waren sowie in denjenigen Arealen, die während der initialen Atemanhaltephase aufgenommen wurden. Die Bildqualität im Oberbauch, im Retroperitonealraum und im Becken erwies sich dabei als reproduzierbar und äquivalent zur stationären MRT. Das Auftreten von die Bildqualität beeinträchtigenden Bewegungsartefakten beschränkte sich auf die Darmanteile des ventralen Mittelbauchs. Schluÿfolgerung Mit der vorliegenden Arbeit wurde die SMS-MRT erstmals erfolgreich in ein klinisches Untersuchungsprotokoll integriert. Sie stellte sich als vielversprechendes Verfahren dar, das groÿes Potential besitzt, sich zu einer Standardmethode der abdominellen Diagnostik bei Erstdiagnose, Staging und Nachsorge von malignen Tumorerkrankungen des Beckens zu entwickeln. 41 42 ZUSAMMENFASSUNG Literaturverzeichnis [Aka 05] Akasu T, Iinuma G, Fujita T, Muramatsu Y, Tateishi U, Miyakawa K, Murakami T, Moriyama N. (2005) Thin-section MRI with a phased-array coil for preoperative evaluation of pelvic anatomy and tumor extent in patients with rectal cancer. Am J Roentgenol 184: 531-538 [Ast 54] Astler VB, Coller FA. (1954) The prognostic signicance of direct extension of carcinoma of the colon and rectum. Ann Surg 139: 846. [Bar 01] Barkhausen J, Quick HH, Lauenstein T, Goyen M, Ruehm SG, Laub G, Debatin JF, Ladd ME. (2001) Whole-body MR-imaging in 30 seconds with real-time true FISP and a continuously rolling table platform: Feasibility study. Radiology 220: 252-256. [Bee 04] Beets-Tan RGH, Beets GL. (2004) Rectal cancer: review with emphasis on MR imaging. Radiology 232: 335-346. [Bee 07] Beer AJ, Wieder HA, Stollfudd JC. (2007) Bildgebendes Staging von Tumoren des Verdauungstrakts. Radiologie up2date 1: 9-32. [Bip 04] Bipat S, Glas AS, Slors FJM, Zwinderman AH, Bossuyt PMM, Stoker J. (2004) Rectal Cancer: Local Staging and Assessment of Lymph Node Involvement with Endoluminal US, CT, and MR ImagingA Meta-Analysis. Radiology 232:773-783. [Bip 05] Bipat S, van Leeuwen MS, Comans EFI, Pijl MEJ, Bossuyt PMM, Zwinderman AH, Stoker J. (2005) Colorectal Liver Metastases: CT, MR Imaging, and PET for DiagnosisMetaanalysis. Radiology 237:123-131. [Bri 00] Brittain JH, McCann RA, Pauly JM. (2002) Incremental table motion for increased volume coverage. In: 8th Proc Intl Soc Magn Reson Med, Denver, p. 1726. 43 44 [Bri 02] LITERATURVERZEICHNIS Brittain JH, Gurr DH, Shimakawa A, Polzin JA, Herfkens RJ, Pauly JM. (2002) Wholebody imaging with a continuously moving patient table. In: 10th Proc Intl Soc Magn Reson Med, Hawaii, p. 2336. [Bro 99] Brown GB, Richards CJ, Newcombe RG, Dallimore NS, Radclie AG, Carey DP, Bourne MW, Williams GT. (1999) Rectal Carcinoma: Thin-section MR imaging for staging in 28 patients. Radiology 211:215-222. [Bro 04] Brown G, Kirkham A, Williams GT, Bourne M, Radclie AG, Sayman J, Newell R, Sinnatamby C, Heald RJ. (2004) High-resolution MRI of the anatomy important in total mesorectal excision of the rectum. Am J Roentgenol 182: 431-439. [Bue 92] Buess G, Mentges B, Manncke K, Starlinger M, Becker HD. (1992) Technique and results of transanal endoscopic microsurgery in early rectal cancer. Am J Surg 163: 63-69. [Cha 02] Chau I, Cunningham D. (2002) Chemotherapy in colorectal cancer: new options and new challenges. Br Med Bull 64: 159-180. [Chu 06] Chun HK, Choi D, Kim MJ, Lee J, Yun SH, Kim SH, Lee SJ, Kim CK. (2006) Preoperative staging of rectal cancer: comparison of 3-T high-eld MRI and endorectal sonography. Am J Roentgenol 187: 1557-1562. [Die 99] Dietrich O, Hajnal JV. (1999) Extending the coverage of true volume scans by continuous movement of the subject. In: 7th Proc Intl Soc Magn Reson Med, Philadelphia, p.1653. [DKG 04] Deutsche Krebsgesellschaft e.V. (2004) Rektumkarzinom. In: Kurzgefasste Interdisziplinäre Leitlinien. Diagnostik und Therapie maligner Erkrankungen. 4. Auage W. Zuckschwerdt Verlag, München, Bern, Wien, New York. [Ear 98] Earls JP, DeSena S, Bluemke DA. (1998) Gadolinium-enhanced three-dimensional MR angiography of the entire aorta and iliac arteries with dynamic manual table translation. Radiology 209: 844-849. [Fai 03] Fain SB, Browning FJ, Polzin J, Zhou Y, Grist TM, Mistretta CA. (2003) Time-resolved whole-body MRA during continuous table motion using oating table isotropic projection acquisition (FLIPR). In: 11th Proc Intl Soc Magn Reson Med, Toronto, p. 253. LITERATURVERZEICHNIS [Fau 06] 45 Fautz H-P, Kannengiesser SAR. (2006) Sliding Multi-Slice (SMS): A new technique for minimum FOV usage in axial continuously moving table acquisitions. Magn Reson Med 55: 363-370. [Fen 06] Fenchel M, Scheule AM, Stauder NI, Kramer U, Tomaschko K, Nägele T, Bretschneider C, Schlemmer HP, Claussen CD, Miller S. (2006) Atherosclerotic Disease: Whole-Body Cardiovascular Imaging with MR System with 32 Receiver Channels and Total-Body Surface Coil Technology Initial Clinical Results. Radiology 238: 280-291. [Gar 02] Garcia-Aguilar J, Pollack J, Lee SH, Hernandez de Anda E, Mellgren A, Wong WD, Finne CO, Rothenberger DA, Mado RD. (2002) Accuracy of endorectal ultrasonography in preoperative staging of rectal tumors. Dis Colon Rectum 45: 10-15. [Gas 85] Gastrointestinal Tumor Study Group. (1985) Prolongation of the disease-free interval in surgically treated rectal carcinoma. N Engl J Med 312: 1465-1472. [GEK 06] Gesellschaft der epidemiologischen Krebsregister in Deutschland e.V. (2006) Krebs in Deutschland. Häugkeiten und Trends, 5. Ausgabe, Saarbrücken. [Gha 03] Ghanem NA, Fautz HP, Weigel M, Speck O, Hennig J, Bley T, Langer M. (2003) Whole body-MRI imaging with a continuously moving table platform in detection of metastatic disease in cancer patients: First results of a feasibility study. In: 11th Proc Intl Soc Magn Reson Med, Toronto, p. 1333. [Gri 02] Griswold MA, Jakob PM, Heidemann RM, Nittka M, Jellus V, Wang J, Kiefer B, Haase A. (2002) Generalized Autocalibrating Partially Parallel Acquisitions (GRAPPA). Magn Reson Med 47, 1202-1210. [Gro 01] Grothey A, Schmoll H-J. (2001) New chemotherapy approaches in colorectal cancer. Curr Opin Oncol 13: 275-286. [Hal 95] Haller DG. (1995) An Overview of Adjuvant Therapy for Colorectal Cancer. Eur J Cancer 31A: 1255-1263. [Hea 82] Heald RJ, Husband EM, Ryall RD. (1982) The mesorectum in rectal cancer surgerythe clue to pelvic recurrence? Br J Surg 69: 613-616. [Her 99] Heriot AG, Grundy A, Kumar D. (1999) Preoperative staging of rectal carcinoma. Br J Surg 86: 17-28. 46 [Her 00] LITERATURVERZEICHNIS Hermanek P, Hermanek PJ. (2000) Role of the surgeon as a variable in the treatment of rectal cancer. Semin Surg Oncol 19: 329-335. [Hoj 82] Hojo K, Koyama Y, Moriya Y. (1982) Lymphatic spread and its prognostic value in patients with rectal cancer. Am J Surg 144: 350-354. [Joh 97] Johnson KM, Levitt GD, Kayser HW. (1997) Total-body MR imaging in as little as 18 seconds. Radiology 202: 262-267. [Jun 99] Junginger T, Hossfeld DK, Sauer R, Hermanek P. (1999) Adjuvante und neoadjuvante Therapie bei Kolon- und Rektumkarzinom. Dtsch Arztebl 96: A-698/B-569/C-535. [Kim 06a] Kim CK, Kim SH, Chun HK, Lee WY, Yun SH, Song SY, Choi D, Lim HK, Kim MJ, Lee J, Lee SJ. (2006) Preoperative staging of rectal cancer: accuracy of 3-Tesla magnetic resonance imaging. Eur Radiol 16: 972-980. [Kim 06b] Kim NK, Baik SH, Seong JS, Kim H, Roh JK, Lee KY, Sohn SK, Cho CH. (2006) Oncologic outcomes after neoadjuvant chemoradiation followed by curative resection with tumorspecic mesorectal excision for xed locally advanced rectal cancer: Impact of postirradiated pathologic downstaging on local recurrence and survival. Ann Surg 244: 1024-1030. [Kin 02] Kinkel K, Lu Y, Both M, Warren RS, Thoeni RF. (2002) Detection of hepatic metastases from cancers of the gastrointestinal tract by using noninvasive imaging methods (US, CT, MR imaging, PET): A meta-analysis. Radiology 224: 748-756. [Koh 05] Koh DM, Brown G, Temple L, Blake H, Raja A, Toomey P, Bett N, Farhat S, Norman AR, Daniels I, Husband JE. (2005) Distribution of mesorectal lymph nodes in rectal cancer: in vivo MR imaging compared with histopathological examination. Initial observations. Eur Radiol 15: 1650-1657. [Koh 06] Koh D, Brown G, Husband J. (2006) Nodal staging in rectal cancer. Abdom Imaging 31: 652-659. [Kol 94] Kollmorgen CF, Meagher AP, Wol BG, Pemberton JH, Martenson JA, Illstrup DM. (1994) The long-term eect of adjuvant postoperative chemoradiotherapy for rectal carcinoma on bowel function. Ann Surg 220: 676-682. LITERATURVERZEICHNIS [Kra 05] 47 Kramer H, Schoenberg SO, Nikolaou K, Huber A, Struwe A, Winnik E, Wintersperger BJ, Dietrich O, Kiefer B, Reiser MF. (2005) Cardiovascular Screening with Parallel Imaging Techniques and a Whole-Body MR Imager. Radiology 236: 300-310. [Kro 91] Krook JE, Moertel CG, Gunderson LL, Wieand HS, Collins RT, Beart RW, Kubista TP, Poon MA, Meyers WC, Mailliard JA, et al. (1991) Eective surgical adjuvant therapy for high-risk rectal carcinoma. N Engl J Med 324: 709-715. [Kru 02] Kruger DG, Riederer SJ, Grimm RC, Rossman PJ. (2002) Continuously moving table data acquisition method for long FOV contrast-enhanced MRA and whole-body MRI. Magn Reson Med 47: 224-231. [Kru 05] Kruger DG, Riederer SJ, Polzin JA, Madhuranthakam AJ, Hu HH, Glockner JF. (2005) Dual-velocity continuously moving table acquisition for contrast-enhanced peripheral magnetic resonance angiography. Magn Reson Med 53: 110-117. [Lau 89] Laurie JA, Moertel CG, Fleming TR, Wieand HS, Leigh JE, Rubin J, McCormack GW, Gerstner JB, Krook JE, Malliard J. (1989) Surgical adjuvant therapy of large-bowel carcinoma: an evaluation of levamisole and the combination of levamisole and uorouracil. J Clin Oncol 7: 1447-1456. [Lau 04] Lauenstein TC, Goehde SC, Herborn CU, Goyen M, Oberho C, Debatin JF, Barkhausen J. (2004) Whole-Body MR Imaging: Evaluation of Patients for Metastases. Radiology 233: 139-148. [Lau 06] Laurent F, Montaudon M, Corneloup O. (2006) CT and MRI of Lung Cancer. Respiration 73: 133-142. [Liu 98] Liu K, Rutt BK. (1998) Sliding interleaved ky (SLINKY) acquisition: A novel 3D MRA technique with suppressed slab boundary artifact. J Magn Reson Imaging 8: 905-911. [Lud 06] Ludwig UA, Sommer G, Zaitsev M, Ghanem NA, Hennig J, Fautz HP. (2006) 2D Axial Moving Table Acquisitions with Dynamic Slice Adaptation. Magn Reson Med 55: 423-430. [Mac 97] Machover D. (1997) A Comprehensive Review of 5-Fluorouracil and Leucovorin in Patients with Metastatic Colorectal Carcinoma. Cancer 80: 1179-1187. 48 LITERATURVERZEICHNIS [Mad 04] Madhuranthakam AJ, Kruger DG, Riederer SJ, Glockner JF, Hu HH. (2004) Time-resolved 3D contrast-enhanced MRA of an extended FOV using continuous table motion. Magn Reson Med 52: 568-576. [Mai 00] Maier AG, Kersting-Sommerho B, Reeders JW, Judmaier W, Schima W, Annweiler AA, Meusel M, Wallengren NO. (2000) Staging of rectal cancer by double-contrast MR imaging using the rectally administered superparamagnetic iron oxide contrast agent ferristene and IV gadodiamide injection: results of a multicenter phase II trial. J Magn Reson Imaging 12: 651-660. [Mar 97] Markus J, Morrissey B, deGara C, Tarulli G. (1997) MRI of recurrent rectosigmoid carcinoma. Abdom Imaging 22: 338-342. [Mil 26] Miles WE. (1926) Cancer of the Rectum. Harrisons, London, p. 63. [Min 94] Minsky BD. (1994) Preoperative combined modality treatment for rectal cancer. Oncology 8: 53-58,61,64-68. [Moe 95] Moertel CG, Fleming TR, Macdonald JS, Haller DG, Laurie JA, Tangen CM, Ungerleider JS, Emerson WA, Tormey DC, Glick JH, Veeder MH, Mailliard JA. (1995) Fluorouracil plus Levamisole as Eective Adjuvant Therapy after Resection of Stage III Colon Carcinoma: A Final Report. Ann Intern Med 122: 321-326. [Mon 99] Monig SP, Baldus SE, Zirbes TK, Schröder W, Lindemann DG, Dienes HP, Hölscher AH. (1999) Lymph node size and metastatic inltration in colon cancer. Ann Surg Oncol 6: 579-581. [Nas 02] Nascimbeni R, Burgart LJ, Nivatvongs S, Larson DR. (2002) Risk of lymph node metastasis in T1 carcinoma of the colon and rectum. Dis Colon Rectum 45: 200-206. [OCo 94] O'Connell MJ, Martenson JA, Wieand HS, Krook JE, Macdonald JS, Haller DG, Mayer RJ, Gunderson LL, Rich TA. (1994) Improving Adjuvant Therapy for Rectal Cancer by Combining Protracted-Infusion Fluorouracil with Radiation Therapy after Curative Surgery. N Engl J Med 331: 502-507. [Oki 96] Okizuka H, Sugimura K, Yoshizako T, Kaji Y, Wada A. (1996) Rectal carcinoma: prospective comparison of conventional and gadopentetate dimeglumine enhanced fat-suppressed MR imaging. J Magn Reson Imaging 6: 465-471. LITERATURVERZEICHNIS [Pes 05] 49 Peschaud F, Cuenod C-A, Benoist S, Julie C, Beauchet A, Siauve N, Taieb-Kasbi F, Penna C, Nordlinger B. (2005) Accuracy of magnetic resonance imaging in rectal cancer depends on location of the tumor. Dis Colon Rectum 48: 1603-1609. [Que 97] Queiÿer W, Lehnert T. (1997) Das Rektumkarzinom. In: Schriftenreihe des Tumorzentrums Heidelberg/Mannheim. [Ren 04] Renz-Polster H, Krautzig S, Braun J. (2004) Basislehrbuch Innere Medizin, 3. Au. Elsevier GmbH, Urban & Fischer-Verlag, München. [Rue 00] Ruehm SG, Hany TF, Pfammatter T, Schneider E, Ladd ME, Debatin JF. (2000) Pelvic and lower extremity arterial imaging: diagnostic performance of three-dimensional contrastenhanced MR angiography. Am J Roentgenol 174: 1127-1135. [Sab 03] Sabati M, Lauzon ML, Frayne R. (2003) Novel undersampled acquisition schemes for continuously moving table peripheral contrast-enhanced MRA. In: 11th Proc Intl Soc Magn Reson Med, Toronto, 2003; p. 252. [Sau 02] Saunders TH, Mendes Ribeiro HK, Gleeson FV. (2002) New techniques for imaging colorectal cancer: the use of MRI, PET and radioimmunoscintigraphy for primary staging and follow-up. Br Med Bull 64: 81-99. [Sch 04] Schaefer O, Oeksuez MO, Lohrmann C, Langer M. (2004) Dierentiation of anal sphincters with high-resolution magnetic resonance imaging using contrast-enhanced fast low-angle shot 3-dimensional sequences. J Comput Assist Tomogr 28: 174-179. [Sch 05] Schlemmer H-P, Schäfer J, Pfannenberg C, Radny P, Korchidi S, Müller-Horvath C, Nägele T, Tomaschko K, Fenchel M, Claussen CD. (2005) Fast Whole-Body Assessment of Metastatic Disease Using a Novel Magnetic Resonance Imaging System. Initial Experiences. Invest Radiol 40: 64-71. [Sch 06] Schäfer J, Schlemmer HPW. (2006) Total-body-MRI in oncology. Eur Radiol 16: 20002015. [Sch 07] Schäfer O, Baumann T, Pache G, Wiech T, Langer M. (2007) Präoperatives Staging des Rektumkarzinoms. Radiologe 47: 635-652. 50 [Sha 03] LITERATURVERZEICHNIS Shankaranarayanan A, Herfkens R, Hargreaves BM, Polzin JA, Santos JM, Brittain JH. (2003) Helical MR: Continuously moving table axial imaging with radial acquisitions. Magn Reson Med 50: 1053-1060. [Sie 01] Siewert JR. (2001) Chirurgie, 7. Au. Springer-Verlag, Berlin, Heidelberg. [Sin 06] Sinha R, Verma R, Rajesh A, Richards CJ. (2006) Diagnostic value of multidetector row CT in rectal cancer staging: comparison of multiplanar and axial images with histopathology. Clin Radiol 61: 924-931. [Soy 04] Soyer P, Poccard M, Boudiaf M, Abitbol M, Hamzi L, Panis Y, Valleur P, Rymer R. (2004) Detection of Hypovascular Hepatic Metastases at Triple-Phase Helical CT: Sensitivity of Phases and Comparison with Surgical and Histopathologic Findings. Radiology 231: 413420. [Sto 00] Stoker J, Rociu E, Wiersma TG. (2000) Imaging of anorectal disease. Br J Surg 87: 10-27. [Stü 05] Stückle CA, Haegele KF, Jendreck M, Kickuth R, Schneider O, Hohlbach G, Liermann D.(2005) Verbesserte Rezidiverkennbarkeit mittels multiplanarer Rekonstruktion beim Rektumkarzinom in der Mehrzeilenspiralcomputertomographie. Radiologe 45: 930-934,936. [Tay 07] Taylor A, Slater A, Mapstone N, Taylor S, Halligan S. (2007) Staging rectal cancer: MRI compared to MDCT. Abdom Imaging 32: 323-327. [Tor 03] Torricelli P, Pecchi A, Luppi G, Romagnoli R. (2003) Gadolinium-enhanced MRI with dynamic evaluation in diagnosing the local recurrence of rectal cancer. Abdom Imaging 28: 19-27. [UICC 02] UICC. (2002) TNM Classication of Malignant Tumors. Wiley & Sons, New York. [Val 01] Valls C, Andia E, Sanchez A, Guma A, Figueras J, Torras J, Serrano T. (2001) Hepatic Metastases from Colorectal Cancer: Preoperative Detection and Assessment of Resectability with Helical CT. Radiology 218: 55-60. [Vli 05] Vliegen RFA, Beets GL, von Meyenfeldt MF, Kessels AGH, Lemaire EMT, van Engelshoven JMA, Beets-Tan RGH. (2005) Rectal Cancer: MR Imaging in Local Staging - Is Gadoliniumbased Contrast Material Helpful? Radiology 234: 179-188. LITERATURVERZEICHNIS 51 [Vog 97] Vogl TJ, Pegios W, Mack MG, Hünerbein M, Hintze R, Adler A, Lobbeck H, Hammerstingl R, Wust P, Schlag P, Felix R. (1997) Accuracy of staging rectal tumors with contrastenhanced transrectal MR imaging. Am J Roentgenol 168: 1427-1434. [vSc 06] von Schulthess GK, Steinert HC, Hany TF. (2006) Integrated PET/CT: current applications and future directions. Radiology 238: 405-422. [Wei 03] Weigel M, Fautz HP, Ghanem N, Speck O, Hennig J. (2003) Adaptation of HASTE for continuous moving table acquisition. In: 11th Proc Intl Soc Magn Reson Med, Toronto, p. 992. [Zhu 03] Zhu Y, Dumoulin CL. (2003) Extended eld-of-view imaging with table translation and frequency sweeping. Magn Reson Med 49: 1106-1112. 52 LITERATURVERZEICHNIS Publikationsliste Artikel in Fachzeitschriften Sommer G, Fautz HP, Ludwig UA, Hennig J. (2006) Multi Contrast Sequences with Continuous Table Motion: A Novel Acquisition Technique for Extended Field of View Imaging. Magn Reson Med 55: 918-922. Ludwig UA, Sommer G, Zaitsev M, Ghanem NA, Hennig J, Fautz HP. (2006) 2D Axial Moving Table Acquisitions with Dynamic Slice Adaptation. Magn Reson Med 55: 423-430. Kos S, Sommer G, Sommer G, Potthast S. (2007) Das Cava-Lipom. Fortschr Roentgenstr 179: 635-636. Schaefer AO, Baumann T, Ludwig UA, Fautz HP. (2008) Sliding Multislice MRI for Abdominal Staging of Patients with Pelvic Malignancies: A Pilot Study. J Magn Reson Imaging 27: 666-672. Paul D, Sommer G, Hentschel M, Baumann T, Leupold J, Ludwig UA. (2008) Chemical Shift Selective Fat Imaging using TIDE-bSSFP for Quantication of Adipose Tissue. J Comput Assist Tomogr, accepted 26.09.2008. Konferenzbeiträge Sommer G, Fautz HP, Ludwig U, Hennig J. (2004) Multikontrastaufnahmen bei kontinuierlich beweg- tem Patiententisch am Beispiel der Ganzkörperbildgebung. In: Proc 7. Jahrestagung der Deutschen Sektion der ISMRM, Mainz, p. 35-36. Sommer G, Ludwig UA, Weigel M, Ghanem N, Hennig J. (2004) Development of Multi-Contrast 53 54 Publikationsliste Sequences Using Continuous Moving Table Acquisition. In: 12th Proc Intl Soc Magn Reson Med, Kyoto, p. 700. Ludwig U, Zaitsev M, Weigel M, Sommer G, Ghanem N, Hennig J. (2004) Adaptive Slice Shifting for Continuous Moving Table Acquisition Using hyperHASTE. In: 12th Proc Intl Soc Magn Reson Med, Kyoto, p. 2671. Ludwig U, Kannengiesser S, Weigel M, Ghanem N, Sommer G, Hennig J. (2004) Comparison of Stationary and Moving Surface Coil Setups for Continuously Moving Table MRI. In: 12th Proc Intl Soc Magn Reson Med, Kyoto, p. 2670. Ghanem N, Winterer J, Schäfer O, Ludwig U, Sommer G, Bley T, Hennig J, Langer M. (2004) Axiale kontinuierliche Ganzkörper-MRT-Bildgebung. 85. Dt Röntgenkongress, Wiesbaden, In: Fortschr Roentgenstr 176: 18. Sommer G, Fautz HP, Ludwig UA, Ghanem N, Hennig J. (2005) Variability of Contrast and Spatial Parameters in Multi Contrast Imaging. In: 13th Proc Intl Soc Magn Reson Med, Miami, p. 2372. Sommer G, Fautz HP, Ludwig UA, Wieben O, Ghanem N, Hennig J. (2005) Whole Body Fat-Water Separation Using Multi Contrast Imaging. In: 13th Proc Intl Soc Magn Reson Med, Miami, p. 1967. Ghanem N, Bley T, Müller-Mall C, Fautz HP, Sommer G, Ludwig U, Hennig J, Langer M. (2005) Move During Scan: Wholebody MRI in Clinical Routine in 50 Patients. In: 13th Proc Intl Soc Magn Reson Med, Miami, p. 796. Ludwig U, Fautz HP, Sommer G, Harter S, Ghanem N, Hennig J. (2005) Multiple Volume coverage in continuously moving Table Acquisitions applied to free breathing STIR imaging. In: 13th Proc Intl Soc Magn Reson Med, Miami, p. 1962. Fautz HP, Kannengiesser SAR, Ludwig U, Ghanem N, Sommer G, Hennig J. (2005) Advances in T2-Weighted Axial Moving Table Acquisitions. In: 13th Proc Intl Soc Magn Reson Med, Miami, p. 1963. Sommer G, Ludwig UA, Fautz HP, Schäfer O. (2006) Abdominal Imaging with Extended Field of View in Rectal Cancer Using a Continuously Moving Table: A Feasibility Study. In: 14th Proc Intl Soc Magn Reson Med, Seattle, p. 1801. Publikationsliste Sommer G, 55 Ludwig UA, Schäfer O, Fautz HP. (2006) One-Breath-Hold Acquisition of the Whole Abdomen in One Minute Using Continuously Moving Table MRI. In: 14th Proc Intl Soc Magn Reson Med, Seattle, p. 2269. Sommer G, Ludwig UA, Baumann T, Paul D. (2008) Intrinsic Water-Suppression in TIDE-bSSFP Applied for Quantication and Dierentiation of Adipose Tissue. In: 16th Proc Intl Soc Magn Reson Med, Toronto, p. 2703. Vorträge Sommer G. (17.03.2005) Multi-Kontrast Ganzkörpermessungen. Seminar MR, Universitätsklinikum Freiburg. Sommer G. (21.03.2005) Multi-Kontrast Ganzkörper MRT: Simultane Akquisition multipler Kon- traste bei fahrendem Tisch. Arbeitskreis Magnetresonanzverfahren der DGMP, Freiburg. Sommer G. (01.07.2005) Simultaneous Multi Contrast Moving Table Examinations. 1st ISMRM endorsed Workshop on Whole Body Magnetic Resonance Imaging, Freiburg. Sommer G. (12.01.2006) Extended FOV Imaging in Rectal Cancer. Seminar MR, Universitätsklinikum Freiburg. Sommer G. (06.05.2006) Assessing Metastatic Spread of Pelvic Tumors in the Abdomen Using Single- Breath-Hold Moving Table MRI: Initial Clinical Experience. Hot Topics from Young Investigators, Cancer Study Group, 14th Annual Meeting of ISMRM, Seattle. Abschluÿarbeiten Sommer G. (2005) Multi-Kontrast-Sequenzen mit kontinuierlich bewegtem Patiententisch: Entwick- lung eines neuartigen Aufnahmeverfahrens für die Ganzkörper-Magnetresonanztomographie. Diplomarbeit der Physik, Fakultät für Mathematik und Physik der Universität Freiburg. 56 Publikationsliste Danksagung Hiermit möchte ich mich bei allen, die zum Gelingen dieser Arbeit beigetragen haben, ganz herzlich bedanken. Mein besonderer Dank gilt: • Herrn Prof. Dr. Jürgen Hennig für die Bereitstellung der Arbeit und die Möglichkeit, mich als Mitarbeiter seiner Abteilung auch über das Thema meiner Arbeit hinaus in weiteren Bereichen der Medizin und MR-Physik fortzubilden. • Meinen Betreuern Dr. Hans-Peter Fautz, Dr. Ute Ludwig und Prof. Dr. Oliver Schäfer für ihre groÿe Hilfsbereitschaft und Geduld bei der Betreuung meiner Arbeit und die kompetente Beantwortung der vielen damit verbundenen Fragen. • Prof. Dr. Oliver Schäfer und Dr. Tobias Baumann für die radiologische Beurteilung der Daten. • Laurence Haller für ihre freundliche und zuverlässige Hilfe bei allen organisatorischen Dingen. • Allen Mitgliedern der Abteilung MR-Physik für ein tolles Arbeitsklima. • Meiner Freundin Christine für ein wundervolles privates Umfeld. • Meinen Eltern für die langjährige moralische und nanzielle Unterstützung vor und während meines Studiums. 57 58 59 Erklärung Ich erkläre hiermit, daÿ ich die vorliegende Arbeit ohne unzulässige Hilfe Dritter und ohne Benutzung anderer als der angegebenen Hilfsmittel angefertigt habe. Die aus anderen Quellen direkt oder indirekt übernommenen Daten und Konzepte sind unter Angabe der Quelle gekennzeichnet. Insbesondere habe ich hierfür nicht die entgeltliche Hilfe von Vermittlungs- beziehungsweise Beratungsdiensten (Promotionsberater oder anderer Personen) in Anspruch genommen. Niemand hat von mir unmittelbar oder mittelbar geldwerte Leistungen für Arbeiten erhalten, die im Zusammenhang mit dem Inhalt der vorgelegten Dissertation stehen. Die Arbeit wurde bisher weder im In- noch im Ausland in gleicher oder ähnlicher Form einer anderen Prüfungsbehörde vorgelegt. Grenzach-Wyhlen, den 28.09.2008. Gregor Sommer