Vollständigen Artikel als PDF
Werbung

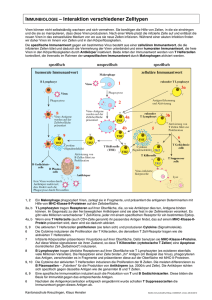
Wiederherstellung der immunologischen Toleranz durch Generierung von regulatorischen T-Lymphozyten Autoren: P. Schleicher und D. Brückl Eine kontinuierliche Zunahme chronischer Erkrankungen ist zu beobachten. Allergien nehmen zu, chronische Infektanfälligkeit, Krankheitsbilder aus dem rheumatischen Formenkreis, Autoimmunerkrankungen und Tumorerkrankungen steigen prozentual an, und das Patientenkollektiv wird immer jünger. Immunologische Abwehrschwächen des Körpers liegen als Hauptursachen zugrunde. Die Gründe für die Entwicklung zellulärer Immunschwächen sind: falsche Ernährung, Bewegungsarmut, psychische Belastung, Distress, Strahlenbelastung, Umweltgifte und toxisch wirkende Pharmaka. Es kommt zu Flexibilitätsverlust des körpereigenen Immunsystems und zur Fehlregulation des zellulären Abwehr. T-Zellen Setzt sich unser Körper mit einem Antigen auseinander, wird unter anderem die T-Zelle aktiviert. Aktivierte T-Zellen produzieren Lymphokine, die verantwortlich sind für lokale oder allgemeine Symptome wie bessere Durchblutung, Überwärmung, Schwellung und Schmerz am immunologischen Reaktionsort. T-Zellen regeln die Antikörperproduktion durch B-Zellen, erkennen und zerstören virusinfizierte Zellen, aktivieren die Phagozytose, um pathogene Antigene zu zerstören und immunologisch erkennbar zu machen, kontrollieren Stärke und Qualität der Immunantwort und regulieren vermutlich DNS-Reperaturmechanismen. B-Zellen B-Zellen leisten die spezifizierte Antikörperproduktion gegen Antigene und sind das „immunologische Gedächtnis“. B-Zellen repräsentieren etwa 5 bis 15 % der zirkulierenden lymphatischen Zellen. Ihre Aufgabe ist es, ausschließlich Immunglobuline zu produzieren. B-Lymphozyten des Menschen erzeugen im peripheren Blut insbesondere Oberflächenimmunglobulin-M- und Immunglobulin-G-Antikörper. B-Zellen können isoliert nicht optimal reagieren. Sie unterliegen einer hochspezifischen Regulation durch weitere Subpopulationen der Lymphozyten: T-Zellen, Helfer-Zellen, Suppressor-Zellen und Makrophagen. T-Zellen können die B-Zellen unterdrücken (supprimieren). Nur in Anwesenheit der T-Zellen, Suppressor-Zellen, Helfer-Zellen und Makrophagen produziert die B-Zelle den passenden Antikörper. Suppressor-Zellen Suppressor/zytotoxische Zellen supprimieren die Immunantwort durch Drosselung der THelfer-Zellproliferation und –aktivität, sie haben zytotoxische Wirkung auf virusinfizierte Zellen, Tumorzellen und Fremdgewebe und regulieren in Interaktion von T- und B-Zellen. Nachgewiesen ist ein Interaktionskreis zwischen Suppressor-, Helfer- und B-Zelle. Die Hauptaufgabe der Suppressor-T-Lymphozyten ist dabei die Kontrolle der Immunantwort. Die T-Suppressor-Zellen beeinflussen die Reaktionsfähigkeit anderer T-Effektorzellen, wie zum Beispiel zytotoxische Zellen oder auch Helfer-Zellen. Um eine einmal ausgelöste Immunantwort optimal zu steuern, geling es auch Helfer-Zellen, Suppressor-Zellen zu stimulieren. So kann eine negative Rückkoppelung der Immunantwort eingeleitet werden, die vor überschießender Immunreaktion schützt. Suppressor-T-Zellen haben einen regulativen Effekt auf die Plasmazelle und deren Produktion von Antikörpern. Sie können die Antikörperproduktion drosseln oder lahm legen. Eine Untergruppe der T-Zellpopulation sind die Helfer-Zellen. Sie sind an der Regulation der Antikörperproduktion der B-Zelle entscheidend beteiligt. Helfer-Zellen stimulieren die Antikörperbildung nach antigenem Reiz. Sie beeinflussen jedoch auch die Suppressor-Zellen und deren zytotoxische Funktion durch einen in sich geschlossenen Regelkreis. Die wichtigsten Aufgaben der Helfer-Zellen sind das Erkennen von Antigenen, die Stimulation von B-Zellen, die Produktion von Lymphokinen und die Umwandlung von T-Suppressor- in TKiller-Zellen. Helfer-Zellen erkennen die Antigene, stimulieren die B-Zellen, produzieren Lymphokine, wandeln T-Suppressor-Zellen in T-Killer-Zellen um und reparieren wahrscheinlich DNSBrüche. Natural Killer-Zellen zerstören virusinfizierte Zellen, zerstören transformierte oder veränderte Zellen, zerstören Tumorzellen und reparieren vermutlich DNS-Brüche. Wirkmechanismus: 1. Bindung an die Zielzelle 2. Programmierung der Zielzelle zur Lyse (kalziumabhängige, vesikuläre Sekretion) 3. Spätphase der Lyse der programmierten Zelle. Granulozyten haben chemotaktische Eigenschaft, können Mikroorganismen und fremde Partikel phagozytieren, zerstören Bakterien, Viren und Pilze und sind Entzündungszellen. Makrophagen haben chemotaktische Eigenschaft, können Mikroorganismen und fremde Partikel phagozytieren, zerstören intrazellulär Bakterien, Viren, Pilze und produzieren Enzyme. Makrophagen spielen die zentrale Rolle in der zellvermittelnden Immunität. Neben ihrer Steuerfunktion übernehmen sie zu Beginn der Immunantwort die Aufgabe, dem T- und BZellsystem Antigene zu präsentieren. In der Effektorphase wirken sie antitumorös, mikrobiozid, antiviral und als Entzündungszellen. Ihre wichtigsten Eigenschaften sind Phagozytose, Zytotoxizität, Kooperation mit Lymphozyten, Sekretion verschiedener biologisch aktiver Produkte. Makrophagen sind hochaktive sekretorische Zellen, wie man sie ähnlich nur bei Leberparenchymzellen findet. Sie sezernieren lysosomale Enzyme, Kollagenasen, Elastase, Plasminogenaktivatoren, Phosphatasen, Proteasen, Thromboplastin, Transferrin, Lactoferrin, Fibronektin, Sauerstoffprodukte, Komplementkomponenten, lymphozytenaktivierende Faktoren wie Interleukin 1, Pyrogen, Interferone. Makrophagen haben eine sehr hohe Migrationsfähigkeit. Tritt an irgendeiner Stelle des Körpers ein Fremdstoff, ein Antigen oder eine bakteriell- oder viral infizierte entartete Zelle auf, gelingt es den Makrophagen aus bisher unbekannten Gründen, durch das Endothel des Gefäßes in das umliegende Gewebe einzuwandern (Diapedese). So kann es seine vielfältigen Eigenschaften gezielt und schnell am Ort des Geschehens einsetzen. Immunkomplexe Die nach antigenem Reiz produzierten Antikörper binden sich mit dem Antigen und bilden so den Immunkomplex. Bei einer normal regulierten Immunantwort bleibt das Verhältnis Antigen zu Antikörper 1:1. Dabei bleiben Immunkomplexe zirkulierend und apathogen. Es wird über Antikörperbildung des Antigen durch eine optimale Immunabwehr neutralisiert und später von Makrophagen abgebaut. Der apathogene zirkulierende Immunkomplex ist außerdem als Stellgröße im regulativen Prozeß der gesamten Immunantwort und fördert oder hemmt die zelluläre Abwehrreaktion je nach Bedarf. Besetzt ein Immunkomplex körpereigenes Substrat, wird die Komplementkaskade aktiviert und führt zur entzündlichen Zerstörung des Substrates. Liegt eine pathologische Immunregulatorische Störung vor, entgleisen meistens mehrere Mechanismen zellulärer Abwehr: 1. zu viel Lymphokine durch T-Zell-Aktivierung 2. vermehrte Produktion von Histamin, Serotonin, Prostaglandin durch Mastzellreize. 3. Produktion pathogener Immunkomplexe, die über Komplementaktivierung körpereigene Strukturen zerstören. Bei einem Überangebot an zirkulierenden Immunkomplexen wird dann das phagozytierende System blockiert. Die Phagozytoseleistung liegt lahm. Makrophagen können so entstehende entzündliche Substrate nicht mehr abbauen. Der Input in die T-Zell-Linie wird gebremst. Es folgen weitere schwere Immundefekte mit starkem Flexibilitätsverlust der zellulären Abwehr. Die Chronifizierung einer Krankheit wird möglich. Immunkomplexe sind Aggregate aus Antigenen und dem jeweils korrespondierenden Antikörper und besitzen in vielen Fällen die Fähigkeit der Komplementaktivierung. Sie entstehen im Rahmen einer Immunantwort auf akute oder chronische Reize. Ab einer gewissen Konzentration können sie von den Makrophagen nicht mehr gebunden und zerstört werden und gelangen als zirkulierende Immunkomplexe in das periphere Blut. Die CIC können sich dann an Gewebsstrukturen anlagern und über die Aktivierung des Komplementsystems schwere lokale, entzündliche Schädigungen verursachen (z.B. Nierenschädigung bei systemischem Lupus erythematodes). Die von der Plasmazelle (B-Zellen) gebildeten Immunglobuline (IgA, IgM, IgD, IgE) sind das Resultat einer Immunantwort eines Organismus auf einen akuten oder chronischen Reiz. Das gesunde Neugeborene wird nahezu ohne eigene Immunglobuline geboren, besitzt jedoch von der Mutter diaplazentar übernommenes IgG. Innerhalb der ersten Lebensmonate bis –jahre erreicht die Immunglobulinproduktion allmählich Erwachsenenwerte. Komplement Die Komplementreaktion ist eine Folge der Antikörperproduktion nach Antigenreiz und primär verantwortlich für die Zerstörung von Substrat im Körper. Es gibt drei klassische Reaktionsstufen: 1. Erkennung 2. enzymatische Aktivierung 3. Angriff der Membranen mit folgendem Zelltod Neue Erkenntnisse Von besonderer Bedeutung für die T-Zell-Entwicklung sind die CD4, CD8 Hilfsrezeptoren (Helfer- und Suppressorzellen). Gibt es ein besonderes Bindungssignal während der Reifung dieser Moleküle, entwickeln sich die CD4 Helferzellen zu TH1 oder TH2 Zellen, die auf präsentierte Fremdantigene bestimmt sind. So entwickelt sich die T-Zelle zur zytotoxischen CD8 Zelle. In dieser CD4, T-Helfer und CD8 T-Suppressorzell-Differenzierung zur echten Effektorzellen spielen Zytokine eine entscheidende Rolle (finetuning). TH1 und CD8 T-Zellen benötigen INF-Gamma, der einen Transkriptionsfaktor aktiviert. So werden aus naiven CD8 T-Zellen effektive. Für TH1 Zellen werden zusätzlich Interleukin 12 und Interleukin 4 Rezeptoren notwendig, in der TH2 Linie fehlt der Transkriptionsfaktor, TH2 Zellen brauchen, um effektiv zu werden zusätzlich zum Interleukin 12 Rezeptor, Interleukin 4. Durch einen anderen Transkriptionsfaktor können dann TH2 Zellen Interleukin 4, Interleukin 5 und Interleukin 13 produzieren. Damit können sie extrazelluläre Parasiten vernichten helfen. Immunologische Beistandsreaktion. Antigene (rote Punkte) in sehr niedriger Dosierung (< 1ug/kg) generieren über APC (antigenpräsentierende) regulatorische Lymphozyten (Th3Zellen), die nach Kontakt mit entzündungsfördernden Th1- und Th2-Zellen (h Helfer) die entzündungshemmenden Zytokine TGF-ß, IL-4 und IL-10 freisetzen. Solange das Gesetz der Harmonie besteht, so lange Toleranz gegenüber Autoantigenen herrscht, bleibt das dynamische System stabil. Zum Erhalt der Toleranz spielen regulatorische T-Lymphozyten eine bedeutende Rolle, die heute als T3 Zellen oder CD4, CD25 positive Zellen bezeichnet werden. T3 Zellen spielen in der peripheren regulatorischen Immunität eine wichtige Rolle. Sie sind natürliche Suppressorzellen, die entscheidend regulieren können. TH3 Zellen spielen eine entscheidende Schlüsselrolle, in den peripheren regulatorischen Immunmechanismen. Sie sind natürliche Suppressorzellen, die hohe Sensitivität gegen Antigene entwickeln. (Persönliche Mitteilungen Prof. Heine 2007). TH3 Zellen sind in der Lage, Autoimmunreaktionen zu unterdrücken. TH3 Zellen vermitteln ihre suppressive Funktion durch Kontakt und Freisetzung von entzündungshemmenden Zytokinen. (IL10, TGF beta). Dadurch werden TH1 und TH2 Zellen in ihrer Funktion und Teilungsfähigkeit gehemmt. Die TH3 Zellen verschalten im regulatorischen Netzwerk alle Immunreaktionen miteinander. Sie sind somit Stabilisator der Toleranz und lassen sich durch Zytokine vermitteln. So gelingt eine ständige Aktivitätsbegrenzung und Kontrolle der immunkompetenten Zellen. So gelingt es, bei Bakterien mehr IGF-Gamma zu sezernieren und TH1 Zellen anzuregen. Bei viralen Infekten entwickelt sich vermehrt CD8 T-Zellen, bei Parasiten stehen TH2 Zellen im Zentrum. Immer sind dabei die TH3 Zellen bei der Immunentscheidung wesentlich beteiligt. (Heine 2007). TH3 Zellen treten stets vermehrt in Gewebebereichen mit erhöhter Antigenlast auf und sind auch vermehrt im Tumorgewebe. So gelingt es, über die weitere Beeinflussung von TH3 Zellen neue Methoden zur Therapie chronischer Immunkrankheiten zu entwickeln. (Diabetes Typ1, multiple Sklerose, Transplantatabstoßung, Allergien etc.) (Übersicht S. Wickelkrehn 2004) Da TH3 schon in geringen Konzentrationen von verschiedenen Peptiden und komplexen Peptid-Gemischen aktiviert werden können, ist dies einer der bedeutendsten Angriffsorte für Homöopathika, Phytotherapeutika aber auch von Nahrungsmitteln. Weitere Wege zur Regulation von Immunreaktionen Makrophagen und Rezeptorsteuerung Durch permanenten antigenen Einfluß, z.B. durch Bakterien, Viren, Pilze, jedoch auch vermehrte Replikation von Tumorzellen in Kombination mit partiellen Immundefekten kann es zu einer dauernden Hyperaktivität bestimmter Immunzellen kommen, so dass die daraus resultierende vermehrte Produktion von Mediatoren (z.B. Interleukin1) im Endeffekt zu einer anhaltenden Blockierung wichtiger Repairmechanismen führt. Dies gilt genauso für den permanenten Einfluss von Umweltnoxen, wie Nikotin, Feinstaub und multiple chemische Einflüsse. Diese vorübergehende Hyperaktivität der Immunzellen endet also in einem Immundefizienzsyndrom. So produziert beispielsweise der persistierend aktivierte Makrophage eine Überdosis von T-Zell stimulierendem Interleukin1 und zusätzlich eine ganze Reihe von anderen Monochinen, diese wechselseitige Überstimulation von T-Zellen und mononukleären Phagozyten ist eng verbunden mit einer unkontrollierten Zytokinproduktion und blockiert das Immunsystem des Patienten. Ein weiterer Weg zur Aktivierung von Phagozyten läuft über den oxydativen Burst. Durch Induktion und Anregung eines Sauerstoffmoleküls wird eine geringe Energie -Delta Efreigesetzt, die am nächsten Phagozyten die Aktivierung einleitet und denselben Vorgang für weitere Phagozytenstimulierung aufbereitet. Eine Immunantwort nach Läsion durch Chemotaxis birgt gewisse Risiken. Nach Entzündung und Gewebsläsion werden durch Komplementaktivierung Lock-Peptide freigesetzt (Chemotaxis). Durch Reiz des Lock-Peptids C5a lagern sich Phagozyten an das Endothel eines Gefäßes, durchwandern es, verlassen die Gefäßbahn und wandern zum Ort der Läsion. Dort leiten sie die Immunantwort ein. Ein ähnlicher Vorgang wird durch den Tumornekrose Faktor Alpha primär oder unterstützend eingesetzt. Bei der Berührung der Zellen oder Immunkomplexe oder Antikörper mit dem Gewebe, oder bei der Diapedese, also der Durchdringung der Gewebswand kommt es nicht selten zur pathogenen Immunreaktion, die ebenfalls die Regulation der Immunantwort verschieben kann. Elektromagnetische Bioinformation Phagozyten senden nach Aktivitätserhöhung während der Phagozytose Licht mit einem Maximum bei 633 nm aus. Als Lichtemitter wurden angeregte (Singulet-)Sauerstoffmoleküle identifiziert. Der Prozess der Photonenemission aus Singulet-Sauerstoff 02 erfolgt nach einem Übergang in den Grundzustand (Triplet302) mit 477 (blau), 578 (grün), 633 (hellrot), 703 und 762 (dunkelrot), 1060 und 1268 nm (infrarot): 2 (l02.) -> 2 (302) + hv (381,477,578,633. 703,762,1060 und 1268 nm) (s. Abb. 13, S. 57). Modulation der Lichtemission Verschiedene Substanzen (Immunmodulatoren) erhöhen die Aktivität der Immunzellen und damit die Lichtemission. So sind Polyanionen (Heparinoide) eine wesentliche pharmakologische Wirkstoffgruppe. Im Darm werden aus Polyanionen kurzkettige polyanionische Polysaccaridoligomere gebildet. Diese Oligomere, genauer Glycosaminoglykane, also Heparin und Heparinoide, kommen im Organismus besonders in Mastzellen und Proteoglykanen der Bindegewebsmatrix vor. Die Heparinoide sind offensichtlich anabolische Gegenspieler der Cortikosteroide, die ihrerseits katabole Mechanismen fördern. Heparinoide heben die steroidinduzierte Suppression der Phagozyten auf. Nach Aktivierung der Phagozyten über diesen Vorgang wird während des Phagozytosevorgangs Licht ausgesendet. Jeder einzelne Phagozyt strahlt in der Ruhephase etwa vier Photonen pro Sekunde aus, beim Phagozytosemaximum etwa 200 Photonen pro Sekunde. Somit verfügt das Immunsystem über einen weiteren sehr schnellen Informationsträger, der die gesamte Kette der Phagozyten wie bei einer Kettenreaktion aktivieren kann. Daraus resultieren neue, interessante Erkenntnisse. Lichtwirkung: Es gibt viele Hinweise darauf, dass Licht das Zellwachstum beeinflusst. Die Quantifizierung der Lichtwirkung auf die Teilung von Stammzellen erbringt folgende Fakten: Die Etabilierung eines durch Licht vermittelten Rückkoppelungsmechanismus zwischen phagozytierenden Zellen mit dem teilungsfähigen Stammzellenpool. Eine derartige Wechselwirkung garantiert das effiziente Nachliefern verbrauchter Effektorzellen. Immunologisch aktive Substanzen modulieren die Lichtemission während der Phagozytose. Damit ist anzunehmen, daß auch über den durch Licht gesteuerten mitotischen Regelkreis eine Wirkung auf den Nachschub von Effektorzellen besteht. Phagozyten verändern entsprechend ihrem Aktivierungsgrad das Lichtfeld im menschlichen Organismus und damit den Kontext der biochemischen Reaktionsabläufe. Rezeptorimpulse Bei allen Krankheitsbildern mit permanentem antigenem Einfluss (Tumorzellen, Viren, Pilze, Schwermetalle, Toxine etc.) folgt wegen dauernder Hyperaktivität meist die Immunblockade. Der Hyperaktivität folgt die Überladung immunkompetenter Effektorzellen mit spezifischen und nicht spezifischen Signalen. Dies führt zu einer lokalen (z. B. durch Asbest) oder systemischen Immunsuppression. Ein neuer Ansatz zur Behandlung dieser Erkrankungen basiert deshalb auf der Hemmung exzessiver Signalübertragungen und dem darauf folgenden Anstieg der cGMP/cAMP-ratio bei immunkompetenten Zellen. Therapie: Nach den heutigen Erkenntnissen der immunologischen Reaktionen ist es unabdingbar bei chronischen Erkrankungen ein exaktes Immunmonitoring durchzuführen. Nur so gelingt eine Einschätzung über den Ist-Zustand der Immunantwort auf mögliche Einflussgrößen, Blockaden oder regulatorische Deffizienzen. Auch ergibt sich oft eine Aussage über einen permanenten Einfluss wie einer Mykose, Toxinen und anderer antigener Reize. Um regulatorisch auf die verstellte Immunantwort einzuwirken gibt es heute eine Vielzahl von Möglichkeiten. Neben der Substitution von Spurenelementen und der unspezifischen Immuntherapie mit bakteriellen, viralen und substanziellen Immunmodulatoren kennen wir spezifische Wege, um die harmonische Immunantwort wieder herzustellen. Der erste Schritt einer Immuntherapie z.B. in der Onkologie ist deswegen nicht selten die Deblockierung in den Subpopulationen der Lymphozyten über die TH3 positiven Zellen. Mit Substanzen, die spezifische Rezeptorwirkung haben, werden unspezifische Signale in der Immunantwort ausgefiltert. Geeignet hierfür sind beispielsweise Beta-Blocker, Calcium Antagonisten, H2 Rezeptoren, Alpha Blocker und Prostaglandin-Synthese Hemmer. Entscheidend ist nach einer Blockade die Verhinderung der Gegenregulation durch die Beeinflussung intrazellulärer ph-Spiegel, so dass eine Alkalisierung auf diesem Weg für längere Zeit sinnvoll erscheint. Betablocker und Ca-Überladungsblocker Die Hemmung der exzessiven („Hintergrund-") Signale kann z. B. durch Ca++ Überladungsblocker erreicht werden. Der Abfall von cAMP bzw. der Anstieg von cGMP/ cAMP kann durch niedrig dosierte Betablocker bewirkt werden. Die Kombination von Betablockern mit Ca++-Überladungsblockern in dieser Indikation ist bereits patentiert und hat in ersten Versuchsreihen gute Ergebnisse erzielt. Von besonderem Interesse sind dabei Ca++-Überladungsblocker vom Piperazin-Typ, besonders Cinnarizin, wegen ihres inhibitorischen Einflusses auf sowohl Ca2+- als auch Na+Kanäle. Mit der reversiblen Hemmung von Na+-Kanälen tragen Ca++-Überladungsblocker wie Cinnarizin zu einer teilweisen Membranrepolarisation und somit zu einer höheren Selektion für immunrelevante Signale bei. Sie antagonisieren die Aktionen von Histamin, Serotonin, Katecholaminen, Vasopressin, Angiotensin, Dopamin und Bradykinin und helfen, einen hyperaktivierten Status immunkompetenter Zellen, der durch exzessive spezifische und unspezifische („Hintergrund") Signale entsteht, zu vermeiden. Von Vorteil ist auch die vaskuläre Selektivität von Cinnarizin, durch die etwaige kardiale Nebenwirkungen entfallen. Für Propranolol sprechen seine Beta-1 und Beta-2 Adrenorezeptorspezifität sowie seine partiell inhibitorische Wirkung auf Na+Kanäle. Es zeigte sich eine erhöhte Wirksamkeit der Substanzen im alkalischen Milieu. In vorläufigen klinischen Einzelbeobachtungen konnte mit oben genannten Substanzen innerhalb von Wochen eine deutliche Verkleinerung von großen Primärtumoren und ausgeprägten Metastasen erreicht werden. In der Durchflußzytometrie zeigte sich dabei eine parallele Abnahme von HLA-DR+ (Kennzeichnung von hyperaktivierten T-Zellen in der FACSAnalyse), ein Abfall CD8-positiver Zellen (= Suppressor-T-Zellen) sowie ein verzögert zu beobachtender, klarer Trend zur Normalisierung der signifikant supprimierten HelferSuppressor-ratio der T-Zellen (Th/Ts ratio). Obwohl erst vorläufige klinische Einzelergebnisse vorliegen, sind diese von theoretischem und praktischem Interesse: Sie demonstrieren deutlich, daß beispielsweise die Tumorgröße ohne gleichzeitige Chemo- oder Radiatiotherapie durch Deblockade selektiv überstimulierter Effektorzellen reduziert werden kann. Selbst ausgeprägte Tumoren scheinen in einem permanenten dynamischen Gleichgewicht mit dem Immunsystem zu stehen. Sowohl die frühe Etablierung als auch das Tumorwachstum reflektieren eine geschädigte Immunüberwachung. Die dargestellten immunologischen Regulationsmechanismen zeigen, wie vielfältig vernetzt die Informationsübertragungen und -Signale innerhalb immunkompetenter Zellen sind. Als therapeutische Konsequenz hinsichtlich der Kenntnisse der Regulationsmechanismen bleibt die Hoffnung, initial mit therapeutischen Impulsen einzelne Regulationskreise anregen zu können, um so eine fortlaufende Information auf das Immunsystem zu übertragen. Da sich viele dieser Regelkreise selbst kontrollieren, besteht die Chance, das System durch Anregung in eine grundsätzlich immunologisch ausgewogene Situation zu bringen. Matrix- und Grundregulation Bedeutende Forschung zu Matix- und Grundregulation hat neben Pischinger besonders Prof. Dr. rer. nat. med. habil. Hartmut Heine durchgeführt. Er zitiert zu diesem Thema zusammenfassend: Das System der Grundregulation stellt die wissenschaftliche Basis der biologischen Medizin (Ganzheitsmedizin) dar. Der Begriff der Ganzheit liegt im kleinsten funktionellen Nenner des Organismus auf den alles bezogen werden kann: der Trias Endstrombahn (Kapillaren, Lymphgefäße), Molekularsieb der ECM (extrazelluläre Matrix) und nachgeschaltete Zellen. Über die Endstrombahn sind die endokrinen Drüsen, über die blind in der ECM endigenden vegetativen Nervenfasern das zentrale Nervensystem zugeschaltet. Beide Systeme sind im ZNS miteinander verschaltet. Auf diese Weise ist die Einheit von Körper, Geist und Seele gegeben. Unser modernes Leben greift vielfältig störend in diese Beziehungen ein. Hier ist jeder Einzelne gefordert seine Verantwortung im Erhalt bzw. in der Regeneration der Grundregulation wahrzunehmen. Dies verlangt eine bewusste Lebensordnung und -führung. (Heine 2007) Immunologische spielt die Matrix eine entscheidende Rolle bei jeder Art von Immunantwort. Durch das feine Netz der Grundsubstanz, also der Matrix, werden alle entscheidenden Substanzen, die dem Körper zugeführt werden, gefiltert und dann entsprechend immunologisch beantwortet. Ist die Matrix überladen, z.B. durch Viren, Bakterien, Pilze oder auch anderen Antigenen aus Nahrungsmitteln, kommt es zur Immunblockade und pathologischen Regulation entsprechender T-Lymphozyten, Helfer-, Suppressor-, TH1, TH2 Lymphozyten. Auch die Phagozytose wird stark beeinträchtigt. Aus diesem Grunde ist es von entscheidender Bedeutung, die Matrix zu säubern. Dafür sind ausleitende Verfahren besonders geeignet. Besonders gut erforscht ist dabei Matricell, eine Kombination aus Gelee Royal (Bienenweisel-Saft), Propolis (Bienenkittharz) und enzymatische aufgeschlossenen Blütenpollen in Honigwein. Eine Therapie von bis zu vier Monaten kann eine erhebliche Reinigung und ein cleaning der Grundsubstanz bewirken. Die Flexibilität der Immunantwort wird wieder hergestellt. Ähnlich wirken Enzyme und phagozytosesteigernde Präparate und ausleitende Verfahren der Naturheilkunde. Weitere immunologisch wichtige Substanzen zur Regulierung der T3, TH1, TH2 Zellen sind Vitamin-/Spurenelemente. Zink Zink hat einen entscheidenden Einfluss bei der Replikation von DNA, RNA und der Biosynthese von Proteinen. Metallionen sind an der Stabilisierung der Ribosomen, der Stabilität der RNA und dem Einbau der Aminosäuren in die wachsende Proteinkette beteiligt. Somit sind sie für die Produktion von Antikörpern, Immunzellen und auch für die Phagozytose Leistung wichtig. Bei Zinkmangel treten auf: Immunregulationsstörung durch vermehrte Helfer- und verringerte Suppressorzellen. Symptome bei Zinkmangel sind - Immunregulationsstörung durch vermehrte Helfer- und verringerte Suppressor-Zellen - Abnahme der immunologischen Aktivitätspotentiale (Zink ist polyklonaler T-Zell-Aktivator) - Abfall der Gesamt-Lymphozytenzahl - Abnahme der Antikörperproduktion und der NK-Zellzahl - Abnahme der Phagozytoseleistung, der Komplementaktivierung sowie der Interleukin-2Sekretion - Abnahme der T- und B-Lymphozyten - Zunahme viraler Infektanfälligkeit - Leukosen - maligne Erkrankungen. Magnesium, Kalzium Magnesium und/oder Kalzium sind wichtige Elemente, die bei allen schnell ablaufenden energetischen Prozessen der Zelle benötigt werden. So steuern sie die Basenpaarung bei der DNA und RNA Synthese und haben Einfluss auf die Packungsdichte des Chromatins im Zellkern und die aktivierten Immunkompetenten Zellen in der schellen Umwandlungsphase. Dabei sind Metalle und besonders Magnesium und Kalzium die Zwischenglieder der Signalübermittlung von der Zellmembran zum Zellkern. Außerdem aktivieren sie ca. 300 Enzyme im Kohlenhydrat-, Fett und Eiweißstoffwechsel, regulieren die Perma abilität der Zellmembran und das Mitochondrium, steuern die Proteinsynthese im Zellkern und beeinflussen DNA und RNA Synthese. Schon gering erniedrigte Magnesium und/oder Kalzium Spiegel blockieren die Immunzellaktivierung. Dies führt nicht nur zum Aktivitätsverlust der Immunzellen, sondern es erfolgt ein Abfall von IgG, eine Erhöhung von IgE und eine unspezifische Komplementaktivierung. Selen Selen zeigt direkten Einfluss auf die Subpopulationen der Lymphozyten. Unter Selensubstitution bei Selenmangel wird die vorher erhöhte Anzahl der Suppressor-Zellen gesenkt und das Immunsystem in eine funktionell bessere Lage gebracht. Selen hat entscheidende Konsequenzen für die humorale und zelluläre Abwehr. So finden sich - Zerstörung von Hydroxyl- und Peroxylradikalen (Schutz von Zellmembranen). - antimutagene Wirkung. - Schutz vor Chromosomenschäden. - Entgiftung von Schwermetallen (Cd, Hg, Pb, Ag u.a.), - Schutz vor Alkylierungsmittel. - Stimulierung der Immunabwehr - Schutz vor Strahlenwirkungen - Leberschutz - Erhöhung der Resistenz gegen bestimmte Viren und andere pathogene Substanzen - Stimulierung des Mikroblutkreislaufs. Die Wirkung des Selens ist dosisabhängig. Bei Überdosierung kommt es zu einer Hemmung verschiedener Immunreaktionen. Anhand der physiologischen Selenwirkungen kann aber eindeutig eine immunologisch aktive Wirkung aufgezeigt werden. Dabei dominiert insbesondere der Zellschutz durch die Radikalfängereigenschaften, die Entgiftung von Schwermetallen, die immunkompetente Zellen schädigen können, und die direkte Stimulierung der zellulären Abwehr. Der Schutz vor Strahleneinwirkungen bringt einen Schutz in der Primärdifferenzierung von immunkompetenten Zellen aus Stammzellen. So erklären sich auch die antimutagene Wirkung und der Schutz vor Chromosomenschäden. Selen stimuliert die Prostaglandinbiosynthese, die ebenfalls auf das Immunsystem wirkt. Bei Selenmangel treffen folgende Störungen auf: - vermehrte Karzinomanfälligkeit - Immundefizienz - höhere allergische Disposition, besonders gegen Chemikalien - Verminderung von Coenzym Q - Verminderung der Entgiftungskapazität von Schwermetallen - verringerte Natural-Killer-Zell-Aktivität - verringerte Makrophagenaktivität - verringerte Antikörpersynthese (besonders IgG 4) - verringerte T-Helfer-Zell-Aktivität - verringerte Gamma-Interferonsynthese. Lithium Neuere Untersuchungen über Lithium beweisen einen direkten Einfluss auf das Immunsystem. Lithium hat einen positiven Effekt auf den Granulozyten-MakrophagenStimulationsfaktor und wirkt direkt leukozytenstimulierend. Einige experimentelle Untersuchungen beweisen den direkten Einfluss von Lithium auf die Immunhomöostase des menschlichen Organismus. Erst unter Lithiumgabe wird bei endogenen Psychosen eine ausreichende Produktion der Lymphokine beobachtet. Dies spricht für eine Wiederherstellung der Immunfunktionen. Memo Vitamine und Spurenelemente sind von entscheidender Bedeutung in der Funktionsfähigkeit des zellulären Abwehrmechanismus. Genauere Untersuchungen über die Wirkung einzelner Vitamine und Spurenelemente auf das humorale und zelluläre Abwehrsystem liegen nicht vor. Nachgewiesen sind lediglich die Radikalfängereigenschaften von Vitaminen und Spurenelementen, die Zellmembranen vor Schäden durch Radikale schützen können. Unter diesem Aspekt sind Vitamine und Spurenelemente für eine normale immunologische Funktion von größter Bedeutung, da die meisten Erkennungsmechanismen und Abwehrleistungen über Membranrezeptoren und deren Bestandteile ablaufen. Entscheidenden Einfluss haben Vitamine und Spurenelemente auch auf die Aminosäuresynthese, die als grundsätzliches Element bei der Bildung von kompetenten Immunantworten benötigt wird. Elimination von Toxinen Giftwirkung von Schwermetallen Folgende Metalle sind relevant: Blei: - schädigt die Erbsubstanz und Keimdrüsenfunktion, - schädigt das Immunsystem, - schädigt die Enzyme, -verändert das Blutbild und fördert die Bildung der normochromen Anämie. Cadmium: -kumuliert bevorzugt im Kortexanteil des Nierengewebes (Halbwertzeit 30 Jahre), - stört die Enzymfunktionen, - fördert die Infektanfälligkeit, - begünstigt die Tumorentstehung. Quecksilber: - wirkt toxisch auf Zellmembranen, - wirkt suppressiv auf das Knochenmark, - stört Rezeptoren an Zelloberflächen, - fördert allergische Reaktionen, - verringert die T-Helfer-Zell-Zahl, - verändert die Zahl der B-Lymphozyten, - erhöht Immunglobulin G. Platin: - wirkt toxisch, - fördert Allergien, - führt zu pathogenen Immunreaktionen (Konjunktivitis, Rhinitis, Husten, Asthma), - erhöht das Lungenkrebsrisiko, - führt zu Ekzemen, - fördert die Entwicklung zu Leukämien, - wirkt knochenmarkdepressiv. Literatur: Heine H.: Die extrazelluläre Matrix als Attrektor für Verschlackungsphänomene. Ärztezeitschrift Naturheilverfahren 2005 Heine H, Andrä F.: Anregung der immunologischen Beistandsreaktion mit Bienenprodukten und aufgeschlossenem Blütenpollen. Erfahrungsheilkunde 2006 : Heine H.: Lehrbuch der biologischen Medizin. Grundregulation und Extrazelluläre Matrix. 3. Auflage. Hippokrates Verlag, Stuttgart 2006 (ISBN 3-8304-5335-3). Heine H.: Die Grundregulation – Schaltstelle für Gesundheit und Krankheit 2. Auflage. Hippokrates Verlag, Stuttgart 2007 (ISBN 978-3-00-023052-3) Worlitschek M., Inderst R.: Verbesserung von Befindensstörungen und des Leistungsvermögens durch Entsäuerung der extrazellulären Matrix. Anwendungsbeobachtung mit einem Multi-Target-Nahrungsergänzungsmittel. Erfahrungsheilkunde 2006 Schleicher P.: Immunologie – Ein System, das Leistung schafft ISU e.V., Mai 2007 Schleicher P.: Innundiagnostik und –therapie 2. Auflage. Hippokrates Verlag, Stuttgart 1997 (ISBN 3-7773-1064-7) Schleicher P.: Zur Frage der Immundiagnostik in der ärztlichen Praxis Therapeutikon 5, 1988 Dostal V., Bayer W., Schleicher P., Schmidt K.H.: Immunmonitoring und additive Immuntherapie, Hippokrates Verlag, Stuttgart 1990 (ISBN 3-773-0819-6) Dostal V., Schleicher P., Tiran B., Schager G., Steiner C.: Immunstatus – Immunmonitoring, Fa. Behring Institut Wien, 1989 Schleicher P.: Der Immunkompass, Verlag das Neue Berlin 2004, (ISBN 3-360-01236-4) Praxis für Immunologie Dr. med. Peter Schleicher Dorothea Brückl Ismaningerstr. 65 81675 München Tel. 089 41 94 53 0 www.praxis-schleicher.de