Neuro - MedUni Wien
Werbung

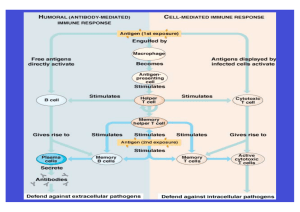
NEUROIMMUNOLOGIE 1. Immunologische Grundlagen mit Bezug zur Neurologie 2. Neuroimmunologische Erkrankungen 2.1. Beispiel für eine Erkrankung des Zentralen Nervensystems: MULTIPLE SKLEROSE ; Tiermodell: chronische experimentelle autoimmune Enzaphalomyelitis 2.2. Beispiel für Erkrankung des Muskels / der neuromuskulären Synapse: 2.2.1. MYASTHENIA GRAVIS; 2.2.2. LAMBERT-EATON-MYASTHENES-SYNDROM Tiermodell: Passivtransfer-Modell (systemische oder lokale Wirkung von IgG-Antikörpern im Tiermodell) 2.3. Beispiel für Erkrankung des Peripheren Nervensystems: GUILLAIN-BARRÉ-SYNDROM ; Tiermodell: experimentelle autoimmune Neuritis Prionenerkrankungen 1. Immunologische Grundlagen mit Bezug zur Neurologie Zelluläre Elemente: Mikrogliazellen, Astrozyten, Oligodendrozyten, Neuron, Endothelium Mastzellen, T-Lymphozyten, B-Lymphozyten Humorale Träger des Immunsystems: Immunglobuline: durch Blut-Liquor-Schranke und Blut-Hirn-Schranke in das ZNS Verteilung der Immunglobuline im Liquor ist wie im Serum polyklonal. Im pathologischen Fall: ZNS-eigenen IgG-Produktion -->Konzentrationserhöhung von Gesamt-Ig und zur oligoklonalen Verteilung Komplementsystem: - Myelin (im zentralen und peripheren NS): Komplementaktivierung - eingewanderte Makrophagen - Mikroglia - Astrozyten: wesentliche Quellen für Komplementfaktoren Kooperation zw. immunkompetenten Zellen über Zytokine: -Zytokine: von einer Vielzahl von Zelltypen, wie Makrophagen, T-Zellen aber auch von Endothelzellen, Astrozyten und Mikroglia an Entzündungsorten freigesetzt - Rezeptoren für Zytokine: gliale und neuronale Strukturen des NS Lymphozytenwanderung: Beispiel: Einwanderung von T-Zellen aus dem Blut in das ZNS durch die Blut-Hirn-Schranke (Homing- und Migrationsprozeß) Immungenetik: Immunpathologische Effektormechanismen: Typ I: spielen in der Neuroimmunologie keine bekannte Rolle Typ II: Myasthenia gravis Typ III: Immunvaskulitis Typ IV: postvakzinalen Erkrankungen des zentralen und peripheren NS; wahrscheinlich auch bei der multiplen Sklerose 2. Neuroimmunologische Erkrankungen 2.1. ZENTRALES NERVENSYSTEM: MULTIPLE SKLEROSE (Enzephalomyelitis disseminata) Definition: Multiple Sklerose (MS):schubförmig oder chronisch progredient verlaufende, multifokale, entzündliche Entmarkungskrankheit; im Gehirn und Rückenmark: multiple Entmarkungsherde unterschiedlicher Größe; Die Entmarkungsherde sind durch einen kompletten Verlust der Myelinscheiden (Isolierschicht der Nervenfasern) gekennzeichnet. Die MS ist charakterisiert durch Entzündung, Demyelinisierung und Gliose. Faktoren: Pathologie: - Ätiologie nicht gesichert -Viele Beobachtungen stammen aus dem Tiermodell, der experimentellautoimmunen Enzephalomyelitis (EAE), und epidemiologischen Studien (Migrationsstudie). -Zerstörung der Myelinscheiden in den MS-Herden: auf Basis einer chronischen bzw. schubförmigen Entzündungsreaktion im ZNS -MS-Herde: zelluläre Infiltrate mit T-Zellen, B-Zellen und Makrophagen Æ TLymphozyten mediierte Immunreaktion - Durch T-Zellen aktivierte Makrophagen und Mikrogliazellen sind für die Zerstörung des Myelins verantwortlich. Gewebeschädigend: von Makrophagen und Mikroglia freigesetzte zytotoxischen Produkte - Antikörper gegen Myelinbestandteile Æ Entmarkung ; Antikörper: im Serum von MS-Patienten gegen zahlreiche Virusantigene (vor allem gegen Masernvirus) und gegen Myelinproteine; „molecular mimikry“ - im Liquor cerebrospinalis : entzündliche Reaktionen mit lymphozytärer Pleozytose und eine verstärkte Immunglobulinproduktion durch eine begrenzte Zahl von B-Zellklonen; Nachweis "Oligoklonaler Banden" (IgG) im Liquor - im Blut: gegen Markscheidenantigene gerichtete T-Zellen, die MHC-restringiert immundominante Epitope erkennen - im Schub: Nachweis im Blut und Liquor von proinflammatorische Th1-Zytokine - im Schub: vermehrte Zirkulation im Blut und Liquor von löslichen Adhäsionsmolekülen (Hinweis auf T-Zellmigration) Pathogenese der MS: MS wird als Autoimmunerkrankung des ZNS angesehen. Tiermodell für MS: Experimentelle autoimmune Enzephalomyelitis (EAE): Therapie der Multiplen Sklerose: 2.2. MUSKEL / NEUROMUSKULÄRE SYNAPSE (MYASTHENIA GRAVIS, LAMBERT-EATON-MYASTHENES SYNDROM) 2.2.1. MYASTHENIA GRAVIS: Definition: Myasthenia gravis (MG): Erkrankung der motorischen Endplatte (erste gesicherte neurologische Autoimmunerkrankung mit molekular definierten Autoantigenen) Krankheit, bei der Autoantikörper gegen Azetylcholinrezeptoren der motorischen Endplatte eine progressive Muskelschwäche verursachen. Ätiopathogenese: Die immunpathologische Reaktion folgt dem Typ II. - Autoantikörper gegen nikotinischen Acetylcholinrezeptor (AChR), der auf Skelettmuskelzellen der neuromuskulären Endplatten vorkommt, führen zu einer Schädigung der postsynaptischen Muskelmembran. --> Blockierung der Signalübertragung (--> progressive Muskelschwäche) Tiermodell: - Immunisierung von Ratten oder Mäusen mit gereinigten Acetylcholinrezeptoren: Auslösung einer Krankheit, die Ähnlichkeiten mit der Myasthenia gravis aufweist (experimentell induzierte Krankheit) -adoptiver Transfer der gebildeten Antikörper gegen Azetylcholinrezeptor auf normale Versuchstiere --> Auslösung der Krankheit -Interessanterweise gelingt dieser adoptive Transfer unter gewissen Versuchsbedingungen auch mit Acetylcholin-Rezeptor-spezifischen CD4+ TLymphozyten. Immundiagnostik: Nachweis der Antikörper gegen den nikotinischen Acetylcholinrezeptor im Serum mittels Doppel-Immunpräzipitationstests Therapie: - Cholinesteraseinhibitoren - Immunsuppression: Corticosteroide und Azathioprin; bei Therapieresistenz alternativ oder zusätzlich: Cyclosporin A - bei myasthenen Krisen Immunadsorption * (Säulen) oder ggf. bei Kontraindikation auch hochdosierte intravenöse Immunglobuline; - Thymektomie * Immunadsorption: Alternative zur Plasmapheresetherapie: selektive Immunadsorption 2.2.2. LAMBERT-EATON-MYASTHENES SYNDROM Definition: Lambert-Eaton-myasthenes Syndrom: Autoimmunerkrankung der neuromuskulären Synapse; primäre physiologische Störung: verminderte Freisetzung des Neurotransmitters Acetylcholin aus den Nervenendigungen in den Synaptischen Spalt Ätiopathogenese: - Bei 70% aller Patienten tritt diese Krankheit als paraneoplastische Erkrankung bei kleinzelligem Bronchialkarzinom auf. -häufig mit autonomen Störungen und anderen Autoimmunerkrankungen verknüpft - humoral vermittelte Autoimmunkrankheit mit zirkulierenden IgG-Autoantikörpern gegen präsynaptische spannungsabhängige Calciumkanäle, die sich an den Freisetzungsstellen für den Neurotransmitter Acetylcholin befinden Immundiagnostik: Nachweis der Antikörper gegen spannungsabhängige Calciumkanäle durch Immunpräzipitationsassays Immuntherapie: -Lambert-Eaton-Syndrom assoziiert mit kleinzelligem Bronchialkarzinom: Therapie des Tumors; Entfernung des Tumors -3,4-Diaminopyridin (Wirkung auf L-Typ-Calciumkanäle; Steigerung der Acetylcholinausschüttung) - Immunsuppression mit Corticosteroide und Azathioprin - Plasmapherese 2.3. PERIPHERES NERVENSYSTEM GUILLAIN-BARRÉ-SYNDROM (Synonym: Akute Polyradikuloneuritis) Definition: Guillain-Barré-Syndrom: wahrscheinlich eine heterogene Krankheitsgruppe mit ähnlichem klinischem Phänotyp und Liquorbefunden, aber mit unterschiedlichen neurophysiologischen Funktionsstörungen, verschiedenen pathologischen Veränderungen im Nerv und vermutlich auch distinkter Pathogenese; Von der akuten ist eine chronische Verlaufsform zu unterscheiden. "Autoimmuner Angriff" auf zelluläre Strukturen (Schwann Zelle) --> resultierend in einer Demyelinisierung und / oder Axonverlust. Ätiopathogenese: - Ursache unbekannt - Assoziation zwischen dem Guillain-Barré-Syndrom und einer vorangegangenen Campylobacter jejuni (gramnegative Enterobakterium) Infektion - molekulare Mimikry - Nachweis von Antikörper gegen Ganglioside im Serum auch Antikörper gegen Myelinproteine P0 und P2, deren pathogene Bedeutung unklar ist - Bedeutung T-Zell mediierter Mechanismen ? Immunpathologische Reaktionen bei Guillain-Barré-Syndrom Tiermodell: Experimentell-autoimmune Neuritis: - Immunisierung mit Markscheidenproteinen P0 und P2 Æ Auslösung von einer akuten Nervenentzündung - Verwendung von antigenspezifischen T-Zellinien - morphologisch: zelluläre Infiltrate und Entmarkung peripherer Nervenfasern Immundiagnostik: - 15-30% aller Patienten : Nachweis von Antikörper der Klassen IgG, IgM und IgA gegen GM1 und verwandte Glykolipide bei etwa 30%: serologische Hinweise auf eine rezente Infektion (insbesondere IgAAntikörper gegen Campylobacter jejuni –Membranproteine oder Lipopolysaccharid) im akuten Stadium: im Serum und Liquor aktivierte Komplementkomponenten sowie Zeichen einer T-Zellaktivierung und T-Zellmigration Therapie: - Plasmapheresetherapie und intravenöse IgG-Gabe - immunsuppressive Therapien Prionenerkrankungen Empfohlene Literatur: - Neurologie Karl F. Masuhr ,Marianne Neumann - Praxis der Neurologie Klaus Kunze Kapitel Immunpathologie und Immuntherapie (Neuroimmunologische Krankheiten) - Abul K. Abbas, Andrew H. Lichtman, Jordan S. Pober IMMUNOLOGIE (Übersetzt von Beda M. Stadler und Max Hess) -Charles A. Janeway, Paul Travers, Mark Walport, Mark Shlomchik IMMUNOLOGIE -Cotran, Kumar, Collins; Robbins PATHOLOGIC BASIS OF DISEASE -Brostoff, Scadding, Male, Roitt CLINICAL IMMUNOLOGY