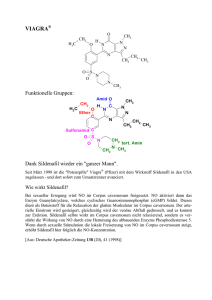
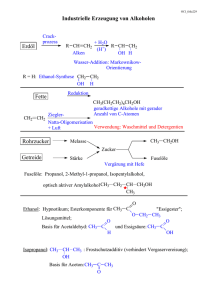
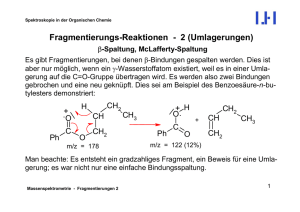
Prof. Peter Hofmann
Werbung

Prof. Peter Hofmann Übungsaufgaben (IV) zur Zyklusvorlesung „Reaktionsmechanismen in der Organischen Chemie“ WS 00 / 01 1. Wie würden Sie die folgenden Umwandlungen möglichst einfach bewerkstelligen? Klassifizieren Sie die vorgeschlagenen Reaktionen genau. O O H H Cl O CHCl CO2CH3 Ph Ph Cl H Cl 2. Schlagen Sie einen Mechanismus für die nachstehende Reaktion vor. CH3 CH2 Cl HCl C CH2 - 70 °C Cl CH3 3. Sagen Sie Regioselektivität und Endprodukt der folgenden Cycloaddition vorher. H N C N2 H3CO2C + ? 4. Welches Bild würden Sie für die graphische Auftragung von log k – Werten der Diels-Alder-Reaktionen (Ordinate) unterschiedlicher, elektronenreicher Diene mit Tetracyanoethylen oder Maleinsäureanhydrid gegen die Differenz von 1. Ionisierungsenergien der Diene und der Elektronenaffinität der beiden Dienophile erwarten (Abszisse)? Begründung? 5. Unter welchen Reaktionsbedingungen würden Sie die nachstehend gezeigte Umwandlung versuchen, wenn der stereochemisch entscheidende Schritt eine elektrocyclische C-C-Verknüpfung sein soll? O O 6. Welche Stereochemie erwarten Sie für das Produkt der folgenden N 2Abspaltung, wenn es sich um einen linearen cheletropen Prozess handelt? Entwickeln Sie ein MO-Korrelationsdiagramm. CH3 N N CH3 7. Erklären Sie anhand des Reaktionsmechanismus, warum der Aldehyd A bei der Umsetzung mit Bu3SnH in Gegenwart von AIBN das Produkt B, nicht aber C bildet. CH2 CHO I (CH2)3 A CH CH2 CH CH2 OH CH3 H B C O 8. Versuchen Sie den mechanistischen Verlauf der folgenden Reaktion abzuleiten. (Es handelt sich um die sog. Hofmann-Löffler-Reaktion). 1.) NaOCl 2.) H2SO4 / h N H N 3.) OH 9. Wie kann man Benzyl-tbutylketon aus Brombenzol und einem geeigneten Reaktionspartner in einer einstufigen Synthese darstellen? 10. Erklären Sie, wie aus Cyclohexanon durch Bestrahlung Hexenal-5 entstehen kann. Rm_ps4.doc