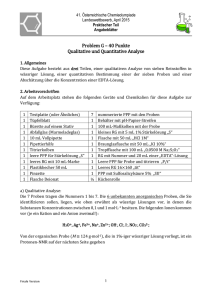
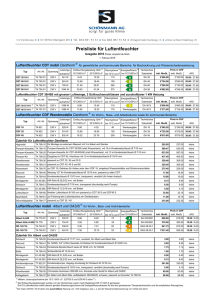
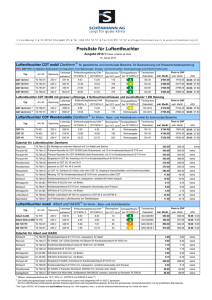
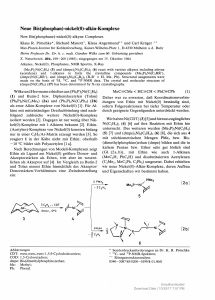
Synthese und Struktur von Ni(2 ,6 -/Pr2 C6 H3 N =CH
Werbung

Synthese und Struktur von Ni( 2 ,6 -/Pr2 C6 H 3 N = C H -C H = N C 6 H 3 - 2 , 6 -/Pr2 ) 2 Synthesis and Structure of Ni(2,6-'Pr2C6H 3N = C H -C H = N C 6H 3-2,6-'Pr2)2 Werner Bonrath, Klaus R. Pörschke*, Richard M ynott und Carl Krüger Max-Planck-Institut für Höhlenforschung, Postfach 10 13 53. D-4330 M ülheim a.d. Ruhr Z. Naturforsch. 45b, 1647- 1650 (1990); eingegangen am 30. April 1990 1,4-Diazadiene, Nickel(O), X-Ray Ni(cdt)** reacts with two equivalents o f the sterically highly demanding 1,4-diazadiene , -'Pr2 C 6 H 3N = C H -C H = N C 6 H 3 - 2 ,6 -'Pr2 to yield the red-brown, crystalline title compound Ni(2,6-'Pr 2 Ph-dad ) 2 (3). The existence o f this com pound was previously uncertain. 'H and l3C N M R , MS, and UV/VIS spectra o f 3 are reported. The X-ray structure analysis o f 3 revealed a strongly distorted tetrahedral coordination o f the nickel center with a dihedral angle o f 51 between the planes of the chelate rings and mean bond lengths N i - N 1.965(4) A and N = CH 1.308(5) A. The poorly soluble com pound appears to be rather unreactive because o f the bulk o f the ligands. 2 6 Nach tom Dieck e t al. lassen sich durch R eduk­ tion von NiBr2 mit Natrium oder aus Ni(cod)2 un­ ter cod-Verdrängung mit der bimolaren Menge N,N'-disubstituierter 1,4-Diazadiene RN = CHCH = NR (R - z. B. 'Bu, Ch, 2,6Me2C6H 3) zahlreiche Komplexe des Typs Ni(R-dad), herstellen. Kristall-Strukturanalysen ergaben für das dialkylsubstituierte Derivat Ni(ChN = CHCH = NCh)2 (1) eine tetraedrische Koordinationsgeometrie (D2d) [1] und für das diarylsubstituierte Derivat Ni(2,6-Me2Ph-dad)2 (2) eine (nur) D2-symmetrische Koordination des Nickels mit einem Diederwinkel der beiden Chelatring-Ebenen von 44,5 [2]; von anderen Autoren wurde diese Koordinationsform auch als „pseudo­ planar“ bezeichnet [3 a], Offenbar bewirken N,N '^/arv/substituierte 1,4-Diazadiene als sehr starke 7r-Akzeptorliganden eine partielle Oxidation von Nickel(O) und hiermit verbunden eine Verzerrung der Koordinationsgeometrie von tetraedrisch in Richtung quadratisch-planar, wie sie für diamagnetische Nickel(II)-Komplexe angetroffen wird. Die Phenyl-Ringe in 2 sind gegen die jeweilige Ni,N,N'-Chelatringebene gegensinnig um 60 bzw. 72 verdreht; die gegenüberliegenden Phenylringe zweier Liganden sind annäherend planar zueinan­ der ausgerichtet (6 bzw. 12) [2], * Sonderdruckanforderungen an Priv.-Doz. Dr. K. R. Pörschke. ** Abkürzungen: cdt = \,5,9-trans,trans,trans-Cyc\ododecatrien. Ch = Cyclohexyl, cod = 1,5-cis,cis-Cyclooctadien, R-dad = N,N'-disubstituiertes 1,4-Diazadien (R N = CHCH = NR). Verlag der Zeitschrift für Naturforschung. D-7400 Tübingen 0932-0776/90/1200- 1647/$ 01.00/0 Die Umsetzung von Ni(cod)2 mit dem sterisch besonders anspruchsvollen 2,6-'Pr2Ph-dad führt zur Verdrängung nur eines cod-Liganden mit Bil­ dung von (2,6-'Pr2Ph-dad)Ni(cod) [2], Das ent­ sprechende N i(R -dad)2-Derivat 3 ist aus Ni(cod)2 offenbar nicht bzw. aus NiBr2/N atrium nur in Spuren zugänglich [2]; darüber hinaus fand die Verbindung an anderer Stelle Erwähnung mit abweichenden spektroskopischen Angaben [3 b]. Im Rahmen unserer Untersuchungen über neue (dad)Ni(Alken)-Komplexe [4] mit nicht-aktivierten Alkenen und deren Reaktion mit Acetylen [4, 5] erhielten wir aus (2,6-'Pr2Ph-dad)Ni(C2H4)2 und (2,6-'Pr2Ph-dad)Ni(/7v/2- 1,5-Hexadien) mit 2,6-'Pr2Ph-dad den Komplex Ni(2,6-'Pr2Ph-dad)2 (3) in bis zu 90% Ausbeute [4]. Wir berichten hier über die präparativ einfachste Herstellung von 3 ausgehend von Ni(cdt) und seine Charakterisie­ rung einschließlich der M olekülstruktur. Synthese und Spektren von Ni(2,6-'Pr2C6H 3N = CH - C H = N C 6H 3-2,6-'Pr2)2 (3) Die rote Lösung von Ni(cdt) [6] in Ether färbt sich bei Zugabe einer etherischen gelben Lösung der bimolaren Menge 2,6-'Pr2Ph-dad [2] bei 20 C sofort dunkelrot, und nach kurzer Zeit fallen feine rotbraune, bei überstehender Lösung grünschim­ mernde Kristalle von Ni(2,6-'Pr2Ph-dad)2 (3) aus. Nach m ehrstündigem Aufbewahren der Reak­ tionslösung bei - 3 0 °C kann die Substanz mit ca. 80% Ausbeute (in Pentan 90%) isoliert werden. 3 zersetzt sich oberhalb 200 C ohne deutlichen Schmelzpunkt und ist in Ether, Pentan und TH F Unauthenticated Download Date | 8/21/17 7:12 PM 1648 W. B onrath et al. ■Synthese und S tru k tu r von N i(2,6-'P r:C 6H 3N = C H - C H = N C 6H r 2,6-'Pr-,): wenig, etwas besser in Toluol löslich. Eine Suspen­ sion von 3 in Toluol nimmt unter Rühren bei 20 C/1 bar langsam CO auf (2d, 2,8 CO/Ni), wo­ bei im Kondensat der Reaktionslösung Ni(CO)4 (51 °/o) aufgefangen und aus dem Rückstand das freigesetzte 'Pr2Ph-dad (80%, Pentan) kristallisiert werden konnten [7], Eine Reaktion von 3 mit cod zu (2,6-'Pr2Ph-dad)Ni(cod) ließ sich nicht feststellen. Auch gegenüber Alkinen, insbesondere Ethin, zeigt die Verbindung keine Reaktivität, die auf eine leichte Abspaltung eines der beiden sterisch sehr anspruchsvollen 2,6-'Pr2Ph-dad-Liganden in Lösung schließen ließe. Ni(cdt) + 2 2,6-'Pr2Ph-dad Ni(2,6-'Pr2Ph-dad)2 + cdt 3 (1) Im Massenspektrum (70 eV, 190 C) von 3 wird das Molekül-Ion M + 810 (4%; für 58Ni) gefunden; dieses fragmentiert durch Abspaltung eines dadLiganden [(2,6-'Pr2Ph-dad)N i+: 434, 20%]. Im UV/VIS-Spektrum einer 10“ ’ M Lösung von 3 in Benzol (20 °C) erscheinen eine H auptbande /lmax = 511,4 nm (e = 7600 lM ^'cm -1) und eine Neben­ bande bei 768,5 nm (e = 5000 l M 'c m -1) in Ü ber­ einstimmung mit den in Lit. [2] angegebenen Wel­ lenlängen (im Unterschied zu denen in Lit. [3 b]). Das Auftreten zweier intensiver A bsorptionsban­ den soll für Ni(R-dad)2-Komplexe mit einer von tetraedrisch nach planar verzerrten K oordina­ tionsgeometrie charakteristisch sein [1,2] und ist aufgrund von MO-Berechnungen durch unter­ schiedliche Charge-Transfer-Übergänge erklärt worden [3 a]. Im 200-MHz-1H -N M R-Spektrum ([D8]THF, 27 C) von 3 beobachtet man neben nicht aufgelö­ sten Phenylprotonen-Signalen ein Azomethin-Protonen-Signal (<5 9,09) sowie zwei C H M e2-Septetts (5,10, 3,25) und vier M ethyl-Dubletts (1,60, 0,87, 0,64, 0,48). Im 75,5-M Hz-13C-N M R -Spektrum von 3 ([D8]THF, 27 C) werden insgesamt 13 Si­ gnale beobachtet, wobei jeweils nur ein Signal für die Azomethin-Kohlenstoffatome (J 139,7) sowie für die ipso- und /?ar<7-Phenyl-C-Atome (163,1 bzw. 126,4) vorliegen. Somit sind die beiden 2.6-'Pr2Ph-dad-Liganden und in diesen die beiden 2.6-'Pr2C6H 3-N = CH-Hälften äquivalent. In den vier identischen 2,6-'Pr2C6H 3-Gruppen sind jedoch alle C-Atome unterschiedlich (weitere 4 PhenylC-Atom-Signale, zwei Methin-C- und vier Methyl- Signale). Diese Befunde lassen auf eine Einschrän­ kung der Drehbarkeit der sehr sperrigen 2,6-'Pr2CflH 3-Substituenten um ihre Bindungen zu den 1,4-Diazadien-Stickstoffatomen schließen (es ist anzunehmen, daß die Phenylring-Ebenen im Zeitmittel senkrecht zur jeweiligen Ni,N ,N '-K oordinationsebene ausgerichtet sind, siehe Kristall­ struktur). Zudem ist aus den NM R-Daten eine D 2symmetrische K oordination des Nickels durch die beiden 2,6-'Pr2Ph-dad-Liganden zu folgern, da bei coplanar oder senkrecht zueinander stehenden Ni,N,N'-Ebenen weniger 2,6-'Pr2C6H 3-Signale aufträten. Kristall-Strukturanalyse von Ni(2,6-'Pr2C6H 3N = CH - CH = NC6H 3-2,6-'Pr2)2 (3) Zur Bestimmung der Koordinationsgeometrie von 3 wurde eine Kristallstrukturanalyse durchge­ führt, deren experimentelle Einzelheiten in Tab. I zusammengefaßt sind. Atom koordinaten und aus­ gewählte Abstände und Winkel sind in den Tabn. II und III aufgeführt. Die gefundene M olekülgeo­ metrie mit Bezifferung der Atome ist Abb. 1 zu entnehmen. Die M olekülstruktur von Ni(2,6-'Pr2Ph-dad)2 (3) zeichnet sich durch eine kristallographisch be- Abb. 1. Molekülstruktur von Ni(2,6-'Pr2C6H 3N = C H -C H = N C 6H3-2,6-'Pr2)2 (3). Unauthenticated Download Date | 8/21/17 7:12 PM 1649 W . B onrath et al. • Synthese und S tru k tu r von N i(2,6-'P r2C 6H 3N = C H - C H = N C 6H 3-2,6-'Pr2)2 Tab. I. Daten zur Kristallstrukturanalyse von S’* Summenformel M olr Kristallgröße Kristallfarbe Kristallsystem Raumgruppe (Nr.) a b c ß V z ^ber. C52H 72N 4N i 811,9 0 ,1 1 x 0 ,1 4 x 0 ,2 2 mm dunkelrot monoklin C 2 /c (15) 2 4 ,653(2)Ä 9 ,1 4 2 (1 )Ä 2 3 ,172(2)Ä 114,38(1)° 4756,8 A 3 4 1,13 g ern"3 8,28 cm -1 1,54178 Ä co,126 20 °C H für C u -K a W ellenlänge k Meßmethode Meßtemperatur N onius C A D -4 Diffraktometer gemessene Reflexe (± h ± k + l) 9417 unabhängige Reflexe 4788 beobachtete Reflexe (I > 2,0er(I)) 2913 verfeinerte Parameter 258 R 0,062 /?w( w = 1/ct2 (Fo)) 0,063 max. Restelektronendichte 0,25 e Ä ' 3 Strukturlösung durch Schweratommethode W asserstoffatome der Methylgruppen berechnet, nicht verfeinert H-Temperaturfaktoren fixiert (0,05 A 2) * Weitere Einzelheiten zur Kristallstrukturuntersuchung können beim Fachinformationszentrum Karls­ ruhe, Gesellschaft für wissenschaftlich-technische In­ formation mbH, D-7514 Eggenstein-Leopoldshafen 2, unter Angabe der Hinterlegungsnummer CSD 54704, der Autoren und des Zeitschriftenzitats angefordert werden. dingte zweizählige Achse aus, die durch das N ik­ keiatom verläuft und die Bindungen C (13)C(13*) sowie C(14)-C(14*) halbiert. Die K oordi­ nationsgeometrie des Zentralatom s entspricht der Ligandenanordnung im 2,6-Me2Ph-dad-Kom plex 2 [2], jedoch beträgt der Diederwinkel der beiden Chelatring-Ebenen 51°. Die für 3 im Vergleich zu 2 um 6,5° geringere Verzerrung der K oordinations­ geometrie von tetraedrisch in Richtung quadra­ tisch-planar ergibt sich vermutlich aus einer steri­ schen Behinderung der sperrigen Isopropyl-Substituenten am Aromaten. Die Phenylring-Ebenen stehen mit Diederwinkeln von 82 bzw. 98° nahezu senkrecht zu den zugehörigen N i,N ,N '-K oordinationsebenen. Die mittleren Bindungslängen Ni —N 1,965(4) Ä und N = CH 1,308(5) Ä (2: 1,93 bzw. 1,34 Ä) wie auch die übrigen Bindungsabstände und -winkel entsprechen den Erwartungswerten. Experimentelles Alle Arbeiten wurden unter Ausschluß von Sau­ erstoff und Feuchtigkeit mit Argon als Schutzgas durchgeführt. Ni(cdt) (95-proz., Rest cokristallisiertes cdt) [6] und 2,6-'Pr2Ph-dad [2] wurden nach Literaturangaben hergestellt. 200 M Hz 'H -N M R : Bruker AM-200; 75,5 M Hz 13C-NM R: Bruker WM-300; chemische Verschiebung (<5) relativ zu internem TMS. Elektronenspektren: Cary 2300. N i(2,6-‘Pr2C6H 3N= CHCH= NC 6H r 2,6-iPr2) 2 (3) Die Lösungen von 1,165 g (5,0 mmol) Ni(cdt) und 3,77 g (10.0 mmol) 2,6-'Pr2Ph-dad in jeweils 30 ml Ether werden bei R.T. vereinigt. Sofort färbt sich die Reaktionslösung dunkelrot, und innerhalb 1 h fallen rotbraune Kristalle aus. Der Nieder­ schlag wird abfiltriert, zweimal mit Ether gewa­ schen und im Vakuum getrocknet. Ausbeute Tab. II. A tom koordinaten und äquivalente isotrope Temperaturfaktoren (A 2) mit Standardabweichungen in Klammern3. Atom Ni N (l) N (2) C (l) C(2) C(3) C(4) C(5) C(6) C(7) C(8) C(9) C(10) C ( ll) C (12) C(13) C(14) C (15) C( 16) C(17) C( 18) C(19) C(20) C(21) C(22) C(23) C(24) C(25) C(26) X y 0,0000 0,3708(1) 0,5321(4) -0 ,0 5 8 0 (1 ) 0,2092(4) -0 ,0 3 5 6 (1 ) 0,5492(4) -0 ,1 2 2 0 (2 ) -0 ,1 4 8 0 (2 ) 0,5841(5) -0 ,2 0 9 1 (2 ) 0,6192(6) -0 ,2 4 1 9 (2 ) 0,6220(6) -0 ,2 1 6 0 (2 ) 0,5842(6) -0 ,1 5 5 9 (2 ) 0,5464(5) -0 ,1 2 8 1 (2 ) 0,5126(6) 0,4068(7) -0 ,1 6 4 6 (3 ) -0 ,1 1 5 6 (3 ) 0,6493(9) -0 ,1 1 2 3 (2 ) 0,5889(5) -0 ,1 4 6 0 (2 ) 0,5251(6) -0 ,0 9 3 7 (3 ) 0,7451(7) -0 ,0 3 1 8 (2 ) 0,6598(5) -0 ,0 2 0 1 (2 ) 0,0815(5) 0,1932(4) -0 ,0 7 8 9 (2 ) -0 ,1 3 8 0 (2 ) 0,1599(5) -0 ,1 7 6 2 (2 ) 0,1274(6) -0 ,1 5 5 9 (3 ) 0,1245(7) 0,1600(6) -0 ,0 9 8 7 (3 ) -0 ,0 5 8 1 (2 ) 0,1971(5) -0 ,1 6 0 5 (2 ) 0,1552(6) -0 ,2 2 2 0 (2 ) 0,2213(6) -0 ,1 6 2 0 (2 ) -0 ,0 0 0 6 (7 ) 0,0060(2) 0,2293(6) 0,0139(3) 0,3310(8) 0,0415(3) 0,0909(8) U eq = 1/3 z u eq 0,2500 0,2237(2) 0,1906(1) 0,1908(2) 0,1262(2) 0,0986(2) 0,1339(3) 0,1970(3) 0,2270(2) 0,2972(2) 0,3173(3) 0,3355(3) 0,0864(2) 0,0203(2) 0,0786(3) 0,2350(3) 0,2181(2) 0,1256(2) 0,1133(2) 0,0503(3) 0,0029(2) 0,0169(2) 0,0779(2) 0,1644(2) 0,1436(3) 0,1887(3) 0,0925(2) 0,0455(3) 0,0992(3) 0,032(1) 0,037(2) 0,034(2) 0,041(3) 0,045(3) 0,058(4) 0,065(4) 0,061(4) 0,049(4) 0,062(4) 0,096(6) 0,114(7) 0,056(4) 0,076(5) 0,106(7) 0,061(4) 0,048(4) 0,040(3) 0,048(3) 0,074(4) 0,078(5) 0,071(5) 0,051(4) 0,059(4) 0,081(5) 0,093(6) 0,062(4) 0,119(7) 0,116(7) £j Uy a *a *ä^äy Unauthenticated Download Date | 8/21/17 7:12 PM 1650 W. B onrath et al. • Synthese und S tru k tu r von N i(2,6-'P r2C 6H 3N = C H - C H = N C fiH r 2,6-'Pr2)2 Tab. III. Ausgewählte Bindungsabstände (Ä ) und W in­ kel (°) von 3. N i-N (l) N i- N ( 2 ) N ( l ) —C (l) N (l) -C ( 1 3 ) N (2 )-C (1 4 ) N (2 )-C (1 5 ) C (l) -C ( 2 ) C (l) -C ( 6 ) C (2 )-C (3 ) C (2 )-C (1 0 ) C (3 )-C (4 ) C (4)—C(5) C (5 )-C (6 ) C (6 )-C (7 ) C (7 )-C (8 ) C (7 )-C (9 ) C ( 1 0 ) - C ( ll) C (10)-C (12) C (13)-C (13)* C (14)-C (14)* C (15)-C (16) C (15)-C (20) C (16)-C (17) C (16)-C (21) C (17)-C (18) C (18)-C (19) C (19)-C (20) C (20)-C (24) C (21)-C (22) C (21)-C (23) C (24)-C (25) C (24)-C (26 ) 1,967(3) 1,962(3) 1,452(6) 1,307(5) 1,309(5) 1,451(6) 1,402(7) 1,408(7) 1,410(7) 1,516(7) 1,367(7) 1,377(9) 1,395(7) 1,515(8) 1,519(8) 1,489(9) 1,525(8) 1,533(8) 1,431(7) 1,400(6) 1,396(7) 1,400(7) 1,403(8) 1,503(7) 1,382(8) 1,350(9) 1,395(7) 1,503(8) 1,515(7) 1,538(8) 1,505(9) 1,510(9) N ( 2 ) * - N i- N i( 2 ) N (2 )* -N i- N ( l) N (l) * -N i-N (l) N (2 )-N i- N ( l) C (1 3 )-N (l)-C (l) C (1 3 )-N (l)-N i C (l)-N (l)-N i C (1 5 )-N (2 )-C (1 4 ) C ( 1 5 )-N (2 ) -N i C (1 4 )-N (2 ) -N i C ( 6 ) -C (l)-C (2 ) C (6 )-C (l)-N (l) C (2 )-C (l)-N (l) C (1 3 )* -C (1 3 ) -N ( l) C (1 4 )* -C (1 4 )-N (2 ) C (2 0 )-C (1 5 )-C (1 6 ) C (2 0 )-C (1 5 )-N (2 ) C (1 6 )-C (1 5 )-N (2 ) 82,3(1) 147,1(1) 82,9(1) 106,8(1) 110,4(3) 111,9(3) 137,5(3) 110,9(3) 136,8(3) 112,0(3) 121,3(4) 118,1(4) 120,2(4) 116,6(4) 116,8(4) 122,4(4) 117,8(4) 119,5(4) [1] M. Svoboda, H. tom Dieck, C. Krüger und Y .-H . Tsay, Z. Naturforsch. 36b, 814 (1981). [2] H. tom Dieck, M. Svoboda und Th. Greiser, Z. N a ­ turforsch. 36b, 823 (1981); M. Svoboda, D isserta­ tion, Universität Frankfurt (1978). [3] a) P. C. Servaas, D. J. Stufkens und A. Oskam, In­ org. Chem. 28, 1774(1989); b) P. C. Servaas, D. J. Stufkens und A. Oskam, In­ org. Chem. 28, 1780(1989). [4] W. Bonrath, K. R. Pörschke und S. M ichaelis, A n ­ gew. Chem. 102, 295 (1990); Angew. Chem., Int. Ed. Engl. 29, 298 (1990). 3,13 g (77%). - Bei Durchführung der Reaktion in Pentan ist das Kristallisat feiner; die Ausbeute beträgt bis zu 90%. C 52H 72N 4Ni (811,9) Ber. C 76,93 Gef. C 76,72 H 8,94 H 9,40 N 6,90 N 6,71 Ni 7,23, Ni 7,12. Zers.: >200 °C ohne Schmp.; MS: siehe Text. IR (KBr): v = 1490 c m '1 (N = CH). - 200 MHz 'H -N M R ([D8]THF, 27 °C): Ö = 9,09 (s, 4H , N = CH), 7 ,2 -7 ,0 (m, zusammen 12H, Ph), 5,10, 3,25 (jeweils Septett, 4H , CHM e,), 1,60, 0,87, 0,64, 0,48 (jeweils d, 12 H, C H 3). - 75,5 MHz 13C-NM R ([D*]THF, 40 °C): ö = 139,7 (dd, 4C, ‘/(C H ) = 171 Hz, N = C H -), 163,1 (s, 4C, Ph(>J , 140,15, 138,05 (jeweils s, 4C, Phor, J , 126,4 (d, 4C, P h ^ J , 124,6, 123,75 (jeweils d, 4C, PhmeJ , 29,3, 28,1 (jeweils d, 4C, CHM e,), 26,3, 24,6, 23,9, 23,1 (jeweils q, 4C, C H 3). - Aufgrund der geringen Löslichkeit von 3 enthalten die NM R-Spektren auch Signale von Restmengen cdt und freiem 2,6-'Pr2Ph-dad als Verunreinigungen. R egistrier-N r.: 3 ,7 8 8 0 2 -1 7 -2 [5] W. Bonrath, S. M ichaelis, K. R. Pörschke, B. Gabor, R. M ynott und C. Krüger, J. Organomet. Chem. (1990), im Druck. [6] B. Bogdanovic, M. Kroner und G. Wilke, Liebigs Ann. Chem. 699, 1 (1966). [7] Zur Synthese und Charakterisierung des bei der Reaktion durchlaufenen (2,6-'Pr2Ph-dad)Ni(CO )2: K. R. Pörschke, W. Bonrath und R. M ynott, Inorg. Chem. 29 (1990), im Druck. Unauthenticated Download Date | 8/21/17 7:12 PM