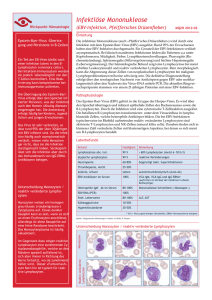
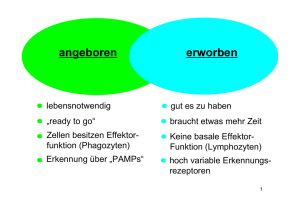
Durchflusszytometrische Analyse von intrazellulären Zytokinen in
Werbung

Aus der Neurologischen Klinik des St. Josef-Hospitals Bochum - Universitätsklinik der Ruhr-Universität Bochum Direktor: Prof. Dr. med. H. Przuntek _________________________________________ Durchflusszytometrische Analyse von intrazellulären Zytokinen in Blut-Lymphozyten von Patienten mit Multipler Sklerose, anderen neurologischen Erkrankungen und gesunden Individuen Inaugural-Dissertation zur Erlangung des Doktorgrades der Medizin einer Hohen Medizinischen Fakultät der Ruhr-Universität Bochum vorgelegt von Thomas Alberti aus Hagen 2004 Dekan: Prof. Dr. med. G. Muhr Referent: Prof. Dr. med. Th. Müller Koreferent: PD Dr. med. E. Sindern Tag der mündlichen Prüfung: 30.11.2004 gewidmet meinem Sohn Silas (* 19.09.2001) Inhaltsverzeichnis Verzeichnis häufig benutzter Abkürzungen 1 Einleitung ……………………..…………………………………………………………. 1 1.1 Das Krankheitsbild der Multiplen Sklerose ………………………………………….. 1 1.1.1 Epidemiologie und Genetik ………………………………………………….…… 1 1.1.2 Exogene Faktoren ………………………………………………………………… 4 1.1.3 Verlaufsformen und Prognose …………………………………………………… 5 1.1.4 Pathophysiologie und -anatomie ………………………………………………... 5 1.1.5 Symptomatik ………………………………………………………………………. 7 1.1.6 Diagnose-Kriterien ………………………………………………………………... 8 1.2 Ausgewählte immunologische Aspekte der Multiplen Sklerose …………….…… 10 1.2.1 Tiermodelle der MS ………………………………………………………………. 1.2.2 Repertoire möglicher Autoantigene beim Menschen …………………………. 10 1.2.3 Die Rolle der T-Lymphozyten …………………………………………………… 1.2.4 Das TH1-/TH2-Paradigma ………………………………………………………… 12 1.2.5 10 11 1.2.4.1 Die Aktivierungsstadien von CD4+ T-Zellen ………………………….. 12 1.2.4.2 Die Zytokine von TH1- und TH2-Zellen ………………………………... 14 Initiierung der Autoimmunreaktion ……………………………………………… 16 1.2.5.1 Wie können naive autoantigenspezifische T-Zellen aktiviert werden? ……………………………………………………………………………. 18 1.2.6 Die Rolle von T-Gedächtnis-Zellen ……………………………………………... 19 1.3 Zielsetzung der Arbeit …………………………………….……………………………… 22 2 Methodik …………………………………………………………………………………. 23 2.1 Auswahl der Patienten und gesunden Kontrollpersonen …………………………. 23 2.2 2.3 2.1.1 Allgemeine Einschlusskriterien ………………………………………………….. 24 2.1.2 Einschlusskriterien in die MS-Patientengruppe ………………………………... 25 2.1.3 Ausschlusskriterien ………………………………………………………….……. 25 Materialien ……………………………………………………………………….…………. 26 2.2.1 Geräte und Gebrauchsmaterialien ……………………………………………… 26 2.2.2 EDV ………………………………………………………………………………… 26 2.2.3 Reagenzien ……………………………………………………………….……….. 27 2.2.4 Antikörper gegen Oberflächenantigene …………………………………….…... 27 2.2.5 ICS-Kits (intracellular staining kits) ……………………………………………... 27 Experimentelle Methodik ………………………………………………………………... 28 2.3.1 Blutentnahme ……………………………………………………………………... 28 2.3.2 Differentialblutbild ……………………………………………………………….… 28 2.3.3 Intrazelluläre Zytokinmessung mittels Durchflusszytometrie ………………… 28 2.3.3.1 Übersicht ……………………………..…………………………..………. 28 2.3.3.2 Schema der Reaktionsansätze ……………………………………….... 30 2.3.4 Spezielle Methodik und Durchführung ………………………………………….. 30 2.3.4.1 Ansetzen der Reagenzien ……………………………….……………… 30 2.3.4.2 Lymphozytenisolierung mittels Ficoll-Gradient …………..…………… 30 2.3.4.3 Zellzahlbestimmung ……………………………………………….…….. 31 2.3.4.4 Stimulation und Sekretionshemmung ……………….………………… 32 2.3.4.5 Fixierung und Permeabilisierung ……………………….……………… 33 2.3.4.6 Intrazellulärer Zytokinnachweis ………………………………………… 33 2.3.4.7 Durchflusszytometrische Messung ……………………..……………… 34 2.4 Auswertungsprotokoll …………………………………………………………………… 39 2.5 Statistische Datenanalyse …………………………………………………….………… 40 3 Ergebnisse …………………………………………………………………….………… 41 3.1 Oberflächenmarker CD45RA und CD45R0 …………………………………………… 41 3.1.1 CD45RA …………………………………………………………………….……… 41 3.1.1.1 CD45RA+ Lymphozyten (Übergruppenvergleich) ………………….… 42 3.1.1.2 CD45RA+ Lymphozyten (Untergruppenvergleich) ……………...…… 3.1.2 42 CD45R0 ……………………………………………………………………………. 42 3.1.2.1 CD45R0+ Lymphozyten (Übergruppenvergleich) ……………….…… 43 3.1.2.2 CD45R0+ Lymphozyten (Untergruppenvergleich) …………………… 43 3.1.3 CD45RA/R0 Ratio ………………………………………………………………… 44 3.1.3.1 CD45RA/R0 Ratio (Übergruppenvergleich) …………….………..…… 44 3.1.3.2 CD45RA/R0 Ratio (Untergruppenvergleich) ………….………….…… 44 3.2 Intrazelluläre Zytokine ……………………………………………………………………. 45 3.2.1 IFN-γ-Produktion …………………………………………………………….…….. 45 3.2.1.1 IFN-γ-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) ….. 45 3.2.1.2 IFN-γ-Produktion in CD4+ Lymphozyten (Untergruppenvergleich) …. 46 3.2.1.3 IFN-γ-Produktion in CD4- Lymphozyten (Übergruppenvergleich) ….. 47 3.2.1.4 IFN-γ-Produktion in CD4- Lymphozyten (Untergruppenvergleich) …. 47 3.2.2 TNF-α-Produktion …………………………………………….…………………… 48 3.2.2.1 TNF-α-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) … 48 3.2.2.2 TNF-α-Produktion in CD4+ Lymphozyten (Untergruppenvergleich) .. 49 3.2.2.3 TNF-α-Produktion in CD4- Lymphozyten (Übergruppenvergleich) … 49 3.2.2.4 TNF-α-Produktion in CD4- Lymphozyten (Untergruppenvergleich) ... 50 3.2.3 Interleukin-2-Produktion ……………………………………………….…………. 50 3.2.3.1 IL-2-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) …… 50 3.2.3.2 IL-2-Produktion in CD4+ Lymphozyten (Untergruppenvergleich) ….. 51 - 3.2.3.3 IL-2-Produktion in CD4 Lymphozyten (Übergruppenvergleich) ……. 51 3.2.3.4 IL-2-Produktion in CD4- Lymphozyten (Untergruppenvergleich) …… 52 3.2.4 Interleukin-4-Produktion ……………………………………………….…………. 52 3.2.4.1 IL-4-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) …… 52 3.2.4.2 IL-4-Produktion in CD4+ Lymphozyten (Untergruppenvergleich) …… 53 3.2.4.3 IL-4-Produktion in CD4- Lymphozyten (Übergruppenvergleich) ……. 53 3.2.4.4 IL-4-Produktion in CD4- Lymphozyten (Untergruppenvergleich) …… 54 3.2.5 Interleukin-10-Produktion …………………………………….…………………... 54 3.2.5.1 IL-10-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) ..… 54 3.2.5.2 IL-10-Produktion in CD4+ Lymphozyten (Untergruppenvergleich) …. 55 3.2.5.3 IL-10-Produktion in CD4- Lymphozyten (Übergruppenvergleich) …... 55 3.2.5.4 IL-10-Produktion in CD4- Lymphozyten (Untergruppenvergleich) ..… 56 3.3 Differentialblutbild ………………………………………………………………………… 57 3.3.1 Leukozyten ………………………………………………………………………… 57 3.3.1.1 Leukozyten/nl (Übergruppenvergleich) ……………………………….. 57 3.3.1.2 Leukozyten/nl (Untergruppenvergleich) ………………………………. 57 3.3.2 Neutrophile Granulozyten …………………………………………………….….. 58 3.3.2.1 Prozentualer Anteil neutrophiler Granulozyten (Übergruppenvergleich) ………………………………………………………….. 58 3.3.2.2 Prozentualer Anteil neutrophiler Granulozyten (Untergruppenvergleich) …………………………………………………………. 59 3.3.3 Lymphozyten ……………………………………………….……………………… 59 3.3.3.1 Prozentualer Anteil von Lymphozyten (Übergruppenvergleich) ….… 59 3.3.3.2 Prozentualer Anteil von Lymphozyten (Untergruppenvergleich) …… 60 3.3.4 Monozyten ………………………………………………………………….……… 61 3.3.4.1 Prozentualer Anteil von Monozyten (Übergruppenvergleich) ………. 61 3.3.4.2 Prozentualer Anteil von Monozyten (Untergruppenvergleich) ……… 61 3.3.5 Eosinophile Granulozyten ……………………………………………………….. 62 3.3.5.1 Prozentualer Anteil eosinophiler Granulozyten (Übergruppenvergleich) ………………………………………………………….. 62 3.3.5.2 Prozentualer Anteil eosinophiler Granulozyten (Untergruppenvergleich) …………………………………………………………. 62 3.3.6 Basophile Granulozyten …………………………………………………….……. 63 3.3.6.1 Prozentualer Anteil basophiler Granulozyten (Übergruppenvergleich) ………………………………………………………….. 63 3.3.6.2 Prozentualer Anteil basophiler Granulozyten (Untergruppenvergleich) …………………………………………………………. 63 4 Diskussion ………………………………………………………………………………. 64 4.1 Oberflächenmarker CD45RA/R0 …………………………………………………….….. 64 4.2 Intrazellulärer Zytokinnachweis …………………………………………….………….. 65 4.2.1 Interferon-γ-Produktion …………………………………………………………… 65 4.2.2 Tumornekrosefaktor-α-Produktion …………………………………….………… 66 4.2.3 Interleukin-2-Produktion …………………………………………………………. 67 4.2.4 Interleukin-4-Produktion …………………………………………………………. 68 4.2.5 Interleukin-10-Produktion ………………………………………………………... 69 4.3 Differentialblutbild ………………………………………………………………………... 71 5 Zusammenfassung ……………………………………………….………………….. 73 6 Literaturverzeichnis …………………………………………………………………. 75 Anhang Danksagung Lebenslauf Verzeichnis häufig benutzter Abkürzungen AK .………………………………………………………………………..………….……..…… Antikörper APC ……………………………………………. antigen presenting cell (antigenpräsentierende Zelle) APL ……………………………………...………..…… altered peptide ligand (alterierter Peptidligand) B7-Moleküle ……………………………… die wichtigsten kostimulatorischen Moleküle der T-Zellen CD ………………………………………………………………………………… cluster of differentiation CP-MS ……………………………………………………………..………… chronisch-progrediente MS CSF ……………………………………………………………………...……. cerebrospinal fluid (Liquor) CTL ………………………………………………….………………………………… zytotoxische T-Zelle DMF …………………………………...………………………………………………… Dimethylformamid DTH ………………………………………………………………………… delayed type hypersensitivity EAE ………………………………… experimentelle autoimmune/autoallergische Enzephalomyelitis EDSS …………………………………………………………………… expanded disability status scale EDTA …………………………………………………….……………………… Ethylendiamintetraazetat ELISA ………………………………...…………………………… enzyme linked immunosorbent assay FACScan® …………………...………………………… fluorescence activated cell sorter and analyser FBS …………………………………………..………………………………………… foetal bovine serum FITC ……………………………………………………………………………… Fluoreszeinisothiozyanat FSC …………………………………….……………………………………………… forward light scatter GM-CSF ………….……………………...………… granulocyte/macrophage colony-stimulating factor h ………………………………………………………..……………………………………………… Stunde HBSS ……………………………..………………………………………… Hank’s balanced salt solution HLA ……………………………………………………………………………… human leukocyte antigen ICS …………………………..………………………………………………………… intracellular staining Ig…………………………………….……………………………………..………………… Immunglobulin IFN ………………………………………………….……………………………………………… Interferon IL …………………………………………..…………………………….………………………… Interleukin LT …………………………………..…………………………………………………………… Lymphotoxin MAG …………...………………………………………………………… Myelin-assoziiertes Glykoprotein MBP ……………………………………………………………………………….. basisches Myelinprotein MHC …………………………… major histocompatibility complex (Haupthistokompatibilitätskomplex) min ……………………………………………………………………..………………………….…… Minute MOG ……………………………………………………………… Myelin-Oligodendrozyten-Glykoprotein mRNA …………………………………………………….…………………… messenger ribonucleic acid MRT …………………………………………………………………….…… Magnetresonanztomographie MS ……………………………………………………………………….………………… Multiple Sklerose NK-Zellen ………………………………………………………………….………… Natürliche Killerzellen OND …………………………………………...……………………………… other neurological diseases PBMC ………………………………………………...……………… peripheral blood mononuclear cells PE ……………………………………………………………………………………....……… Phykoerythrin PE-Cy5 ………….…..……………………………………………………………… Phykoerythrin-Zyanin-5 PLP ……………………………………...………………………………………………… Proteolipidprotein PMA ………………………………………………………………………… Phorbol-12-Myristat-13-Azetat PNP ……………………………………………………….………………………………… Polyneuropathie RPMI ………………………………………..………………… Rockwell Park Memorial Institute Medium RR-MS ………….…...………… relapsing remitting multiple sclerosis (hier: stabile schubförmige MS) Schub-MS ……………………………………………………… hier: schubförmige MS im akuten Schub SSC …………………………………………………………………………………… sideward light scatter TCR ………………………………..………………………………………………………… T-Zell-Rezeptor TGF ……………………………………………………………………………… transforming growth factor TH-Zelle ………………………………...……………………………………………………… T-Helfer-Zelle TNF …………………………………..………………………………………………… Tumornekrosefaktor ZNS ………………..……………………………………………………………… Zentrales Nervensystem Einleitung 1 1 Einleitung „Anfangs war die Diagnose MS nur ein böser Traum, jetzt ist sie wie ein Knüppel, der mir Tag für Tag zwischen die Beine geworfen wird.“ Dieser Ausspruch einer in diese Studie eingeschlossenen Probandin im Anamnesegespräch verdeutlicht die mögliche Implikation der Erkrankung für Betroffene. Die Multiple Sklerose (MS) wird synonym als Enzephalomyelitis disseminata bezeichnet, beide Bezeichnungen weisen bereits auf wesentliche Charakteristika der Erkrankung hin: Es handelt sich um eine entzündliche Erkrankung von Hirn und Rückenmark mit räumlich und/oder zeitlich disseminierten Läsionen. Als Folge der Entzündungen kommt es zur Ausbildung multipler gliöser Herde im ZNS. Die Ätiologie der Erkrankung gilt weiterhin als ungeklärt. Anhand neuerer Forschungsergebnisse muss von einer multifaktoriellen Genese der Multiplen Sklerose ausgegangen werden, wobei exogene Faktoren, wie z.B. das lokale Reservoir an Erregern auf dem Boden genetisch determinierter Suszeptibilität, eine entscheidende Rolle zu spielen scheinen. Die Multiple Sklerose wird heute weithin anerkannt als T-Zell-vermittelte Erkrankung mit Autoimmuncharakter (Poeck & Hacke, 2001; Rosche et al., 2003). In der vorliegenden Arbeit wird die Rolle der T-Helfer-Zellen (TH-Zellen) hinsichtlich bestimmter von ihnen synthetisierter Zytokine untersucht. MS-Patienten werden diesbezüglich mit gesunden Kontrollpersonen und mit Patienten mit anderen neurologischen Erkrankungen verglichen, um spezifische Phänomene der Multiplen Sklerose aufdecken zu können. 1.1 Das Krankheitsbild der Multiplen Sklerose 1.1.1 Epidemiologie und Genetik Die Multiple Sklerose ist eine der häufigsten organischen Nervenkrankheiten. In Mitteleuropa wird die Prävalenz üblicherweise mit 30-60/100.000 Einwohnern angegeben (Gold & Rieckmann, 2000), in Deutschland von Lauer (1994) mit 80-100/100.000, in Bochum mit 95/100.000 Einwohnern (Haupts et al., 1994). Das Erstmanifestationsalter liegt typischerweise zwischen dem 20. und 40. Lebensjahr, wobei Frauen etwa doppelt so häufig betroffen sind wie Männer (Poeck & Hacke, 2001; Rosche et al., 2003). In Untersuchungen zur geographischen Verteilung der MS weltweit wurde auf der nördlichen Halbkugel bei Angehörigen der weißen Rasse eine Zunahme der Erkrankungshäufigkeit mit wachsender Entfernung vom Äquator beobachtet. So wurde beispielsweise in Schottland die wohl höchste weltweit beschriebene Prävalenz mit bis zu 193/100.000 beschrieben (Rosati et al., 2001), in Äquatorialafrika dagegen eine Prävalenz von nur 0-4/100.000. Es gibt allerdings einige Ausnahmen zur Abhängigkeit der Prävalenz vom Breitengrad (z.B. Foki = Regionen besonders großer Häufigkeit an MS in vielen Ländern) (Poeck & Hacke, 2001). Insbesondere eine unterschiedliche Prävalenz in verschiedenen ethnischen Gruppen einer Region weist auf Einleitung 2 eine starke Beteiligung genetischer Faktoren hin. So wird für Südafrika unter der weißen englisch-sprechenden Bevölkerung eine Prävalenz von 13/100.000 Einwohnern angegeben, dagegen unter farbigen Südafrikanern eine vergleichsweise extrem niedrige Prävalenz von nur 3/100.000 (Rosati et al., 2001). Farbige US-Amerikaner haben unabhängig von der Lebensregion ein nur ca. 50 prozentiges Erkrankungsrisiko im Vergleich zu weißen Amerikanern (Gold & Rieckmann, 2000). Die von Martin & McFarland (1995) aufgestellte Hypothese der Exposition gegenüber einem ortsgebundenen Umweltfaktor als Voraussetzung für die Multiple Sklerose wurde durch Migrationstudien untermauert. Das MS-Erkrankungsrisiko nahm für Menschen, die aus Hochrisikoregionen wie Nordeuropa in Äquatorbereiche umsiedelten, deutlich ab; dagegen stieg umgekehrt das Risiko an für Menschen, die aus Gegenden niedriger Prävalenz in Hochrisikoregionen umsiedelten. Interessanterweise spielte das Lebensalter bei der Umsiedelung eine entscheidende Rolle: Erfolgte die Migration nach dem 15. Lebensjahr, wurde das Risiko des Herkunftslandes beibehalten, erfolgte sie vor dem 15. Lebensjahr, passte sich das Risiko dem des neuen Heimatlandes an (Kurtzke, 1995). Ob diese Tatsachen mit der Exposition gegenüber lokalen Erregerreservoirs oder Bedingungen der Ernährungs- und Lebensweise zusammenhängen, ist ungeklärt (Poeck & Hacke, 2001). MS Prävalenz per 100.000 Einwohner Über 100 80 bis 100 60 bis 80 30 bis 60 Weniger als 30 Keine Daten Abbildung 1. MS-Prävalenz weltweit (nach http://www.mult-sclerosis.org/ms_world.html). Das gelegentlich zu beobachtende endemische Auftreten der MS, z.B. auf den Färöer Inseln, in Florida und in der Schweiz, veranlasste zur fieberhaften Suche nach pathogenen Umweltfaktoren, insbesondere viralen Erregern, zumal in Tiermodellen viral ausgelöste, der MS ähnelnde Erkrankungen bekannt sind (Martin & McFarland, 1995). Derartige Versuche blieben jedoch letztlich ohne spezifisches Ergebnis, d.h. es wurde bisher nicht nachgewiesen, dass ein bestimmtes infektiöses Agens die Ursache einer MS-Erkrankung darstellt. Die im Einleitung 3 Liquor von MS-Patienten meist nachweisbaren oligoklonalen Banden beinhalten zwar auch Antikörper, die extrinsische Antigene wie bestimmte Viren (z.B. Masern, Röteln, VarizellaZoster, HSV-6) erkennen, aber diese machen nur einen kleinen Teil der Banden aus (Compston & Coles, 2002). Bereits im Jahr 1985 wurde von Fujinami und Oldstone allerdings diskutiert, dass die Ähnlichkeit zwischen viralen Erregern und antigenen Epitopen auf Myelinbestandteilen in Form des sogenannten „molekularen Mimikry“ die Fehlleitung der überschießenden Entzündungsreaktion begünstigen könnte. Zumindest spricht der Nachweis der oligoklonalen Banden im Liquor für die inflammatorische Pathogenese der Erkrankung (Gold & Rieckmann, 2000; Poeck & Hacke, 2001). In Familienstudien wurde gezeigt, dass Verwandte von MS-Patienten ein deutlich erhöhtes Erkrankungsrisiko aufweisen, wie in Abbildung 2 ausführlich dargelegt. Verwandtschaftsgrad Eineiiger Zwilling Geschwister, zwei erkrankte Elternteile Geschwister, ein erkranktes Elternteil Zweieiiger Zwilling Geschwister Elternteil Kind Halbgeschwister Onkel oder Tante Neffe oder Nichte Cousin oder Cousine Adoptivkind Allgemeine Bevölkerung Altersgemäßes Lebenszeitrisiko Abbildung 2. Erkrankungsrisiko an MS in Familien (nach Compston & Coles, 2002). Altersgemäßes Lebenszeitrisiko für Verwandte von MS-Patienten. 95% Konfidenzintervalle angezeigt . Dennoch ist die Multiple Sklerose keine Erbkrankheit im Sinne eines monogenen Mendel’schen Erbgangs. Versuche, spezifische krankheitsbestimmende Gene zu identifizieren, blieben bislang weitgehend erfolglos oder führten zu mehrdeutigen Ergebnissen. Lediglich das HLADR-2-Allel der menschlichen Klasse-II-Leukozytenantigene (human leukocyte antigen, HLA) zeigt bei Kaukasiern eine reproduzierbare Assoziation mit der Multiplen Sklerose mit einem relativen Risiko von 2 - 4 (Oksenberg et al., 2001). Es herrscht heute übereinstimmend die Meinung, dass für das Erkrankungsrisiko eine große Anzahl unterschiedlicher Gene im Sinne einer polygenetischen Vererbung eine Rolle spielt (Ebers & Dyment, 1998; Oksenberg et al., 2001). In großangelegten weltweiten Genomanalysen konnten zwar weitere Genregionen identifiziert werden, die möglicherweise mit einer MS-Suszeptibilität zusammenhängen, es gab jedoch keine gemeinsame Schnittmenge dieser Studien, also Genregionen, die überall als positiv erkannt wurden. Dem gemäß scheinen Risikogene in unterschiedlichen Populationen zu variieren (Heterogenität) (Rosche et al., 2003). Einleitung 1.1.2 4 Exogene Faktoren Als modifizierende Risikofaktoren werden diskutiert: Infektionen, Impfungen, Schwangerschaft und Stress. Wenngleich infektiöse Agenzien keine ursächliche Auslösung der MS zu bewirken scheinen, gibt es doch Beobachtungen, dass sich der Zustand von Patienten mit Autoimmunerkrankungen, z.B. bei der Myasthenia gravis, im Rahmen eines unspezifischen Virusinfektes deutlich verschlechtern kann. Bei der MS fand sich die stärkste Korrelation mit Virusinfektionen des Respirationstraktes. Diese Tatsache wird mit einer generellen Aktivierung der Immunantwort bei Virusinfekten erklärt, wobei es als unerwünschter Nebeneffekt zur Verstärkung der Autoimmunreaktion kommen kann (Gold & Rieckmann, 2000). Theoretisch würde man auch bei Impfungen erwarten, dass eine Verstärkung der Immunantwort durch das - dem spezifischen Antigen zugefügte - Adjuvans die Auslösung eines Schubes begünstigt. Bisher fand diese Vermutung allerdings keine Bestätigung (Fenichel, 1999). Der Einfluss der Schwangerschaft auf den Verlauf der MS hat einige interessante Erkenntnisse hervorgebracht: Während der Schwangerschaft liegt die Schubrate um etwa 30 - 50% niedriger als zuvor (Damek & Shuster, 1997). Dagegen ist in der Phase nach der Schwangerschaft das Schubrisiko deutlich erhöht, so dass sich kurzfristig die Effekte der Schwangerschaft auf die Schubhäufigkeit neutralisieren (Confavreux et al., 1998). Langfristig wurde zumindest kein negativer Effekt einer Schwangerschaft auf den MS-Verlauf festgestellt, es scheint eher ein positiver Effekt zu dominieren - insbesondere angesichts des selteneren bzw. späteren Überganges der schubförmigen in die prognostisch ungünstigere chronisch-progrediente Verlaufsform (Damek & Shuster, 1997). In einigen Studien ergaben sich Hinweise dafür, dass psychosozialer Stress einen negativen Einfluss auf die MS-Schubhäufigkeit haben könnte. Demgegenüber weiß man aus tierexperimentellen Studien, dass Stress eine generelle Hemmung der Immunantwort und damit auch eine schlechtere Induzierbarkeit und einen milderen Verlauf von Autoimmunerkrankungen zur Folge haben kann. In einer Metaanalyse von humanen Untersuchungen mit dieser Fragestellung fanden Goddin et al. im Jahr 1999 keine Evidenz für einen Kausalzusammenhang zwischen psychosozialem Stress (oder physischem Trauma) und dem Auftreten oder Exazerbationen der MS. Bereits im Jahr 2000 stellte Martinelli anderslautende Ergebnisse aus neueren MRT-morphologischen und experimentellen immunologischen Untersuchungen unter besonderer Berücksichtigung der Interaktionen zwischen Immunsystem und hypothalamisch-hypophysärer-adrenaler Achse sowie sympathischem Nervensystem vor. Einleitung 1.1.3 5 Verlaufsformen und Prognose Bei der Multiplen Sklerose werden grundsätzlich zwei Verlaufsformen unterschieden, eine schubförmige und eine chronisch-progrediente Form, wobei Übergangsformen vorkommen (Gold & Rieckmann, 2000). Eine differenziertere Betrachtung liefert Abbildung 3. Als Schub definiert man nach Ausschluss physiologischer Schwankungen akute oder subakute, ohne assoziierte Infekte oder Fieber auftretende neurologische Ausfälle bzw. eine Verschlechterung vorbestehender Symptome von mindestens 24 Stunden Dauer (Gold & Rieckmann, 2000). Schubhäufigkeit und -schwere variieren interindividuell stark, dementsprechend ist eine individuelle Prognose zu Beginn der Erkrankung nicht zu stellen. Die statistische Lebenserwartung ist kaum verkürzt. Bei etwa 25% der Patienten sind die Aktivitäten des täglichen Lebens nie beeinträchtigt, bis zu 15% erleben in kurzer Zeit eine schwere Behinderung (Compston & Coles, 2002). Am häufigsten ist der schubförmige Verlauf. Etwa 10% der MS-Patienten haben nie Schübe und die Erkrankung nimmt von Beginn an einen primär chronisch-progredienten Verlauf. Daneben wurden auch andere seltene Sonderformen beschrieben, namentlich Manifestationen des Kindes- und Jugendalters als Konzentrische Sklerose und als besonders bösartige Variante die Encephalitis pontis et cerebelli, desweiteren die Neuromyelitis optica (Devic Syndrom) - nach Meinung einiger Autoren ein eigenständiges Krankheitsbild - auf die hier nicht näher eingegangen werden soll (Poeck & Hacke, 2001). a c a b e f d g Abbildung 3. Die wichtigsten Verlaufsformen der MS. a) schubförmiger Verlauf mit vollständigen Remissionen b) schubförmiger Verlauf mit unvollständigen Remissionen c) sekundär progredienter Verlauf d) sekundär progredienter Verlauf mit Schub und leichter Remission e) progredient-schubförmiger Verlauf f) primär progredienter Verlauf mit Perioden von Stillstand und/oder Besserung g) primär progredienter Verlauf 1.1.4 Pathophysiologie und -anatomie Die Multiple Sklerose befällt disseminiert das ZNS und zeichnet sich durch eine fortschreitende Entmarkung von Neuronen der weißen Substanz des Gehirns aus. Als typisch gelten periventrikulär lokalisierte sogenannte Demyelinisierungsplaques, die im chronischen Stadium von gliösem Narbengewebe ausgefüllt sind (Sklerosierung). Charakteristisch ist der Nachweis einer Vene im Zentrum der Plaques. Lucchinetti et al. beschrieben (2000) vier Typen von Läsionsmustern bei MS-Patienten. Gemeinsames Kennzeichen ist eine T-Zell- und Makrophagen-dominierte entzündliche Reaktion. Die Typen I und II zeigen den „klassisch autoimmunen Typ“ perivenös verteilter Läsionen mit vorherrschenden Zeichen der Myelinschädigung (unter relativer Schonung der Oligodendrozyten), wobei sich in aktiv Einleitung 6 demyelinisierenden Regionen bei Typ II eine deutliche Ablagerung von Immunglobulinen und Komplement findet, die bei Typ I fehlt. Dies spricht für eine wichtige Rolle von Antikörpern bei Typ II und von Produkten von aktivierten Makrophagen und T-Zellen bei Typ I. Typ III-Läsionen zeigen nicht die typische zentrale Vene, sind unscharf begrenzt und bieten Zeichen einer Oligodendrozytendystrophie, die einer solchen bei toxischer oder virusinduzierter primärer Oligodendrozytenschädigung ähnelt. Typ IV-Läsionen unterscheiden sich von Typ I- und IILäsionen durch Zeichen einer primären Oligodendrozytenschädigung. Typ IV-Läsionen wurden von Lucchinetti et al. ausschließlich bei Patienten mit primär chronisch-progredienter MS gefunden. Lucchinetti et al. folgerten, die von ihnen erhobenen Daten geben einen Hinweis darauf, dass die Mechanismen und Ziele der Demyelinisierung in verschiedenen Untergruppen und Stadien der MS fundamental unterschiedlich sind. Die fortschreitende Demyelinisierung und damit verbundene Beeinträchtigung der saltatorischen Erregungsfortleitung in Axonen erklärt einige Symptome und labortechnische Befunde von MS-Patienten: Partiell demyelinisierte Axone leiten Impulse mit verminderter Geschwindigkeit, so dass in den evozierten Potentialen charakteristisch verzögerte Leitzeiten gemessen werden. Demyelinisierte Axone können spontan entladen und zeigen eine erhöhte mechanische Irritabilität, so dass Lichtblitze bei Augenbewegungen (Phosphene) und elektrisierende Missempfindungen im Bereich der Wirbelsäule bei Nackenbeugung (LhermittePhänomen) auftreten können. Partiell demyelinisierte Axone können den durch erhöhte Temperaturen induzierten Abfall der Membrankapazität nicht kompensieren, so dass die Leitfähigkeit vorübergehend zusammenbricht (Leitungsblock), was zum Auftreten von Symptomen bei körperlicher Betätigung oder Genuss eines heißen Bades führt (UhthoffPhänomen). Zwischen benachbarten demyelinisierten Axonen kann eine sogenannte ephaptische Transmission (cross talk) auftreten, was zu paroxysmalen Symptomen wie einer Trigeminusneuralgie oder durch Berührung oder Bewegung ausgelöster kurz dauernder schmerzhafter Tonuserhöhung der Gliedmaßen führen kann (Compston & Coles, 2002). Während die Demyelinisierung prinzipiell reversibel ist, ist ein Untergang von Axonen (mit Waller’scher Degeneration) irreversibel. Einem solchen fortschreitenden Axonverlust, der insbesondere bei progredienten Verlaufsformen zu beobachten ist, wird die bleibende Behinderung der betroffenen Patienten zugeschrieben (Prineas et al., 2001). Axonale Schäden sind jedoch bereits in frühen Stadien auch bei schubförmigen Verlaufsformen nachzuweisen. (Losseff et al., 1996; Trapp et al., 1999 ; Bitsch et al., 2000 ; Rosche et al., 2003). Einleitung 1.1.5 7 Symptomatik Nachfolgend wird eine tabellarische Auflistung ausgewählter Symptome samt topodiagnostischer Zuordnung dargestellt (nach Poeck & Hacke, 2001 und Compston & Coles, 2002). Tabelle 1. Läsionstopographie im MRT in T2-Wichtung und mögliche Symptome. MRT Läsionsort Symptome Cerebrum Sensible und/oder motorische Hemisymptomatik Psychische Alterationen (Euphorie, Depression, kognitive Defizite bis zur Demenz) Epilepsie (selten) Fokale kortikale Defizite (selten) Nervus opticus Visusstörung Cerebellum Tremor Dysarthrie Ataxie Hirnstamm Bulbusmotilitätsstörungen Vertigo Dysarthrie, Dysphagie Paroxysmale Symptome Myelon Spastische Tetra-, Para-, oder Hemiparese Blasenfunktionsstörungen Erektionsstörungen Obstipation Andere Schmerzen Fatigue Einleitung 8 Als besondere Symptomkonstellation bei Befall des zerebellären Systems verdient die sogenannte Charcot-Trias Erwähnung, die Charcot anhand von Beobachtungen auf seinen Visiten im Pariser Armenkrankenhaus La Salpêtrière aufstellte: Nystagmus, Intentionstremor und skandierendes Sprechen (Kitze, 2000; Poeck & Hacke, 2001). Als pathognomonisch für die Multiple Sklerose führen Poeck & Hacke das Syndrom paroxysmale Dysarthrie und Ataxie an. Es handelt sich um täglich mehrmals einsetzende Anfälle von bulbärer Dysarthrie und schwerer Ataxie von bis zu 15 Sekunden Dauer, gelegentlich mit Gefühlsstörungen im Trigeminusgebiet einhergehend. Da es für die Multiple Sklerose jedoch weder spezifische Tests noch im Querschnitt beweisende klinische Symptome oder Syndrome gibt, sollen zur differentialdiagnostischen Abgrenzung gegenüber anderen multifokalen Erkrankungen des ZNS (hier nicht näher erörtert) und zur internationalen Vereinheitlichung diagnostische Kriterien unter Einbeziehung geeigneter Zusatzdiagnostik herangezogen werden: Routinemäßig werden die sogenannten Poser-Kriterien (welche ab 1983 die Schumacher Kriterien ablösten) verwendet, die Befunde von MRT, Elektrophysiologie und Liquordiagnostik neben klinischanamnestischen Daten berücksichtigen (Poser et al., 1983). Die Rekrutierung der MSProbanden der vorliegenden Arbeit wurde nach den Poser-Kriterien vorgenommen. 1.1.6 Diagnose-Kriterien Diagnose-Kriterien nach Poser (1983) Allgemeine Voraussetzungen: Der Erkrankungsbeginn sollte nicht vor dem 10. oder nach dem 59. Lebensjahr liegen, es ist der Ausschluss anderer neurologischer Erkrankungen durch einen kompetenten Neurologen erforderlich. Als gesicherte MS wird die post mortem histopathologisch gesicherte Diagnose (in Abgrenzung zur tabellarisch aufgeführten klinisch gesicherten MS) gewertet. Einleitung 9 Tabelle 2. Poser Kriterien. MS-Kategorie Schubanzahl Nachweis separater Läsionen Klinisch Liquor Paraklinisch A Klinisch gesichert 2 2 2 1 und 1 2 1 oder 1 oder 1 2 oder 1 1 2 1 oder 1 2 oder 1 1 oder B Laborunterstützt gesichert + + und 1 und 1 + C Klinisch wahrscheinlich D Laborunterstützt wahrscheinlich 2 + Anmerkungen: Paraklinische Nachweise beruhen auf MRT und/oder evozierten Potentialen. Positive Liquorbefunde beinhalten den Nachweis oligoklonaler Banden oder autochthoner IgG-Synthese. Nach den neueren, in letzter Zeit zunehmende Verwendung findenden McDonald-Kriterien (Mc Donald et al., 2001) kann die Diagnose einer Multiplen Sklerose bereits dann gestellt werden, wenn nach einem ersten Krankheitsschub mit nachweisbaren Auffälligkeiten in mindestens einem neurologischen Funktionssystem der Liquor Multiple Sklerose-typische Veränderungen zeigt, sich mindestens zwei typische Herde im Kernspintomogramm (Magnetresonanztomogramm, MRT) finden und im Verlaufs-MRT drei Monate nach dem Schubereignis mehrere entzündliche Herde in definierter Lage vorhanden sind, wovon mindestens einer Kontrastmittel (Gadolinium) anreichert. Krankheitsbilder, die zu ähnlichen Erscheinungen führen können, müssen ausgeschlossen sein. Die McDonald-Kriterien ermöglichen eine frühere defintive Diagnosestellung der Multiplen Sklerose, so dass Patienten frühestmöglich von einer modernen immunmodulierenden Therapie profitieren können. 1.2 Einleitung Ausgewählte immunologische Aspekte der Multiplen Sklerose 10 Die immunpathologischen Vorgänge in der Pathogenese der Multiplen Sklerose waren in den letzten Jahren und Jahrzehnten Gegenstand zahlreicher wissenschaftlicher Untersuchungen, über deren Erkenntnisse im Folgenden ein Überblick gegeben wird. Die Bedeutung des Immunsystems ging bereits aus im Jahr 1928 veröffentlichten klinischen Beobachtungen Remlingers von Komplikationen nach Impfungen mit myelinkontaminiertem Tollwutimpfstoff hervor: Es traten akut demyelinisierende Enzephalomyelitiden auf, die durch eine Immunantwort gegen Myelinantigene charakterisiert waren. 1.2.1 Tiermodelle der MS Rivers et al. bestätigten diese Beobachtung (1933) im Tiermodell, der sogenannten Experimentell Autoimmunen/Allergischen Enzephalomyelitis (EAE). Immunisierungen mit Myelinantigenen und Adjuvans verursachten akute oder chronische Entzündungen des ZNS in bestimmten Nager- und Affenstämmen. Je nach gewähltem Antigen und Versuchstierstamm mit definiertem genetischen Hintergrund konnten Verlaufsformen induziert werden, die den menschlichen stark ähnelten (Wekerle et al., 1994). Durch den Transfer von myelinspezifischen CD4+-T-Zellen konnte eine EAE in einem gesunden Tier ausgelöst werden (Paterson, 1960; Mokhtarian et al., 1984). Besondere Enzephalitogenität boten CD4+ T-Zellen, die bestimmte Zytokine – namentlich Interleukin-2 (IL-2), Tumornekrosefaktor-α (TNF-α) sowie Interferon-γ (IFN-γ) freisetzten (Ando et al., 1989; Powell et al., 1990; Zamvil & Steinman, 1990). Kontrastierend hierzu erwiesen sich CD4+ T-Zellen, die Zytokine wie IL-4, IL-10 und transforming growth factor-β (TGF-β) sezernierten, als krankheitsunterdrückend (Johns et al., 1991; Rocken et al., 1996). Entsprechende T-Zellen wurden auch beim Menschen nachgewiesen (Pette et al., 1990). Zytokine werden definiert als von Zellen sezernierte Polypeptide, die das Verhalten anderer Zellen, die Rezeptoren für diese Polypeptide besitzen, beeinflussen. Sie sind als Signalmoleküle an zahlreichen physiologischen Prozessen beteiligt, u.a. der Hämatopoese, der Differenzierung und Proliferation von Zellen sowie der Initiierung, Aufrechterhaltung und Modulation von Immunantworten. Die Wirkung der Zytokine erstreckt sich typischerweise nur auf einen kleinen Aktionsradius (autokrin und parakrin) (Janeway et al., 2002). 1.2.2 Repertoire möglicher Autoantigene beim Menschen Potentielle Autoantigene der besprochenen T-Zellen sind immunogene Bestandteile des Myelins, darunter das Proteolipidprotein (PLP), das etwa 50% des Proteingehalts im Myelin des ZNS einnimmt, das Myelin-basische Protein (MBP) (Anteil von 10-20%), das Myelin-assoziierte Glykoprotein (MAG) (Anteil von etwa 1%) und das Myelin-Oligodendrozyten-Glykoprotein (MOG) (Anteil von etwa 0,1%) (Gold & Rieckmann, 2000). Jedoch können nicht nur Myelinantigene, sondern auch andere im ZNS Einleitung 11 vorkommende Antigene Ziel der Autoimmunreaktion sein, z.B. das in Gliazellen nachweisbare Protein S-100 (Kojima et al., 1994). 1.2.3 Die Rolle der T-Lymphozyten Es werden zwei Haupttypen von T-Lymphozyten anhand ihres auf der Oberfläche exprimierten Korezeptors unterschieden, und zwar CD4+ und CD8+ T-Lymphozyten. CD4+ T-Lymphozyten werden auch als T-Helfer-Zellen (TH-Zellen) bezeichnet und binden an MHC-Moleküle der Klasse II. TH-Zellen aktivieren Makrophagen oder regen B-Zellen dazu an, zu proliferieren und zu antikörperproduzierenden Plasmazellen zu differenzieren. CD8+ T-Lymphozyten werden auch als zytotoxische T-Zellen bezeichnet und binden an MHCMoleküle der Klasse I. Aktivierte zytotoxische T-Zellen können infizierte Zellen direkt abtöten (Janeway et al., 2002). Abbildung 4. Die drei Gruppen von T-Effektorzellen (Janeway et al., 2002), die im Rahmen der normalen Immunantwort auf verschiedene Arten von Krankheitserregern spezialisiert sind . Einleitung 12 T-Zellen erkennen ihr Zielantigen nur im Kontext mit den oben erwähnten MHC-Molekülen (MHC-Restriktion). MHC-Moleküle der Klasse I kommen ubiquitär auf fast sämtlichen somatischen Zellen vor und präsentieren spezifischen CD8+ T-Zellen antigene Strukturen von Krankheitserregern, die sich im Zytosol vermehren. MHC-Moleküle der Klasse II werden vornehmlich von antigenpräsentierenden Zellen (APC, antigen presenting cells) exprimiert und präsentieren Antigene, die von endozytotischen pathogenen Erregern oder Toxinen abstammen. Die wichtigsten antigenpräsentierenden Zellen sind dendritische Zellen, Makrophagen und B-Zellen, unter bestimmten Bedingungen auch Mikrogliazellen und Astrozyten. Aus den obigen Ausführungen wird deutlich, dass die MHC-Restriktion die Spezifität der beteiligten T-Zellen festlegt. Beim Menschen werden die Gene des Haupthistokompatibiltätskomplexes (MHC) auf Chromosom 6 auch human leukocyte antigen (HLA)-Gene genannt, da sie aufgrund von Unterschieden in den Antigenen von Leukozyten entdeckt wurden. Durch zwei Mechanismen ist gewährleistet, dass das Immunsystem auf eine Vielzahl unterschiedlicher und sich verändernder Pathogene reagieren kann: Es gibt mehrere MHC-Klasse-I- und MHC-Klasse-II-Gene, der MHC ist polygen. Für jedes Gen existieren mehrere Allele, der MHC weist einen ausgeprägten Polymorphismus auf. Ein Zusammenhang zwischen MHC-Genotyp und Autoimmunerkrankung erscheint plausibel, da die Fähigkeit von T-Zellen, auf ein spezifisches Antigen zu reagieren, vom MHC-Genotyp abhängt (Janeway et al., 2002). 1.2.4 Das TH1/TH2-Paradigma CD4+ T-Zellen bzw. TH-Zellen können wiederum in distinkte Untergruppen unterteilt werden. Einen breiten Konsens findet dabei zur Zeit die Einteilung in TH1- und TH2-Zellen, die sich anhand der von ihnen produzierten Zytokine und daraus folgernd ihrer funktionellen Potenz unterscheiden (Mosmann & Coffman, 1989; Janeway et al., 2002). 1.2.4.1 Die Aktivierungsstadien von CD4+ T-Zellen Naive ruhende CD4+ T-Zellen reagieren zunächst mit Proliferation und Produktion von Interleukin-2 auf den Kontakt des T-Zell-Rezeptors (TCR) mit einem passenden Peptid-MHCKlasse-II-Komplex auf einer antigenpräsentierenden Zelle (APC) bei Kostimulation (mittels Interaktion von B7 auf der antigenpräsentierenden Zelle und CD28 auf T-Zellen) (Greenfield et al., 1998). Unter dem autokrinen Einfluss des IL-2 proliferieren diese und entwickeln sich zu TH0-Zellen, die als unreife T-Effektorzellen einige Eigenschaften von TH1- und TH2-Zellen vereinen. Aktivierte T-Zellen exprimieren einen IL-2-Rezeptor mit deutlich höherer Affinität als ruhende, so dass die aktivierte T-Zelle bereits auf eine sehr geringe IL-2-Konzentration Einleitung 13 ansprechen kann. Die Bindung von IL-2 an den hochaffinen Rezeptor führt zur schnelleren Zellteilung und fördert die Differenzierung zu reifen T-Effektorzellen. Naive CD4+ T-Zelle Proliferierende T-Zelle Unreife T-Effektorzelle (TH0) TH1-Zelle TH2-Zelle Abbildung 5. Die Aktivierungsstadien von CD4+ T-Zellen. Bedeutsam ist die Tatsache, dass sowohl die Antigenerkennung durch den T-Zell-Rezeptor als auch das kostimulierende Signal zur Aktivierung der naiven T-Zelle erforderlich ist. Wird ein Antigen ohne Kostimulierung erkannt, werden naive T-Zellen inaktiviert und anergisch bzw. apoptotisch. Dieser Umstand gewährleistet normalerweise die Toleranz gegenüber körpereigenen Antigenen, die auf Gewebezellen exprimiert werden. Essentiell für die Proliferation und Ausreifung der T-Zelle ist eine Steigerung der IL-2-Produktion. Die Antigenerkennung durch den T-Zell-Rezeptor führt zunächst über die Synthese verschiedener Transkriptionsfaktoren zur Aktivierung der Transkription von IL-2-messenger-RNA. Die Transkription von IL-2-mRNA ist jedoch nicht gleichbedeutend mit der Bildung von IL-2. ZytokinmRNAs besitzen eine „Instabilitätssequenz“, so dass eine permanente Synthese und Freisetzung von Zytokinen verhindert und ihre Aktivität streng reguliert wird. Die Signalgebung über das durch Interaktion mit B7 auf der antigenpräsentierenden Zelle aktivierte CD28-Molekül auf der T-Zelle bewirkt eine Stabilisierung der mRNA (und eine Synthese von weiteren Transkriptionsfaktoren), infolgedessen die IL-2-Produktion um etwa das Hundertfache gesteigert wird. B7-Moleküle sind die wichtigsten kostimulatorischen Moleküle der T-Zellen (Janeway et al., 2002). Ob sich aus naiven CD4+ T-Zellen letztlich TH1- oder TH2-Zellen entwickeln, scheint vor allem vom umgebenden Zytokinspektrum bereits in den Anfangsstadien einer Immunreaktion in den peripheren Lymphgeweben abhängig zu sein (Sher & Coffman, 1992; Romagnani, 1994; Abbas et al., 1996; Janeway et al., 2002). Einleitung 14 Aus Untersuchungen der adaptiven Immunität gegenüber verschiedenen Erregern weiß man, dass eine Aktivierung von naiven CD4+ T-Zellen bei Überwiegen von IL-12 und IFN-γ zur Differenzierung in TH1-Zellen, dagegen bei Überwiegen von IL-4 zur Differenzierung in TH2Zellen führt (Moser & Murphy, 2000; Janeway et al., 2002). TH1-Zellen produzieren die proinflammatorischen Zytokine Interferon-γ (IFN-γ), Tumornekrosefaktor-α (TNF-α), Lymphotoxin (LT) und Interleukin-2 (IL-2), jedoch kein IL-4, IL-5, IL-6 und IL10 (Voskuhl et al., 1993; Mosmann & Sad, 1996; Janeway et al., 2002). TH2-Zellen produzieren die antiinflammatorischen Zytokine IL-4, IL-5, IL-6 und IL-10, jedoch kein IFN-γ und IL-2. TNF-α wird von einigen TH2-Zellen in geringerem Ausmaß als von TH1Zellen synthetisiert (Mosmann & Sad, 1996; Janeway et al., 2002). Desweiteren wurden TH3-Zellen beschrieben, die IL-4, IL-10 und transforming growth factor-ß (TGF-β) bilden und als regulatorische T-Zellen sowohl autoimmune inflammatorische TH1- als auch pathologische TH2-Reaktionen unterdrücken können (Mosmann & Sad, 1996). Sie sollen insbesondere bei der Entstehung der sogenannten oralen Toleranz eine Rolle spielen (Bridoux et al., 1997; Weiner, 1997; Miller et al., 1998; Janeway et al., 2002). Das Phänomen der oralen Toleranz wird bei der Aufnahme von Fremdantigenen über die Nahrung beobachtet: Das Immunsystem spricht in einer spezifischen aktiven Weise nicht an. 1.2.4.2 Die Zytokine von TH1- und TH2-Zellen Um die Rolle der T-Helfer-Zell-Untergruppen näher zu beleuchten, wird im Folgenden gezielt auf die in dieser Arbeit untersuchten von ihnen produzierten Zytokine und ihre Relevanz bei der Multiplen Sklerose eingegangen. IFN-γ wird von T-Zellen und zytotoxischen T-Zellen produziert. Es bewirkt die Aktivierung von Makrophagen und die Steigerung der Expression von MHC-Klasse-I- und MHC-Klasse-IIMolekülen (Nguyen et al., 1999). Darüberhinaus hemmt IFN-γ das Wachstum von TH2-Zellen (Maggi et al., 1992; Sher & Coffman, 1992). Es bewirkt die Differenzierung von B-Zellen und induziert die Synthese von IgG2a, einer bestimmten IgG-Subklasse (Janeway et al., 2002). TNF-α kann von TH1-Zellen, einigen TH2-Zellen, zytotoxischen T-Zellen, Makrophagen/ Monozyten, Astrozyten und Mikroglia produziert werden (Renno et al., 1995). Es aktiviert Makrophagen und induziert die Produktion des toxischen Faktors Stickstoffmonoxid (NO). Die Injektion von TNF-α ins ZNS ruft eine akute inflammatorische Reaktion und eine reversible Leitungsverzögerung der Axone hervor (Sharief & Hentges, 1991; Rieckmann et al., 1995). Mit Antikörpern gegen TNF-α und das eng verwandte Lymphotoxin (LT, synonym TNF-β) konnte im Tiermodell ein Schutz vor der EAE erzielt werden (Ruddle et al., 1990). Therapiestudien mit Einleitung 15 anti-TNF-Antikörpern an MS-Patienten zeigten allerdings keinen positiven Effekt (van Oosten et al., 1996; The Lenercept Multiple Sclerosis Study Group, 1999). TNF-α ist Induktor der Expression von Adhäsionsmolekülen auf Endothelzellen und Astrozyten (McCarron et al., 1993) sowie ein Mitogen für Astrozyten, welche im ZNS als antigenpräsentierende Zellen fungieren können (Selmaj et al., 1990). Ferner ist TNF-α für Oligodendrozyten direkt zytotoxisch (Selmaj & Raine, 1988). IL-2 wird von T-Helfer-Zellen und einigen zytotoxischen T-Zellen produziert. Es besitzt keine direkte inflammatorische Aktivität, ist aber ein notwendiger Wachstumsfaktor für T-Zellen (Gallo et al., 1998) und ist in die Proliferation von Oligodendrozyten involviert. Anhand der Wirkungen der oben genannten von TH1-Zellen sezernierten proinflammatorischen Zytokine kann man ihre potentielle Relevanz bei der Entstehung von Läsionen im ZNS von Multiple Sklerose Patienten ableiten. Es wurde Anfang der 90er Jahre beschrieben, dass eine EAE allein durch Injektion von MBP-reaktiven TH1-Zellen ausgelöst werden konnte, aber nicht durch Injektion von MBP-reaktiven TH2-Zellen. Jedoch konnte in späteren Versuchen unter bestimmten Bedingungen auch mit TH2-Klonen eine EAE induziert werden (Lafaille et al., 1997). Zusammengefasst kann man sagen, dass TH1-Zellen vor allem bei inflammatorischen Reaktionen mit Makrophagenaktivierung (Janeway et al., 2002) sowie bei der verzögerten Überempfindlichkeit (delayed type hypersensitivity, DTH) eine Rolle spielen. Demgegenüber sind TH2-Zellen aufgrund ihres Zytokinspektrums in der Lage, besonders effektiv die Proliferation und Antikörperbildung von B-Zellen zu stimulieren. Es wurde gezeigt, dass durch bestimmte TH2-Zellen atopische Erkrankungen ausgelöst werden können (Mosmann & Sad, 1996). Diese Wirkungen werden vor allem durch die Zytokine IL-4 und IL-5 vermittelt. IL-4 kann außerdem die Differenzierung von T-Zellen in TH1-Zellen behindern. Dieser Aspekt macht deutlich, dass insbesondere über IL-4 und IFN-γ gegensätzliche regulatorische Effekte auf die Entwicklung von TH1- und TH2-Zellen vermittelt werden, d.h. TH1und TH2-Zellen sind gegenseitig-inhibitorisch und selbst-stimulierend (Mosmann & Sad, 1996). Darauf weist auch die Tatsache hin, dass sich bei experimentell ausgelösten starken Immunreaktionen DTH-Antworten (TH1-vermittelt) und Antikörperproduktion (TH2-vermittelt) weitgehend ausschließen. Bei normalen Immunantworten in vivo können ebenfalls zelluläre (TH1) oder humorale (TH2) Abwehr überwiegen, jedoch treten häufig beide Abwehrreaktionen gemeinsam auf, z.B. gegen bestimmte Erreger im Rahmen der Granulombildung (Alwan et al., 1994; Janeway et al., 2002). IL-10, ein weiteres von TH2-Zellen synthetisiertes Zytokin, inhibiert die Synthese von Zytokinen des TH1-Spektrums, nicht jedoch die von Zytokinen des TH2-Spektrums. Besonders effektiv ist IL-10 in der Inhibition der Produktion von IFN-γ (Moore et al., 1993). Einleitung 16 Einige Autoren haben die Hypothese aufgestellt, dass im Verlauf der Multiplen Sklerose die TH1-Zellen für die Auslösung eines Schubs verantwortlich sind, während TH2-Zellen die Entzündungsreaktion eindämmen und nach einem Schub ein die Remyelinisierung begünstigendes Milieu herstellen können (Mosmann & Coffman, 1989; Powrie & Coffman, 1993; Williams et al., 1994). Diese These beruht auch darauf, dass bei MS-Patienten vor einem Schub signifikant erhöhte Konzentrationen von Zytokinen des TH1-Typs gefunden wurden, wohingegen nach einem Schub Zytokine des TH2-Typs in erhöhten Konzentrationen gemessen wurden. Somit könnte eine Dysregulation des durch verschiedene Faktoren bestimmten TH1/TH2-Gleichgewichtes (ein Zuviel an TH1- oder ein Zuwenig an TH2-Gewichtung) ätiopathogenetisch entscheidend sein. Im Hinblick auf die funktionelle Potenz der beschriebenen Zytokine des TH1-Typs zum einen und des TH2-Typs zum anderen könnte sich in Zukunft ein therapeutischer Einsatz der TH2-Zytokine IL-4 und IL-10 als sinnvoll erweisen, nachdem humane Therapiestudien mit Antikörpern gegen das von TH1-Zellen produzierte TNFα, mit löslichem TNF-α-Rezeptor oder mit TNF-α-Antagonisten (The Lenercept Multiple Sclerosis Study Group, 1999) enttäuschend verliefen. Zustände, die mit einer erhöhten IL-10Synthese einhergehen, haben einen positiven Einfluss auf den Verlauf der MS (Wegmann et al., 1993; Mosmann & Sad, 1996). Nicht unerwähnt bleiben soll an dieser Stelle, dass die Annahme einer klaren TH1/TH2Dichotomie des Immunsystems möglicherweise eine starke Vereinfachung der Verhältnisse in vivo darstellt. Interpretationen der möglichen Komplexität von T-Zell-Untereinheiten reichen von einem einfachen TH1/TH2- (und TH0/TH3-) Modell mit quantitativen Differenzen der Zytokinsekretion in verschiedenen Entwicklungs- und/oder Aktivierungsstadien bis hin zu einem Kontinuum von verschiedenen Kombinationen der Zytokinsekretion ohne klar unterscheidbare T-Zell-Untereinheiten (Mosmann & Sad, 1996). 1.2.5 Initiierung der Autoimmunreaktion Warum und auf welche Weise die Autoimmunantwort gegen körpereigene ZNS-Antigene bei der MS entsteht, ist bis heute nicht sicher geklärt. Die Existenz ZNS-antigenspezifischer T-Lymphozyten setzt voraus, dass sie der negativen Selektion und klonalen Deletion im Thymus entkommen sind, da nachgewiesen wurde, dass sowohl MBP als auch PLP im Thymus exprimiert werden (Voskuhl, 1998). Damit verlor die lange Zeit vorherrschende Sequestrationshypothese an Glaubwürdigkeit, die besagte, dass organspezifische Autoimmunität aus einem Versagen der zentralen Selbst-Toleranz durch die Unzugänglichkeit von bestimmten gewebsspezifischen Antigenen für naive T-Zellen hinter anatomischen Barrieren wie der Blut-Hirn-Schranke resultiert. Es wurde bis dahin angenommen, dass ein Zusammenbruch der Barriere den Influx von T-Zellen zur Folge hat und deren Erkennung von nicht-thymischen Antigenen als fremd die Autoimmunerkrankung induziert. (Weller et al., 1996). Einleitung 17 Es wurden von Kuchroo et al. (2002) im Wesentlichen drei Mechanismen diskutiert, auf welche Art und Weise autoreaktive T-Lymphozyten der klonalen Deletion im Thymus entkommen können: T-Zellen mit hoher Affinität zu gewebsspezifischen Selbst-Antigenen werden tatsächlich deletiert, die in der Peripherie nachgewiesenen autoreaktiven Zellen weisen eine niedrige Affinität zu Selbst-Antigenen verglichen mit ihrer Affinität zu Fremd-Antigenen auf. Autoreaktive T-Zellen entkommen der klonalen Deletion im Thymus, da die Form des im Thymus exprimierten Selbst-Antigens sich von der im peripheren Gewebe unterscheidet. Aufgrund ineffizienter Antigen-Präsentation durch krankheitsassoziierte MHC-Allele kommt es nicht zur negativen Selektion autoreaktiver T-Zellen. Autoreaktive Zellen konnten allerdings sowohl bei MS-Patienten als auch bei gesunden Personen nachgewiesen werden. Somit erklärt das bloße Vorhandensein autoreaktiver Zellen nicht allein die Entstehung einer Autoimmunerkrankung. Eine Autoimmunerkrankung entwickelt sich nur dann, wenn autoreaktive Zellen in der Peripherie aktiviert werden. Die Mehrheit der Daten spricht in diesem Zusammenhang für eine pathogene Rolle von TH1-Zellen und eine protektive Rolle von TH2-Zellen (Kuchroo et al., 2002). Kuchroo et al. legten des Weiteren dar, dass bereits auf der Ebene naiver für ein bestimmtes Autoantigen spezifischer (PLP 139-151-reaktiver) TH-Zellen funktionell verschiedene (pathogene und nicht pathogene) Populationen existieren mit einer großen Bandbreite an verschiedenen T-Zell-Rezeptoren. Pathogene und nicht pathogene Populationen wiesen jeweils gemeinsame sich gegenseitig ausschließende Charakteristika ihrer T-Zell-Rezeptor-Spezifität auf. Pathogene T-Zellen erkannten alle PLP 139-151 primär über Tryptophan an Position 144, jede Substitution an Position 144 führte nicht zur Aktivierung der pathogenen Populationen. Nicht pathogene Populationen waren nicht auf Tryptophan an Position 144 angewiesen, sondern auf Leucin und Glyzin an Position 141 und 142. Kuchroo nahm an, dass diese zwei Populationen normalerweise ihre entgegengesetzten Effekte balancieren, die bevorzugte Aktivierung einer Population dagegen die Krankheitssuszeptibilität beeinflussen könnte. Es wurden drei mögliche Erklärungen einer solchen differentiellen Aktivierung diskutiert: Die erste besagt, dass die beiden TH-Zell-Populationen mit unterschiedlichen Aviditäten auf PLP 139-151 reagieren könnten, weil sie unterschiedliche MHC-Peptid-Kontaktstellen des TZell-Rezeptors benutzen. Das unterschiedliche Ausmaß der Dichte von MHC-Molekülen auf antigenpräsentierenden Zellen und/oder der Kostimulation durch antigenpräsentierende Zellen könnte so die Proliferation einer Population fördern. Einleitung 18 Die zweite Erklärungsmöglichkeit besteht in einer unterschiedlichen Sensitivität gegenüber der Initiierung einer Autoimmunreaktion, die durch peripher aktivierte dysregulierte Monozyten bzw. Makrophagen vermittelt wird, welche unspezifisch ins ZNS einwandern und dort die Aktivierung und Proliferation vorhandener autoreaktiver T-Zellen bewirken können (sogenannte bystander activation) (Stoy, 2002). Die dritte Möglichkeit ist, dass die unterschiedlichen TH-Zell-Populationen von unterschiedlichen kreuzreagierenden Liganden aktiviert werden. Kuchroo et al. gingen davon aus, dass autoreaktive Zellen immer kreuzreagierend sind, da es überwältigende Evidenz dafür gibt, dass alle T-Zell-Rezeptoren eine große Anzahl von Peptiden erkennen können (Kersh & Allen, 1996). Die von einem gegebenen T-Zell-Rezeptor erkannten Peptide müssen noch nicht einmal zwingend Homologien in ihrer Primärsequenz aufweisen, entscheidend ist vielmehr die Konformation der Peptide (Sloan-Lancaster & Allen, 1996). Aus der Bandbreite an Liganden eines gegebenen T-Zell-Rezeptors kann eine Hierarchie hinsichtlich der Aktivierungsfähigkeit erstellt werden. Einige Liganden sind Antagonisten der T-Zell-Aktivierung, einige führen gar zur Anergie. Da manche T-Zell-Rezeptoren mit bis zu 107 verschiedenen Peptiden interagieren können (Mason, 1998), muss die Wahrscheinlichkeit, dass ein bestimmter T-Zell-Rezeptor mehr als ein Antigen erkennt und dass darunter ein (kreuzreagierendes) Selbst-Antigen ist, als relevant für die mögliche Initiierung einer Autoimmunerkrankung erachtet werden. 1.2.5.1 Wie können naive autoantigenspezifische T-Zellen aktiviert werden? Eine Hypothese besagt, dass autoreaktive T-Zellen in einem proinflammatorischen MikroMilieu, z.B. in einem virusinfizierten Gewebe, aktiviert werden (Horwitz et al., 1998). Krankheitserreger induzieren die vermehrte Expression von MHC-Molekülen und kostimulierenden Molekülen auf der Oberfläche von antigenpräsentierenden Zellen, die Gewebeantigene aufgenommen haben, so dass die Aktivierungsschwelle der autoreaktiven TZellen gesenkt wird. Wenn man Mäuse mit MBP und komplettem Freund’schen Adjuvans (inklusive Mycobacterium tuberculosis) immunisiert, entwickeln sie eine EAE. Bei Verwendung eines inkompletten Adjuvans ohne Bakterien erkranken die Tiere nicht und entwickeln sogar eine T-Zell vermittelte Resistenz gegenüber Induktion einer EAE (Janeway et al., 2002; Kuchroo et al., 2002). Eine weitere Hypothese besagt, dass Antikörper oder T-Zellen, die als Reaktion auf eine Infektion gebildet wurden, mit körpereigenen Antigenen kreuzreagieren und so zu Gewebeschäden führen. Dieser Mechanismus wird als molekulare Mimikry bezeichnet (Wucherpfennig & Strominger, 1995; Gold & Rieckmann, 2000; Janeway et al., 2002; Kuchroo et al., 2002). Einleitung 19 Ein Mechanismus, der sowohl für die Initiierung als auch Ausweitung der Autoimmunantwort in Betracht kommt, ist das sogenannte epitope spreading. Durch Gewebeschädigung (infektiös bedingt oder aber durch einen bereits in Gang gebrachten Autoimmunprozess) können bislang unzugängliche (kryptische) Autoantigene freigesetzt werden mit der Folge der Aktivierung weiterer autoreaktiver Zellen. Im Rahmen einer chronischen Autoimmunerkrankung kommt es folglich zur zunehmenden Heterogenität der autoantigenen Epitope, so dass eine spezifische Immuntherapie der MS erschwert wird (Lehmann et al., 1992; Gold & Rieckmann, 2000; Janeway et al., 2002). 1.2.6 Die Rolle von T-Gedächtnis-Zellen Die Aktivierung naiver T-Zellen nach Kontakt mit passendem Antigen führt zur Entwicklung von meist kurzlebigen an Apoptose sterbenden T-Effektorzellen und zu langlebigen T-GedächtnisZellen. T-Gedächtnis-Zellen haben eine niedrigere Aktivierungsschwelle und sind weniger abhängig von Kostimulation als naive T-Zellen, reagieren nach Antigenkontakt schneller und effektiver und haben dann alle Eigenschaften aktivierter TH1- oder TH2-Zellen, so dass Infektionen mit „bekannten“ Erregern effizient bekämpft werden können. Dies hat aber auch zur Folge, dass T-Gedächtnis-Zellen von Autoantigenen restimuliert werden können, die von naiven T-Lymphozyten ignoriert worden wären. Die Differenzierung von naiven und T-Gedächtnis/Effektor-Lymphozyten ist durch Markierung der Oberflächenstrukturen CD45RA und CD45R0 möglich. Es handelt sich um Isoformen des „allgemeinen Leukozytenantigens“ (Transmembranprotein Tyrosinphosphatase CD45), die für die Signalgebung in T-Zellen von essentieller Bedeutung sind. Aktivierte T-Gedächtnis/EffektorZellen exprimieren die Isoform CD45R0 mit niedrigerem Molekular-gewicht, die sich mit dem TZell-Rezeptor-Komplex (TCR-CD3-Komplex, Σ-Homodimer, CD4-Korezeptor) zusammenlagern kann und durch Enthemmung von bestimmten Kinasen die Signalgebung des Rezeptors erleichtert. Die Isoform naiver T-Zellen CD45RA (mit höherem Molekulargewicht) ist dazu nicht in der Lage (Young et al., 1997). Das CD45 enkodierende Gen liegt auf Chromosom 1q31-32 und umfasst 35 Exone. Alternatives Splicing der Exone 4,5 und 6 (synonym A,B und C) bringt insgesamt 5 Isoformen hervor, die sich in der extrazellulären Domäne unterscheiden. Eine genetisch determinierte Variante der CD45-Expression (Punktmutation in Exon 4) wurde in einer kleinen Prozentzahl einer Population gefunden und war verbunden mit dem Vorhandensein von Isoformen sowohl mit niedrigerem als auch mit höherem Molekulargewicht auf T-Gedächtnis/Effektor-Zellen. Dies resultierte in abnormal hoher CD45-Aktivität und prolongierter T-Zell-Aktivation, so dass eine Rolle dieses Exon 4 C77G-Polymorphismus in der Entwicklung von einigen Autoimmunerkrankungen gesehen wurde (Schwinzer et al., 2003). Einleitung 20 Eine von Jacobsen et al. (2000) gefundene Assoziation des C77G-Polymorphismus mit der Entwicklung einer MS konnte jedoch in der Mehrzahl von Folgestudien in verschiedenen Populationen und einer Metaanalyse nicht bekräftigt werden (Gomez-Lira et al., 2003). Durch die Selektion im Thymus haben T-Zell-Rezeptoren in der Regel eine niedrigere Affinität für Autoantigene als für fremde Antigene. Wenn das Fremdantigen in der Hierarchie eines gegebenen T-Zell-Rezeptors viel höher liegt als das Autoantigen, kann die Aktivierung der TZelle durch das („superagonistische“) Fremdantigen dazu führen, dass die resultierende Gedächtniszelle nach Kontakt mit dem Fremdantigen anergisch geschaltet wird oder durch Apoptose untergeht. Dieses Phänomen bezeichnete Kuchroo als protektives/regulatorisches Gedächtnis gegenüber dem Selbst. Ist allerdings das Fremdantigen niedriger in der Hierarchie als das Autoantigen, wird die resultierende Gedächtniszelle eine gesteigerte Ansprechbarkeit und eine niedrigere Aktivierungsschwelle gegenüber dem Autoantigen zeigen und somit das Potential haben, eine Autoimmunreaktion zu induzieren. Dieses Phänomen bezeichnete Kuchroo als pathogenes Gedächtnis gegenüber dem Selbst (Kuchroo et al., 2002). Autoreaktive aktivierte T-Zellen können durch ein Zusammenspiel von zellulären Adhäsionsmolekülen, Chemokinen und Metalloproteasen unspezifisch die Blut-Hirn-Schranke überwinden und so ins ZNS gelangen (Kieseier et al., 1999). Stoßen sie dort auf ihr Zielantigen, reichern sie sich lokal an und schädigen durch toxische Zytokine wie TNF-α und IFN-γ sowie Proteasen, Stickstoffmonoxid und Sauerstoffradikale die Myelinscheiden und Axone. Neben inflammatorischen TH1-Zellen können in diesem Prozess auch andere Bestandteile der adaptiven Immunität wie autoreaktive Antikörper aus Plasmazellen sowie zytotoxische (CD8+) T-Zellen eine Rolle spielen, des Weiteren Komponenten der unspezifischen Immunität wie Makrophagen, Granulozyten, Komplementfaktoren, etc. (Gold & Rieckmann, 2000; Rosche et al., 2003). Einleitung Abbildung 6. Gewebeschädigung im akuten Schub (nach Giovannoni & Hartung, 1996). 21 Einleitung 1.3 22 Zielsetzung der Arbeit Im Rahmen der hier dargestellten Arbeit soll untersucht werden, ob und inwieweit sich MSPatienten von gesunden Kontrollpersonen und Patienten mit anderen neurologischen Erkrankungen in Bezug auf den prozentualen Anteil der untersuchten von Blut-Lymphozyten synthetisierten Zytokine unterscheiden und ob die Ergebnisse mit dem geschilderten TH1/TH2Paradigma in Einklang zu bringen sind. Durch die zusätzliche Bestimmung des prozentualen Anteils von naiven und T-Gedächtnis/Effektor-Helferzellen soll untersucht werden, ob deren Verhältnis sich in den eingeschlossenen Untergruppen unterscheidet. Von besonderem Interesse ist, ob sich verschiedene Entitäten der MS (z.B. die schubförmige Verlaufsform und chronisch-progrediente Verlaufsform) abgrenzen lassen im Sinne einer immunologischen Subtypisierung. Auf diese Weise charakterisierte Patienten könnten in Zukunft möglicherweise spezifischer als bisher behandelt werden. Eine weitere interessante Fragestellung ist, ob sich unterschiedliche Zytokinmuster bei schubförmigen MS-Patienten im akuten Schub und im schubfreien Intervall eruieren lassen. Da in Längsschnittstudien beschrieben wurde, dass der Anstieg proinflammatorischer Zytokine einem Schub vorausgeht (Rieckmann et al., 1994; Olsson, 1995; Rentzos et al., 1996), könnte eine Therapie bei Nachweis eines schubtypischen Zytokinmusters frühzeitiger erfolgen. Aus MRT-Verlaufsstudien ist des Weiteren bekannt, dass entzündliche Läsionen auch ohne klinische Symptomatik im Verlauf der Erkrankung entstehen können (Gehlen, 1997). Da eine Anhäufung solcher subklinischer Läsionen jedoch beispielsweise zu kognitiven Defiziten führen kann, wäre gegebenenfalls auch die Detektion subklinischer entzündlicher Aktivität relevant (Calabrese, 1997). Methodik 2 23 Methodik In diesem Kapitel werden zunächst die Auswahlkriterien der teilnehmenden Patienten und gesunden Kontrollpersonen dargestellt. Es folgt eine Auflistung der verwendeten Materialien. Daraufhin werden Bestimmung der die verwendeten Zytokinsynthese Nachweisverfahren auf Einzelzell-Niveau zur und durchflusszytometrischen zur Markierung der Oberflächenantigene beschrieben. Die konkreten experimentellen Schritte werden zur besseren Übersichtlichkeit nach vorangehender Erläuterung in Form einer Arbeitsanleitung aufgelistet. Das Kapitel schließt mit der Darstellung der verwendeten statistischen Analyseverfahren der experimentellen Daten. 2.1 Auswahl der Patienten und gesunden Kontrollpersonen Folgende Gruppen von Patienten und gesunden Kontrollpersonen nahmen an der Studie teil: Gruppe A: 30 gesunde Kontrollpersonen im Alter von 20 Jahren bis 65 Jahren, Durchschnittsalter 37,73 Jahre; 8 männlichen und 22 weiblichen Geschlechts. Gruppe B: 25 Patienten mit Multipler Sklerose im Alter von 18 Jahren bis 65 Jahren, Durchschnittsalter 39,64 Jahre; 8 männlichen und 17 weiblichen Geschlechts. 14 Patienten waren an schubförmiger MS erkrankt, davon konnten 3 im akuten Schub noch vor geplanter Kortikoidstoßtherapie einbezogen werden. 11 Patienten waren an chronisch-progredienter MS erkrankt. Gruppe C: 35 Patienten mit anderen neurologischen Erkrankungen (other neurological diseases, OND) im Alter von 18 Jahren bis 65 Jahren, Durchschnittsalter 43,06 Jahre; davon 25 mit nicht inflammatorischer und 10 mit inflammatorischer (entzündlicher, paraneoplastischer und autoimmuner) Genese. 14 Patienten waren männlichen und 21 weiblichen Geschlechts. Methodik 24 Tabelle 3. Erkrankungen der Patienten in Gruppe C. Erkrankung Patientenanzahl Inflammatorische OND 10 Patienten Postinfektiöse Enzephalitis 1 Patient Dermatomyositis 1 Patient Paraneoplastische Kleinhirndegeneration 1 Patient Lymphozytäre Meningitis 2 Patienten PNP bei Hashimoto-Thyreoditis 1 Patient Myasthenia gravis 1 Patient Paraneoplastische Monoparese linkes Bein 1 Patient Herpes Enzephalitis 1 Patient Zerebelläre Ataxie bei Hashimoto-Thyreoditis 1 Patient Nicht inflammatorische OND 25 Patienten Syringomyelie 1 Patient M. Parkinson 9 Patienten Alkoholtoxische Polyneuropathie 2 Patienten Zervikale Myelopathie 1 Patient Medikamentös induzierte PNP 1 Patient Epilepsie 2 Patienten Ischämischer zerebraler Insult 3 Patienten Machado-Joseph-Disease 1 Patient Idiopathische Sinusvenenthrombose 1 Patient Spannungskopfschmerz 1 Patient Migräne 1 Patient Lumbale Myelopathie 1 Patient Hallervorden-Spatz-Syndrom 1 Patient 2.1.1 Allgemeine Einschlusskriterien Alter: 18 - 65 Jahre Jede teilnehmende Person musste eine schriftliche Einverständniserklärung abgeben. Bei jedem Patienten wurde eine Medikamentenanamnese sowie eine Anamnese zum Ausschluss anderer Erkrankungen als der Grunderkrankung durchgeführt. Bei jeder gesunden Kontrollperson wurden anamnestisch Krankheiten mit vermuteter oder nachgewiesener immunologischer Implikation, typischerweise aus dem allergischen, rheumatischen und dermatologischen Formenkreis wie auch entzündliche Darmerkrankungen ausgeschlossen. Methodik 2.1.2 25 Einschlusskriterien in die MS-Patientengruppe Nach den Poser-Kriterien (1983) klinisch oder laborunterstützt gesicherte MS Schubförmige MS-Patienten mit einer Schubfrequenz von mindestens zwei pro Jahr Chronisch-progrediente MS-Patienten mit einer Progredienz von mindestens 0,5 Punkten auf der EDSS-Skala pro Jahr EDSS-Wert von < 6 Tabelle 4. Zusammenfassung der expanded disability status scale (EDSS) (nach Kurtzke, 1983). Grad Befund 0 Neurologischer Referenzbefund 1 Keine Behinderung, abnorme Untersuchungsbefunde 2 Minimale Behinderung 3 Mäßiggradige Behinderung 4 Gehfähig ohne Hilfe für mindestens 500 m 5 Gehfähig ohne Hilfe für mindestens 200 m, starke Einschränkung der Arbeitsfähigkeit 6 Gehhilfe, Stock etc. nötig, um 100 m zu gehen 7 Rollstuhlpflicht (weniger als 5 m gehfähig) 8 Bett oder Rollstuhl, Hilfe bei der Körperpflege 9 Hilflos bettlägeriger Patient, erhaltene Kommunikations- und Essfähigkeit 10 Tod infolge Multipler Sklerose 2.1.3 Ausschlusskriterien Als Ausschlusskriterien galten bei allen 3 Gruppen: Immunsuppressive oder immunmodulierende Therapie, Vakzination innerhalb der letzten 90 Tage vor Aufnahme in die Studie Akute infektiöse Erkrankungen wie z.B. Harnwegsinfekt, Bronchitis, Infektionen des Gastrointestinaltrakts oder grippaler Infekt zum Zeitpunkt der Blutabnahme, innerhalb der vorangegangenen 4 Wochen sowie 2 Wochen danach (abgesehen von der Grunderkrankung bei inflammatorischen OND) Schwangerschaft oder Stillzeit Anamnestisch überlieferte Krankheiten unbekannter Ätiologie Methodik 2.2 Materialien 2.2.1 Geräte und Gebrauchsmaterialien 26 Tabelle 5. Geräte und Gebrauchsmaterialien. Durchflusszytometer FACScan® Sysmex-NE Hämatologisches Becton Dickinson (BD) Analysensystem (kleines Digitana AG Blutbild und Differentialblutbild) Kühlschrank „Santo“ (bis +4°C) AEG Gefrierschrank „Santo“ (bis -20°C) AEG Sicherheitssterilbank Heraeus Instruments Begasungsbrutschrank Heraeus Electronic Zentrifuge Minifuge RF Heraeus Sepatech Lichtmikroskop Zeiss Neubauerzählkammer W. Schreck Vortexer L48 GLW Gewebekulturplatten Microtest 3 Falcon/BD (96 well flat bottom) Präzisionspipetten Eppendorf/Finn Pipettenspitzen Greiner Combitips 12,5 ml Greiner Reagenzröhrchen 50 ml konisch „Blue Max“ Falcon/BD Reagenzröhrchen „Stil“ 12x75 mm Falcon/BD Messzylinder, Eppendorfgefäße Schott Venofix Venenpunktionskanüle Braun Lithium-Heparinat-Röhrchen 5 und 10 ml Kabe Labortechnik EDTA-Kalium-Röhrchen 3,5 ml Kabe Labortechnik Zellstofftupfer Pur-Zellin Hartmann Einmalhandschuhe Baxter Cutasept F Desinfektionsspray Bode 2.2.2 EDV Tabelle 6. EDV. Macintosh Quadra 650 Apple/Macintosh Drucker HP Deskjet 1200C/PS Hewlett-Packard Software: CellQuest ® Version 1.2 Apple/Macintosh/BD Methodik 2.2.3 27 Reagenzien Tabelle 7. Reagenzien. Ficoll separating solution (isotonisch, Dichte 1,077) Seromed Biochrom KG Berlin RPMI Medium 1640 mit L-Glutamin Gibco BRL Life Technologies Dimethylformamid (DMF) D-8654 Sigma Trypanblau 0,4% Gibco BRL Life Technologies Natriumhydrogencarbonat Merck Foetal bovine serum Gibco BRL Life Technologies (FBS, heat inactivated, Mycoplasmen and virus screened) 2.2.4 Antikörper gegen Oberflächenantigene Tabelle 8. Antikörper gegen Oberflächenantigene. mouse anti-human anti-CD45R0-PE-konjugiert BD mouse anti-human anti-CD45RA-FITC-konjugiert BD mouse anti-human PE und FITC-konjugierte Isotypenkontrolle BD mouse anti-human anti-CD4-PE-Cy5-Tandemkonjugat Immunotech mouse anti-human PE-Cy5-konjugierte Isotypenkontrolle Immunotech 2.2.5 ICS-Kits (intracellular staining kits) Alle ICS-Kits von Hölzel Diagnostika/Laboserv beinhalten folgende Reagenzien: Stimulatoren 1 - 3 (Lyophilisat) HBSS (Hank`s balanced salt solution)-Puffer Fixativ (Paraformaldehyd) (Stocklösung) Permeabilisator (Saponin) (Stocklösung) Methodik 28 Tabelle 9. Antikörper zur intrazellulären Zytokinmarkierung. human TNFα-ICS-Kit: Monoklonaler mouse anti-human anti-TNF-α-Antikörper (FITC-konjugiert) human IFN-γ-ICS-Kit: Monoklonaler mouse anti-human anti-IFN-γ-Antikörper (FITC-konjugiert) human IL-2-ICS-Kit: Monoklonaler mouse anti-human anti-IL-2-Antikörper biotinyliert Streptavidin-PE-Konjugat human IL-4-ICS-Kit: Monoklonaler mouse anti-human anti-IL-4-Antikörper biotinyliert Streptavidin-PE-Konjugat human lL-10-ICS-Kit: Monoklonaler mouse anti-human anti-IL-10-Antikörper biotinyliert Streptavidin-PE-Konjugat 2.3 Experimentelle Methodik 2.3.1 Blutentnahme Jedem Probanden wurden 3 ml venöses Blut in EDTA (Di-Kalium-Ethylendiamintetraazetat) für die Bestimmung des Differentialblutbildes sowie 20 ml venöses Blut in Lithium-Heparinat für die intrazelluläre Zytokinmessung entnommen. 2.3.2 Differentialblutbild Die Bestimmung der Leukozytenzahl sowie der prozentualen Anteile von Lymphozyten, Granulozyten (neutrophile, eosinophile und basophile) und Monozyten erfolgte mittels Zählautomat nach dem Coulter-Prinzip. Dies beruht auf der quantitativen Bestimmung der Blutzellen durch Impedanzmessung. In Abhängigkeit von der Größe der Zellen kommt es zu Widerstandsänderungen in einem Gleichstromkreis zwischen zwei Behältern mit Elektrolytlösungen, von denen einer die verdünnte Blutprobe enthält. 2.3.3 Intrazelluläre Zytokinmessung mittels Durchflusszytometrie 2.3.3.1 Übersicht Der direkte Nachweis von Zytokinen im peripheren Blut erbrachte bei der Multiplen Sklerose uneinheitliche Ergebnisse (Sivieri et al., 1998). Dies wurde u.a. darauf zurückgeführt, dass der Wirkungsradius der Zytokine begrenzt ist. Messungen, in denen Zytokine nach Inkubation im Überstand bestimmt werden, haben den Nachteil, dass die Charakterisierung der Methodik 29 zytokinproduzierenden Zelltypen nicht möglich ist. Die Durchflusszytometrie ermöglicht den Zytokinnachweis auf Einzelzell-Niveau. Das Prinzip der von Jung 1993 etablierten Methode besteht darin, aus Vollblut isolierte Lymphozyten zur Produktion von Zytokinen anzuregen und gleichzeitig ihre Sekretion zu hemmen, so dass die Zytokine in den Zellen akkumulieren. Im Anschluss werden die Zellen fixiert und ihre Zellmembranen permeabilisiert, woraufhin zugegebene Fluoreszenzfarbstoff-markierte Antikörper (hier gegen IFN-γ, TNF-α, IL-2, IL-4 und IL-10) in die Zellen eindringen können (Jung et al., 1993). Das Ergebnis der Messung spiegelt letztlich nicht die tatsächliche Zytokinproduktion wider, sondern die Bereitschaft der Zelle, das jeweilige Zytokin zu synthetisieren. Anhand von simultan hinzugegebenen mit einem anderen Fluoreszenzfarbstoff konjugierten Antikörpern gegen das Oberflächenantigen CD4 als Marker von T-Helfer-Zellen können die zytokinproduzierenden Zellen charakterisiert werden. In einem parallelen Ansatz werden Antikörper gegen CD45RA als Marker naiver T-Zellen und CD45R0 als Marker von T-Zellen nach Antigenkontakt zugefügt, um den prozentualen Anteil CD45RA+ und CD45R0+ Lymphozyten Zellen in der Probe zu bestimmen. Die so präparierten Zellen werden mit Hilfe eines Durchflusszytometers analysiert. Die Durchflusszytometrie ermöglicht die Messung verschiedener physikalischer und chemischer Eigenschaften von Zellen, die hintereinander in einem Flüssigkeitsstrom angeordnet separat untersucht werden. Dabei können Fluoreszenz- und Streulichtsignale gleichzeitig gemessen werden. Die Messung der Lichtstreuung erlaubt Aussagen über Zelleigenschaften wie Größe und Granularität, so dass sich auf diese Weise Lymphozyten, Granulozyten und Monozyten unterscheiden lassen. Das zur Verfügung stehende Analysegerät FACScan® (fluorescence activated cell sorter and analyzer) erlaubt darüber hinaus die simultane Detektion dreier verschiedener Fluoreszenzfarbstoffe. Die von uns verwendeten Fluoreszenzfarbstoffe Fluoreszeinisothiozyanat (FITC), Phykoerythrin (PE) und Phykoerythrin-Zyanin-5 (PE-Cy5) bieten geeignete Absorptions- und Emissionsoptima. Die folgenden Reaktionsansätze ermöglichen eine Messung von TNF-α, IFN-γ, IL-2, IL-4 und IL-10 sowie die Identifikation der Herkunft der Zytokine von CD4+ bzw. CD4- Lymphozyten. Parallel kann der Anteil von naiven und aktivierten T-Lymphozyten anhand der Marker CD45RA und CD45R0 in der gemessenen Population bestimmt werden. Methodik 30 2.3.3.2 Schema der Reaktionsansätze Tabelle 10. Reaktionsansätze. Ansatz Kanal 1 (FL1): FITC- Kanal 2 (FL2): PE- Kanal 3 (FL3): PEDetektion Detektion Cy5-Detektion Isotypenkontroll- Isotypenkontroll- Isotypenkontroll- antikörper antikörper antikörper 2 Anti-CD45RA Anti-CD45R0 3 Anti-IFN-γ Anti-IL-2 Anti-CD4 4 Anti-TNF-α Anti-IL-4 Anti-CD4 5 Anti-CD4 Anti-IL-10 1 (Negativkontrolle) 2.3.4 Spezielle Methodik und Durchführung 2.3.4.1 Ansetzen der Reagenzien Durchführung: Lyophilisat der Stimulatoren 1 - 3 in je 100 µl DMF lösen Aliquotieren: Je 10 µl Stimulatorlösung in ein Eppendorfgefäss pipettieren, einfrieren Für den Gebrauch Aliquot auftauen und frisch mit 90 µl Kulturmedium auffüllen HBSS-Pulver in 1000 ml Aqua bidestillata auflösen 350 mg Natriumhydrogenbicarbonat zugeben Fixierungslösung 1:10 mit HBSS verdünnen Permeabilisatorlösung 1:100 mit HBSS verdünnen Kulturmedium: 450 ml RPMI-Medium mit 50 ml FBS versetzen 2.3.4.2 Lymphozytenisolierung mittels Ficoll-Gradient Mit Hilfe des Ficoll-Gradienten wurden Lymphozyten aus Vollblut isoliert. Aufgrund der unterschiedlichen Dichte der Blutelemente konnten nach Zentrifugation der Blutprobe mit Ficoll-Lösung (Dichte von 1,077 g/ml) die Lymphozyten in einer separaten Schicht abpipettiert werden. Nach zwei Waschvorgängen zum Entfernen von Verunreinigungen durch Erythrozyten und Thrombozyten sowie Ficoll-Resten wurden die Lymphozyten dann weiter präpariert. Methodik 31 Abbildung 7. Lymphozytenisolierung mittels Ficoll-Gradient (Jacobs, 1996). Nach Zentrifugation von vorsichtig auf Ficoll-Lösung geschichtetem Vollblut (links) bei etwa 1000g bildet sich eine charakteristische Schichtung (rechts). Die vier Schichten von unten nach oben: 1. Erythrozyten/Granulozyten 2. Wässrig durchsichtige Ficoll-Lösung 3. Weißlich schimmernde dünne Schicht mit Lymphozyten und Monozyten 4. Plasma mit Thrombozyten. Durchführung: In einem 50 ml Falcon-Röhrchen 10 ml heparinisiertes Vollblut vorsichtig auf 20 ml Ficoll-Lösung schichten, die beiden Flüssigkeiten dürfen sich nicht vermischen 20 min ungebremst bei 2000 U/min zentrifugieren Interphase mit Lymphozyten vorsichtig abpipettieren, in ein weiteres Röhrchen füllen und mit Kulturmedium auffüllen Waschen: 10 min bei 1200 U/min zentrifugieren Überstand dekantieren Röhrchen mit Kulturmedium auffüllen und Waschvorgang einmal wiederholen Pellet in 1 ml Kulturmedium aufnehmen 2.3.4.3 Zellzahlbestimmung Die isolierten Zellen wurden unter dem Mikroskop mittels einer Neubauerkammer gezählt. Durch die Verdünnung mit Trypanblau-Lösung war eine Beurteilung der Vitalität der Zellen und dementsprechend eine Qualitätskontrolle der Präparation möglich, da Trypanblau in tote Zellen eindringt. Um vergleichbare Bedingungen für verschiedene Blutproben zu schaffen, wurde die Zellkonzentration auf 2 x 106/ml eingestellt. Durchführung: Zellsuspension vorsichtig gut durchmischen Methodik 32 10 µl Probe entnehmen und in ein Eppendorfhütchen mit 90 µl Trypanblau-Lösung pipettieren Probe auf Neubauerkammer auftragen Zellzahl bestimmen: 4 x 16 Quadrate auszählen, arithmetisches Mittel bilden und mit 105 multiplizieren Zellsuspension in geeigneten Verdünnungsschritten mit Kulturmedium verdünnen und auf eine Zellkonzentration von 2 x 106/ml einstellen Abbildung 8. Zellzählung mittels Neubauerkammer (Jacobs, 1996). Die Kammer (links) enthält zwei Zählgitter, eines davon ist rechts vergrößert dargestellt. 2.3.4.4 Stimulation und Sekretionshemmung Die Lymphozyten wurden zur Produktion der Zytokine angeregt (Stimulation mit Ionomyzin und Phorbol-12-Myristat-13-Azetat (PMA), im Folgenden Stimulatoren 1 und 2 genannt). Gleichzeitig wurde die Sekretion durch Monensin (im Folgenden Stimulator 3 genannt) gehemmt. Monensin bewirkt die Zerstörung des Ionengradienten in biologischen Membranen und führt damit zur Unterbrechung intrazellulärer Transportprozesse. Hierdurch kommt es zu einer Anreicherung der Zytokine im Bereich des Golgi-Komplexes. In diesem Arbeitsschritt wurden des Weiteren die Oberflächenantikörper (CD4, CD45RA/R0) hinzugefügt. Durchführung: Je 200 µl Zellsuspension in ein Depot einer 96er Mikrotiterplatte geben Pro Reaktionsansatz werden 2 Depots bestückt Nun je 5 µl der Oberflächenantikörper in die entsprechenden Depots pipettieren Eingefrorene aliquotierte Stimulatorlösungen 1 - 3 im Verhältnis 1:10 verdünnen Je 2 µl Stimulatorlösung 1 - 3 pro Depot zugeben, durchmischen Fünf Stunden Inkubation der so bestückten Mikrotiterplatte unter konstanten Bedingungen im Brutschrank (37°C, 7% CO2-Spannung) Methodik 33 2.3.4.5 Fixierung und Permeabilisierung Im Anschluss an die Inkubation wurden die Zellen mit Paraformaldehyd fixiert und mit Saponin permeabilisiert. Dies ermöglichte den Durchtritt von Antikörpern in den Intrazellulärraum der Lymphozyten bei Erhaltung der meisten Oberflächenstrukturen. Durchführung: Zellen von der Mikrotiterplatte ernten: Zellsuspension abpipettieren, mit HBSS spülen, den Inhalt von je 2 Depots (= 1 Reaktionsansatz) in ein entsprechendes FACS-Röhrchen pipettieren 2 - 3 ml HBSS in jedes FACS-Röhrchen geben und 5 min bei 1200 U/min zentrifugieren Überstand dekantieren, Vorgang einmal wiederholen Zellpellet in 1ml kalter Fixierungslösung aufnehmen, mehrfach mit 1ml Pipette resuspendieren 5 min im Kühlschrank bei +4°C inkubieren 3 ml HBSS hinzugeben, schwenken und bei 1200 U/min 5 min zentrifugieren Überstand dekantieren, Vorgang einmal wiederholen Zellen in 100 µl Permeabilisierungslösung resuspendieren Inkubation im Kühlschrank bei +4°C über Nacht (für mindestens 60 min bis zu 24 h möglich) 2.3.4.6 Intrazellulärer Zytokinnachweis Am folgenden Morgen wurden die Markierungen intrazellulärer Zytokine durchgeführt. Die Interleukine-2, -4 und -10 wurden mit Hilfe von biotinylierten Antikörpern nachgewiesen, die in einem zweiten Schritt mit Streptavidin-PE-Konjugat inkubiert wurden, welches spezifisch mit dem Biotin der Antikörper reagierte. IFN-γ und TNF-α wurden mit direkt FITC-konjugierten Antikörpern markiert. Methodik 34 Abbildung 9. Immunfluoreszenz (Jacobs, 1996). Immunfluoreszenz mit direkt (links; IFN-γ und TNF-α) und indirekt (rechts; IL-2, -4 und -10) Fluoreszenzfarbstoff-markierten Antikörpern. Durchführung: Im Falle der PE-Messung (IL-2, -4 und -10) je 2 µl des biotinylierten Antikörpers zur Zellsuspension in die vorgesehenen Depots geben, gut durchmischen 20 min im Kühlschrank bei +4°C inkubieren Mit 2 ml Permeabilisierungslösung auffüllen und bei 1200 U/min für 5 min zentrifugieren Überstand dekantieren Pellet in 100 µl Permeabilisierungslösung resuspendieren 2 µl Streptavidin-PE-Konjugat dazugeben, gut durchmischen Im gleichen Schritt je 2 µl FITC-markierten Antikörper (IFN-γ und TNF-α) in die vorgesehenen Depots hinzufügen 20 min bei +4°C inkubieren 2 ml Permeabilisierungslösung dazugeben und bei 1200 U/min für 5 min zentrifugieren. Überstand dekantieren, 500 µl HBSS zugeben Aufbewahrung im Kühlschrank bei +4°C für maximal 24 h möglich Die auf diese Weise präparierten Proben wurden anschließend mit Hilfe des Durchflusszytometers analysiert. 2.3.4.7 Durchflusszytometrische Messung Zur Analyse im Durchflusszytometer werden mittels fluoreszierender Antikörper markierte Zellen über ein Schlauchsystem aufgesaugt und durch Überdruck in die Meßküvette injiziert. Um Signale von einzelnen Zellen erfassen zu können, muss gewährleistet sein, dass die Zellen Methodik 35 separat den Analysepunkt passieren. Dies wird durch das Prinzip der hydrodynamischen Fokussierung erreicht, indem der Probenstrom im Zentrum der konisch geformten Küvette durch einen sogenannten Mantelstrahl stabilisiert und verengt wird. Die Zellen werden so beschleunigt und hintereinander aufgereiht und gelangen dann einzeln in die Messkammer. Am Analysepunkt trifft der Laserstrahl auf die einzelne Zelle. Mit geeigneten Detektoren in Form von Photodioden und Photoröhren werden die Signale von Streulicht und Fluoreszenz, die aus der Interaktion von Lichtstrahl und Zelle resultieren, erfasst. Die Detektoren erzeugen einen zum optischen Signal proportionalen elektrischen Impuls, welcher im Folgenden verstärkt und digitalisiert wird. Abbildung 10. Fluoreszenzanalyse am Beispiel eines 4-Kanal-Gerätes (Jacobs, 1996). 2 Kanäle für die Streulichtdetektion (FSC und SSC), 2 Kanäle für die Detektion von jeweils mit PE- und FITC-konjugierten Antikörpern erzeugte Signale. Die digitalisierten Signale werden in einem Mehrkanalsystem registriert und können mit dem integrierten Softwarepaket CellQuest® graphisch und numerisch dargestellt und analysiert werden. In Richtung des einfallenden Laserstrahls gestreutes Licht wird als Vorwärtsstreulicht (FSC = forward light scatter) bezeichnet und erlaubt Aussagen über die Zellgröße. Im rechten Winkel zum einfallenden Lichtstrahl gestreutes Licht (Rechtwinkelstreulicht, SSC = sideward light scatter) hängt hauptsächlich von der Zellgranularität (Oberflächeneigenschaften und intrazelluläre Einschlüsse) ab. Anhand einer Darstellung dieser Streulichtsignale mittels zweidimensionaler dot plot-Graphen (Abszisse - FSC; Ordinate - SSC) können die Zellen Methodik 36 morphologisch differenziert werden. Abbildung 11 zeigt einen dot plot mit verschiedenen abgrenzbaren Punktwolken, die verschiedene Zellpopulationen einer Analyse von Vollblut enthalten. Der erhaltene dot plot erlaubt Aussagen über die Qualität der zur Lymphozytenisolierung durchgeführten Ficoll-Separation. Die Lymphozytengesamtpopulation lässt sich von Verunreinigungen durch Zelltrümmer und andere Zellarten differenzieren und kann als Punktwolke mit einem Fenster umgeben werden (gating). Die Software betrachtet daraufhin nur die Zellen in diesem gate (entsprechend 100%) als Ausgangspopulation für weitere Analysen. Abbildung 11. Dot plot der Streulichtsignale von Vollblut (Jacobs, 1996). Abbildung 12. Dot plot einer Blutprobe nach Lymphozytenisolierung mittels Ficoll-Gradient. Gating der Lymphozytengesamtpopulation. Das zur Verfügung stehende FACScan ® Methodik 37 erlaubt darüber hinaus neben der zweikanaligen Streulichtdetektion als Fünfkanalgerät die Erfassung dreier Fluoreszenzfarbstoffe. Um falsch positive Resultate durch unspezifische Antikörperbindung und Autofluoreszenz zu eliminieren, erfolgt vor der Messung der intrazellulären Zytokine und Oberflächenmarker eine Negativkontrolle. Mit Isotypenkontrollantikörpern wird das Ausmaß unspezifischer Bindung ermittelt. Hierzu werden Fluoreszenzfarbstoff-markierte Antikörper derselben Immunglobulinsubklasse wie für die anderen Markierungen (hier IgG1), allerdings ohne Spezifität für Epitope auf oder in menschlichen Blutzellen, verwendet. Darüber hinaus zeigen Zellen bei Beleuchtung mit dem Laserstrahl aufgrund ihrer chemischen Zusammensetzung auch ohne fluoreszierenden Farbstoff eine gewisse Fluoreszenz, die als Autofluoreszenz bezeichnet wird. Durch Messung der Negativkontrolle können dementsprechend Fluoreszenzsignale, die durch unspezifische Antikörperbindung und physiologische Autofluoreszenz bedingt sind, identifiziert werden und als „negativ“ gekennzeichnet werden. Durch Fluoreszenzfarbstoff bedingte Signale werden als „positiv“ charakterisiert. Abbildung 13. Unspezifische Antikörperbindung (Jacobs, 1996). Darstellung einer unspezifischen Antikörperbindung (links, hier über Fc-Rezeptoren) neben der spezifischen Antikörper/AntigenBindung (rechts). Anhand des Fluoreszenzhistogramms in Abbildung 14 wird deutlich, wie die Software durch den Schwellenwert, der die links des Markers gelegene Hintergrundfluoreszenz ausschließt, positive Signale (rechts des Markers) diskriminieren kann. Man erhält dadurch die prozentuale Verteilung der negativen und positiven Zellen, wobei die Expressionsdichte entsprechenden Moleküls durch die Höhe der Fluoreszenzintensität repräsentiert wird. des Methodik 38 Abbildung 14. Histogramme der Fluoreszenzintensität gegen die Zellzahl (Jacobs, 1996). Links der Graph einer Negativkontrolle ohne Farbstoff mit Nachweis der physiologischen Autofluoreszenz links des Markers (Cursor). Nur rechts des Markers gelegene Signale werden berücksichtigt und als positiv bezeichnet, im rechten Histogramm beispielhaft für mit CD3-Antikörpern angefärbte Lymphozyten dargestellt. Der Fluoreszenzfarbstoff wird durch das monochromatische Licht (λ = 488 nm) angeregt und emittiert Lichtsignale von bekannter Wellenlänge, die mit geeigneten Photodetektoren erfasst werden können (siehe Abbildung 10). Das FACScan® verfügt über drei Photodetektoren, die jeweils unterschiedliche Fluoreszenzen nachweisen können: FL1 (Spektralmessbereich λ = 515 - 545 nm) erfasst Emissionen des Farbstoffes Fluoreszeinisothiozyanat (FITC), während Phykoerythrin (PE) von Kanal FL2 (Spektralmessbereich λ = 564 - 606 nm) und PhykoerythrinZyanin-5 (PE-Cy5) von Kanal FL3 (Spektralmessbereich λ > 650 nm) detektiert werden. Abbildung 15. Kontourgraph für Doppelfluoreszenz (Jacobs, 1996). Quadrant 3 beinhaltet für beide Antigene negative Zellen. In den Quadranten 1 und 4 liegen jeweils für ein Antigen positive Zellen. In Quadrant 2 liegen für beide Antigene positive Zellen. Methodik 2.4 39 Auswertungsprotokoll Unmittelbar im Anschluss an die Markierung der Proben mittels Fluoreszenzfarbstoffkonjugierter Antikörper zur intrazellulären Zytokinanfärbung erfolgte die durchflusszytometrische Messung. Die Akquisition und Auswertung der erhaltenen Daten wurde standardisiert nach folgendem Protokoll vorgenommen: Kontrolle der Geräteeinstellungen Negativkontrolle (Ansatz 1, siehe Tabelle 10) Messvorgang (Beendigung des Messvorgangs jeweils nach insgesamt 10.000 registrierten Ereignissen [events]) Gating der Lymphozytengesamtpopulation über Streulichtsignale im gate G1 des initialen dot plot-Graphen Im Ansatz 2 Bestimmung des prozentualen Anteils CD45RA+ bzw. CD45R0+ Lymphozyten In den Ansätzen 3 - 5 Selektion der CD4+ bzw. CD4- Lymphozyten und Markierung des Anteils für die jeweiligen angefärbten Zytokine positiver Lymphozyten mittels entsprechender Histogramme Übertragung der prozentualen Verteilungen in die statistische Datenverarbeitung Anhand von Abbildung 16 wird die Bestimmung des prozentualen Anteils IFN-γ-produzierender jeweils CD4+ und CD4- Lymphozyten erläutert. Der dot plot links oben zeigt auf Kanal 1 (FL1, Abszisse) die Registrierung von Fluoreszenzereignissen durch IFN-γ-FITC-markierte Antikörper, auf Kanal 2 (FL2, Ordinate) die Registrierung von Fluoreszenzereignissen durch CD4-PE-markierte Antikörper. Im linken unteren Quadranten liegen für beide Antikörper negative Lymphozyten, im rechten unteren Quadranten liegen CD4- IFN-γ-produzierende Lymphozyten und im rechten oberen Quadranten CD4+ IFN-γ-produzierende Lymphozyten. Im linken unteren Histogramm erkennt man das mit R2 gekennzeichnete gate G2, welches Ereignisse von CD4+ Lymphozyten einschließt und für das rechte obere Histogramm sowie die Statistik rechts oben relevant ist. Im dargestellten Fall beträgt der prozentuale Anteil IFN-γsynthetisierender CD4+ Lymphozyten 3,14%. Darüber hinaus ist im linken unteren Histogramm das mit R3 gekennzeichnete gate G3 dargestellt, welches Ereignisse von CD4- Lymphozyten erfasst und für das rechte untere Histogramm sowie die Statistik rechts unten relevant ist. In diesem Fall beträgt der prozentuale Anteil IFN-γ-synthetisierender CD4- Lymphozyten 1,37%. Methodik 40 Abbildung 16. Dot plot und Histogramme zur Bestimmung des prozentualen Anteils IFN-γ-synthetisierender CD4+ und CD4Lymphozyten. 2.5 Statistische Datenanalyse Die statistische Auswertung erfolgte mit Hilfe des Softwarepaketes SPSS Version 9.0.1 (SPSS, München). Eine Voranalyse zeigte, dass die erhobenen Rohdaten in den Übergruppen überwiegend eine Normalverteilung aufwiesen. Wegen der verhältnismäßig kleinen Stichproben, insbesondere hinsichtlich der Untergruppen, wurde jedoch nichtparametrischen Verfahren der Vorzug gegeben. Im Rahmen der deskriptiven Statistik wurde deshalb als Lagemaß der Median verwendet. Die graphische Darstellung erfolgte mittels column scatterDiagrammen (Streudiagrammen), die sich für die Visualisierung der hier vorhandenen Daten eignen. Um Unterschiede zwischen den Versuchsgruppen und somit MS-spezifische Phänomene aufzudecken, wurde der nichtparametrische Mann-Whitney-U-Test für zwei unabhängige Stichproben durchgeführt. Die Analysen erfolgten getrennt für CD4+ und CD4Lymphozyten. Das Signifikanzniveau wurde bei p = 0,05 angesetzt. Ergebnisse 3 41 Ergebnisse Die Darstellung der erhobenen Ergebnisse erfolgt in drei Abschnitten. Zunächst werden die prozentualen Anteile CD45RA+ und CD45R0+ Lymphozyten im Blut der Probanden aufgeführt, danach die prozentualen Anteile Interferon-γ-, Tumornekrosefaktor-α-, Interleukin-2-, + Interleukin-4- und Interleukin-10-produzierender CD4 (T-Helfer-) Lymphozyten sowie CD4Lymphozyten, zuletzt werden die erhobenen Befunde des Differentialblutbildes dargestellt; jeweils erst im Vergleich der drei Übergruppen - Gruppe 1: gesunde Kontrollpersonen (Kontrolle), Gruppe 2: andere neurologische Erkrankungen (OND), Gruppe 3: MS-Patienten (MS) - dann im Vergleich der sechs Untergruppen - Gruppe 1: gesunde Kontrollpersonen (Kontrolle), Gruppe 2: nicht inflammatorische OND (N.I.OND), Gruppe 3: inflammatorische OND (Infl.OND), Gruppe 4: schubförmige MS im schubfreien Intervall (RR-MS) Gruppe 5: schubförmige MS im akuten Schub (Schub-MS) Gruppe 6: chronisch-progrediente MS (CP-MS) - mit Streugrafiken, die Punktwolken der Einzelparameter sowie den zugehörigen Median zeigen. Statistisch signifikante Differenzen werden einschließlich zugehörigem p-Wert mittels durchgezogenen bidirektionalen Pfeilen kenntlich gemacht, knapp über der definierten Signifikanzschwelle von p < 0,05 liegende Differenzen anhand gestrichelter Pfeile. 3.1 Oberflächenmarker CD45RA und CD45R0 Der Oberflächenmarker CD45RA ist charakteristisch für naive T-Lymphozyten, CD45R0 für TEffektor- und T-Gedächtnis-Lymphozyten. 3.1.1 CD45RA Ergebnisse 42 + 3.1.1.1 CD45RA Lymphozyten (Übergruppenvergleich) Die Mediane des prozentualen Anteils naiver Lymphozyten im Blut von Probanden der Kontrollgruppe und der MS-Gruppe zeigten ein vergleichbares Niveau, der Median der ONDGruppe ein etwas niedrigeres Niveau ohne statistisch signifikante Differenz im Vergleich der Übergruppen. % Anteil CD45RA+ Lymphozyten 100 75 50 25 0 Kontrolle OND MS Gruppe Abbildung 17. Prozentualer Anteil CD45RA+ Lymphozyten im Übergruppenvergleich. 3.1.1.2 CD45RA+ Lymphozyten (Untergruppenvergleich) In der Untergruppenanalyse hatte die N.I.OND-Gruppe den niedrigsten Median des prozentualen Anteils naiver Lymphozyten, der Unterschied zur Kontrollgruppe und RR-MSGruppe lag jeweils knapp über der geforderten Signifikanzschwelle. % Anteil CD45RA+ Lymphozyten 100 75 50 25 0,058 0,079 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 18. Prozentualer Anteil CD45RA+ Lymphozyten im Untergruppenvergleich. 3.1.2 CD45R0 Ergebnisse 43 + 3.1.2.1 CD45R0 Lymphozyten (Übergruppenvergleich) Die Kontrollgruppe hatte den niedrigsten Median des prozentualen Anteils von T-Gedächtnis/ Effektor-Lymphozyten. Höher lagen die Mediane der OND-Gruppe und der MS-Gruppe, die Unterschiede zur Kontrollgruppe waren jeweils statistisch signifikant (p = 0,010 bzw. 0,006). 0,006 % Anteil CD45R0+ Lymphozyten 50 0,010 40 30 20 10 0 Kontrolle OND MS Gruppe Abbildung 19. Prozentualer Anteil CD45R0+ Lymphozyten im Übergruppenvergleich. 3.1.2.2 CD45R0+ Lymphozyten (Untergruppenvergleich) Anhand der Mediane der prozentualen Anteile von T-Gedächtnis/Effektor-Lymphozyten konnten die Untergruppen in zwei „Kategorien“ eingeteilt werden: „Kategorie A“: Untergruppen mit einem Median von < 20 (Kontrolle, N.I.OND, RR-MS). „Kategorie B“: Untergruppen mit einem Median von > 20 (Infl.OND, Schub-MS, CP-MS). Bemerkenswert ist, dass jede einzelne der Untergruppen der „Kategorie A“ gegenüber einer beliebigen anderen der „Kategorie B“ (und vice versa) einen statistisch signifikanten Unterschied aufwies. 0,001 0,005 0,002 0,041 0,025 0,015 <0,001 50 % Anteil CD45R0+ Lymphozyten 0,004 <0,001 40 30 20 10 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 20. Prozentualer Anteil CD45R0+ Lymphozyten im Untergruppenvergleich. Ergebnisse 3.1.3 44 CD45RA/R0 Ratio 3.1.3.1 CD45RA/R0 Ratio (Übergruppenvergleich) Die Kontrollgruppe hatte den höchsten Median der CD45RA/R0 Ratio. Niedriger lagen - auf ähnlichem Niveau - die Mediane der OND- und der MS-Gruppe, der Unterschied zur Kontrollgruppe war jeweils statistisch signifikant. 0,014 0,011 CD45RA/R0 Ratio 15 10 5 0 Kontrolle OND MS Gruppe Abbildung 21. CD45RA/R0 Ratio im Übergruppenvergleich. 3.1.3.2 CD45RA/R0 Ratio (Untergruppenvergleich) Es gelten ähnliche Überlegungen wie unter 3.1.2.2, wiederum lassen sich die Untergruppen in zwei „Kategorien“ einteilen: „Kategorie A“: Untergruppen mit einem Median von > 3,5 (Kontrolle, N.I.OND, RR-MS). „Kategorie B“: Untergruppen mit einem Median von < 3,5 (Infl.OND, Schub-MS, CP-MS). Allerdings wiesen hier die Unterschiede der N.I.OND-Gruppe zu den Gruppen der „Kategorie B“ keine statistische Signifikanz auf (Vergleich zwischen N.I.OND- und Kontroll-Gruppe mit p = 0,077 knapp über der geforderten Signifikanzschwelle). Ergebnisse 45 0,001 0,077 0,022 0,012 <0,001 0,008 0,004 CD45RA/R0 Ratio 15 10 5 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 22. CD45RA/R0 Ratio im Untergruppenvergleich. 3.2 Intrazelluläre Zytokine Durchflusszytometrisch wurden die aus dem Blut der Probanden isolierten Lymphozyten simultan hinsichtlich des Oberflächenmarkers CD4, der T-Helfer-Lymphozyten kennzeichnet, und der proinflammatorischen Zytokine IFN-γ, TNF-α, IL-2 sowie der antiinflammatorischen Zytokine IL-4 und IL-10 untersucht. Schließlich wurden die Vergleiche der Zytokinproduktion in den CD4+ und CD4- Lymphozyten der differenzierten Gruppen statistisch analysiert. 3.2.1 IFN-γ-Produktion 3.2.1.1 IFN-γ-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) Den niedrigsten Median des prozentualen Anteils IFN-γ-produzierender T-Helfer-Zellen hatte die Kontrollgruppe mit statistisch signifikantem Unterschied jeweils zur OND- und MS-Gruppe. Der Unterschied zwischen der MS-Gruppe (mit dem höchsten Median) und der OND-Gruppe lag knapp über der geforderten Signifikanzschwelle. Ergebnisse 46 0,079 <0,001 + % Anteil IFN-γ -produzierender CD4 Lymphozyten <0,001 12.5 10.0 7.5 5.0 2.5 0.0 Kontrolle OND MS Gruppe Abbildung 23. IFN-γ-Produktion in CD4+ Lymphozyten im Übergruppenvergleich. 3.2.1.2 IFN-γ-Produktion in CD4+ Lymphozyten (Untergruppenvergleich) Den niedrigsten Median des prozentualen Anteils IFN-γ-produzierender T-Helfer-Zellen wies die Kontrollgruppe auf, die Unterschiede zu allen anderen Untergruppen waren statistisch signifikant. Die höchsten Mediane boten die CP-MS- und die Schub-MS-Untergruppe, dazwischen lagen die der RR-MS-Untergruppe und der OND-Untergruppen. <0,001 0,011 % Anteil IFN-γ -produzierender CD4+ Lymphozyten <0,001 12.5 0,003 <0,001 10.0 7.5 5.0 2.5 0.0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 24. IFN-γ-Produktion in CD4+ Lymphozyten im Untergruppenvergleich. Ergebnisse 47 - 3.2.1.3 IFN-γ-Produktion in CD4 Lymphozyten (Übergruppenvergleich) Die Analyse CD4- Lymphozyten zeigte im Vergleich zu CD4+ Lymphozyten jeweils etwas höhere Mediane prozentualer Anteile IFN-γ-produzierender Zellen, ansonsten boten sich analoge Ergebnisse zu 3.2.1.1. Der niedrigste Median des prozentualen Anteils IFN-γproduzierender CD4- Lymphozyten zeigte sich in der Kontrollgruppe mit statistisch signifikantem Unterschied jeweils zur OND- und MS-Gruppe. Der Unterschied zwischen der MS-Gruppe (mit dem höchsten Median) und der OND-Gruppe lag knapp über der geforderten Signifikanzschwelle. 0,054 <0,001 0,001 % Anteil IFN-γ -produzierender CD4Lymphozyten 20 15 10 5 0 Kontrolle OND MS Gruppe Abbildung 25. IFN-γ-Produktion in CD4- Lymphozyten im Übergruppenvergleich. 3.2.1.4 IFN-γ-Produktion in CD4- Lymphozyten (Untergruppenvergleich) Bei etwas höheren Medianen prozentualer Anteile IFN-γ-produzierender CD4- Lymphozyten im Vergleich zu den CD4+ Zellen konnten hier Analogien zu den Ausführungen unter 3.2.1.2 erkannt werden. Den niedrigsten Median des prozentualen Anteils IFN-γ-produzierender THelfer-Zellen zeigte die Kontrollgruppe, die Unterschiede zu den anderen Untergruppen - hier mit Ausnahme der Schub-MS-Untergruppe - waren statistisch signifikant. Die höchsten Mediane boten die CP-MS- und die Schub-MS-Untergruppe, dazwischen lagen die der RR-MSUntergruppe sowie der OND-Untergruppen. Ergebnisse 48 % Anteil IFN-γ -produzierender CD4 Lymphozyten 0,004 <0,001 0,022 20 0,002 15 10 5 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 26. IFN-γ-Produktion in CD4- Lymphozyten im Untergruppenvergleich. 3.2.2 TNF-α-Produktion 3.2.2.1 TNF-α-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) Im Übergruppenvergleich zeigten sich keine statistisch signifikanten Unterschiede der prozentualen Anteile TNF-α-produzierender T-Helfer-Zellen, die MS-Gruppe weist den höchsten % Anteil TNF-α -produzierender CD4+ Lymphozyten Median auf. 20 15 10 5 0 Kontrolle OND MS Gruppe Abbildung 27. TNF-α-Produktion in CD4+ Lymphozyten im Übergruppenvergleich. Ergebnisse 49 + 3.2.2.2 TNF-α-Produktion in CD4 Lymphozyten (Untergruppenvergleich) Den höchsten Median des prozentualen Anteils TNF-α-produzierender T-Helfer-Lymphozyten zeigte die CP-MS-Gruppe mit deutlichem Abstand zu allen anderen Untergruppen, die % Anteil TNF-α -produzierender CD4+ Lymphozyten Unterschiede waren nicht statistisch signifikant. 20 15 10 5 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 28. TNF-α-Produktion in CD4+ Lymphozyten im Untergruppenvergleich. 3.2.2.3 TNF-α-Produktion in CD4- Lymphozyten (Übergruppenvergleich) Es stellten sich etwa auf gleichem Niveau liegende Mediane des prozentualen Anteils CD4- % Anteil TNF-α -produzierender CD4Lymphozyten TNF-α-produzierender Lymphozyten im Übergruppenvergleich dar. 30 20 10 0 Kontrolle OND MS Gruppe Abbildung 29. TNF-α-Produktion in CD4- Lymphozyten im Übergruppenvergleich. Ergebnisse 50 - 3.2.2.4 TNF-α-Produktion in CD4 Lymphozyten (Untergruppenvergleich) Auch im Untergruppenvergleich fanden sich keine statistisch signifikanten Unterschiede der % Anteil TNF-α -produzierender CD4Lymphozyten prozentualen Anteile TNF-α-produzierender CD4- Lymphozyten. 30 20 10 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 30. TNF-α-Produktion in CD4- Lymphozyten im Untergruppenvergleich. 3.2.3 Interleukin-2-Produktion 3.2.3.1 IL-2-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) Der Median des prozentualen Anteils IL-2-produzierender T-Helfer-Zellen lag in der MS-Gruppe (Median = 0,53) niedriger als in der OND-Gruppe (Median = 0,76) und der Kontrollgruppe (Median = 1,71). Der Unterschied zwischen der MS-Gruppe und der Kontrollgruppe lag knapp über der geforderten Signifikanzschwelle. 0.061 % Anteil IL-2-produzierender CD4+ Lymphozyten 40 30 20 10 0 Kontrolle OND MS Gruppe Abbildung 31. IL-2-Produktion in CD4+ Lymphozyten im Übergruppenvergleich. Ergebnisse 3.2.3.2 IL-2-Produktion in CD4 Lymphozyten (Untergruppenvergleich) 51 + Der Median der prozentualen Anteile IL-2-produzierender T-Helfer-Zellen lag in der RR-MSGruppe am niedrigsten, der Unterschied zur Kontrollgruppe war statistisch signifikant, im Vergleich zur N.I.OND-Gruppe wurde die geforderte Signifikanzschwelle knapp überschritten. 0,072 0,021 % Anteil IL-2-produzierender CD4+ Lymphozyten 40 30 20 10 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 32. IL-2-Produktion in CD4+ Lymphozyten im Untergruppenvergleich. 3.2.3.3 IL-2-Produktion in CD4- Lymphozyten (Übergruppenvergleich) Die Mediane der prozentualen Anteile IL-2-produzierender CD4- Lymphozyten lagen niedriger als bei CD4+ Lymphozyten, es bestanden keine statistisch signifikanten Unterschiede im Übergruppenvergleich. % Anteil IL-2-produzierender CD4Lymphozyten 15.0 12.5 10.0 7.5 5.0 2.5 0.0 Kontrolle OND Gruppe Abbildung 33. IL-2-Produktion in CD4- Lymphozyten im Übergruppenvergleich. MS Ergebnisse 3.2.3.4 IL-2-Produktion in CD4 Lymphozyten (Untergruppenvergleich) 52 - Den niedrigsten Median des prozentualen Anteils IL-2-produzierender CD4- Lymphozyten hatte die RR-MS-Gruppe mit 0,10. Der Unterschied zur N.I.OND-Gruppe (Median = 0,34) verfehlte das geforderte Signifikanzniveau knapp. % Anteil IL-2-produzierender CD4Lymphozyten 15.0 0,063 12.5 10.0 7.5 5.0 2.5 0.0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 34. IL-2-Produktion in CD4- Lymphozyten im Untergruppenvergleich. 3.2.4 Interleukin-4-Produktion 3.2.4.1 IL-4-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) Die Mediane der prozentualen Anteile IL-4-produzierender T-Helfer-Lymphozyten lagen auf insgesamt vergleichsweise niedrigem Niveau, der Unterschied zwischen OND-Gruppe und Kontrollgruppe war statistisch signifikant. 0,008 % Anteil IL-4-produzierender CD4+ Lymphozyten 10.0 7.5 5.0 2.5 0.0 Kontrolle OND MS Gruppe Abbildung 35. IL-4-Produktion in CD4+ Lymphozyten im Übergruppenvergleich. Ergebnisse 3.2.4.2 IL-4-Produktion in CD4 Lymphozyten (Untergruppenvergleich) 53 + Der Median des prozentualen Anteils IL-4-produzierender T-Helfer-Zellen lag in der Infl.ONDund der RR-MS-Gruppe höher als in den anderen Untergruppen. Der Unterschied von Infl.ONDzur CP-MS-Gruppe und zur Kontrollgruppe war jeweils statistisch signifikant. Der Unterschied zwischen N.I.OND-Gruppe und Kontrollgruppe verfehlte knapp das geforderte statistische Signifikanzniveau. 0,029 0,005 % Anteil IL-4-produzierender CD4+ Lymphozyten 10.0 0,055 7.5 5.0 2.5 0.0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 36. IL-4-Produktion in CD4+ Lymphozyten im Untergruppenvergleich. 3.2.4.3 IL-4-Produktion in CD4- Lymphozyten (Übergruppenvergleich) Im Übergruppenvergleich der prozentualen Anteile IL-4-produzierender CD4- Lymphozyten zeigten sich keine statistisch signifikanten Unterschiede. % Anteil IL-4-produzierender CD4Lymphozyten 12.5 10.0 7.5 5.0 2.5 0.0 Kontrolle OND MS Gruppe Abbildung 37. IL-4-Produktion in CD4- Lymphozyten im Übergruppenvergleich. Ergebnisse 3.2.4.4 IL-4-Produktion in CD4 Lymphozyten (Untergruppenvergleich) 54 - Der Median des prozentualen Anteils IL-4-produzierender CD4- Lymphozyten war in der RRMS-Gruppe am niedrigsten, der Unterschied zur Infl.OND- und CP-MS-Gruppe war jeweils statistisch signifikant. Statistische Signifikanz wies auch der Unterschied zwischen der Infl.OND-Gruppe und der Kontrollgruppe auf. % Anteil IL-4-produzierender CD4Lymphozyten 12.5 0,022 0,023 < 0,001 10.0 7.5 5.0 2.5 0.0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 38. IL-4-Produktion in CD4- Lymphozyten im Untergruppenvergleich. 3.2.5 Interleukin-10-Produktion 3.2.5.1 IL-10-Produktion in CD4+ Lymphozyten (Übergruppenvergleich) Die Mediane der prozentualen Anteile IL-10-produzierender T-Helfer-Zellen lagen noch unter denen IL-4-produzierender T-Helfer-Zellen. Im Übergruppenvergleich zeigte sich der höchste Median in der OND-Gruppe, der Unterschied zur Kontrollgruppe war statistisch signifikant. 0,007 % Anteil IL-10-produzierender CD4+ Lymphozyten 3 2 1 0 Kontrolle OND MS Gruppe Abbildung 39. IL-10-Produktion in CD4+ Lymphozyten im Übergruppenvergleich. Ergebnisse 3.2.5.2 IL-10-Produktion in CD4 Lymphozyten (Untergruppenvergleich) 55 + Der höchste Median des prozentualen Anteils IL-10-produzierender T-Helfer-Zellen zeigte sich in der Infl.OND-Gruppe gefolgt von der RR-MS- und der N.I.OND-Gruppe, auf niedrigerem Niveau lagen die Mediane der CP-MS-, Schub-MS-Gruppe und Kontrollgruppe. Der Unterschied von Infl.OND-Gruppe zur Kontrollgruppe und zur CP-MS-Gruppe war jeweils statistisch signifikant, die Unterschiede zur N.I.OND- und zur Schub-MS-Gruppe lagen knapp über dem geforderten statistischen Signifikanzniveau. Die Untergruppe der RR-MS-Patienten wies einen statistisch signifikanten Unterschied zur Kontrollgruppe auf, die Schwelle zur statistischen Signifikanz wurde im Vergleich zu den beiden anderen MS-Untergruppen knapp überschritten. 0,077 0,056 0,074 0,060 0,029 0,076 0,011 % Anteil IL-10-produzierender CD4+ Lymphozyten 3 0,001 2 1 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 40. IL-10-Produktion in CD4+ Lymphozyten im Untergruppenvergleich. 3.2.5.3 IL-10-Produktion in CD4- Lymphozyten (Übergruppenvergleich) Die OND-Gruppe zeigte den höchsten Median des prozentualen Anteils IL-10-produzierender CD4- Lymphozyten, der Unterschied zur Kontrollgruppe und zur MS-Gruppe war jeweils statistisch signifikant. Ergebnisse 56 0,015 0,022 % Anteil IL-10-produzierender CD4Lymphozyten 7 6 5 4 3 2 1 0 Kontrolle OND MS Gruppe Abbildung 41. IL-10-Produktion in CD4- Lymphozyten im Übergruppenvergleich. 3.2.5.4 IL-10-Produktion in CD4- Lymphozyten (Untergruppenvergleich) Der Median des prozentualen Anteils IL-10-produzierender CD4- Lymphozyten lag in der Infl.OND-Gruppe mehr als 100% so hoch wie in der N.I.OND-Gruppe, bei allen anderen Untergruppen lagen die Mediane deutlich unter 0,10. Statistisch signifikant war allerdings nur der Unterschied zwischen Infl.OND-Gruppe und Kontrollgruppe. In den Vergleichen zwischen Infl.OND-Gruppe und den MS-Untergruppen wurde das geforderte Signifikanzniveau jeweils knapp verfehlt. 0,072 0,077 0,072 0,026 % Anteil IL-10-produzierender CD4Lymphozyten 7 6 5 4 3 2 1 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 42. IL-10-Produktion in CD4- Lymphozyten im Untergruppenvergleich. Ergebnisse 3.3 57 Differentialblutbild Neben den bisher dargestellten durchflusszytometrischen Analysen wurde bei den Probanden ein Differentialblutbild bestimmt. 3.3.1 Leukozyten 3.3.1.1 Leukozyten/nl (Übergruppenvergleich) Der Median der Leukozytengesamtkonzentration im Differentialblutbild lag in der MS-Gruppe statistisch signifikant höher als in der Kontrollgruppe. Es bestand kein statistisch signifikanter Unterschied zur dazwischengelegenen OND-Gruppe. 0,003 20 Leukozyten/nl 15 10 5 0 Kontrolle OND MS Gruppe Abbildung 43. Leukozytenkonzentration im Übergruppenvergleich. 3.3.1.2 Leukozyten/nl (Untergruppenvergleich) Auf dem höchsten Niveau lagen die Mediane der Leukozytengesamtkonzentration der MSUntergruppen, gefolgt von der N.I.OND-Gruppe. Die Mediane der Infl.OND-Gruppe und der Kontrollgruppe lagen auf niedrigerem Niveau. Statistisch signifikant waren die Unterschiede zwischen Infl.OND-Gruppe und N.I.OND-, RR-MS- sowie Schub-MS-Gruppe, darüber hinaus zwischen Kontrollgruppe und wiederum N.I.OND-, RR-MS- sowie Schub-MS-Gruppe. Ergebnisse 58 0,007 0,005 0,014 0,011 20 0,007 0,020 Leukozyten/nl 15 10 5 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 44. Leukozytenkonzentration im Untergruppenvergleich. 3.3.2 Neutrophile Granulozyten 3.3.2.1 Prozentualer Anteil neutrophiler Granulozyten (Übergruppenvergleich) Die Mediane des prozentualen Anteils neutrophiler Granulozyten von MS- und OND-Gruppe lagen höher als der der Kontrollgruppe. Der Unterschied zwischen der Kontrollgruppe und der MS- sowie der OND-Gruppe war jeweils statistisch signifikant. 0,047 0,049 % Anteil Neutrophiler 80 70 60 50 40 Kontrolle OND MS Gruppe Abbildung 45. Prozentualer Anteil neutrophiler Granulozyten im Übergruppenvergleich. Ergebnisse 3.3.2.2 Prozentualer Anteil neutrophiler Granulozyten (Untergruppenvergleich) 59 Im Untergruppenvergleich lag der Median des prozentualen Anteils neutrophiler Granulozyten in der Schub-MS-Gruppe am höchsten. Der Unterschied zu den zwei anderen MS-Untergruppen und zur Kontrollgruppe war statistisch signifikant, der Unterschied zur Infl.OND-Gruppe lag knapp über der geforderten statistischen Signifikanzschwelle. Des Weiteren war der Unterschied zwischen N.I.OND-Gruppe und Kontrollgruppe statistisch signifikant. 0,064 0,049 0,022 0,004 0,040 % Anteil Neutrophiler 80 70 60 50 40 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 46. Prozentualer Anteil neutrophiler Granulozyten im Untergruppenvergleich. 3.3.3 Lymphozyten 3.3.3.1 Prozentualer Anteil von Lymphozyten (Übergruppenvergleich) Der Median des prozentualen Anteils von Lymphozyten im Differentialblutbild lag in der Kontrollgruppe höher als in der OND- und der MS-Gruppe. Der Unterschied zwischen Kontrollgruppe und MS-Gruppe war statistisch signifikant. Ergebnisse 60 0,011 % Anteil Lymphozyten 50 40 30 20 10 0 Kontrolle OND MS Gruppe Abbildung 47. Prozentualer Anteil von Lymphozyten im Übergruppenvergleich. 3.3.3.2 Prozentualer Anteil von Lymphozyten (Untergruppenvergleich) Im Untergruppenvergleich lagen die Mediane des prozentualen Anteils von Lymphozyten im Differentialblutbild in der Schub-MS-Gruppe unter denen aller anderen Untergruppen. Die Mediane der Kontrollgruppe und der Infl.OND-Gruppe lagen höher als die der anderen Untergruppen. Statistische Signifikanz hatten die Unterschiede zwischen der Schub-MS-Gruppe und jeweils der RR-MS-Gruppe sowie der Kontrollgruppe. Im Vergleich zur Infl.OND-Gruppe wurde die geforderte Signifikanzschwelle knapp überschritten. Knapp lag auch der Unterschied zwischen der Kontrollgruppe und der N.I.OND-Gruppe über dem geforderten statistischen Signifikanzniveau. 0,064 0,063 0,038 0,003 % Anteil Lymphozyten 50 40 30 20 10 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 48. Prozentualer Anteil von Lymphozyten im Untergruppenvergleich. Ergebnisse 3.3.4 61 Monozyten 3.3.4.1 Prozentualer Anteil von Monozyten (Übergruppenvergleich) Der Median des prozentualen Anteils von Monozyten im Differentialblutbild lag in der MSGruppe höher als in der Kontrollgruppe, der Median der Kontrollgruppe war wiederum höher als der der OND-Gruppe. Es lagen keine statistisch signifikanten Unterschiede vor. 12.5 % Anteil M onozyten 10.0 7.5 5.0 2.5 0.0 Kontrolle OND MS Gruppe Abbildung 49. Prozentualer Anteil von Monozyten im Übergruppenvergleich. 3.3.4.2 Prozentualer Anteil von Monozyten (Untergruppenvergleich) Der Median des prozentualen Anteils von Monozyten im Differentialblutbild lag in der N.I.ONDGruppe am niedrigsten. Die Unterschiede zur Kontrollgruppe, zur Schub-MS- und zur CP-MSGruppe waren jeweils statistisch signifikant. Im Vergleich zur Infl.OND-Gruppe wurde die statistische Signifikanzschwelle knapp überschritten. 0.047 12.5 0,041 0,078 0,030 % Anteil M onozyten 10.0 7.5 5.0 2.5 0.0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 50. Prozentualer Anteil von Monozyten im Untergruppenvergleich. Ergebnisse 3.3.5 62 Eosinophile Granulozyten 3.3.5.1 Prozentualer Anteil eosinophiler Granulozyten (Übergruppenvergleich) Der Median des prozentualen Anteils eosinophiler Granulozyten lag in der Kontrollgruppe niedriger als in der OND- und der MS-Gruppe. Es bestanden keine statistisch signifikanten Unterschiede im Übergruppenvergleich. 7 % Anteil Eosinophiler 6 5 4 3 2 1 0 Kontrolle OND MS Gruppe Abbildung 51. Prozentualer Anteil eosinophiler Granulozyten im Übergruppenvergleich. 3.3.5.2 Prozentualer Anteil eosinophiler Granulozyten (Untergruppenvergleich) Der Median des prozentualen Anteils eosinophiler Granulozyten im Differentialblutbild lag in der RR-MS-Gruppe am höchsten, mit relativ geringem Abstand folgte darunter der Median der Infl.OND-Gruppe. Etwas deutlicher darunter lagen die Mediane der N.I.OND-, der CP-MSGruppe sowie der Kontrollgruppe, am niedrigsten lag der Median der Schub-MS-Gruppe. Die Unterschiede von RR-MS-Gruppe jeweils zur Kontrollgruppe und zur N.I.OND-Gruppe waren statistisch signifikant. 0,038 7 0,008 % Anteil Eosinophiler 6 5 4 3 2 1 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 52. Prozentualer Anteil eosinophiler Granulozyten im Untergruppenvergleich. Ergebnisse 3.3.6 63 Basophile Granulozyten 3.3.6.1 Prozentualer Anteil basophiler Granulozyten (Übergruppenvergleich) Die Mediane des prozentualen Anteils basophiler Granulozyten lagen auf vergleichbarem Niveau, es fanden sich keine statistisch signifikanten Unterschiede im Übergrupppenvergleich. % Anteil Basophiler 3 2 1 0 Kontrolle OND MS Gruppe Abbildung 53. Prozentualer Anteil basophiler Granulozyten im Übergruppenvergleich. 3.3.6.2 Prozentualer Anteil basophiler Granulozyten (Untergruppenvergleich) Im Untergruppenvergleich lag der Median des prozentualen Anteils basophiler Granulozyten im Differentialblutbild der RR-MS-Gruppe höher als der der Infl.OND-Gruppe. Dazwischen lagen die Mediane aller anderen Untergrupppen. Der Unterschied zwischen der RR-MS- und der Infl.OND-Gruppe war statistisch signifikant. % Anteil Basophiler 3 0,046 2 1 0 Kontrolle N.I.OND Infl.OND RR-MS Schub-MS CP-MS Gruppe Abbildung 54. Prozentualer Anteil basophiler Granulozyten im Untergruppenvergleich. Diskussion 4 64 Diskussion Die Fragestellung der vorliegenden Arbeit war vorrangig, inwieweit sich Multiple SklerosePatienten untereinander sowie von gesunden Kontrollpersonen und Patienten mit anderen neurologischen Erkrankungen (OND) hinsichtlich der untersuchten Parameter unterscheiden. Von besonderem Interesse war hierbei die Frage, ob man Untergruppen der Multiplen Sklerose wie schubförmige Patienten in stabilem Zustand (RR-MS) von schubförmigen Patienten mit akutem Schub (Schub-MS) und von Patienten mit chronisch-progredienter MS (CP-MS) anhand einer TH1- oder TH2-Zell-Dominanz unterscheiden kann. 4.1 Oberflächenmarker CD45RA/R0 Über die Markierung der Oberflächenstrukturen CD45RA und CD45R0 konnten naive und TGedächtnis/Effektor-Zellen differenziert werden. Über die Ausstattung mit verschiedenen CD45-Isoformen ist eine Möglichkeit gegeben, in Lymphozyten den Schwellenwert für die Auslösung eines Rezeptorsignals zu steuern (Janeway et al., 2002). Es gibt Hinweise dafür, dass die Reaktion auf MBP von MS-Patienten im Wesentlichen von T-Zellen aus dem Gedächtnis-Zell-Kompartiment stammt (Burns et al., 1999). Die Antwort von T-Gedächtnis-Zellen auf ihr spezifisches Antigen ist weniger abhängig von Kostimulation als die von naiven T-Zellen. Diese Konstellation bestätigte sich beim Vergleich der T-Zell-Antwort auf MBP von MS-Patienten mit gesunden Individuen (Croft et al., 1994; Scholz et al., 1998). Die Unterscheidung dieser mit unterschiedlichen CD45-Isoformen bestückten Zelltypen könnte bei der Beurteilung des Aktivierungszustandes der T-Zellen bei den genannten Untergruppen der MS eine Rolle spielen. Die Ergebnisse der vorliegenden Arbeit zeigten keine statistisch signifikanten Unterschiede des prozentualen Anteils naiver T-Lymphozyten im Blut der differenzierten Über- oder Untergruppen, jedoch war der prozentuale Anteil von T-Gedächtnis/Effektor-Zellen im Blut der MS- und der OND-Gruppe jeweils statistisch signifikant höher als in der Kontrollgruppe (siehe Abbildung 19). Im Untergruppenvergleich stellte sich eine interessante Konstellation dar (siehe Abbildung 20): Die Untergruppen mit einem Median des prozentualen Anteils von T-Gedächtnis/EffektorZellen, der deutlich über 20 lag, also Infl.OND- (Patienten mit inflammatorischen OND), SchubMS- (Patienten mit schubförmiger MS im akuten Schub) und CP-MS-Gruppe (Patienten mit chronisch-progredienter MS) unterschieden sich jeweils statistisch signifikant von den Untergruppen, deren Median deutlich unter 20 lag, also Kontrollgruppe, RR-MS- (Patienten mit schubförmiger MS im schubfreien Intervall) und N.I.OND-Gruppe (Patienten mit nicht inflammatorischen OND). Dies untermauert die oben aufgeführte These, dass der Aktivierungszustand der T-Zellen eine Hilfe zur Differenzierungsmöglichkeit verschiedener MS- Diskussion 65 Krankheitsentitäten darstellen könnte, möglicherweise auch bei der Differenzierung anderer neurologischer Erkrankungen, bei denen unklar ist, ob eine inflammatorische oder eine nicht inflammatorische Ätiologie vorliegt. Betrachtet man die MS-Untergruppen, kann man die vorliegenden Ergebnisse dieser Arbeit dahingehend interpretieren, dass sich die T-Zellen im Blut der Schub-MS- und der CP-MSGruppe durch einen höheren Aktivierungszustand (bzw. durch eine effizientere Aktivierbarkeit) von den T-Zellen der RR-MS-Gruppe unterscheiden lassen. Die Gruppe der MS-Patienten im schubfreien Intervall (RR-MS) unterschied sich diesbezüglich nicht von der Kontrollgruppe. Von Interesse wären weitergehende Studien, in denen untersucht wird, ob sich die Bestimmung des prozentualen Anteils von CD45R0+ T-Zellen im Längsschnitt bei Patienten mit schubförmigem Verlauf zur Früherkennung des Übergangs in eine chronisch-progrediente Form oder aber eines bevorstehenden Schubes eignen könnte. 4.2 Intrazellulärer Zytokinnachweis 4.2.1 Interferon-γ-Produktion IFN-γ ist ein proinflammatorisch wirkendes Zytokin und wird von T- und NK-Zellen produziert. Betrachtet man sowohl die CD4+ (also T-Helfer-) Zellen als auch die CD4- Lymphozyten im Blut der im Rahmen dieser Arbeit untersuchten Probanden im Übergruppenvergleich (siehe Abbildungen 23 und 25), waren die Mediane des prozentualen Anteils IFN-γ-produzierender Zellen bei MS-Patienten und OND-Patienten jeweils statistisch signifikant höher als bei gesunden Kontrollpersonen, deren Mediane bei 0,03 bzw. 0,16 lagen. Die Unterschiede von IFN-γ-produzierenden Lymphozyten bei MS-Patienten gegenüber OND-Patienten (Mediane mehr als 300% höher) waren nicht statistisch signifikant. Im Untergruppenvergleich war der Median des prozentualen Anteils IFN-γ-produzierender THelfer-Zellen bei allen MS- und OND-Patientenuntergruppen statistisch signifikant höher als in der Kontrollgruppe (siehe Abbildung 24). Betrachtet man diesbezüglich CD4- Lymphozyten, gelten analoge Aussagen mit der Ausnahme, dass hier der Unterschied zwischen Kontrollgruppe und Schub-MS-Gruppe keine statistische Signifikanz aufwies (siehe Abbildung 26). Der Unterschied der deutlich höher gelegenen Mediane bei chronisch-progredienten und MS-Patienten im akuten Schub im Vergleich zu MS-Patienten im schubfreien Intervall und den OND-Untergruppen war ebenfalls nicht statistisch signifikant. Ein höherer prozentualer Anteil IFN-γ-produzierender Lymphozyten bei MS-Patienten im Vergleich zu gesunden Kontrollpersonen wurde mittels Durchflusszytometrie auch von Inoges et al. (1999) gezeigt, dies galt für CD4+ und CD8+ Lymphozyten. Inoges et al. beschrieben einen Diskussion 66 statistisch signifikanten Unterschied auch zwischen „chronisch-aktiven“ und schubförmigen MSPatienten im schubfreien Intervall, was die eigenen Ergebnisse trotz hier fehlender Signifikanz untermauern könnte. Inoges et al. haben keine MS-Patienten im akuten Schub und keine ONDPatienten untersucht. Petereit et al. fanden im Jahr 2000 eine statistisch signifikante positive Korrelation zwischen durchflusszytometrisch in Blut-Lymphozyten gemessener IFN-γ-Produktion und Behinderungsgrad bei MS-Patienten (gemessen anhand des EDSS). Beck et al. fanden bereits im Jahr 1988 im Überstand von Zellkulturen mittels ELISA erhöhte IFN-γ-Konzentrationen von schubförmigen MS-Patienten vor und im akuten Schub gegenüber gesunden Kontrollpersonen. Eine Erhöhung von IFN-γ wurde des Weiteren schon in einigen Studien mittels verschiedener Nachweismethoden im Blut, in CSF und in Läsionen von MS-Patienten gezeigt, andere erbrachten jedoch teilweise widersprüchliche Ergebnisse. Navikas & Link führten in einem Review (1996) als mögliche Ursache für widersprüchliche Ergebnisse Nachteile bestimmter Nachweisverfahren im Vergleich zur Durchflusszytometrie an, ebenso differierten der Zeitpunkt der Probeentnahme und/oder die Aufbewahrungsbedingungen des Untersuchungsmaterials. 4.2.2 Tumornekrosefaktor-α-Produktion TNF-α ist ein proinflammatorisch wirkendes Zytokin und kann von T-Zellen, NK-Zellen, Monozyten/Makrophagen und Astrozyten sowie Mikroglia produziert werden. Im Übergruppenvergleich wiesen MS-Patienten einen höheren Median des prozentualen Anteils TNF-α-produzierender T-Helfer-Zellen im Vergleich zu OND-Patienten und Kontrollpersonen auf, allerdings war dieser Unterschied statistisch nicht signifikant (siehe Abbildung 27). Hinsichtlich TNF-α-produzierender CD4- Zellen bestand kein Unterschied zwischen MS-, ONDPatienten und gesunden Kontrollpersonen. Dies spricht für eine besondere Rolle von TNF-α-produzierenden T-Helfer-Zellen bei MSPatienten, insbesondere wenn man die Konstellation des Untergruppenvergleichs (siehe Abbildung 28) berücksichtigt: Der höchste Median (mehr als 200% höher als in der RR-MSGruppe) TNF-α-produzierender T-Helfer-Zellen war in der CP-MS-Gruppe zu finden als Hinweis für einen mit der klinischen Symptomatik zu vereinbarenden fortwährenden degenerativen und demyelinisierenden Prozess. Eine Vielzahl von Arbeiten belegte Erhöhungen von TNF-α bei MS-Patienten auch mit statistischer Signifikanz, z.B. anhand von TNF-α-Detektion im Serum und CSF mittels ELISA Diskussion 67 (Rentzos et al., 1996); immunzytochemisch in MS-Läsionen (Selmaj et al., 1991); des Weiteren mittels PCR über mRNA-Transkripte (Navikas et al., 1996). Auch gab es Studien, die eine Assoziation zwischen TNF-α und Krankheitsprogression bzw. aktivität nahe legten. Sharief & Hentges fanden eine solche Assoziation (1991) mittels ELISA in CSF von CP-MS-Patienten, nicht aber im Serum. Rieckmann et al. (1995) gelang der Nachweis einer Assoziation zwischen TNF-α und Krankheitsprogression mittels semiquantitaver cDNAPCR und Analyse des Musters der mRNA-Expression von Mitogen-stimulierten Lymphozyten. Renno et al. zeigten (1995) im Tiermodell EAE mittels RT-PCR und Durchflusszytometrie (zur Differenzierung von CD4+, CD8+, CD45+, CD3+ und Mac1+ Zellen), dass die TNF-αTranskription im ZNS nicht vorzugsweise von T-Zellen, sondern vielmehr von Makrophagen und Mikroglia geleistet wird - im Gegensatz zu den vornehmlich von CD4+ Zellen stammenden Zytokinen IL-2 und IFN-γ. 4.2.3 Interleukin-2-Produktion Interleukin-2 wird von antigenaktivierten T-Lymphozyten synthetisiert und spielt als Wachstumsfaktor eine essentielle Rolle in der T-Lymphozyten-Proliferation und -Differenzierung in Effektorzellen (Gallo et al., 1988) und induziert darüber hinaus Maturation und Proliferation von anderen Immunzellen wie Natürlichen Killerzellen (Weigent et al., 1983) und BLymphozyten (Waldmann, 1986). Es soll allerdings keine direkte inflammatorische Aktivität im ZNS entfalten (Simmons & Willenborg, 1990). Darüber hinaus wird IL-2 eine (möglicherweise indirekte) Rolle in der Oligodendrozyten-Proliferation zugesprochen (Benveniste & Merill, 1986). Naive T-Zellen werden anergisch, wenn ein Antigen ohne kostimulierende Faktoren (z.B. Bindung von B7 auf antigenpräsentierenden Zellen an CD28 auf T-Zellen) erkannt wird. Die entscheidende Veränderung anergischer T-Zellen besteht darin, dass sie kein IL-2 synthetisieren können (Greenfield et al., 1998). In dieser Studie waren die Mediane des prozentualen Anteils IL-2-produzierender Zellen bei THelfer-Zellen in allen Gruppen höher als bei CD4- T-Zellen, was die besondere Rolle der THelfer-Zellen in der Vermittlung IL-2-spezifischer Effekte unterstreichen könnte. Betrachtet man die prozentualen Anteile der IL-2-Produktion von T-Helfer-Zellen im Untergruppenvergleich (siehe Abbildung 32), fällt auf, dass der Median im Vergleich der MSPatientenuntergruppen bei schubförmigen Patienten im akuten Schub am höchsten lag (allerdings ohne statistisch signifikanten Unterschied zu den anderen Untergruppen), dagegen bei Patienten im schubfreien Intervall am niedrigsten. Der Unterschied von Patienten im schubfreien Intervall zu Kontrollpersonen war statistisch signifikant. Auch dies spricht für eine Dominanz der TH1-Zell-Antwort im akuten Schub, wie zuvor die geschilderten Ausführungen hinsichtlich TNF-α- und IFN-γ-Produktion. Dagegen war bei Patienten im schubfreien Intervall sogar eine unter das Niveau gesunder Individuen supprimierte IL-2-Produktion zu finden, Diskussion 68 welches durch eine im schubfreien Intervall vorliegende Dominanz einer TH2-Zell-Antwort erklärbar ist. Eine TH2-Dominanz bei schubförmigen MS-Patienten im schubfreien Intervall wird durch die weiter unten diskutierten Ergebnisse der IL-4- und IL-10-Produktion durch T-HelferZellen in der vorliegenden Arbeit bekräftigt. Die IL-2-Produktion von T-Helfer-Zellen im Blut von chronisch-progredienten MS-Patienten glich anhand der vorliegenden Ergebnisse der von gesunden Individuen. Die protrahierte demyelinisierende und degenerative Krankheitsaktivität scheint sich bei dieser Krankheitsentität also eher durch von TH1-Zellen vermittelte Effekte von IFN-γ und TNF-α zu erklären. Trotter et al. (1991) fanden allerdings in Seren von chronisch-progredienten MS-Patienten mittels ELISA eine Erhöhung der IL-2-Konzentration im Vergleich zu gesunden Kontrollpersonen und nicht inflammatorischen sowie inflammatorischen OND-Patienten. Darüber hinaus fanden Trotter et al. in der gleichen Studie eine Korrelation zwischen IL-2- und TNF-αKonzentration in allen Untergruppen. Eine Erhöhung von IL-2 in Seren von chronischprogredienten und schubförmigen MS-Patienten mittels ELISA wurde auch in anderen Untersuchungen gefunden (Trotter et al., 1988; Capra et al., 1990). Allerdings merkten Peter et al. (1991) kritisch hinsichtlich der ELISA-Methode an, dass die zelluläre Herkunft des IL-2 unklar bliebe, darüber hinaus fehlten gut dokumentierte Normwerte. Inoges et al. (1999) fanden mittels Durchflusszytometrie, analog zu den in dieser Arbeit beschriebenen Resultaten, keinen Unterschied des prozentualen Anteils IL-2-produzierender Lymphozyten zwischen chronisch-progredienten MS-Patienten und gesunden Individuen. Auch beschrieben sie einen geringeren Anteil IL-2-produzierender Lymphozyten im Blut von stabilen MS-Patienten. 4.2.4 Interleukin-4-Produktion Interleukin-4 wird von T-Zellen, Mastzellen und basophilen Granulozyten produziert. IL-4 ist ein Zytokin, welches in der Lage ist, inflammatorische Reaktionen zu unterdrücken. Es inhibiert (insbesondere die IFN-γ-Synthese durch) TH1-Zellen und stimuliert die Differenzierung von TZellen in TH2-Zellen, welche wiederum IL-4 synthetisieren. Es vermag des Weiteren B-Zellen zu aktivieren und damit die Antikörperbildung zu induzieren, auch bewirkt es einen IgKlassenwechsel zu IgE (Seder et al., 1992; Link et al., 1994). Die Ergebnisse der vorliegenden experimentellen Arbeit zeigten keine statistisch signifikanten Unterschiede des prozentualen Anteils IL-4-produzierender T-Helfer-Zellen zwischen gesunden Kontrollpersonen und MS-Patienten. Betrachtet man die MS-Patientenuntergruppen (siehe Abbildung 36), fällt auf, dass der Median des prozentualen Anteils IL-4-produzierender T-HelferZellen bei MS-Patienten im schubfreien Intervall höher lag als bei den anderen Untergruppen. Diskussion 69 Wenngleich nicht statistisch signifikant, ist dieser Unterschied mit der These einer TH2-ZellDominanz im schubfreien Intervall vereinbar. Deutlicher und statistisch signifikant war der Unterschied zwischen inflammatorischen ONDPatienten und gesunden Kontrollpersonen. Der höhere Median des prozentualen Anteils IL-4produzierender T-Helfer-Zellen im Blut inflammatorischer OND-Patienten kann durch eine humoral bzw. zugunsten von B-Zellen gewichtete Immunantwort erklärt werden. Im Untergruppenvergleich von CD4- Zellen (siehe Abbildung 38) lag der Median des prozentualen Anteils IL-4-produzierender Zellen im Blut von schubförmigen MS-Patienten im schubfreien Intervall am niedrigsten, bei Patienten im akuten Schub am höchsten, wobei der Unterschied nicht statistisch signifikant war. Signifikant war jedoch der Unterschied von schubförmigen MS-Patienten im schubfreien Intervall zu chronisch-progredienten MS-Patienten und inflammatorischen OND-Patienten. In vielen Studien wurde diskutiert, dass bei ablaufender TH1-Zell-vermittelter autoimmuner entzündlicher Aktivität im Rahmen der MS-Erkrankung schon früh durch insbesondere IL-4-vermittelte Effekte ein die inflammatorische Reaktion eindämmmendes und die Remyelinisierung förderndes Milieu geschaffen wird (Chao et al., 1993; Link et al., 1994; Racke et al., 1995). 4.2.5 Interleukin-10-Produktion Interleukin-10 wird von T-Zellen, Makrophagen sowie EBV-transformierten B-Zellen (virales = v-IL-10) synthetisiert (de Waal Malefyt et al., 1991). Es gilt als wichtiges antiinflammatorisch wirkendes Zytokin, das die Synthese proinflammatorischer Zytokine und Chemokine in aktivierten Makrophagen, T-Zellen und NKZellen inhibiert (Moore et al., 1993). IL-10 reduziert die antigenspezifische T-Zell-Proliferation durch eine Herabsetzung der Kapazität zur Antigenpräsentation auf antigenpräsentierenden Zellen mittels verminderter Expression von MHC-Klasse-II-Molekülen auf der Zelloberfläche (de Waal Malefyt et al., 1991). Eine herabgesetzte intrazelluläre Produktion von IL-10-mRNA ist mit erhöhter Krankheitsaktivität bei MS-Patienten assoziiert (Boxel-Dezaire et al., 1999). Eine gesteigerte Produktion von IL-10 fand sich bei stabilen MS-Patienten (Rieckmann et al., 1994), so dass diesem Zytokin eine wichtige Rolle in der Kontrolle der Progression der Erkrankung zugeschrieben wird (Mäurer et al., 2000). In der vorliegenden Studie waren die prozentualen Anteile IL-10-produzierender T-Zellen im Vergleich zu denen andere Zytokine produzierender T-Zellen niedrig. Im Untergruppenvergleich lagen die Mediane der prozentualen Anteile von IL-10- produzierenden T-Helfer-Zellen bei beiden OND-Untergruppen über denen aller anderen, dabei waren die Unterschiede zwischen inflammatorischen OND-Patienten und gesunden Kontrollpersonen sowie chronisch-progredienten MS-Patienten statistisch signifikant (siehe Abbildung 40). Diskussion 70 Interessant ist die Tatsache, dass sich schubförmige MS-Patienten im schubfreien Intervall (RR-MS) durch einen höheren Median der prozentualen Anteile an IL-10-produzierenden THelfer-Zellen von gesunden Kontrollpersonen (statistisch signifikant) und den beiden „aktiven“ MS-Untergruppen (Schub-MS und CP-MS) unterschieden. Die Unterschiede zu den anderen MS-Untergruppen verfehlten das geforderte statistische Signifikanzniveau nur knapp. Zustände, die mit einer erhöhten IL-10-Synthese einhergehen, haben einen positiven Einfluss auf den Verlauf der MS. Ein bereits in der Einleitung erwähntes eindrucksvolles Beispiel ist die Schwangerschaft, die aus immunologischer Sicht mit einer Verschiebung des TH1/TH2Gleichgewichts in Richtung einer TH2-Dominanz einhergeht. Als Quelle des IL-10 gilt in diesem Fall die fetoplazentare Einheit (Wegmann et al., 1993). Ein weiteres Beispiel stellen Erkrankungen aus dem atopischen Formenkreis dar (Mosmann & Sad, 1996). In der OND-Gruppe fand sich der höchste Median des prozentualen Anteils IL-10produzierender CD4- Lymphozyten, was eine besondere Rolle dieses Zytokins in der Regulation der Immunantwort bei inflammatorischen Erkrankungen auch abseits der MS nahelegt. Unklar ist die genaue zelluläre Identität dieser IL-10-produzierenden Lymphozyten, möglicherweise handelt es sich um regulatorische T-Zellen. Eine nachgewiesene therapeutische Wirksamkeit von IL-10 wurde kürzlich beispielsweise bei der Psoriasis gezeigt (Friedrich et al., 2002). Als Fazit der bisher dargestellten Ergebnisse können folgende Hypothesen angeführt werden: Es ist von verschiedenen Krankheitsentitäten der MS auszugehen, wobei immunologisch MS-Patienten im schubfreien Intervall als „inaktive“ Patienten von solchen im akuten Schub und von chronisch-progredienten als „aktive“ Patienten differenziert werden können. Das (vereinfachte) TH1/TH2-Paradigma kann bekräftigt werden, insofern „aktive“ MS-Patientenuntergruppen meist höhere Mediane prozentualer Anteile proinflammatorische Zytokine produzierender T-Helfer Zellen aufweisen als „inaktive“, „inaktive“ MS-Patientenuntergruppen dagegen vornehmlich höhere Mediane prozentualer Anteile antiinflammatorische Zytokine produzierender T-Helfer Zellen aufweisen als „aktive“. Diskussion 71 Die hier verwendete Methodik und das experimentelle Protokoll könnten zukünftig dazu beitragen, bei klinisch unklarer Zuordnung zu einer MS-Krankheitsentität dennoch eine Differenzierung mit ihren möglichen therapeutischen und prognoseverbessernden Konsequenzen vorzunehmen, möglicherweise eine Früherkennung der MS-Erkrankung zu ermöglichen, noch bevor eine gesicherte Diagnose anhand der bisher gültigen Kriterien gestellt werden kann. 4.3 Differentialblutbild An dieser Stelle werden die für die Zielsetzung der Arbeit wichtigsten Befunde des Differentialblutbilds diskutiert. Im Übergruppenvergleich wiesen MS-Patienten den höchsten Median der Leukozytenkonzentration im Blut auf, der Unterschied zu gesunden Kontrollpersonen war statistisch signifikant (siehe Abbildung 43). Eine mögliche Erklärung für dieses Ergebnis ist, dass die vermehrte Freisetzung von TNF-α bei MS-Patienten insbesondere über eine Erhöhung der Anzahl zirkulierender neutrophiler Zellen zu einem Leukozytenanstieg führen kann (Janeway et al., 2002). In der Untergruppenanalyse lagen die Mediane der MSPatientenuntergruppen ebenfalls höher als die der anderen Untergruppen, es ließen sich statistisch signifikante Unterschiede zwischen den schubförmigen MS-Patientenuntergruppen und gesunden Kontrollpersonen nachweisen (siehe Abbildung 44). Der höhere Median des prozentualen Anteils von neutrophilen Granulozyten im Blut von ONDund MS-Patientenuntergruppen mit statistisch signifikanter Differenz gegenüber gesunden Kontrollpersonen und im Untergruppenvergleich höchste Median bei MS-Patienten im akuten Schub bekräftigt eine Beteiligung von neutrophilen Granulozyten als Komponenten der unspezifischen, angeborenen Immunität an den gewebeschädigenden Prozessen im Krankheitsverlauf der MS. Zwar ist das Verständnis von der Rolle der Granulozyten in der Immunpathogenese der MS noch lückenhaft, es gibt jedoch erste Berichte darüber, dass zumindest bei einigen Enzephalomyelitiden Granulozyten an der Entzündungsreaktion innerhalb des ZNS beteiligt sind und vor allem über die von ihnen produzierten Chemokine den Krankheitsverlauf negativ beeinflussen können (McColl et al., 1998; Nygardas et al., 2000). Vergleicht man die Abbildungen der prozentualen Anteile neutrophiler Granulozyten (Abbildungen 45 und 46) mit denen der prozentualen Anteile von Lymphozyten (Abbildungen 47 und 48) jeweils im Über- und Untergruppenvergleich, fällt eine gewissermaßen spiegelbildliche Konstellation auf. Der Median des prozentualen Anteils von Lymphozyten im Blut von gesunden Kontrollpersonen war höher als der von OND- und MS-Gruppe und im Untergruppenvergleich bei MS-Patienten im akuten Schub am niedrigsten. Dagegen war der Median des prozentualen Diskussion 72 Anteils von neutrophilen Granulozyten bei MS-Patienten im akuten Schub am höchsten und in der Kontrollgruppe am niedrigsten. Eine derartige dichotome Immunzell-Deviation ist bemerkenswert, insofern bei MS-Patienten im akuten Schub eher eine lymphozytäre Reaktion erwartet wurde als eine der unspezifischen angeborenen Immunität. Möglicherweise ist dieses Ergebnis durch eine Verschiebung der Lymphozyten in Kompartimente abseits des zirkulierenden Blutes wie lymphatische Organe und/oder das ZNS jenseits der Blut/HirnSchranke bedingt. Eine weitere Erklärungsmöglichkeit ist ein erhöhter Verbrauch von Lymphozyten, z.B. durch aktivierungsinduzierten Zelltod/Apoptose. Die Ergebnisse der prozentualen Anteile von Monozyten, eosinophilen und basophilen Granulozyten in den MS-Untergruppen fügen sich gut in das Konzept von „aktiver/inaktiver“ MS sowie einer TH1/TH2-Dichotomie ein: Wenngleich ohne statistische Signifikanz im Direktvergleich, fällt in den Abbildungen 50, 52 und 54 auf, dass „aktive“ MS-Patientenuntergruppen höhere Mediane prozentualer Anteile von Monozyten aufwiesen als „inaktive“. TH1-typische Zytokine und Wachstumsfaktoren wie IFN-γ, TNF-α, IL-3 und GM-CSF vermitteln eine Stimulierung der Bildung neuer Monozyten und führen zur Makrophagenaktivierung und Chemotaxis (Janeway et al., 2002; Martinez-Moczygemba & Huston, 2003). „inaktive“ MS-Patientenuntergruppen einen höheren Median prozentualer Anteile von eosinophilen und basophilen Granulozyten aufwiesen als „aktive“. Dies kann durch eine Aktivierung von TH2-Zellen mit resultierender Ausschüttung von TH2-typischen Zytokinen wie IL-10 und IL-5, die ihrerseits die Entstehungsrate von eosinophilen und basophilen Granulozyten im Knochenmark und ihre Freisetzung in den Blutkreislauf verstärken, erklärt werden (Collins et al., 1995; Thomas, 1995; Janeway et al., 2002). Zusammenfassung 5 73 Zusammenfassung Die vorliegende experimentelle Arbeit befasst sich mit der durchflusszytometrischen Analyse von intrazellulären Zytokinen in Blut-Lymphozyten von Patienten mit Multipler Sklerose (MS), Patienten mit anderen neurologischen Erkrankungen (OND) und gesunden Kontrollpersonen (Kontrolle). Die Multiple Sklerose gilt als T-Zell-vermittelte Erkrankung mit Autoimmuncharakter. Eine besondere ätiopathogenetische Rolle bei der MS haben die T-Helfer-Zellen (TH-Zellen, CD4+ Lymphozyten), die wiederum in distinkte Subtypen eingeteilt werden können. Die weithin anerkannten und für diese Arbeit relevanten Subtypen 1 und 2 oder TH1- und TH2-Zellen können anhand des Musters der von ihnen produzierten Zytokine unterschieden werden. Entzündungsreaktionen werden durch TH1-typische, proinflammatorisch wirkende Zytokine wie Interferon-γ und Interleukin-2 stimuliert und durch TH2-typische, antiinflammatorisch wirkende Zytokine wie Interleukin-4 und Interleukin-10 supprimiert. TNF-α wird in größeren Mengen von TH1-Zellen und in geringeren Mengen von TH2-Zellen produziert. Als möglicher ätiopathogenetischer Faktor der MS wird ein quantitatives und qualitatives Ungleichgewicht der genannten T-Helfer-Zell-Subtypen bzw. der von ihnen synthetisierten Zytokine in Richtung einer TH1-Dominanz diskutiert. Fragestellung dieser Studie war, ob und inwieweit sich MS-Patienten hinsichtlich TH1- oder TH2-typischer Zytokinmuster von gesunden Kontrollpersonen und Patienten mit anderen neurologischen Erkrankungen unterscheiden. Von besonderem Interesse war darüber hinaus, ob man verschiedene Untergruppen (bzw. Phasen/Aktivitätszustände) der Multiplen Sklerose wie stabile schubförmige MS-Patienten von schubförmigen Patienten im akuten Schub und chronisch-progredienten MS-Patienten anhand des Zytokinmusters und/oder des TH1/TH2-Zell-Verhältnisses unterscheiden kann. Die Charakterisierung von TH1- und TH2-Zellen ist bislang nur durch ihre funktionelle Unterscheidung anhand ihres Zytokinspektrums möglich. Da die zu messenden Zytokine jedoch auch von anderen Zelltypen produziert werden und im Organismus nur eine sehr kurze Zeit zirkulieren, korrelieren die Konzentrationen der im peripheren Blut messbaren Zytokine nicht notwendigerweise mit der Anzahl von TH1- und TH2-Zellen. Die Bestimmung des Zytokinspektrums einzelner Zellen wurde in vielen Studien über die Messung der ZytokinmRNA nach in situ-Hybridisierung durchgeführt. Allerdings bedeutet die Existenz einer ZytokinmRNA nicht, dass das entsprechende Zytokin von der betreffenden Zelle tatsächlich produziert wird, da die Translation der mRNA von komplexen intrazellulären Regulationsmechanismen beeinflusst wird. In der vorliegenden Arbeit wurde die Methode der Durchflusszytometrie eingesetzt. Zur intrazellulären Zytokin-Bestimmung wurden aus peripherem Blut isolierte Lymphozyten zunächst zur Zytokinproduktion angeregt und gleichzeitig die Ausschleusung der synthetisierten Zytokine verhindert, so dass sie intrazellulär akkumulierten. Anschließend wurden die Zellen fixiert und permeabilisiert, so dass hinzugegebene Fluoreszenzfarbstoff- Zusammenfassung 74 markierte Antikörper je nach Spezifität intrazellulär an Zytokine oder extrazellulär an Oberflächenstrukturen binden konnten. Auf diese Weise wurde die gleichzeitige Bestimmung intrazellulärer Zytokine und des extrazellulären CD4-Markers, der T-Helfer-Zellen kennzeichnet, ermöglicht. Des Weiteren konnten über die Messung der Oberflächenstrukturen CD45RA und CD45R0 naive T-Zellen von T-Gedächtnis/Effektor-Zellen unterschieden werden. Zusätzlich wurden die Befunde des Differentialblutbildes der eingeschlossenen Probanden analysiert. In der vorliegenden Arbeit konnten immunologisch verschiedene Krankheitsentitäten der MS hinsichtlich ihres Zytokinmusters als „aktive“ und „inaktive“ Untergruppen differenziert werden. „Aktive“ MS-Untergruppen (schubförmige Patienten im akuten Schub und chronischprogrediente MS-Patienten) wiesen in der Regel höhere Anteile proinflammatorische Zytokine produzierender T-Helfer-Zellen auf als die „inaktive“ Untergruppe (schubförmige Patienten im schubfreien Intervall). Die „inaktive“ MS-Untergruppe dagegen hatte im Gegensatz dazu typischerweise höhere Anteile antiinflammatorische Zytokine produzierender T-Helfer-Zellen als die „aktiven“ Untergruppen. Somit konnte auch das TH1/TH2-Paradigma bekräftigt werden, insofern sich in den genannten Untergruppen jeweils ein in Richtung TH1-Dominanz („aktiv“) oder TH2- Dominanz („inaktiv“) gehendes Ungleichgewicht fand. Die Ergebnisse der Markierung der Oberflächenstruktur CD45R0 als Charakteristikum von TGedächtnis/Effektor-Lymphozyten boten eine statistisch noch überzeugendere Bestätigung der Heterogenität der MS. Die „aktiven“ MS-Untergruppen unterschieden sich durch einen höheren Anteil CD45R0+ Lymphozyten von der „inaktiven“ MS-Untergruppe und gesunden Kontrollpersonen. Hierdurch wird die These unterstrichen, dass sich die T-Helfer-Zellen von schubförmigen MS-Patienten im akuten Schub und chronisch-progredienten MS-Patienten durch einen höheren Aktivierungszustand von stabilen schubförmigen MS-Patienten unterscheiden, letztere unterscheiden sich dagegen diesbezüglich nicht von gesunden Individuen. Die genannten Ergebnisse bekräftigen damit sowohl eine immunologische Heterogenität im zeitlichen Verlauf der schubförmigen MS als auch eine konstante Heterogenität zwischen chronisch-progredienter MS und stabiler schubförmiger MS. Darüber hinaus war auch die Analyse der Befunde des Differentialblutbildes mit dem Konzept der Unterscheidung von „aktiven“ und „inaktiven“ MS-Untergruppen sowie einer TH1/TH2Dichotomie vereinbar. Die Erkennung eines „aktiven“ immunologischen Profils eines Patienten noch vor klinischer Beschwerdemanifestation/-verschlimmerung könnte zum frühzeitigeren Einsatz einer entzündungshemmenden bzw. immunmodulierenden Therapie beitragen oder helfen, nonresponder einer laufenden Therapie zu detektieren und damit dem betroffenen Patienten eine spezifischere Therapieform zu ermöglichen. Literaturverzeichnis 6 75 Literaturverzeichnis Abbas AK, Murphy KM, Sher A (1996). Functional diversity of helper T lymphocytes. Nature 383, 787-793 Alwan WH, Kozlowska WJ, Openshaw PJ (1994). Distinct types of lung disease caused by functional subsets of antiviral T cells. J Exp Med 179, 81-89 Ando DG, Clayton J, Kono D, Urban JL, Sercarz EE (1989). Encephalitogenic T cells in the B10.PL model of experimental allergic encephalomyelitis (EAE) are of the Th-1 lymphokine subtype. Cell Immunol 124, 132-143 Barnett LA, Fujinami RS (1992). Molecular mimicry: a mechanism for autoimmune injury. FASEB J 6, 840-844 Beck J, Rondot P, Catinot L, Falcoff E, Kirchner H, Wietzerbin J (1988). Increased production of interferon gamma and tumor necrosis factor precedes clinical manifestation in multiple sclerosis: do cytokines trigger off exacerbations? Acta Neurol Scand 78, 318-323 Benveniste EN, Merrill JE (1986). Stimulation of oligodendroglial proliferation and maturation by interleukin-2. Nature 321, 610-613 Bitsch A, Schuchardt J, Bunkowski S, Kuhlmann T, Bruck W (2000). Acute axonal injury in multiple sclerosis. Correlation with demyelination and inflammation. Brain 123, 1174-1183 van Boxel-Dezaire AH, Hoff SC, van Oosten BW, Verweij CL, Drager AM, Ader HJ, van Houwelingen JC, Barkhof F, Polman CH, Nagelkerken L (1999). Decreased interleukin-10 and increased interleukin-12p40 mRNA are associated with disease activity and characterize different disease stages in multiple sclerosis. Ann Neurol 45, 695-703 Bridoux F, Badou A, Saoudi A, Bernard I, Druet E, Pasquier R, Druet P, Pelletier L (1997). Transforming growth factor beta (TGF-beta)-dependent inhibition of T helper cell 2 (Th2)induced autoimmunity by self-major histocompatibility complex (MHC) class II-specific, regulatory CD4(+) T cell lines. J Exp Med 185, 1769-1775 Burns J, Bartholomew B, Lobo S (1999). Isolation of myelin basic protein-specific T cells predominantly from the memory T-cell compartment in multiple sclerosis. Ann Neurol 45, 33-39 Calabrese P (1997). Neuropsychologische Aspekte bei multipler Sklerose. Psycho 23, 751-763 Literaturverzeichnis Capra R, Mattioli F, Marciano N, Vignolo LA, Bettinzioli M, Airo P, Cattaneo R (1990). 76 Significantly higher levels of soluble interleukin 2 in patients with relapsing-remitting multiple sclerosis compared with healthy subjects. Arch Neurol 47, 254 Chao CC, Molitor TW, Hu S (1993). Neuroprotective role of IL-4 against activated microglia. J Immunol 151, 1473-1481 Collins PD, Marleau S, Griffiths-Johnson DA, Jose PJ, Williams TJ (1995). Cooperation between interleukin-5 and the chemokine eotaxin to induce eosinophil accumulation in vivo. J Exp Med 182, 1169-1174 Confavreux C, Hutchinson M, Hours MM, Cortinovis-Tourniaire P, Moreau T (1998). Rate of pregnancy-related relapse in multiple sclerosis. Pregnancy in Multiple Sclerosis Group. N Engl J Med 339, 285-291 Croft M, Bradley LM, Swain SL (1994). Naive versus memory CD4 T cell response to antigen. Memory cells are less dependent on accessory cell costimulation and can respond to many antigen-presenting cell types including resting B cells. J Immunol 152, 2675-2685 Damek DM, Shuster EA (1997). Pregnancy and multiple sclerosis. Mayo Clin Proc 72, 977-989 de Waal Malefyt R, Abrams J, Bennett B, Figdor CG, de Vries JE (1991). Interleukin 10(IL-10) inhibits cytokine synthesis by human monocytes: an autoregulatory role of IL-10 produced by monocytes. J Exp Med 174, 1209-1220 de Waal Malefyt R, Haanen J, Spits H, Roncarolo MG, te Velde A, Figdor C, Johnson K, Kastelein R, Yssel H, de Vries JE (1991). Interleukin 10 (IL-10) and viral IL-10 strongly reduce antigen-specific human T cell proliferation by diminishing the antigen-presenting capacity of monocytes via downregulation of class II major histocompatibility complex expression. J Exp Med 174, 915-924 Ebers GC, Dyment DA (1998). Genetics of multiple sclerosis. Semin Neurol 18, 295-299 Fenichel GM (1999). Assessment: Neurologic risk of immunization: report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Neurology 52, 1546-1552 Friedrich M, Docke WD, Klein A, Philipp S, Volk HD, Sterry W, Asadullah K (2002). Immunomodulation by interleukin-10 therapy decreases the incidence of relapse and prolongs the relapse-free interval in Psoriasis. J Invest Dermatol 118, 672-677 Literaturverzeichnis 77 Fujinami RS, Oldstone MB (1985). Amino acid homology between the encephalitogenic site of myelin basic protein and virus: mechanism for autoimmunity. Science 230, 1043-1045 Gallo P, Piccinno M, Pagni S, Tavolato B (1988). Interleukin-2 levels in serum and cerebrospinal fluid of multiple sclerosis patients. Ann Neurol 24, 795-797 Gehlen W (1997). Zur Symptomatologie und Diagnostik der Multiplen Sklerose. Psycho 23, 726-736 Giovannoni G, Hartung HP (1996). The immunopathogenesis of multiple sclerosis and GuillainBarre syndrome. Curr Opin Neurol 9, 165-177 Goodin DS, Ebers GC, Johnson KP, Rodriguez M, Sibley WA, Wolinsky JS (1999). The relationship of MS to physical trauma and psychological stress: report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Neurology 52, 1737-1745 Gold R, Rieckmann P (2000). Pathogenese und Therapie der Multiplen Sklerose. 2. Auflage. UNI-MED Verlag Bremen Gomez-Lira M, Liguori M, Magnani C, Bonamini D, Salviati A, Leone M, Andreoli V, Trojano M, Valentino P, Savettieri G, Quattrone A, Pignatti PF, Momigliano-Richiardi P, Giordano M (2003). CD45 and multiple sclerosis: the exon 4 C77G polymorphism (additional studies and metaanalysis) and new markers. J Neuroimmunol 140, 216-221 Greenfield EA, Nguyen KA, Kuchroo VK (1998). CD28/B7 costimulation: a review. Crit Rev Immunol 18, 389-418 Haupts M, Schejbal P, Pöhlau D, Malin JP, Przuntek H, Gehlen W (1994). Epidemiological data on multiple sclerosis from an industrial area in northwest Germany. In: Firnhaber W, Lauer K (Herausgeber). Multiple sclerosis in Europe: an epidemiological update. Leuchtturm, LTV Press Darmstadt, 143-146 Horwitz MS, Bradley LM, Harbertson J, Krahl T, Lee J, Sarvetnick N (1998). Diabetes induced by Coxsackie virus: initiation by bystander damage and not molecular mimicry. Nat Med 4, 781785 Inoges S, Merino J, Bandres E, e Castro P, Subira ML, Sanchez-Ibarrola A (1999). Cytokine flow cytometry differentiates the clinical status of multiple sclerosis (MS) patients. Clin Exp Immunol 115, 521-525 Literaturverzeichnis 78 Jacobs R (1996). Methoden der Immunologie. In: Schedlowski M, Tewes U (Herausgeber). Psychoneuroimmunologie. Spektrum Akademischer Verlag Heidelberg Jacobsen M, Schweer D, Ziegler A, Gaber R, Schock S, Schwinzer R, Wonigeit K, Lindert RB, Kantarci O, Schaefer-Klein J, Schipper HI, Oertel WH, Heidenreich F, Weinshenker BG, Sommer N, Hemmer B (2000). A point mutation in PTPRC is associated with the development of multiple sclerosis. Nat Genet 26, 495-499 Janeway CA, Travers P, Walport M, Shlomchik MJ (2002). Immunologie. 5.Auflage. Spektrum Akademischer Verlag Heidelberg Berlin Johns LD, Flanders KC, Ranges GE, Sriram S (1991). Successful treatment of experimental allergic encephalomyelitis with transforming growth factor-beta 1. J Immunol 147, 1792-1796 Jung T, Schauer U, Heusser C, Neumann C, Rieger C (1993). Detection of intracellular cytokines by flow cytometry. J Immunol Methods 159, 197-207 Kersh GJ, Allen PM (1996). Essential flexibility in the T-cell recognition of antigen. Nature 380, 495-498 Kieseier BC, Seifert T, Giovannoni G, Hartung HP (1999). Matrix metalloproteinases in inflammatory demyelination: targets for treatment. Neurology 53, 20-25 Kitze B (2000). Diagnose und Differentialdiagnose der Multiplen Sklerose. Nervenheilkunde 6, 303-309 Kojima K, Berger T, Lassmann H, Hinze-Selch D, Zhang Y, Gehrmann J, Reske K, Wekerle H, Linington C (1994). Experimental autoimmune panencephalitis and uveoretinitis transferred to the Lewis rat by T lymphocytes specific for the S100 beta molecule, a calcium binding protein of astroglia. J Exp Med 180, 817-829 Kurtzke JF (1983). Rating neurologic impairment in multiple sclerosis: an expanded disability status scale (EDSS). Neurology 33, 1444-1452 Kurtzke JF (1995). MS epidemiology world wide. One view of current status. Acta Neurol Scand Suppl 161, 23-33 Lafaille JJ, Keere FV, Hsu AL, Baron JL, Haas W, Raine CS, Tonegawa S (1997). Myelin basic protein-specific T helper 2 (Th2) cells cause experimental autoimmune encephalomyelitis in immunodeficient hosts rather than protect them from the disease. J Exp Med 186, 307-312 Literaturverzeichnis 79 Lauer K (1994). Multiple sclerosis in the old world: the new old map. In: Firnhaber W, Lauer K (Herausgeber). Multiple sclerosis in Europe: an epidemiological update. Leuchtturm, LTV Press Darmstadt, 14-27 Lehmann PV, Forsthuber T, Miller A, Sercarz EE (1992). Spreading of T-cell autoimmunity to cryptic determinants of an autoantigen. Nature 358, 155-157 Link J, Soderstrom M, Olsson T, Hojeberg B, Ljungdahl A, Link H (1994). Increased transforming growth factor-beta, interleukin-4, and interferon-gamma in multiple sclerosis. Ann Neurol 36, 379-386 Losseff NA, Wang L, Lai HM, Yoo DS, Gawne-Cain ML, McDonald WI, Miller DH, Thompson AJ (1996). Progressive cerebral atrophy in multiple sclerosis. A serial MRI study. Brain 119, 20092019 Lucchinetti C, Bruck W, Parisi J, Scheithauer B, Rodriguez M, Lassmann H (2000). Heterogeneity of multiple sclerosis lesions: implications for the pathogenesis of demyelination. Ann Neurol 47, 707-717 Maurer M, Kruse N, Giess R, Toyka KV, Rieckmann P (2000). Genetic variation at position 1082 of the interleukin 10 (IL10) promotor and the outcome of multiple sclerosis. J Neuroimmunol 104, 98-100 Maggi E, Parronchi P, Manetti R Simonelli C, Piccinni MP, Rugiu FS, De Carli M, Ricci M, Romagnani S (1992). Reciprocal regulatory effects of IFN-gamma and IL-4 on the in vitro development of human Th1 and Th2 clones. J Immunol 148, 2142-2147 Martinelli V (2000). Trauma, stress and multiple sclerosis. Neurol Sci 21, 849-852 Martinez-Moczygemba M, Huston DP (2003). Biology of common beta receptor-signaling cytokines: IL-3, IL-5, and GM-CSF. J Allergy Clin Immunol 112, 653-665 Mason D (1998). A very high level of crossreactivity is an essential feature of the T-cell receptor. Immunol Today 19, 395-404 McCarron RM, Wang L, Racke MK, cFarlin DE, Spatz M (1993). Cytokine-regulated adhesion between encephalitogenic T lymphocytes and cerebrovascular endothelial cells. J Neuroimmunol 43, 23-30 Literaturverzeichnis 80 McColl SR, Staykova MA, Wozniak A, Fordham S, Bruce J, Willenborg DO (1998). Treatment with anti-granulocyte antibodies inhibits the effector phase of experimental autoimmune encephalomyelitis. J Immunol 161, 6421-6426 McDonald WI, Compston A, Edan G, Goodkin D, Hartung HP, Lublin FD, McFarland HF, Paty DW, Polman CH, Reingold SC, Sandberg-Wollheim M, Sibley W, Thompson A, van den Noort S, Weinshenker BY, Wolinsky JS (2001). Recommended diagnostic criteria for multiple sclerosis: guidelines from the International Panel on the diagnosis of multiple sclerosis. Ann Neurol 50, 121-127 Mokhtarian F, McFarlin DE, Raine CS (1984). Adoptive transfer of myelin basic proteinsensitized T cells produces chronic relapsing demyelinating disease in mice. Nature 309, 356358 Moore KW, O'Garra A, de Waal Malefyt R, Vieira P, Mosmann TR (1993). Interleukin-10. Annu Rev Immunol 11, 165-190 Mosmann TR, Sad S (1996). The expanding universe of T-cell subsets: Th1, Th2 and more. Immunol Today 17, 138-146 Miller A, Shapiro S, Gershtein R, Kinarty A, Rawashdeh H, Honigman S, Lahat N (1998). Treatment of multiple sclerosis with copolymer-1 (Copaxone): implicating mechanisms of Th1 to Th2/Th3 immune-deviation. J Neuroimmunol 92, 113-121 Moser M, Murphy KM (2000). Dendritic cell regulation of TH1-TH2 development. Nat Immunol 1, 199-205 Mosmann TR, Coffman RL (1989). TH1 and TH2 cells: different patterns of lymphokine secretion lead to different functional properties. Annu Rev Immunol 7, 145-173 Navikas V, He B, Link J, Haglund M, Soderstrom M, Fredrikson S, Ljungdahl A, Hojeberg J, Qiao J, Olsson T, Link H (1996). Augmented expression of tumour necrosis factor-alpha and lymphotoxin in mononuclear cells in multiple sclerosis and optic neuritis. Brain 119, 213-223 Navikas V, Link H (1996). Review: cytokines and the pathogenesis of multiple sclerosis. J Neurosci Res 45, 322-333 Nguyen LT, Ramanathan M, Munschauer F, Brownscheidle C, Krantz S, Umhauer M, Miller C, De Nardin E, Jacobs LD (1999). Flow cytometric analysis of in vitro proinflammatory cytokine secretion in peripheral blood from multiple sclerosis patients. J Clin Immunol 19, 179-185 Literaturverzeichnis 81 Nygardas PT, Maatta JA, Hinkkanen AE (2000). Chemokine expression by central nervous system resident cells and infiltrating neutrophils during experimental autoimmune encephalomyelitis in the BALB/c mouse. Eur J Immunol 30, 1911-1918 Oksenberg JR, Baranzini SE, Barcellos LF, Hauser SL (2001). Multiple sclerosis: genomic rewards. J Neuroimmunol 113, 171-184 Olsson T (1995). Cytokine-producing cells in experimental autoimmune encephalomyelitis and multiple sclerosis. Neurology 45, 11-15 Paterson PY (1960). Transfer of allergic encephalomyelitis in rats by means of lymph node cells. J Exp Med 111, 119-136 Peter JB, Boctor FN, Tourtellotte WW (1991). Serum and CSF levels of IL-2, sIL-2R, TNF-alpha, and IL-1 beta in chronic progressive multiple sclerosis: expected lack of clinical utility. Neurology 41, 121-123 Petereit HF, Richter N, Pukrop R Bamborschke S (2000). Interferon gamma production in blood lymphocytes correlates with disability score in multiple sclerosis patients. Mult Scler 6, 9-23 Pette M, Fujita K, Wilkinson D, Altmann DM, Trowsdale J, Giegerich G, Hinkkanen A, Epplen JT, Kappos L, Wekerle H (1990). Myelin autoreactivity in multiple sclerosis: recognition of myelin basic protein in the context of HLA-DR2 products by T lymphocytes of multiple-sclerosis patients and healthy donors. Proc Natl Acad Sci U S A 87, 7968-7972 Poeck K, Hacke W (2001). Neurologie. 11. Auflage. Springer Verlag Berlin Heidelberg New York Poser CM, Paty DW, Scheinberg L, McDonald WI, Davis FA, Ebers GC, Johnson KP, Sibley WA, Silberberg DH, Tourtellotte WW (1983). New diagnostic criteria for multiple sclerosis: guidelines for research protocols. Ann Neurol 13, 227-231 Powell MB, Mitchell D, Lederman J, Buckmeier J, Zamvil SS, Graham M, Ruddle NH, Steinman L (1990). Lymphotoxin and tumor necrosis factor-alpha production by myelin basic proteinspecific T cell clones correlates with encephalitogenicity. Int Immunol 2, 539-544 Powrie F, Coffman RL (1993). Cytokine regulation of T-cell function: potential for therapeutic intervention. Immunol Today 14, 270-274 Prineas JW, Kwon EE, Cho ES, Sharer LR, Barnett MH, Oleszak EL, Hoffman B, Morgan BP (2001). Immunopathology of secondary-progressive multiple sclerosis. Ann Neurol 50, 646-657 Literaturverzeichnis 82 Racke MK, Burnett D, Pak SH, Albert PS, Cannella B, Raine CS, McFarlin DE, Scott DE (1995). Retinoid treatment of experimental allergic encephalomyelitis. IL-4 production correlates with improved disease course. J Immunol 154, 450-458 Remlinger P (1928). Les paralysies du traitement antirabique. Annals Inst Pasteur 55, 35-68 Renno T, Krakowski M, Piccirillo C, Lin JY, Owens T (1995). TNF-alpha expression by resident microglia and infiltrating leukocytes in the central nervous system of mice with experimental allergic encephalomyelitis. Regulation by Th1 cytokines. J Immunol 154, 944-953 Rentzos M, Nikolaou C, Rombos A, Voumvourakis K, Segditsa I, Papageorgiou C (1996). Tumour necrosis factor alpha is elevated in serum and cerebrospinal fluid in multiple sclerosis and inflammatory neuropathies. J Neurol 243, 165-170 Rieckmann P, Albrecht M, Kitze B, Weber T, Tumani H, Broocks A, Luer W, Poser S (1994). Cytokine mRNA levels in mononuclear blood cells from patients with multiple sclerosis. Neurology 44, 1523-1526 Rieckmann P, Albrecht M, Kitze B, Weber T, Tumani H, Broocks A, Luer W, Helwig A, Poser S (1995). Tumor necrosis factor-alpha messenger RNA expression in patients with relapsingremitting multiple sclerosis is associated with disease activity. Ann Neurol 37, 82-88 Rivers TM, Sprunt DH, Berry GP (1933). Observations on attempts to produce acute disseminated encephalomyelitis in monkeys. J Exp Med 58, 39–53 Rocken M, Racke M, Shevach EM (1996). IL-4-induced immune deviation as antigen-specific therapy for inflammatory autoimmune disease. Immunol Today 17, 225-231 Romagnani S (1994). Lymphokine production by human T cells in disease states. Annu Rev Immunol 12, 227-257 Rosati G (2001). The prevalence of multiple sclerosis in the world: an update. Neurol Sci 22, 117-139 Rosche B, Kieseier B, Hartung HP, Hemmer B (2003). Neue Einblicke in die Immunpathogenese der Multiplen Sklerose. Nervenarzt 74, 654-663 Ruddle NH, Bergman CM, McGrath KM, Lingenheld EG, Grunnet ML, Padula SJ, Clark RB (1990). An antibody to lymphotoxin and tumor necrosis factor prevents transfer of experimental allergic encephalomyelitis. J Exp Med 172, 1193-1200 Literaturverzeichnis 83 Scholz C, Patton KT, Anderson DE, Freeman GJ, Hafler DA (1998). Expansion of autoreactive T cells in multiple sclerosis is independent of exogenous B7 costimulation. J Immunol 160, 1532-1538 Schwinzer R, Witte T, Hundrieser J, Ehlers S, Momot T, Hunzelmann N, Krieg T, Schmidt RE, Wonigeit K (2003). Enhanced frequency of a PTPRC (CD45) exon A mutation (77C-->G) in systemic sclerosis. Genes Immun 4, 168-169 Seder RA, Paul WE, Davis MM, Fazekas de St Groth B (1992). The presence of interleukin 4 during in vitro priming determines the lymphokine-producing potential of CD4+ T cells from T cell receptor transgenic mice. J Exp Med 176, 1091-1098 Selmaj KW, Farooq M, Norton WT, Raine CS, Brosnan CF (1990). Proliferation of astrocytes in vitro in response to cytokines. A primary role for tumor necrosis factor. J Immunol 144, 129-135 Selmaj KW, Raine CS (1998). Tumor necrosis factor mediates myelin and oligodendrocyte damage in vitro. Ann Neurol 23, 339-346 Selmaj KW, Raine CS, Cannella B, Brosnan CF (1991). Identification of lymphotoxin and tumor necrosis factor in multiple sclerosis lesions. J Clin Invest 87, 949-954 Sharief MK, Hentges R (1991). Association between tumor necrosis factor-alpha and disease progression in patients with multiple sclerosis. N Engl J Med 325, 467-472 Sher A, Coffman RL (1992). Regulation of immunity to parasites by T cells and T cell-derived cytokines. Annu Rev Immunol 10, 385-409 Simmons RD, Willenborg DO (1990). Direct injection of cytokines into the spinal cord causes autoimmune encephalomyelitis-like inflammation. J Neurol Sci 100, 37-42 Sivieri S, Ferrarini AM, Gallo P (1998). Multiple sclerosis: IL-2 and sIL-2R levels in cerebrospinal fluid and serum. Review of literature and critical analysis of ELISA pitfalls. Mult Scler 4, 7-11 Sloan-Lancaster J, Allen PM (1996). Altered peptide ligand-induced partial T cell activation: molecular mechanisms and role in T cell biology. Annu Rev Immunol 14, 1-27 Stoy NS (2002). Monocyte/macrophage initiation of organ-specific autoimmunity: the ultimate 'bystander' hypothesis? Med Hypotheses 58, 312-326 Literaturverzeichnis 84 The Lenercept Multiple Sclerosis Study Group and The University of British Columbia MS/MRI Analysis Group (1999). TNF neutralization in MS: results of a randomized, placebo-controlled multicenter study. Neurology 53, 457-465 Thomas LL (1995). Basophil and eosinophil interactions in health and disease. Chem Immunol 61, 186-207 Trapp BD, Ransohoff R, Rudick R (1999). Axonal pathology in multiple sclerosis: relationship to neurologic disability. Curr Opin Neurol 12, 295-302 Trotter JL, Clifford DB, Anderson CB, van der Veen RC, Hicks BC, Banks G (1988). Elevated serum interleukin-2 levels in chronic progressive multiple sclerosis. N Engl J Med 318, 1206 Trotter JL, Collins KG, van der Veen RC (1991). Serum cytokine levels in chronic progressive multiple sclerosis: interleukin-2 levels parallel tumor necrosis factor-alpha levels. J Neuroimmunol 33, 29-36 van Oosten BW, Barkhof F, Truyen L, Boringa JB, Bertelsmann FW, von Blomberg BM, Woody JN, Hartung HP, Polman CH (1996). Increased MRI activity and immune activation in two multiple sclerosis patients treated with the monoclonal anti-tumor necrosis factor antibody cA2. Neurology 47, 1531-1534 Voskuhl RR (1998). Myelin protein expression in lymphoid tissues: implications for peripheral tolerance. Immunol Rev 164, 81-92 Voskuhl RR, Martin R, Bergman C, Dalal M, Ruddle NH, McFarland HF (1993). T helper 1 (Th1) functional phenotype of human myelin basic protein-specific T lymphocytes. Autoimmunity 15, 137-143 Waldmann TA (1986). The structure, function, and expression of interleukin-2 receptors on normal and malignant lymphocytes. Science 232, 727-732 Wegmann TG, Lin H, Guilbert L, Mosmann TR (1993). Bidirectional cytokine interactions in the maternal-fetal relationship: is successful pregnancy a TH2 phenomenon? Immunol Today 14, 353-356 Weigent DA, Stanton GJ, Johnson HM (1983). Interleukin 2 enhances natural killer cell activity through induction of gamma interferon. Infect Immun 41, 992-997 Weiner HL (1997). Oral tolerance: immune mechanisms and treatment of autoimmune diseases. Immunol Today 18, 335-343 Literaturverzeichnis Wekerle H, Kojima K, Lannes-Vieira J, Lassmann H, Linington C (1994). Animal models. 85 Ann Neurol 36, 47-53 Weller RO, Engelhardt B, Phillips MJ (1996). Lymphocyte targeting of the central nervous system: a review of afferent and efferent CNS-immune pathways. Brain Pathol 6, 275-288 Williams KC, Ulvestad E, Hickey WF (1994). Immunology of multiple sclerosis. Clin Neurosci 2, 229-245 World Map of Prevalence of Multiple Sclerosis (Zugriff vom 04.04.2004). http://www.multsclerosis.org/ms_world.html Wucherpfennig KW, Strominger JL (1995). Molecular mimicry in T cell-mediated autoimmunity: viral peptides activate human T cell clones specific for myelin basic protein. Cell 80, 695-705 Young JL, Ramage JM, Gaston JS, Beverley PC (1997). In vitro responses of human CD45R0brightRA- and CD45R0-RAbright T cell subsets and their relationship to memory and naive T cells. Eur J Immunol 27, 2383-2390 Zamvil SS, Steinman L (1990). The T lymphocyte in experimental allergic encephalomyelitis. Annu Rev Immunol 8, 579-621 Anhang Tabelle 11. Mediane der untersuchten Parameter (1. Spalte) in den Über- und Untergruppen (1. Zeile). Kontrolle OND MS N.I.OND Infl.OND RR-MS Schub-MS CP-MS CD45RA% 66,59 59,62 67,97 58,64 63,52 68,64 60,09 63,49 CD45R0% 13,31 19,71 18,29 16,93 26,81 15,06 25,87 22,17 RA/R0-Ratio 4,83 3,46 3,42 3,55 2,37 4,65 2,32 2,91 0,03 0,78 2,56 0,74 0,96 1,77 3,33 4,14 0,16 1,13 5,53 1,26 0,86 3,18 10,47 11,60 2,34 2,05 3,89 2,80 1,95 3,11 1,13 7,03 5,05 4,16 5,51 4,16 4,65 5,95 0,64 5,51 1,71 0,76 0,53 1,29 0,68 0,12 0,86 0,53 0,32 0,33 0,17 0,34 0,31 0,10 0,18 0,20 0,16 0,47 0,38 0,38 0,55 0,59 0,46 0,27 0,06 0,15 0,07 0,13 0,44 0,04 0,32 0,13 0,09 0,24 0,15 0,18 0,50 0,25 0,04 0,07 CD4 IL-10 0,02 0,14 0,00 0,10 0,35 0,00 0,00 0,03 Leuko/nl 5,63 6,02 7,49 6,32 5,08 7,54 7,70 6,37 Neutro% 59,25 61,9 64,05 63,00 60,50 61,90 70,80 63,65 Lympho% 32,90 30,25 27,15 29,70 32,80 29,30 18,70 29,70 Mono% 4,70 3,90 5,35 3,60 5,40 4,30 5,30 5,55 Eosino% 1,65 1,95 2,40 1,70 2,60 2,80 0,60 1,35 Baso% 0,80 0,85 0,90 0,90 0,50 1,20 0,80 0,90 + CD4 IFN-γ - CD4 IFN-γ + CD4 TNF-α - CD4 TNF-α + CD4 IL-2 - CD4 IL-2 + CD4 IL-4 - CD4 IL-4 + CD4 IL-10 - Mein Dank gilt … … allen Patienten und Kontrollpersonen, die an dieser Untersuchung teilnahmen. … Prof. Dr. med. Thomas Müller für die Übernahme der Betreuung und Begutachtung der Arbeit. … Dr. med. Dieter Pöhlau für die Überlassung dieses wirklich spannenden Themas. … Dipl. biol. Dr. rer. nat. Maike Rieks für die Betreuung der Arbeit vom ersten (Labor-) Tag an, für die Motivation, konstruktive Kritik und Bereitstellung von Heißgetränken. … Martin Hörstgen für die freundschaftliche Zusammenarbeit in der neuroimmunologischen Arbeitsgruppe. … Martin, David, Alan, Andy, Ronan, Joakim, Clas, Eskil, Henrik, Vasi u.a. für die „lautstarke Unterstützung“. … meinen Eltern für ihre Hilfe. … Marc Lienemann für die gegenseitige Motivation „kurz vor Schluss“. … Dorothee für das aufmerksame Korrekturlesen mit geschulten Pädagogenaugen ganz im Sinne der Rechtschreibreform. … meiner Frau Maria für oben genanntes und noch mehr … Lebenslauf Name Alberti Vorname Thomas Geburtstag 22.11.1970 Geburtsort Hagen Wohnort Hauptstr. 79, 46244 Bottrop Familienstand verheiratet Kinder Silas Alberti, geboren am 19.09.2001 Schulbildung 1977-1981 Vinckeschule Hagen 1981-1990 Christian-Rohlfs-Gymnasium Hagen Erwerb der Allgemeinen Hochschulreife Grundwehrdienst 1990-1991 Fernmeldeaufklärung in Frankenberg/Eder Studium 1991-1998 Studium der Humanmedizin an der Ruhr-Universität Bochum 1998 3. Staatsexamen, Note Sehr Gut Prüfung in den Fächern Innere Medizin, Chirurgie, Neurologie und Orthopädie Gesamtnote 1,66 Tätigkeiten 1998-2003 Assistenzarzt in der Klinik für Neurologie und Neuroradiologie bei Herrn Dr. med. von Both, St. Johannes-Hospital Hagen seit 2000 Dozent für Neurologie und Psychiatrie an der Schule für Logopädie der AWO in Hattingen seit 2003 Assistenzarzt in der Klinik für Psychiatrie und Psychotherapie bei Frau Dr. med. Bongardt, Johanniter Klinikum Oberhausen