Deutsches Ärzteblatt 1991: A-33
Werbung

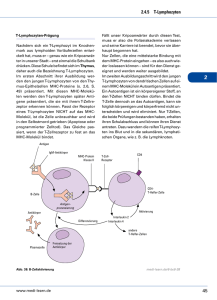
DEUTSCHES ÄRZTEBLATT Transplantationen (2) Dieter Kabelitz ährend die hyperakute Abstoßungsreaktion (innerhalb von Stunden nach Transplantation) auf präformierte Antikörper im Serum des Empfängers zurückzuführen ist, sind an der chronischen Abstoßung in aller Regel T-Lymphozyten wesentlich beteiligt. Zirkulierende T-Lymphozyten des Organempfängers erkennen die fremden Gewebsantigene („Histokompatibilitätsantigene" oder HLA-Antigene) auf den Parenchymzellen des transplantierten Organs; hierdurch kommt es zur T-Zell-Aktivierung mit anschließender Differenzierung der T-Lymphozyten in Effektorzellen, welche entweder zytolytisch aktiv sind oder diverse Entzündungsmediatoren/Zytokine sezernieren können. HIA-Antigene und T-Zell Aktivierung Man unterscheidet zwei Klassen von HLA-(Human Leukocyte Antigen-)Antigenen (Tabelle 1): HLAAntigene der Klasse I werden in HLA-A-, HLA-B- und HLA-C-Regionen unterteilt; diese Antigene sind auf allen kernhaltigen Zellen des Organismus sowie auf Thrombozyten zu finden. HLA-Klasse-I-Antigene werden von CD8-positiven T-Lymphozyten erkannt; Gewebezellen, die fremde (das heißt Spender-) HLA-Klasse-I-Antigene exprimieren, können somit von CD8-positiven T Zellen zytotoxisch attackiert werden. Im Unterschied zu HLA-KlasseI-Antigen en ist die Gewebeverteilung - Perspektiven der TransplantationsImmunologie Die Transplantation eines fremden Organs stellt für das Immunsystem des Empfängers eine Alarmsituation dar. Der Kontakt mit fremden Gewebsantigenen aktiviert die Zellen des Immunsystems, es kommt zur „Abstoßungsreaktion". Nachdem die chirurgische Problematik der Organtransplantation heute weitgehend als gelöst angesehen werden darf, konzentrieren sich die Erwartungen bezüglich einer weiteren Verbesserung vor allem auf die Immunologie. der Klasse-Il-Antigene (HLA-DR, HLA-DP, HLA-DQ) wesentlich eingeschränkter (Tabelle 1). So findet man HLA-Klasse-II-Antigene auf B-Lymphozyten, Makrophagen, dendritischen Zellen sowie auf Langerhans-Zellen der Haut. HLA-KlasseII-Antigene sind die Zielantigene für CD4-positive T-Lymphozyten, welche nach Aktivierung vor allem Zytokine (zum Beispiel Interleukin-2 und Gamma-Interferon) sezernieren. Der genetische Polymorphismus der HLA-Antigene ist groß. Da zudem von jedem Genlocus (HLA-A, -B, -C, -DR, -DP, -DQ) zwei Allele (ein väterliches, ein mütterliches) exprimiert werden, ist die Vielzahl unterschiedlicher HLA-Konstellationen in der Bevölkerung nahezu grenzenlos. Abteilung Transplantations-Immunologie (Direktor: Prof. Dr. med. Gerhard Opelz) und Institut für Immunologie (Direktor: Prof. Dr. med. Klaus Rother) der Ruprecht-Karls-Universität Heidelberg Die T-Lymphozyten-Aktivierung, wie sie nach Transplantation fremden Gewebes im Empfänger stattfinden kann, ist in Form eines „Minimalmodells" in Abbildung 1 dargestellt. Ruhende CD4-positive T-Zellen erkennen über ihr T-Zellrezeptor-(TZR-)Molekül fremde HLA-Klasse-II-Antigene; hierdurch wird die T-Zelle aktiviert, sie produziert den T-Zell-Wachstumsfaktor Interleukin-2 (11-2) und bildet zugleich Rezeptoren für 11-2 auf ihrer Oberfläche aus. Die Bindung von 11-2 an den I1-2-Rezeptor stimuliert die Zellteilung; die CD4-positive T-Zelle proliferiert und sezerniert neben 11-2 weitere Zytokine (unter anderem Interleukin-4, Gamma-Interferon, Tumor-Nekrose-Faktor-a). CD8-positive T-Zellen erkennen dagegen fremde HLA-Klasse-I-Antigene und exprimieren im Anschluß ebenfalls I1-2-Rezeptoren. Wenn 11-2 von aktivierten CD4-positiven T-Lymphozyten zur Verfügung gestellt wird, kann die 11-2-Rezeptorpositive CD8 -LT-Zelle sich ebenfalls teilen und in eine zytotoxische Effektorzelle ausreifen (Abbildung 1). Die CD8+-T-Zelle ist also in aller Regel auf die Hilfe (in Form von 11-2) von CD4-positiven T-Zellen angewiesen. Für die Pathophysiologie der Abstoßungsreaktion von besonderer Wichtigkeit ist die Tatsache, daß HLA-DR-(Klasse II-)Antigene auf vielen Körperzellen (zum Beispiel Endothelzellen) durch Zytokine (insbesondere Gamma-Interferon) induziert werden können. So können Transplantat-infiltrierende CD4-positive T-Lymphozyten durch die Sekretion von Gamma-Interferon die Dt. Ärztebl. 88, Heft 1/2, 7. Januar 1991 (33) A-33 • Expression von HLA-DR-Antigenen im Transplantat stimulieren, was wiederum zu einer verstärkten Aktivierung CD4-positiver T-Zellen führt (Abbildung 2). Die aberrante HLA-DR-Expression im Rahmen einer zellulären Abstoßungsreaktion läßt sich immunhistologisch an Biopsie-Material häufig nachweisen. Tabelle 1: Eigenschaften und Gewebeverteilung von HLA-Antigenen HLA Klasse I HLA Klasse II Regionen HLA-A, -B, -C HLA-DR, -DP, -DQ Vorkommen alle kernhaltigen Zellen, Thrombozyten B-Lymphozyten, Makrophagen, dendritische Zellen, Langerhans-Zellen „Matching" von Spender und Empfänger Je besser Organspender und -empfänger in ihren HLA-Antigenen übereinstimmen, desto geringer ist die Gefahr der T-Zell-Aktivierung durch Donor-HLA-Antigene. Multizentrische Studien haben zweifelsfrei belegt, daß die Erfolgsrate bei Nierentransplantation mit dem Grad der HLA-Kompatibilität („match") von Spender und Empfänger korreliert (1). Der zuverlässigen HLA-Typisierung kommt daher eine zentrale Bedeutung in der Transplantationsmedizin zu. Die HLA-Typisierung erfolgt serologisch in einem Mikrozytotoxizitäts-Test unter Einsatz von Aktivierung V Induktion durch Gamma-Interferon Ziel-Antigen für T-ZellSubpopulation +++ CD8 Seren mit definierter HLA-Spezifität. Die serologische Typisierung von HLA-DR ist jedoch problematisch und gelegentlich nicht interpretierbar. Hier zeichnen sich durch den Einsatz molekular-biologischer Methoden neue Perspektiven ab. So läßt sich durch eine Kombination der Polymerase-Kettenreakti- Proliferation 1 HLA-II 1 (IL-2 Rezeptor+) v CD4+ Zytokine: - IL-2, IL-4 -TNF-a - IFN-y CD82 —.■ zytotoxische Effektorzelle CD8+ 1 Ä 1 HLA-I 1 CD8+ CD8+ Abbildung 1: Aktivierung von T-Lymphozyten durch HLA-Antigene des Organ-Spenders CD4+ -T-Zellen des Empfängers erkennen fremde HLA-Klasse-II-(HLA-DR-)Antigene und werden hierdurch aktiviert, das heißt, sie produzieren Interleukin-2 (11-2) und exprimieren selbst 11-2-Rezeptoren. Nach Bindung von 11-2 an den Rezeptor kann die CD4+ -T-Zelle proliferieren. Neben 11-2 werden von der aktivierten CD4+ -T-Zelle weitere Zytokine sezerniert, unter anderem Interleukin-4 (11-4), Tumor-Nekrose-Faktor (TNF-a) und Gamma-Interferon (IFN-a). CD8-positive T-Zellen des Empfängers erkennen dagegen die fremden HLA-Klasse-I-Antigene (HLA-A, HLA-B) des Spenders. Falls 11-2 von CD4 ± -T-Zellen bereitgestellt wird, können die aktivierten CD8+ -T-Zellen proliferieren und in zytotoxische Effektorzellen ausreifen, welche schließlich das Transplantat zerstören A-34 (34) Dt. Ärztebl. 88, Heft 1/2, 7. Januar 1991 CD4 + an (PCR, polymerase chain reaction) mit der Methode des RFLP (restriction fragment length polymorphism) unter Verwendung spezifischer GenSonden die HLA-Klasse-II-Typisierung zweifelsfrei durchführen. Hiermit lassen sich auch HLA-Regionen typisieren, die serologisch schlecht oder gar nicht (zum Beispiel HLADP) typisierbar sind. Der mögliche Einfluß einer HLA-DP-Inkompatibilität konnte aus den genannten Gründen bisher klinisch nicht berücksichtigt werden; diese Frage wird in prospektiven Studien unter Einsatz der PCR-RFLP untersucht werden können. Darüber hinaus ist zu hoffen, daß die Methoden der Organkonservierung weiter verbessert werden. Während die explantierte Niere über mindestens 24 Stunden gut konservierbar ist (und somit ausreichend Zeit besteht, um die HLA-Typisierung an Lymphozyten des Organspenders durchzuführen und die Niere zu einem geeigneten [HLAkompatiblen] Empfänger zu transportieren), ist dieses Zeitintervall bei Leber und Herz so kurz, daß auf eine Empfängerauswahl, basierend auf HLA-Kompatibilität, bisher verzichtet werden muß. Interessanterweise ist die fehlende HLA-Kompatibilität zwischen Empfänger und Spender bei der Leber- oder Herztransplantation nicht notwendigerweise mit einer schlechten Erfolgsrate verknüpft (2, 3). Zu diesem Punkt sind jedoch multizentrische Studien mit großen Patientenzahlen erforderlich, bevor ein endgültiges Urteil gefällt werden kann. Immunsuppressive Therapie: Neue Substanzen, neue Konzepte Die immunsuppressive Basistherapie besteht heute aus Methylprednisolon, Azathioprin (Imurek®) und Cyclosporin A (Sandimmun®). Die Einführung von Cyclosporin A hat die Erfolgsraten in der Transplantation-Medizin ganz entscheidend verbessert; die nicht unerheblichen Nebenwirkungen von Cyclosporin A (Nephrotoxizität) stellen jedoch für die Langzeittherapie eine bedeutende Komplikation dar (Tabelle 2). Der Wirkungsmechanismus von Cyclosporin A liegt in der Hemmung der Produktion von Zytokinen wie Interleukin-2 (Abbildung 3), wodurch die T-Zell-Aktivierung blockiert wird (vergleiche Abbildung 1). Zur Behandlung von aktuen Abstoßungsreaktionen wird heute vielfach der monoklonale Antikörper (MAK) Orthoclone OKT3R gegeben. OKT3 ist gegen das CD3-Antigen auf T-Lymphozyten gerichtet (Abbildung 3), welches in der T-ZellAktivierung eine wichtige Rolle als „Signalübermittler" spielt. Über einen ähnlichen Mechanismus wirkt der MAK BMA031, der gegen das Abbildung 2: Gamma-Interferon induziert HLA-DR-Antigene auf Endothelzellen. Eine transplantatinfiltrierende CD4positive T- Zelle erkennt fremdes HLADR-Antigen und produziert Gamma-Interferon. Sezerniertes Gamma-Interferon stimuliert die Expression von HLA-DR-Antigenen auf Endothelzellen, wodurch weitere CD4-positive T- Zellen aktiviert werden 7-Interferon In UI CsA O FK 506 • anti-CD3 (OKT3) anti-TCR (BMA031) anti-TCR VB anti-IL-2R IL-2-Toxin anti-CD4 BI la III BI • • T-Zellrezeptor-Molekül auf der Oberfläche von T-Lymphozyten gerichtet ist und dadurch die Fremdantigen-Erkennung durch T-Zellen verhindert (Abbildung 3). Grundsätzlich ist bei der therapeutischen Anwendung von monoklonalen Antikörpern damit zu rechnen, daß der Patient Antikörper gegen den MAK bildet, da es sich hierbei um MausImmunglobuline handelt, die vom menschlichen Immunsystem als Fremdprotein erkannt werden. Nach Auftreten von Anti-Maus-Immunglobulin-Antikörpern ist die therapeutische Wirksamkeit der monoklonalen Antikörper stark beeinträchtigt. Folgende Entwicklungen versprechen für die nahe Zukunft wei- O • HLA-DR tere Verbesserungen in der immunsuppressiven Therapie: > Klinische Prüfung neuer Substanzen wie FK 506; > Erprobung von monoklonalen Antikörpern gegen Subpopulationen von T-Zellen; > „Humanisierung" von monoklonalen Antikörpern. FK 506 wurde vor vier Jahren in Japan als Antibiotikum aus Streptomyces tsukubaensis isoliert. Ähnlich wie Cyclosporin A wirkt FK 506 vor allem über die Blockierung der Interleukin-2-Synthese (Abbildung 3); ein vergleichbarer immunsuppressiver Effekt wird jedoch bei etwa 100fach geringerer Dosis erzielt (4). Klinische Studien mit FK 506 sind in erster Linie am TransplantationsZentrum Pittsburgh durchgeführt worden. Die bisherigen Ergebnisse sind vielversprechend (5); Toxizität und Nebenwirkungen in der Langzeittherapie (Tabelle 2) lassen sich jedoch zum jetzigen Zeitpunkt noch nicht endgültig beurteilen. Der Einsatz von monoklonalen Antikörpern zur Prophylaxe und Therapie von Abstoßungsreaktionen wird weiter zunehmen. Obwohl sich Abbildung 3: Angriffspunkte immunsuppressiver Therapie. Cyclosporin A (1) und FK 506 (2) blockieren die Produktion von Interleukin 2 und anderer Zytokine durch Hemmung der Transkription. Monoklonale Antikörper gegen CD3 (3), konstante (4) und variable (5) Bereiche des T-Zellrezeptors, I1-2-Rezeptor (6) oder CD4 (8) blockieren dieAktivierung von T-Lymphozyten, indem sie die Bindung des natürlichen Ligaeden an die genannten Strukturen hemmen. Interleukin-2-Toxine (7) binden an I1-2-Rezeptor-positive (das heißt aktivierte) T-Zellen und eliminieren diese durch die Toxin-Wirkung Dt. Arztebl. 88, Heft 1/2, 7. Januar 1991 (35) A-35 OKT3 in der Behandlung akuter Abstoßungskrisen bewährt hat (6), sind unerwünschte Nebenwirkungen vor allem aufgrund der OKT3-vermittelten transienten T-Zell-Aktivierung zu beobachten. So steigen die Serumspiegel von Interleukin-2, Gamma-Interferon und Tumor-NekroseFaktor nach einmaliger OKT3-Gabe drastisch an (7), wodurch sich Nebenwirkungen wie Fieber erklären lassen. Monoklonale Antikörper wie OKT3 reagieren mit allen T-Zellen und führen daher zu einer massiven Verminderung der zirkulierenden T-Lymphozyten. Wünschenswert ist dagegen die selektive Ausschaltung derjenigen T-Zellen, die an der Abstoßungsreaktion beteiligt sind. Dieses Ziel wird mit mehreren Strategien verfolgt (Abbildung 3). Monoklonale Antikörper gegen den I1-2Rezeptor erkennen nur I1-2-Rezeptor-positive, das heißt „aktivierte" T-Zellen; derartige MAK sind also wesentlich selektiver als OKT3, und ermutigende klinische Erfahrungen liegen bereits vor. Anti-CD4-Antikörper blockieren die für die Initiierung der Abstoßungsreaktion so wichtigen CD4-positiven T-Zellen (siehe Abbildung 1) und können somit zumindest im Tiermodell „Toleranz" erzeugen. Schließlich ist denkbar (Abbildung 3), daß monoklonale Antikörper gegen den variablen Bereich des T-Zellrezeptors (anti-Vß) zur Prophylaxe oder Therapie der Abstoßungsreaktion einsetzbar sind. Entsprechende Anti-Vß-Antikörper reagieren nur mit denjenigen T-Zellen des Empfängers, welche tatsächlich die fremden (Spender-)HLA-Antigene erkennen, während alle anderen T-Zellen unberührt bleiben. Monoklonale Anti-Vß-Antikörper würden also ein Höchstmaß an spezifischer Immunsuppression vermitteln; allerdings ist der logistische Aufwand beträchtlich, da für jeden Patienten ein „maßgeschneiderter" Anti-Vß-Antikörper verwendet werden müßte. Der therapeutische Effekt von monoklonalen Antikörpern wird stark eingeschränkt, wenn der Patient selbst Antikörper gegen das Maus-Immunglobulin entwickelt. Tabelle 2: Wirkungsmechanismen und Nebenwirkungen von einigen Immunsuppressiva. Stoffklasse Handelsname Mechanismus Nebenwirkung Cyclosporin A Sandimmun® Hemmung der Zytokinproduktion nephrotoxisch, Lymphom? Hemmung der Zytokinproduktion nephrotoxisch (?) diabetogen (?) Blockierung und teilweise Eliminierung von T-Zellen Fieber, Schüttelfrost, Anti-Maus-Antikörper FK 506 Anti-CD3Antikörper Orthoclone OKT3® Um dies zu verhindern, versucht man, entsprechende monoklonale Antikörper zu „humanisieren". Hierbei wird der monoklonale Antikörper so modifiziert, daß die Antigenbindende Region des Maus-Antikörpers erhalten bleibt, der Rest aber (einschließlich Fc-Region) durch menschliches Immunglobulin ersetzt wird. Hierdurch kann die Gefahr der Sensibilisierung gegen Maus-Protein ausgeschaltet werden. Schließlich können aktivierte T-Zellen selektiv durch Interleukin-2-Toxine ausgeschaltet werden (Abbildung 3). Fusionsproteine aus 11-2 und Diphtherie-Toxin binden an I1-2-Rezeptor-positive (das heißt aktivierte) T-Zellen und zerstören diese durch die Toxin-Wirkung (8). Ob sich hieraus ein klinisch nutzbarer Zugang zur Behandlung von Abstoßungsreaktionen ergibt, muß jedoch in Tierversuchen weiter überprüft werden. Ziel: Individuell angepaßte Immunsuppression Da immunsuppressive Medikamente wie Cyclosporin A bei chronischer Anwendung erhebliche Nebenwirkungen haben (vor allem Nephrotoxizität; Tabelle 2), ist eine individuell angepaßte, möglichst niedrige Dosierung bei Dauertherapie wünschenswert. Leider gibt es derzeit keine Kriterien, aufgrund derer die immunsuppressive Therapie bei klinisch gut funktionierendem A-36 (36) Dt. Ärztebl. 88, Heft 1/2, 7. Januar 1991 Transplantat reduziert oder eventuell ganz abgesetzt werden könnte. In der Gewebekultur läßt sich bei einigen Nierentransplantierten eine selektive Nicht-Reaktivität der zytotoxischen T-Zellen gegenüber Spenderzellen nachweisen (9). Es wird zu prüfen sein, ob der In-vitro-Nachweis einer „erworbenen Toleranz" auf der T-Zell-Ebene als ausreichendes Kriterium für ein Absetzen der immunsuppressiven Therapie gewertet werden kann. Für die Transplantationsmedizin sind die Ergebnisse der immunologischen Grundlagen-Forschung von ganz besonderer Bedeutung. Es bleibt zu hoffen, daß uns weitere Fortschritte der Immunologie dem eigentlichen Ziel näherbringen: das Immunsystem des Organempfängers so zu überlisten, daß es das tranplantierte Organ nicht mehr als „fremd" erkennt. Die Zahlen in Klammem beziehen sich auf das Literaturverzeichnis im Sonderdruck, anzufordem über den Verfasser. Meinem Vater, Herrn Professor Dr. med. Hans-Joachim Kabelitz zum 70. Geburtstag gewidmet Anschrift des Verfassers: Prof. Dr. med. Dieter Kabelitz Abteilung TransplantationsImmunologie, Institut für Immunologie der Universität Im Neuenheimer Feld 305 W-6900 Heidelberg