Pseudomonas aeruginosa - Institut für Hygiene und Öffentliche
Werbung

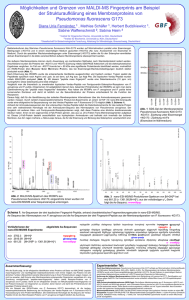
Kupfer und Pseudomonas aeruginosa Pseudomonas aeruginosa Biofilme, Kultivierbarkeit und Kupferionen unter Berücksichtigung der Trinkwasser-Installation Dr. Jost Wingender Biofilm Centre, Aquatische Mikrobiologie, Universität Duisburg-Essen 10. Hygiene Forum Bonn, 12. September 2013 Biofilm Centre Pseudomonas aeruginosa Natürliches Umweltbakterium Weltweit verbreitet, in Oberflächengewässern, in technischen Wassersystemen (besonders relevant in Trinkwasser-Installationen und im Schwimmbädern); Vermehrung unter nährstoffreichen und nährstoffarmen Bedingungen, im Wasser und in Biofilmen. Bedeutung als fakultativ pathogener Krankheitserreger - Häufige Ursache (10 % - 20 %) von nosokomialen Infektionen. - Ursache systemischer und lokaler, akuter oder chronischer Infektionen: Pneumonien bei Patienten mit zystischer Fibrose oder intubierten Patienten, Infektionen von Brandwunden, chronische Wundinfektionen, Harnwegsinfektionen, Endokarditis, Haut- und Augeninfektionen, Otitis externa. - Erreger mit höchster Priorität (gemäß RKI). (Priorisierung übertragbarer Infektionserreger unter dem Aspekt der Surveillance und epidemiologischen Forschung, Epidemiol. Bull. 2011 Nr. 44) Biofilm Centre Vorkommen von P. aeruginosa im Trinkwasser Ergebnisse einer Befragung unter DVGW-Mitgliedsunternehmen mit Daten aus den Jahren 2003 und 2004. Probenahmestellen (Anzahl der Proben) Anzahl der auf P. aeruginosa untersuchten Positive Proben, gruppiert nach Befundhöhe Befunde (%) Befundhöhe (KBE/100 mL) 0 1-5 6-10 11-30 31-100 > 100 Wasserwerksausgang 53 0 0 0 0 0 0 (53) Verteilungsnetz, 5069 35 2 5 0 4 0,9 Routine (5115) Trinkwasser1205 66 13 11 22 21 9,9 Installation (1338) Neubauleitung 2791 121 26 56 25 32 8,5 (3051) Sonstiges 172 26 14 7 3 3 23,5 (225) Alle Stellen (Summe) 9290 248 55 79 50 60 5,0 (9782) Quelle: Wingender, Hambsch und Schneider, 2009 Biofilm Centre 3 Trinkwasser-Installation (Hausinstallation) TrinkwV 2013 (§ 3 Nr. 3): Trinkwasser-Installation ist die Gesamtheit der Rohrleitungen, Armaturen und Apparate, die sich zwischen dem Punkt des Übergangs von Trinkwasser aus einer Wasserversorgungsanlage an den Nutzer und dem Punkt der Entnahme von Trinkwasser befinden. Die letzten Meter auf dem Weg zum Wasserhahn Die Trinkwasser-Installation stellt aus technischer und hygienischer Sicht eine sehr kritische Komponente in der Versorgungskette mit Wasser vom Wasserwerk bis zum Zapfhahn des Nutzers dar. Biofilm Centre P. aeruginosa in der Trinkwasser-Installation P. aeruginosa ist insbesondere in der Trinkwasser-Installation von medizinischen Einrichtungen von hoher Relevanz. Regelwerk Empfehlung Umweltbundesamt (2006) Anforderung Krankenhäuser sowie andere medizinische Einrichtungen und Pflegeeinrichtungen: 0 KBE/100 mL (Höchstwert) Richtlinie VDI 6023 (2013) Inbetriebnahme einer Trinkwasser-Installation in Hygiene in Trinkwassermedizinischen Einrichtungen in Gebäuden; Installationen Füllwasser: nicht nachweisbar in 100 mL Auswertung von Erhebungen deutscher Gesundheitsbehörden in über 4400 öffentlichen Gebäuden (2003 – 2009; Kistemann et al., 2010): Überschreitung von 0 KBE/100 mL (Pseudomonas sp.) Mikrobiologischer Parameter Gebäudenutzung Pseudomonas sp. Gesamt Krankenhaus Biofilm Centre Probenanzahl Überschreitung (%) 3468 670 2,9 7,2 P. aeruginosa-Infektionen und deren Assoziation mit Wasser (Beispiele) Zwischen 30 % - 40 % aller nosokomialen Infektionen mit P. aeruginosa sind assoziiert mit der Kontamination von Leitungswasser (Reuter et al., 2002). Schätzung: in den USA ereignen sich ca. 1 400 Todesfälle pro Jahr aufgrund von krankenhauserworbenen Pneumonien durch wasserassoziierte Infektionen mit P. aeruginosa (Anaissie et al., 2002). Das Vorkommen von P. aeruginosa in Freizeitgewässern (Schwimmbäder, Whirlpools, Badegewässer) und Hydrotherapiebecken kann zu Erkrankungen und Ausbrüchen von Dermatitis/Follikulitis und Otitis externa führen. P. aeruginosa wird als eines der wichtigsten Pathogene angesehen, die als bakteriellen Kontaminanten von Trinkwasser-Installationen auftreten und in Trinkwasserbiofilmen persistieren. Biofilm Centre Was sind Biofilme? Biofilme sind Lebensgemeinschaften von Mikroorganismen, häufig an Grenzflächen (fest-flüssig, flüssig-Luft), in hoher Zelldichte und eingebettet in eine wasserhaltige Matrix aus extrazellulären polymeren Substanzen. Biofilm-Modell: Heterogene Biofilme an natürlichen und technischen aquatischen Standorten unter nährstoffarmen Bedingungen. Biofilm Centre Verbreitung von Biofilmen Biofilme sind die vorherrschende Lebensform von Mikroorganismen in der natürlichen Umwelt, in technischen Systemen (z. B. Wasserverteilungsanlagen) und im medizinischen Bereich (z. B. bei Infektionen). Ca. 65 % aller mikrobiellen Infektionen werden durch Biofilme verursacht (National Institutes of Health, USA). Erkrankungen mit Beteiligung von Biofilmen: Lungeninfektionen bei zystischer Fibrose, chronische Wundinfektionen, Endokarditis, Harnwegsinfektionen, Zahnerkrankungen, Otitis media, Infektion von Implantaten. Biofilm von Pseudomonas aeruginosa in der Lunge von CF-Patienten (oben, Chan et al., 1980; unten: Bjarnsholt et al., 2013) Biofilm Centre Mikroorganismen in Trinkwassersystemen Verteilung der Mikroorganismen - 95 % in Biofilmen an Oberflächen (ca. 4 x 105 – 2 x 108 Zellen/cm²) - 5 % in der Wasserphase (und dort werden üblicherweise Proben genommen!) (ca. 2 x 104 – 6 x 105 Zellen/mL) Trinkwasser Bild: M. Moritz, Biofilm Centre, UDE planktonische Bakterien Biofilme Freisetzung Trinkwasserbiofilm (7 Tage alt) auf einer Stahloberfläche Vorherrschende Mikroorganismen in Trinkwasserbiofilmen sind natürliche Wasserbakterien und Protozoen (z. B. Amöben), ohne gesundheitliche Bedeutung für den Menschen. Biofilm Centre Spezifische Bedingungen der Biofilmbildung in der Trinkwasser-Installation Unterschiede der Trinkwasser-Installation im Vergleich zum Trinkwasserverteilungsnetz: Kleinere Rohr/Schlauchinnendurchmesser größeres Oberfläche-Volumen-Verhältnis, Überwiegend Stagnation in den Trinkwasserleitungen, Erwärmung des Kaltwassers oder Abkühlung des Warmwassers bei längerer Stagnation, Vielfalt an Werkstoffen (Kupfer, Kunststoffe wie vernetztes Polyethylen (PE-X), PP, PVC, Edelstahl, verzinkter Stahl, elastomere Werkstoffe wie EPDM), die ggf. durch Nährstoffabgabe die Biofilmbildung fördern können. Biofilm Centre Fakultativ-pathogene Bakterien in Trinkwasserbiofilmen In Trinkwasser-Installationen kann es zur Einnistung, Persistenz und Vermehrung von fakultativ Pathogenen in Biofilmen kommen. Fakultativ pathogene Bakterien (z. B. P. aeruginosa) Trinkwasser Einnistung Persistenz Vermehrung Freisetzung Bild: M. Moritz, Biofilm Centre, UDE Biofilme stellen ein Reservoir für fakultativ pathogene Bakterien und eine Kontaminationsquelle für das Trinkwasser dar. P. aeruginosa kann alle mit Wasser in Kontakt stehenden Komponenten von Wassersystemen besiedeln (Primärbesiedler, Einnistung in bestehende Biofilme) und sich dort ggf. vermehren. Biofilm Centre P. aeruginosa – ein typischer Biofilmorganismus Pseudomonas aeruginosa auf Glasoberfläche (Flemmming und Wingender, 2010) Überleben von P. aeruginosa im Biofilm an der Innenoberfläche eines PVC-Rohrs nach 7-tägiger Exposition in Wasser mit 10-15 mg/L freiem Chlor (Vess et al., 1993) Pseudomonas aeruginosa im Silicon-Schlauch (Singh et al., 2000) Biofilm Centre P. aeruginosa – Einnistung in Trinkwasserbiofilme Einnistung von P. aeruginosa in 14 Tage alte Trinkwasserbiofilme (Anzucht in Kaltwasser aus einer Trinkwasser-Installation aus Kupfer) kulturell (CN-Agar, KBE) kultivierungsunabhängig (FISH, vitale Zellen) Laborkleinreaktor Werkstoffe Tage nach Animpfen P. aeruginosa nistet sich in Trinkwasserbiofilme ein. Die Anzahl kultivierbarer P. aeruginosa ist deutlich geringer als die Konzentration der FISH-positiven P. aeruginosa. Hinweis auf P. aeruginosa in einem nicht kultivierbaren („VBNC“) Zustand. Biofilm Centre Nachweis von pathogenen Bakterien: Kultivierungsmethoden Kultivierungsmethoden basieren auf der Fähigkeit lebender Bakterien auf Agar-Nährmedien Kolonien zu bilden oder sich in Flüssigmedien zu vermehren. zentrale Bedeutung in der Wasserpraxis - Überwachung der mikrobiologisch-hygienischen Qualität von Trinkwasser, - Überprüfung der Wirksamkeit von Desinfektionsmaßnahmen, - Basis von Risikobewertungen. P. aeruginosa-Kolonien auf einem Membranfilter auf CN-Agar nach Bebrütung für 2 Tage bei 36 °C. Genormte Methode: DIN EN ISO 16266, Nachweis und Zählung von Pseudomonas aeruginosa – Membranfiltrationsverfahren Schneider, 2009 Biofilm Centre Die Dunkelziffer – der VBNC-Zustand Lebend, aber nicht-kultivierbar („viable but nonculturable“, VBNC-Zustand): Kultivierbar Nicht kultivierbar, aber noch lebensfähig! Biofilm Centre Zustand von Bakterien, die sich normalerweise auf konventionellen Nährmedien unter üblichen Bebrütungsbedingungen kultivieren lassen, sich aber nun im Erhaltungsstoffwechsel befinden und nicht mehr vermehren. Sie bilden keine Kolonien auf AgarNährmedien, obwohl ihre Lebensfähigkeit (Vitalität) potenziell erhalten bleibt. VBNC-Bakterien lassen sich mit kultivierungsunabhängigen (häufig biochemischen oder molekularbiologischen) Verfahren nachweisen. Der “viable but non-culturable" (VBNC)-Zustand Auf üblichen Nährmedien kultivierbar VBNC-Zustand auslösende Faktoren (Stress): Wiederbelebung aus dem VBNC-Zustand: Nährstoffmangel Ungünstige Umgebungstemperaturen Hitze, Desinfektionsmittel, toxische Metallionen (z. B. Kupfer) Günstige Nährstoffbedingungen Günstige Umgebungstemperaturen Eliminierung/Neutralisierung von Stressfaktoren Auf üblichen Nährmedien nicht mehr kultivierbar, aber noch lebend und nicht mehr infektiös. Revitalisierung („resuscitation“) und Wiedererlangung der Infektiosität der Bakterien ist möglich. Biofilm Centre Bakterien, für die der VBNC-Zustand beschrieben wurde Aeromonas hydrophila Aeromonas salmonicida Agrobacterium tumefaciens Alcaligenes eutrophus Aquaspirillum sp. Burkholderia cepacia Burkholderia pseudomallei Campylobacter coli Camplyobacter jejuni Klebsiella planticola Lactobacillus plantarum Lactococcus lactis Legionella pneumophila Listeria monocytogenes Micrococcus flavus Micrococcus luteus Micrococcus varians Mycobacterium tuberculosis Pasteurella piscida Serratia marcescens Shigella dysenteriae Shigella flexneri Shigella sonnei Sinorhizobium meliloti Campylobacter lari Cytophaga allerginae Enterobacter aerogenes Enterobacter cloacae Enterococcus faecalis Enterococcus hirae Enterococcus faecium Escherichia coli incl. EHEC Francisella tularensis Helicobacter pylori Klebsiella aerogenes Klebsiella pneumoniae Mycobacterium smegmatis Pseudomonas aeruginosa Pseudomonas fluorescens Pseudomonas putida Pseudomonas syringae Ralstonia solanacearum Rhizobium leguminosarum Rhizobium meliloti Rhodococcus rhodochrous Salmonella Enteritidis Salmonella Typhi Salmonella Typhimurium Vibrio campbellii Vibrio cholerae Vibrio fischeri Vibrio harveyi Vibrio mimicus Vibrio natriegens Vibrio parahaemolyticus Vibrio proteolytica Vibrio shiloi Vibrio vulnificus Xanthomonas campestris Tenacibaculum sp. Vibrio anguillarum (Nach Oliver, 2010) Rot: Wasserhygienisch relevante Bakterien, überwiegend gram-negative Bakterien Biofilm Centre Kultivierungsunabhängige Methoden zum Nachweis von VBNC-Bakterien (zwei Beispiele) Vitalitätsmarker Membranintegrität Proteinbiosynthese (Ribosomen, 16S rRNA) Live/Dead-Färbung Grüne Zellen: lebend Rote Zellen: membrangeschädigt/tot Biofilm Centre Methode (mikrokopisch, molekularbiologisch, biochemisch) Live/Dead-System (mikroskopisch, Durchflusszytometrie), PMA-qPCR Fluoreszenz-in-situ-Hybridisierung (FISH) mit fluoreszenzmarkierten Gensonden FISH P. aeruginosa Bild: J. Heise, 2013 Kupferionen im Trinkwasser und P. aeruginosa Beobachtung: P. aeruginosa wird unkultivierbar in kupferhaltigem Trinkwasser aus der Trinkwasser-Installation. Trinkwasser mit Kupferionen Nennungen verbauter Rohrmaterialien in der Hausinstallation Blei 1% n=1.137 sonstiges 4% verzinkter Stahl 3% Kupfer 52% Edelstahl 3% Eisen 3% Stahl 7% Herkunft von Kupfer im Trinkwasser primär aus der Kupferinstallationen. Mittlerer Kupfergehalt des Trinkwassers in Deutschland (1990/92): 0,182 mg/L, Maximalwert: 4,8 mg/L. (Angaben: Dieter, 2003) Kunststoff 13% Biofilm Centre verzinktes Eisen 14% Erhebungen in öffentlichen Gebäuden in Deutschland (Kistemann et al., 2010) P. aeruginosa in kupferhaltigem Trinkwasser P. aeruginosa (Zellen oder KBE/mL) 1,0E+07 Gesamtzellzahl Koloniezahl 1,0E+06 1,0E+05 1,0E+04 1,0E+03 1,0E+02 1,0E+01 1,0E+00 Leitungswasser Leitungswasser + DDTC Gebäude mit Kupfer-Installation 0.066 mg/L (1.04 µM) Cu Trinkwasser Trinkwasser + DDTC Trinkwasserverteilungssystem ≤ 0.002 mg/L Cu Kupferhaltiges Trinkwasser verminderte die Kultivierbarkeit von P. aeruginosa (106 Zellen/mL, Exposition: 20 °C, 24 h), während die Gesamtzellzahl konstant blieb. Der Kupfer-Chelator DDTC (Natriumdiethyldithiocarbamat) verhinderte den Verlust der Kultivierbarkeit. Biofilm Centre Kupferionen und Vitalität von P. aeruginosa Gesamtzellzahl Zellen mit intakter Membran FISH-positive Zellen Koloniezahlen Vitalitätsmarker 1,0E+06 1,0E+05 1,0E+04 1,0E+03 Nicht kultivierbar 1,0E+02 1,0E+01 n.n. P. aeruginosa (Zellen oder KBE/mL) 1,0E+07 1,0E+00 Deionat ohne Kupfer Deionat mit Kupfer (10 µM) (106 Zellen/mL, Exposition: 20 °C, 24 h) n.n. – nicht nachgewiesen Kupferionen verursachen Verlust der Kultivierbarkeit, aber nicht der Vitalität Induktion des VBNC-Zustands in planktonischen P. aeruginosa. Biofilm Centre Rückkehr in die kultivierbare Form P. P. aeruginosa aeruginosa (cfu/ml) (KBE/ml) Kupfergestresste P. aeruginosa (VBNC-Bakterien) können ihre Kultivierbarkeit wieder erlangen, wenn der Kupfereffekt aufgehoben wird (Revitalisierung). 1,0E+07 Kontrolle Revitalisierung Gesamtzellzahl 1,0E+06 1,0E+05 1,0E+04 VBNC-Zustand 1,0E+03 1,0E+02 n.d. 1,0E+01 1,0E+00 untreated bacteria 0h copper-stressed bacteria copper-stressed bacteria + DDTC (resuscitation) 24 h 4d 7d 14 d Vorbehandlung: 24 h Inkubation mit 10 µM Cu, 20 °C Kupfer-Chelator DDTC hebt Inaktivierung auf Völlige Wiederherstellung der Kultivierbarkeit nach 14 Tagen Gesamtzellzahl bleibt gleich – nur der Anteil kultivierbarer Zellen ändert sich! Biofilm Centre VBNC-Zustand von P. aeruginosa und Zytotoxizität Bestimmung der Zytotoxizität von P. aeruginosa gegenüber humanen bronchialen Epithelzellen (BEAS-2B). Vitalität: Membranschädigung (Trypanblau-Assay) Richard et al. 2013 P. aeruginosa wirkt zytotoxisch gegenüber BEAS-Zellen. P. aeruginosa im VBNC-Zustand (kupfergestresst) wirkt nicht zytotoxisch. Kupfer-Chelator DDTC hebt VBNC-Zustand auf und Bakterien sind erneut zytotoxisch. VBNC-Zellen sind potenziell cytotoxisch. Biofilm Centre Kupferinduzierter VBNC-Zustand von gram-negativen Bakterien Der kupferinduzierte VBNC-Zustand ist nicht auf P. aeruginosa beschränkt. Spezies Referenz Agrobacterium tumefaciens Alexander et al., 1999 Erwinia amylovora Ordax et al., 2006 Escherichia coli Grey and Steck, 2001 Escherichia coli EHEC/EAEC O104:H4 Aurass et al., 2011 Pseudomonas aeruginosa Dwidjosiswojo et al., 2011 Ralstonia solanacearum Grey and Steck, 2001 Rhizobium leguminosarum Alexander et al., 1999 Xanthomonas campestris Ghezzi and Steck, 1999 Xanthomonas axonopodis pv. citri Del Campo et al., 2009 Biofilm Centre Zusammenfassung Biofilme können als Reservoir für fakultativ pathogene gramnegative Bakterien wie P. aeruginosa dienen und das Trinkwasser kontaminieren potenzielle Kontaminations- bzw. Infektionsquelle. Fakultativ Pathogene wie P. aeruginosa können im Wasser und in Biofilmen im VBNC-Zustand vorliegen, in dem sie dem kulturellen Nachweis entgehen, obwohl die Bakterien in lebensfähiger und potenziell infektiöser Form vorhanden sind. Kupferionen in Konzentrationen, die für die Trinkwasser-Installation relevant sind, können den VBNC-Zustand von P. aeruginosa im Wasser und in Biofilmen induzieren. Die Wiedererlangung der Kultivierbarkeit ist möglich durch die Aufhebung des Kupferstresses. Kupfergestresste (VBNC) P. aeruginosa verlieren ihre Zytotoxizität gegenüber Säugerzellen (humane Lungenzellen), wiederbelebte Bakterien sind erneut zytotoxisch. Biofilm Centre Konsequenzen: Biofilme und der VBNCZustand Konsequenzen in der Praxis für die Trinkwasser-Installation: - Bei Problemfällen (Ursachenaufklärung, Sanierungsmaßnahmen): zusätzlich zu Wasserproben auch Biofilme in Untersuchungen mit berücksichtigen, und zusätzlich zu Kultivierungsmethoden auch kultivierungsunabhängige, molekularbiologische Methoden einsetzen. - VBNC-Zustand in Risikobetrachtung einbeziehen. Berücksichtigung der allgemein anerkannten Regeln der Technik! Minimierung von Problemen durch Biofilme zu erwarten. Biofilm Centre VBNC-Zustand: offene Fragen Wann sind Bakterien wirklich tot? Welche physikalischen, chemischen und biologischen Faktoren induzieren den VBNC-Zustand? Welche Bedingungen führen zur Revitalisierung? Welche trinkwasserrelevanten Faktoren sind an diesen Prozessen beteiligt? Wie korreliert der VBNC-Zustand mit der Infektiosität bzw. Virulenz von Krankheitserregern. Was ist die hygienisch-medizinische Bedeutung des VBNC-Zustands? Was sind die Konsequenzen für die Praxis im Trinkwasserbereich? Biofilm Centre Danksagung Biofilm Centre Prof. Dr. Hans-Curt Flemming Dr. Miriam Moritz Zenyta Dwidjosiswojo Universitätsklinikum Essen und IWW Zentrum Wasser, Mülheim an der Ruhr Prof. Dr. Elke Dopp Dr. Jessica Richard Erkenntnisse aus zwei BMBF-geförderten Verbundprojekten 5 Forschungsinstitute: - Institut für Hygiene und öffentliche Gesundheit der Universität Bonn, - Biofilm Centre der Universität Duisburg-Essen, - IWW Zentrum Wasser in Mülheim an der Ruhr, - Umweltmikrobiologie der Technischen Universität Berlin - DVGW-Forschungsstelle an der Technischen Universität Hamburg-Harburg, und 25 Industriepartner. Biofilm Centre