Wissenschaftler des UKE und des DKFZ identifizieren
Werbung

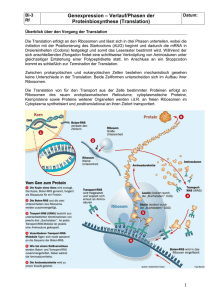
Wissenschaftler des UKE und des DKFZ identifizieren neues Kontrollsystem bei Gewebewachstum Publikation im angesehenen Wissenschaftsjournal „Nature“ Wie ein Buch, eine Zeitung oder eine Website aus einer anderen Sprache, so müssen auch die Informationen der meisten unserer ca. 20.000 Gene von der „Sprache“ der DNA in die „Sprache“ der Proteine übersetzt werden, damit die genetischen Informationen im Körper ihre Wirkung entfalten können. Dieser Prozess heißt Translation. Fehler in jedem Zwischenschritt dieser „Übersetzung“ können zu Krankheiten wie Krebs oder Demenz führen. In einer Arbeit, die am 14. August in „Nature“ veröffentlicht wird, zeigen Wissenschaftler des UKE und des DKFZ, dass es einen bis dato unbekannten Kontrollmechanismus für die Übertragung von Informationen aus DNA in gibt. Dr. Kent Duncan (UKE), Dr. Aurelio Teleman (DKFZ) und ihre Mitarbeiter konnten darüber hinaus nachweisen, dass dieses Kontrollsystem in Tieren große Auswirkungen auf die Zellteilung und das Gewebewachstum hat. Die Arbeit eröffnet ganz neue Wege sowohl für das Verständnis der molekularen Regulierung von Zellwachstum und –vermehrung durch translationale Kontrolle als auch zur späteren Entwicklung von Medikamenten gegen Krebs und andere Krankheiten, die eben maßgeblich durch die fehlgeleitete Regulierung von Zellvermehrung entstehen. Hintergrundinformationen: In allen Zellen sind molekulare Maschinen, Ribosomen genannt, aktiv, um die Translation von Genen in Proteine sicherzustellen. Ribosomen „übersetzen“ die Gene nicht direkt, sondern über den Umweg von Kopien der Gene, die sogenannte Messenger (m)RNA. Diese (m)RNA Kopien enthalten normalerweise einen mittleren Teil mit dem zu übersetzenden Abschnitt („Open Reading Frame“ ORF) und an beiden Enden Abschnitte, die nicht in Proteine übersetzt werden. Tierische Ribosomen beginnen also den „Leseprozess“ am vordersten Ende der mRNA und arbeiten sich bis zu dem Teil vor, in dem genetische Informationen in Proteine übersetzt werden sollen. Vergleichen ließe sich das mit einem Flugzeug, das die Landebahn entlang rollt bis es endlich abhebt. Das Problem ist, dass mindestens die Hälfte unserer Gene mRNA produziert, die sogenannte „upstream ORF“ (kurz: uORF) enthält. Um im Flugzeugbeispiel zu bleiben, befinden sich also Signale zum Abheben und Landen mitten auf der Landebahn. Wie kommen die Ribosomen dann also überhaupt bis zu dem Punkt, an dem sie tatsächlich die Herstellung der richtigen Proteine beginnen? Ein neues Kontrollsystem der Translation von mRNA mit „uORF“ Das Team aus UKE und DKFZ hat, wenn man so will, ein molekulares Äquivalent zu einem neuen Fluglotsen entdeckt: Einen Proteinkomplex, der bestimmt, ob das Ribosom trotz der „überflüssigen“ Start‐ und Landesignale auf der Landebahn an den Punkt kommt, an dem dann das gewünschte und notwendige Protein tatsächlich hergestellt wird. Dabei konnten die Wissenschaftler zeigen, dass der Proteinkomplex tatsächlich nur Auswirkungen auf mRNA mit uORF hat, nicht aber auf mRNA, die frei von solchen „Störsignalen“ ist. Diese Erkenntnis ist aus zwei Gründen wichtig: Erstens haben die Zellen ein bisher unbekanntes Kontrollsystem für Translation, welches so reguliert werden kann, dass nur bestimmte Mengen bestimmter Proteine produziert werden. Und zweitens scheint dieses System sehr viel wichtiger für Zellen zu sein, die sich noch teilen und vermehren, was es potenziell zu einem interessanten Ziel für Krebstherapien macht. Denn tatsächlich hat die Arbeit anderer Wissenschaftler schon gezeigt, dass ein Teil des Kontrollsystems genetisch bedingten Krebs fördern kann, also eine onkogene Wirkung hat. Darüber hinaus lassen sich aus der vorgestellten Arbeit aber auch allgemeinere Schlussfolgerungen ziehen. „uORF sind ein bisher vernachlässigter Aspekt von biologischer Regulierung und bei der Entstehung von Krankheiten.“, sagt Dr. Kent Duncan, Studienleiter und Forschergruppenleiter am Zentrum für Molekulare Neurobiologie (ZMNH) am UKE. „Die Hälfte unserer Gene enthält mindestens ein uORF und viele sogar mehr als zehn. Wir wissen seit einiger Zeit, dass uORF einen großen Einfluss auf die Translation haben, aber viele Wissenschaftler scheinen noch nie von ihnen gehört zu haben. Wir hoffen, dass wir das mit unserer Arbeit ändern können.“ Dr. Duncan arbeitet im Rahmen der Landesforschungsförderung auch mit Arbeitsgruppen am UKE zusammen, die an der Funktion von uORF im Zusammenhang mit dem Nervensystem interessiert sind. Diese Zusammenarbeit sollte neue interessante Hinweise für Störungen der Gehirnfunktion, vor allem neurodegenerative Erkrankungen und angeborene geistige Behinderungen, liefern. „Unsere Arbeit sollte Humangenetiker daran erinnern, sich auch die „Landebahnen“ der Ribosomen vorzunehmen, wenn sie bei Patienten nach Mutationen suchen. Ich denke, was wir bisher gefunden haben, ist nur die Spitze eines Eisbergs.“, ergänzt Duncan. Einige der beteiligten Wissenschaftlerinnen und Wissenschaftler am UKE werden teilweise von der Hans und Ilse Breuer Stiftung sowie einem Stipendium der Fritz Thyssen Stiftung finanziert. Literature: Schleich, S., Strassburger, K., Janiesch, P.C., Koledachkina, T., Miller, K.K., Haneke, K., Cheng, Y., Kuechler, K., Stoecklin, G., Duncan, K.E., Teleman, AA (2014). DENR‐MCT‐1 promotes translation reinitiation downstream of uORFs to control tissue growth. Nature, July 6, 2014. http://www.nature.com/nature/journal/vaop/ncurrent/full/nature13401.html Contact: Dr. Kent Duncan Neuronal Translational Control Research Group Center for Molecular Neurobiology (ZMNH) University Medical Center Hamburg‐Eppendorf Falkenried 94, 20251 Hamburg Phone: +49‐40‐7410‐56274 E‐mail: [email protected]‐hamburg.de