Einführung in die Physik I Wärme 1
Werbung

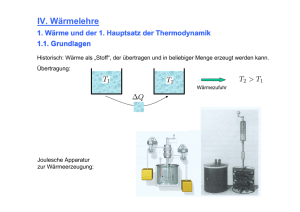
Einführung in die Physik I Wärme 1 - Grundlagen O. von der Lühe und U. Landgraf Wärme und Temperatur • Wärme ist eine Form von Energie, die ausgedehnten Körpern zu eigen ist • Wärmeenergie besteht aus der kinetischen Energie der ungeordneten Bewegung von Bestandteilen ausgedehnter Körper • Kinetische Energie wird über Stöße und Fernwirkung zwischen den Teilchen ausgetauscht • Die Temperatur ist ein lineares Maß der mittleren kinetischen Energie der Teilchen Wärme 1 Ideales Gas: Teilchen bewegen sich unabhängig, Wechselwirkung nur bei Stößen von Teilchen Gleichverteilungssatz: im Mittel ist die kinetische Energie für jedes Teilchen dieselbe 2 1 Definition der Temperatur • Allgemein: – Bei einer Temperatur T beträgt die mittlere kinetische Energie pro Freiheitsgrad eines Teilchens • Einatomiges Gas: – Mittlere kinetische Energie jedes Teilchens (3 FG) • Zweiatomiges Gas (z. B. Luft): – Mittlere kinetische Energie und Rotationsenergie (5 FG) • Mehratomige Gase und Festkörper: • Einheit der Temperatur: Kelvin [K] • Boltzmann-Konstante k EFG = 1 ⋅ k ⋅T 2 Ekin = 1 3 ⋅ m ⋅ v2 = ⋅ k ⋅T 2 2 Etrans + rot = Ekin = ( ) 1 5 ⋅ m ⋅ v2 + J ⋅ω 2 = ⋅ k ⋅T 2 2 1 6 ⋅ m ⋅ v 2 + Epot = ⋅ k ⋅ T 2 2 [ k = 1.381⋅10 −23 J K -1 ] Wärme 1 3 Temperaturskala • Es gibt eine absoluten Nullpunkt der Temperaturskala, welcher der mittleren Energie von Null entspricht • Kein Körper kann eine Temperatur kleiner als 0 [K] haben! • Eine praktische Temperaturskala ist die Celsius-Skala mit den Fixpunkten 0 °C und 100 °C (Gefrier- und Siedepunkt des Wassers bei einem Druck von 1.013 [bar]) • Ein Temperaturunterschied von 1 [K] entspricht 1 °C • Eine andere in den USA gebräuchliche Temperaturskala ist Fahrenheit (°F) Wärme 1 1[K ] ≡ 1°C 0 [K ] = − 273,2 °C 0 °C = 32 °F 100 °C = 212 °F 4 2 Wärmeenergie - Beispiel • Luft hat eine Wärmekapazität von 710 [J kg-1 K-1] • Bei temperaturunabhängiger Wärmekapazität ergibt sich bei einer Temperatur von 300 [K] (= 27 °C) ein Wärmeenergieinhalt von 710 · 300 = 213.000 [J] pro Kilogramm Luft • Luftmoleküle sind i. d. R. zweiatomig. Es entfallen drei Freiheitsgrade für die Translation und zwei Freiheitsgrade für dir Rotation • Pro Kilogramm erhält man damit 3/5 · 213 [kJ] = 128 [kJ] kinetische Energie 1 2 Ekin Ekin = mv 2 → v = m 2 • v = (256.000)½ = 505 [m s-1] Wärme 1 5 Thermometer • Messbare Größen, die reproduzierbar von der Temperatur abhängen, können für Thermometer verwendet werden – Thermische Ausdehnung von Flüssigkeiten und Festkörpern – Temperaturabhängigkeit des elektrischen Widerstands – Direkte Messung der mittleren Geschwindigkeit der Teilchen (optischer Dopplereffekt) – Strahlungsleistung • Eichung durch Fixpunkte Wärme 1 l = l0 (1 + α ⋅ T ) V = V0 (1 + γ ⋅ T ) γ = 3α Lin. Ausdehnungskoeffizient α / 10-6 [K-1] bei 100 °C Quarzglas Jenaer Glas Eisen Kupfer Aluminium Blei NaCl 0.510 8.1 12.0 16.7 23.8 29.4 40.0 Raumausdehnungskoeffizient γ / [K-1] bei 18 °C Aceton Benzol Quecksilber 0.00143 0.00106 0.00018 6 3 Wärmekapazität • Erwärmt man einen Körper, so muss man ihm Energie zuführen. Die Wärmekapazität ist die Menge von Energie, die eine Stoffmenge zur Erhöhung der Temperatur um 1 [K] benötigt • Die Energiezunahme pro Teilchen ist bei f Freiheitsgraden bei einer Temperaturänderung von ΔT f k ⋅ ΔT 2 ΔETeilchen = ΔEmol = N A ⋅ • Die Energiezunahme pro mol ist • Die Energiezunahme pro kg ist ΔE = – rel. Atomgewicht μ – Masse des Wasserstoffatoms mH f k ⋅ ΔT 2 f k ⋅ ΔT 2 ⋅ μ ⋅ mH Wärme 1 7 Wärmekapazität [ • Molare Wärmekapazität C C= f ΔEmol = N A ⋅ ⋅ k J mol-1 K -1 2 ΔT • Spezifische Wärmekapazität c= ΔE f ⋅k = ΔT 2 ⋅ μ ⋅ mH • Festkörper: f = 6 (Dulong–Petit‘sche Regel) C = 3 N A k = 24.9 J mol-1 K -1 [ [J kg -1 K -1 ] ] ] Wärmekapazität von Wasser: cH2O = 4185 [J kg-1 K-1] Für eine Temperaturerhöhung von 1g Wasser um 1 °C braucht man eine Energie von 4.185 [J] = 1 [cal] Kalorie Wärme 1 8 4