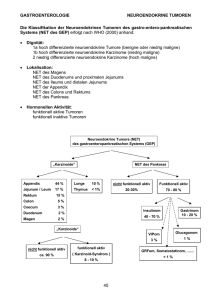
GEP-NET-Tumore
Werbung

SOP KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Gebiet: Gastroenterologie GEP-NET-Tumore Ausrichtung: diagnostisch therapeutisch Version: Gültig ab: Revision: Verfasser: Geprüft: Genehmigt: 2.0 (5 Seiten) 01.02.2009 01.02.2011 GP/EE EE, CBO JS (1.0) Grundsätzliches: GEP-NET-Tumore: GEP-NET-Tumore sind neuroendokrine Tumore des gastroenteropankreatischen Systems und haben ihr nicht-neoplastisches Äquivalent in Zellen des diffusen neuroendokrinen Systems. Normale und neoplastische neuroendokrine Zellen können – ähnlich wie Neuronen – sekretorische Granula und helle kleine Vesikel enthalten und die hierfür charakteristischen Marker (z.B. Chromogranin A) exprimieren. 1) Einteilung nach Primärlokalisation • Foregut: Ösophagus, Magen, Duodenum, Pankreas, Lunge (5-JÜR 58 %) • Midgut: Jejunum, Ileum, Appendix, rechtsseitiges Kolon (5-JÜR 61 %) • Hindgut: Colon transversum, linksseitiges Kolon, Sigma, Rektum (5-JÜR 79%) (Anmerkung: Unterteilung Midgut und Hindgut wurde für das Kolon verlassen, stattdessen Unterscheidung nach Kolon- und Rektum-NET) 2) Einteilung nach Funktionalität/Hormonaktivität 3) Einteilung n. Größe, Angioinvasion, Metastasierung, Grading (WHO-Klassifikation) Neuroendokrine Tumore (NET) Tumorklassifikation - Prognosekriterien WHO-Klassifikation • hoch differenzierte neuroendokrine Tumore (benigne oder niedrig maligne) • hoch differenzierte neuroendokrine Karzinome (niedrig maligne) • niedrig differenzierte neuroendokrine Karzinome (hoch maligne) Biologisches Verhalten Metastasen M. propriaInfiltrationa Histologische Differenzierung Tumorgröße Angoinvasion Ki-67Index Hormonelles Syndrom Benigne - - Hoch <1cm³ - <2% - Benigne oder niedrig maligne - - Hoch <2cm -/+ <% - Niedrig maligne + + Hoch <2cm + <2% + Hoch maligne + + Niedrig Beliebig + >20 a b Ausnahme: maligne duodenale Gastrinome sind meist kleiner als 1cm und noch auf die Submukosa beschränkt Ausnahme: benigner NET der Appendix infiltrieren meist die Lamina muscularis propria b a - 4) Einteilung nach dem Erbgang • Sporadisch versus MEN I (autosomal dominant erblicher Gendefekt auf Chromosom 11, Tumorsuppressorgen, Proteinprodukt: Menin) • MEN I bei 14% der NET im Pankreas, Gastrinom 20%, Insulinom 4% 5) TNM-Klassifikation Histologische Graduierung der NET Mitosezahl (10 HPF) <2 2-20 >20 Grad Grad 1 Grad 2 Grad 3 Ki-67 (%) <2 3-20 >20 TNM-Klassifikation für Magen, Duodenum, Pankreas, Appendix, K l Stadium Stadium Stadium Stadium Stadium Stadium Stadium 0 I IIa IIb IIIa IIIb IV Tis T1 T2 T3 T4 jedes T jedes T N0 N0 N0 N0 N0 N1 jedes N M0 M0 M0 M0 M0 M0 M1 (Bei Tumoren des Kolon und Rektum wird für T1a und T1b Tumoren zwischen einem Stadium Ia und 1b unterschieden) Inzidenz neuroendokriner gastrointestinaler Tumore: 2,5 bis 5 pro 100.000 pro Jahr Anamnese / Klinik • • • • • • • • • Gastrointestinale Symptome wie Übelkeit/Erbrechen, Schmerzen (intermittierend, kolikartig, „Ulkusschmerz“), Blutungen [→ Karzinoid, → Glucagonom, → VIPom] Flush-Symptomatik [→ Karzinoid]? asthmatische Beschwerden [→ Karzinoid]? Gewichtsverlauf (Gewichtszunahme [→ Insulinom])? Neurologische (Bewusstseinsverlust!) oder psychiatrische Symptome [→ Glucagonom, → Insulinom]? (Nüchtern-)Hypoglykämien [→ Insulinom]? Hautveränderungen (Pellagra [→ Karzinoid], nekrolytisches migratorisches Erythem [→ Glucagonom])? Auftreten von Thrombembolien [→ Glucagonom] ? Auftreten von Diabetes mellitus [→ Glucagonom] ? Technische Untersuchungen Diagnostik, allgemein Chromogranin A (CgA) im Serum, eventuell auch NSE (CgA korreliert mit Tumormasse und gilt daher als progn. Marker, falsch positive Ergebnisse u. a. bei atroph. Gastritis und Therapie mit PPI) Bei endokriner Aktivität (nach klinischer Symptomatik): • [Karzinoid] [a] 24h-SU auf 5-HIES [b] Serotonin im Serum (bei Foregut sowie bei Middle- bzw. Hindgut-Karzinoiden mit kleinem Tumorvolumen bisweilen 5-HIES-Bestimmung überlegen. • [Insulinom:] [a] BZ-Tagesprofil oder [b] insulinogener Index (Nü-Seruminsulin [IE/ml] / Nü-BZ [mg/dl] > 0,5 verdächtig!). Ggf. [c] 72-Stunden-Hungerversuch (→ eigenständiges SOP) • [Gastrinom / Zollinger-Ellison-Syndrom] [a] ÖGD mit Histologiegewinnung [b und c] Nach mindestens siebentägiger Pausierung von Protonenpumpenhemmern oder H2-Blockern [b] Basaler Gastrinspiegel (> 1000 pg/ml beweisend), [c] Sekretintest (Anmeldung über GastroLabor Tel. 7041) bei Gastrinspiegel zwischen 200 bis 1000 pg/ml (paradoxer Anstieg um ∆ > 200 pg/ml: pathologisch) [d] Magensäuresekretionsanalyse wird bei uns nicht mehr durchgeführt. • [Glucagonom] Glucagon • [VIPom / Verner-Morrison-Syndrom] [a] Kalium und Chlorid (verdächtig Hypokaliämie und Hypochlorhydrie, deshalb wird VIPom auch noch WDHA-Syndrom [Watery Diarrhea, Hypokaliemia, Achlorhydria] genannt) [b] ViP. Mit oder ohne endokrine Aktivität: • Abdomensonographie • Ggf. Endosonographie mit Histologiegewinnung • Somatostatin-Rezeptor-Szintigraphie (Octreotidscan) Diagnostik, Spezielles: • Spiral-CT oder MRT • Probe-Laparotomie • Selektive Angiographie • MIBG (123-Jod-Metajodbenzylguanidin) Szintigraphie (geringere Sensitivität als Octreotidscan!) • 68 Gallium DOTATOC-PET (höhere Auflösung als Octreotidscan, anatom. Zuordnung möglich) Konsequenzen Therapie lokalisierter Prozesse In Abhängigkeit von Größe und Lokalisation und Funktionalität endoskopische Abtragung oder chirurgische Exzision • • • • Magen bei ECL-Zell-Hyperplasie -Tumor bis 1cm: endoskop. Abtragung ->1cm: nach EUS-Befund endoskopische Abtragung oder transmurale Exzision ggf. mit Antrektomie -bei soliden Tumoren: Vollwandexzision Magen ohne ECL-Zell-Hyperplasie -Tumor bis 1cm: nicht-radikale chir. Therapie ->1cm: radikale chir. Therapie Duodenum -Tumor bis 1cm, nicht funktionell : endoskop. Abtragung/nichtradikale OP -Tumor bis 1cm, funktionell: Tumorresektion, Lymphadenektomie bzw. Resektion hepatischer Metastasen ->1cm oder mit Angioinvasion: Whipple-OP Restlicher Dünndarm -Resektion (Sicherheitsabstand bei Tumor >1cm: 10cm) plus Lymphadenektomie, Metastasenresektion • • • Appendix -Tumor bis 2cm und Lokalisation an der Appendixspitze: Appendektomie ggf. plus Ileozökalresektion -> 2cm oder Beteiligung von Mesoappendix oder Angioinvasion oder Neuroinvasion oder Lokalisation des Tumors an der Basis oder histolog. Klassifikation als verschleimender oder gemischt endokrin-exokriner Tumor: Hemikolektomie mit Lymphadenektomie Kolon und Rektum -Tumor bis 1cm: endoskop. Abtragung -1-2cm: transanale Vollwandexzision bei Rektum-NET ->2cm oder Angioinvasion bei fehlender Metastasierung: radikale bzw. ggf. palliative OP Pankreas (OP-Technik abhängig von Lokalisation und Subentität) -Enukleation bei im allgemeinen Tumor <2cm (Insulinom <3cm), ggf. gewebserhaltende Pankreaslinksresektion -Gastrinom: Pankreas(links)resektion und Lymphadenektomie -Multilokuläre Tumore: Whipple-OP Symptomatische Therapie bei funktionell aktivem NET • Karzinoid -Octreotid (bis 3x 500µg, bei guter Verträglichkeit LAR-Präparat (effektive Symptomkontrolle in 70-80 %) -Ggf. H1- und H2-Rezeptorblocker, z.B. Ranitidin -Behandlung der Diarrhoe: Pankreasfermente, Methysergid -ggf. Behandlung einer konkomitanten Herzinsuffizienz (ACE-Hemmer, Diuretika) -ggf. Behandlung eines konkomitanten Asthma bronchiale -Nicotinamid bei Hautveränderungen (z.B. Nicobion 3 x 200 mg) • • • Insulinom -Hypoglykämieprävention (z.B. GlucaGen® HypoKit) -Diazoxid 200 bis 600 mg / Tag (antihypertensiv wirkendes Benzothiadiazin mit hyperglykämischer Wirkung aber erheblichen Nebenwirkungen [Übelkeit Natriumretention, Arrhythmien, KM-Depression]) -(Octreotid) Gastrinom -hochdosiert PPI, z.B. 60-80mg Omeprazol / Tag -Gastrektomie bei Therapie-refraktären Ulcera Gucagonom/VIPom -Octreotid, bei guter Verträglichkeit LAR-Präparat Therapiemöglichkeiten der fortgeschrittenen Erkrankung • Vor Therapieeinleitung/ -entscheidung Beurteilung des Spontanverlaufes bei hoch differenzierten Karzinomen und Bewertung der Therapienotwendigkeit • Chirurgische Therapie -Tumordebulking -Umgehungsoperationen bei Obstruktionen • Antiproliferative Therapie -Somatostatinanaloga und / oder alpha-Interferon (midgut und hindgut) -Bei foregut-Tumoren oder Versagen der Octreotid-Therapie: Systemische Chemotherapie, z.B. (Foregut-Chemotherapie): Streptozotozin-basiert mit Doxorubicin u/o 5-FU, auch Capecitabin in Kombination mit Oxaliplatin, oder Temozolomid -Anaplast. Tumore: Cisplatin plus Etoposid • Metastasenbehandlung -Operation, falls möglich -Chemoembolisation, RITA oder Ethanolinjektion -Nur bei Karzinoiden: Therapie mit 131Iod-Metajodbenzylguanidin (MIBG,) oder In-situ-Radiojodtherapie: z.B. mit 90Yttrium-markiertem Octreotid (DOTATOC) -in Einzelfällen Lebertransplantation -- in Einzelfällen fokale od. auch segmentale Radioembolisation mit nuklidgebundenen Mikrosphären (Selective Internal Radiation Therapy = SIRT) Häufige Fehler Kein ausreichender Austausch mit anderen Disziplinen (Chirurgie, Nuklearmedizin, Dermatologie, Neurologie/ Psychiatrie) © Klinik und Poliklinik für Innere Medizin I der Universität Regensburg, 04.02.2009 Verfasser E-mail: [email protected] Hausfunk: 1515 Literatur AWMF Leitlinien: nicht vorhanden Internationale Leitlinien: http://www.up-to-date.com ENETS Guidelines, Neuroendocrinology 2008;87:1-62. Klöppel G et al, Best Pract Res Clin Gastroenterol 2005;19:507-517. Rindi et al, Virchows Arch 2006;449:395-401. Rindi et al, Virchows Arch 2007;451:757-762. Aktuelle Übersichtsartikel: Bornschein J, Kidd M, Malfertheiner P, Modlin M, Dtsch Med Wochenschr 2008;133:1505-1510. Modlin IM, Oberberg K, Chung DC et al, Lancet Oncol 2008;9:61-72. Empfehlungen ohne Gewähr, Verantwortung liegt bei behandelnder Ärztin/Arzt!