Diagn. u. Therapie der Schilddrüsenerkrankungen
Werbung
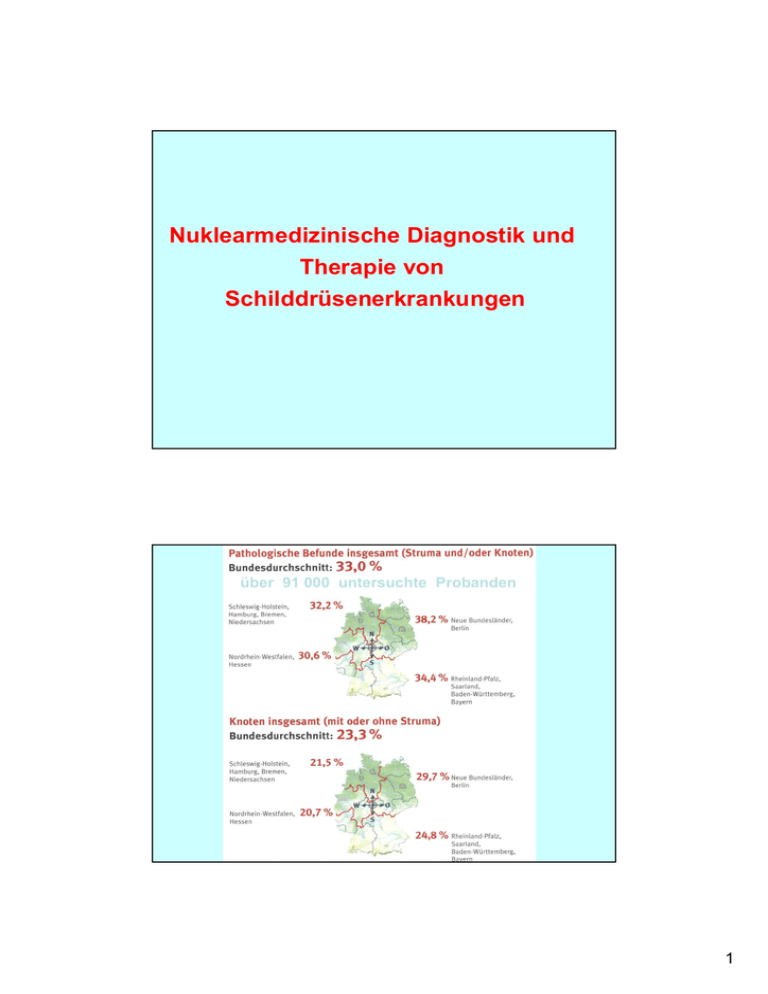
Nuklearmedizinische Diagnostik und Therapie von Schilddrüsenerkrankungen über 91 000 untersuchte Probanden 1 Diagnostik • Anamnese (Symptome, Medikamente) • (Status praesens) • Labor (TSH, FT3, FT4) • Sonographie (Schallmuster,Volumen, Knoten?) • Szintigraphie • FNP - Zytologie / Histologie • Weitere: Röntgen / PET-CT / MRT Diagnostisches Vorgehen bei Struma nodosa Palpation Struma diffusa - Struma nodosa obligat Schilddrüsenvolumen, Knotengröße echoarmer - echoreicher Knoten Sonographie wenn Knoten > 1 ml Szintigraphie warmer - kalter Knoten wenn Knoten kalt Feinnadelpunktion benigner maligner Knoten 2 Radionuklide zur Schilddrüsen-Diagnostik h Gammastrahlung Iodstoffwechsel in der Schilddrüse I I JI TRIIODTHYRONIN (T3) I I I I THYROXIN (T4) I = Iod 3 Szintigraphie der Schilddrüse Iod: natürliches nichtradioaktives Iod (127I) Radioiod: 131I, 123I 99mTc - Pertechnetat Aufnahme in Zelle durch modifizierte Ionenpumpe, weil identischer Ionenradius 4 Bestimmung des Iod - Uptake mittels Kamera (Gamma-Kamera und ROI-Auswertung) Messung der Gamma-Strahlung aus der Schilddrüse Auswahl der Impulse im Energiefenster des Iod-Peaks (364 keV ± 20%) und Zuordnung zu den Bildpunkten Berechnung der Gesamtimpulszahl in der Schilddrüse und in der ROI (Region of Interest) 5 Sondenmessung zur Uptake - Bestimmung (Radioiod -Test) Abstandshalter 1. Aktivität wird in Phantom in gleicher Position wie später der Patient vor der Sonde gemessen gemessene Impulse entspr. 100% 1. 3. Szintillationssonde mit Kollimator (Bleitrichter) 2. Patient schluckt diese Aktivität die 100% werden im Körper verteilt, ein Teil wandert in die SD. Wieviel ? Stativ 3. Patient kommt nach x Stunden zur Messung (mehrfach, versch. Zeiten) gemessene Impulse aus dem Bereich der SD entspr. Uptake nach x Stunden 2. RIU[%] = Impulse von SD ∗100% Impulse der appl. Aktivität im Phantom Stör- und Einflussgrößen beim 99mTc-Uptake(TcTU) Störgrößen TcTU ↑ „Rebound“ nach Absetzen von - Levothyroxin - Liothyronin - Thyreostatika TcTU ↓ Einnahme von - Levothyroxin - Liothyronin - Perchlorat - Iodkontamination Einflussgrößen TcTU ↑ Hyperthyreose Iodmangel Hypothyreose (primär) Lymphozytäre Thyreoiditis TcTU ↓ Subakute Thyreoiditis Chronisch-athrophische Thyreoiditis Hypothyreose (sekundär) Niereninsuffienz Nach Reiners Chr.: Nuklearmedizinische Diagnostik des hypofunktionellen Strumaknotens, Nuklearmediziner 1992b;15:19 6 Untersuchungs-Ablauf der Aktivität messen Messung 10 Minuten 99mTc-Pertechnetat-Szintigraphie Applikation Restaktivität messen Auswertung Prinzip der Suppressions - Szintigraphie ( wenn TSH > 0,1 mU /L) Nachweis einer funktionellen Autonomie (TSH >0,1 mE/L) 7 Quantitative Schilddrüsenszintigraphie Tc-99m Uptake (TcTU in %) (% der applizierten Aktivität in der Schilddrüse) Bifokale Autonomie Durchführung der Feinnadel-Punktion Beispiel: FNP eines Schilddrüsenknotens 8 Tc-99m Pertechnetat - Szintigramm Farbkodiertes Sonogramm mit Hyperperfusion des Knotens Unifokale Autonomie rechts Auswertung: Bestimmung des Uptake •Aufnahme der SD mit Gamma-Kamera mit festgelegter Messzeit •Festlegen einer ROI um die SD •Programm addiert alle Zählimpulse in der ROI zur Gesamtimpulszahl •Aus Aufnahmen bekannter Aktivitäten ist der Zusammenhang zwischen Aktivität und Impulsrate (Effizienz) in der ROI bekannt (z.B. 7 cps/MBq) •Uptake ergibt sich dann zu: RIU = Gesamtimpulszahl ∗100% Messzeit[s] ∗ Effizienz[cps/MBq] ∗ appl.Aktivität[MBq] 9 131I-Therapie bei funktioneller Autonomie Radioiodtherapie Es wird nur krankes (autonomes) Schilddrüsengewebe zerstört Bedingung: TSH < 0,1 mU/L Suppressionstest ( Ziel: TSH < 0,1 mE/l ) • L-Thyroxin 100 – 200 µg / die, 14 Tage • Liothyronin (Thybon) 50 – 100 µg / die, 10 Tage • L-Thyroxin 3 mg einmalig / Szintigraphie nach 7 Tagen TcTU (%) = Schilddrüsenimpulse – Untergrundimpulse Nettoimpulse der injizierten Aktivität 10 L-Thyroxin 100 µg/d Prämedikation, 14 Tage Vor Suppression unter L-Thyroxin Radioiodtherapie (1022 MBq 131Iod, 200 Gy) TcTU: 1,49 % TcTUs: 0,51 % TSH 0,8 mE/l TSH 0.02 mE/l (supprimiert, normal 0,27-4,2) fT3 6,2 pmol/l (normal bis 6,8) fT4 31.6 pmol/l (normal bis 24,5) Frau, 48 Jahre Unifokale Autonomie links M.Basedow Diffuse Anreicherung Frau, 43 Jahre TRAK 5.3 U/l (<1.5) TPO 12.5 U/ml (<60) Radioiodtherapie (105 MBq 131Iod / 150 Gy) TSH 0.008 mE/l fT3 7.9 pmol/l fT4 19.9 pmol/l 11 Wirkungsweise der Thyreostase ohne Thiamazol unter Thiamazol 15 mg/die TcTU : TcTU : 3.73 % 2.61 % 24 Std ITU: 24 Std ITU: 63 % 3.4 % Hormonsynthese intakt Iodidraffung intakt, aber Iodeinbau in Hormon geblockt Szintigraphisch Kalter Knoten rechts (Minderanreicherung im Knoten) 12 Durchführung der Schilddrüsenpunktion Schätzwerte zur Treffsicherheit der Malignitätsbeurteilung diagnostischer Verfahren bei Schilddrüsenläsionen Methode Merkmal Sensitivität Spezifität Palpation Knoten ca. 90% ca. 5% Szintigraphie Speicherdefekt ca. 95% ca. 10% Sonographie Echoarmut ca. 99% ca. 25% Zytologie suspekt / positiv ca. 80% ca. 90% Nach Reiners Chr., Becker W., Spiegel W., Börner W., Müller H.A. 13 Zytologische Klassifizierung Gruppe 0 Ungenügendes Material (nicht beurteilbarer Ausstrich, keine oder nur vereinzelte Schilddrüsenepithelien nachweisbar) Gruppe I/II Unverdächtige Befunde (unauffällige Thyreozyten, regressive Veränderungen, resorptive Vorgänge) Gruppe IIIa b Zellen zweifelhafter Dignität Tumorzellen zweifelhafter Dignität (follikuläre Neoplasie) Gruppe IV Tumorzellen OP des Schilddrüsenkarzinoms Thyreoidektomie / Thyreoidektomie mit LK-Dissektion Parathyreoidea N.recurrens (Ex- und Re-Implantation) (Neuromonitoring) Metastasektomie Rezidiv-OP (Re-Operation / Metastasektomie) Besonderheit: low-risk Tumore (< 1cm, histologisch papilläres SD-Ca) keine ergänzende totale Thyreoidektomie notwendig 14 Differenziertes Schilddrüsen-Karzinom links (pT2N0M / UICC2002) 10/05 Thyroidektomie rechts und subtotale Resektion links 01/06 Restthyroidektomie und Lymphknoten-Dissektion zentral TSH 85 mE/L Thyreoglobulin 2 ug/l Frau, 39 Jahre Radioiodtherapie 2 GBq 131I TSH 51 mE/L Thyreoglobulin 0,03 ug/l Radio-Nuklid-Therapie 131I- Szintigraphie Papilläres Schilddrüsen-Karzinom mit ossärer Metastasierung (pT4bN1bM1 / UICC 1987) Mann 59 Jahre Z.n. Thyreoidektomie und zervikaler Lymphknotendissektion Nach zweimaliger 131 I-Therapie (11 GBq) 15 Radio-Nuklid-Therapie 131I-Szintigraphie Papilläres SchilddrüsenKarzinom mit ossärer Metastasierung (pT4bN1bM1/ UICC 1987) Mann 59 Jahre Z.n. Thyreoidektomie und zervikaler Lymphknoten-Dissektion Nach erster 131I Therapie vor 3 Monaten Lymphknotenmetastase eines gering differenzierten Schilddrüsen-Ca Nachsorge: Ultraschall 131Iod [18F]FDG Sonographisch echoarmer Knoten Kein Tumormarkeranstieg (Thyreoglobulin) Keine Radioodaufnahme Deutliche [18F]FDG-Aufnahme (PET) Gering differenziertes papilläres Schilddrüsen-Ca Radioiodtherapie nicht möglich 16 FDG - PET Koronale Ansichten Präoperativ 17 Lokalisation in 3 Ebenen Nachsorge bei 131I-Therapie (II) Schilddrüsen-Karzinom Nachsorge SD-Hormonsubstitution (T3 besser T4) TSH <1,0 mU/l des differenzierten low-risk Tumoren (pT1 und pT2) sonst TSH suppressiv (<0,1 mU/l) 131I-Ganzkörper-Szintigraphie (3 Monate nach RIT) entweder SD-Hormonkarenz oder TSH-Stimulation durch rTSH (ThyrogenR) Sonographie des Halses Thyreoglobulin - Bestimmung - bei negativem TG (<0,4 µg/ml) und 131I-Szintigraphie negativ) 5 Jahre lang halbjährliche Kontrolle von TG und Sonographie Danach 1x jährlich lebenslang (aber Spätrezidive mgl.!) - Bei Restspeicherung weitere Szintigraphie-Kontrolle nach 1 Jahr (funktionsgemindertes Restgewebe ohne weitere 131I-Therapie noch bis zu 3 Jahre nachweisbar ) 18 Metastasierendes differenziertes Schilddrüsen-Ca 131Iod HWZ: 8.04 d Beta- und Gamma- Strahlung 24 h p.o. 72 h p.o. Klinik für Nuklearmedizin, Universitätsklinikum Rostock R Follikuläres Schilddrüsen-Karzinom mit pulmonaler Metastase (pT2aN1bM1 / UICC 1987) L 18FDG-PET Mann, 43 Jahre 19 Hormonsubstitution der SD-Ca Füher: Nach Thyreoidektomie keine Substitution bis zur 131I-Ablation Neu: Nach Operation L-Thyroxin (2 – 3 µg/kg Körpergewicht) ! TSH <1,0 mE/L (pT1 und pT2, differenzierte Karzinome) TSH <0,1 mE/L (pT3, pT4, N1, M1, undifferenzierte Karzinome und Metastasen) fT3-Spiegel im Normbereich ! Vor 131I-Ganzkörper-Szintigraphie bzw. -Therapie Thyrogen 0,9 i.m. Indikationen zur Radioiodtherapie bei Struma in Euthyreose sogen. Radioiodverkleinerungstherapie Vorr: TSH i. Normbereich Kein Ansprechen auf konservative Therapie (weiteres Wachstum) Absolute oder relative Kontraindikationen zur Operation Rezidivstruma mit Wachstumstendenz trotz konservativer Therapie Bestehende Reccurensparese Wunsch des Patienten 20 Kontraindikationen zur Radioiodtherapie Absolute Kontraindikationen Gravidität Laktation Malignomverdacht Niedrige Radioiodaufnahme im Radioiodtest (< 8 %) Kinderwunsch innerhalb von 4-6 Monaten nach Radioiodtherapie Stark hyperthyreote Stoffwechsellage – zwischenzeitllich thyreostatische Überbrückungstherapie dann notw. Relative Kontraindikationen Kinder (Jugendliche), Ausnahme SD-Ca Große Strumen (>60 ml) Mechanische Komplikationen (enge Trachea) Berechnung der Therapieaktivität (Marinelli-Formel) Applikationsdosis (MBq) = Energiedosis (Gy) x Volumen (ml) x Faktor maximaler Uptake (%) x effektiveHWZ (d) Funktionelle Autonomie Zielherddosis (Gy) Morbus Basedow 100 - 250 Adaptiert nach Multifokale/Disseminierte Autonomie 100 - 250 Funktion und Unifokale Autonomie 300 Volumen Elimination 400 Verkleinerung 100 - 150 ____________________________________________________ Tumorbehandlung Aktivität (GBq) Eliminationsbehandlung (Restgewebe) 3,7 – 5,5 Metastasenbehandlung 7,5 (bis 11) 21