Hämoglobin
Werbung

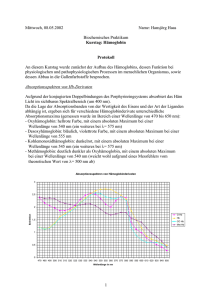
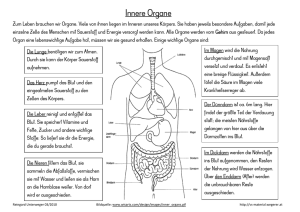
Biochemie-Protokoll Gruppe 1 HÄMOGLOBIN 13.05.16 Julia Gnann & Christoph Hartmann Einleitung Hämoglobin Allgemein Hb ist der rote Blutfarbstoff der Wirbeltiere, der in den Erythrocyten (roten Blutkörperchen) des Blutes enthalten ist und 95% von deren Trockenmasse ausmacht. Er wird während der Erythropoese genannten Entstehung dieser Zellen in den Blutbildungs-Zentren des Körpers (beim erwachsenen Menschen im Knochenmark) synthetisiert. Der Hb-Gehalt der Erythrocyten ist im erwachsenen Organismus eine Konstante, die auch im Tierreich weitgehend gültig ist: ca. 31 pg pro Zelle. Die auf das Blutvolumen bezogene Menge an Hb beträgt bei erwachsenen Frauen ca. 140 g/l Vollblut gegenüber etwa 160 g/l beim Mann. Demnach stehen dem Körper bei 5–6 l Blut ca. 700–900 g Hb zur Verfügung. Da Hb 0,334% Eisen enthält, sind ca. 3 g oder 70% des Gesamtkörper-Eisens darin gebunden. Struktur Chemisch ist Hb ein tetrameres Eisenprotein, dessen Monomere aus je einer Globin-Kette mit einem Molekül Häm als prosthetischer Gruppe bestehen. Die Abbildung zeigt schematisch den Aufbau eines Hb-Monomers mit der α-Globin-Kette in charakteristischer Faltung und mit der Häm-Gruppe in koordinativer Bindung an die HistidinAbbildung 1: Hb-Struktur Reste 58 und 87. Die Polypeptid-Kette ist schematisch durch ein Band dargestellt. Untereinander sind die 4 Monomeren durch Nebenvalenzkräfte verbunden und bilden ein globuläres Makromolekül vom MG 64500 mit einem Durchmesser von ca. 5–6 nm. Die 4 Häm-Einheiten liegen in „Taschen“ nahe der Oberfläche des Moleküls. Je zwei Globin-Untereinheiten eines Tetrameren sind einander gleich: Beim erwachsenen Menschen tritt in der Hauptsache (zu 96,5–98,5%) das Hb A1 auf, das aus 2 α-Ketten mit je 141 und 2 β-Ketten mit je 146 Aminosäure-Resten gebildet wird und somit durch die Stöchiometrie α2β2 beschrieben werden kann. Daneben kommen noch 1,5–3,5% Hb A2 vor, das δ- statt β-Globin enthält (α2δ2). Der Embryo synthetisiert kurz nach der Konzeption das Hb mit der Zusammensetzung ζ2ε2, im Fötalstadium findet sich α2γ2 (vgl. Globine). Diese Hb besitzen erhöhte Sauerstoff-Affinität, so daß Sauerstoff aus dem mütterlichen Blut in den embryonalen bzw. fötalen Kreislauf abgegeben wird. Neben diesen Normal-Hb kennt man heute über 150 abnorme Hb, die durch Mutationen entstanden sind und ggf. zu schweren Anämien führen wie Sichelzellenanämie, bei der der Austausch nur eines Aminosäure-Restes in der β-Kette zur Schwerlöslichkeit des Hb führt Bei Thalassämie ist die Biosynthese der α- oder β-Ketten gestört. Biologische Funktion Die Aufgabe des Hb besteht in der Aufnahme des eingeatmeten Sauerstoffs in der Lunge und dessen Transport zu den Muskeln (wo das Myoglobin den Weitertransport übernimmt) und zu anderen atmenden Geweben. Außerdem wird ein großer Teil (ca. 60%) des Kohlendioxids, das als Stoffwechsel-Endprodukt im peripheren Gewebe entsteht, durch Bindung an das Hb des Blutes zur Lunge geführt und dort ausgeschieden. Das Kohlendioxid reagiert dabei mit den terminalen AminoGruppen der Globin-Ketten zum Carbamat. Die Bindung des Sauerstoffs findet an einer der Koordinations-Stellen des Eisens statt, die über bzw. unter der Ebene des Häm-Moleküls liegen. Das Tetramer kann insgesamt 4 Sauerstoffmoleküle binden. Die Aufnahme eines Moleküls Sauerstoff in den Verband eines Hb-Moleküls bewirkt eine Konformationsänderung des Makromoleküls (Allosterie), die sich durch Kontakt-Wechselwirkungen von einer Untereinheit auf die andere fortpflanzt, so daß sich die folgenden Sauerstoffmoleküle leichter mit dem betreffenden Hb-Molekül verbinden können. Dieser Effekt wird als Kooperativität Seite 1 Biochemie-Protokoll Gruppe 1 HÄMOGLOBIN 13.05.16 Julia Gnann & Christoph Hartmann bezeichnet. Das Hb-Molekül liegt je nach Sauerstoff-Beladung entweder in einer gespannten (TStruktur von engl.: tense) oder entspannten (R-Struktur von engl.: relaxed) Form vor. Bei der Sauerstoff-Aufnahme wechselt die Farbe des Blutes von Purpurrot (venöses Blut) zu hellem Scharlachrot (arterielles Blut). Das mit Sauerstoff beladene Hb wird als Oxyhämoglobin bezeichnet. Die theoretische Gesamt-Bindungskapazität des Hb für Sauerstoff in den 5–6 l Blut des Erwachsenen, die jedoch im allg. nur zu 25% ausgenutzt wird, liegt bei 1100–1400 ml; in der gleichen Menge Wasser lösen sich (bei 20°) dagegen nur 150–180 ml Sauerstoff. Das Eisen im Oxyhämoglobin bleibt bei der koordinativen Bindung des Sauerstoffs unverändert in der Oxidationsstufe 2. Dies steht im Gegensatz zu den Verhältnissen im freien Häm, das durch Sauerstoff leicht oxidiert wird, und ist als spezifischer Effekt des Globins anzusehen. Durch verschiedene Oxidationsmittel – im Organismus wird Hb normalerweise durch die Wirkung der Glutathionperoxidase geschützt – kann Hb leicht in Methämoglobin (Hämiglobin, Ferrihämoglobin), das Eisen(III) enthält und als Sauerstoff-Überträger ungeeignet ist, überführt werden. Hb hingegen ist als Sauerstoff-Überträger gerade durch die leichte Aufnahme und Abgabe des Sauerstoffs geeignet. Diese Reaktionen sind vom jeweiligen Partialdruck (von der jeweiligen Konzentration) des Sauerstoffs abhängig. In der an Sauerstoff reichen Umgebung der Lunge wird dieser aufgenommen und in der Sauerstoff-ärmeren Umgebung der peripheren Gewebe wieder abgegeben. Auslösend für die Sauerstoff-Abgabe wirkt auch die Anwesenheit von Kohlendioxid und Milchsäure (niederer pH-Wert) im Blut (sog. BOHR-Effekt). Ein weiterer Regulator des Hb ist 2,3Bisphosphoglycerat, das dessen Sauerstoff-Affinität herabsetzt, indem es die Sauerstoff-freie Form (Desoxy-Hb) stabilisiert. Die Sauerstoff-Reserven des Menschen sind nicht groß; nach erfolgtem Herzstillstand (z.B. bei Unfall) enthält die Lunge noch Sauerstoff für 100 Sek., das Blut für 140 Sek., und das Gehirn bleibt noch weitere 180 Sek. ohne Blutzirkulation funktionsfähig, ehe es irreversible Schädigungen erleidet. Erythrozyt Abbau und Neusynthese Da ein Erythrocyt im Durchschnitt 120 Tage alt wird und der Blutkreislauf des Erwachsenen 25–30 Billionen der roten Blutkörperchen enthält, sind Tag für Tag Milliarden von Erythrocyten in Neubildung und Abbau begriffen. Das aus den zerfallenden Erythrocyten ausgetretene Hb wird in den Zellen des retikuloendothelialen Systems1 abgebaut. Dabei entsteht unter oxidativer Aufspaltung des Porphyrin-Ringes im Häm-Molekül (wobei ungünstigerweise auch Kohlenoxid frei wird) über Verdoglobin und Biliverdin der Gallenfarbstoff Bilirubin; durch weiteren Abbau bilden sich die Fäkalpigmente. Das freigesetzte Eisen wird zum geringeren Teil aus dem Körper ausgeschieden (ca. 7 mg/24 Std.), zum größeren Teil jedoch wird es – ergänzt durch Eisen aus der täglichen Nahrung, z.B. aus Brot, Gemüse und Fleisch (bes. Leber) – über die Milz erneut in den Kreislauf zurückgebracht. Die Menge des während der Hämatopoese im Knochenmark des Erwachsenen neugebildeten Hb liegt bei normalem EisenStoffwechsel zwischen 3 und 6 g pro Tag. Die Biosynthese des Häm geht von 5Amino-4-oxovaleriansäure aus und führt über Porphobilinogen und Uroporphyrinogen III in mehreren Schritten schließlich zu Protoporphyrin. Hämoglobin Biliverdin RES1 Bilirubin indirektes Bilirubin direktes Bilirubin Blut Leber Mesobilirubin Urobilirubin Darm Urobilin Abbildung 2 Versuche Absorptionsspektren von Hb-Derivaten Die Absorptionsspektren liegen im sichtbaren Lichtbereich, da konjugierte Doppelbindungen vorliegen. Sie hängt ab vom Zustand des Hämoglobins, sprich von der Wertigkeit des Eisens und Art des gebundenen Liganden. 1 Die Zellen des RES finden sich in Knochenmark (als Promonocyten), in Blut u. Lymphe (als Monocyten), in Milz, Lymphknoten u. Lunge (als Makrophagen), in den Nieren (als Mesangiumzellen), im Gehirn (Mikroglia) sowie in der Leber (als KUPFFERSternzellen) Seite 2 HÄMOGLOBIN Biochemie-Protokoll Gruppe 1 13.05.16 Julia Gnann & Christoph Hartmann Absorptionsspektren von Hb-Derivaten 2,5 2,25 2 1,75 Extinktion 1,5 1,25 1 0,75 0,5 0,25 0 470 480 490 495 500 505 510 520 530 535 540 545 550 560 565 570 575 580 585 590 600 610 620 625 630 635 640 650 nm HbO2 Hb HbCO MetHb Fragen Warum liegen die Absorptionsmaxima von HbO2 und HbCO sehr ähnlich? die Maxima liegen sehr ähnlich da Sauerstoff und Kohlenmonoxid auf die gleiche Weise an Hb binden. Wie kann man HbO2 und HbCO unterscheiden? die HbO2-Lösung ist sattrot, die HbCO-Lösung hellrot und durch die große Affinität (210x) und den langsamen Abbau ist der Sauerstofftransport unterbunden. Was geschieht mit Methämoglobin im Organismus? Das MetHb wird durch die NADH + H+ / NADPH + H+ - abhängige MetHb-Reduktase wieder zu Hb reduziert. MetHb ist nicht zum Sauerstofftransport fähig. Wie erfolgt der CO2-Transport im Blut? CO2 bindet an endständige Aminogruppen Carbamat-Gruppe. Bei Beladung mit O2 in der Lunge zerfallen die Carbamat-Gruppen wieder in CO2 und die freien Aminogruppen (50%). Die verbleibenden 50% werden durch den BOHR-Effekt transportiert und ausgeatmet Hb + 4O2 Hb(CO2)4 + H+ (BOHR-Effekt Protonenbildung) H+ + HCO3- H2CO3 CO2 + H20 Wird im Gewebe O2 abgegeben, dann nimmt Hb als schwache Säure gleichzeitig H + auf; dabei dissoziiert H2CO3 vermehrt zu H+ und HCO3-. Wird das Hb in der Lunge wieder mit O2 beladen, dann liegt die stärkere Säure HbO2 vor, H+ wird abgegeben und reagiert mit HCO3- zu H2CO3 und dann zu CO2 + H2O. Bestimmung von 5-Aminolävulinsäure (5-ALA) und Porphobilinogen (PBG) Versuch entfiel! Seite 3 Biochemie-Protokoll Gruppe 1 HÄMOGLOBIN 13.05.16 Julia Gnann & Christoph Hartmann Fragen Beschreiben Sie die Ionenaustauschvorgänge in den Säulen Ionenaustauscher sind hochpolymere organische Harze, die saure (COOH, SO 3H) oder basische (NH3+) Gruppen enthalten. das Grundgerüst besteht häufig aus Polystyrolketten, die durch wechselnde Mengen an Divinylbenzol vernetzt sind. Ionenaustauscher die saure Gruppen enthalten, bezeichnet man als Kationenaustauscher, weil sie in der Lage sind, Kationen auszutauschen. Solche, die basische Gruppen enthalten, bezeichnet man als Anionenaustauscher, weil sie in der Lage sind, Anionen auszutauschen. Bringt man einen Ionenaustauscher in Wasser, so dringen Wassermoleküle in die Poren des Harzgerüstes ein und ionisieren die dort eingebauten Gruppen. dies soll am Beispiel eines Kationenaustauschers mit SO3H-Gruppen erläutert werden: ~SO3H + H2O ~SO3- + H3O+ Wegen der Fixierung der SO3--Gruppen am Harz sind die H3O+-Ionen durch elektrostatische Anziehung ebenfalls in der Nähe der SO3--Gruppen fixiert. Läßt man nun auf diesen Kationenaustauscher andere positiv geladene Ionen, z.B. Na+ einwirken, so konkurrieren diese mit den H3O+-Ionen um das Gegenion SO3- nach folgendem Schema: ~SO3- H3O+ + Na+ ~SO3- Na+ + H3O+ Dabei stellt sich ein Gleichgewicht ein, dessen Lage von der Art des Harzes und der Art der Ionen abhängt. Dabei werden Metallionen fester gebunden als H 3O+; außerdem nimmt in der Regel die Affinität an den Austauscher mit steigender Ladung zu, d.h. 2-fach positiv geladene Ionen werden fester gebunden als einfach positive. Wenn man nun dafür sorgt, daß die H3O+-Ionen laufend aus dem GG entfernt werden, kann man erreichen, daß sämtliche Na+-Ionen am Austauscher gebunden werden. das erreicht man am einfachsten dadurch, daß man den Ionenaustauscher in eine lange, dünne Säule füllt und die Lösung mit dem auszutauschendem Ion langsam durch die Säule kaufen läßt. Die aus der Säule abtropfende Lösung enthält nun die dem auf der Säule aufgebrachten Kation äquivalente Menge an H3O+-Ionen, die maßanalytisch bestimmt werden können. Bei unserem Versuch wäscht man im zweiten Säulendurchlauf mit einer Lösung (anderer pH, andere Salzkonzentrationen) die zu bestimmenden Ionen aus und erhält sie im Eluat Nachweisreaktionen möglich. Bestimmung des Bilirubins im Serum Häm wird zu Gallenfarbstoffen abgebaut, der wichtigste ist das Bilirubin. Es kommt als freies Bilirubin (gebunden an Albumin) und als konjugiertes Bilirubin (gut löslich) vor. Zusammen ergibt sich das Gesamtbilirubin. Die Bilirubinmenge ist diagnostisch relevant für: Lebererkrankungen, Gallengangsverschluß oder erhöhten Hämabbau. die getrennte Bilirubinbestimmung ist zur DD für verschieden Ikterusformen wichtig. Bestimmung des Gesamtbilirubins ε578nm = 6,8*104 MGBilirubin = 585 Extinktion bei l mol*cm g mol = 578nm: 2,65 E V * * F * MG *d 2,65 * mol * cm 2,45 g mg g * 585 mol * c= = 0,279 l = 27,9 100ml 4 0,2 6,8 *10 l *1cm c= mg [Norm: 0,5 – 1 100ml ] Seite 4 Biochemie-Protokoll Gruppe 1 HÄMOGLOBIN 13.05.16 Julia Gnann & Christoph Hartmann Bestimmung des direkten Bilirubins ε546nm = 5,12*104 MGBilirubin = 585 Extinktion bei l mol*cm g mol = 546nm: 0 0 * mol * cm 2,45 mg g c= = 0 100ml * 585 mol * 4 0,2 5,12 *10 l *1cm mg [Norm: bis 0,25 100ml ] Der Wert des Gesamtbilirubins ist sehr hoch und deutet auf einen schweren Fall von Ikterus hin! Der Wert des direkten Bilirubins ist normal. Ursachen für den Ikterus können erhöhte Produktion (Produktionsikterus) oder verminderte Konjugation (Konjugationsikterus) sein. Nachweis von Urobilinogen und Bilirubin im Harn mit Teststäbchen Urobilinogen und Bilirubin lassen sich im Harn mittels Teststäbchen durch Eintauchen derselben in eine Urinprobe („Mittelstrahl“!!) halbquantitativ bestimmen. Die Teststäbchen enthalten auf einer Reaktionszone stabile Diazoniumsalze, die mit Urobilinogen und Bilirubin Farbstoffe bilden, die mit einem Farbcode auf der Testpackung verglichen werden können. Ergebnis: Alle Werte lagen bei mir im Normalbereich. Fragen In welchen Organen findet der Porphyrinabbau statt? Die Porphyrine werden im RES1 abgebaut. Wodurch ist die gelbe Farbe des Harns bedingt? Die normale Gelbfärbung des Harns ist auf sog. Urochrome zurückzuführen, die Abbauprodukte des Bilirubins wie z.B. Urobilin und Stercobilin enthalten. Bei verschiedenen Krankheiten treten im Harn anormale Bestandteile auf, so z.B. Gallenfarbstoffe (insbes. Propentdyopente, Abbauprodukte des Bilirubins) bei Leberentzündungen, Bakterien bei bakteriellen Infektionen der Harnwege und der Niere, Jod bei Kropfbildung und Leukocyten bei Mykosen und Harnsteinen. Welche Ikterus-Formen unterscheidet man? Einteilung nach pathogenetischen Kriterien: 1. Produktionsikterus: bei erhöhter Bilirubinproduktion (gesteigerter Häm-Abbau) wird das Glukuronyltransferasesystem funktionell überfordert, was zu einer Vermehrung des unkonjugierten (indirekten) Bilirubins führt; z.B. bei allen Formen der Hämolyse, bei sog. Shunthyperbilirubinämie oder Hyperbilirubinämie des Neugeborenen. 2. Transportikterus/Absorptionsikterus: Störung des Bilirubintransports von den Lebersinusoiden zu den Mikrosomen der Leberzellen; z.B. bei intermittierender Hyperbilirubinämie, Meulengracht-Krankheit und wahrscheinlich z.T. bei best. Hepatitisformen bzw. ikterischer Leberzirrhose. 3. Konjugationsikterus: Störung der Konjugation von Bilirubin mit Glukuronsäure in den Mikrosomen der Leberzelle infolge relativen oder absoluten Mangels der Glukuronyltransferase. Das wasserlösliche konjugierte (direkte) Bilirubin kann nicht gebildet werden; z.B. bei Crigler-Najjar-Syndrom, physiologischem Neugeborenenikterus mit relativem Enzymmangel oder Konjugationsstörungen beim Neugeborenen durch Inhibitoren der Glukuronyltransferase (z.B. Pregnandiolderivate in der Muttermilch, Medikamente). 4. Exkretionsikterus: Vermehrung des konjugierten Bilirubins durch Störung der Ausscheidung in die Gallengänge; z.B. bei Dubin-Johnson-Syndrom, Rotor-Syndrom, Hepatitis, Leberzirrhose, Alkoholhepatitis, Schwangerschaftsikterus, sog. Drogenikterus oder nach MedikamentenSeite 5 HÄMOGLOBIN Biochemie-Protokoll Gruppe 1 13.05.16 Julia Gnann & Christoph Hartmann einnahme (z.B. durch Methyltestosteron, in C17-Stellung alkylierte Steroide, Ovulationshemmer, Isoniazid, Paracetamol, Rifampicin). 5. Verschlußikterus (mechanisch bedingter post- bzw. extrahepatischer Ikterus): Störung des Bilirubintransports durch partielle oder totale Verlegung des Ductus choledochus; z.B. bei Gallengangkarzinom, Cholelithiasis, primär-sklerosierender Cholangitis oder Gallengangatresie. Das in der Leber gebildete Bilirubinglukuronid kann nicht oder nur geringfügig in den Darm abfließen und tritt daher in das Blut über (sog. Resorptionsikterus). Einteilung nach der Farbe der verschiedenen Ikterusformen 1. Flavinikterus (strohgelbe Hautfarbe, v.a. bei hämolytischem Ikterus); 2. Melasikterus (schmutzig-dunkelgrüne Hautfarbe, v.a. bei länger bestehendem Verschlußikterus); 3. Rubinikterus (rötliche Hautfarbe, v.a. bei akuter Hepatitis); 4. Verdinikterus (grüne Hautfarbe, v.a. bei Verschlußikterus). Welche Ursache hat der Neugeborenen-Ikterus? = Icterus neonatorum; Ursache ist ein physiologischer Konjugationsikterus infolge transitorischer Unreife der Transport- und Koppelungssysteme (UDP-Glukuronyltransferase) in der Leber. Beim Neugeborenen kommt es zu einer beträchtlichen enteralen Rückresorption von nicht konjugiertem Bilirubin; post natum steigt die Serumbilirubinkonzentration an, erreicht bei Reifgeborenen als Maximum ca. 100µmol/l (6mg/dl) am 3.-5. Lebenstag und fällt dann innerhalb von 2-3 Wochen zur Norm ab. Problematik der der Rhesus-Unverträglichkeit in diesem Zusammenhang In den letzten SSW/bei der Geburt treten Erythrozyten des Embryos mit Antigenstruktur in die mütterlich Blutbahn über. Diese produziert Antikörper, die ihrem ersten Kind nicht schaden. Bei einer erneuten Schwangerschaft aber erfolgt die Immunreaktion bei den Vorgängen in den letzten SSW. Dabei passieren Antikörper die Plazenta und gelangen in die embryonale Blutbahn hämolytischer Ikterus. Bestimmung des Eisens im Serum Eisen wird im Serum durch Transferrin, ein β-Globulin, transportiert. Zur Bestimmung wird das Eisen mit einem schwach sauren Phosphatpuffer abgespalten und mit Natriumascorbat reduziert, mit einem sulfonierten Bathophenanthrolin in eine rotgefärbte Verbindung überführt und photometrisch gemessen. ε535nm = 3,19*104 l mol*cm AtomgewichtFe = 55,85 Extinktion bei E = 0,134 c= g mol = 535nm: EA = 1,054; EB = 1,188 0,134 * mol * cm 3 g * 55,85 mol * = 7,038*10-4 gl = 70,38 dlg 4 1 3,19 *10 l * cm g g [Norm: : 80-120 100ml ; : 90-140 100ml ] Dieser Wert ist etwas zu niedrig. Es handelt sich hierbei wahrscheinlich um einen Meßfehler. Bestimmung des Kupfers im Serum Versuch entfiel! Seite 6 Biochemie-Protokoll Gruppe 1 HÄMOGLOBIN 13.05.16 Julia Gnann & Christoph Hartmann Fragen Zählen Kupfer und Eisen zu den Spurenelementen? Cu und Fe zählen zu den essentiellen Spurenelementen. Sie sind Bestandteile von Hormonen, Chromoproteinen, Enzymen. Welche anderen Metalle spielen im Organismus eine Rolle? Tabelle1 Tabelle 2 Was versteht man unter Morbus Wilson? = hepatolentikuläre Degeneration. Es handelt sich um eine autosomal-rezessiv erbliche Erkrankung mit Kupferstoffwechselstörung und Störung der Caeruloplasminsynthese. Pathologie: Degeneration von Ganglienzellen, reaktive Vermehrung abnormer Gliazellen in den Stammganglien und im Cortex, multilobuläre Leberzirrhose. Symptome: extrapyramidales Syndrom mit Hyperkinesen, Flapping-Tremor und Myoklonien, Störungen der Affektivität, Gedächtnisstörungen, Psychose, in späteren Stadien evtl. Demenz; Hepatosplenomegalie. Diagnose: Caeruloplasmin im Serum erniedrigt, Kupferausscheidung im Urin erhöht; in der kranialen Computertomographie evtl. hypodense Areale. Seite 7 Biochemie-Protokoll Gruppe 1 HÄMOGLOBIN 13.05.16 Julia Gnann & Christoph Hartmann Wie bestimmt man die LEBK und die Gesamt-EBK? Gesamt-EBK: Durch Fällung mit Mg-Carbonat, radiochemisch mit 59Fe oder durch Bestimmung des Transferrins mittels radialer Immundiffusion. LEBK: 2 3 des Eisens liegen im Körper frei vor. Bestimmung über indirekte Berechnung von Gesamt-EBK aus. Abbildungsverzeichnis: Abbildung 1: CD-Römpp Chemielexikon; Thieme Abbildung 2: ckjh Tabellenverzeichnis: Tabelle 1: Pschyrembel, 258. Auflage; WdeG Tabelle 2: Pschyrembel, 258. Auflage; WdeG Quellen: CD-Römpp Chemielexikon; Thieme Pschyrembel, 258. Auflage; WdeG Seite 8








![Vortrage-5 [Kompatibilis mód]](http://s1.studylibde.com/store/data/006676220_1-cb815e9f1c2d143e057e7d76cabd28d9-300x300.png)
