Proteine - Fachdidaktik Chemie ETH
Werbung
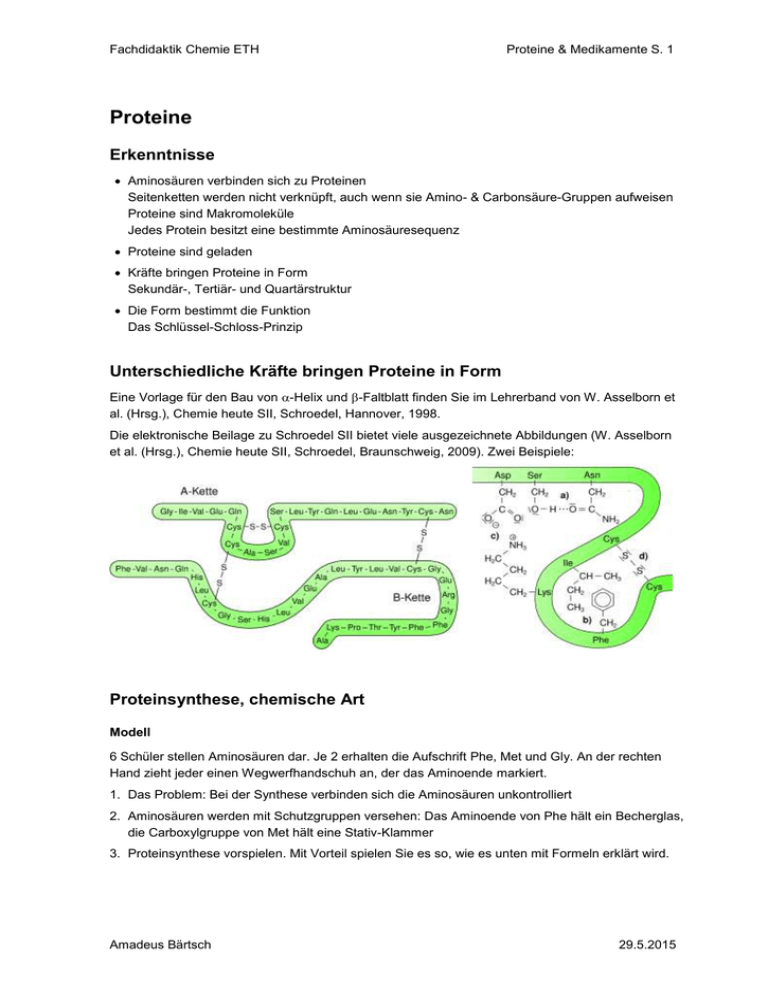
Fachdidaktik Chemie ETH Proteine & Medikamente S. 1 Proteine Erkenntnisse Aminosäuren verbinden sich zu Proteinen Seitenketten werden nicht verknüpft, auch wenn sie Amino- & Carbonsäure-Gruppen aufweisen Proteine sind Makromoleküle Jedes Protein besitzt eine bestimmte Aminosäuresequenz Proteine sind geladen Kräfte bringen Proteine in Form Sekundär-, Tertiär- und Quartärstruktur Die Form bestimmt die Funktion Das Schlüssel-Schloss-Prinzip Unterschiedliche Kräfte bringen Proteine in Form Eine Vorlage für den Bau von -Helix und -Faltblatt finden Sie im Lehrerband von W. Asselborn et al. (Hrsg.), Chemie heute SII, Schroedel, Hannover, 1998. Die elektronische Beilage zu Schroedel SII bietet viele ausgezeichnete Abbildungen (W. Asselborn et al. (Hrsg.), Chemie heute SII, Schroedel, Braunschweig, 2009). Zwei Beispiele: Proteinsynthese, chemische Art Modell 6 Schüler stellen Aminosäuren dar. Je 2 erhalten die Aufschrift Phe, Met und Gly. An der rechten Hand zieht jeder einen Wegwerfhandschuh an, der das Aminoende markiert. 1. Das Problem: Bei der Synthese verbinden sich die Aminosäuren unkontrolliert 2. Aminosäuren werden mit Schutzgruppen versehen: Das Aminoende von Phe hält ein Becherglas, die Carboxylgruppe von Met hält eine Stativ-Klammer 3. Proteinsynthese vorspielen. Mit Vorteil spielen Sie es so, wie es unten mit Formeln erklärt wird. Amadeus Bärtsch 29.5.2015 Fachdidaktik Chemie ETH Proteine & Medikamente S. 2 Einsatz von Schutzgruppen 1. Aminosäuren werden mit Schutzgruppen versehen 2. Geschützte Aminosäuren reagieren miteinander 3. Eine nächste Aminosäure kommt dazu Proteinsynthese, biologische Art Zellen benützen die DNS: Die Basen bestimmen die Reihenfolge der Aminosäuren. Eine einfache Animation finden Sie auf der Plattform http://fdchemie.pbworks.com. Amadeus Bärtsch 29.5.2015 Fachdidaktik Chemie ETH Proteine & Medikamente S. 3 Die Form bestimmt die Funktion Die folgende Abbildung aus dem Taschenatlas der Biochemie zeigt, dass es viele verschiedene Proteine gibt Proteine wichtig sind und unterschiedlichste Aufgaben im Körper erfüllen. Es ist eine Zelle, ein Erythrozyt und das Blutplasma dargestellt. Den Text zur Abbildung finden Sie auf http://fdchemie.pbworks.com. (J. Koolman et al., Taschenatlas der Biochemie, Thieme, S. 62-63, 1994) Amadeus Bärtsch 29.5.2015 Fachdidaktik Chemie ETH Proteine & Medikamente S. 4 Die Form ist empfindlich Experiment: Proteine denaturieren Variante 1: Ein Ei aufschlagen, Eiweiss abtrennen und gleichmässig in 4 kleine Kristallisierschalen verteilen. Auf dem Hellraumprojektor ins erste Glas 3 Tropfen 2 M Salzsäure, ins zweite Glas 3 Tropfen 2 M Natronlauge und ins dritte Glas 3 Tropfen einer Quecksilbersalz-Lösung geben. Das vierte Glas mit einem Zündholz oder einem Feuerzeug erwärmen. Die Gründe für die Denaturierung erklären. Variante 2: Demonstration von Esther Lenherr im Experimentierkurs 2012 (Anleitung siehe http://fdchemie.pbworks.com/w/page/66568556/Proteine%20und%20Medikamente) Amadeus Bärtsch 29.5.2015 Proteine & Medikamente S. 5 Fachdidaktik Chemie ETH Enzyme sind wählerisch Labor: Substratspezifität von Trypsin und Chymotrypsin http://www.swisseduc.ch/chemie/labor/tryp_chymotryp/docs/exptryps.pdf (21.5.12) O H N O H N + H2O O O O + HO + H+ + HO + H+ O NH H2N NH NH2 H2N NH2 N-Benzoyl-L-arginin-ethylester O H N O H N + H2O O O O O OH OH N-Benzoyl-L-tyrosin-ethylester Im Gegensatz zu Phenylalanin ist die Seitenkette von Arginin positiv geladen. Diese Ladung, die in der Abbildung eingetragen werden muss, ist entscheidend für die Spezifität. aus: R. E. Dickerson & I. Geis, Chemie - eine lebendige und anschauliche Einführung, Verlag Chemie, Weinheim (1981) Amadeus Bärtsch 29.5.2015 Fachdidaktik Chemie ETH Proteine & Medikamente S. 6 Die Substratspezifität von Trypsin Quelle: M. Jäckel et al. (Hrsg.), Lehrerband von Chemie heute SII, Schroedel, Hannover, 1988 Die Hydrolyse wird in der "Enzymanimation Chymotrypsin 13" von H. U. Ehrensperger interaktiv erklärt. www.klangheimlich.ch/chemie/ Amadeus Bärtsch 29.5.2015 Fachdidaktik Chemie ETH Proteine & Medikamente S. 7 Medikamente Enzyme gezielt blockieren Erkenntnisse Meist wirken Medikamente in dem sie Enzyme gezielt blockieren Wenn man Krankheiten biochemisch verstanden hat, können Medikamente entwickelt werden, die die Ursache bekämpfen Wie können Nebenwirkungen vermieden werden? 1. Bsp. Allopurinol gegen Gicht – ein gutes Konzept NZZ: Gicht - eine alte Wohlstandskrankheit Ein ausgezeichneter Zeitungsartikel zu üppigem Essen, Harnsäure und plötzlichen Gelenkschmerzen. Früher ein Leiden der Oberschicht, ist die Gicht längst zur Volkskrankheit geworden, bei deren Entstehung die Ernährung eine wesentliche Rolle spielt. Moderne Medikamente haben die oft zu Verkrüppelungen führenden Spätfolgen inzwischen selten gemacht. (Neue Zürcher Zeitung; 03.05.2006; Seite 65 zu finden auf der Plattform) Ursache für die Erkrankung sind Harnsäurekristalle in den Gelenken, die die Reibung drastisch erhöhen und zu Entzündungen führen. Exp. Harnsäure in Wasser Vorgehen Eine Spatelspitze Harnsäure in 200 ml Wasser geben und rühren. Wenig Bromthymolblau, dann Natronlauge zugeben und rühren Mit 2 M Salzsäure sauer stellen und rühren Skizze kleine Stücke farblose, transparente Lösung einige Kristalle am Boden Beobachtung Das Gemisch ist trübe Das Gemisch wird klar Das Gemisch bleibt klar. Es dauert mindestens 1 Stunde bis Kristalle zu sehen sind. Erklärung Harnsäure ist schwer löslich Harnsäure gibt ein H+ ab und erhält eine negative Ladung, die das Molekül wasserlöslich macht. Harnsäure kristallisiert verzögert. Gichtanfälle sind schubweise Amadeus Bärtsch 29.5.2015 Proteine & Medikamente S. 8 Fachdidaktik Chemie ETH Labor: Xanthinoxidase hemmen Der Abbau von DNA führt über Hypoxanthin zu Harnsäure, die sich schlecht in Wasser löst. Wenn die Konzentration zu gross ist, kann Harnsäure in den Gelenken auskristallisieren und Gicht hervorrufen. Weil Allopurinol dem Hypoxanthin gleicht, passt es auf das aktive Zentrum von Xanthinoxidase. Eine kompetitive Hemmung vermindert die Harnsäurebildung. Andere Enzyme sind nicht betroffen, weil Enzyme spezifisch sind und Allopurinol nur auf die Xanthinoxidase passt. Deshalb wird das Medikament gut vertragen. Details und Versuchsanleitung sind auf http://fdchemie.pbworks.com eingestellt. 2. Bsp: Antibiotika gegen Bakterien Antibiotika sind ausgezeichnete Medikamente, weil sie sehr gut wirken und die Bakterien im menschlichen Körper – also die Ursache der Infektion – bekämpfen. Sie verhindern die Vernetzung der Zellwand von Bakterien. Da Menschen keine Zellwand besitzen, werden Antibiotika gut vertragen. Resistente Bakterien besitzen Plasmide, die Lactamase – ein Enzym, das Antibiotika inaktiviert – erzeugen. H N S O N O O O H Penicillin G Auf molekularer Ebene lässt sich die Wirkung gut erklären: Antibiotika besitzen einen gespannten viergliedrigen Ring. Die Ringspannung macht das Antibiotikum reaktionsfähig und führt zu einer kovalenten(!) Bindung an das bakterielle Enzym. (J. Koolman et al., Taschenatlas der Biochemie, Thieme, S. 93, 1994) -Lactamase, die von resistenten Bakterien gebildet wird, öffnet den Ring und das Antibiotikum wird inaktiv bevor es auf das Vernetzungsenzym trifft. Amadeus Bärtsch 29.5.2015 Proteine & Medikamente S. 9 Fachdidaktik Chemie ETH 3. Bsp. Sulfonamide gegen Bakterien Sulfonamide hemmen die ersten beiden Stufen der Synthese von Folsäure und damit das Wachstum von Bakterien. Auch Menschen können nicht ohne Folsäure auskommen. Im Unterschied zu den Bakterien nehmen Menschen Dihydrofolsäure aber mit der Nahrung auf. Sulfonamide wirken deshalb gezielt gegen Bakterien. (Unterrichtsmaterial von Roger Deuber ist auf http://swisseduc.ch/chemie/sulfonamide zugänglich) H2N Bakterien N N H N O OH N COOH H2N NH2 O OH p-AminobenzoesЉ ure PABA Dihydropteridin H2N N Enzym: DihydropteroinsЉure-Synthase H N N CH2 OH HN DihydropteroinsЉ ure N N Menschen nehmen DihydrofolsЉ ure mit der Nahrung auf H N N OH CH2 HN N H N OH N H N H COOH GlutaminsЉ ure O H COOH C N C CH2CH2 COOH H Enzym: DihydrofolsЉ ure-Reduktase CH2 HN TetrahydrofolsЉure Amadeus Bärtsch H2N C CH2CH2 COOH + Enzym: DihydrofolsЉ ure-Synthase DihydrofolsЉ ure H2N Sulfonamide hemmen DihydropteroinsЉ ure-Synthase, ein Enzym das nur in Bakterien vorkommt. COOH N H2N S NH2 O H COOH C N C CH2CH2 COOH H 29.5.2015 Fachdidaktik Chemie ETH Proteine & Medikamente S. 10 Neben der Erklärung des Wirkmechanismus zeigt Roger Deuber mit dem pdb-Viewer, warum Sulfonamide stärker an die in die aktive Stelle passen als das Substrat. Die Schülerinnen erfahren in einer selbständigen Arbeit, wie Enzyme am Computer dargestellt und die Wirkung von Medikamenten optimiert werden können. Abb. Die Form der Enzyme kann am Computer dargestellt werden. Die Abbildung mit dem Programm "iMol" zeigt Sulfonamid im aktiven Zentrum von Dihydropteroinsäure-Synthase 4. Bsp. Acetazolamid erhöht die Wasserausscheidung – ein schlechtes Medikament Labor: Sulfonamide hemmen Carboanhydrase (Anleitung auf http://fdchemie.pbworks) Zuerst wird das Enzym Carboanhydrase aus Schweineblut isoliert. Weil jeder Schritt erklärt werden kann, lohnt es sich die Vorschrift mit den Schülerinnen zu hinterfragen. Amadeus Bärtsch 29.5.2015 Fachdidaktik Chemie ETH Proteine & Medikamente S. 11 Carboanhydrase ist ein Enzym, das die Reaktion von Kohlendioxid mit Wasser beschleunigt: CO2 + H2O HCO3- + H+ + Dabei entsteht Hydrogencarbonat und H Nach der Isolation wird die Zeit bis zum Farbumschlag des Indikators Phenolrot gemessen. Das Medikament Acetazolamid hemmt die Carboanhydrase. Es dauert länger bis der Indikator die Farbe ändert. Carboanhydrase kommt in vielen menschlichen Zellen vor. Sie ist wichtig für die Rückresorption von Wasser in der Niere, erleichtert die Bildung von Kohlendioxid in der Lunge und anderes mehr. Mit dem Carboanhydrasehemmern soll mehr Wasser ausgeschieden werden. Acetazolamid wird bei Glaukom (Grünem Star) verschrieben, weil es den osmotischen Druck und damit die Wassermenge im Auge. Zudem wird es zur Vorbeugung der Höhenkrankheit eingesetzt. Bei der Höhenkrankheit bildet sich Wasser in der Lunge. Wie beim Glaukom verstärkt Acetazolamid auch hier die Wasserausscheidung. Es erhöht die Urinmenge, senkt den Blutdruck, steigert die Ausscheidung von Hydrogencarbonat, Kalium- und Natrium-Ionen und führt zu einer leichten Azidose. Wegen der vielfältigen Wirkung von Carboanhydrase führt die Hemmung zu einem Medikament mit Nebenwirkungen. Erwünscht ist die vermehrte Wasserausscheidung. Die andern Effekte müssen in Kauf genommen werden. Auch Sulfamethoxazol wird getestet: Dieses Sulfonamid hat keine Wirkung auf die Carboanhydrase. Sulfamethoxazol ist ein Medikament gegen bakterielle Infektionen. Es hemmt die Synthese von Folsäure und soll die Carboanhydrase nicht beeinflussen. Bei einer Bekämpfung der Infektion soll ja nicht der Blutdruck gesenkt werden. Die Resultate des Labors führen zum nächsten Abschnitt in dem mit den Skelettformeln der Medikamente gezeigt wird wie Nebenwirkungen verhindert werden können. Nebenwirkungen verhindern Der erste Satz zu Nebenwirkungen in meinem Pharmakologiebuch heisst: "Wenn behauptet wird, dass ein Medikament keine Nebenwirkungen zeigt, so besteht der dringende Verdacht, dass es auch keine Hauptwirkung hat." (G. Kuschinsky, zitiert aus E. Mutschler, Arzneimittelwirkungen, Wissenschaftliche Verlagsgesellschaft, Stuttgart, S. 73, 1986) Es lohnt sich den ausgezeichneten Aufsatz von John Emsley über die Risiken von Medikamenten zu lesen. (siehe "Nebenwirkungen.Emsley.doc" auf http://fdchemie.pbworks) Amadeus Bärtsch 29.5.2015 Proteine & Medikamente S. 12 Fachdidaktik Chemie ETH Im Menschen hemmen Sulfonamide die Carboanhydrase. In Bakterien unterbinden Sulfonamide die Bildung von Folsäure. Mit geeigneten Gruppen kann die Wirkung gesteuert werden: O H2N S H N passt nicht auf die Carboanhydrase N O O Sulfamethoxazol kaum Nebenwirkungen Wirkstoff von Bactrim Hemmung der FolsЉ uresynthese in Bakterien O NH2 S NH2 O Sulfanilamid wird nicht verkauft. Wegen Nebenwirkungen als Medikament unbrauchbar beeinflusst Bakterien nicht O N N H N O S S hemmt die Carboanhydrase: Wasser wird vermehrt ausgeschieden. Augendruck sinkt. Nebenwirkungen: - Blutdruck sinkt - mehr HCO3-, K+ & Na+ wird ausgeschieden - Azidose NH2 O Acetazolamid einige Nebenwirkungen NH O S S S O O O Dorzolamid kaum Nebenwirkungen Amadeus Bärtsch NH2 hemmt die Carboanhydrase im Auge. Augendruck sinkt, weil Wasser ausgeschieden wird keine weiteren Wirkungen, weil Dorzolamid auf das Auge getropft und nicht eingenommen wird 29.5.2015 Proteine & Medikamente S. 13 Fachdidaktik Chemie ETH Vorlage für ein Arbeitsblatt Nebenwirkungen verhindern Im Menschen hemmen Sulfonamide die Carboanhydrase. In Bakterien unterbinden Sulfonamide die Bildung von Folsäure. Mit geeigneten Gruppen kann die Wirkung gesteuert werden: O H2N S H N N O O Sulfamethoxazol O NH2 S NH2 O Sulfanilamid O N N O S S N H NH2 O Acetazolamid NH O S S S O NH2 O O Dorzolamid Amadeus Bärtsch 29.5.2015 Proteine & Medikamente S. 14 Fachdidaktik Chemie ETH Vorlage für ein Arbeitsblatt Sulfonamide gegen Bakterien Sulfonamide hemmen die ersten beiden Stufen der Synthese von Folsäure und damit das Wachstum von Bakterien. Auch Menschen können nicht ohne Folsäure auskommen. Im Unterschied zu den Bakterien nehmen Menschen Dihydrofolsäure aber mit der Nahrung auf. Sulfonamide wirken deshalb gezielt gegen Bakterien. H2 N N H N N COOH H2N OH N OH p-AminobenzoesЉ ure PABA Dihydropteridin H2 N N Enzym: DihydropteroinsЉ ure-Synthase H N COOH N N CH2 H2N + OH HN DihydropteroinsЉure H2 N N H N C CH2 CH2 COOH H COOH GlutaminsЉ ure Enzym: DihydrofolsЉ ure-Synthase N N CH2 OH HN O C H N COOH C CH2CH2 COOH H DihydrofolsЉ ure H2 N N Enzym: DihydrofolsЉ ure-Reduktase H N N OH CH2 N H HN TetrahydrofolsЉ ure Amadeus Bärtsch O C H N COOH C CH2 CH2 COOH H 29.5.2015