Radikalische Substitution
Werbung

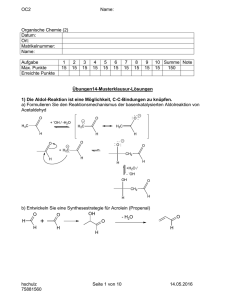
OC 2 Organische Chemie (II) für BC und T Übungen 1- Radikalische Substitution - Lösungen 1. In der Technik spielt die direkte Chlorierung von Methan in der Gasphase eine bedeutende Rolle. a. Formulieren Sie die Reaktion zum Chlormethan und beschreiben Sie den Reaktionsmechanismus und die Reaktionsbedingungen Siehe Skript Folie 18-24 b. Welche weiteren Reaktionsprodukte erwarten Sie? CH3Cl, CH2Cl2, CHCl3, CH3CH3, CH3CH2Cl u.a. c. Kommentieren Sie die Reaktivität der Halogene bezüglich obiger Umsetzung Siehe Skript Folie 25-26 2. Erklären Sie die unterschiedliche Stabilität von Methyl-, primären, sekundären und tertiären Alkylradikalen. Wie ist die räumliche Struktur? Die Stabilität nimmt in folgender Reihenfolge zu: Methyl-Radikal<primäres<sekundäres<tertiäres Radikal Je mehr Alkylgruppen an das Radikal-C-Atom gebunden sind, desto stabiler das Radikal. Grund: Hyperkonjugation. Struktur: zwischen sp3 und sp2-Hybrid (d.h. fast planar) 3. Radikale sind im allgemeinen sehr reaktiv. Es gibt aber auch recht stabile Radikale. a) Folgende Verbindungen werden als Initiatoren (Radikalbildner) für RadikalKettenreaktionen eingesetzt. Geben Sie die Reaktionsgleichung für den Zerfall dieser Verbindungen an. O O 2 O N NC CN N 2 NC + N2 b) Warum sind folgende Radikale bei Raumtemperatur überraschend stabil? Verwenden Sie zur Erklärung Grenzstrukturen. hschulz 68618547 Seite 1 von 46 14.05.2016 OC 2 H CH2 CH2 H CH2 H2C Resonanzstabilisierung c) Zu welcher Struktur dimerisiert das Triphenylmethylradikal? Beachten Sie, dass sich das Hexaphenylethan aus sterischen Gründen nicht bildet. H d) Bei radikalischen Kettenreaktionen kommt es früher oder später zu Kettenabbrüchen. Formulieren und benennen Sie die zwei wichtigsten Kettenabbruchreaktionen. Radikalkombination (Radikalrekombination): H2 C R CH2 2 R C R H2 Disproportionierung: hschulz 68618547 Seite 2 von 46 14.05.2016 OC 2 CH2 CH2 2 R + R R CH3 4) Diethylether, der schon jahrelang im Abzug steht, wird für eine Reaktion als Lösungsmittel eingesetzt. Beim Abrotieren gibt es eine heftige Explosion. Beschreiben Sie was geschah. Autoxidation: Siehe Skript Folie S. 38 5) Folgende Verbindungen werden durch radikalische Substitution monochloriert. Da radikalische Reaktionen meist nur wenig selektiv sind, müssen Sie ggf. mit Produktgemischen rechnen. Formulieren Sie das jeweils thermodynamisch stabilste Monochlorierungsprodukt CH3 H3C H3C CH2 CH3 CH4 H CH3 CH3 Cl H3C Cl hschulz 68618547 H3C Cl CH3 Seite 3 von 46 Cl 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 2 – Nucleophile Substitution - Lösungen 1) (R)-2-Chlor-3-methylbutan reagiert durch Hydrolyse mit Natronlauge zum entsprechenden Alkohol. a) Formulieren Sie das Geschwindigkeitsgesetz erster Ordnung und zweiter Ordnung für diese Reaktion und erklären Sie, wie Sie experimentell entscheiden können, nach welchem Gesetz die Reaktion abläuft. CH3 CH3 H H2O + NaOH + NaCl (R) Cl Geschwindigkeitsgesetz 1. Ordnung: Geschwindigkeitsgesetz 2. Ordnung: OH v = k [C5H11Cl] v = k [C5H11Cl] [OH-] Verdopplung der NaOH-Konzentration führt zu keiner Erhöhung der Reaktionsgeschwindigkeit SN1 Verdopplung der NaOH-Konzentration führt zu Verdopplung der Reaktionsgeschwindigkeit SN2 b) Wie würden Sie die Reaktionsbedingungen wählen, um obige Reaktion nach S N1 bzw. nach SN2 ablaufen zu lassen? Reaktionsbedingungen für SN1: - Lösungsmittel Wasser (Carbeniumion wird stabilisiert, OH- -Ion ist stark solvatisiert und damit weniger reaktiv) - keine Basenkatalyse, sondern im neutralen Bereich mit Wasser als Nucleophil arbeiten (schwaches Nucleophil kann nur Carbeniumion angreifen) Reaktionsbedingungen für SN2: - aprotisches, polares Lösungsmittel, z.B. Aceton (Carbeniumion wird weniger stabilisiert, OH- -Ion ist reaktiver) c) Zeichnen Sie die Strukturformeln der möglichen Produkte bei einer S N1- Reaktion bzw. einer SN2-Reaktion. Mögliche Produkte bei SN1-Reaktion: hschulz 68618547 Seite 4 von 46 14.05.2016 OC 2 CH3 CH3 OH H CH3 (S) (R) H OH OH Mögliche Produkte bei SN2-Reaktion: CH3 OH (S) H 2. (S)-2-Iodbutan reagiert in der Kälte mit Natrium-Methanthiolat (NaSCH3) a. Formulieren Sie den Reaktionsmechanismus SN2-Mechanismus siehe Skript Folie 47 b. Benennen Sie das Reaktionsprodukt einschliesslich absoluter Konfiguration CH3 CH3 S 2 N H I +NaSCH3 -NaI H3CS C2H5 C2H5 (S)-2-Iodbutan H (R)-2-Butylmethylsulfid 3) Die abgebildete enantiomeren-reine Milchsäure wird in zwei aufeinanderfolgenden SN2Reaktionen zuerst in 2-Chlorpropansäure und dann mit Azid (N3-) in 2-Azidopropion-säure umgewandelt. Die Azidopropionsäure wird mittels H2/Pt zum Alanin reduziert. a. Stellen Sie die Reaktionsfolge in der Fischerprojektion dar und bestimmen Sie die absolute Konfiguration der asymmetrischen C-Atome. COOH COOH COOH COOH HO H O H OH H NH2 Cl H H N3 OH (R)-Milchsäure (S)-2-Chlorpropionsäure (R)-2-Azidopropionsäure (R)-2-Amino propionsäure (D-Alanin) b. L-Alanin ((S)-Alanin) ist eine wichtige Chemikalie in biologischen Systemen. Wo kommt es vor? Kommentieren Sie warum die Wirksamkeit von Arzneimitteln oft stark von der absoluten Konfiguration abhängt. hschulz Seite 5 von 46 14.05.2016 68618547 OC 2 Vorkommen: Baustein der Proteine und Enzyme Aktive Zentren der Enzyme sind chiral. Während ein Enantiomer gut wechselwirken kann, passt das Spiegelbild evtl. nicht in das aktive Zentrum und kann sich folglich nur schlecht oder gar nicht an das Enzym anlagern. 4) Die Hydrolyse von t-Butylchlorid ergibt t-Butanol. a. Beschreiben Sie ausführlich den Reaktionsmechanismus - H+ + H2O - Cl- O Cl H OH H SN1 b. Zeichnen Sie für obige Reaktion ein detailliertes Energiediagramm (Energie/Reaktionskoordinate) mit allen Übergangszuständen und Zwischenprodukten ÜZ1 ÜZ3 ÜZ2 Cl O H H ZP1 O H H O H H ZP2 Cl OH 6. (R)-2-Chlor-3-hexen wird durch Wasser hydrolysiert. a. Formulieren Sie den Reaktionsmechanismus hschulz 68618547 Seite 6 von 46 14.05.2016 OC 2 H H H -ClCl (R)-2-Chlor-3-hexen H + +H2O, -H +H2O, -H+ H (R)-4-hexen-3-ol (R)-3-hexen-2-ol OH OH OH OH H (S)-4-hexen-3-ol H b. Erklären Sie anhand dieser Reaktion die Begriffe „thermodynamische Reaktionskontrolle“ und „kinetische Reaktionskontrolle“ (S)-3-hexen-2-ol Leider ist dies kein gutes Beispiel. c. Benennen Sie alle möglichen Reaktionsprodukte nach IUPAC einschliesslich absoluter Konfiguration Siehe a. hschulz 68618547 Seite 7 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 3- Eliminierung - Lösungen 1. Folgende Verbindung reagiert mit starken Mineralsäuren bei hoher Temperatur OH a. Welche Reaktionsprodukte erwarten Sie? -H2O +H+ OH2 OH Umlagerung -H+ -H+ -H+ Hauptprodukt: Saytzev -H+ (kin. kontr.) Nebenprodukt Hoffmann Zweithäufigstes Produkt: Saytzev b. Erklären Sie wie diese Produkte gebildet werden und kommentieren Sie die Mengenverhältnisse Siehe a. c. Obige Reaktion wird bei moderater Temperatur in Anwesenheit von Methanol durchgeführt. Wie beeinflusst dies das Ergebnis der Reaktion? hschulz 68618547 Seite 8 von 46 14.05.2016 OC 2 SN1, H+,CH3OH OH OCH3 Umlagerung SN1, H+,CH3OH OCH3 2) a) Formulieren Sie die Produkte, die durch Eliminierung von HCl aus folgenden Edukten entstehen Cl Verbindung 1 Cl Verbindung 2 b) Warum ist die HCl-Eliminierung aus Verbindung 1 thermodynamisch günstiger als aus Verbindung 2? Bildung eines konjugierten Diens = resonanzstabilisiewrungsenergie, delokalisierte Elektronen 3) trans-1-Methyl-2-tosyl-cyclohexan geht durch E2-Eliminierung in ein MethylcyclohexenDerivat über. Beschreiben Sie den Reaktionsmechanismus. Welches Derivat entsteht fast ausschliesslich? Begründen Sie Ihre Entscheidung mit Hilfe von NewmanProjektionen. CH3 O Ts = S O OTs E2 hschulz 68618547 Seite 9 von 46 14.05.2016 OC 2 H CH3 H CH3 H H OTs H OTs kein H in anti-Stellung zu OTs H in anti-Stellung zu OTs Mechanismus: siehe Skript S. 81 Reaktionsprodukt fast ausschliesslich 3-Methyl-cyclohexen: trans-ständiges H steht anti zur Tosylgruppe. Dies ist für eine E2-Eliminierung Voraussetzung. 4) 2-Chlor-3-methylbutan wird bei erhöhter Temperatur mit Kalium-t-butanolat umgesetzt. a) Welches Hauptprodukt erwarten Sie? CH3 CH3 H + KCl + HO + K O Cl b) Beschreiben Sie zwei mögliche Reaktionsmechanismen zur Bildung des Hauptprodukts. E1-Mechanismus: CH3 CH3 H H + Cl - H H Cl CH3 CH3 H + HO + O H E2-Mechanismus: hschulz 68618547 Seite 10 von 46 14.05.2016 OC 2 O H CH3 H - + Cl + HO H3C Cl c) Durch Eliminierung von Wasser aus 3,3-Dimethyl-2-butanol entsteht nicht das erwartete 3,3-Dimethyl-1-buten, sondern das 2,3-Dimethyl-2-buten. Erklären Sie, wie dieses Produkt entsteht. H OH +H+/ -H2O H -H+ H Umlagerung durch Wanderung einer CH3-Gruppe 5) Beschreiben Sie den Mechanismus einer -Eliminierung anhand eines Beispiels siehe Skript Folie 99 hschulz 68618547 Seite 11 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 4- Addition an die CC-Doppelbindung - Lösungen 1) Brom addiert bereits bei Raumtemperatur an (Z)-1-Chlorpropen a. Beschreiben Sie den Mechanismus der Addition H H Cl CH3 Siehe Skript Folie 117 b. Benennen Sie das Reaktionsprodukt nach IUPAC einschliesslich absoluter Konfiguration (1S), (2R)-1,2-Dibrom-1-chlorpropen und (1R), (2S)-1,2-Dibrom-1-chlorpropen 2) Geben Sie Reaktionsgleichungen an für die Herstellung von vicinalen und von geminalen Dihalogenen. X + X2 X + HX X H + HX X X H H 3) Durch Additionsreaktionen kann man aus Alkenen Alkohole herstellen Beschreiben Sie den Reaktionsmechanismus der säurekatalysierten Addition von Wasser an Propen H H H +H+ +H2O -H+ O + O H H + H 4) Durch Hydroborierung ist aus Propen 1-Propanol darstellbar. Formulieren Sie die Reaktion unter Verwendung von Dicyclohexylboran hschulz 68618547 Seite 12 von 46 14.05.2016 OC 2 B H B 2 2 H H +H2O2 H H HO + B OH 5) Alkene reagieren mit Halogenen normalerweise unter elektrophiler Addition. a) Bei der Umsetzung von Isobutylen (2-Methylpropen) mit Cl2 entsteht nicht das erwartete 1,2-Dichlor-2-methylpropan als Hauptprodukt, sondern 3-Chlor-2-methyl-1-propen und HCl. Erklären Sie, wie dieses Produkt entsteht. H3C - + Cl-Cl / - Cl H3C Cl Cl Cl H3C Cl -H+ - + Cl Cl + Das Chloronium-Ion stabilisiert sich durch Abspaltung von H und nicht durch Addition von Cl . Grund ist die sterische Hinderung am tertiären C-Atom. b) Pent-1-en-4-in wird mit einem Äquivalent Br2 umgesetzt. Welches Hauptprodukt entsteht? Warum? Br + Br2 + Br Br Br Hauptprodukt: Doppelbindung wird leichter elektrophil angegriffen! 6) Acrylnitril reagiert mit Ethanol unter Basenkatalyse (Natriumethanolat). a) Formulieren Sie den Reaktionsmechanismus. hschulz 68618547 Seite 13 von 46 14.05.2016 OC 2 H C H H O N H C H H H C2H5 H N C N H H C N H +C2H5OH OC2H5 H -C2H5OOC2H5 H b) Erklären Sie die Regioselektivität der Reaktion anhand von Resonanzformeln Resonanzformel siehe a. Positive Partialladung am C3-Atom c) Das Reaktionsprodukt wird in verdünnter Säure erhitzt. Was entsteht? 3-Ethoxy-propansäure 8) Die AE von HBr an die Doppelbindung führt zum Markovnikov-Produkt. Nennen Sie zwei Synthesemethoden um aus 1-Alkenen 1-Bromalkane herzustellen und formulieren Sie die Reaktionsmechanismen AR siehe Skript Folie 135 Hydroborierung Folie 166 9) Aus Acetylen kann Acetaldehyd hergestellt werden. Beschreiben Sie den Mechanismus. Siehe Skript Folie S. 160 hschulz 68618547 Seite 14 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 8-Diels-Alder - Lösungen 1) Die Diels-Alder-Reaktion ist eine wichtige Reaktion in der Organischen Chemie zum Aufbau von komplexen Strukturen. c. Beschreiben Sie das Diels-Alder-Reaktionsprodukt aus folgenden Edukten. O O H H H + O O H O O d. Wie ist die Lage der beiden H-Atome des Maleinsäureanhydrids im Endprodukt cis oder trans? Begründen Sie Ihre Entscheidung. cis, konzertierte syn-Addition, [4+2]-Cycloaddition c. Aus welchen Edukten ist folgendes Diels-Alder-Produkt entstanden? CN CN NC CN + CN NC CN CN 2. a. Formulieren Sie den Mechanismus der Reaktion von p-Chinon (siehe Formel) mit zwei Äquivalenten Butadien O O O O b. Wie nennt man solche Reaktionen und unter welchen Reaktionsbedingungen finden sie statt? Diels-Alder-Reaktion: [2+4]-Cycloaddition, konzertierte syn Addition Reaktionsbedingungen: höhere Temperatur, ggf. Druck hschulz 68618547 Seite 15 von 46 14.05.2016 OC 2 c. Zeichnen Sie für Butadien und Ethen die Grenzorbitale (HOMO/LUMO) und beschreiben Sie, welche Orbitale gemäss obigem Reaktionsmechanismus mit einander wechselwirken. LUMO HOMO hschulz 68618547 Seite 16 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 6 – aromatische Substitution - Lösungen 1) Die Friedel-Crafts-Alkylierung wird durch katalytische Mengen an AlCl3 ermöglicht. Bei der Acylierung werden hingegen mindestens äquimolare Mengen benötigt. Warum? Bildung eines Komplexes zwischen AlCl3 und dem Reaktionsprodukt. Dieser Komplex muss später durch Hydrolyse gespalten werden (giessen auf Eiswasser). Cl3Al O C R 2) Formulieren Sie den Eliminierungs-Additions-Mechanismus der Reaktion von Chlorbenzol zu Anilin Siehe Skript Folie 231 3) Beschreiben Sie eine Möglichkeit Phenol herzustellen Siehe Skript Folie 234 4) Betrachten Sie folgende Strukturen. a) Wie ist die Reaktivität gegenüber Brom? Begründung Benzol: aromatisch, SE, Reaktion nur mit Katalysator, Rückbildung des aromatischen Systems Cyclopentadien: AE, Reaktion spontan bei RT, Addition führt zum energieärmeren Produkt im Vergleich zur möglichen Substitution. b) Welches Hauptprodukt entsteht , wenn Cyclopentadien mit einem Äquivalent Brom reagiert? 3,5-Dibromcyclopenten: 1,4-Addition am konjugierten System 5) Anilin ist ein wichtiger Grundstoff in der Farbstoffchemie a) Beschreiben Sie zwei Wege zur Darstellung von Anilin aus Benzol hschulz 68618547 Seite 17 von 46 14.05.2016 OC 2 1. Weg: Elektrophile aromatische Substitution (Nitrierung) gefolgt von einer Reduktion NH2 NO2 + NO2+/-H+ Fe, HCl Reduktion 2. Weg: Elektrophile aromatische Substitution (Chlorierung) zum Chlorbenzol gefolgt von einer nucleophilen Substitution mit NaNH2 nach einem Additions-/EliminierungsMechanismus NH2 Cl + Cl2/FeCl3/-HCl + NH2-, +H+ -HCl b) Für eine elektrophile Zweitsubstitution stehen im Anilin grundsätzlich 3 Positionen zur Verfügung. Wo wird die Zweitsubstitution bevorzugt stattfinden? NH2 ortho para hschulz 68618547 Seite 18 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 7 – Metallorganische Reagenzien-Lösungen 1) Beschreiben Sie die Grignard-Reaktion von Methylbromid und Formaldehyd Reaktionsgleichungen: CH3Br + Mg H3CMgBr H H3CMgBr + O H3C CH2 OMgBr H3C CH2 OH + MgBr(OH) H H3C CH2 OMgBr + H2O Mechanismus siehe Skript Folie S. 242 2) Methyllithium ist eine metallorganische Verbindung a) Beschreiben Sie eine Synthesemöglichkeit Siehe Skript Folie 243 b) Vergleichen Sie die Methyl-Alkalimetallverbindungen bezüglich der Reaktivität Zunehmender ionischer Charakter vom MeLi zum MeCs. Deshalb zunehmende Reaktivität, aber abnehmende Löslichkeit in unpolaren bzw. polaren aprotischen Lösungsmitteln c) Wie können Sie die Konzentration einer MeLi-Lösung bestimmen? H3CLi + H2O CH4 + LiOH LiOH kann mit einer HCl-Masslösung titriert werden 3) Grignard-Reaktionen sind wichtige metallorganische Reaktionen zur Knüpfung neuer CC-Bindungen. a) Beschreiben Sie ausführlich die Grignard-Reaktion von 1-Brombutan mit Formaldehyd (Reaktionsmechanismus und Reaktionsgleichung) Br + Mg Ether Mg Br H2C H H O MgBr+ MgBr+ O + H2O OH + MgBr(OH) Reaktionsgleichung: hschulz 68618547 Seite 19 von 46 14.05.2016 OC 2 H H Br + Mg + O + H2O Ether OH + MgBr(OH) b) Wie kann man durch Grignard-Reaktion sekundäre und tertiäre Alkohole darstellen ? Formulieren Sie allgemeine Reaktionsgleichungen. Sekundäre Alkohole: H R´ R´ Ether + MgBr(OH) R X OH + Mg + O + H2O R H Tertiäre Alkohole: R´ R X + Mg + hschulz 68618547 O R´´ + H2O Ether R´ OH + MgBr(OH) R R´´ Seite 20 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 10 - Carbonylgruppe-Lösungen 1. Ketone und Aldehyde stehen mit ihrer Enol-Form im Gleichgewicht a. Beschreiben Sie den Reaktionsmechanismus der säurekatalysierten Enolisierung H R H R H +H+ R O O R H H H H -H+ R + O H R OH b. Auf welcher Seite liegt das thermodynamische Gleichgewicht bei Raumtemperatur im Acetaldehyd? O OH H H c. Formulieren Sie die Enol-Form von 2,4-Pentandion und kommentieren Sie die Gleichgewichtslage. O O OH O Gleichgewicht liegt auf seiten des Enols, da im Enol ein konjugiertes System vor liegt 2. Folgende Carbonylverbindung hat vier reaktive Zentren a. Kennzeichnen Sie die reaktiven Zentren (z.B. mit einem Pfeil) und beschreiben Sie, wie diese Zentren angegriffen werden können (z.B. durch ein Nucleophil, ein Elektrophil, eine Base oder eine Säure) elektrophiler Angriff elektrophiler Angriff O H3C CH2 C nucleophiler Angriff Angriff durch Base am acidenWasserstoff (C-H-Acidität) hschulz 68618547 Seite 21 von 46 14.05.2016 OC 2 b. Aus obiger Verbindung (siehe 5.a.) kann folgende Verbindung dargestellt werden. Formulieren Sie den Reaktionsmechanismus eines möglichen Synthesewegs. O Na +NaH/-H2 H3C CH2 C + O H3C CH C O Br H3C CH C SN2 -NaBr CH2 CH3 3. Phthalsäure geht bei ca. 230°C in das cyclische Phthalsäureanhydrid über a. Formulieren Sie die Reaktionsgleichung O COOH -H2O O +H2O COOH O b. Erklären Sie warum Terephthalsäure kein cyclisches Anhydrid bildet HOOC COOH Cyclisches Anhydrid ist aus der 1,4-Position nicht möglich! c. Formulieren Sie den Reaktionsmechanismus der säurekatalysierten Veresterung von Essigsäure mit Propanol Mechanismus für die säurekatalysierte Veresterung und Esterhydrolyse Schritt 1: Protonierung der Carboxygruppe O R C OH H+ +H O R C OH H O H O R C OH R C + O H + H-O-R R C OH Schulz, OC2ht-WS01-02.ppt hschulz 68618547 R C OH +O H R - H+ Schritt 3: Wasserabspaltung + OH O H R C OH O R Tetraedrisches Zwischenprodukt 257 O H H R C O+ H O R O H R C OH Schritt 2: Nucleophiler Angriff durch Alkohol + H O O R +H O +H+ -H+ H O -HOH +HOH O -H+ +H+ R C O R R C O R + Additions-Eliminierungs-Reaktion: Addition von Alkohol gefolgt von Eliminierung von Wasser R C O R Schulz, OC2ht-WS01-02.ppt Seite 22 von 46 258 14.05.2016 OC 2 4. Acylhalogenide können leicht in verschiedenste Carbonsäure-Derivate überführt werden a. Nennen Sie eine mögliche Methode zur Darstellung von Acetylchlorid und formulieren Sie die Reaktionsgleichung O O 3 PCl3 + 3 + H3PO3 OH Cl b. Welche Produkte entstehen bei folgenden Umsetzungen? Reaktion Produkt Produkt Strukturformel IUPAC-Name O Acetylchlorid + Ethanol Ethansäureethylester O Acetylchlorid + Ammoniak O Ethansäureamid NH2 Acetylchlorid + Dimethylamin O N,N-Dimethylethansäureamid N Acetylchlorid + Natriumpropanoat O O Ethansäurepropansäureanhydrid O 5) Die Carbonylgruppe im Acetaldehyd kann nucleophil angegriffen werden. a) Beschreiben Sie die Reaktion von Acetaldehyd mit einem Überschuss an Ethanol im saueren Milieu. hschulz 68618547 Seite 23 von 46 14.05.2016 OC 2 O O + H+ -H+ O O O + HOC2H5 H H C2H5 OC2H5 + H+ OH C H OC2H5 O H O H H -H+ H + HOC2H5/-H2O C2H5 OH C H H H H H C2H5 H OC2H5 H OC2H5 b) Zu welchen Verbindungsklassen gehören das Produkt und evtl. auftretende Zwischenprodukte? Zwischenprodukt: Halbacetal Endprodukt: Acetal c) Welche Produkte entstehen bei der Umsetzung von Acetaldehyd mit folgenden Aminen? Amin Struktur des Produkts Verbindungsklasse H3C N CH3 H3CNH2 Imin H N(CH3)2 H (H3C)2NH Enamin H H (H3C)3N keine Reaktion - 6) Acetaldehyd wird mit einem Überschuss an Ethanolumgesetzt. Beschreiben Sie den Reaktionsmechanismus unter folgenden Reaktionsbedingungen: a) im basischen Milieu hschulz 68618547 Seite 24 von 46 14.05.2016 OC 2 Mechanismus für die basenkatalysierte Halbacetal-Bildung Schritt 1: Nucleophiler Angriff von OR- am Carbonyl-C-Atom R RO OR- C O R R´ R´ - C O Schritt 2: Übertragung eines Protons vom Alkohol auf das Alkoxid-Ion unter Rückbildung des Katalysators RO R RO - H-OR C O C O H + OR- R R´ R´ hschulz, OC2ht-SS-02.ppt 253 b) im saueren Milieu Säurekatalysierte Halbacetal-Bildung und Weiterreaktion zum Acetal Schritt 1: R Elektrophiler Angriff von H+ am Carbonyl-O-Atom H-OH2+ C O R´ R R´ C O H R R´ C O H + RO H-OH2+ C O H R´ H R R´ C O R hschulz, OC2ht-SS-02.ppt -HOH + R R´ Schritt 5: R R´ R´ S N1 R´ Deprotonierung unter Bildung des Halbacetals C O R 256 C O H + H3O+ R R´ + 255 Nucleophiler Angriff von Alkohol am Carbenium-C-Atom + H R O R C O R R´ H-O-R C O R Schritt 6: + H R O R C O R R´ + RO H-O-H hschulz, OC2ht-SS-02.ppt + C O H R Schritt 3: Nucleophiler Angriff von Alkohol am Carbenium-C-Atom + H R O H-O-R R C O H H + H R O R C O H R´ Schritt 4: Elektrophiler Angriff von H+ an der OHGruppe des Halbacetals und Abstraktion von H2O R + C O + 254 RO Schritt 2: R R´ hschulz, OC2ht-SS-02.ppt hschulz, OC2ht-SS-02.ppt Deprotonierung unter Bildung des Acetals H-O-H RO R C O R + H3O+ R´ 257 7) Formulieren Sie die Reaktionsgleichungen für die Umsetzung von Propanal mit folgenden Aminen und benennen Sie die Verbindungsklassen der Produkte: a) Amoniak Analog Skript: Imin-Bildung CH3CH2CHO + NH3 CH3CH2CH=NH + H2O b) Methylamin Analog Skript: Imin-Bildung CH3CH2CHO + H2NR CH3CH2CH=NR + H2O hschulz Seite 25 von 46 68618547 14.05.2016 OC 2 c) Dimethylamin Analog Skript: Enamin-Bildung CH3CH2CHO + HNR2 CH3CH=CHNR2 + H2O 8) Bestimmte Hydroxycarbonsäuren reagieren intramolekular zu Lactonen a) Welche Hydroxycarbonsäuren reagieren besonders leicht zu Lactonen? Warum? OH R COOH COOH R OH -Hydroxycarbonsäure ergibt einen 6-Ring -Hydroxycarbonsäure ergibt einen 5-Ring b) Beschreiben Sie den Reaktionsmechanismus der intramolekularen Veresterung von -Hydroxypentansäure. H O O + +H H3C H3C OH OH OH OH OH OH OH OH2 H3C O OH + +H + O H3C OH -H O H3C -H2O H H O H3C O -H + O H3C O c) Was entsteht aus folgenden Verbindungen durch intramolekularen Ringschluss (Name der Verbindungsklasse und Struktur): 4-Aminobutansäure hschulz 68618547 Seite 26 von 46 14.05.2016 OC 2 H2N COOH -H2O O N H Lactam Diammoniumsalz der Bernsteinsäure O COO- NH4+ - NH3, - H2O NH COO- NH4+ Imid O Maleinsäure O COOH - H2O O COOH Anhydrid O 9) Carbonylverbindungen sind C-H-acide. a) Beschreiben Sie den Reaktionsmechanismus der basenkatalysierten Aldolreaktion von Acetaldehyd mit Benzaldehyd hschulz 68618547 Seite 27 von 46 14.05.2016 OC 2 O O - + OH / -H2O H3C O H2C H2C H H H O O O + H2C O Ph CH2 H H H H +H2O / - -OH O OH H Ph - H2O O CH2 H H b) Acetessigester wird aus Essigsäureethylester unter Alkoholabspaltung hergestellt (Claissen-Kondensation). Beschreiben Sie den Mechanismus. + -OC2H5 / O - HOC2H5 H3C O H2C H2C OC2H5 OC2H5 O OC2H5 O + H3C O O H2C OC2H5 O H3C CH2 OC2H5 OC2H5 OC2H5 - -OC2H5 - O + OC2H5 / O O - HOC2H5 H3C hschulz 68618547 C H OC2H5 Seite 28 von 46 H3C O C H2 OC2H5 14.05.2016 OC 2 c) Vinylmethylketon wird unter Basenkatalyse mit Wasser hydrolysiert. Beschreiben Sie den Reaktionsmechanismus und benennen Sie das Reaktionsprodukt. H OH H O O + H2O / - OH H H + -OH HO HO H H O H HO H (2-Hydroxyethyl)methylketon 10) Phosgen (COCl2) dient als Edukt für viele Kohlensäurederivate. a) Formulieren Sie die Reaktionsgleichungen für die Herstellung folgender Produkte OC2H5 O COCl2 + 2 C2H5OH OC2H5 2 HCl + NH2 O COCl2 + 2 NH3 NH2 2 HCl + OC2H5 O COCl2 + C2H5OH + H2NCH3 2 HCl + NHCH3 b) Kohlensäurederivate, die OH-Gruppen enthalten sind instabil. Formulieren Sie die Reaktionsgleichung für den Zerfall folgender Verbindungen. OH O OH OH CO2 + H2O OR CO2 + HOR O hschulz 68618547 Seite 29 von 46 14.05.2016 OC 2 OH O NH2 CO2 + NH3 c) Im Jahre 1828 hat Herr Wöhler Ammoniumcyanat erhitzt und damit ein Dogma umgestossen. Formulieren Sie die Reaktionsgleichung. Warum war das eine so wichtige Entdeckung? NH2 NH4+ OCNO NH2 Aus einer anorganischen Verbindung wurde erstmals eine organische Verbindung hergestellt. Dies war ein Beweis gegen die sog. Vitalismus-Theorie. 11) Milchsäure kann aus einem Cyanhydrin hergestellt werden a) Beschreiben Sie wie das entsprechende Cyanhydrin hergestellt werden kann b) Wie reagiert das Cyanhydrin zur Milchsäure? Siehe Skript Folie 283.285. Als Carbonylverbindung wird Acetaldehyd eingesetzt 12) Formaldehyd liegt in wässeriger Lösung als geminales Diol vor. Das Diol kann aber nicht isoliert werden. a) Beschreiben Sie den Mechanismus der Wasseraddition an die Carbonylgruppe. Siehe Skript Folie 265 b) Welche geminalen Diole sind stabil? Warum? Siehe Skript Folie 264, Die –I-Substituenten erzeugen eine grosse positive Partialladung am Carbonyl-C-Atom. Der Wasserangriff wird dadurch erleichtert. 13) Cyclische Acetale werden oft als Schutzgruppen eingesetzt a) Erklären Sie den Mechanismus der Bildung des cyclischen Acetals aus Benzaldehyd und Glycol b) In welchem Milieu kann die Schutzgruppe verwendet werden und warum? Siehe Skript Folie 276. Schutzgruppe ist im basischen Milieu stabil, im sauren Milieu findet die Rückreaktion zum Aldehyd statt. hschulz 68618547 Seite 30 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 5-Wittig-Ozonolyse-Lösungen 1. Durch Ozonolyse kann die Lage von Doppelbindungen bestimmt werden. Beschreiben Sie den Mechanismus am Beispiel des Zimtsäureethylesters. Siehe Skript Folie S. 154 2. Beschreiben Sie die Synthese von 2-Methyl-1,1-diphenylpropen mit Hilfe der WittigReaktion Siehe Skript Folie 288 3).Beschreiben Sie den Mechanismus der Wittig-Reaktion am Beispiel der Edukte Brommethan und Diphenylketon H (C6H5)P H + 3P Br H 3P C C H H 3 P Ph H H O C Ph 3P C H C H H Br Ph H Ph O C +BuLi/-Bu-H,-LiBr Ph O 3P H + C Ph C H H 4) Styrol kann aus den unten aufgeführten Edukten hergestellt werden. Beschreiben Sie den Reaktionsmechanismus. Beachten Sie, dass neben den aufgeführten Edukten weitere Edukte benötigt werden könnten. Wie nennt man diese Reaktionen? H H Br H H a. HO- E2 H H Br H2O + + Br- H H hschulz 68618547 Seite 31 von 46 14.05.2016 OC 2 H Br CH3 O b. Wittig-Reaktion H (C6H5)P H + Br H 3P C 3P C Ph H H H 3 P O C Ph 3P C H H H C H H Br H H H O C +BuLi/-Bu-H,-LiBr H O 3P + C Ph C H H 5) Aus Isoeugenol wird durch Ozonolyse Vanillin hergestellt. Beschreiben Sie den Reaktionsmechanismus OH OCH3 OH C H OCH3 CH3 C H Isoeugenol hschulz 68618547 =R Seite 32 von 46 14.05.2016 OC 2 O O O O R - 78°C CH3 H H CH3 H O H hschulz 68618547 O O + R CH3 H H Primärozonid R O O O R H R O CH3 H O H CH3 O O Sekundärozonid Reduktion H Seite 33 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 11-Amine: Nitrosierung-Azokupplung-Lösungen 2. Ein Labormitarbeiter setzt im saueren Milieu Dimethylamin mit NaNO2 um. Das Reaktionsgefäss fällt versehentlich auf den Boden. Der Laborleiter lässt sofort das ganze Labor evakuieren. a. Warum? Das Reaktionsprodukt Dimethyl-N-Nitrosamin ist krebserregend b. Erstellen Sie die Reaktionsgleichung obiger Umsetzung. H3C H3C H + NaNO2 + HCl N H3C N NO + H2O + NaCl H3C c. Welches Reaktionsprodukt entsteht bei der Oxidation von Trimethylamin mit Wasserstoffperoxid? CH3 H3C N CH3 O Trimethylaminoxid 3. Anilin reagiert mit dem Nitrosonium-Ion zum Diazonium-Ion. a. Beschreiben Sie den Reaktionsmechanismus der Bildung des Nitrosonium-Ions und des Diazonium-Ions. hschulz 68618547 Seite 34 von 46 14.05.2016 OC 2 H O N O H Ph H +H3O+/-H2O H -H2O O N H N O Ph N N H N O +H2O/-H3O+ N N O H Ph N N N O N N +H3O+/-H2O OH H H + +H3O /-H2O N Ph O H H +H2O/-H3O+ N O H Ph Ph N O Ph OH N N O -H2O N H N b. Methylorange (siehe Formel) wird durch Diazokupplung hergestellt. Beschreiben Sie die Kupplungsreaktion und benennen Sie den Reaktionsmechanismus. O HO S N N N N N(CH3)2 -H+ O O HO S + H N(CH3)2 O SN(Ar) 3) Amine reagieren mit dem Nitrosonium-Ion. a) Beschreiben Sie Mechanismus und Reaktionsprodukt der Reaktion von Diethylamin mit NO+. C2H5 C2H5 H C2H5 - H+ + N NO N NO N H + NO C2H5 C2H5 C2H5 b) Formulieren Sie die Reaktionsgleichungen der Reaktionen folgender Amine mit NaNO 2 / HCl: H2NC2H5 H5C2NH2 + NaNO2 + 2 HCl hschulz 68618547 C2H5 N Seite 35 von 46 - N Cl + NaCl + 2 H2O 14.05.2016 OC 2 N(C2H5)3 C2H5 C2H5 C2H5 N + NaNO2 + 2 HCl C2H5 C2H5 hschulz 68618547 N NO Cl + H2O + NaCl C2H5 Seite 36 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 9 - Synthesestrategien-Lösungen 3. Entwickeln Sie eine Synthesestrategie für folgende Aromaten ausgehend von Benzol: a. p-Chloranilin a1: Nitrierung von Benzol, Reduktion zum Anilin, Monohalogenierung a2: Chlorierung von Benzol zum 1,4 Dichlorbenzol, SN mit einem Äquivalent Amid b. m-Nitrobenzoesäure Nitrierung von Benzol, FC-Alkylierung in meta-Stellung, Oxidation c. o-Nitrobenzoesäure FC-Alkylierung von Benzol zum Toluol, Nitrierung in o-Stellung, Oxidation d. 2-Brom-4-cyano-benzolsulfonsäure Monobromierung von Benzol, SN mit Cyanid zum Benzonitril, Bromierung in mStellung, Sulfonierung in o-Stellung zum Brom 2) Entwickeln Sie für folgende Produkte eine Synthesestrategie, ausgehend von den genannten Edukten. Edukt: Toluol Produkt: CH3 CH3 CH3 CH3 CH3 Br NO2 Edukt: Benzol NH2 Br Br NH2 Br N2 Br Produkt: CH3 Edukt: Benzol hschulz 68618547 Br COOH Produkt: Seite 37 von 46 14.05.2016 OC 2 Cl OH OH O2N NO2 NO2 Edukt: keine SR! H Produkt: Br H Br Br +2 Br2 -2 HBr H H Br Br Br H Edukte: zwei Aldehyde H + O Produkt: H O O H3C H H H 3) Entwickeln Sie für folgende Produkte eine Synthesestrategie, ausgehend von den genannten Edukten. Bemerkung: Zeichnen Sie die Strukturen der einzelnen Vorstufen und geben Sie stichwortartig an, welche Reaktionen Sie durchführen wollen. Die Beschreibung des Reaktionsmechanismus ist nicht erforderlich. Edukt: Benzol Produkt: Benzylchlorid CH3 CH2Cl FC-Alk. SR,Cl2,h Edukt: Benzol hschulz 68618547 Produkt: p-Nitroanilin Seite 38 von 46 14.05.2016 OC 2 H2N NO2 SN, NH3 oder NH2 Cl HNO3/H2SO4 NO2 Cl Cl2/FeCl3 Edukt: Benzol Produkt: p-Phenolsulfonsäure (p-Hydroxybenzolsulfonsäure) HO HO SN, NaOH SO3H SE, H2SO4/SO3 Cl SE, Cl2/FeCl3 Edukt: Benzol Produkt: Benzophenon O O + Cl FC-Ac. Edukt: Benzol Produkt: m-Phenylendiamin (m-Diaminobenzol) NH2 NO2 Fe/HCl SE, HNO3/H2SO4 NO2 hschulz 68618547 Seite 39 von 46 NH2 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 12 - Polymere-Lösungen 1) Styrol kann auf mehreren Wegen polymerisiert werden a) Beschreiben Sie den Reaktionsmechanismus der anionischen Polymerisation von Styrol Mechanismus der anionischen Polymerisation Startreaktion (Initiierung) Li+ Bu- + H2C=CHR - Bu-H2C-CHR + Li+ Kettenwachstum - Bu-H2C-CHR + n H2C=CHR Bu (CH2-CHR )nCH2-CHR Schulz, OC2ht-WS01-02.ppt 324 b) Beschreiben Sie typische Reaktionsbedingungen für die anionische Polymerisation und kommentieren Sie mögliche Kettenabbruchreaktionen Tiefe Temperaturen (ca. 0°C), sehr reine Edukte. Abbruch nur durch Verunreinigungen oder durch gezielten Zusatz von z.B. Wasser, Ammoniak, Alkohol, Kohlendioxid c) Was versteht man unter einem lebenden Polymer? Das kettenende des Polymers enthält noch die reaktive Gruppe, die mit weiterem Monomer zu längeren Ketten reagieren kann 2) Polyvinylether werden durch kationische Polymerisation hergestellt. a) Nennen Sie typische Initiatoren für die kationische Polymerisation. - starke Mineralsäuren: HClO4, H2SO4, HI - starke Säuren mit grossen sperrigen Anionen: F3C-(C6H4)-SO3H - Lewis-Säuren mit Spuren von Wasser b) Beschreiben Sie typische Bedingungen, damit ein Alken polymerisiert und nicht unter elektrophiler Addition mit dem Initiator reagiert. - geringe Konzentrationen des Initiators - keine nucleophilen Lösungsmittel - sehr reine Edukte - tiefe Temperaturen (< 0°C) c) Beschreiben Sie die Startreaktion, die Kettenwachstumsreaktion und eine Kettenabbruchreaktion der kationischen Polymerisation von Methyl-vinyl-ether. Startreaktion: hschulz 68618547 Seite 40 von 46 14.05.2016 OC 2 OCH3 H H2SO4 H H + OCH3 H H Kettenwachstum: HSO4- + C H H OCH3 OCH3 H H OCH3 C OCH3 H + H H H Kettenabbruch: OCH3 OCH3 H H H H H H H H OCH3 OCH3 C H3C C H3C C HSO4- + H H3C H SO4H H H H 3) a) Beschreiben Sie den Mechanismus der radikalischen Polymerisation von Styrol analog OC2-Skript S. 364 RO CH2CH2 mOR Mechanismus der radikalischen Polymerisation 2 RO CH2CH2 nCH2 CH2 Initiierung (Kettenstart) RO OR R O + H2C CH2 RO CH2CH2 n CH2 CH3 + RO CH2CH2 2 R O ROCH2 CH2 Kettenverzweigung +R Kettenwachstum ROCH2 CH2 + H2C CH2 Kettenabbruch CH2 CH CH2 -R-H H H CH2 C CH2 CH2 ROCH2CH2CH2 CH2 +(n-1) H2C CH2 RO CH2CH2 n CH2CH2 hschulz, OC2ht-SS-02.ppt n CH CH2 H CH2 C CH2 + H2C CH2 H2C 395 hschulz, OC2ht-SS-02.ppt 396 b) Nennen Sie vier Reaktionsmechanismen (nur die Namen!) zur Polymersiation von Alkenen - radikalische Polymerisation - anionische Polymerisation - kationische Polymerisation - Übergangsmetall-Katalyse (z.B. Ziegler-Natta) c) Beschreiben Sie an einem beliebigen Beispiel den Reaktionsmechanismus einer Polykondensation hschulz 68618547 Seite 41 von 46 14.05.2016 OC 2 Polypeptide Die Polyester-Synthese -Aminosäuren bilden unter Polykondensation Polypeptide (Proteine) H R1 H H R2 H O + N C C OH H H H O N C C H - 3 H2O N C H H C R2 O N C H H C H + R3 n R´ OH O H OH O O HO - (n-1) H2O OH C R C O R´ O H n PET: Polyethylenterephthalat Polykondensat aus Terephthalsäure und Ethylenglycol O N C C OH H H HO Tripeptid hschulz, OC2ht-SS-02.ppt C O R1 O R HO -Aminocarbonsäuren H C N C C + OH R3 O O n O O C C O O H n 425 hschulz, OC2ht-SS-02.ppt 427 Mechnanismus: Addition-Eliminierung hschulz 68618547 Seite 42 von 46 14.05.2016 OC 2 Organische Chemie (II) für BC und T Übungen 13 – Verschiedenes - Lösungen 1) Vervollständigen Sie folgende Tabelle. Bitte nennen Sie durchschnittliche, ungefähre Werte Bindung Bindungsenergie (kj/mol) Bindungslänge (pm) C-H 380-440 108-111 C-C 350-380 150-154 C=C 600 133 C-C-Dreifach 840 121 C-Cl 355 178 2) Erklären Sie kurz folgende Begriffe Begriff Erklärung Basizität Thermodynamische Gleichgewichtslage der Reaktion: B + H+ → BH+ Polarisierbarkeit Konstitutionsisomerie Homopolymer Block-Copolymer Makromolekulares Netzwerk Mass für die Verschiebbarkeit von Elektronen in einem Atom oder Molekül Gleiche Summenformel, unterschiedliche Konnektivität Polymer, das aus nur einer Monomer-Sorte aufgebaut ist: AAAAAAAAAAAAAA AAAAAABBBBBBBAAAAAAABBBBBB Thermodynamisch kontrollierte Reaktion Lineare oder verzweigte Polymerketten sind untereinander verknüpft, so dass riesige dreidimensionale Gebilde entstehen Es entsteht das thermodynamisch günstigste Reaktionsprodukt: Die Reaktion ist maximal exotherm. Kinetisch kontrollierte Reaktion Es entsteht das reaktionsprodukt, das die kleinste Aktivierungsenergie benötigt (der einfachste Weg!) -I-Effekt Elektronenziehender Effekt aufgrund von EN-Unterschieden. Er wirkt nicht nur auf das unmittelbar benachbarte Atom, sondern über bis zu 4 Bindungen Monomolekulare Substitution. Der geschwindigkeitsbestimmende Schritt hängt nur vom Zerfall eines Edukts in ein Carbeniumion ab Bimolekulare Eliminierung: Die Konzentrationen von Base und Substrat gehen beide in das Geschwindigkeitsgesetz mit ein. SN1-Reaktion E2-Reaktion hschulz 68618547 Seite 43 von 46 14.05.2016 OC 2 Konjugiertes -System Alternierende Reihenfolge von Einfach- und Mehrfachbindungen CH-acide Verbindung An Kohlenstoffe gebundene Wasserstoffe sind saurer als in Alkanen, wenn elektronenziehende gruppen in Nachbarstellung sind 3) Vervollständigen Sie folgende Tabelle. Edukt Produkt Reaktion NO2 NH2 Reduktion Cl OH SN Br AE HBr Br HBr Ph Ph O Ph Ph ()3P Wittig Ph Ph AR Ph Ph O OH H2O H3C I Mg S O HS S Grignard Thioacetalbildung 4) Entscheiden Sie, ob folgende Aussagen richtig oder falsch sind. Aussage Richtig Bei der E2-Eliminierung ist die Konformation mit antiperiplanarer Anordnung der Abgangsgruppen besonders X günstig. Die E1-Eliminierung ist nicht stereoselektiv. X Die nucleophile Substitution und die Eliminierung sind X Konkurrenzreaktionen. Bei tiefen Temperaturen ist die Eliminierung gegenüber der nucleophilen Substitution bevorzugt. Die Csp-H-Bindung ist acider als die Csp3-H-Bindung. X Im saueren Milieu sind Halbacetale stabil und reagieren nicht zu Acetalen weiter. Glucose liegt in wässeriger Lösung überwiegend in der X Halbacetal-Form vor. hschulz 68618547 Seite 44 von 46 Falsch X X 14.05.2016 OC 2 Die Reaktion von Ketonen mit primären Aminen führt zur Bildung von Iminen. Sekundäre Amine reagieren nicht mit Ketonen Wasserstoffe am C-Atom von Carbonylen sind besonders reaktionsträge. Im basischen Milieu werden Methylketone mittels Iod zur entsprechenden Carbonsäure und Iodoform abgebaut Butadien reagiert mit HCl unter thermodynamischer Reaktionskontrolle bevorzugt zu 1-Chlorbut-2-en. Organische Chemie macht Spass. Zur Bildung des kinetisch kontrollierten Reaktionsprodukts wird weniger Aktivierungsenergie benötigt Die Hoffmann-Eliminierung führt ganz überwiegend zum thermodynamisch stabileren Saytzeff-Produkt X X X X X X X X 5) Formulieren Sie für folgende Verbindungen jeweils eine Reaktionsgleichung zu ihrer Herstellung. Die Edukte können Sie frei wählen. Ethanol CH3CH2OH + H2O Maleinsäureanhydrid H H HOOC O COOH O O + H2O Acetylchlorid O 3 CH3COOH + PCl3 + H3PO3 3 Cl Phenylacetylen Ph-CH2BrCH2Br Ph C C H + 2 HBr 1-Brombutan OH + HBr Buttersäurehexylester O + OH Br + H2O O + H2O OH C3H7 OC6H13 Acetamid hschulz 68618547 Seite 45 von 46 14.05.2016 OC 2 O O + HCl + NH3 NH2 Cl Butannitril Br CN + NaCN + NaBr 6) In der Pharmaindustrie ist die Herstellung enantiomeren-reiner Stoffe sehr wichtig. Hierzu gibt es prinzipiell zwei Methoden: Herstellung eines Racemats und anschliessende Trennung der Enantiomere oder die enantiomeren-reine Synthese. a) Nennen Sie fünf Möglichkeiten ein Racemat zu trennen. 1. Falls beide Enantiomere unterschiedlich Kristallisieren, durch „Handauslese“ der Kristalle. 2. Reaktion mit einer enantiomeren-reinen Verbindung liefert Diastereomere, die physikalisch getrennt werden können 3. eine chirale Säule wechselwirkt mit beiden Enantiomeren unterschiedlich und folglich haben die Enantiomere eine unterschiedliche Elutionszeit 4. Das Racemat wird einem Mikroorganismus ausgesetzt, dass selektiv ein Enantiomer abbaut, d.h. ein Enantiomer geht verloren. 5. Das Racemat wird einem Mikroorganismus ausgesetzt, das selektiv ein Enantiomer derivatisiert, d.h. beide Enantiomere können gewonnen werden. b) Wie können Sie ein Racemat einer Carbonsäure durch Säure-Base-Reaktion in ihre Enantiomere auftrennen? Beschreiben Sie den Prozess mittels Reaktionsgleichungen am Beispiel der Milchsäure und einer Base ihrer Wahl. COOH COOH H COOH Rac OH + H2N COOH (S) (S) H2N H H2N C4H8NH3+ H COO C4H8NH2 (S) HO CH3 - H + C4H8NH3 + H (S) COO H (R) - OH CH3 S/S und S/R = Diastereomere c) Nennen Sie zwei Wege um enantiomeren-reine Stoffe direkt herzustellen, ohne über den Umweg des Racemats zu gehen. 1. Asymmetrische Synthesen mittels stereospezifischer synthetischer Katalysatoren (Übergangsmetall-Komplexe) 2. Asymmetrische Synthesen mittels Biokatalysatoren (Enzyme, Mikroorganismen) = Biotechnologie hschulz 68618547 Seite 46 von 46 14.05.2016
![6.3.1 1-Oxa-spiro[2.5]octan - Institut für Organische Chemie](http://s1.studylibde.com/store/data/001356875_1-96e669e5c88ad586db9f9f199d424d05-300x300.png)