Übungen14-Musterklausur
Werbung
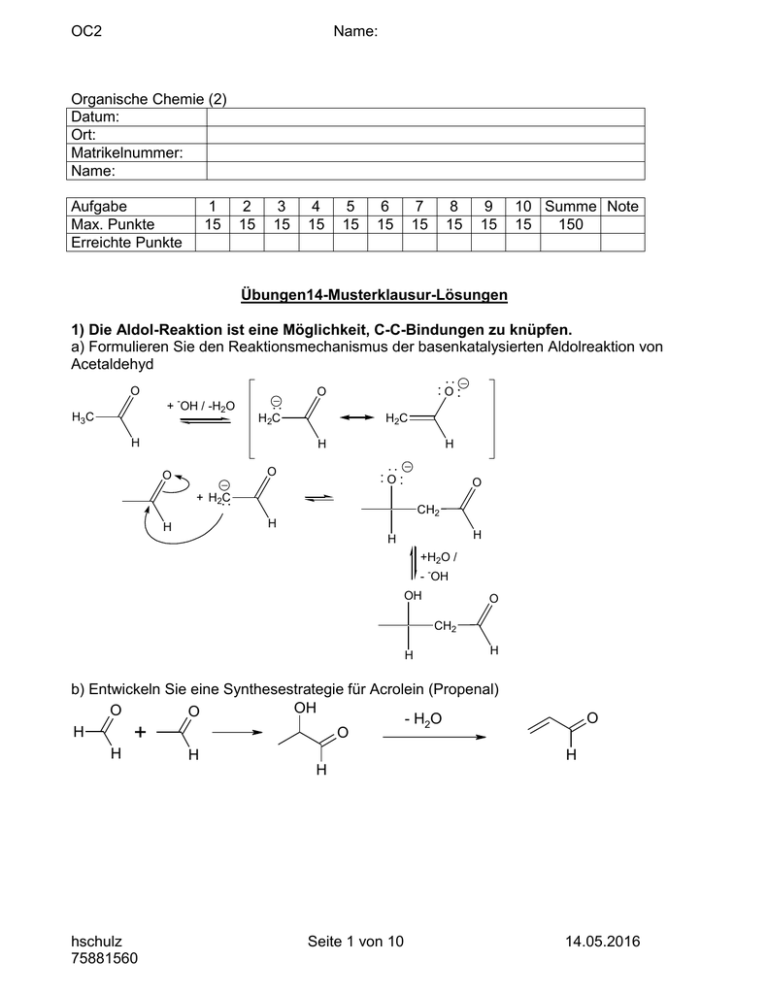
OC2 Name: Organische Chemie (2) Datum: Ort: Matrikelnummer: Name: Aufgabe Max. Punkte Erreichte Punkte 1 15 2 15 3 15 4 15 5 15 6 15 7 15 8 15 9 15 10 Summe Note 15 150 Übungen14-Musterklausur-Lösungen 1) Die Aldol-Reaktion ist eine Möglichkeit, C-C-Bindungen zu knüpfen. a) Formulieren Sie den Reaktionsmechanismus der basenkatalysierten Aldolreaktion von Acetaldehyd O + -OH / -H2O H3C O H2C H O H2C H O O H O O + H2C H CH2 H H H +H2O / - -OH OH O CH2 H H b) Entwickeln Sie eine Synthesestrategie für Acrolein (Propenal) OH O O - H2O H O + H H H hschulz 75881560 Seite 1 von 10 O H 14.05.2016 OC2 Name: 2) Die Wittig-Reaktion dient zur Herstellung von C-C-Doppelbindungen a) Beschreiben Sie den Reaktionsmechanismus anhand der Synthese von 2-Butenal H3C (C6H5)P H + 3P Br H 3P C CHO C CH3 CH3 3 P H H O C CHO 3 P C H CH3 C H H Br H H H O C +BuLi/-Bu-H,-LiBr O 3P + CH3 C CHO C H CH3 b) Entwickeln Sie eine Synthesestrategie zur Darstellung von folgendem Alken ausgehend von Cyclohexan Cl2/h Cl PPh3 PPh3 hschulz 75881560 + O KMnO4 H2O/OH- + OH - PPh3 Cl OPPh3 Seite 2 von 10 + BuLi - BuH, -LiCl O PPh3 + 14.05.2016 OC2 Name: 3. Halogene reagieren mit Ketonen unter elektrophiler Substitution a) Beschreiben Sie den Reaktionsmechanismus der Mono-Bromierung von Methylphenylketon im sauren Milieu. O OH + Br2 H+ CH3 - Br-H+ OH + C CH2Br O CH2Br b) Beschreiben Sie den Reaktionsmechanismus der Mono-Bromierung von Methylphenylketon im basischen Milieu. O O + OH+ Br2 CH3 - Br- H2O O CH2Br c) Kommentieren Sie die Wahrscheinlichkeit der Mehrfach-Halogenierung in obigen Reaktionen Im basischen Milieu geht die Reaktion durch bis zur dreifach-halogenierten Methylgruppe. Danach bildet sich unter C-C-Spaltung Carbonsäure und Bromoform. Dies liegt daran, dass das Produkt jeweils reaktiver ist als das Edukt. Die C-H-Bindungen sind durch die Halogenatome (-I-Effekt) stärker acide und reagieren leichter mit der Base zum Enolat-Ion. Im saueren Milieu ist die Enolisierung nach der Mono-Halogenierung erschwert. hschulz 75881560 Seite 3 von 10 14.05.2016 OC2 Name: 4. Die Gabriel-Synthese dient zur selektiven Darstellung von primären Aminen a) Beschreiben Sie eine Synthesestrategie zur Darstellung des Phthalimid-Kaliums ausgehend von Benzol Fr.Cr.Alk. COOH KMnO4 COONH4 NH3 COONH4 COOH O COONH4 NH O + KNH2 N K+ - NH3 COONH4 O O b) Beschreiben Sie den Reaktionsmechanismus der Darstellung von N-1-Butyl-Phthalimid aus Phthalimid-Kalium O O C3H7 N N Br Br H O O O N - Br- H C4H9 SN2-Mechanismus O hschulz 75881560 Seite 4 von 10 14.05.2016 OC2 Name: 5) a) Chlorbenzol reagiert mit NaOH zu Phenol. Formulieren Sie den Reaktionsmechanismus - - HCl + OH Cl OH - OH +H2O / -OH O H b) Wie heisst der Mechanismus, nachdem p-Nitro-chlorbenzol mit NaOH reagiert? Additions-Eliminierungs-Mechanismus c) Beim Erhitzen des Diazonium-Salzes der Anthranilsäure mit Cyclopentadien entsteht Benzonorbornadien. Erklären Sie, wie dieses Produkt entsteht. COOH + NH2 Anthranilsäure Benzonorbornadien COOH + N2 + CO2 NN hschulz 75881560 Seite 5 von 10 14.05.2016 OC2 Name: 6. a) Beschreiben Sie den Reaktionsmechanismus der Ozonolyse von cis-2-Buten mit anschliessender reduktiver Aufarbeitung O H3C - 78°C CH3 H H3C O O O O CH3 H3C H H H Primärozonid H3C H O O O + Reduktion CH3 H CH3 O O Sekundärozonid O O H O H CH3 H H3C O H b) Bei der Ozonolyse und anschliessender reduktiven Aufarbeitung eines Naturstoffs erhält man folgende Produkte in equimolaren Mengen. Welcher Naturstoff lag vor? O O O H H H O O O O Ph H H hschulz 75881560 Zimtaldehyd H H Seite 6 von 10 H H 14.05.2016 OC2 Name: 7. Entwickeln Sie für folgende Produkte eine Synthesestrategie, ausgehend von den genannten Edukten. Edukt: Toluol Produkt: CH3 CH3 CH3 CH3 CH3 Br NO2 Br Br NH2 Br NH2 Br N2 Edukt: Benzol Br Produkt: p-Nitroacetanilid Cl Cl2/FeCl3 NH2 NaNH2 +Cl(O)CCH3 -HCl O O HN H N CH3 CH3 HNO3/H2SO4 NO2 Edukt: Benzol Produkt: CN Cl Cl2/FeCl3 CN NaCN SO3/H2SO4 SO3H hschulz 75881560 Seite 7 von 10 14.05.2016 OC2 Name: Edukte: Benzol Produkt: CH2NH2 Cl Cl2/FeCl3 CN CN Zn/HCl Cl2/FeCl3 NaCN Cl Cl Edukte: 2,3-Dimethyl-2-buten Produkt: Cl HCCl3 Cl C -HCl Cl Cl Cl + C Cl 8) Die Glucose liegt in wässeriger Lösung überwiegend in der Halbacetalform vor. a) Beschreiben Sie den Mechanismus der Halbacetalbildung an einem einfachen Beispiel. H O O H H O + H+ O C 2H 5 + HOC2H5 OH C H H -H + O H C 2H 5 H OH H b) Beantworten Sie kurz folgende Fragen: Wie ist die Struktur eines (Voll)-Acetals? OR R In welchem Milieu können sich Acetale bilden? Warum ist die Halbacetalform der Glucose so stabil? Welche Acetale sind stabiler –offenkettige oder cyclische? Warum? Wie ist die Struktur eines Halbaminals? R OR Im saueren Milieu Intramolekularer Ringschluss zum thermodynamisch stabilen 6-Ring Cyclische - Chelateffekt OH R R NR2 hschulz 75881560 Seite 8 von 10 14.05.2016 OC2 Name: 9. Borane können an Doppelbindungen addiert werden. a) Beschreiben Sie den Reaktionsmechanismus der 1-Propanol-Synthese durch Hydroborierung von Propen H3C H + HBR2 H H3C H H H H H B H3C H H H H R BR2 R OH H2O2 / NaOH / H2O b) Erklären Sie kurz, warum man durch Hydroborierung Anti-Markovnikov-Alkohole darstellen kann Konzertierte Addition der B-H-Bindung an die Doppelbindung erfolgt so, dass die grosse R2B-Gruppe an den weniger sterisch gehinderten Kohlenstoff bindet. Das ist der Kohlenstoff mit den meisten Wasserstoffen. c) Ordnen Sie folgende Hydroborierungsreagenzien nach steigender Regioselektivität und nach steigender Reaktionsgeschwindigkeit H B2H6 HB(CH3)2 A B B H B H B E D C A B E D C E B A Regioselektivität nimmt zu C D Reaktionsgeschwindigkeit nimmt zu hschulz 75881560 Seite 9 von 10 14.05.2016 OC2 Name: 10. Amine können mit der Carbonylgruppe reagieren. a) Beschreiben Sie den Mechanismus der Bildung von N-Methyl-2-propanimin H3C O + H NCH OH 2 3 O CH3 NH2CH3+ NHCH3 NCH3 - H2O H b) Beschreiben Sie den Mechanismus der Reaktion von Aceton mit Dimethylamin. H3C O + HN(CH ) OH 3 2 O CH3 NH(CH3)2+ N(CH3)2 N(CH3)2 - H2O c) Wie reagieren tertiäre Amin unter den obigen Bedingungen? Tertiäre Amine reagieren nicht. hschulz 75881560 Seite 10 von 10 14.05.2016
![6.3.1 1-Oxa-spiro[2.5]octan - Institut für Organische Chemie](http://s1.studylibde.com/store/data/001356875_1-96e669e5c88ad586db9f9f199d424d05-300x300.png)