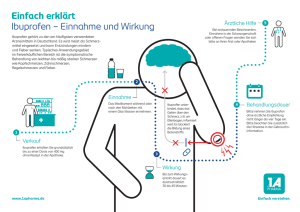
ibuTAD 800 mg Retard FI Juni15
Werbung

_____________________Fachinformation______________________________ ibuTAD® 800 mg Retard schiedliche Episoden nachgewiesener 1. BEZEICHNUNG DES ARZNEI- Art und Dauer der Anwendung: Ulzeration oder Blutung) MITTELS ibuTAD 800 mg Retard wird unzerkaut mit ibuTAD® 800 mg Retard, Retardtabletten - gastrointestinalen Blutungen oder Perforeichlich Flüssigkeit und nicht auf ration in der Anamnese im Zusammenhang 2. QUALITATIVE UND QUANTITATI- nüchternen Magen eingenommen. Bei mit einer vorherigen Therapie mit nichtempfindlichem Magen empfiehlt es sich, VE ZUSAMMENSETZUNG steroidalen Antirheumatika/Antiphlogistika ibuTAD 800 mg Retard während der (NSAR) Mahlzeiten einzunehmen. 1 Retardtablette enthält 800 mg Ibuprofen. - zerebrovaskulären oder anderen aktiven Blutungen Über die Dauer der Anwendung entscheidet Vollständige Auflistung der sonstigen - schweren Leber- oder Nierenfunktionsstöder behandelnde Arzt. Bestandteile, siehe Abschnitt 6.1 rungen Bei rheumatischen Erkrankungen kann die Einnahme/Anwendung von ibuTAD 800 mg - schwerer Herzinsuffizienz (NYHA-Klasse 3. DARREICHUNGSFORM IV) Retard über einen längeren Zeitraum Retardtabletten erforderlich sein. - Schwangerschaft, im letzten Drittel (s. Weiße oblongförmige Retardtabletten mit Nebenwirkungen können minimiert werden, Abschnitt 4.6) doppelseitiger Bruchkerbe. wenn die zur Symptomkontrolle - Kindern und Jugendlichen unter 18 Jahren. erforderliche niedrigste wirksame Dosis über 4. KLINISCHE ANGABEN den kürzest möglichen Zeitraum angewendet Kinder und Jugendliche unter 18 Jahren 4.1 Anwendungsgebiete dürfen ibuTAD 800 mg Retard nicht wird (s. Abschnitt 4.4). Symptomatische Behandlung von Schmerz einnehmen/anwenden, da der Wirkstoffgehalt und Entzündung bei zu hoch ist. Für diese Altersgruppe stehen Besondere Patientengruppen - akuten Arthritiden (einschließlich Gichtandere Ibuprofen-Zubereitungen mit Ältere Patienten: anfall) geringerer Wirkstoffkonzentration zur - chronischen Arthritiden, insbesondere bei Es ist keine spezielle Dosisanpassung Verfügung. erforderlich. Wegen des möglichen Nebenrheumatoider Arthritis (chronische Polywirkungsprofils (s. Abschnitt 4.4) sollten arthritis) 4.4 Besondere Warnhinweise und Vor- Spondylitis ankylosans (Morbus ältere Menschen besonders sorgfältig über- sichtsmaßnahmen für die Anwendung Bechterew) und anderen entzündlich- wacht werden. Gastrointestinale Sicherheit rheumatischen Wirbelsäulenerkrankungen Die Anwendung von ibuTAD in Kombi- Reizzuständen bei degenerativen Gelenk- Eingeschränkte Nierenfunktion: nation mit NSAR, einschließlich selektiver Bei Patienten mit leichter bis mäßiger Einund Wirbelsäulenerkrankungen (Arthrosen schränkung der Nierenfunktion ist keine Cyclooxygenase-2 Hemmer, sollte verund Spondylarthrosen) mieden werden. - entzündlichen weichteilrheumatischen Dosisreduktion erforderlich. (Patienten mit schwerer Niereninsuffizienz s. Abschnitt 4.3). Nebenwirkungen können reduziert werden, Erkrankungen indem die niedrigste wirksame Dosis über - schmerzhaften Schwellungen und EntzünEingeschränkte Leberfunktion (siehe den kürzesten, zur Symptomkontrolle dungen nach Verletzungen. Abschnitt 5.2): erforderlichen Zeitraum angewendet wird (s. Wegen der verzögerten Freisetzung des Bei Patienten mit leichter bis mäßiger Ein- Abschnitt 4.2 und gastrointestinale und Wirkstoffes Ibuprofen ist ibuTAD 800 mg schränkung der Leberfunktion ist keine kardiovaskuläre Risiken weiter unten). Retard nicht zur Therapieeinleitung bei Dosisreduktion erforderlich. (Patienten mit Erkrankungen geeignet, bei denen ein rascher schwerer Leberfunktionsstörung s. Abschnitt Ältere Patienten: 4.3). Wirkungseintritt benötigt wird. Bei älteren Patienten kommt es unter NSARTherapie häufiger zu unerwünschten WirIbuprofen, der Wirkstoff von ibuTAD, wird kungen, vor allem zu gastrointestinalen 4.2 Dosierung und Art der Anwendung nicht empfohlen bei Kindern unter 6 Jahren, Zur Therapie rheumatischer Erkrankungen: Blutungen und Perforationen, auch mit da hierfür keine ausreichenden Erfahrungen Ibuprofen wird in Abhängigkeit vom Alter vorliegen. letalem Ausgang (s. Abschnitt 4.2). bzw. Körpergewicht dosiert. Der empfohlene Dosisbereich für ErwachKinder und Jugendliche: 4.3 Gegenanzeigen sene und Jugendliche ab 15 Jahren liegt Es besteht ein Risiko für ibuTAD darf nicht angewendet werden bei: zwischen 1200 und 2400 mg Ibuprofen pro Nierenfunktionsstörungen bei dehydrierten - Überempfindlichkeit gegen den Wirkstoff Tag. Die maximale Einzeldosis sollte höchsJugendlichen. oder einen der in Abschnitt 6.1 genannten tens 800 mg Ibuprofen betragen. sonstigen Bestandteile Gastrointestinale Blutungen, Ulzera und - bekannten Reaktionen von BronchoibuTAD 800 mg Retard: Perforationen: spasmus, Asthma, Rhinitis oder Urtikaria Alter: Einzeldosis: TagesgesamtGastrointestinale Blutungen, Ulzera oder nach der Einnahme von Acetylsalicylsäure Tabletten dosis: Tabletten Perforationen, auch mit letalem Ausgang, oder anderen nicht-steroidalen EntzünibuTAD 800 ibuTAD 800 mg wurden unter allen NSAR berichtet. Sie dungshemmern in der Vergangenheit mg Retard Retard traten mit oder ohne vorherige Warnsympungeklärten Blutbildungsstörungen Erwachse- 1 (entspre2-3 (entspretome bzw. schwerwiegende gastrointestinale ne chend 800 mg chend 1600-2400 - bestehenden oder in der Vergangenheit Ereignisse in der Anamnese zu jedem ZeitIbuprofen) mg Ibuprofen) wiederholt aufgetretenen peptischen Ulzera punkt der Therapie auf. oder Hämorrhagien (mindestens 2 unter1 _____________________Fachinformation______________________________ ibuTAD® 800 mg Retard Das Risiko gastrointestinaler Blutung, Ulzeration oder Perforation ist höher mit steigender NSAR-Dosis, in Patienten mit Ulzera in der Anamnese, insbesondere mit den Komplikationen Blutung oder Perforation (s. Abschnitt 4.3), und bei älteren Patienten. Diese Patienten sollten die Behandlung mit der niedrigsten verfügbaren Dosis beginnen. Für diese Patienten sowie für Patienten, die eine begleitende Therapie mit niedrig dosierter Acetylsalicylsäure (ASS) oder anderen Arzneimitteln, die das gastrointestinale Risiko erhöhen können, benötigen (s. Abschnitt 4.5), sollte eine Kombinationstherapie mit protektiven Arzneimitteln (z. B. Misoprostol oder Protonenpumpenhemmer) in Betracht gezogen werden (s. unten und Abschnitt 4.5). Dosen (z. B. ≤1 200 mg/Tag) mit einem erhöhten Risiko arterieller thrombotischer Ereignisse assoziiert ist. Bei Patienten mit unkontrollierter Hypertonie, Herzinsuffizienz (NYHA II-III), bestehender ischämischer Herzkrankheit, peripherer arterieller Verschlusskrankheit und/oder zerebrovaskulärer Erkrankung sollte Ibuprofen nur nach sorgfältiger Abwägung angewendet und hohe Dosen (2 400 mg/Tag) vermieden werden. - nisch-entzündlichen Darmerkrankungen (Colitis ulcerosa, Morbus Crohn) in der Vorgeschichte bei Bluthochdruck oder Herzinsuffizienz bei eingeschränkter Nierenfunktion bei Leberfunktionsstörungen direkt nach größeren chirurgischen Eingriffen bei Patienten, die an Heuschnupfen, Nasenpolypen oder chronisch obstruktiven Atemwegserkrankungen leiden, da für sie ein erhöhtes Risiko für das Auftreten allergischer Reaktionen besteht. Diese können sich äußern als Asthmaanfälle (sog. Analgetika-Asthma), Quincke-Ödem oder Urtikaria bei Patienten, die auf andere Stoffe allergisch reagieren, da für sie bei der Anwendung von ibuTAD ebenfalls ein erhöhtes Risiko für das Auftreten von Überempfindlichkeitsreaktionen besteht Eine sorgfältige Abwägung sollte auch vor Beginn einer Langzeitbehandlung von Patienten mit Risikofaktoren für kardiovaskuläre Ereignisse (z. B. Hypertonie, Hyperlipidämie, Diabetes mellitus, Rauchen) stattfinden, insbesondere wenn hohe Dosen Patienten mit einer Anamnese gastrointesti- von Ibuprofen (2 400 mg/Tag) erforderlich naler Toxizität, insbesondere in höherem sind. Alter, sollten jegliche ungewöhnliche Schwere akute ÜberempfindlichkeitsreakSymptome im Bauchraum (vor allem Hautreaktionen gastrointestinale Blutungen) insbesondere am Unter NSAR-Therapie wurde sehr selten tionen (zum Beispiel anaphylaktischer Anfang der Therapie melden. über schwerwiegende Hautreaktionen, einige Schock) werden sehr selten beobachtet. Bei Vorsicht ist angeraten, wenn die Patienten mit letalem Ausgang, einschließlich ersten Anzeichen einer Überempfindlichgleichzeitig Arzneimittel erhalten, die das exfoliative Dermatitis, Stevens-Johnson- keitsreaktion nach Einnahme/Verabreichung Risiko für Ulzera oder Blutungen erhöhen Syndrom und toxische epidermale Nekrolyse von ibuTAD muss die Therapie abgebrochen können, wie z. B. orale Kortikosteroide, (Lyell-Syndrom) berichtet (s. Abschnitt 4.8). werden. Der Symptomatik entsprechende, erforderliche Maßnahmen Antikoagulanzien wie Warfarin, selektive Das höchste Risiko für derartige Reaktionen medizinisch Serotonin-Wiederaufnahmehemmer oder scheint zu Beginn der Therapie zu bestehen, müssen durch fachkundige Personen einThrombozytenaggregationshemmer wie ASS da diese Reaktionen in der Mehrzahl der geleitet werden. (s. Abschnitt 4.5). Fälle im ersten Behandlungsmonat auftraten. Beim ersten Anzeichen von Hautausschlä- Ibuprofen, der Wirkstoff von ibuTAD, kann Wenn es bei Patienten unter ibuTAD zu gen, Schleimhautläsionen oder sonstigen vorübergehend die Blutplättchenfunktion gastrointestinalen Blutungen oder Ulzera Anzeichen einer Überempfindlichkeitsreak- (Thrombozytenaggregation) hemmen. kommt, ist die Behandlung abzusetzen. Patienten mit Gerinnungsstörungen sollten tion sollte ibuTAD abgesetzt werden. NSAR sollten bei Patienten mit einer In Ausnahmefällen kann es zu einem daher sorgfältig überwacht werden. gastrointestinalen Erkrankung in der Anamnese Auftreten von schweren Hautinfektionen und (Colitis ulcerosa, Morbus Crohn) mit Vorsicht Weichteilkomplikationen während einer Ergebnisse experimenteller Untersuchungen kommen (siehe weisen auf eine Abschwächung der angewendet werden, da sich ihr Zustand Varizelleninfektion Abschnitt 4.8). Bis jetzt konnte die thrombozytenaggregationshemmenden verschlechtern kann (s. Abschnitt 4.8). Beteiligung von NSAR an einer Wirkung von Acetylsalicylsäure bei gleichKardiovaskuläre und zerebrovaskuläre Wir- Verschlimmerung dieser Infektionen nicht zeitiger Gabe von Ibuprofen hin. Diese Interausgeschlossen werden. Es ist daher aktion könnte den erwünschten protektiven kungen Eine angemessene Überwachung und empfehlenswert, die Anwendung von kardiovaskulären Effekt von ASS reduzieren. Beratung von Patienten mit Hypertonie ibuTAD bei Vorliegen einer Varizellen- Ibuprofen sollte daher bei Patienten, die zur Hemmung der Thrombozytenaggregation und/oder leichter bis mittelschwerer dekom- Infektion zu vermeiden. ASS erhalten, nur mit besonderer Vorsicht pensierter Herzinsuffizienz in der Anamnese angewendet werden (siehe Abschnitt 4.5). Sonstige Hinweise: sind erforderlich, da Flüssigkeitseinlagerungen und Ödeme in Verbindung mit ibuTAD sollte nur unter strenger Abwägung des Nutzen-Risiko-Verhältnisses angewendet Bei länger dauernder Gabe von ibuTAD ist NSAR-Therapie berichtet wurden. eine regelmäßige Kontrolle der Leberwerte, werden: Klinische Studien weisen darauf hin, dass die - bei angeborener Störung des Porphyrin- der Nierenfunktion sowie des Blutbildes Anwendung von Ibuprofen insbesondere in stoffwechsels (z. B. akute intermittierende erforderlich. hohen Dosen (2 400 mg/Tag) Porphyrie); möglicherweise mit einem geringfügig - bei systemischem Lupus erythematodes Bei längerem Gebrauch von Schmerzmitteln erhöhten Risiko arterieller thrombotischer (SLE) sowie Mischkollagenose (mixed können Kopfschmerzen auftreten, die nicht Ereignisse (zum Beispiel Myokardinfarkt connective tissue disease) (s. Abschnitt 4.8). durch erhöhte Dosen des Arzneimittels oder Schlaganfall) assoziiert ist. Insgesamt behandelt werden dürfen. weisen epidemiologische Studien nicht Eine besonders sorgfältige ärztliche ÜberGanz allgemein kann die gewohnheitsmäßige darauf hin, dass Ibuprofen in niedrigen wachung ist erforderlich: - bei Magen-Darm-Störungen oder bei chro- Einnahme von Schmerzmitteln, insbesondere 2 _____________________Fachinformation______________________________ ibuTAD® 800 mg Retard bei Kombination mehrerer schmerzstillender Wirkstoffe, zur dauerhaften Nierenschädigung mit dem Risiko eines Nierenversagens (Analgetika-Nephropathie) führen. Bei Anwendung von NSAR können durch gleichzeitigen Genuss von Alkohol, Wirkstoff-bedingte Nebenwirkungen, insbesondere solche, die den Gastrointestinaltrakt oder das zentrale Nervensystem betreffen, verstärkt werden. Bezüglich weiblicher Abschnitt 4.6. Fertilität siehe 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Ibuprofen (wie andere NSAR) sollte nur mit Vorsicht zusammen mit den folgenden Arzneistoffen eingenommen werden: Niedrig dosierte Acetylsalicylsäure: Die gleichzeitige Verabreichung von Ibuprofen und Acetylsalicylsäure wird im Allgemeinen aufgrund des Potenzials für vermehrte Nebenwirkungen nicht empfohlen. Experimentelle Daten weisen darauf hin, dass Ibuprofen die Wirkung niedrig dosierter Acetylsalicylsäure auf die Thrombozytenaggregation kompetitiv hemmen kann, wenn beide gleichzeitig verabreicht werden. Obwohl Unsicherheiten in Bezug auf die Extrapolation dieser Daten auf die klinische Situation bestehen, kann die Möglichkeit, dass eine regelmäßige Langzeitanwendung von Ibuprofen die kardioprotektive Wirkung niedrig dosierter Acetylsalicylsäure reduzieren kann, nicht ausgeschlossen werden. Bei gelegentlicher Anwendung von Ibuprofen ist eine klinisch relevante Wechselwirkung nicht wahrscheinlich (siehe Abschnitt 5.1). Andere NSAR einschließlich Salicylate: Die gleichzeitige Gabe mehrerer NSAR kann das Risiko gastrointestinaler Ulzera und Blutungen auf Grund eines synergistischen Effekts erhöhen. Daher soll die gleichzeitige Anwendung von Ibuprofen mit anderen NSAR vermieden werden (s. Abschnitt 4.4). Digoxin, Phenytoin, Lithium: Die gleichzeitige Anwendung von ibuTAD mit Digoxin-, Phenytoin- oder Lithiumpräparaten kann den Serumspiegel dieser Arzneimittel erhöhen. Eine Kontrolle der SerumLithium-Spiegel ist nötig, eine Kontrolle der Serum-Digoxinspiegel und der SerumPhenytoinspiegel wird empfohlen. Diuretika, ACE-Hemmer, Betarezeptorenblocker und Angiotensin-II Antagonisten: Nicht-steroidale Antirheumatika können die Wirkung von Diuretika und Antihypertensiva abschwächen. Bei Patienten mit eingeschränkter Nierenfunktion (z. B. exsikkierte Patienten oder ältere Patienten mit eingeschränkter Nierenfunktion) kann die gleichzeitige Einnahme eines ACEHemmers, Betarezeptorenblockers oder Angiotensin-II-Antagonisten mit einem Arzneimittel, das die Cyclooxygenase hemmt, zu einer weiteren Verschlechterung der Nierenfunktion, einschließlich eines möglichen akuten Nierenversagens, führen, was gewöhnlich reversibel ist. Daher sollte eine solche Kombination, vor allem bei älteren Patienten, nur mit Vorsicht angewendet werden. Die Patienten müssen zu einer adäquaten Flüssigkeitseinnahme aufgefordert werden und eine regelmäßige Kontrolle der Nierenwerte sollte nach Beginn einer Kombinationstherapie in Erwägung gezogen werden. Die gleichzeitige Gabe von ibuTAD und kaliumsparenden Diuretika kann zu einer Hyperkaliämie führen. Klinische Untersuchungen haben Wechselwirkungen zwischen nicht-steroidalen Antirheumatika und oralen Antidiabetika (Sulfonylharnstoffen) gezeigt. Obwohl Wechselwirkungen zwischen Ibuprofen und Sulfonylharnstoffen bisher nicht beschrieben sind, wird vorsichtshalber bei gleichzeitiger Einnahme eine Kontrolle der Blutzuckerwerte empfohlen. Tacrolimus: Das Risiko der Nephrotoxizität ist erhöht, wenn beide Arzneimittel gleichzeitig verabreicht werden. Zidovudin: Es gibt Hinweise auf ein erhöhtes Risiko für Hämarthrosen und Hämatome bei HIV-positiven Hämophilie-Patienetn, die gleichzeitig Zidovudin und Ibuprofen einnehmen. Probenecid und Sulfinpyrazon: Arzneimittel, die Probenecid oder Sulfinpyrazon enthalten, können die Ausscheidung von Ibuprofen verzögern. Glucocorticoide: 4.6 Fertilität, Schwangerschaft und erhöhtes Risiko gastrointestinaler Ulzera Stillzeit oder Blutungen (s. Abschnitt 4.4) Schwangerschaft: Die Hemmung der Prostaglandinsynthese Thrombozytenaggregationshemmer wie kann die Schwangerschaft und/oder die Acetylsalicylsäure und selektive Serotonin- embryo-fetale Entwicklung negativ beeinWiederaufnahmehemmer (SSRI): flussen. Daten aus epidemiologischen erhöhtes Risiko gastrointestinaler Blutungen Studien weisen auf ein erhöhtes Risiko für (s. Abschnitt 4.4) Fehlgeburten sowie kardiale Missbildungen Bei gleichzeitiger Anwendung von Ibuprofen und Gastroschisis nach der Anwendung eines kann die Thrombozytenaggregationshemmen- Prostaglandinsynthesehemmers in der Frühde Wirkung niedrig-dosierter Acetylsalicylsäure schwangerschaft hin. Es wird angenommen, beeinträchtigt sein (s. Abschnitt 4.4). dass das Risiko mit der Dosis und der Dauer der Therapie steigt. Methotrexat: Die Gabe von ibuTAD innerhalb von 24 Bei Tieren wurde nachgewiesen, dass die Stunden vor oder nach Gabe von Methotrexat Gabe eines Prostaglandinsynthesehemmers kann zu einer erhöhten Konzentration von zu erhöhtem prä- und post-implantärem Methotrexat und einer Zunahme seiner toxi- Verlust und zu embryo-fetaler Letalität führt. schen Wirkung führen. Ferner wurden erhöhte lnzidenzen verschiedener Missbildungen, einschließlich kardioCiclosporin: vaskulärer Missbildungen, bei Tieren Das Risiko einer nierenschädigenden berichtet, die während der Phase der Wirkung durch Ciclosporin wird durch die Organogenese einen Prostaglandinsynthesegleichzeitige Gabe bestimmter nicht-steroi- hemmer erhielten. daler Antirheumatika erhöht. Dieser Effekt kann auch für eine Kombination von Während des ersten und zweiten SchwangerCiclosporin mit Ibuprofen nicht ausgeschlos- schaftstrimesters sollte Ibuprofen nur sen werden. gegeben werden, wenn dies unbedingt notwendig ist. Falls Ibuprofen von einer Frau Antikoagulanzien: angewendet wird, die versucht schwanger zu Nicht-steroidale Antirheumatika können die werden oder wenn es während des ersten Wirkung von Antikoagulanzien wie Warfarin oder zweiten Schwangerschaftstrimesters verstärken (s. Abschnitt 4.4.) angewendet wird, sollte die Dosis so niedrig und die Behandlungsdauer so kurz wie mögSulfonylharnstoffe: lich gehalten werden. 3 _____________________Fachinformation______________________________ ibuTAD® 800 mg Retard Während des dritten Schwangerschaftstrimesters können alle Prostaglandinsynthesehemmer: - den Fetus folgenden Risiken aussetzen: • kardiopulmonale Toxizität (mit vorzeitigem Verschluss des Ductus arteriosus und pulmonaler Hypertonie); • Nierenfunktionsstörung, die zu Nierenversagen mit Oligohydramniose fortschreiten kann; - die Mutter und das Kind, am Ende der Schwangerschaft, folgenden Risiken aussetzen: • mögliche Verlängerung der Blutungszeit, ein thrombozyten-aggregationshemmender Effekt, der selbst bei sehr geringen Dosen auftreten kann; • Hemmung von Uteruskontraktionen, mit der Folge eines verspäteten oder verlängerten Geburtsvorganges. 4.8 Nebenwirkungen Bei der Bewertung von Nebenwirkungen werden folgende Häufigkeiten zugrunde gelegt: Sehr häufig: mehr als 1 von 10 Behandelten Häufig: weniger als 1 von 10, aber mehr als 1 von 100 Behandelten Gelegentlich: weniger als 1 von 100, aber mehr als 1 von 1000 Behandelten Selten: weniger als 1 von 1000, aber mehr als 1 von 10.000 Behandelten Sehr selten: 1 oder weniger von 10.000 Behandelten, einschließlich Einzelfälle Bei den folgenden unerwünschten Arzneimittelwirkungen muss berücksichtigt werden, dass sie überwiegend dosisabhängig und interindividuell unterschiedlich sind. Daher ist Ibuprofen während des dritten Die am häufigsten beobachteten NebenwirSchwangerschaftstrimesters kontraindiziert. kungen betreffen den Verdauungstrakt. Peptische Ulzera, Perforationen oder Blutungen, manchmal tödlich, können auftreten, Stillzeit: Der Wirkstoff Ibuprofen und seine Abbau- insbesondere bei älteren Patienten (s. Sektion produkte gehen nur in geringen Mengen in 4.4) Übelkeit, Erbrechen, Diarrhö, Blädie Muttermilch über. Da nachteilige Folgen hungen, Verstopfung, Verdauungsbeschwerfür den Säugling bisher nicht bekannt den, abdominale Schmerzen, Teerstuhl, geworden sind, wird bei kurzfristiger Hämatemesis, ulzerative Stomatitis, VerAnwendung eine Unterbrechung des Stillens schlimmerung von Colitis und Morbus Crohn in der Regel nicht erforderlich sein. Wird (s. Abschnitt 4.4) sind nach Anwendung eine längere Anwendung bzw. Einnahme berichtet worden. Weniger häufig wurde höherer Dosen verordnet, sollte jedoch ein Gastritis beobachtet. Insbesondere das Risiko für das Auftreten von Magen-Darmfrühzeitiges Abstillen erwogen werden. Blutungen ist abhängig vom Dosisbereich und der Anwendungsdauer. Fertilität: Die Anwendung von ibuTAD kann, wie die Ödeme, Bluthochdruck und Herzinsuffizienz Anwendung anderer Arzneimittel, die wurden im Zusammenhang mit NSARbekanntermaßen die Cyclooxygenase/ Behandlung berichtet. Prostaglandinsynthese hemmen, die weibliche Fertilität beeinträchtigen und wird Klinische Studien weisen darauf hin, dass die daher bei Frauen, die schwanger werden Anwendung von Ibuprofen insbesondere in möchten, nicht empfohlen. Bei Frauen, die hohen Dosen (2 400 mg/Tag) Schwierigkeiten haben schwanger zu werden möglicherweise mit einem geringfügig oder bei denen Untersuchungen zur Infertili- erhöhten Risiko arterieller thrombotischer tät durchgeführt werden, sollte das Absetzen Ereignisse (zum Beispiel Myokardinfarkt von ibuTAD in Betracht gezogen werden. oder Schlaganfall) assoziiert ist (siehe Abschnitt 4.4). 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen Herzerkrankungen von Maschinen Selten: Herzrhythmusstörungen (SinustachyDa bei der Anwendung von ibuTAD in kardie, Sinusbradykardie) höherer Dosierung zentralnervöse Nebenwir- Sehr selten: Palpitationen, Ödeme, Herzkungen wie Müdigkeit und Schwindel auf- insuffizienz, Herzinfarkt treten können, kann im Einzelfall die Reaktionsfähigkeit verändert und die Fähig- Erkrankungen des Blutes und des Lymphkeit zur aktiven Teilnahme am Straßenver- systems kehr und zum Bedienen von Maschinen Selten: Azidose beeinträchtigt werden. Dies gilt in verstärk- Sehr selten: Störungen der Blutbildung tem Maße im Zusammenwirken mit Alkohol. (Anämie, Leukopenie, Thrombozytopenie, 4 Panzytopenie, Agranulozytose) Erste Anzeichen können sein: Fieber, Halsschmerzen, oberflächliche Wunden im Mund, grippeartige Beschwerden, starke Abgeschlagenheit, Nasenbluten und Hautblutungen. Bei Langzeittherapie sollte das Blutbild regelmäßig kontrolliert werden. Erkrankungen des Nervensystems Häufig: Zentralnervöse Störungen wie Kopfschmerzen, Schwindel, Schlaflosigkeit, Erregung, Reizbarkeit oder Müdigkeit Selten: Pseudotumor cerebri, Halluzinationen, Parästhesie, Traumabnormitäten Augenerkrankungen Gelegentlich: Sehstörungen Selten: Katarakt, Konjunktivitis, Sehnerventzündungen, Trockenheit der Augen Erkrankungen des Ohrs und des Labyrinths Sehr selten: Tinnitus, Hörstörungen, Gehörverlust Erkrankungen des Gastrointestinaltrakts Sehr häufig: Gastrointestinale Beschwerden wie Sodbrennen, Bauchschmerzen, Übelkeit, Erbrechen, Blähungen, Diarrhoe, Verstopfung und geringfügige Magen-DarmBlutverluste, die in Ausnahmefällen eine Anämie verursachen können. Häufig: Gastrointestinale Ulzera, unter Umständen mit Blutung und Durchbruch. Ulzerative Stomatitis, Verstärkung einer Colitis und eines Morbus Crohn (siehe Abschnitt 4.4). Gelegentlich: Gastritis, Appetitlosigkeit Selten: Mundtrockenheit, Rhinitis Sehr selten: Ösophagitis, Pankreatitis Der Patient ist anzuweisen, bei Auftreten von stärkeren Schmerzen im Oberbauch oder bei Meläna oder Hämatemesis das Arzneimittel abzusetzen und sofort einen Arzt aufzusuchen. Sehr selten: Ausbildung von intestinalen, diaphragmaartigen Strikturen Erkrankungen der Nieren und Harnwege Gelegentlich: Ausbildung von Ödemen, insbesondere bei Patienten mit arterieller Hypertonie oder Niereninsuffizienz; nephrotisches Syndrom; interstitielle Nephritis, die mit einer akuten Niereninsuffizienz einhergehen kann. Sehr selten können Nierengewebsschädigungen (Papillennekrosen) und erhöhte Harnsäurekonzentrationen im Blut auftreten. Die Nierenfunktion sollte regelmäßig _____________________Fachinformation______________________________ ibuTAD® 800 mg Retard lichen Schock. Beim Auftreten einer dieser Erscheinungen, Erkrankungen der Haut und des Unterhaut- die schon bei Erstanwendung vorkommen können, ist sofortige ärztliche Hilfe erforderzellgewebes lich. Selten: photoallergische Hautreaktionen Sehr selten: Bullöse Hautreaktionen wie Stevens-Johnson-Syndrom und toxische Leber- und Gallenerkrankungen epidermale Nekrolyse (Lyell-Syndrom), Sehr selten: Leberfunktionsstörungen, LeberAlopezie. schäden, insbesondere bei der Langzeittherapie, Leberversagen, akute Hepatitis In Ausnahmefällen kann es zu einem Auftreten von schweren Hautinfektionen und Bei länger dauernder Gabe sollten die Weichteilkomplikationen während einer Leberwerte regelmäßig kontrolliert werden. Varizelleninfektion kommen (s. auch „InfekPsychiatrische Erkrankungen tionen und parasitäre Erkrankungen“). Sehr selten: psychotische Reaktionen, Infektionen und parasitäre Erkrankungen Depression Sehr selten ist im zeitlichen Zusammenhang mit der systemischen Anwendung von nicht- Stoffwechsel- und Ernährungsstörungen steroidalen Antiphlogistika eine Verschlech- Selten: hypoglykämische Reaktionen terung infektionsbedingter Entzündungen (z. B. Entwicklung einer nekrotisierenden Erkrankungen der Fortpflanzungsorgane und Fasciitis) beschrieben worden. Dies steht der Brust möglicherweise im Zusammenhang mit dem Selten: Gynäkomastie Wirkmechanismus der nicht-steroidalen Antiphlogistika. Meldung des Verdachts auf Nebenwirkungen Wenn während der Anwendung von ibuTAD Die Meldung des Verdachts auf Zeichen einer Infektion neu auftreten oder Nebenwirkungen nach der Zulassung ist von sich verschlimmern, wird dem Patienten großer Wichtigkeit. Sie ermöglicht eine daher empfohlen, unverzüglich den Arzt kontinuierliche Überwachung des Nutzenaufzusuchen. Es ist zu prüfen, ob die Indika- Risiko-Verhältnisses des Arzneimittels. tion für eine antiinfektiöse/antibiotische Angehörige von Gesundheitsberufen sind Therapie vorliegt. aufgefordert, jeden Verdachtsfall einer Sehr selten wurde unter der Anwendung von Nebenwirkung dem Bundesinstitut für Ibuprofen die Symptomatik einer aseptischen Arzneimittel und Medizinprodukte, Abt. Kurt-Georg-Kiesinger Meningitis mit Nackensteifigkeit, Kopf- Pharmakovigilanz, Allee 3, D-53175 Bonn, Website: schmerzen, Übelkeit, Erbrechen, Fieber oder Bewusstseinstrübung beobachtet. Prädispo- www.bfarm.de anzuzeigen. kontrolliert werden. niert scheinen Patienten mit Autoimmunerkrankungen (SLE, mixed connective tissue 4.9 Überdosierung a) Symptome einer Überdosierung disease) zu sein. Als Symptome einer Überdosierung können zentralnervöse Störungen wie KopfschmerGefäßerkrankungen zen, Schwindel, Benommenheit und Sehr selten: Arterielle Hypertonie Bewusstlosigkeit (bei Kindern auch myoklonische Krämpfe) sowie AbdominalErkrankungen des Immunsystems Gelegentlich: Überempfindlichkeitsreaktio- schmerzen, Übelkeit und Erbrechen aufnen mit Hautausschlägen und Hautjucken treten. Des Weiteren sind gastrointestinale sowie Asthmaanfällen (ggf. mit Blutdruck- Blutungen und Funktionsstörungen von Leber und Nieren möglich. Ferner kann es zu abfall). Hypotension, Atemdepression und Zyanose Der Patient ist anzuweisen, in diesem Fall kommen. umgehend den Arzt zu informieren und b) Therapiemaßnahmen bei Überdosierung ibuTAD nicht mehr einzunehmen. Selten: Lupus erythematodes, Serumkrank- Ein spezifisches Antidot existiert nicht. heit, Schoenlein-Henoch-Vaskulitis Sehr selten: Schwere allgemeine Über- 5. PHARMAKOLOGISCHE empfindlichkeitsreaktionen. Sie können sich EIGENSCHAFTEN äußern als: Gesichtsödem, Zungenschwel- 5.1 Pharmakodynamische Eigenschaften lung, innere Kehlkopfschwellung mit Ein- Pharmakotherapeutische Gruppe: engung der Luftwege, Luftnot, Herzjagen, Nichtsteroidale Antiphlogistika und Blutdruckabfall bis hin zum lebensbedroh- Antirheumatika 5 ATC-Code: M01AE01 Ibuprofen ist ein nicht-steroidales Antiphlogistikum-Analgetikum, das sich über die Prostaglandinsynthesehemmung in den üblichen tierexperimentellen Entzündungsmodellen als wirksam erwies. Beim Menschen reduziert Ibuprofen entzündlich bedingte Schmerzen, Schwellungen und Fieber. Ferner hemmt Ibuprofen reversibel die ADP- und die kollageninduzierte Plättchenaggregation. Experimentelle Daten weisen darauf hin, dass Ibuprofen die Wirkung niedrig dosierter Acetylsalicylsäure auf die Thrombozytenaggregation kompetitiv hemmen kann, wenn beide gleichzeitig verabreicht werden. Einige pharmakodynamische Studien zeigten, dass es bei Einnahme von Einzeldosen von 400 mg Ibuprofen innerhalb von 8 Stunden vor oder innerhalb von 30 Minuten nach der Verabreichung von Acetylsalicylsäure-Dosen mit schneller Freisetzung (81 mg) zu einer verminderten Wirkung der Acetylsalicylsäure auf die Bildung von Thromboxan oder die Thrombozytenaggregation kam. Obwohl Unsicherheiten in Bezug auf die Extrapolation dieser Daten auf die klinische Situation bestehen, kann die Möglichkeit, dass eine regelmäßige Langzeitanwendung von Ibuprofen die kardioprotektive Wirkung niedrig dosierter Acetylsalicylsäure reduzieren kann, nicht ausgeschlossen werden. Bei gelegentlicher Anwendung von Ibuprofen ist eine klinisch relevante Wechselwirkung nicht wahrscheinlich (siehe Abschnitt 4.5). 5.2 Pharmakokinetische Eigenschaften Bei oraler Applikation wird Ibuprofen zum Teil schon im Magen und anschließend vollständig im Dünndarm resorbiert. Nach hepatischer Metabolisierung (Hydroxylierung, Carboxylierung) werden die pharmakologisch unwirksamen Metabolite vollständig, hauptsächlich renal (90 %), aber auch biliär eliminiert. Die Eliminationshalbwertszeit beträgt beim Gesunden und Leberund Nierenkranken 1,8-3,5 Stunden, die Plasmaproteinbindung etwa 99 %. Maximale Plasmaspiegel werden nach oraler Gabe einer normal freisetzenden Arzneiform nach 1-2 Stunden erreicht. Bioverfügbarkeit Eine im Jahr 1988 durchgeführte Bioverfügbarkeitsuntersuchung an 16 Probanden ergab im Vergleich zum Referenzpräparat (2 x 400 mg Ibuprofen, schnellfreisetzende Dragees): _____________________Fachinformation______________________________ ibuTAD® 800 mg Retard Testpräparat: x VK AUC 214,59 26 Css,max 26,24 25 Css,min 9,53 43 HVD 9,89 24 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung Referenzpräparat: x VK AUC 198,04 25 Verbundfolienbeutel mit 20 (N1), 48, 50 (N2) 98 und 100 Retardtabletten (N3). Anstaltspackung mit 500 (ggf. 5x100), 2500 und 5000 Retardtabletten. Css,max 54,38 21 Css,min 2,09 68 HVD 2,58 15 Keine 7. INHABER DER ZULASSUNG Angabe der Werte als Mittelwert und Streu- TAD Pharma GmbH breite Heinz-Lohmann-Straße 5 27472 Cuxhaven Mittlere Plasmaspiegelverläufe im Vergleich Tel.: (04721) 606-0 zu einem Referenzpräparat in einem Fax: (04721) 606-333 Konzentrations-Zeit-Diagramm (s. Abb. 1). E-Mail: [email protected] 5.3 Präklinische Daten zur Sicherheit Die subchronische und chronische Toxizität von Ibuprofen zeigte sich in Tierversuchen vor allem in Form von Läsionen und Ulzera im Magen-Darm-Trakt. In-vitround In-vivo-Untersuchungen ergaben keine klinisch relevanten Hinweise auf mutagene Wirkungen von Ibuprofen. In Studien an Ratten und Mäusen wurden keine Hinweise auf kanzerogene Effekte von Ibuprofen gefunden. 8. ZULASSUNGSNUMMER 10428.00.00 9. DATUM DER ERTEILUNG DER ZULASSUNG/ VERLÄNGERUNG DER ZULASSUNG ibuTAD 800 mg Retard: 27. April 1989/06. Mai 2003 10. STAND DER INFORMATION 06.2015 Ibuprofen führte zu einer Hemmung der 11. VERKAUFSABGRENZUNG Ovulation beim Kaninchen sowie zu Stö- Verschreibungspflichtig rungen der Implantation bei verschiedenen Tierspezies (Kaninchen, Ratte, Maus). Experimentelle Studien an Ratte und Kaninchen haben gezeigt, dass Ibuprofen die Plazenta passiert. Nach Gabe von maternal toxischen Dosen traten bei Nachkommen von Ratten vermehrt Missbildungen auf (Ventrikelseptumdefekte). 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Glucose-Monohydrat (Ph. Eur.), Povidon K. 30, Sucrosemonopalmitat, Stearinsäure (Ph. Eur.), Talkum, Magnesiumstearat (Ph. Eur.) Abbildung 1: Mittlere Ibuprofen-Plasmakonzentrationen [µg/ml] im steady state bei 16 Probanden nach Gabe von ibuTAD 800 mg Retard bzw. Referenzpräparat (schnellfreisetzend, 2x 400 mg): 50 6.2 Inkompatibilitäten Nicht zutreffend. Dieses Arzneimittel soll nach Ablauf des Verfallsdatums nicht mehr angewendet werden. 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Nicht über +30°C lagern! Konzentration [µg/ml] 40 6.3 Dauer der Haltbarkeit Die Dauer der Haltbarkeit beträgt 3 Jahre. 30 20 10 0 6.5 Art und Inhalt des Behältnisses PVC/PVDC/Aluminium-Blister 0 4 oder 8 12 16 20 Z e it n a c h A p p lik a t io n [ h ] 6 Ib u T A D 8 0 0 m g R e t a r d Re fe r e n z p r ä p a r a t 24