82~1.FL - Johannes Gutenberg
Werbung

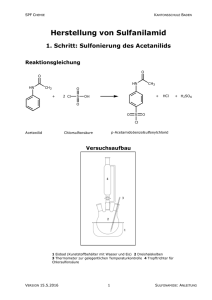
23.04.2008 Versuchsprotokoll 11 8. Einfache physikalisch-chemische Versuche 8.2. Stoffverteilung in zwei Phasen II: Flüssig-Flüssig-Extraktion Einführung Der Stoffverteilung eines Stoffes A in zwei Phasen, in diesem Fall flüssig-flüssig, liegt ein Verteilungsgleichgewicht zugrunde. Bei dem Verteilungsgleichgewicht besitzen die beiden Phasen eine unterschiedliche chemische Zusammensetzung wie A. Ist der Quotient der Konzentrationen des Stoffes A zweier Phasen, die im Gleichgewicht stehen, bei konstanter Temperatur konstant, so gilt das Nernst`sche Verteilungsgesetz: c(A)I= α c(A)II. (Phase I und II werden so gewählt, dass α >1; ist α >1, so ist A in einer Phase deutlich besser löslich; α ist abhängig von den zwischenmolekularen Wechselwirkungen zwischen A und den beiden Phasen) Der Verteilungskoeffizient α lässt sich bestimmen, indem man A in zwei Lösungsmittel bekannten Volumens gibt, diese in einen Gleichgewichtszustand versetzt. Aus den Phasen wird ein bestimmtes Volumen genommen und A durch Titration bestimmt. Dieses Verfahren wird im Folgenden angewendet. Experimentelle Durchführung Chemikalien: ToluolischeIod-Lsg. (10, 20, 30g*L-1), 0,01 Natriumthiosulfatlsg. (Na2S2O3), Stärke Materialien: 100ml Scheidetrichter, Stopfen, Reagenzgläser, Erlenmeyerkolben, Bürette 4ml der toluolischen Iodlösung werden in einem Scheidetrichter mit 40ml entionisiertem Wasser versetzt. Der Trichter wird mit einem Stopfen verschlossen und 10 min lang geschüttelt, wobei der Hahn zum Entlüften gelegentlich geöffnet wird. Dieser Prozess wird mit der 20, bzw. 30g Iodlösung wiederholt. Anschließend wird eine Separation der wässrigen und der toluolischen Phase im Scheidetrichter durchgeführt. Die wässrige Phase wird in drei kleine Bechergläser gegeben, die toluolische in drei Reagenzgläser. 20ml der wässrigen Phase werden in einen 100ml Erlenmeyerkolben gegeben und mit wenigen Tropfen frischer Stärkelösung (2 Spatelspitzen mit 20ml entionisiertes Wasser aufgekocht, bis die Lösung durchsichtig ist) versetzt. Die entstandene blaue Lösung wird mit 0,01 Na2S2O3 titriert, bis eine vollständige Entfärbung eintritt. Dieses Verfahren wird bei den beiden restlichen wässrigen Phasen ebenfalls angewendet. Die Titration wird zur Konzentrationsbestimmung genutzt. 2ml der toluolischen Phase werden in einen 100ml Erlenmeyerkolben gegeben, mit wenigen Tropfen frischer Stärkelösung, 20ml entionisiertem Wasser und einer Mikro-Ssp. KI versetzt. Die entstandene blaue Lösung wird mit 0,01 Na2S2O3 titriert, bis eine vollständige Entfärbung eintritt. Dieses Verfahren wird bei den beiden restlichen toluolischen Phasen ebenfalls angewendet. Die Titration wird zur Konzentrationsbestimmung genutzt. Die stöchiometrischen Reaktionsgleichungen von Thiosulfat mit Iod werden aufgestellt, die Ausgleichsgerade y= α*x erstellt, sowie die Gleichgewichtskonzentrationen c(I 2) der aliquoten Teile beider Phasen anhand der I2-Stoffmengen bestimmt. Ergebnis Lösung (1a) wässrig (2a) wässrig (3a) wässrig (1b) toluolisch (2b) toluolisch (3b) toluolisch Iod in g 10 20 30 10 20 30 m(Na2S2O3) in ml 0,35 0,85 1,2 14,75 39 46,7 30 23.04.2008 Versuchsprotokoll 11 Schlussfolgerung I2 + 2e- 2I2 S2O32- S4O62- + 2e-_________ I2 + 2 Na2S2O3 2NaI + Na2S4O6 Reaktionsgleichung: Konzentrationen der wässrigen Lsg.: (c(Na2S2O3)= 0,01mol/l) n= c*V= 0,01mol/l * 0,35ml= 3,5*10-3mmol c(1a)= n/V= 3,5*10-3mmol/ 0,02l= 0,175mmol/l n= c*V= 0,01mol/l * 0,85ml= 8,5*10-3mmol c(2a)= n/V= 8,5*10-3mmol/ 0,02l= 0,425mmol/l n= c*V= 0,01mol/l * 0,35ml= 0,012mmol c(3a)= n/V= 0,012mmol/ 0,02l= 0,6mmol/l Konzentrationen der toluolischen Lsg.: (c(Na2S2O3)= 0,01mol/l) n= c*V= 0,01mol/l *14,75ml= 0,1475mmol c(1b)= n/V= 0,1475mmol/ 0,002l= 73,75mmol/l n= c*V= 0,01mol/l * 39ml= 0,39mmol c(2b)= n/V= 0,39mmol/ 0,002l= 195mmol/l n= c*V= 0,01mol/l * 46,7ml= 0,467mmol c(3b)= n/V= 0,467mmol/ 0,002l= 223,5mmol/l Nernst'scher Verteilungskoeffizient 250 t,i c(I2) in mmol/l 200 150 100 50 0 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 w,i c(I2) in mmol/l Iod ist ungefähr 361mal besser in Toluol löslich als in Wasser. α ~ 361,438 Literatur Praktikum Chemie für Biologen: Anorganische, Organische und Physikalische Chemie für Biologen, von Holger Fleischer, erschienen WS 2004/05, Institut für Anorganische Chemie und Analytische Chemie Johannes Gutenberg-Universität Mainz 31