2_2_Praktikum Kunststofftechnik
Werbung

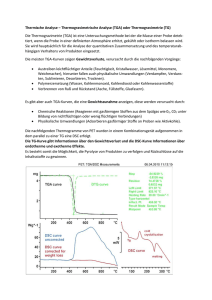
Praktikum Thermische Analyse - Differential Scanning Calorimetry (DSC) 1. Grundlagen und Geräte Mit dem Verfahren der DSC (Differential Scanning Calorimetry) lassen sich die thermische Stabilität von Kunststoffen sowie die Oxidationsstabilität bei sauerstoffempfindlichen Polymeren bestimmen. Bei amorphen Kunststoffen ist die Glasübergangstemperatur Tg von Bedeutung, bei teilkristallinen Kunststoffen werden außerdem das Schmelzverhalten, die Kristallinität K und das Kristallisationsverhalten bestimmt. Das Prinzip des Verfahrens beruht auf der Messung der Energie, mit der Phasenübergänge immer verbunden sind. Die Probe wird zusammen mit einer thermisch inerten Referenzsubstanz in einem Ofen einem zeitlinearen Temperaturprogramm unterworfen, dabei sind sowohl Temperaturerhöhung als auch Temperaturerniedrigung im Vergleich zur Referenzsubstanz möglich. Das Auftreten einer Temperaturdifferenz ΔT zwischen Probe und Referenz ist immer mit einer Enthalpieänderung in der Probe verbunden, die elektrisch als Thermospannung an zwei gegeneinander geschaltete Thermoelemente gemessen wird. Die gemessen Thermospannung ist proportional dem Wärmestrom Q zur Probe. Durch anschließende Integration des Wärmestroms Q über die Zeit erhält man die Enthalpieänderung ΔH der Probe. Abbildung 1 zeigt schematisch das Messprinzip der im Praktikum eingesetzten DSCMesszelle. Abbildung 1 Thermoanalytisches Diagramm Eine DSC-Messkurve entsteht durch Auftragung des Wärmestroms Q (in mW) oder des auf die Probeneinwaage bezogenen Wärmefluss (Heat Flux in mW/mg) gegen die Temperatur T. Abbildung 2 zeigt eine DSC-Kurve einer Polyethylenterephthalat (PET)-Folie. Die Probe wurde aus der Schmelze abgeschreckt, so dass sie ohne Kristallisation in den amorphen Zustand überging. Abbildung 2 DSC-Kurve einer PET-Folie Der endotherme Glasübergangsbereich ist als Verschiebung der Messkurve bei ca. 80°C zu erkennen. Für amorphe und auch eingeschränkt für teilkristalline Polymere gilt, dass sich das Polymer unterhalb der Glasübergangstemperatur im festen, oft spröden Glaszustand befindet, oberhalb in einem kautschukartigen Zustand. Bei etwa 160°C liegt bei dieser PET-Probe ein exothermer Kristallisationspeak vor. Die bei Temperaturen oberhalb der Glasübergangstemperatur beweglichen Molekülketten richten sich aus und kristallisieren, dabei wird Wärme frei. Bei ca. 220°C beginnt der endotherme Schmelzvorgang mit einem Kristallitschmelzpunkts Tm bei 210°C. Die Fläche unter dem Kristallisationspeak bzw. dem Schmelzpeak ist proportional der umgesetzten Wärmemenge Q bzw. dem Wärmestrom (Heat Flux) also der Schmelzenthalpie ΔHm oder der Kristallisationsenthalpie ΔHK. Aus dem für die Probe ermittelten Wert für die Schmelzenthalpie ΔHm lässt sich der Kristallinitätsgrad K teilkristalliner Polymere berechnen. Teilkristallinität bedeutet, dass ein Teil des Polymers geordnet in einem Kristallgitter vorliegt, der Rest ist ungeordnet amorph. Mit zunehmendem Gehalt an Kristalliten steigt der Wert für die Schmelzenthalpie ΔHm, aus 0 dem gemessenen Wert und der tabellierten Schmelzenthalpie ∆𝐻𝑚 für ein 100% kristallines Polymer lässt sich der Kristallinitätsgrad K der Probe berechnen. Die in einer DSC gemessenen Temperaturunterschiede sind sehr klein und der gesamte Messvorgang muss deshalb mit Standardsubstanzen, von denen die Schmelztemperatur und auch deren Schmelzenthalpie bekannt sind, kalibriert werden. Es werden Metalle, wie Indium, Zink und Zinn) eingesetzt. 2. Durchführung 2.1. DSC – Zusammenhang zwischen Umwandlungsart, Peakrichtung und Probenhistorie Glasumwandlung/Glasübergang – kein Peak, sondern Stufe in endotherme Richtung Endothermer Vorgang Schmelzen, Verdampfen, Sublimation, Absorption, Desorption, magnetische Umwandlung (Curie-Punkt), Flüssig-Kristall-Übergang, Desolvatation, Dehydratation, Thermische Zersetzung, Redoxreaktion, Festphasenreaktion Exothermer Vorgang Kristallisation, Polymerisation, Härtung, Vernetzung, Adsorption, Chemisorption, Oxidative Zersetzung, Verbrennung, Redoxreaktion, Festphasenreaktion, Katalytische Reaktion Die Abbildung veranschaulicht den Einfluss der thermischen Vorgeschichte auf eine PET Probe auf das DSC-Thermogramm. Die PET Probe wurde unter 3 verschiedenen Bedingungen abgekühlt, danach wurden mit einer DSC die nachfolgenden Thermogramme erhalten. Obere schwarze Kurve wurde nach schockartigem Abkühlen der PET-Schmelze erhalten. Die mittlere rote Kurve zeigt das Verhalten der PET-Probe nach schockartigem Abkühlen unter die Glasübergangstemperatur und einer anschließenden Konditionierungslagerung (engl. Annealing) für 10 Stunden bei 65 °C. Die untere blaue Kurve lieferte eine PET-Probe, die sehr langsam abgekühlt wurde. Die DSC-Thermogramme der unterschiedlich konditionierten PETProben zeigen deutliche Unterschiede bei dem Glasübergang und der Rekristallisation. 2.1. Probenvorbereitung Etwa 15-20 mg der Probe werden mit Hilfe einer Mikrowaage in den Probentiegel (Aluminiumtiegel) eingewogen und lose mit einem Tiegeldeckel abgedeckt, um eine Messung in inerter Atmosphäre zu gewährleisten. Tiegel und Tiegeldeckel sollten nur mit einer Pinzette angefasst werden, weiterhin ist darauf zu achten, dass kein Probenmaterial auf den Tiegelrand gelangt. Tiegel und Tiegeldeckel werden anschließend mittels einer Verschließpresse kaltverschweißt. Damit eine gute Wärmeübertragung zur Probe gewährleistet ist, muss die Probe gut auf dem Tiegelboden aufliegen und der Tiegelboden eben sein. 2.2. Einsetzen des Probentiegels Zum Öffnen der Messzelle wird der Gerätedeckel mit Hilfe einer Pinzette aus der Messzelle genommen. Der Probentiegel wird auf die rechte Auflagefläche gesetzt, auf der linken Auflageseite befindet sich der Referenztiegel (Leertiegel aus Aluminium). Anschließend wird die Messzelle wieder mit den Gerätedeckeln verschlossen. 2.3. Messung Die Messung wird unter Stickstoff als inertem Schutzgas durchgeführt. Die Steuerung und Auswertung der Messung erfolgt über einen angeschlossenen Rechner mit entsprechender Software. Die einzustellenden Versuchsparameter sind Starttemperatur 30°C, Endtemperatur 300°C, Aufheizrate 10 und 20K/min. Für die richtige Wahl der Heizrate müssen Sie drei Zusammenhänge verstehen. Erstens, der der Temperatursensor ist nicht direkt in der Probe, sondern nur in der Nähe und bei jeder Thermoanalysenmesszelle tritt eine Temperaturdifferenz zwischen Probe und Temperatursensor auf. Nur der Onset (Bestimmung siehe nächsten Punkt) der Übergänge (Glasübergang, Kristallisationspeaks, Schmelzpeaks …) wird identisch. Zweitens, wie zu sehen, werden die Peaks bei steigender Heizrate größer und die Empfindlichkeit der Methode nimmt zu. Kleine Effekte werden so auf einfache Weise verstärkt. Praktisch eine Zeitrafferfunktion für den Energiefluss. Drittens, die Auflösung, also die Trennung dicht nebeneinander liegender Peaks wird mit kleinerer Heizrate besser. Der Temperatursensor hat bei kleiner Heizrate mehr Zeit kleine Effekte sauber zu trennen. Praktisch eine Zeitlupenfunktion für den Energiefluss. 3. Auswertung 3.1. Die Bestimmung der Glasübergangstemperatur Tg Das nachfolgende Verfahren für die Bestimmung des Onset und des Offset ist universell und wird nicht nur bei Tg-Stufen sondern auch bei der Bestimmung des Onset und des Offset an Peaks in Thermogrammen eingesetzt. Bitte daran denken, Stufen lassen sich durch differenzieren in Peaks und Peaks durch integrieren in Stufen überführen. Wie wird’s gemacht? Zur Bestimmung der Glasübergangstemperatur Tg werden wie im nachfolgenden Bild drei Geraden t1 (blau), t2 (orange) und t3 (grün) konstruiert. Die zwei Geraden t1 (blau) und t2 (orange) zur Verlängerung der Basislinie vor und nach der Umwandlung und eine Gerade t3 (grün) durch die größte Steigung während der Umwandlung. Der Schnittpunkt T1 (blau-grün) wird als Onset-Punkt und der Schnittpunkt T2 (grün-orange) als Offset-Punkt bezeichnet. Der Mittelpunkt T3 des durch die Basisliniengeraden t1 und t2 begrenzten Teils der Wendegeraden T1 – T2 gibt die Glasübergangstemperatur Tg (roter Pfeil) an. Je nach Art der Bestimmungsmethode und den Versuchsbedingungen schwank Tg erheblich und kann nicht universell definiert werden. Faustformel: Die Glasübergangstemperatur Tg in Kelvin entspricht 2/3 der Schmelztemperatur Tm in K. Beispiel PET: Tm = 256 °C = 529.16 K Tg = 2/3 * 529,16 K = 352,8 K = 79,6 °C Der amorphe Körper von Kunststoffen erweicht bei der Glasübergangstemperatur Tg, dieses ist ungefähr in der Mitte des Glasübergangsbereiches, der sich über mehrere zig °C erstreckt. Unterhalb von Tg sind die Kettenmoleküle starr und unbeweglich. Bei Belastung können die Kettenmoleküle nicht ausweichen, das Material ist also fest und spröde. Bei Tg erreicht die Brownsche Molekularbewegung der Teilchen durch die zugeführte Energie einen materialspezifischen Wert, die Kettenmoleküle werden beweglich, das Material erweicht. Bei Thermoplasten ist die Glasübergangstemperatur vom chemischen Aufbau, zugefügten Weichmachern, dem Feuchtigkeitsgehalt sowie Orientierungen des amorphen Teils abhängig. Die Bestimmung der Glasübergangstemperatur Tg ist der Norm zu entnehmen (DIN 53765). 3.2. Die Bestimmung des Kristallisationspunktes TK (falls es einen gibt) Wird nach der Produktion der Kunststoff sehr schnell abgekühlt, hat er keine Zeit zur Kristallisation. Unterhalb des Glasübergangs Tg ist die Beweglichkeit der großen Moleküle gering, es gibt deshalb keine Kaltkristallisation. Oberhalb des Glasübergangs Tg werden die Ketten beweglich ordnen sich und bilden sich kleine Kristalle bei relativ tiefen Temperaturen, was als Kaltkristallisation bezeichnet wird. Bei etwa 160°C wird sehr viel Kristallisationswärme ΔHK frei und es tritt ein großer Kristallisationspeak in exothermer Richtung im Thermogramm auf. Der Kristallisationspunkt TK liegt bei 157,4°C, die Kristallisationsenthalpie ΔHK hat einen Wert von 37,2 J/g. Schwierig wird es, wenn sich Kristallisation und Schmelzen im Thermogramm überlagern. Das Problem kann mit unterschiedlichen Heizraten angegangen werden. 3.3. Die Bestimmung des Kristallitschmelzpunkts Tm Der Prozess des Schmelzens erfolgt für Reinstoffe bei definierter Temperatur. Während des Übergangs bleibt die Temperatur konstant, sämtliche zugeführte Wärme ΔHm wird in die Zustandsänderung investiert und deshalb als sogenannte latente Wärme bezeichnet. Schmelzen ist ein endothermer Vorgang. Der Kristallitschmelzpunkt Tm eines teilkristallinen Polymers ist definiert als die Probentemperatur an der Spitze des Schmelzpeaks (hier ca. 210°C). Während der Glasübergang nicht mit einer Änderung der Struktur verbunden ist, tritt beim Schmelzen eine Strukturumwandlung auf. Die kristalline Ordnung geht in eine flüssige, amorphe Struktur über. Dabei muss die molekulare Anziehungskraft zwischen den Makromolekülen des Kristallverbundes überwunden werden. Dazu muss viel Energie in das System hineingegeben werden (Schmelzwärme ΔHm = -40,2 J/g). Der sehr viel größere Energiebetrag ist ein wesentlicher Unterschied zum Glasübergang. Die Schmelztemperatur Tm ist charakteristisch für jeden teilkristallinen Kunststoff. Bei teilkristallinen Kunststoffen besitzen die nichtkristallinen (amorphen) Bereiche ebenfalls einen Glasübergang, der mit der DSC-Messung leicht und rasch ermittelt werden kann. Die DSC-Kurve eines teilkristallinen Thermoplasts besitzt also eine kleine Glasübergangsstufe und einen großen Schmelzpeak, aufgrund ihrer unterschiedlich großen Kristalllamellen keinen festen Schmelzpunkt wie Metalle, sondern einen Schmelzbereich. Dennoch stellt die Peaktemperatur Tm als Temperatur, bei der die meisten Kristalle schmelzen, eine markante Temperatur dar, die auch als Schmelztemperatur bezeichnet wird. Kleinere weniger perfekt aufgebaute Kristallite schmelzen bei einer tieferen Temperatur als große Kristallite. Deshalb ist die thermische Vorgeschichte der Prüflinge so wichtig und es sind mehrere Heiz- und Kühlversuche nötig. Die Bestimmung der Schmelztemperatur Tm ist der Norm (DIN 53765) zu entnehmen. 3.4. Die Bestimmung der Schmelzenthalpie ΔHm Die Schmelzenthalpie ΔHm wird durch Integration der Fläche unter dem Peak ermittelt. Es gilt die Beziehung: ∆𝐻𝑚 = 𝐹 𝑚 ∗𝐶 ∆𝐻𝑚 = Schmelzenthalpie, F= Peakfläche = h*b1/2, C = Kalibrierfaktor, m = Masse der Probe Die Anfangs- und Endpunkte der Peakfläche werden durch Interpolation der Basislinie festgelegt. Heute erledigen das Integratoren in den DSC-Anlagen. Aus der Peakfläche F, der Probenmasse m und dem geräteabhängigen Kalibrierfaktor C wird ΔHm = -40,2 J/g berechnet. 3.5. Die Bestimmung des Kristallinitätsgrads K Der Kristallinitätsgrad K, d.h. der Gehalt an Kristalliten eines Polymers in Prozent wird aus 𝑜 den Werten für die Schmelzenthalpie ∆𝐻𝑚 und den tabellierten Größen ∆𝐻𝑚 berechnet. wie folgt bestimmt: 𝐾= ∆𝐻𝑚 0 ∆𝐻𝑚 ∗ 100% K = Kristallinitätsgrad in %, ∆𝐻𝑚 gemessene Schmelzenthalpie der Probe in J/g, 0 ∆𝐻𝑚 Schmelzenthalpie der reinen Kristallite in J/g aus der Literatur. Polymer Polyethylen niedriger Dichte (LDPE) Polyethylen hoher Dichte (HDPE) Polypropylen (PP) Polyamid (PA) Polyamid-6,6 (PA 6,6) Polyamid-12 (PA 12) Polystyrol (PS) Polyethylenterephthalat (PET) Polymethylmethacrylat (PMMA) Berechnung PET: 0 ∆𝐻𝑚 in J/g (Literaturwerte) 290 290 190 190 200 95 86 115 96 𝐾𝑟𝑖𝑠𝑡𝑎𝑙𝑙𝑖𝑛𝑖𝑡ä𝑡𝑠𝑔𝑟𝑎𝑑 𝐾 = ∆𝐻𝑚 0 ∆𝐻𝑚 ∗ 100% = 𝐽 𝑔 𝐽 115 𝑔 40,2 ∗ 100% = 40,3% 3.6. Die Bestimmung der spezifischen Wärmekapazität cp Die spezifische Wärmekapazität cp gibt an, wieviel Energie aufgewendet werden muss, um 1 g eines Stoffes um 1°C bei konstantem Druck zu erwärmen. Da die Bestimmung von cp gerätetechnisch aufwendig ist, wird bei der Dynamischen Differenzkalorimetrie DSC der Wärmefluss Q (Heat Flux in mW/mg), d.h. die Wärmemenge pro Zeiteinheit und Masse ermittelt. Dieser ist der spezifischen Wärmekapazität cp direkt proportional. Der Proportionalitätsfaktor zwischen cp und dem Heat Flux ist die Heizrate v. 𝑄 = 𝑣 ∗ 𝑐𝑝 𝑚 Eine DSC-Kurve stellt praktisch nichts anderes dar als die Temperaturfunktion der spezifischen Wärme cp. Thermische Effekte sind auffällige Abweichungen von dieser mehr oder weniger stetigen cp-Temperaturfunktion (Basislinie), die, solange keine besonderen physikalischen und chemischen Effekte auftreten, geradlinig verläuft. Berechnung PET: Einwaage: 2 mg Heizrate: 10K/min Berechnung cp für PET bei verschiedenen Temperaturen: cp (T): 40°C (als einzelner Messpunkt, Standard cp PET = 2,5 J/K bei 25°C) 𝑐𝑝 = 𝑄 0,18𝑚𝑊 ∗ 𝑚𝑖𝑛 1,8𝑊 ∗ 60𝑠 1,8𝐽 ∗ 60𝑠 10,8 𝐽 = = = = = 10,8 𝐽𝐾 −1 𝑚∗𝑣 1 𝑚𝑔 ∗ 10 𝐾 1𝑔 ∗ 10𝐾 𝑠 ∗ 𝑔 ∗ 10 𝐾 𝑠∗𝐾 cp (T): 60 -70 °C Plateau vor der Glasübergangstemperatur Tg: 𝑐𝑝 = 𝑄 0,25𝑚𝑊 ∗ 𝑚𝑖𝑛 2,5𝑊 ∗ 60𝑠 2,5𝐽 ∗ 60𝑠 12,5 𝐽 = = = = = 12,5 𝐽𝐾 −1 𝑚∗𝑣 1 𝑚𝑔 ∗ 10 𝐾 1𝑔 ∗ 10𝐾 𝑠 ∗ 𝑔 ∗ 10 𝐾 𝑠∗𝐾 cp (T): 90-100°C Plateau nach der Glasübergangstemperatur Tg: 𝑐𝑝 = 𝑄 0,35𝑚𝑊 ∗ 𝑚𝑖𝑛 3,5𝑊 ∗ 60𝑠 3,5𝐽 ∗ 60𝑠 21 𝐽𝑠 = = = = = 21 𝐽𝐾 −1 𝑚∗𝑣 1 𝑚𝑔 ∗ 10 𝐾 1𝑔 ∗ 10𝐾 𝑠 ∗ 𝑔 ∗ 10 𝐾 𝑠 ∗ 𝐾 Deutlich ist die für den Glasübergang typische Änderung der Wärmekapazität cp messbar. Aufgabenstellung Bei einem Kunststoff (Polyethylenterephthalat, PET) sind mittels Differential Scanning Calorimetry (DSC) im Temperaturbereich von 30 °C bis 300 °C die Glasübergangstemperatur, das Schmelzverhalten, das Kristallisationsverhalten, der Kristallisationsgrad und cp vor und nach der Glasübergangstemperatur zu bestimmen. Die erhaltenen Heiz- und Kühlkurven sind auszuwerten und die Ergebnisse zu diskutieren. Die komplette Messung umfasst 2 Heizläufe bei Heizraten von 10 K/min und 20 K/min. Quellen (bearbeitet für Praktikumsversuch DSC) https://www.whs.de/fileadmin/public/dokumente/erkunden/fachbereiche/FB8/pers.Seiten/Dipl.%20Chem.I ng.Junghans/Analytik%20II/DSC.pdf http://www.google.de/url?sa=t&rct=j&q=&esrc=s&source=web&cd=1&cad=rja&uact=8&ved =0CCIQFjAA&url=http%3A%2F%2Fwww.gm.fh-koeln.de%2F~werkst%2FHauptseiten%2FDSC- DIL_oK.pdf&ei=N_Q3VYSHJMGYsgGH5YCYCQ&usg=AFQjCNEq0qS1fjkZc_YDd6iXImHXHraXRQ &bvm=bv.91071109,d.bGg, http://www.gm.fhkoeln.de/~werkst/Versuche/Thermoanalyse%20PET%20+%20Glas_SS%202013.pdf D.A. Skoog, J.J. Leary, Instrumentelle Analytik, Springer Verlag, Berlin, 1996, Naumer, Heller (Hrsg.), Untersuchungsmethoden in der Chemie, Georg-Thieme Verlag, Stuttgart, 1997 G. Schwedt, Taschenatlas der Analytik, Georg Thieme Verlag, Stuttgart, 1996 H. Utschick, Awendungen der thermischen Analyse, ecomed Verlagsgesellschaft, Landsberg, 1996 DIN EN ISO 11357-1: 2010: Kunststoffe - Dynamische Differenz-Thermoanalyse DIN 53765: 1994: Prüfung von Kunststoffen und Elastomeren - Thermische Analyse EN ISO 11357-1, DIN 53765) zur Ermittlung charakteristischer Temperaturen wie Kristallitschmelztemperatur Tm teilkristalliner Thermoplaste, Glasübergangstemperaturen Tg amorpher Thermoplaste und zur Bestimmung kalorischer Größen wie Wärmekapazität Q, spezifische Wärme cp, Kristallinität und Kristallinitätsgrad K, sowie Temper- und Aushärtungsvorgänge